Вступ
ПЕ (прееклампсія) є захворюванням, що виникає у II половині вагітності, супроводжується генералізованим судинним спазмом, хронічною формою синдрому ДВЗ (дисеміноване внутрішньосудинне згортання), підвищенням АТ (артеріальний тиск), протеїнурією та синдромом поліорганної недостатності (Anthony J. et al. 2016; Ramirez Avila G. M. et al. 2013; McCarthy E. A. et al. 2015; S. Shinar et al. 2016; Cunningham F. G. Et al. 2015). ПЕ є гестаційною патологією, яка зустрічається лише у людини. Діагностичні критерії ПЕ протягом останнього часу залишаються незмінними. Серед них: початок після 20 тижнів вагітності, добова протеїнурія більше 0,3 г або наявність двох позитивних тестів на протеїнурію у разових порціях сечі (>0,3 г/л) з інтервалом 4–6 годин, систолічний АТ вище 140 мм рт. ст. і діастолічний АТ більший або рівний 90 мм рт. ст. двічі з інтервалом 4–6 годин, а також зникнення або регресування вказаних ознак захворювання протягом 6 тижнів пуерперію.
Нещодавно у рекомендаціях АСОG (американського коледжу акушерів-гінекологів) і ISSHP (міжнародної спільноти вивчення гіпертензії під час вагітності) було зазначено, що протеїнурія не є обов’язковим діагностичним критерієм ПЕ.
У Фінляндії протягом останнього року єдиним критерієм ПЕ залишається лише АТ. При цьому, за даними Finnish Pre-eclampsia Consortium, чутливість і специфічність діагнозу не тільки не знизилася, а й, навіть підвищилася. Це можна пояснити наявністю атипових форм ПЕ, при яких протеїнурія відсутня (Kallela J. et al. 2016).
Пацієнтки з ПЕ легкого і середнього ступеня традиційно вважаються досить однорідною за клініко-лабораторними характеристиками групою хворих.
Тяжкою ПЕ вважають при наявності систолічного АТ³160 мм рт. ст., а діастолічного АТ³110 мм рт. ст., тромбоцитопенії, більше, ніж двократного перевищення нормального рівня трансаміназ, HELLP-синдрому, ниркової недостатності, тривалого болю в епігастрії або правому підребір’ї, порушень зору, неврологічної симптоматики або набряку легень (Dennis A. T. et al. 2014; Gathiram P. 2016; Uzan J. et al. 2011; Young B. C. et al. 2016).
Розповсюдженість ПЕ є приблизно однаковою у всіх регіонах Землі, складає від 5,0 до 16,0% та не залежить від рівня соціально-економічного розвитку. ПЕ ускладнює біля 3–8% загальної кількості вагітностей у країнах Європи (Jadli A. S. et al. 2016; Leeman L. et al. 2016). У структурі материнської смертності ПЕ і еклампсії відводиться у останні роки 10–15%. ПЕ – одна з провідних причин життєзагрозливих станів матері, значного рівня перинатальних втрат. Відомо, що ПЕ у 5 разів підвищує ризик перинатальних втрат і обумовлює більше, ніж 50 тисяч випадків материнських смертей у світі щорічно (Berhan Y. 2016; Fratto V. M. et al. 2016; Hu W. S. et al. 2016; Omotayo M. et al. 2016).
Список скорочень
АГ – артеріальна гіпертензія;
АФС – антифосфоліпідний синдром;
ВШ – відношення шансів;
ДНК – дезоксирибонуклеїнова кислота;
ДП – дисфункція плаценти;
ПІ – пульсаційний індекс;
РДС – респіраторний дистрес синдром;
РНК – рибонуклеїнова кислота;
САТ – середній артеріальний тиск;
С-РБ – С-реактивний білок;
СІ – серцевий індекс;
Flt – fms-like tyrosine (англ., тирозинові);
HbF – fetal hemoglobin (англ., плодовий гемоглобін);
HELLP-синдром – синдром гемолізу, підвищення рівня трансаміназ і тромбоцитопенії (англ., hemolysis, elevated liver ferments, low platelet count);
IL – interleukin (англ., інтерлейкін);
РАРР-А – pregnancy-associated plasma protein A (англ., білок плазми, асоційований з вагітністю А);
PlGF – placental growth factor (англ., фактор росту плаценти);
PP – placental protein (англ., плацентарний протеїн);
TNF – tumor necrosis factor (англ., фактор некрозу пухлин);
VEGF – vascular endothelial growth factor (англ. судинний ендотеліальний фактор росту)
Патогенез
У патогенезі ПЕ провідну роль відіграє дисбаланс між ангіогенними і антиангіогенними факторами, що порушує формування матково-плацентарного кровообігу (Turpin C. A. et al. 2015; Bolla D. et al. 2016; Redman C. W. et al. 2015). До числа перших відноситься поліпептид з сімейства судинного ендотеліального фактору росту (vascular endothelial growth factor – VEGF) – PlGF (placental growth factor), а також білка плазми, асоційованого з вагітністю А (pregnancy-associated plasma protein A – PAPP-A). Ці речовини підтримують інвазію трофобласту, а тирозинові рецептори (fms-like tyrosine – Flt) і ендоглін, навпаки, спроможні пригнічувати ангіогенез, блокуючи їх активність. Процес інвазії позаворсинкового трофобласту контролюють також плацентарні макрофаги шляхом продукції ангіогенних або антиангіогенних цитокінів (Aguilar A. et al. 2016; Das U. N. et al. 2015; Gezer C. et al. 2016; Emmery J. et al. 2016).
Ішемія плаценти сприяє синтезу прозапальних цитокінів і вазоконстрикторів. Потрапляння зазначених речовин у кровоплин матері викликає системні зміни ЦМГ (центральної материнської гемодинаміки), що призводять до гіповолемії та гіпоперфузії внутрішніх органів (Elliot M. G. et al. 2016; Lankhorst S. et al. 2016). Серед відомих механізмів патологічного впливу гіперцитокінемії наступні: активація процесів ПОЛ (перекисного окислення ліпідів) і пригнічення АОСЗ (антиоксидантної системи захисту) у ендотеліоцитах з накопиченням продуктів протеолізу, протеїнів середньої маси, порушення тромбоцитарного і коагуляційного гемостазу з ураженням мікроциркуляторного русла, і ендотоксикоз (Miranda Guisado M. L. et al. 2012; Afroze S. H. et al. 2016; Jin W. Y. et al. 2016; Nikolic A. et al. 2016).
У останні десятиліття активно вивчається роль тромбофілії у розвитку ускладнень вагітності. Гіпергомоцистеїнемія є одним з добре відомих чинників, що призводять до пошкодження судинної стінки і тромбозу. Гомоцистеїн здатний пошкоджувати клітини ендотелію, знижувати продукцію оксиду азоту, пригнічувати ефект простацикліну. Його тромбогенний ефект також пов'язаний з активацією фактора V, гальмуванням протеїну С, пригніченням експресії тромбомодулліна і блокадою зв'язування тканинного активатора плазміногену клітинами ендотелію (Morton J. S. et al. 2016). Гомоцистеїн надлишково накопичується в організмі на тлі недостатнього рівня реакцій реметилювання і сульфування. У цих реакціях основну роль грають вітамін В6 і активна форма фолієвої кислоти (Ji Y. et al. 2006).
Для запобігання надлишку гомоцистеїну і трансформації у метіонін необхідна, перш за все, достатня кількість активної форми фолієвої кислоти. Це забезпечується роботою ферменту метилентетрагідрофолат-редуктази. Дефіцит останньої має спадкову природу і призводить до вродженої тромбофілії (Polat M. et al. 2016; Polonia J. et al. 2016; Berks D. 2015; Fakhouri F. et al. 2016).
Велика роль у розвитку гемодинамічних розладів відводиться порушенням автономної нервової регуляції матері (C. Ghossein-Doha et al. 2016). У жінок з ПЕ вже з самого початку процесу гестації відмічається підвищена симпатична активність. Це сприяє підтриманню матково-плацентарного кровообігу на тлі гіповолемії та периферичного вазоспазму (Murphy M. S. et al. 2015; Musa S. M. et al. 2016).
Зростання потужності симпатичної ланки модулює загальний рівень і потужність парасимпатичної ланки автономної нервової регуляції шляхом їх пригнічення. На сьогодні відомі деякі механізми формування гіперсимпатикотонії. Підвищення симпатичної вазоконстрикторної активності може бути обумовленим зниженням барорецепторного обмеження завдяки центральному або периферичному механізмам. З іншого боку, гуморальні та паракринні фактори можуть стимулювати активність симпатичних нервів (K. H. Lampinen et al., 2014). Також відомо, що зростання потужності симпатичної ланки може бути обумовлено значним зростанням внутрішньочеревного тиску (Maeda K. 2014; Sugerman H. J. et al. 2011).
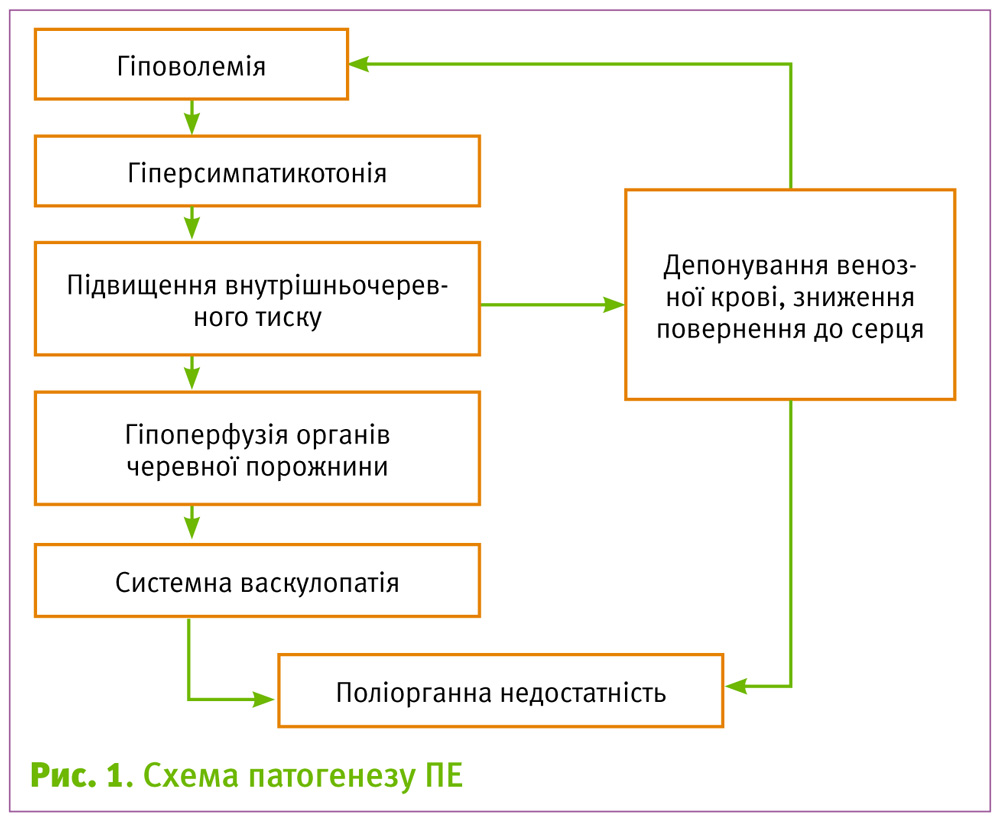
Остання обставина призводить до утруднення венозного повернення з нижньої половини тулуба, що додатково сприяє активації симпатичних механізмів підтримання судинного тонусу та розвитку хронічної венозної недостатності.
Крім цього, погіршення внутрішньоорганної гемодинаміки у черевній порожнині сприяє порушенню функції печінки, що призводить до розвитку атерогенезу, поглиблення оксидативного стресу та ендотеліальної дисфункції (Su G. L. 2008; D'Souza V. et al. 2016; Oztas E. et al. 2016).
Ендотеліальна дисфункція – ключове явище у механізмі ураження внутрішніх органів на тлі ПЕ. Підвищена проникність судин у поєднанні з гіпопротеїнемією призводить до набряків різної локалізації (C. K. Kao et al. 2016; Possomato-Vieira J. S. et al. 2016; Wang P. H. et al. 2015). Ураження ендотелію судин печінки призводить до HELLP-синдрому, судин нирок – до гострої ниркової недостатності, судин мозку – до набряку мозку і еклампсії, тощо. Такий шлях виникнення ускладнень можливий при ПЕ з раннім початком (до 32 тижнів). При цьому материнська смертність від ранньої ПЕ у 20 разів вища, ніж у ПЕ з пізнім виникненням (Young B. C. et al. 2016; Khodzhaeva Z. S. et al. 2016). ПЕ з пізнім початком за своїми рисами нагадує метаболічний синдром, при якому ураження судин є вторинними по відношенню до обмінних розладів. Жирова тканина може бути «полем» для підтримання ССЗВ (синдром системної запальної відповіді). Матково-плацентарне коло гемодинаміки вторинно залучається до патогенезу ПЕ у жінок з пізнім її початком. Тому на тлі ПЕ з раннім виникненням значно частіше зустрічається синдром ЗРП (затримки росту плода), дистрес плоду і антенатальна загибель плоду (Pluta R. et al. 2015; Eggers A. E. et al. 2015).
Значне підвищення симпатовагального балансу відображає зміни ЦМГ у жінок з ПЕ. У жінок з ПЕ гіперкатехоламінемія є фактором, що підвищує ЗПОС і АТ (Maeda K. 2016). Антигіпертензивні препарати не мають змоги відновити симпатовагальний баланс у пацієнток з ПЕ. У жінок, що перенесли ПЕ під час вагітності, відновлення симпатовагального балансу відбувається сповільнено і не повністю (Scholten R. R. et al. 2015). У багатьох породіль зберігається підвищена активність симпатичного барорефлексу. Це створює передумови для виникнення АГ у майбутньому та супроводжується підвищенням ризику коронарної хвороби та інсульту (Theilen L. H. et al. 2016; Mangos G. J. et al. 2012). Однак, у патогенезі ПЕ залишається багато невирішених питань. Тому ПЕ можна віднести до категорії «загадкових» хвороб.
Проведені дослідження дозволили вважати, що ПЕ розвивається на тлі підвищеного СІ (Andreas M. et al. 2016). У жінок з ПЕ легкого або середнього ступеня було переважно встановлено наявність гіперкінетичного типу ЦМГ. У цього контингенту пацієнток зберігалася гіперволемія і нормальний або незначно підвищений ЗПОС (загальний периферичний опір судин). У разі прогресування ступеня тяжкості ПЕ підвищення проникності судин, гіповолемія і низький СІ характеризували гіпокінетичний тип ЦМГ. Гіперсимпатикотонію у пацієнток з ПЕ легкого або середнього ступеня можна вважати компенсаторною реакцією, спрямованою на підтримання перфузії кінцевих органів (Riedl M. et al. 2010; Lakhno I. 2017). Максимальне зростання симпатовагального балансу відповідає гіпокінетичному типу ЦМГ у пацієнток з ПЕ тяжкого ступеня. У цих вагітних спостерігаються ознаки централізації гемодинаміки та гіпоперфузії життєво важливих органів (Lakhno I. 2015). Загалом, ПЕ характеризується руйнуванням базового для вагітності вагального механізму затримки рідини та вазодилатації.
Фактори ризику
Відомими факторами, що сприяють зростанню ризику виникнення ПЕ, є африканська раса, вік більше 35 років, багатоплодова вагітність, міхуровий занесок, наявність ПЕ у попередніх вагітностях, хронічна АГ, захворювання нирок, діабет, ожиріння і вроджені вади розвитку плоду (Cormick G. et al. 2016; Andrietti S. et al. 2008). Розвитку ПЕ може сприяти проживання у гірський місцевості. Це можна пояснити ішемією плаценти внаслідок зниженого діаметру маткових артерій та сповільненого матково-плацентарного кровоплину.
У багатьох епідеміологічних дослідженнях отримано докази спадкової або імунологічної природи ПЕ. Наявність ПЕ у матері підвищує ризик у доньки цього ускладнення вагітності у 2–5 разів (Jauniaux E. et al. 2016). Спадкову природу ПЕ підтверджує наявність генів, які сприяють розвитку ПЕ. Ці гени, ймовірно, можуть впливати на серцево-судинну систему і систему гемостазу, регулювати виразність ССЗВ (Bulbul M. et al. 2015). Деякі з них вже ідентифіковані. Знайдено взаємозв’язок з синтезом вазоактивних речовин, у тому числі, з ангіотензиногеном, у 1-q42-43, 7q36, 2p12, 2p25, 9p13 і 10q22.1 локусах (Ali S. M. et al. 2015). Ступінь вродженої схильності до ПЕ полігенна і залежить від багатофакторних патогенів. Гени-кандидати, що приймають участь у різноманітних біологічних процесах, включаючи імунітет, контроль судинної резистентності, коагуляцію крові, метаболізм, були предметом численних досліджень їх ймовірної ролі у ПЕ (Murphy M. S. et al. 2016).
Деякі систематичні огляди і мета-аналізи оцінили взаємозв’язок між материнськими генами і ПЕ. У одному з мета-аналізів був доведений підвищений ризик тяжкої ПЕ на тлі поліморфізму гену фактору згортання V rs6025 (ВШ – було 1,90), мутації гену фактору згортання ІІ G20210 A (rs179963) (ВШ – 2,01), поліморфізму гена рецептора лептину rs1137100 (ВШ – 1,75) і поліморфізму генів з групи тромбофілії (ВШ – 1,87) (Fakhouri F. et al. 2016; Berks D. et al. 2015). На сьогодні відомі декілька генетично обумовлених варіантів ПЕ. Серед них мутації гена ангіотензин-перетворюючого ферменту, цитоксичного Т-лімфоцитасоційованого протеїну 4, фактору 2, фактору V, ліпопротеїнліпази та гена І інгібітору серинової пептидази. Результати мета-аналізу дозволяють вважати, що у патогенезі ПЕ можуть приймати участь ренін-ангіотензинова система, система коагуляції та фібринолізу, ПОЛ і прозапальний каскад (He Y. et al. 2016; Markova A. D. et al. 2016).
Розвитку ПЕ також сприяють деякі прегестаційні особливості фізіології жінок. Так, гіповолемія, що існує до вагітності, може перешкоджати процесу затримки рідини і зростанню об’єму циркулюючої крові (Logue O. C. et al. 2016). Ці особливості можуть бути множинними. Про це свідчать результати досліджень, згідно яких підвищення рівня симпатичної регуляції, гіповолемія, високий рівень прозапальних цитокінів, С-РБ і перша вагітність є ознаками прегравідарного фенотипу, що призводить до розвитку ПЕ (Berks D. et al. 2015; Daneva A. M. et al. 2016).
Можливим механізмом гіперцитокінемії також може бути наявність хронічних захворювань інфекційної етіології. Хоча теорія інфекційної природи ПЕ не знайшла багатьох прихильників, відомо, що хронічний ендометрит супроводжується порушеннями формування матково-плацентарних судин. Наявність бактеріального вагінозу значно підвищує ризик латентного ендометриту. Крім цього, відомо, що безсимптомна бактеріурія, запальні захворювання пародонту також збільшують ризик ПЕ (Lee H. J. et al. 2016; A. S. Parihar et al. 2015).
Прогнозування ПЕ
Раннє виявлення жінок з високим ризиком розвитку ПЕ під час вагітності можливе за допомогою предикторних маркерів ПЕ, значення яких у таких випадках має характерні особливості. На цей час відомі біохімічні та біофізичні маркери, вивчення яких дозволяє прогнозувати її розвиток вже на початку ІІ триместру. Основні категорії маркерів наступні: ангіогенні/антиангіогенні фактори, плацентарні протеїни, плодовий гемоглобін (HbF), ниркові маркери, ультразвукові та материнські фактори. Специфічними біохімічними маркерами вважаються: PAPP-A, PIGF, а також співвідношення s-Flt-1/ PIGF, ендоглін, PP-13, цистатин-С (показник функції нирок), лейцил/цистиніл амінопептидаза, вазопресиназа і a1-мікроглобулін (Lagana A. S. et al. 2016; Elmas O. et al. 2016; Song Y. et al. 2016).
Значні перспективи використання для прогнозування ПЕ мають розчинний PlGF і Flt-1 (Friedman A. M. et al. 2014). Відомо, що ангіогенез визначається взаємодією ангіогенних факторів PlGF і VEGF з їх рецепторами Flt-1 і VEGF-2, що мають антиангіогенні властивості. Середні значення концентрації PlGF у сироватці крові демонструють прямо пропорційну залежність від гестаційного терміну з підвищенням у І і ІІ триместрах. Максимального рівня PlGF досягає приблизно у 30 тижнів вагітності, а потім поступово знижується. Встановлена наявність зниженого рівня PlGF у 11–13 тижнів вагітності у ситуаціях, пов’язаних з анеуплоїдією, порушеннями плацентації, що призводять до ПЕ і синдрому ЗРП плода. Тобто клінічна значущість вивчення рівня PlGF існує при ПЕ з раннім початком. Знижений рівень PlGF у ІІ і ІІІ триместрах також обумовлений розвитком ПЕ і (або) порушенням живлення або травлення плоду. Однак, в одному з досліджень було отримано суперечливі дані відносно рівня PlGF як біохімічного маркера ПЕ (Tsiakkas A. et al. 2016).
PlGF циркулює вільно або у зв’язаному з sFlt-1 стані. Розчинні sFlt-1 – це варіант мембранних рецепторів Flt-1, що вільно циркулюють у сироватці крові, де зв’язують і нейтралізують VEGF і PlGF. У багатьох дослідженнях був доведений зв’язок між підвищенням концентрації sFlt-1 і ПЕ (Costa R. A. et al. 2016). Рівень sFlt-1 починає зростати за 5 тижнів до початку ПЕ і залишається на більш високому рівні порівняно з жінками з неускладненим перебігом вагітності (Palmer K. R. et al. 2015). Визначення співвідношення sFlt-1/PlGF мала частоту виявлення ПЕ 87,5% при фіксованій частоті хибнопозитивних результатів у 10,0% у популяції жінок з низьким ризиком (Kurtoglu E. et al. 2016).
Можливим біомаркером ПЕ може бути розчинний ендоглін – це зменшена форма рецептору до трансформуючого фактору росту. Цей рецептор є потенційним антиангіогенним фактором, який зв’язується з трансформуючим фактором росту, порушує продукцію оксиду азоту і процеси вазадилатації (Nikuei P. et al. 2015).
PAPP-A – це гликозильований протеїн з великою масою, що виробляється у клітинах трофобласту. PAPP-A відомий як протеаза білка, який зв’язує інсуліноподібний фактор росту (Wang J. et al. 2014). Інсуліноподібний фактор росту відіграє значну роль у рості та розвитку плаценти. Досить логічно, що низький рівень PAPP-A пов’язаний з високою частотою маніфестації ПЕ. Мультицентрове дослідження 8839 жінок продемонструвало значну кореляцію між рівнем PAPP-A нижче 5 перцентилю і синдромом ЗРП, передчасними пологами, ПЕ і мертвонародженням (Wright A. et al. 2016).
Моделі, що дозволяють оцінювати індивідуальний ризик розвитку ПЕ з пізнім початком, базуються на комбінованому визначенні PAPP-A у І триместрі та співвідношення sFlt-1/PlGF у ІІ триместрі. Частота виявлення ПЕ при застосуванні таких моделей становила 87,5% при фіксованому співвідношенні хибний/позитивний результат у 5,0%. У жінок, вагітність яких ускладнилася розвитком ПЕ, концентрації PlGF і PAPP-A у сироватці крові знижуються. Ці білки виробляються у трофобласті, а їх знижений рівень відображає порушення плацентації (Tsiakkas A. et al. 2016).
Нещодавно була відкрита можливість використання у якості біохімічного маркеру ПЕ позаклітинного HbF. Підвищення рівня HbF у плацентарному екстрацелюлярному матриксі призводить до оксидативного стресу і підвищення проникності матково-плацентарного бар’єра. Аномальний плацентарний гемопоез руйнує материнсько-плодове територіальне розмежування, що призводить до ендотеліальної дисфункції, гіпертензії і протеїнурії, які є ознаками ПЕ. НbF вважається предиктором ПЕ у І і ІІ триместрах вагітності (Triunfo S. et al. 2016).
PAPP-A і HbF продемонстрували значну прогностичну значущість з 70,0% чутливістю і 95,0% специфічністю. Однак, PAPP-A не є суто специфічним для ПЕ і має бути доповненим допплерометрією кровотоку в маткових артеріях. Показники прогностичності цієї комбінації досягли рівня чутливості співвідношення HbF/a1-мікроглобулін (Lagana A. S. et al. 2016).
Інгібін-А і активін-А – глікопротеїни, що є членами сімейства трофобластспецифічних факторів росту. Ці білки у значних кількостях виробляються фетоплацентарною системою протягом вагітності. Інгібін-А має негативний зворотній зв’язок з гонадотропінами, а активін-А приймає участь у значній кількості біологічних процесів (Wu Y. et al. 2016). При наявності порушень плацентації концентрація інгібіну-А і активіну-А значно зростає, що відображає компенсаторний механізм, який сприяє покращенню інвазії трофобласту. Інгібін-А як предиктор ПЕ має суперечливі характеристики (Yong H. E. Et al. 2015). Підвищений рівень інгібіну-А у сироватці крові відображає розвиток ПЕ. Але чутливість інгібіну-А у прогнозуванні ПЕ є низькою. Однак, у деяких дослідженнях було встановлено, що у ІІ триместрі інгібін-А є найкращим біохімічним маркером ПЕ. Різниця у рівні активіну-А значно вище при ПЕ з пізнім початком, ніж при ранньому розвитку ПЕ. Інгібін-А і активін-А підвищуються до 14 тижнів у жінок з ПЕ (P. Nikuei et al. 2015).
Дезінтегрин і металлопротеїназа 12 (a disinegrin and metalloprotease 12 – ADAM12) – це протеаза білків, які зв’язують інсуліноподібний фактор росту. Низький рівень ADAM12 відображає підвищену кількість інсуліноподібного фактору росту у зв’язаному стані, що блокує потенції останнього до стимуляції росту і розвитку плаценти. У декількох дослідженнях була встановлена предикторна роль ADAM12 у ПЕ. При цьому низький рівень ADAM12 був характерним для жінок з ПЕ, а комбінація з PAPP-A дозволяє підвищити прогностичну значущість (Christians J. K. et al. 2016).
Перспективним маркером ПЕ може бути й цистатин С – маркер функції нирок, підвищення рівня якого демонструє пригнічену гломерулярну фільтрацію. Плацентарна експресія цистатину С підвищується на тлі ПЕ. Це сприяє зростанню концентрації цистатину С у плазмі крові жінок з ПЕ. Середня концентрація цистатину С у І триместрі вагітності значно вища у пацієнток, у яких у подальшому розів’ється ПЕ, ніж у жінок з нормальним перебігом вагітності (Cabarkapa V. 2015; Yalamati P. et al. 2015).
Пентраксин 3 (TNF-стимулюючий ген-14) належить до того ж самого сімейства, що й С-РБ і плазмовий компонент амілоїду Р. Пентраксин 3 складається з 381 амінокислоти. На тлі синдрому ССЗВ, який є частиною патогенезу ПЕ, рівень пентраксину 3 значно підвищується (Zhao J. et al. 2016).
Р-селектин – представник групи адгезивних молекул поверхні клітини. Ця речовина синтезується тромбоцитами і ендотеліальними клітинами на тлі активації. Вона відіграє ініціюючу роль у ряді запальних і прокоагулянтних реакцій шляхом активації циркулюючих лейкоцитів. Р-селектин швидко розповсюджується з клітинних мембран активованих тромбоцитів у розчинних ізоформах (Valino N. et al. 2016). ПЕ супроводжується значною активацією тромбоцитів. Мікрочастки з прокоагулянтною активністю, що містять Р селектин, вивільнені з активованих тромбоцитів, були знайдені у периферичній крові жінок з ПЕ. Встановлено підвищення концентрації розчинного Р-селектину у сироватці крові пацієнток з ПЕ (Biberoglu E. et al. 2016). Однак, в іншому дослідженні не було встановлено значних відмінностей між рівнем Р-селектину, каталази, супероксиддисмутази у жінок з ПЕ і пацієнток з нормальним перебігом вагітності (Elliot M. G. et al. 2016). Наявність непослідовних і суперечливих результатів стосовно Р-селектину як предиктора ПЕ потребує поширення фундаментальних досліджень біологічної ролі цієї речовини під час вагітності.
Розчинний подібний до фактору некрозу пухлин індуктор апоптозу (soluble tumor necrosis factor-like weak inducer of apoptosis – sTWEAK) нещодавно був відкритий як цитокін, що має відношення до TNF-a. Було встановлено, що sTWEAK відображає наявність ендотеліальної дисфункції у жінок з хронічним захворюванням нирок. У жінок з ПЕ концентрація sTWEAK була підвищеною порівняно до здорових вагітних (Zeisler Y. et al. 2016). Тому вивчення ролі цього прозапального цитокіну у патогенезі ПЕ, а також можливостей його використання як біохімічного маркера цього захворювання можна вважати доцільним.
Фетуїн-А (FA) – поліфункціональний протеїн, відомий як інгібітор ектопічної кальцифікації та регулятор рівня глюкози у сироватці крові, був досліджений у ролі маркеру запалення. Було встановлено, що рівень FA на тлі запалення знижується. У пацієнток з ПЕ з раннім початком концентрація FA була зниженою, а на тлі ПЕ з пізнім початком, навпаки, – підвищеною. Кореляція між маркерами ССЗВ і FA була виявлена лише у жінок з раннім початком ПЕ (Sanhal C. Y. et al. 2016).
У жінок з ПЕ спостерігається майже п’ятикратне збільшення концентрації вільної ДНК плоду. Імуномодулюючі властивості вільної ДНК відомі вже давно. Плодова ДНК людини активує запальну відповідь шляхом продукції Il-6 у В-лімфоцитах і мононуклеарах периферичної крові (Afroze S. H. et al. 2016). Експериментально встановлено, що вільна плодова ДНК підвищує рівень TNF-a і Il-6 та сприяє лімфоцитарній інфільтрації плацентарної ділянки (Das U. N. et al. 2015). Відомі ступені відповіді на різну кількість вільної ДНК плода, від яких залежить ризик ПЕ. Найбільший рівень відповіді спостерігається у жінок з HELLP-синдромом. Підвищення розповсюдження ДНК на тлі ПЕ є маркером гіпоксичної смерті клітини. Рівень вивільнення ДНК значно зростає в умовах зниження оксигенізації плаценти (Mc Master-Fay R. A. et al. 2016).
Таким чином, потрапляння вільної ДНК плоду в системний кровоток матері може бути пусковим моментом у виникненні ССЗВ. На сьогодні, перспективність використання вільної ДНК плоду як предиктора ПЕ, переважно з раннім початком, доведена у декількох багатоцентрових дослідженнях (Bredaki F. E. et al. 2016). Однак, отримані результати мають певну різнорідність показників вільної ДНК плоду, що не дозволяє розглядати визначення цього показника як метод скринінгу на ПЕ.
Перспективним предиктором розвитку синдрому ЗРП і ПЕ є значення мікроРНК. Концентрація мікроРНК знижується при розвитку ДП, що характерно для цих станів (Sheikh A. M. et al. 2016).
Крім цього, вивчення ангіогенних і антиангіогенних маркерів може бути корисним для диференційної діагностики захворювань, які супровод-жуються підвищенням АТ під час вагітності. У двох ретроспективних аналізах була підтверджена роль допплерометрії кровотоку в маткових артеріях, Flt-1 і PlGF у диференціації між хронічним захворюванням нирок і ПЕ у вагітних з протеїнурією та АГ. При наявності первинної маніфестації цих симптомів вивчення рівня Flt-1 і PlGF містить важливу клінічну інформацію. Значення Flt-1/PlGF нижче 30 було патогномонічним для хронічного захворювання нирок (Stubert J. et al. 2014). Це дослідження є дуже важливим, коли відсутність будь-яких даних про захворювання нирок до вагітності та у І половині гестації не дозволяє виключити коморбідну патологію.
Кілька досліджень були присвячені ролі копептину у прогнозуванні ПЕ. Рівень цієї речовини був підвищеним у пацієнток як з раннім початком ПЕ, так і пізнім початком ПЕ (Tuten A. 2016). Копептин – глікопептид, який є С-термінальним фрагментом препроаргініна вазопрессина і прекурсором вазопресину. Вазопресин приймає участь у регуляції водно-електролітного балансу і рівня АТ (Roland L. et al. 2010). Вивчення рівня копептину як предиктора ПЕ можливо проводити вже з 6 тижня вагітності. Чутливість цього біохімічного маркера була 88,0%, а специфічність – 81,0% (Gandley R. E. et al. 2016). Тому вивчення рівня цієї речовини у І триместрі вагітності є повністю обґрунтованим і практично доцільним.
Крім біохімічних маркерів ПЕ, досить широко з метою прогнозування використовують біофізичні показники, визначення яких можливе за допомогою малозатратних неінвазивних методів, зокрема, доплерографії матково-плацентарних судин.
У багатьох дослідженнях було доведено, що підвищена резистентність кровотоку в маткових артеріях, за даними доплерометрії, була пов’язана з подальшим розвитком ПЕ, що відображало релевантність до даних гістологічного дослідження плацент вагітних (Weel I. C. et al. 2016). У більшості робіт вивчено дані доплерометрії у ІІ триместрі вагітності. Однак, у деяких дослідженнях встановлена значна прогностична цінність доплерометричного скринінгу на ПЕ у І триместрі (Walther T. et al. 2006). Але мета-аналіз 74 досліджень (79 547 одноплодових вагітностей) довів більшу інформативність скринінгу резистентності кровотоку в маткових артеріях у ІІ триместрі переважно для тяжкої ПЕ з раннім початком. Чутливість складала 78,0%, а специфічність – 95,0%. Наявність підвищеного ПІ з дикротичною виїмкою у фазі ранньої діастоли було найкращим біофізичним маркером не лише для пацієнток з групи високого, а й низького ризику виникнення ПЕ (Friedman A. M. et al. 2014). Але нещодавно у 11 дослідженнях, що були проведені на 43 122 вагітних у І триместрі, була доведена низька чутливість ПІ – 26,0% і висока специфічність – 91,0%. На показник ПІ у І триместрі вагітності негативно впливали: термін вагітності, маса тіла матері, расова приналежність, наявність прегестаційного цукрового діабету (Kim J. Y. et al. 2015; Baumfeld Y. et al. 2015). Тому підрахування ПІ треба проводити у МоМ з поправкою на зазначені фактори. Значення ПІ у МоМ значно зростає у жінок, в яких розів’ється ПЕ з раннім початком, у терміні 11–13 тижнів. Встановлено наявність значної негативної лінійної кореляції між ПІ у МоМ і терміном розродження. Це підтверджує не лише доцільність скринінгу за допомогою ПІ у МоМ, а той факт, що ПЕ потребує дострокового розродження.
Використання об’ємного 3D ультразвукового дослідження з визначенням індексу васкуляризації плаценти поки що не підтвердило доцільність використання у якості скринінгового методу. Показник кровотоку, що вимірювали у 3D-режимі, не відрізнявся у здорових пацієнток з жінками, у яких у подальшому розвилась ПЕ (Gathiram P. et al. 2016).
Серед біофізичних маркерів високу інформативність має САТ, що підвищується ще до появи клінічних проявів ПЕ. САТ легко підрахувати шляхом ділення суми систолічного АТ і подвійного діастолічного АТ на 3. Мета-аналіз, із залученням 60000 вагітних з 3300 випадками ПЕ серед цього контингенту, довів переваги визначення САТ над вимірюванням систолічного або діастолічного АТ у жінок з низьким ризиком ПЕ І або ІІ триместрі (N. Valino et al. 2016), але для пацієнток з високим ризиком ПЕ визначення діастолічного АТ у терміну 13–20 тижнів вагітності вважається найбільш інформативним біофізичним маркером ПЕ (Tayyar A. et al. 2016).
У одному дослідженні підвищення САТ у 11–13 тижнів у комбінації з материнськими факторами ризику продемонстрував частоту виявлення ПЕ 72,4%, 62,9% і 49,3% для ПЕ з раннім початком, пізнім початком і загалом. У термінах 20–24 тижні підвищення САТ поряд з підвищенням у терміні 11–13 тижнів супроводжувалося ранньою ПЕ у 84,3%, пізньою ПЕ у 65,7% і, загалом, 52,5%. Це свідчить про необхідність визначення САТ у межах скринінгу на ПЕ двічі – у термінах 11–13 тижнів і 20–24 тижні (Morton J. S. et al. 2016; Tejera E. et al. 2012). На підставі цієї закономірності була розроблена двостадійна стратегія виявлення вагітних з високим ризиком виникнення ПЕ.
Мета першої стадії – виявлення жінок з підвищеним ризиком розвитку ранньої ПЕ у 11–13 тижнів вагітності для початку проведення медикаментозної профілактики малими дозами ацетилсаліцилової кислоти до 16 тижнів. Друга стадія здійснюється у 30–33 тижні. Вона спрямована на активний пошук показань до дострокового розродження (Duckworth S. et al. 2016).
У дослідженні, що проводили на 35215 вагітних у термінах 11–13 тижнів, вивчали ПІ у маткових артеріях і САТ. Результати свідчили, що приблизно 80,0% жінок з ПЕ народили до 34 тижнів вагітності (Tayyar A. et al. 2016). У іншому проспективному дослідженні доведено, що комбінований скринінг у термінах 30–33 тижні з використанням ПІ у маткових артеріях і САТ дозволив виявити 90,0% жінок з ПЕ, які потребували розродження у найближчі 4 тижні після клінічної маніфестації захворювання. Автори прийшли до висновку, що впровадження активного скринінгу на ПЕ у 30–33 тижні вагітності додає значних переваг до результатів скринінгу у 11–13 тижнів (Zhao J. et al. 2016). Відомо, що існує сильний взаємозв’язок між ПІ у маткових артеріях і САТ при фізіологічному перебігу вагітності. Прогнозована частота розродження у термінах до 34, 37 і 42 тижнів при проведенні біофізичного скринінгу з використанням ПІ у маткових артеріях і САТ відповідно складала 80,0%, 55,0% і 35,0% (Bredaki F. E. et al. 2016). Тому проведення скринінгу на ПЕ, що включає материнські біофізичні маркери, дозволяє втілити двостадійну концепцію і активно сприяти покращенню перинатальних наслідків завдяки своєчасному розродженню.
Декілька досліджень, проведених під егідою Фонду медицини плоду, продемонстрували переваги комбінованого використання даних анамнезу, ПІ у маткових артеріях, САТ, сироваткової концентрації PAPP-A, PlGF, PP13, інгібіну-А, активіну-А, ендогліну, пентраксину-3 і Р-селектину. Застосовані алгоритми скринінгу у 11–13 тижнів вагітності дозволили потенційно ідентифікувати 90,0%, 80,0% і 60,0% ПЕ, що виникла відповідно до 34 тижнів, у терміні 34–36 тижнів та після 37 тижнів вагітності (частота хибнопозитивних результатів 5,0%) (Wright A. et al. 2016; Elmas O. et al. 2016).
У двох дослідженнях були використані моделі, які базуються на теоремі Байеса, що враховували ПІ у маткових артеріях, САТ, сироваткову концентрацію PAPP-A і PlGF у 11–13 тижнів вагітності. За допомогою цього методу можливо ідентифікувати більшість випадків ПЕ з раннім початком. Також було виявлено 90,0% випадків, що потребували дострокового розродження у термінах до 34 тижнів вагітності (Stubert J. et al. 2015). Прогностичну модель на базі логістичної регресії було використано у проспективному когортному дослідженні 9462 вагітних у І триместрі вагітності. Найкраща модель для виявлення ПЕ з раннім початком включала оцінку первинного ризику, САТ, ПІ у маткових артеріях, PlGF і sFlt-1. За її допомогою було ідентифіковано 87,7% випадків ПЕ при частоті хибнопозитивних результатів 5,0%. Для ПЕ з пізнім початком ця модель дала змогу виявити 68,3% випадків при частоті хибнопозитивних результатів 5,0% (Kurtoglu E. et al. 2016).
В цілому, слід зазначити, що на сьогодні не існує жодного скринінгового тесту, який може забезпечити достатньо вірогідну оцінку ризику розвитку ПЕ, особливо на пізніх термінах вагітності.
Продовження у наступному номері.
Перелік літератури знаходиться у редакції.

коментарів