Менопауза вважається невід'ємним етапом старіння, кожна жінка переносить його по-своєму. Деякі не помічають особливих змін ні в тілі, ні в свідомості, інші відчувають себе некомфортно і погано переносять цей етап їхнього життя. Вік 48–50 років для жінок у нашій країні асоціюється, на жаль, з різними порушеннями сечостатевого тракту, зумовленими дефіцитом естрогенів
Для певних стадій репродуктивного стану жінки характерний відповідний бактеріальний асортимент. Нормальна мікрофлора піхви підрозділяється на облігатну, факультативну та транзиторну [1]. Облігатні мікроорганізми (непатогенні й умовно-патогенні) в обов’язковому порядку входять до складу нормальної мікрофлори, перешкоджають розвитку патогенних мікробів, що потрапили у піхву. Представники факультативних мікроорганізмів досить часто, але не завжди, зустрічаються у здорових жінок. Транзиторні мікроорганізми (непатогенні, умовно-патогенні, патогенні) випадково заносяться в генітальний тракт з навколишнього середовища. В умовах нормального біотопу вони перебувають у піхві короткий час і швидко видаляються зі слизом, за рахунок діяльності мукоциліарного епітелію. У разі порушення захисних механізмів патогенні чи умовно-патогенні мікроорганізми транзиторної або факультативної флори прикріплюються до клітин вагінального епітелію з подальшим розмноженням і пошкодженням тканин.
Склад усіх біотопів, в тому числі і вагінального, регулюється ендокринною, нервовою та імунною системами, які діють як єдине ціле [2]. З переходом жінки в період постменопаузи в генітальному тракті істотно знижуються рівні естрогенів і, відповідно, глікогену. Слизова оболонка піхви потоншується, проліферативні процеси у вагінальному епітелії припиняються, значно зменшується загальний рівень бактерій, перш за все лакто- та біфідобактерій. Якісний склад мікрофлори стає мізерним, з переважанням облігатно-анаеробних бактерій. У цей період рН вагінального середовища набуває нейтрального значення. Це призводить до зміни навколишнього середовища для лактобацил і, відповідно, до змін в мікрофлорі. Все це сприяє розвитку й персистенції інфекційного процесу і пояснює велику поширеність рецидивуючих інфекцій статевих шляхів у жінок з урогенітальною атрофією в менопаузі [3]. Таким чином, зміни в гормональному статусі слід розглядати не як єдину причину розвитку вульвовагініту, а як один з важливих чинників поряд зі змінами мікробіоценозу піхви.
Тривале існування вагінальної атрофії призводить до елімінації або різкого зниження титру лактобацил (до 75,7%) при відсутності масивної колонізації піхви умовно-патогенними мікроорганізмами (ентерококами, стрептококами, кишковою паличкою) [3]. Дані мікроорганізми проявляють антагоністичну активність відносно патогенних й умовно-патогенних мікроорганізмів і створюють сприятливі умови для розвитку корисної мікрофлори кишечника за рахунок ферментації глюкози, манози, фруктози й сахарози до молочної кислоти, яка не викликає метаболічний ацидоз; вироблення бактеріоцинів, що пригнічують розмноження інших умовно-патогенних і патогенних мікроорганізмів; нормалізують вагінальну мікрофлору, відновлюючи природне кисле середовище в піхві (рН 3,8–4,5), та підвищують стійкість слизової оболонки до дії патогенних мікроорганізмів [4].
Традиційним лікуванням вульвовагінальної атрофії є спеціальні вагінальні креми, що містять гормональні компоненти. Однак далеко не всі жінки згодні приймати гормони у будь-якому вигляді. Крім того, деякі гормональні креми негативно впливають на бактеріальну мікрофлору піхви, аж до підвищення уразливості жінки для інфекцій [5]. Крім того, у даної групи жінок часто застосовуються також антимікробні засоби, що не тільки викликає глибокі мікроекологічні порушення в усьому організмі, в тому числі і в вагінальному біотопі, позбавляючи його природного захисту, а й сприяє формуванню мультирезистентних популяцій умовно-патогенних мікроорганізмів, а також штучної селекції нових патогенів, які все частіше залучаються у процес розвитку інфекційно-запальних патологій піхви [6].
Важливим компонентом є не тільки терапія, а й профілактика рецидивів вульвовагініту у жінок в менопаузі, враховуючи вираженість клінічних проявів і високу частоту рецидивів порушень мікробіоценозу статевих шляхів. У зв'язку з цим значний інтерес представляє застосування вагінальних пробіотиків, що коригують склад вагінальної мікрофлори з метою зниження ризиків лікування і профілактики порушень мікробіоценозу статевих шляхів [7, 8].
Мета дослідження
Оптимізація терапії вульвовагінітів у пацієнток в менопаузі зі зниженням частоти рецидивів порушень мікробіоценозу статевих шляхів із застосуванням сучасних пробіотиків.
У дослідження включалися пацієнтки в менопаузі різної тривалості з симптомами вагінальної атрофії і рецидивуючими вульвовагінітами. Критерієм виключення були жінки, які мають інфекції, що передаються статевим шляхом.
Проведено обстеження 62 жінок у віці 48–65 років, що перебувають у постменопаузі. Тривалість захворювання – від 1 до 7 років (у середньому 3,7±1,8 років). Число рецидивів коливалося від 3 до 18 епізодів на рік (у середньому за останній рік склало 5,3±2,9 епізодів). В анамнезі усі пацієнтки отримували лікування антибіотиками від 3 до 12 курсів протягом року, що призводило до розвитку кандидозного вагініту і посилення дисбіотичних порушень. На момент звернення жодна пацієнтка не отримувала гормональної терапії.
Перед початком терапії всі пацієнтки були розподілені на дві групи: I група – 30 пацієнток з вульвовагінітом, яким проводилася інтравагінальна терапія метронідазолом у комбінації з міконазолом нітратом протягом 10 днів; II група – 32 пацієнтки з таким же діагнозом, для лікування яких протягом 10 днів додатково застосовувались вагінальні супозиторії Неопробіо, що містять ліофілізат трьох пробіотичних штамів: Lactobacillus plantarum, Enterococcus faecium, Enterococcus durans, живильне середовище для бактерій – лактозу, а також додаткові речовини. Вибір групи відбувався випадково, за допомогою генератора випадкових чисел (рандомізація). Але препарати не маскувались – пацієнтка і дослідник не були «сліпі» (проспективне відкрите рандомізоване дослідження).
Результати дослідження та обговорення
До лікування і в кінці третього місяця терапії всім пацієнткам проводилися загальне гінекологічне обстеження, бактеріоскопічні і бактеріологічні методи дослідження виділень з піхви і каналу шийки матки, вимірювання рН піхви.
Значення рН вагінального вмісту коливалося від 5,5 до 7,0 (в середньому 6,3±0,7), у пацієнток старшої вікової групи (>60 років) значення рН склало 6,0–7,0.
Комплексне мікробіологічне дослідження вагінальних виділень показало, що у всіх випадках відзначалося різке зниження титру або елімінація (у 23,3% випадків) лактобацил. Зростання колоній умовно-патогенних мікроорганізмів виявлялося у всіх жінок, включаючи: стрептококи (45,8%), гриби роду Candida у високому титрі (29,2%), стрептокок групи В (25%), клебсієллу (4,2%), кишкову паличку (33,3%), дифтероїди (45,8%).
Групи, що досліджувались, не відрізнялися статистично значимо за переліченими параметрами (p>0,05).
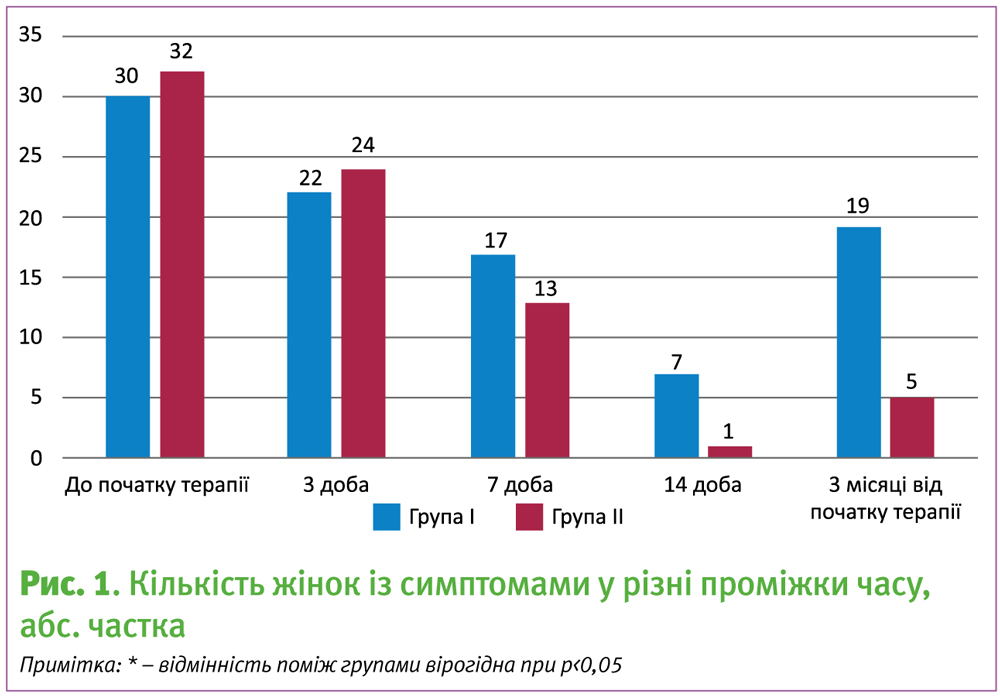
Слід зазначити, що вже через 3 дні від початку лікування пацієнтки обох груп відзначили значне зменшення виділень і відсутність дискомфорту, але повна відсутність симптомів спостерігалась лише у 26,7% жінок І групи та 25% жінок групи ІІ (рис. 1), що не мало вірогідної різниці. На 7 добу від початку лікування частка симптомних жінок у групі І склала 56,7%, а в групі ІІ дорівнювала 40,6%, що також не мало статистично значимої різниці. Відразу після закінчення терапії – на 14 добу від початку у групі І було 7 симптомних жінок (23,3%), тоді як у групі ІІ – лише 1 жінка із залишковими симптомами вульвовагініту (3,1%), що було вірогідно нижче, ніж у групі І (p<0,05). Однак, найбільш цікаві дані були отримані через 3 місяці лікування – 19 жінок І групи мали рецидив (63,3%), коли в групі ІІ – лише 5 (15,6%), що вказує на протирецидивні властивости пробіотичної терапії.
Відразу після закінчення курсу лікування у хворих обох груп відзначалося зниження рівня рН до 3,5–4,5 (в середньому 3,8±0,3).
Повторне повне клініко-лабораторне обстеження проводилося по закінченню третього місяця після лікування. При контрольному комплексному мікробіологічному дослідженні вагінальних виділень після закінчення лікування клінічна ефективність терапії була досягнута у 65% пацієнток I групи і у 97% – II групи (p<0,05). У 100% пацієнток II групи було встановлено нормалізацію біоценозу статевих шляхів, що виражалося у зменшенні лейкоцитарної реакції і скороченні темпів росту факультативних мікроорганізмів. У 100% випадків домінували морфотипи лактобацил.
Висновки
Розвиток рецидивуючих інфекцій на тлі урогенітальної атрофії відносять до важкої форми їх прояву. Порушення гормонального фону зі зниженям продукції естрогенів у пацієнток в менопаузі активізує умовно-патогенну флору, впливаючи при цьому на місцеву бар'єрну функцію. Необдумане і нераціональне призначення курсів антибактеріальної терапії призводить до ще більшого порушення мікробіоценозу у пацієнток, розвитку дисбіозу в піхві і, ймовірно, може бути однією з причин рецидивів захворювання. Адекватна патогенетично обґрунтована терапія вульвовагінітів у жінок менопаузального періоду препаратом Неопробіо є досить ефективним методом лікування та одночасно профілактики порушень мікробіоценозу статевих шляхів. Використання пробіотику дозволяє швидше відновитися вагінальному біоценозу і підтримувати природну мікрофлору, активізуючи захисну дію лактобацил, їх антагоністичні властивості щодо умовно-патогенних мікроорганізмів, що перешкоджає розвитку рецидивів захворювання.
Перелік літератури
на сайті extempore.info


коментарів