«Люк, я твій батько і твоя мама. Люк, я заплутався у термінах»
На обрії з’являються дивовижні дослідження у галузі репродуктивних технологій. Хоча стосовно того, про що йтиметься далі, світанок був у 2000–2010 роках, зараз вже, мабуть, близько до зеніту. А йтиметься про можливість отримання потомства з генетичним матеріалом від двох батьків-чоловіків, двох матерів або ж навіть самозапліднення.
Ці технології відкриють новий підхід до лікування неплідності, а також дозволять одностатевим парам мати генетично спільне потомство, а якщо зайти далі від всепроникаючого антропоцентризму, то це й нові можливості для збереження видів вимираючих тварин, наприклад, коли в природі не лишилося особин певної статі, або наявна лише одна особина.
Чи можна створити гамети in vitro?
На шляху дослідників, що намагалися вирішити проблему створення гамет in vitro, довго стояла перешкода під назвою «геномний імпринтинг». Це явище пов’язане з епігенетичними чинниками, за умов якого певні гени експресуються по різному в залежності від їх походження – від батька або від матері. Відомими захворюваннями, пов’язаними з генетичним імпринтингом, є синдром Ангельмана і синдром Прадера–Віллі. При цих захворюваннях спостерігається делеція ділянки хромосоми 15q11-13, але, якщо вражена батьківська хромосома, то у дитини розвивається синдром Прадера–Віллі (гіпотонія, ожиріння, гіпогонадизм), а якщо материнська – то синдром Ангельмана (епілепсія, тремор, «усміхнений» вираз обличчя).
Ще 1984 року дослідження зі створенням ембріону з пронуклеусами особин однієї статі показало, що плід гине на стадії бластоцисти [1]. Це вказувало на важливість процесу сперматогенезу у чоловіків і оогенезу у жінок. Довгий час ці чинники були невідомі, а їх відтворення in vitro не уявлялося можливим. Тепер відомо, що гамети отримують певні епігенетичні чинники (описано близько 80 генів, епігенетичні модифікації яких пов’язані з геномним імпринтингом) під час цих процесів, що й забезпечує нормальний розвиток після запліднення.
Обхідний шлях
Є інші шляхи для створення правильного епігенетичного коду гамет, окрім його штучного відтворення in vitro. Наприклад, у 2011 році в журналі «Biology of reproduction» з’явилася робота, у ході якої дослідникам вдалося відтворити у мишей потомство з генетичним матеріалом від двох мишей чоловічої статі [2]. Для цього була розроблена досить складна технологія. Для початку з міофібробластів треба було зробити індуковані плюрипотентні стовбурові клітини (іПСК). Створення іПСК – це технологія, що дозволяє за допомогою індукції певних генів (Oct3/4, Sox2, c-Myc, та Klf4) і культивування в умовах, потрібних для стовбурових клітин, повернути дифференційовані клітини в стан плюрипотентності [3]. Після отримання індукованих стовбурових клітин автори використали вже відомий факт, що в культурі стовбурових клітин приблизно 1% клітин спонтанно втрачають 1 статеву Y-хромосому, набуваючи каріотипу 45Х0. Хоча у людей такий каріотип призводить до смерті ще на ембріональному періоді, а в рідкісних випадках до народження дитини з синдромом Шерешевського–Тернера, однією з ознак якого є неплідність, у мишей даний каріотип призводить до розвитку життєздатної особини жіночої статі з нормальною репродуктивною функцією.
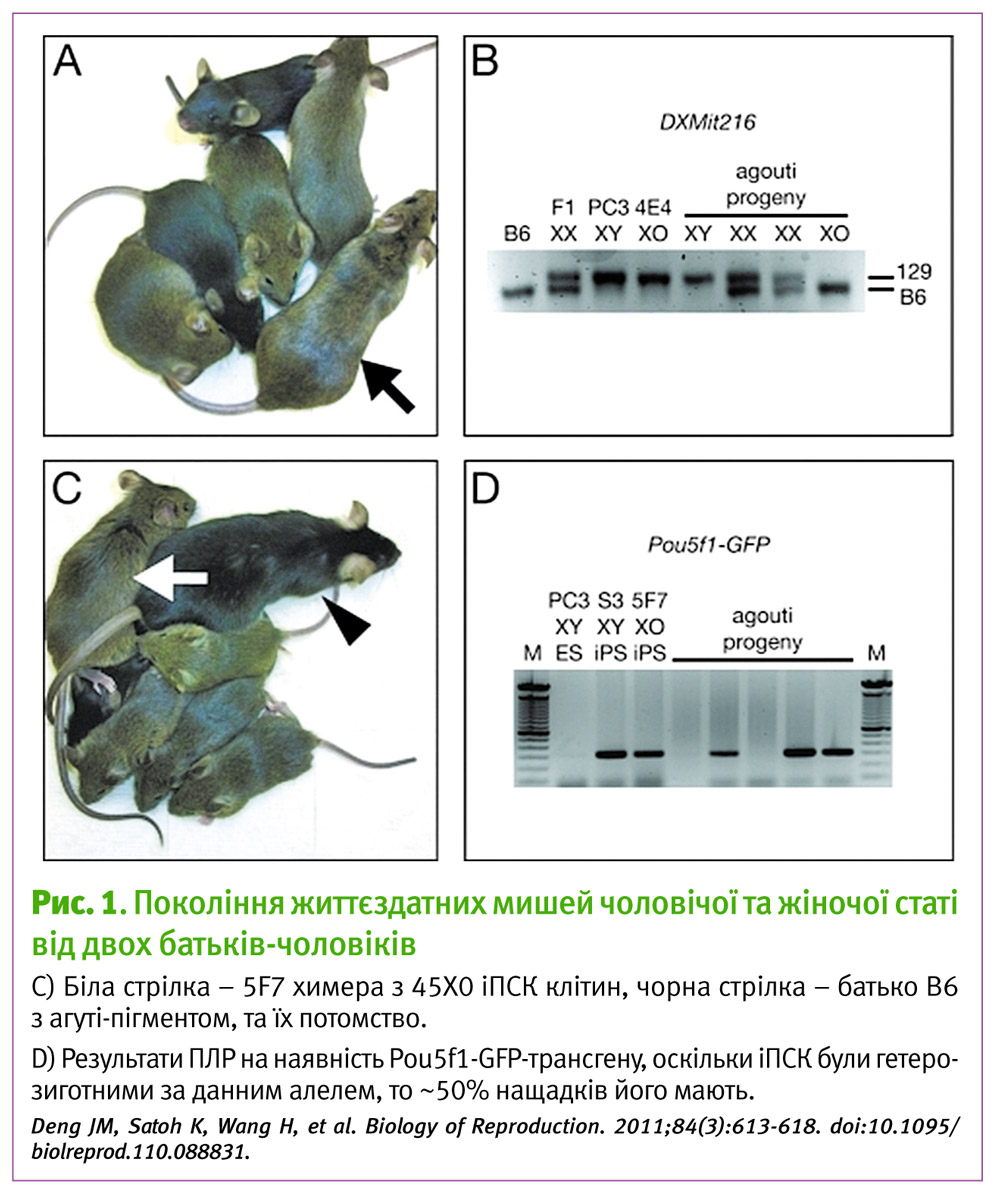
Після появи в культурі іПСК 45Х0 їх використовували для ін’єкції у бластоцисту нормальної лінії мишей, таким чином створюючи мишей-химер жіночої статі. Наявність клітин, що походили з 45Х0 іПСК підсажених клітин підтверджувалась так: 45Х0 клітини мали ген Agouti, наявність якого забезпечує специфічне забарвлення хутра, а також Pou5f1-GFP – трансген, що кодує білок з флуоресцентною міткою. Відповідно, якщо в миші було наявне хутро такого забарвлення та клітини, що містили флуоресцентну мітку, то вона походила з клітин 45Х0. Відповідно, ці миші мають і яйцеклітини, що походять із попередників іПСК 45Х0.
Далі химер (з клітинами від батька №1) схрещували зі звичайними мишами тої ж лінії чоловічої статі (батько №2) і отримували потомство з генетичним матеріалом від двох батьків-чоловіків. Нащадки були як чоловічої – 46ХУ(Х від батька №1 та Y від батька №1), так і жіночої статі 46ХХ та 46Х0 (Х або 0 від батька №1 та Х від батька №2), усі мали Агуті-забарвлення й Pou5f1-GFP+ клітини.
Таким заплутаним методом і отримали потомство з генетичним матеріалом від двох батьків-чоловіків, створивши по дорозі новий спосіб розмноження (рис. 1).
Сьогодення
Для клітинної біології та генетики наших днів кожен рік – це вічність і тисячі нових досліджень, і гаметогенез in vitro перестав бути чимось недосяжним. Вже є результати успішного відтворення потомства з використанням штучно індукованих яйцеклітин у мишей. Автори роботи, нещодавно опублікованої в журналі «Nature», створили протокол для проведення повного циклу диференціації жіночих статевих клітин з плюрипотентних стовбурових (ембріонального походження та іПСК) до яйцеклітин, з яких вдалося отримати здорове потомство, а також після запліднення яких вдалося відібрати з бластоцисти ембріональні стовбурові клітини і провести наступний цикл з відтворенням потомства [4].
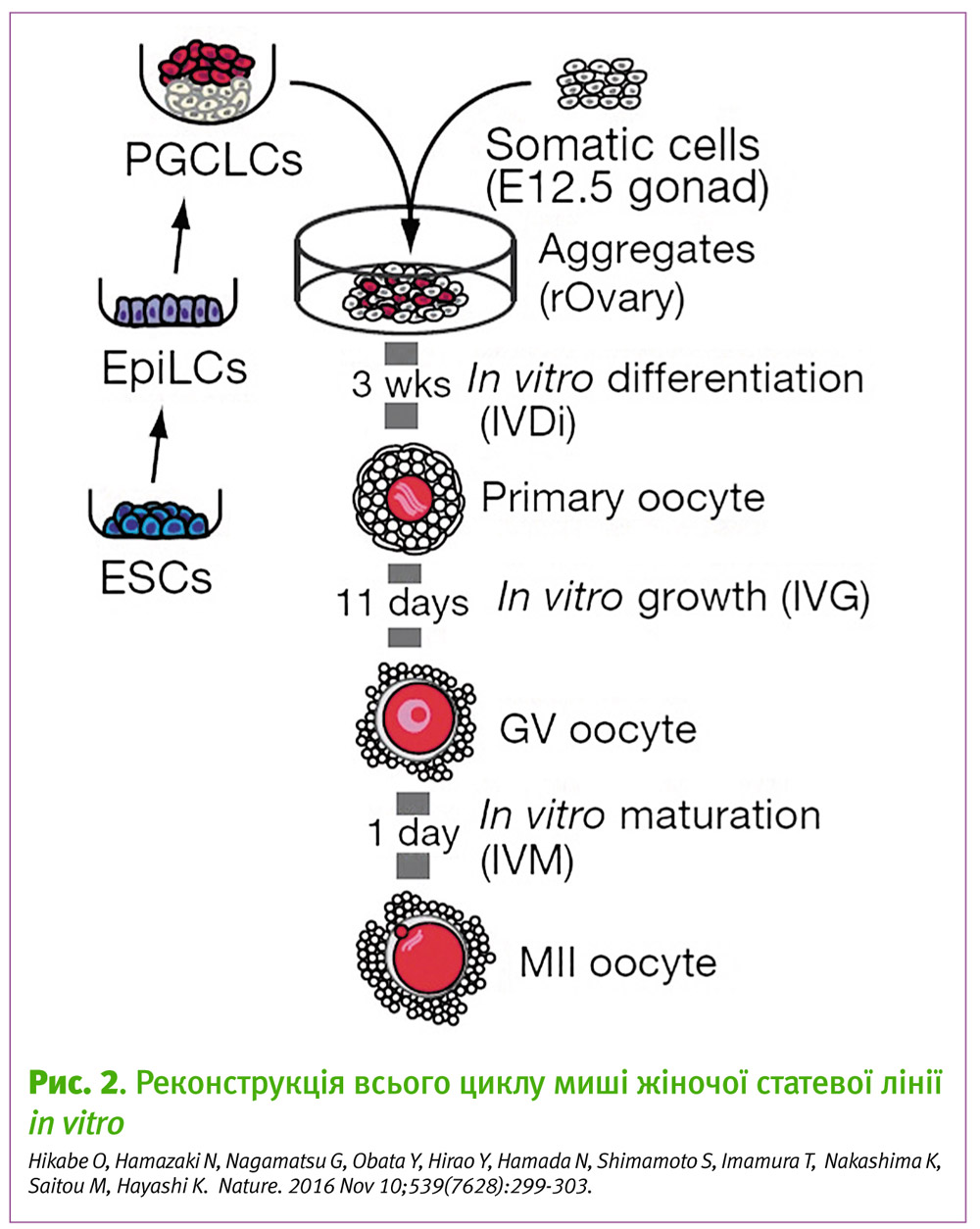
Систему, що слугувала середовищем для розвитку яйцеклітин, дослідники назвали rOvary (reconstituted ovary). Скаладалась вона з примордіальних гермінативних клітин (ПГК), попередників гаметогенезу, які були диференційовані з іПСК (що походили як з ембріональних міофібробластів, так і з фібробластів дорослих особин) або з ембріональних стовбурових клітин (ЕСК), а також суміші соматичних клітин яєчників мишей і специфічного культурального середовища. Розвиток гамет в чашці Петрі умовно був розділений на 3 етапи: 1) диференціація in vitro, 2) ріст in vitro 3) дозрівання in vitro. Дослідники намагалися імітувати фізіологічні етапи гаметогенезу, на кожному етапі модифікуючи середовище і контролюючи стан клітин.
На 3 день культивування в культурі з’явилися фолікулоподібні структури, а експресія Blimp1 (BV) підвищилася, що відображає природний розвиток ПГК. Ще через 2 тижні, коли маркер BV зник, з’явився маркер яйцеклітин stella (SC).
Імуногістохімічне дослідження підтвердило нормальний перебіг мейозу, за винятком підвищення частоти порушення коньюгації. Вся перша частина займала приблизно 3 тижні, наприкінці якої був сформований ооцит І порядку. В другій частині до культури додавалися середовище, збагачене фолікулостимулюючим гормоном (ФСГ), і через 11 днів змінювали умови і переходили до 3 частини, під час якої приблизно у 30% ооцитів спостерігалося відходження першого полярного тільця.
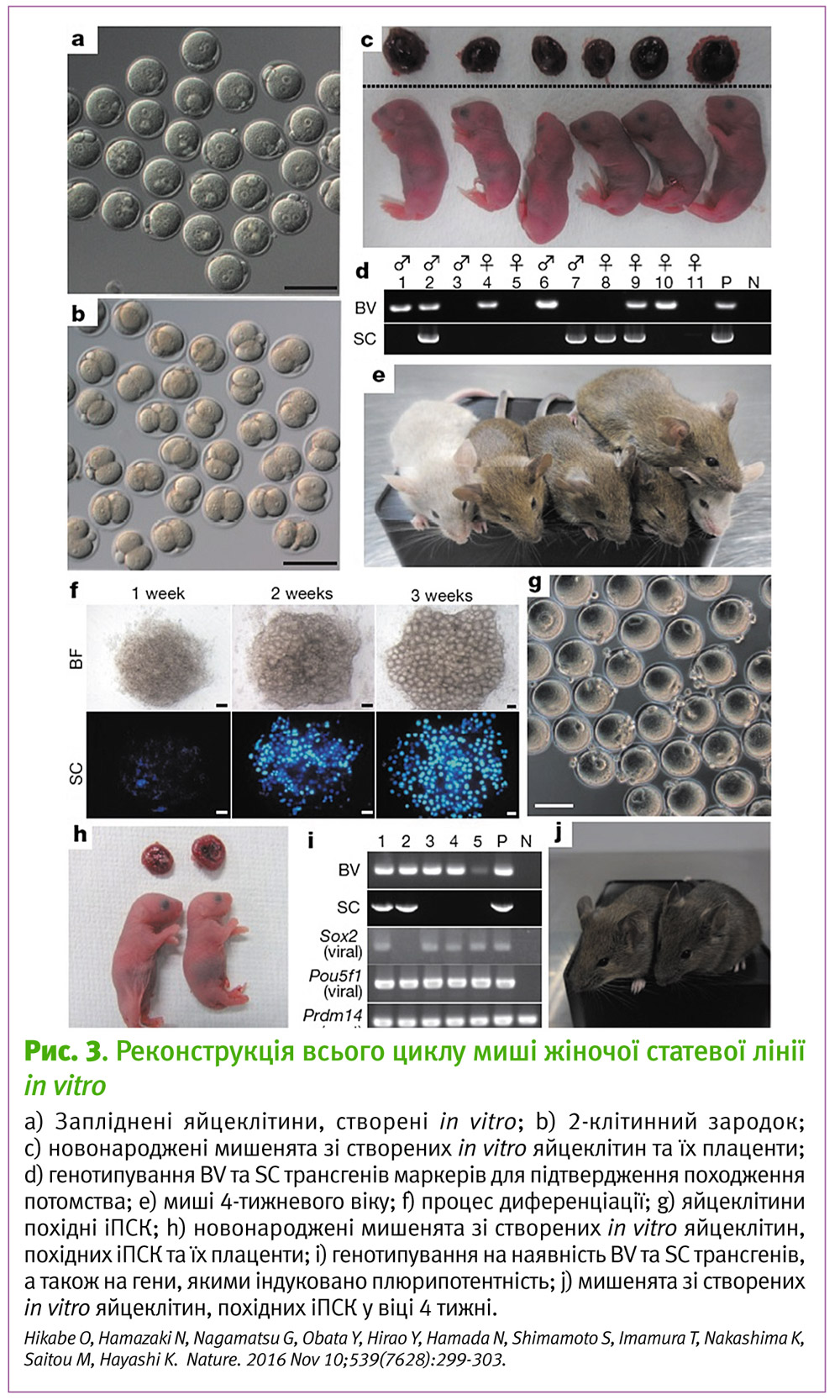
Фенотипово ооцити, вирощені в чашці, мало відрізнялися від вирощених in vivo як за морфологією, так і за розподілом епігенетичних міток на маркерних генах (H19 та Igf2r) (рис. 2).
Для детального порівняння розвитку ооцитів in vitro та in vivo, проводилося динамічне дослідження транскриптому з використанням технології секвенування РНК. Такий вид дослідження показує детальний профіль всіх генів, що експресуються на даному етапі. Ці дані дозволять порівняти розвиток ооцитів in vitro та in vivo, що допоможе вдосконалити технологію. Крім того, таким чином створюється нова модель для дослідження гаметогенезу.
Для остаточного підтвердження нового методу ооцити були запліднені за допомогою IVF (in vitro fertilization), та з використанням сурогатної матері отримано потомство як чоловічої, так і жіночої статі. Хоча при цьому спостерігалося підвищення частоти зупинки розвитку ембріона, більшість особин у потомстві не відрізнялися від мишей дикого типу і в подальшому були здатні до репродукції. У лютому 2018 року лабораторія Единбурзького університету заявила, що їм вдалося провести подібну диференціацію in vitro і з людськими оогоніями, проте на час публікації цієї статті опис дослідження є недоступним. Робота японських біологів розвитку відкриває потенційну можливість отримати «етично чисті» яйцеклітини прямо з соматичних клітин. Втім, ще один короткий етап поки лишається нездоланним: для початку розвитку ооцитів все одно потрібні клітини яєчника.
Щодо сперматогенезу, то у цьому напрямку таких карколомних результатів ще не отримано, хоча є роботи, що in vitro доводили примордіальні гермінативні клітини до фенотипу сперматогонієподібних клітин, частина з яких була здатна до мейозу та утворення гаплоїдних клітин [5].
Поки чоловічий бік питання ще не вирішений, можна продовжити спекулювати на тему майбутьного репродуктивних технологій, і хоча штучна диференціація гамет теоретично можлива навіть за сучасного стану речей, беручи до уваги експерименти з химерами, до майбутнього з конвеєрами зі створення людей, описаного Олдосом Гакслі у своїй антиутопії «О дивний світ новий», не вистачає ще багатьох складових, наприклад, штучної матки (про яку ми писали в одному з попередніх номерів журналу).
Повний перелік літератури знаходиться у редакції.

коментарів