Огляд матеріалів консенсусної Міжнародної групи аналізу глибокого ендометріозу IDEA (International Deep Endometriosis Analysis group) та пропозицій щодо їх практичного застосування
Ендометріоз – це захворювання, що уражає переважно жінок дітородного віку з поширеністю 4,7–5% (Falcone, 2018; Bazot, 2017). Це гетерогенне захворювання з типовими і атиповими ураженнями, що зустрічаються у різних його видах від перитонеальних імплантатів до ендометріоми яєчників, глибоких інфільтративних ендометріоїдних вузлів (Deep Infiltrating Endometriosis – DIE). Такі вузли інфільтрують очеревину на глибину понад 5 мм і можуть спричинити ретроцервікальну облітерацію (Guerriero, 2016). Такі ураження виникають у результаті відкладання тканини ендометрію поза порожниною матки: у яєчниках, на очеревині тазу, в дугласовому просторі, прямій кишці, ректосигмоїдному відділі, ректовагінальній перегородці, на крижово-маткових зв’язках, у стінках піхви та сечовому міхурі (Ajossa, 2015). Ендометріоз може бути як безсимптомним, так і проявлятися хронічним тазовим болем та субфебрилітетом, з неплідністю або без неї.
У сучасній клінічній практиці золотим стандартом для остаточної діагностики та планування лікування симптомного ендометріозу є лапароскопія. Правильно встановлений діагноз має принципово важливе значення для вибору оптимальної стратегії та лікувальної тактики (Tompsett, 2018).
Значення ультрасонографії
Ультрасонографія – це надійний метод первинної візуалізації для обстеження пацієнток з гінекологічними захворюваннями. У хворих з підозрою на ендометріоз ультрасонографія, по-перше, використовується для оцінки та визначення етіології симптомів у пацієнтки; по-друге, дозволяє потенційно визначати локалізацію хвороби. Зрештою, названий метод дозволяє встановити ступінь захворювання.
З клінічної точки зору, результати фахово виконаноної ультрасонографії можуть бути корисними для пацієнтів, тим самим забезпечуючи глибоке розуміння захворювання як пацієнткою, якій необхідно надати інформовану згоду для вибору лікування, так і лікарем, який може адекватно підготуватися до потенційно складного хіруругічного втручання. У більшості випадків, коли йдеться про глибокий інфільтративний ендометріоз (deep infiltrative endometriosis – DІE), для лікаря необхідно та важливо розглянути питання про скерування такої пацієнтки до відповідного досвідченого гінеколога-хірурга. Також може знадобитися залучення до операції інших фахівців, таких як проктологи чи урологи. Адже все частіше хірургічне лікування ендометріозу виконується за медичними показами і операції можна уникнути або ж її відтермінувати (Holland, 2013).

Настанови щодо обстеження при ендометріозі
У 2016 році Міжнародна група із аналізу глибокого ендометріозу (International Deep Endometriosis Analysis group –IDEA) опублікувала інформацію щодо системного підходу до сонографічної оцінки тазу у пацієнток із підозрою на ендометріоз (Guerriero, 2016). Ця консенсусна заява була розроблена для стандартизації анатомічних орієнтирів, номенклатури захворювання та застосування режимів ультразвуку з метою виявлення DІE. Метою консенсусу є забезпечення того, щоб ультрасонографічне дослідження у пацієнток із потеційно початковим ендометріозом виконували згідно зі стандаризованою схемою. Це стосується вимірювань ендометріоїдних вогнищ; термінології, яка використовується; описів локалізації гетеротопій, а також ультрасонографічних особливостей проявів ендометріозу (аденоміозу, злукового процесу малого тазу), які теж повинні бути спільними. Цей консенсус також включає рекомендації щодо того, як збирати анамнез, як правильно виконати клінічне обстеження, як виконувати УЗД і який з методів УЗД застосовувати при обстеження пацієнток з підозрою чи вже підтвердженим ендометріозом.
Деталізований клінічний анамнез повинен бути ефективно зібраним у всіх пацієнток з підозрою на ендометріоз, з особливою увагою на симптоми, що відносять до ендометріозу (табл. 1).
Гінекологічне дослідження слід проводити до або після ультрасонографічного дослідження з метою визначення наявності чи відсутності ендометріозу піхви чи прямої кишки. Таке обстеження повинне включати огляд у дзеркалах слизової стінок піхви та шийки матки на наявність DIE та вагінальну пальпацію, при якій ретельно оцінюють мобільність, фіксацію та/або болючість матки.
Ультрасонографічне дослідження
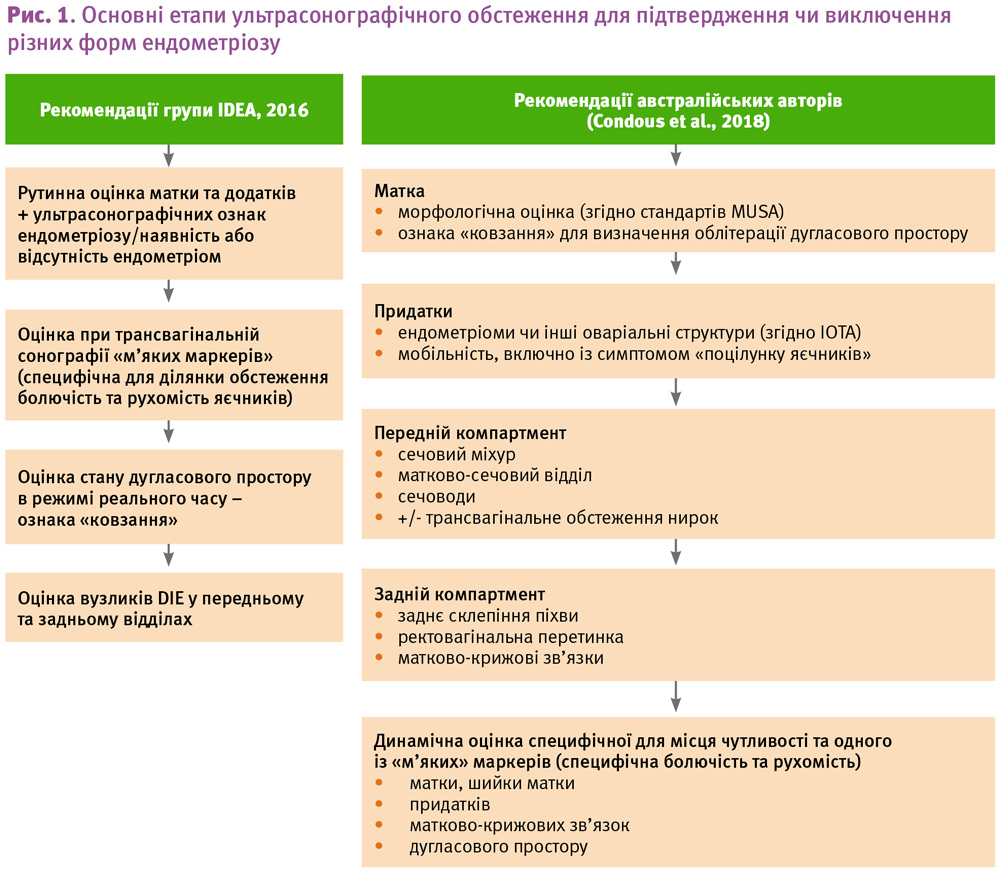
Для оглядової сонографії експерти запропонували алгоритм із чотирьох етапів, який включає рутинне обстеження матки і придатків, виявлення так званих «м’яких маркерів», таких як специфічна локальна чутливість (site-specific tenderness – SST), оцінка дугласового простору за допомогою «ознаки ковзання» та оцінка наявності вузлів DІE в кожній частині тазу. Автори наголошують, що порядок виконання цих етапів може змінюватися з урахуванням часу та комфорту для пацієнтки (рис. 1).
Перший крок. Трансвагінальне УЗД застосовують як інструмент візуалізації першої лінії. При цьому сонографіст насамперед повинен вивчити стан матки та придатків. Рухомість матки слід оцінити як: нормальну, обмежену або фіксовану (сонографічні ознаки аденоміозу слід шукати та описувати, використовуючи терміни та визначення, згідно з опублікованим консенсусом «Morphological Uterus Sonographic Assessment (MUSA) group» (Van den Bosch, Dueholm, 2015). Сонографічні характеристики будь-якої ендометріоми повинні бути описані відповідно до Міжнародної термінології аналізу пухлини яєчників ІОТА (Timmerman D, Valentin L, Bourne TH, 2000).
Другий крок – пошук сонографічної ознаки специфічної локальної чутливості (SST), чи «м’яких маркерів»: локальної чутливості, болючості та фіксованості яєчників. Наявність «м’яких маркерів» підвищує вірогідність поверхневого ендометріозу та гетеротопій. Застосовуючи компресію між маткою та яєчником, можна оцінити, як фіксований яєчник до матки – до середини, до бокової стінки тазу в бічному напрямку чи до зв’язок. Також визначають, чи є вільна рідина в порожнині тазу, тонкі ниткоподібні структури (зрости), які можна побачити між яєчниками, маткою та очеревиною.
Третій крок – оцінка стану Дугласового простору. Використовуючи трансвагінальний датчик в режимі реального часу, визначають ознаку «ковзання» шляхом застосування динамічної ультрасонографії. При цьому лікар виконує ультразвукове дослідження, оцінюючи органи малого і їх мобільність в реальному часі в Дугласовому просторі. Якщо при трансвагінальному дослідженні бачимо, що передня, або задня стінки прямої кишки чи передня стінка сигмовидної кишки не ковзають плавно над ретроцервіксом або задньою стінкою матки чи її дном відповідно, тобто принаймі одна із локалізацій має негативну ознаку «ковзання», то дугласів простір оцінюється як облітерований.
Останій, четвертий крок – пошук вогнищ глибокого інфільтративного ендометріозу (DIE) у передніх та задніх відділах малого тазу.
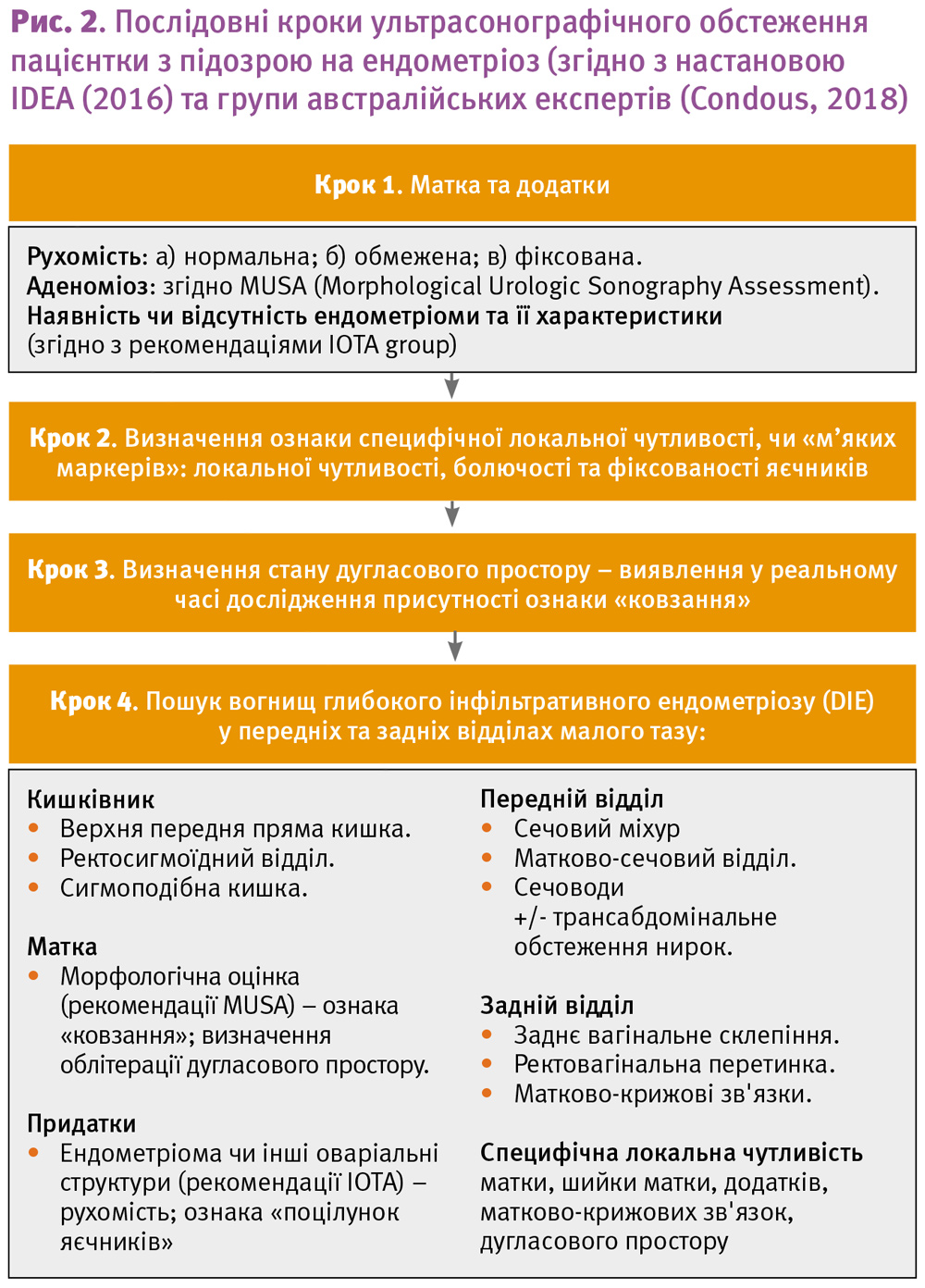
Дослідження придатків
Візуалізація придатків включає оцінку яєчників і фалопієвих труб. Будь-які аномалії повинні бути кількісно визначені, виміряні та задокументовані. Сонографічні характеристики будь-яких структур яєчників повинні бути описані відповідно до термінології, опублікованої групою Міжнародного аналізу пухлини яєчників (IOTA) (Timmerman D, Valentin L, Bourne TH, 2000). Якщо візуалізується ендометріома, існує значно вища ймовірність множинних уражень DІE.
Про рухомість яєчників можна стверджувати, застосувавши тиск на яєчники за допомогою датчика. Немобільні яєчники вважаються «м’яким маркером», що потенційно вказує на наявність поверхневого ендометріозу тазу та/або DІE. Лікар повинен відстежувати рухомість яєчників щодо бокових стінок тазу – латерально, матки – медіально, матково-крижові зв’язки – знизу, і один відносно другого. «Поцілунок» яєчників – ультразвукова діагностична ознака яєчників, що прикріплені один до одного, додатково вказує на внутрішньочеревні спайки, можливо також маткових труб та/або кишок.
При ендометріозі можна виявити патологію маткових труб: гідросальпінкс або гематосальпінкс. Це слід враховувати при диференціальній діагностиці.
Порядок дослідження простору між маткою і суміжними органами
Передній відділ цього простору складається з сечового міхура, маткової зони і сечоводів. На цьому етапі сканування невелика кількість сечі у сечовому міхурі не спричинює труднощів, оскільки трохи наповнений сечовий міхур може зменшити частоту помилкових негативних результатів.
Анатомічні орієнтири сечового міхура мають відношення до місць розташування DІE. М’язова оболонка стінки сечового міхура є найбільш вразливим місцем, що зазнає впливу DІE, тоді як основа міхура є найбільш вірогідною ділянкою DІE. Ураження можуть проявлятися як гіпоехогенні лінійні або сферичні ураження, з або без чітких контурів.
Матково-міхурову зону слід досліджувати щодо фіксації до матки (тобто облітерації простору). Тут також може бути застосована концепція «знаку ковзання».
Лікар, який описує результати ультрасонографії, повинен аналізувати анамнез хвороби пацієнтки. Він повинен тримати датчик в передньому відділі однією рукою, а іншу над лоном на передній черевній стінці. Балотуючи матку між датчиком і рукою, сонографіст може визначити, чи задня стінка міхура вільно переміщується по передній стінці матки. Оцінка облітерації переднього дугласового простору: незалежне переміщення сечового міхура з матки є позитивною «ознакою ковзання». Якщо сечовий міхур і матка рухаються разом, сонографіст повинен задокументувати це як негативну «ознаку ковзання».
Для ідентифікації сечоводів слід утримувати датчик по серединній лінії у сагітальній площині, спрямовуючи його на сечовий міхур, і спочатку ідентифікувати уретру. Далі датчик потрібно перемістити у бік до тазової стінки. Необхідно оцінювати дилатацію сечоводу, а при наявності – вимірювати відстань між дилатацією і дистальним отвором сечоводу. При діагностиці DIE слід сканувати нирки для виключення гідроуретеронефрозу, який може існувати при безсимптомному стенозі сечоводу.
Зони задніх відділів включають крижово-маткові зв’язки, заднє склепіння піхви, ректовагінальну перегородку, передню стінку прямої кишки, передній ректосигмоїдний згин і сигмоподібну кишку. Оскільки кишку вже досліджено, автори пропонують, щоб цей етап ультразвуку передбачав оцінку заднього склепіння піхви, ректовагінальну перегородку та крижово-маткові зв’язки. Група IDEA опублікувала схему для диференціації ректовагінальної перегородки від заднього склепіння піхви. Для кращої ідентифікації виявлення DIE у піхві та/або ректовагінальнй перегородці можна застосувати соновагінографію.
Подібно до маткових труб, крижово-маткові зв’язки зазвичай не візуалізуються при ультрасонографії (якщо немає вільної рідини у дугласовому просторі). Їх можна візуалізувати лише у випадку патології.
Останнім елементом сканування є динамічна оцінка ковзання як одного з м’яких маркерів». Автори рекомендують цей етап дослідження виконувати останнім, щоб запобігти перериванню або припиненню сканування, при виникненні больового синдрому, також лікар до цього є вже більше знайомий із анатомією даної пацієнтки. Як зазначено вище, важливо інформувати пацієнтів, що вони можуть відчувати дискомфорт або біль. Більше того, їхній зворотний зв’язок із сонографістом, який виконує сканування, має важливе значення. Ключовими анатомічними місцями для оцінки в цьому компоненті сканування є матка, придатки, матково-крижові зв’язки і дугласів простір. Необхідно підготувати детальний звіт, який охоплює всі результати, нормальні або патологічні.
Критичний перегляд настанов IDEA
Група австралійських вчених у квітні 2018 року на основі аналізу власних спостережень опублікували статтю під назвою «Як виконувати ультрасонографічне дослідження при ендометріозі?» («How to perform an ultrasound to diagnoses endometriosis»), яка мала на меті чітко окреслити практичний, ефективний і комплексний метод проведення ультразвуку тазових органів для оцінки DІE (George Condous, Mathew Leonardi et. al., 2018). Ще раніше ними ж було проведене декілька досліджень, в т. ч. багатоцентрове ретроспективне когортне дослідження (канадська класифікація цільових груп II-2) щодо застосування системи ультразвукового стадіювання ендометріозу (UBESS) для прогнозування труднощів при лапароскопічній хірургії ендометріозу (Tompsett J, Leonardi M, 2018).
Автори запропонували проводити оцінку ендометріозу в іншій послідовності (див. рис. 1). Розпочинати обстеження слід з прямої кишки, а саме, із четвертого етапу системи IDEA, що включає оцінку задніх відділів. Вони пропонують проводити окремо оцінку кишок від інших структур заднього відділення У той час як датчик поступово вводять у піхву (під кутом в напрямку до крижів), можна оглянути на наявність ендометріозу передню стінку прямої кишки, ректосигмоїдний згин і сигмовидну кишку, оскільки вони є ділянками, які уражені найчастіше. Автори запропонували розрізняти верхню і нижню частини передньої стінки прямої кишки, враховуючи хірургічні особливості втручань на них: при лапароскопії видно лише верхню частину прямої кишки, оскільки нижня її частина розташована заочеревинно.
Лікарі-сонографісти повинні розуміти анатомію стінки кишки, помічати потовщення гіпоехогенних м’язових структур або наявність гіпоехогенних вузлів. Ці ураження можуть містити гіперехогенні вогнища. Будь-яке ураження, виявлене у стінці кишки, слід записувати у трьох ортогональних площинах (довжина у середній сагітальній площині, товщина у передньо-задній площині та поперечний діаметр у поперечній площині), а відстань між нижнім краєм найбільш каудального і анальний край необхідно вимірювати. Якщо виявляють ураження, морфологічний вид його потрібно задокументувати згідно типу ураження, що описані у консенсусі IDEA. Крім того, прилеглі ділянки слід уважно оцінювати щодо наявності DІE стінки кишки. Підготовка кишки є корисною для ліпшого виявлення уражень на прямій кишці, однак автори вважають, що найважливішим аспектом для ідентифікації уражень є досвід та експертний клас сонографіста.
Наступним кроком є опис матки, її орієнтація, розміри в трьох площинах. Пацієнтки з ендометріозом мають високу вірогідність одночасного аденоміозу, тому треба ретельно описувати його ознаки згідно стандартів MUSA (Van den Bosch T, Dueholm M, 2015).
Третім кроком автори пропонують оцінювати стан сечового міхура із застосуванням ознаки «ковзання».
Висновки
Отже, у поданих публікаціях висвітлені нові, сучасні рекомендації щодо методології, термінології, системності та послідовності виконання УЗД пацієнток із клінічними проявами ендометріозу та раніше діагностованим захворюванням. Підходи ґрунтуються як на консенсусному висновку групи IDEА, так і на практичному досвіді, що оптимізує ефективність та підвищує комфорт пацієнтки. Кожна установа може вирішити для себе, які рекомендації застосовувати у своїй повсякденній практиці, або ж розробити власні. Автори наголошують на важливості виконання таких обстежень лікарем із певним досвідом та включення всіх етапів з консенсусної заяви IDEA.


коментарів