Нарушения сердечного ритма плода вызывают большой практический интерес у перинатологов и детских кардиологов, так как могут быть проявлением врожденных структурных аномалий и (или) внутриутробного страдания плода. Проводящая система сердца созревает к 16 неделям беременности и функционирует в соответствии с регулирующим влиянием вегетативной нервной системы. Чаще всего аритмии у плода (АП) проходят спонтанно еще во время внутриутробного периода жизни или после родов, но могут приводить и к фатальным осложениям [3, 10]
АП – это изменения частоты сердечных сокращений регулярного или нерегулярного характера, выходящие за пределы от 100 до 200 ударов в минуту. Частота АП составляет всего 1%, но около 10% из них имеют риск перинатальной смертности [12, 13]. Хотя большинство вариантов АП имеют доброкачественный характер, некоторые сопровождаются развитием водянки плода и приводят к его антенатальной гибели [3, 16, 19]. Приведенные данные демонстрируют, что 1 плод из 100 может нуждаться в проведении мониторинга сердечной деятельности и антиаритмической терапии.
Известны определенные ограничения диагностических возможностей существующих методов выявления АП. Наибольшей популярностью пользуются ультразвуковые методы изучения сердечного ритма плода. Они позволяют оценить сокращения предсердий и желудочков и внутрисердечную гемодинамику (М-режим, тканевой Доплер, гемодинамический Доплер и цветное Доплеровское картирование) [9, 17, 20]. К недостаткам следует отнести кратковременность исследования (всего несколько секунд), необходимость наличия квалифицированного специалиста и возможность проведения только в клинических условиях.
Ультразвуковая кардиотокография (КТГ) является широко доступным и очень популярным методом оценки частоты сердечных сокращений плода. Однако этот метод основан на отражении ультразвуковой волны от сокращающегося сердца, то есть способен лишь регистрировать механические кардиоинтервалы. Помимо этого, в технологии обработки сигналов испльзуется методика временного усреднения за период 2,6 с, что не позволяет рассматривать КТГ как информативный метод диагностики АП [8, 18 ].
Наилучшими диагностическими возможностями, основанными на регистрации первичных электрофизиологических процессов в сердце плода, обладает магнитокардиография. Однако в виду чрезвычайной договизны этот метод не может быть использован в практическом здравоохранении [7]. Возможно изучение морфологии комплексов PQRST с помощью фетального монитора STAN (STAN, Neoventa Medical, Molndal, Швеция). В этом оборудовании используется технология инвазивной ЭКГ плода, которую регистрируют с предлежащей части плода. Поэтому может быть применено для получения зубцов и интервалов фетальной ЭКГ только в родах после разрыва плодных оболочек. В ряде исследований было установлено некоторое улучшение перинатальных исходов в случае использования монитора STAN в родах [15].
В качестве перспективы неинвазивного мониторинга ЭКГ плода может рассматриваться регистрация биоэлектрической активности сердечной деятельности плода с передней брюшной стенки матери. Неинвазивная ЭКГ плода является недорогим и высокоинформативным, но до настоящего времени недостаточно изученным методом. Портативные приборы для осуществления неинвазивной ЭКГ плода совместимы с компьютерными системами обработки данных и беспроводными передающими устройствами, что обеспечивает возможность длительного непрерывного мониторинга [1–6]. Данные некоторых исследований демонстрируют, что этот метод позволяет изучать характеристики сердечного ритма плода. Хотя возможности клинической интерпретации полученных данных пока только на начальной стадии изучения [3, 11].
Ряд работ, проведенных совместно с иностранными коллегами на базе Харьковского городского перинатального центра, позволил установить целый ряд достоинств неинвазивной ЭКГ плода. Некоторые результаты были включены в международную базу данных АП PhysioNet [3, 13].
Основным выводом, который можно сделать на основании этих исследований, является положение о том, что неинвазивная ЭКГ плода позволяет диагонстировать нарушения сердечного ритма плода.
Прежде всего, неинвазивная ЭКГ плода дает возможность более длительной регистрации по сравнению с ультразвуковыми методами исследования. Это позволяет получить дополнительную информацию, что способствует лучшему пониманию природы АП.
Использование алгоритмов выявления АП, разработанных J. Behar (Tecnion, Israel), обеспечивает автоматизированную диагностику АП. Это было подтверждено проверкой двумя независимыми перинатальными кардиологами. В дальнейшем подобное программное обеспечение может быть использовано для проведения Холтеровского мониторирования ЭКГ плода в домашних условиях. Это дает возможность регистрировать эпизоды АП – пароксизмальной тахикардии. Неинвазивная ЭКГ плода позволяет диагностировать нарушения проводимости в виде АВ-блока и блокады ножки пучка Гиса. Последнее недоступно в случае использования УЗД. К сожалению, только в 69% случаев текущая технология неинвазивной ЭКГ плода может обеспечить достоверную идентификацию зубца P на записи [3]. Проблема кроется в низком соотношении сигнал/шум. Хотя кардиологи очень часто заинтересованы в качественной регистрации предсердного зубца. Действительно, в случае необходимости подтверждения АВ-блока II степени (проведение сигнала от предсердий к желудочкам составляет 2:1) наличие или отсутствие зубца P является одним из ключевых моментов.
Полный АВ блок у плода является необратимым без лечения. Его возникновение связывают с аутоиммунным механизмом. АВ-блок I или II степени может сопровождаться спонтанным восстановлением сердечного ритма [14]. Брадикардия является спутником АВ-блока. АВ-блок II степени может быть результатом нарушенного проведения импульса к желудочкам ввиду трепетания предсердий. При этом варианте АП частота сокращений предсердий составляет от 300 до 600 в минуту, а желудочков – в два раза меньше. Трепетание предсердий встречается в 1/3–1/4 случаев тахиаритмии у плода [10, 12].
Лечение АП начинают in utero с учетом трансплацентарного проникновения антиаритмических препаратов к плоду. Терапия АВ блока зависит от природы и степени этого расстройства. Наличие водянки плода является неблагоприятным фактором, ухудшающим прогноз. При этом незрелость плода снижает его чувствительность к антиаритмическим препаратам [16]. Также неблагоприятными прогностическими факторами являются трикуспидальная регургитация и конгестивная сердечная недостаточность [19].
Возможно использование инвазивных методик введения лекарственных средств плоду. Среди них выделяют: интраамниальное, интраперитонеальное, внутрипуповинное и внутрисердечное введение. При полном АВ-блоке возможно использование кортикостероидов, несмотря на противоречивые результаты их применения [10]. Накоплен опыт применения дигоксина, флекаинида, соталола и амиодарона в лечении АП. Наилучшей биодоступностью ввиду полного перехода через плаценту обладает соталол. Иногда введение антиаритмиков продолжают после рождения [12, 14].
Экстрасистолия часто встречается в сочетании с АВ-блоком I и II степени и удлиненном интервале QT [16, 19]. Иногда злокачественная желудочковая экстрасистолия (torsade de pointes) может повышать риск фибрилляции и асистолии. Предсердные экстрасистолы могут приводит к тахикардии и нерегулярному ритму. Желудочковые экстрасистолы при отсутствии врожденных пороков развития плода, миокардита, АВ-блока или удлиненного интервала QT обычно являются доброкачественными [7, 16]. Поэтому наличие экстрасистол у плода требует дальнейшего наблюдения и дообследования. В данной статье мы приводим 3 собственных наблюдения АП. Во всех этих случаях неинвазивная ЭКГ плода была использована для диагностики АП. Неинвазивную ЭКГ плода получали путем методики абдоминального отведения с помощью оборудования Кардиолаб Бебикард.

Случай 1
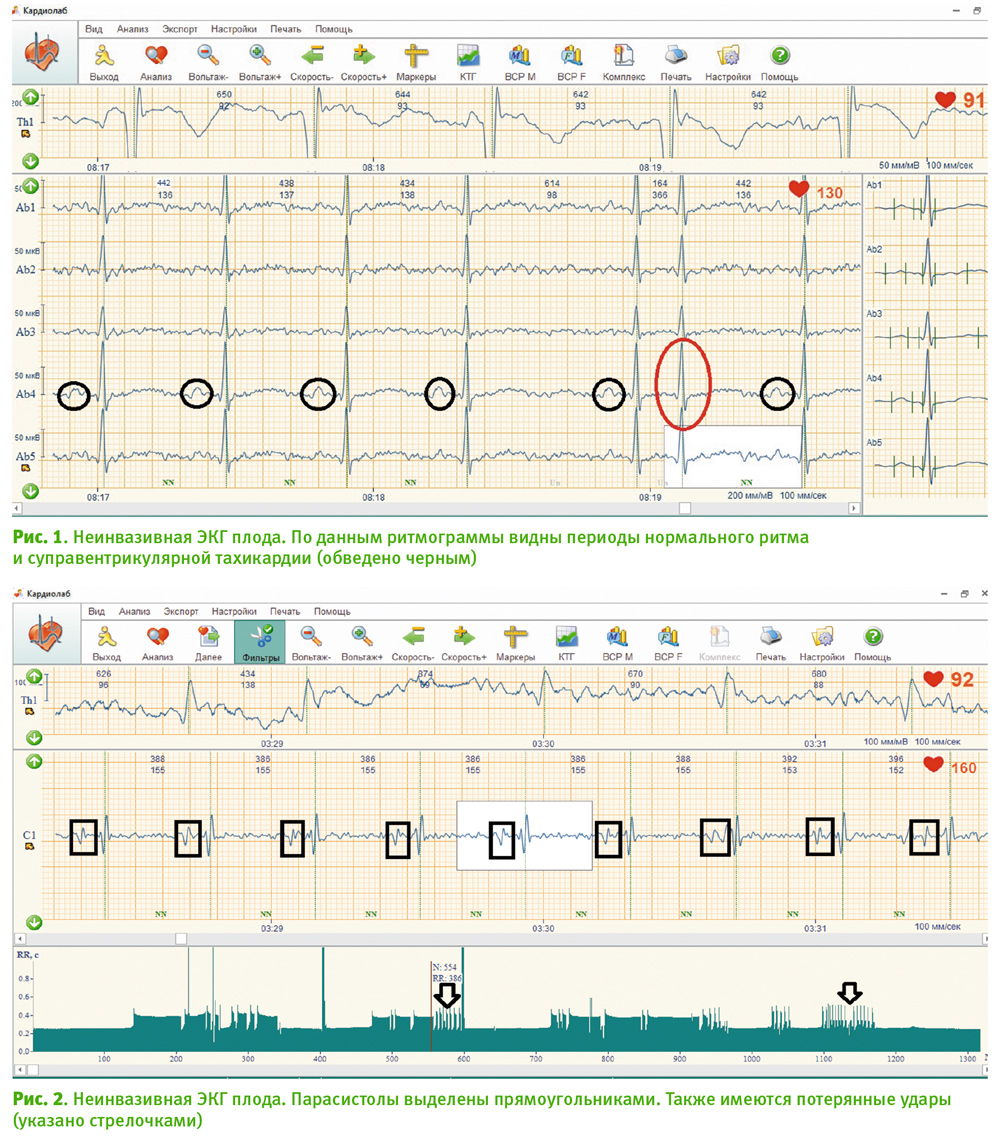
Беременная 29 лет находилась на лечении в связи с угрожающими преждевременными родами в сроке беременности 23 недели. Получала токолитическую терапию. Ввиду «короткой» шейки было проведено введение разгружающего пессария. По данным УЗИ, была диагностирована суправентрикулярная тахикардия плода. Данные о наличии структурных аномалий у плода отсутствовали. Была проведена неинвазивная ЭКГ плода (рис. 1). Установлено наличие суправентрикулярной тахикардии (ЧСС около 230 уд./мин.) и парасистолии (рис. 2). В процессе наблюдения произошло спонтанное восстановление синусового ритма. Пациентка выписана домой через 10 дней. По данным УЗИ и неинвазивной ЭКГ плода в 26 и 32 недели беременности, АП обнаружено не было. Родила в сроке беременности 37 нед. живого доношенного мальчика массой 3100 г, длиной тела 50 см в состоянии по Апгар 8/9 баллов.
Случай 2
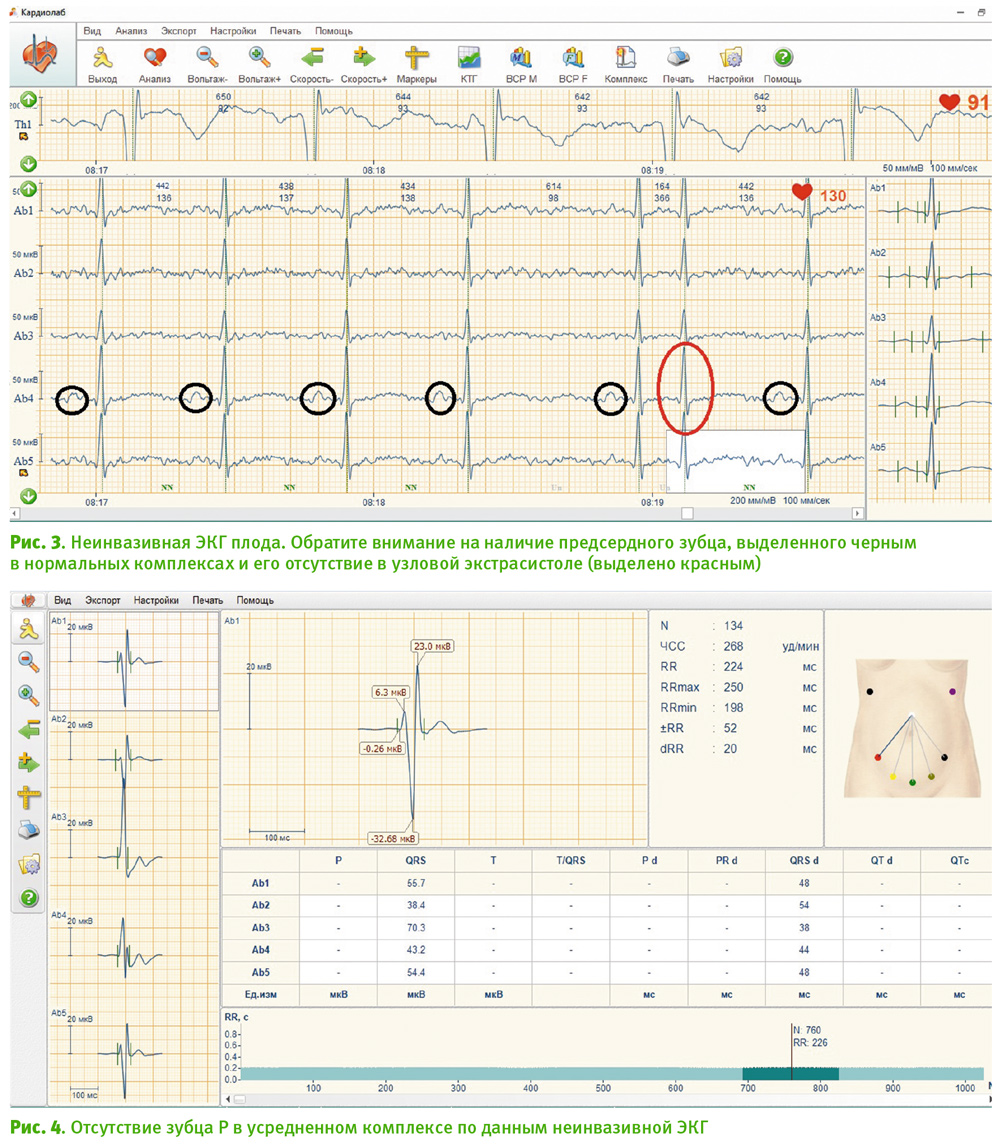
Беременная 30 лет была госпитализирована для подготовки к родам в сроке 37 нед. Данная беременность первая, наступила вследствие ЭКО. По данным КТГ и УЗИ, был диагностирован дистресс плода (ареактивный нестрессовый тест и нулевой кровоток в артерии пуповины). Проведена неинвазивная ЭКГ плода. Обнаружено наличие узловых экстрасистол (рис. 3).
Было проведено экстренное кесарево сечение. Извлечена живая доношенная девочка массой 2900 г, длиной тела 48 см в состоянии по Апгар 6/7 баллов с двухкратным тугим обвитием вокруг шеи плода. У новорожденной сохранялась экстрасистолия. Выписана под наблюдение детского кардиолога.
Случай 3
У первобеременной 25 лет была диагностирована суправентрикулярная тахикардия у плода в сроке 25 нед. Анамнез без особенностей. Течение беременности гладкое. По данным УЗИ структурных аномалий у плода не выявлено, показатели маточно-плацентарной и плодово-пуповинной гемодинамики нормативные. По данным неинвазивной ЭКГ плода, было обнаружено отсутствие зубца Р (рис. 1). Это можно объяснить тем, что на фоне значительной тахикардии зубец Т наслаивается на зубец Р [1, 16, 19]. Частота сердечных сокращений была около 270 ударов в минуту. После консультации кардиолога была начата трансплацентарная «атака» соталола (по 80 мг 3 раза в сутки). В течение 2 суток синусовый ритм восстановился.
В дальнейшем беременность протекала гладко. Родила в сроке 40 недель живую доношенную девочку массой 3600 г, длиной тела 55 см в состоянии по Апгар 8/9 баллов. Новорожденная выписана домой в удовлетворительном состоянии.
Проведенная работа демонстрирует хорошие предпосылки для разработки междисциплинарного консенсуса совместно с детскими кардиологами в связи с появлением новых данных о возможностях использования неинвазивной ЭКГ плода в перинатологии.


коментарів