Огляд клінічних настанов Ендокринологічного товариства
Шановні читачі, пропонуємо ознайомитися з основними положеннями настанов, опрацьованих Ендокринологічним товариством за участі Американського товариства репродуктивної медицини, Європейського ендокринологічного товариства та педіатричного ендокринологічного товариства та опублікованих у травні 2017 року, щодо функціональної гіпоталамічної аменореї
Коротка довідка
Функціональна гіпоталамічна аменорея (ФГА) – це форма хронічної ановуляції за відсутності її органічних причин (Yen 1973).
Термін «функціональний» означає, що корекція або поліпшення стану причинних поведінкових факторів може відновити овуляторну функцію яєчників. Безпосередньою причиною ановуляції є функціональне зменшення впливу ГнРГ, яке проявляється як зниження частоти пульсацій ЛГ (Berga, 1975). Зменшення впливу ГнРГ призводить до недостатності рівнів ЛГ і ФСГ для підтримки повного циклу фолікулогенезу і овуляторних функцій яєчників. Забезпечення екзогенного надходження ГнРГ або гонадотропінів відновлює фолікулогенез (Hurley, 1993). Klinefelter et al. (1943), щоб описати цей стан, спочатку використовували термін «гіпоталамічна гіпоестрогенія». Крім того, схильність до розвитку ФГА може бути генетичною, такою як гетерозиготний вроджений гіпогонадотропний гіпогонадизм (Caronia, 2011).
Нейромодуляторних сигналів, які впливають на вісь гіпоталамус-гіпофіз-статеві залози, досить багато. Відомо, що суттєву роль тут відіграє вісь гіпоталамус-гіпофіз-наднирники (ГГН). Відомо, що гіперкортизолемія пригнічує секрецію гонадотропін-рилізинг-гормонів (ГнРГ), Такий ефект може ініціюватися обмеженням харчування, надто інтенсивним фізичним навантаженням з використанням більшої кількості калорій, ніж надходить в організм (наприклад, у професійних спортсменок або військових), екстремальним стресом тощо. Активність ГнРГ і системи кіспептинів можуть порушувати й ендокринні дизраптори, наприклад бісфенол А, який є практично у будь-якому пластиковому посуді.
Стресові чинники, незалежно від їх типу, активують вісь ГГН і вегетативну нервову систему, що призводить до появи комплексу нейроендокринних розладів. Це, зокрема, гіпоталамічний гіпотиреоз, який забезпечує економію енергетичних ресурсів (Berga, 1997). Відомо також, що добова екскреція кортизолу у жінок з ФГА є підвищеною. Така «стресова система» задіює низку цілком конкретних анатомічних структур: гіпоталамічні паравентрикулярні ядра, центральну симпатичну нервову систему, синє ядро та норадреналінову систему стовбура мозку (Mastorakos, 2006).
Негативні наслідки ФГА зумовлені безпосередньо розладами метаболізму, нейроендокринної функції та відсутністю адекватної функції яєчників. Дослідження засвідчили про вищу поширеність серед жінок із ФГА розладів харчування, зокрема, дотримання дієт, булімії, надмірної стурбованості їдою та самообмежень у харчуванні. Відомо також, що відповідні поведінкові інтервенції відновлюють усі ці патофізіологічні ланки.
Найвагомішими наслідками ФГА є запізнілий статевий розвиток, аменорея, неплідність і віддалені наслідки гіпоестрогенії. Неплідність звичайно зумовлена ановуляцією, однак можливими є також пролонгована фолікулярна фаза та неадекватна фаза жовтого тіла (Pirke, 1985, Schweiger, 1991). Тривалість аменореї зумовлена особливістю етіологічного чинника ФГА. Типово, чим довша тривалість аменореї, тим довше відновлюється цикл. У жінок із поєднанням інтенсивних фізичних навантажень та обмеженнями у харчуванні може розвинутися остеопороз і зумовлені ним переломи кісток. Відомо, що повторні переломи кісток трапляються у 30% балерин (Warren, 2002) та представниць інших спеціальностей, де суттєвим є фізичне навантаження. При вагітності, яка настає після зворотного розвитку ФГА, підвищені ризики втрати плода та малого для гестаційного віку плода, особливо якщо цей розлад був зумовлений розладами харчування. Зрештою, тривала гіпоестрогенія може зумовлювати зростання серцевого ризику (Kaplan, 2009).
Діагностика, диференціальна діагностика та обстеження
«Лікарі можуть встановити діагноз функціональної гіпоталамічної аменореї (ФГА) лише після виключення анатомічної або органічної причини аменореї (Некласифікована заява з належної практики)».
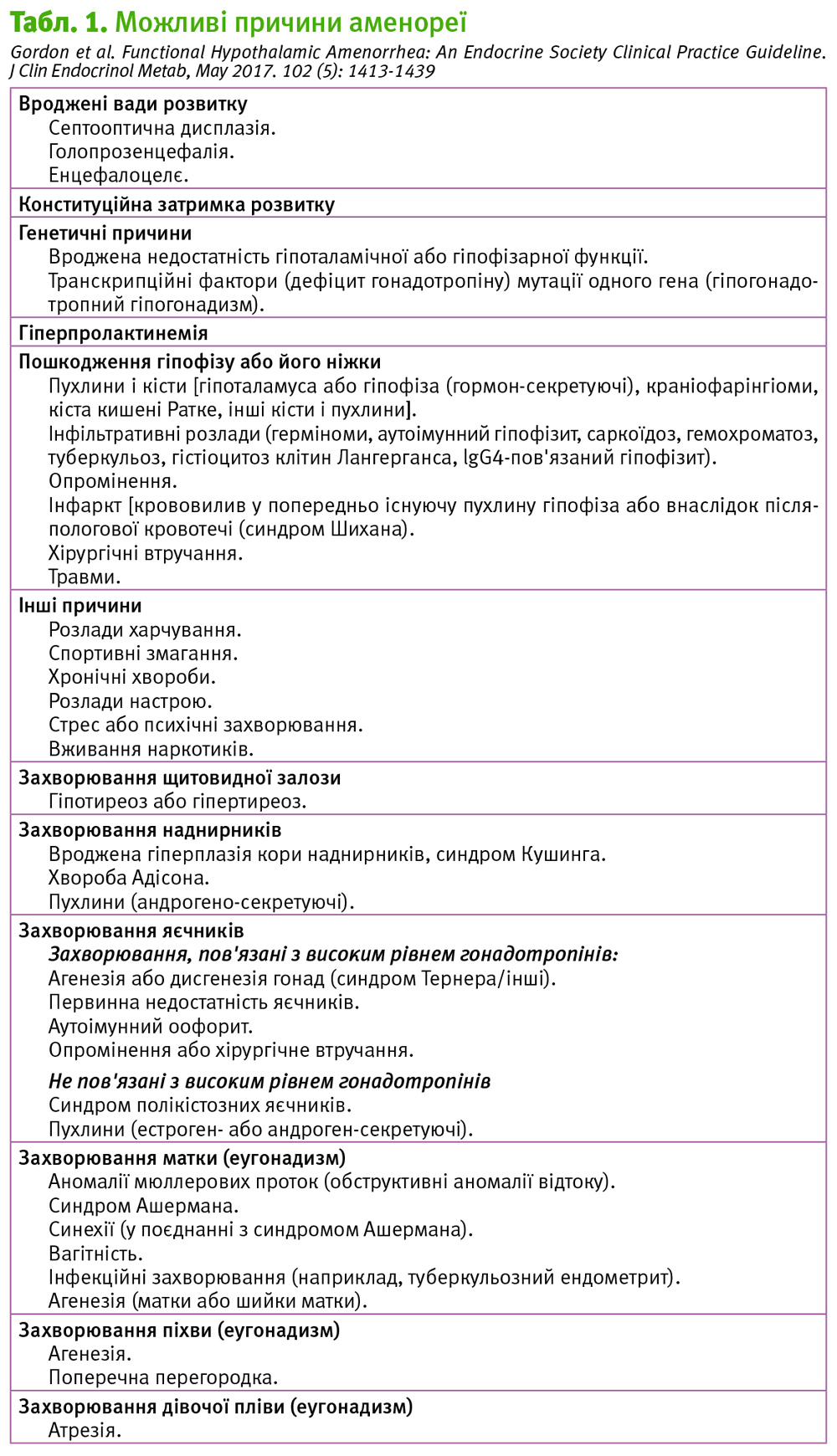
На основі менструальної функції у дівчаток-підлітків клініцисти можуть оцінювати їх естрогенний статус і визначати наявність проблем. ФГА характеризується як відсутність або нерегулярність менструацій і дефіцит естрогенів внаслідок недостатньої стимуляції або пригнічення ГГЯ осі за відсутності анатомічної або органічної патології. У цьому контексті ми використовуємо термін «органічний» для випадків аменореї з неадекватно низькими рівнями гонадотропіну, де існує чітка патологічна етіологія (вони можуть включати в себе випадки, коли рівні гонадотропіну знаходяться в межах нормального діапазону лабораторних значень). У цих випадках треба розглянути широкий діапазон диференціальних діагнозів, щоб переконатись у відсутності фонових етіологій, які можуть проявлятись у формі аменореї (табл. 1). Крім вагітності, найбільш поширеними причинами вторинної аменореї є ФГА і СПКЯ (Balasubramanian, 2010, Golden, 2008).
Основними етіологічними чинниками ФГА є втрата ваги та/або надмірне фізичне навантаження, та/або стрес. Таке визначення дає можливість запідозрити діагноз у пацієнток як з низькою, так і нормальною масою тіла, Крім того, етіологія може включати поєднані чинники. Незалежно від тригера, ФГА характеризується аномальною секрецією та динамікою ГнРГ. Дефіцит енергії (який не завжди супроводжується втратою маси тіла) є критичним чинником як при втраті ваги, так і при надмірному фізичному навантаженні. Williams et al. (2015) виявили, що експериментальне обмеження добової калорійності на 470–810 калорій збільшує частоту розладів менструального циклу. Індивідуальний поріг дефіциту калорій може бути дуже різним, проте відомо, що для молодих дівчат і підлітків він набагато нижчий, ніж для старших жінок.
У дівчат-підлітків та дорослих жінок з ФГА внаслідок дефіциту енергії, існує цілий спектр проявів і/або захворювань внаслідок цього дефіциту. Межі спектру коливаються від випадків навмисного та свідомого споживання недостатньої кількості калорій, що не відповідає енергетичним витратам, до розладів харчової поведінки і тяжкого недоїдання.
Таким чином, маса тіла цих підлітків або дорослих жінок може коливатися від нормальної до дуже низької. Аналогічним чином, існує цілий спектр менструальних статусів, який включає в себе нормальну овуляторну менструацію, субклінічні стани менструальної дисфункції (недостатність лютеїнової фази і нормальну ановуляторну менструацію), та аменорею. У цих молодих жінок мінеральна щільність кісткової тканини коливається від нормальної до низької. Більш високий показник поширеності викликаної фізичним навантаженням аменореї може відбуватися в тих видах спорту і фізичної активності, в яких худорлявість може давати перевагу (наприклад, гімнастика, черлідинг, фігурне катання, біг). Коли вага близька до норми, аменорея може змінюватись нормальною менструацією у періоди, коли тренування менш інтенсивні або відсутні, що свідчить про те, що дисфункцію викликають енергетичні потреби тренування. Було показано, що тяжкість порушення менструального циклу збільшується пропорційно до показників економії енергоресурсів жінкою, яка займається фізичною активністю.
Хоча жінки можуть намагатись зменшити стрес шляхом ініціювання відповідної поведінки, їхні поведінкові реакції часто функціонують, як підсилювач стресу. Таким чином, критичною є психологічна оцінка з метою виключити або перевірити наявність психічного розладу (Американська психіатрична асоціація, 2013). У разі встановлення діагнозу DSM-5 (№5 за Діагностичним керівництвом з діагностики і статистики психічних розладів) рекомендують скеровувати жінок для надання відповідної психіатричної допомоги.
Важливо визнати, що лікарські препарати, такі як нейролептики (типові та атипові), деякі антидепресанти, протизаплідні засоби і опіати зазвичай впливають на менструацію, тому не слід плутати аменорею або нерегулярні менструації внаслідок їх вживання з ФГА. Це пов'язано з антагоністичним ефектом цих засобів на гіпофізарні рецептори допаміну, що зменшує його інгібуючий ефект на секрецію пролактину. Результуюча гіперпролактинемія пригнічує пульсаційне вивільненняГнРГ. Тривале застосування препаратів прогестерону у поєднанні з КОК (у вигляді тривалого прийому препаратів з пролонгованою дією), ін'єкції депо медроксипрогестерону ацетату та тривале застосування внутрішньоматкових систем з гестагенами може призвести до аменореї.
«Діагностику ФГА слід проводити у дівчат-підлітків і жінок, у яких тривалість менструального циклу постійно перевищує 45 днів і/або у яких аменорея триває протягом 3 місяців і більше. (2lÅÅOO)»
Пацієнтки підліткового або дорослого віку з ФГА зазвичай звертаються до лікаря при тривалості аменореї 6 місяців або довше. У жінок підлітковго віку цей стан може бути складно відрізнити від сповільненого дозрівання ГГЯ осі протягом перших років після менархе. Однак, деякі повідомлення свідчать, що тривалість менструального циклу в підлітків зазвичай не перевищує 45 днів, навіть протягом першого року після менархе. Спортсменки можуть повідомляти про різну тривалість періодів аменореї, що віповідають інтервалам інтенсивної фізичної активності, з подальшим періодом нерегулярних менструальних циклів або нормальних менструацій після закінчення сезону тренування. Слід зазначити, що ФГА знаходиться на крайньому кінці шкали функціонального гіпоталамічного гіпогонадизму, яка включає в себе ановуляторну менструацію і нормальну менструацію з недостатністю лютеїнової фази, які асоціюються з неплідністю. Таким чином, у жінок з функціональним гіпоталамічним гіпогонадизмом можуть спостерігатись нормальна менструація і неплідність, а не аменорея. Нарешті, слід зазначити, що мати ФГА можуть близько половини пацієнтів із СПКЯ із фенотипом без гіперандрогенії (тобто, з олігоменореєю та полікістозним виглядом яєчників при ультрасонографії).
Для ФГА характерна відсутність менструації або нерегулярність менструальних циклів внаслідок недостатньої стимуляції і/або пригнічення ГГЯ осі. Це може бути пов'язане зі стресом, занепокоєнням, змінами ваги, енергетичним дисбалансом і/або надмірними фізичними навантаженнями.
«Ми пропонуємо виконувати скринінг пацієнтів з ФГА на психологічні стресори (пацієнти з ФГА можуть добре справлятися зі стресором, а чутливість до стресу визначається багатьма детермінантами) (2lÅÅÅO)».
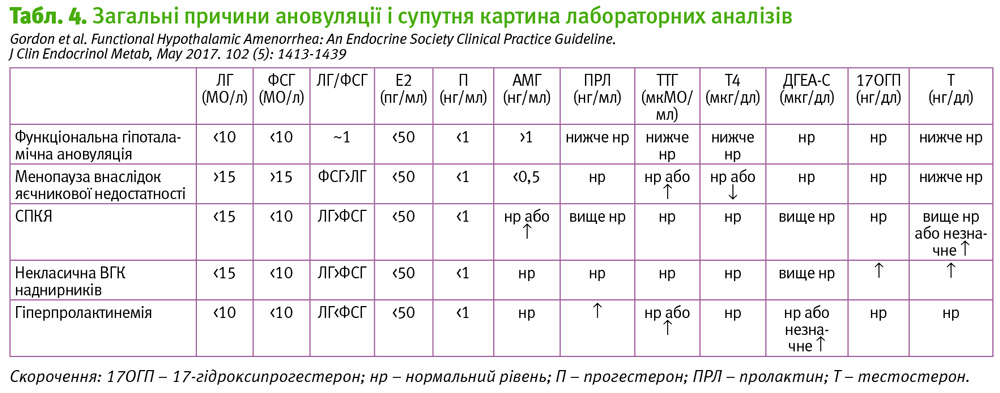
Наявні дані свідчать, що психогенні стимули, як зовнішні, так і внутрішні, активують вісь гіпоталамус-гіпофіз-наднирники. Будь-яка психогенна подія (наприклад, початок навчання у коледжі, глибоке горе, втрата ваги), може викликати збільшення секреції кортизолу, що забезпечує метаболічну адаптацію. Крім того, метаболічна адаптація породжує супутні психогенні захворювання. Незважаючи на те, що комплекс психологічних і метаболічних факторів, пов'язаних з ФГА, може відрізнятися, кінцевим спільним наслідком є пригнічення вивільнення ГнРГ. Психологічні механізми адаптації вимагають перерозподілу ресурсів на системні потреби виживання (Pauli, 2010). У жінок, які активно займаються спортом, вісь ГГН активується для вивільнення глюкози для енергетичних потреб. Крім того, організм зводить до мінімуму енергетичні витрати, що проявляється задіянням осі гіпоталамус-гіпофіз-щитоподібна залоза. При цьому типовими є нормальний або низький ТТГ та низькі рівні тироксину (Т4) та трийодтироніну (Т3) (табл. 2).
Існують дві основні гіпотези, що пояснюють механізм, за допомогою якого негативний енергетичний баланс призводить до ФГА. Гіпотеза метаболічного палива стверджує, що периферичні тканини (печінка, жирова тканина, підшлункова залоза, шлунок, дванадцятипала кишка і задній мозок) здатні виявити короткострокове зменшення кількості доступного для окислення палива (наприклад, здатні короткотривало обмежувати процес окислення глюкози, жирних кислот або кетонових тіл через нейронні або гуморальні сигнали.
Згодом секретуються численні гормони і нейропептиди, які змінюють чутливість зворотного зв'язку в задньому мозку. Інша гіпотеза (гіпотеза критичної кількості жирової тканини) стверджує, що для початку статевого дозрівання і збереження репродуктивної функції необхідна мінімальна кількість жирової тканини. Ці результати не були остаточно підтверджені і не є взаємовиключними, оскільки жирова тканина тіла є відображенням накопичення енергії. Подібно, що жирова тканина бере участь в активації осі ГГН через адипокіни, наприклад, лептин і адипонектин. Одужання від ФГА супроводжується зниженням рівня кортизолу та підвищенням рівнів ТТГ і лептинів без збільшення маси тіла, що засвідчує, що зменшення стресу ослаблює нейроендокринну і метаболічну реакції незалежно від маси тіла.
«Після встановлення діагнозу ФГА клініцистами ми пропонуємо їм ознайомити пацієнтів з різними варіантами відновлення менструального циклу, що відбуваються в фазі одужання. Ми пропонуємо лікарю інформувати пацієнта, що нерегулярні менструації не вимагають негайної оцінки стану, і що ця нерегулярність не виключає можливості зачаття (Некласифікована заява з належної практики)».
У фазі одужання після рестриктивних розладів харчування та інтенсивних фізичних навантажень звичайно спостерігаються різні субоптимальні варіанти менструального циклу (табл. 3). Типовими у цей період є дезорганізований фолікулогенез та неадекватна фаза жовтого тіла. У деяких жінок помірний гіпогонадотропний статус може тривати роками, що проявляється нижчими рівнями статевих гормонів, ніж це типово для віку пацієнток. Клінічно це проявляється, наприклад, довгими менструальними циклами з короткою другою фазою, інколи з передменструальним плямленням, або ж короткими циклами з ранньою менструацією через недостатність жовтого тіла.
Значення таких довготривалих відхилень у перебігу менструального циклу для здоров’я жінки остаточно невідоме, однак припускають, що це може призводити до остеопорозу, серцево-судинних розладів і зниженої плідності.
Обстеження
«У пацієнтів з підозрою на ФГА ми рекомендуємо зібрати докладний анамнез з акцентом на дієті; розладах харчування; заняттях фізичними вправами і спортивними тренуваннями; особливостях поведінки, таких як перфекціонізм і висока потреба у соціальному схваленні; амбіціях і очікуваннях стосовно себе та інших; коливаннях ваги; звичках сну; стресорах; настрої; картині менструацій; наявності переломів і вживанні наркотиків. Клініцисти повинні також зібрати вичерпний сімейний анамнез з підвищеною увагою до харчових і репродуктивних розладів. (Некласифікована заява з належної практики)»
У пацієнтів з підозрою на ФГА необхідно виявити наявність галактореї, тяжких або частих епізодів болю голови, нудоти, блювання або змін зору, спраги або сечовипускання (об'єму і частоти), що вказує на можливість пролактиноми або іншої гіпофізарної чи внутрішньочерепної пухлини. Клініцисти повинні також отримати анамнез симптомів, що свідчать про дисфункцію щитовидної залози (гіпотиреоз або гіпертиреоз), надлишок андрогенів і СПКЯ, або симптомів, які наводять на думку про інші хронічні захворювання.
У пацієнтів з первинною аменореєю аносмія або гіпосмія може вказувати на синдром Кальмана, який пов'язаний з нездатністю нейронів ГнРГ мігрувати з нюхової плакоди до гіпоталамуса.
З аменореєю можуть бути також пов'язані тривожність, депресія і хронічні захворювання, і лікарі повинні шукати ознаки і симптоми кожного з цих станів.
Клініцисти повинні розпитати пацієнтку про недавню фізичну активність і дієтичні звички (і можливі зміни в них), в тому числі порушення харчової поведінки і застосування послаблюючих, триваючі або недавні зміни ваги і вплив стресорів.
Медикаменти, зокрема антипсихотичні, антиепілептичні, контрацептиви і опіоїди також можуть порушувати менструальний цикл.
Крім того, приймання ліків є індикатором стресу та порушеного харчування. Пацієнтка може потребувати звичайного психіатричного обстеження, оскільки стани, які асоціюються з активацією осі ГГН, можуть пригнічувати секрецію ГнРГ та потребувати медикаментозної корекції.
«У пацієнток з підозрою на ФГА слід виключити вагітність і провести комплексний медичний огляд, в тому числі гінекологічне обстеження (зовнішнє, а в окремих випадках, бімануальне), щоб оцінити можливість органічного походження аменореї. (1lÅÅÅO)»
Фізикальне обстеження, включаючи визначення ваги, зросту і проведення зовнішнього гінекологічного і бімануального обстеження, дозволяє лікарю виконати диференцальну діагностику жінкам підліткового або дорослого віку з ФГА. Вона повинна включати оцінку стану очного дна і поля зору (щоб виключити набряк диску зорового нерва або дефіцит поля зору) і перевірку наявності галактореї, тиромегалії, гірсутизму, акне або кліторомегалії. Латерелізація неврологічних ознак може вказувати на внутрішньочерепну патологію.
Додатково до втрати ваги, ФГА також проявляється такими симптомами, як брадикардія, покриті плямами і холодні кінцівки, шкірні прояви гіперкаротинемії. Іноді у молодих жінок з тяжкою формою гіперандрогенії розвивається аменорея, відображаючи атрофічний ефект постійного андрогенного навантаження на ендометрій. Зовнішній гінекологічне обстеження може виявити почервоніння, стоншення слизової оболонки піхви у молодих жінок з дефіцитом естрогенів, і випинання синюшного кольору в пацієнток з непорушеною дівочою плівою.
У деяких випадках може бути корисним виконання бімануального дослідження, наприклад, щоб виключити наявність пухлини придатків. У залежності від кваліфікації лікаря і уподобань/готовності до співпраці пацієнта, у хворих з аменореєю (і деяких дівчат-підлітків) замість бімануального дослідження можна розглянути виконання трансабдомінального або трансвагінального УЗД тазових органів на початковій стадії патологічного стану.
«Жінкам підліткового або дорослого віку з підозрою на ФГА ми рекомендуємо пройти наступні скринінгові лабораторні тести: дослідження на хоріонічний b-гонадотропін людини, загальний аналіз крові, визначення рівнів у крові електролітів, глюкози, бікарбонату, азоту сечовини, креатиніну, печінкові тести, а також (у разі необхідності) ШОЕ і/або рівні С-реактивного білка. (1lÅÅÅÅ)»
Виконання загальних лабораторних тестів, починаючи з дослідження на бета-хоріонічний гонадотропін людини, з метою виключити вагітність, ініціює початок комплексних досліджень для підлітків або молодих жінок з ФГА. Клініцисти повинні отримати результати загального аналізу крові, біохімічних досліджень, печінкових тестів, швидкості осідання еритроцитів і/або рівня С-реактивного білка у пацієнток з підозрою на хронічне захворювання, яке маніфестує як гіпогонадизм. Підвищення рівня глюкози при випадковому вимірюванні або натщесерце повинне спонукати клініцистів до вимірювання рівня гемоглобіну A1c. Висока швидкість осідання еритроцитів і/або рівень С-реактивного білка свідчить про наявність хронічного запалення. Дослідження показали, що у підлітків і молодих жінок з екстремальними обмеженнями енергетичного споживання функції печінки змінюються.
Однак, дані за підтримку економічної ефективності специфічних скринінгових оцінок відсутні.

«Для початкової оцінки ендокринного балансу пацієнтів з ФГА рекомендуємо виконати наступні лабораторні дослідження: визначити сироватковий рівень тиротропного гормону (ТТГ), вільного тироксину (Т4), пролактину, лютеїнізуючого гормон (ЛГ), фолікулостимулюючого гормону (ФСГ), естрадіолу (Е2) і антимюллерового гормону (АМГ). Клініцисти повинні визначити рівні загального тестостерону і дегідроепіандростерону-сульфату (ДГЕА-С) у хворих з клінічними ознаками гіперандрогенії та рівні 17-гідроксипрогестерону на 8 годину ранку за підозри на вроджену гіперплазію кори наднирників з пізнім початком. (1lÅÅÅÅ)»
Така панель досліджень дає змогу виявити усі найчастіші причини аменореї. Слід пам’ятати, що динаміка рівнів гормонів важливіші, ніж їх абсолютні значення. Звичайно у пацієнтів з ФГА є низькі або нормальні рівні ЛГ, нормальні ФСГ, рівень естрадіолу не перевищує 50 пг/мл. Тест зі стимуляцією ГнРГ підвищує рівні ФСГ і ЛГ у 2–3 рази. Інтерпретація рівня естрадіолу ускладнється тим, що звичайно маємо тільки один показник, а не рівень цього гормону в динаміці. Однак при рівні естрадіолу менше 20 пг/мл тест зі стимуляцією ГнРГ є єдиним способом, який дає змогу диференціювати ФГА від гіпоталамічного гіпогонадизму. При гіпоталамічному гіпогонадизмі первинна реакція ЛГ на стимуляцію ГнРГ буде низькою, але нормалізується при пульсаційному введенні ГнРГ.
Дуже низькі рівні ЛГ і ФСГ засвідчують про органічну гіпоталамічну аменорею, наприклад, через пухлину або через генетичні мутації.
При підозрі на гіперкортицизм досліджують добову екскрецію кортизолу з сечею, рівень кортизолу в слині пізно ввечері або виконують тест з 1 мг дексаметазону. При виявленні гіперкортизолемії якомось зі способів клініцист повинен виконати ще один тест для підтвердження цього стану. При стресовому походженні аменореї підвищення рівня кортизолу менш виражене, ніж при синдромі Кушинга, спостерігається у вечірні та ранкові години і повертається до норми протягом дня.
При акромегалії підвищується рівень IGF-1 та інколи пролактину.
Аменорея внаслідок зниженої пульсації ГнРГ може виникати при некомпенсованому цукровому діабеті, тоді цінним для діагностики є рівень HbA1C.
«Після виключення вагітності ми пропонуємо виконання проби з прогестином у пацієнтів з ФГА, щоб викликати кровотечу відміни (як показника хронічного впливу естрогену) і переконатися в цілісності шляхів відтоку. (1lÅÅÅÅ)»
Відсутність кровотечі відміни після курсу прогестинів може вказувати на обструкцію шляхів відтоку або низький вплив естрогенів на ендометрій. Характер відповіді на тест із прогестином може надати додаткову інформацію про естрогеновий статус пацієнта, особливо у випадках, коли ФГА і СПКЯ співіснують. Варіанти включають застосування медроксипрогестерону ацетату (від 5 до 10 мг/добу протягом від 5 до 10 днів), норетиндрона ацетату (5 мг/добу протягом від 5 до 10 днів), або мікронізованого прогестерону (від 200 до 300 мг/добу протягом 10 днів).
Деякими пацієнтами прогестини переносяться погано. Таким чином, деякі лікарі можуть призначити спочатку їх більш короткий п'ятиденний курс і повторити протягом декількох тижнів за відсутності кровотечі відміни. Наступне спостереження з виконанням УЗД органів малого тазу може бути необхідним, якщо у пацієнтки не розвивається кровотеча відміни і є корисним для визначення товщини ендометрію і цілісності мюллерового тракту. Для останнього може бути потрібним виконання МРТ.
«Ми рекомендуємо виконання магнітно-резонансної томографії (МРТ) головного мозку (зі зрізами ділянки гіпофіза і контрастуванням) дівчатам-підліткам та жінкам з передбачуваною ФГА і тяжким або тривалим болем голови; сильним блюванням, що виникає самостійно без провокацій пацієнткою, розладів зору, спрагою, сечовипусканнями, які не можна пояснити іншими причинами; латералізацією неврологічних проявів; та клінічними ознаками і/або результатами лабораторних досліджень, які свідчать про недостатність або надлишок гіпофізарних гормонів. (1lÅÅÅÅ)»
За відсутності названих клінічних проявів діагностична цінність МРТ є незначною. Однак, за відсутності чітких показань або інших пояснень причин аменореї (наприклад, анорексії або надмірних фізичних навантажень в анамнезі, втрати ваги або розладів харчової поведінки), клініцистам слід розглянути питання про виконання МРТ головного мозку. Синдром порожнього турецького сідла також може бути як діагноз первинного захворювання. Слід зазначити, що індукований голодуванням характер функціональних тестів щитоподібної залози може нагадувати ознаки центрального гіпотиреозу в пацієнтів з розладами харчової поведінки. Значні травми голови у анамнезі повинні викликати підозри на пошкодження ніжки гіпофіза і пов'язаний дефіцит гіпофізарних гормонів.
«Ми вважаємо, що лікарі повинні визначати базовий рівень мінеральної щільності кісткової тканини (МЩКТ) з використанням двоенергетичної рентгенівської абсорбціометрії (ДРА) у будь-якої жінки підліткового або дорослого віку з тривалістю аменореї 6 або більше місяців, і що фахівці визначають МЩКТ раніше в цих хворих з анамнезом або підозрою на тяжкий дефіцит харчування, при інших станах енергетичного дефіциту і/або крихкості кісток. (2l ©©©©)»
Метою денситометрії МЩКТ є виявлення осіб, схильних до ризику крихкості кісток, визначення величини скомпрометованої кісткової маси у пацієнтів зі встановленою крихкістю кісток, а також керівництво і контроль лікування.
Рестриктивні розлади харчової поведінки, такі як анорексія, являють собою крайній кінець спектру доступності енергії. У пацієнтів з порушеннями виявляють втрати кісткової маси і/або відсутність зрощення кісток. Як відомо, такі пацієнти схильні до високого ризику переломів, порівняно з пацієнтами із нормальною вагою.
Хоча ми знаємо, що вправи з обтяженнями є корисними для здорової молоді, зі сприятливим впливом на зростання кісткової маси та її пікові значення, ми спостерігаємо відсутність зростання, і навіть значну втрату кісткової маси у спортсменок з розладами харчової поведінки і низькою вагою і спортсменок з нормальною вагою і аменореєю у підлітковому віці.
Відомо, що молоді жінки з розладами харчової поведінки мають у сім разів вищий ризик переломів, також переломи втомлення є постійною проблемою жінок-спортсменок з аменореєю.
Останні рекомендації груп спортивного консенсусу, в тому числі Тріади коаліції спортсменок і Міжнародного олімпійського комітету рекомендують спортсменкам пройти скринінг на компоненти тріади і потенційну відповідність певним вимогам доступності енергії, перш ніж продовжувати тренування.
«У випадках первинної аменореї ми пропонуємо оцінити наявність аномалій мюллерових шляхів (вроджених чи набутих). Діагностичні варіанти включають фізикальне обстеження, виконання проби з прогестином, абдомінальне або трансвагінальне УЗД і/або МРТ, залежно від випадку і уподобань пацієнта. (2lÅÅÅO)»
Визначення анатомії статевих шляхів завжди являє собою перший крок у виключенні анатомічних причин аменореї, особливо важливим це є для первинних аменорей (Табл. 1).
Аномалії нижніх відділів статевих шляхів часто є причиною первинної аменореї і вимагають як фізичного обстеження (яке має вирішальне значення у визначенні неперфорованої дівочої пліви), так і отримання УЗД або МРТ зображень органів малого тазу, щоб виключити і/або визначити анатомічні аномалії.
«У пацієнток зі синдромом ФГА на фоні синдрому полікістозних яєчників (СПКЯ), ми пропонуємо:
- визначення базового рівня МЩКТ за допомогою денситометрії у хворих з тривалістю аменореї 6 або більше місяців і з анамнезом або підозрою на тяжкий дефіцит харчування, інших станах енергетичного дефіциту і/або крихкості кісток (2/ÅÅOO); і
- клінічне спостереження за гіперчутливими пацієнтами, що лікувались від неплідності із застосуванням екзогенних гонадотропінів. (1l ÅÅÅÅ)»
СПКЯ є частою причиною аменореї у жінок репродуктивного віку, яка може співіснувати з ФГА. У деяких пацієнток із ФГА суттєве обмеження харчування може призвести до маскування симптомів СПКЯ. Типовим для таких пацієнток є підвищення рівнів АМГ за відсутності гіперандрогенії та типового полікістозного вигляду яєчників при ультрасонографії. Однак при збільшенні маси тіла у таких пацієнток можуть проявлятися інші фенотипічні ознаки СПКЯ, зокрема, гіперандрогенія. Звичайно, менструальні цикли в таких жінок ніколи не стають адекватними, однак ризик остеопорозу є таким же, як і в інших жінок з ФГА. Такі пацієнтки звичайно бурхливо реагують на гонадотропіни, якщо такі препарати застосовують для лікування неплідності.


коментариев