Гемолітична хвороба новонародженого (або фетальний еритробластоз) займає друге місце серед причин мертвонародження і діагностується приблизно у 0,5% новонароджених.
Захворювання виникає внаслідок плодово-материнської кровотечі, внаслідок потрапляння крові плода в материнське кров’яне русло протягом вагітності чи під час пологів.
Резус-конфлікт – це гуморальна імунна відповідь резус-негативної матері на еритроцитарні антигени резус-позитивного плода, при якій утворюються антирезусні антитіла. Антитіла проходять через плаценту, зв’язуються з антигеном, присутнім на еритроцитах плода, і викликають їх гемоліз. Захворювання характеризується трьома типовими проявами – генералізований набряк, неонатальна жовтяниця та анемія. При важкому перебігу захворювання може призвести до внутрішньоутробної загибелі плода. При відсутності своєчасної діагностики та лікування резус-сенсибілізації у вагітних, перинатальна смертність складає близько 17,5%, мертвонародження – до 14%. Частота резус-несумісності у популяції обумовлена поширеністю Rh-антигена: 15% у європейців (до 70% серед басків, що проживають на території Франції та Іспанії), до 5,5% серед афроамериканців, в Японії, Китаї – до 0,5% (Avery’s Neonatology: Pathophysiology & Management of the Newborn. Mhairi G.MacDonald, Mary M. K. Seshia, Martha D. Mullett. Lippincott Williams & Wilkins, 2005).
Перше нагадування про набряк новонародженого зустрічається у працях Гіпократа. У літературних джерелах за період ХVII–XIX сторіччя були описані кілька подібних випадків. Schridde у 1905 році зробив припущення, що екстрамедулярний гемопоез в печінці та селезінці, а також велика кількість молодих еритроцитів в крові є реакцією на анемію та впровадив термін «еритробластоз». (Schriedde, H. Weitere Untersuchungen uber die Kornelungen der Plasmazellen/ H. Schriedde// Centralbl. Allg. Pathol. Anat. – 1905).
У 1931 році вперше був доведений зв’язок між водянкою плода, жовтяницею та гемолітичною хворобою новонародженого. Darrow (Icterus gravis (erythrobla stosis neonatorum, examination of etiologic considerations)/ R. R. Darrow// Arch. Pathol.– 1938) у 1938 році висунув теорію щодо імунного походження гемолізу еритроцитів. На його думку, еритроцити плода, проникаючи у судинне русло матері, сприяють утворенню антитіл на чужорідний гемоглобін, які трансплацентарно переходять у кров’яне русло плода та руйнують його еритроцити. Відкриття резус-антигена в 1940 році сприяло точному розумінню патофізіологічних механізмів еритробластозу плода. Трохи згодом вчені Великобританії та Америки встановили, що антирезус-імуноглобулін, введений резус-негативним жінкам у післяпологовому періоді, знижує вірогідність розвитку імунізації при наступних вагітностях (Finn, R. Clarke C. A., Donohoe W. T. A. et al. // Br. Med. J. 1961), а дослідники з Німеччини(Schneider, J. Die profyla xe der Thesis-sensibilisierung mit Immu noglobulin anti-D/ J . Schneider // Arztl. Forschung. –1967) довели, що при вже наявній сенсибілізації анти резус імуноглобулін неефективний.
При введенні антигенів системи «резус» в організм людей з резус-негативною кров’ю виробляються антирезус-антитіла. Іноді сенсибілізація відбувається при першій вагітності, але в деяких випадках – лише при 4–5-й вагітностях. Встановлено, що при наступних вагітностях захворювання має тяжчий перебіг, ніж при сенсибілізації, виявленій при першій вагітності.
На сьогодні виявлено 236 антигенів еритроцитів, які містяться у 29 генетично незалежних системах, серед них 55 різновидів антигенів системи «резус», які виявляються за допомогою специфічних антисироваток. Гемолітична хвороба плоду або новонародженого також може бути викликана іншими антигенами групи резус (Rh-система крові складається з антигенів C, c, D, E, e та G-антигену), а також так званими «нерегулярними антигенами» не резус-групи, такими як антигени Kell, Duffy, Kidd, MNSs, Lutheran, Diego, Xg, P, Ee та Cc, та іншими. Тому частіше використовується термін «еритроцитарна» або «резус»-аллоімунізація. Не завжди титр материнських антитіл та анамнез захворювання при попередніх вагітностях прогнозують початок анемії плода. Несумісність типів крові за АВО не викликає фетального еритробластозу.
Імунні антитіла відносяться до класу глобулінів M, G, A. За серологічними властивостями антитіла поділяють на «повні» (сольові аглютиніни) та «неповні». «Повні» антитіла виявляються на ранніх стадіях імунної відповіді та відносяться до фракції Ig M, вони мають велику молекулярну масу та не проникають через плацентарний бар’єр. Тому ці антитіла не відіграють особливої ролі у розвитку гемолітичної хвороби. «Неповні» антитіла відносяться до фракції Ig G, беруть участь в аглютинації, преципітації та імунному лізісі, легко проникають через плацентарний бар’єр та є основною причиною розвитку гемолітичної хвороби у плода.
Рівень Ig G у плода та тяжкість гемолітичної хвороби пов’язані з концентрацією материнських антитіл. До 24 тижнів вагітності трансплацентарний перенос Ig G повільний, тому гемолітична хвороба плода до цих термінів зустрічається рідко. У пізні терміни рівень переносу антитіл збільшується, а під час пологів рівень Ig G плода стає більшим рівня Ig G матері і гемоліз стає максимальним.
Під час нормальної вагітності еритроцити плода проникають через плацентарний бар’єр у 5% жінок в I триместрі, в 15% – протягом II триместру, та до 30% – протягом III. Сприяє резус-сенсибілізації порушення цілісності ворсин хоріона (гестози, загроза переривання вагітності, екстрагенітальна патологія, інвазивні втручання). Фето-материнська кровотеча при амніоцентезі трапляється у 20%, при штучних пологах – у 15% випадків. Частота допологової первинної імунізації протягом першої резус-несумісної вагітності складає менше 1%.
На першому пренатальному візиті всі жінки проходять діагностику типу крові та Rh-належності. Якщо жінка має резус-негативну кров, то визначається тип крові та зиготності батька (якщо батьківство є певним). Коли батько має резус-негативну кров, подальше тестування непотрібне. Якщо він є резус-позитивним, вимірюється рівень антирезусних антитіл у матері. Якщо титри є позитивними, але меншими, ніж критичне лабораторне значення (зазвичай від 1:8 до 1:32), повторні вимірювання проводяться кожні 2–4 тижні після 20-го тижня гестації. Якщо значення титрів антитіл перевищує критичне, визначається кровоплин середньої мозкової артерії плоду (CМA) з інтервалом від 1 до 2-х тижнів (залежно від вихідних даних та історії пацієнта) з метою прогнозування тяжкості анемії плода. Найбільш розповсюджений спосіб виявлення антирезусних антитіл – пряма та непряма проба Кумбса із застосуванням антиглобулінової сироватки. Пряма проба застосовується для визначення антитіл, вже фіксованих антигенами на поверхні еритроцитів. Непряма проба Кумбса широко застосовується для виявлення антитіл у сироватці крові: у вагітних, при проведенні проб на сумісність крові, при посттрансфузійних ускладненнях.
Тест Kleinchauer-Betke розроблений у 1957 р. для визначення фетального гемоглобіну в кров’яному руслі матері, він підтверджував факт плодово-материнської кровотечі, яка і призводить до початку захворювання. Тест базується на розбіжностях у розчинності фетального гемоглобіну та зрілого гемоглобіну в кислому середовищі. Більш точним, швидким і сучасним є метод проточної цитометрії (QuikQuant), для якого використовують моноклональні антитіла до фетального гемоглобіну та реагент (пропія йодид).
Протягом останніх 10 років впроваджується неінвазивне визначення резус-фактору плода (на сьогодні доступне генотипування D, C, с, E, е та K антигенів) з виділеної вільної фетальної фракції ДНК з плазми крові вагітних жінок. Визначення гену RHD в материнській крові проводиться у Північній Америці, неінвазивне тестування інших генів (наприклад, RHCE, KEL) доступне в Європі. Це дозволяє на ранніх стадіях вагітності визначити плоди групи ризику та уникнути непотрібної імунізації.
Дослідження показали, що приблизно 99% жінок мають плодово-материнську кровотечу до 4 мл при пологах.
Антенатальна плодово-материнська кровотеча є патологічним станом з широким спектром клінічних змін. Призводячи вторинно до виникнення анемії, плодово-материнська кровотеча може мати руйнівні наслідки для плода.
Найбільш вірогідний час отримання первинного стимула – післяпологовий період. У пологах найбільш часто відбувається трансплацентарна трансфузія, особливо при оперативних втручаннях.
Клінічні обставини, що частіше пов’язані з великою плодово-материнською кровотечею:
- травматичні пологи, включаючи кесарів розтин;
- ручне виділення плаценти;
- мертвонародження;
- травма живота протягом ІІІ триместру;
- багатоплодова вагітність;
- невияснений набряк плода.
Посилений гемоліз еритроцитів призводить до підвищення рівня непрямого білірубіну в крові та жовтяниці. Непрямий білірубін токсичний та не виводиться нирками, порушує тканевий метаболізм, включаючи тканеві ферменти та процеси фосфорилювання. В результаті, у печінці порушується синтез білків, що призводить до гіпопротеїнемії та підвищення проникливості судин, зниження онкотичного тиску в плазмі крові. Виникає серцева недостатність, застій у великому колі кровообігу, що призводять до випоту рідини в тканини та порожнини – розвивається анасарка (підшкірний набряк, гідроторакс, гідроперикард, асцит).
При гіпербілірубінемії вражаються підкоркові та стовбурові ядра головного мозку, в результаті чого розвивається ядерна жовтяниця – білірубінова енцефалопатія. Ризик такого ускладнення у доношених дітей з гемолітичною хворобою виникає при концентрації непрямого білірубіну близько 340 мкмоль/л. Факторами ризику розвитку білірубінової енцефалопатії є недоношеність та низька маса тіла при народженні, гіпоксія, ацидоз, інфекція, гіпотермія, гіпоглікемія, тяжка анемія, внутрішньочерепні крововиливи. У недоношених дітей таким небезпечним рівнем є 256–270 мкмоль/л.
При руйнуванні еритроцитів, поряд з гемоглобіном, який є джерелом білірубіну, вивільнюється велика кількість біологічно активних речовин, в тому числі ферментів тромбогенезу та фібринолізу. Під впливом тромбопластичних елементів розвивається ДВЗ-синдром, з’являються крововиливи, порушується трофіка тканин плаценти, печінки, мозку плода.
Найбільші труднощі викликає антенатальна діагностика гемолітичної хвороби плода. Вона передбачає як встановлення факту сенсибілізації еритроцитарними антигенами, так і ступінь ураження плода антитілами матері. За даними літератури, між ступенем ізоімунізації матері та тяжкістю захворювання плода у багатьох випадках встановлюється пряма залежність: при меншому титрі (від 1:2 до 1:16) частіше діти народжуються неушкодженими чи з легкою формою захворювання.
Показання до дострокового розродження при Rh-конфлікті (згідно чинного наказу МОЗ України №676 від 31.12.2004):
- Титр антитіл дорівнює чи перевищує 1:64 (критичний рівень);
- Наростання титру при повторному аналізі у 4 рази;
- Оптична щільність навколоплідних вод 0,35–70 і вище; концентрація білірубіну в амніотичній рідині 4,7–9,5 мг/л;
- УЗ-ознаки гемолітичної хвороби у плода;
- Мертвонародження та народження дітей із гемолітичною хворобою в анамнезі.
Тактика ведення вагітності та пологів при резус-ізоімунізації (алгоритм з наказу МОЗ України №676) (див. рис. 1).
Вибір тактики ведення вагітних з ізоімунізацією по Rh-фактору представлений у алгоритмі (наказ МОЗ України №676) (див. рис. 2).
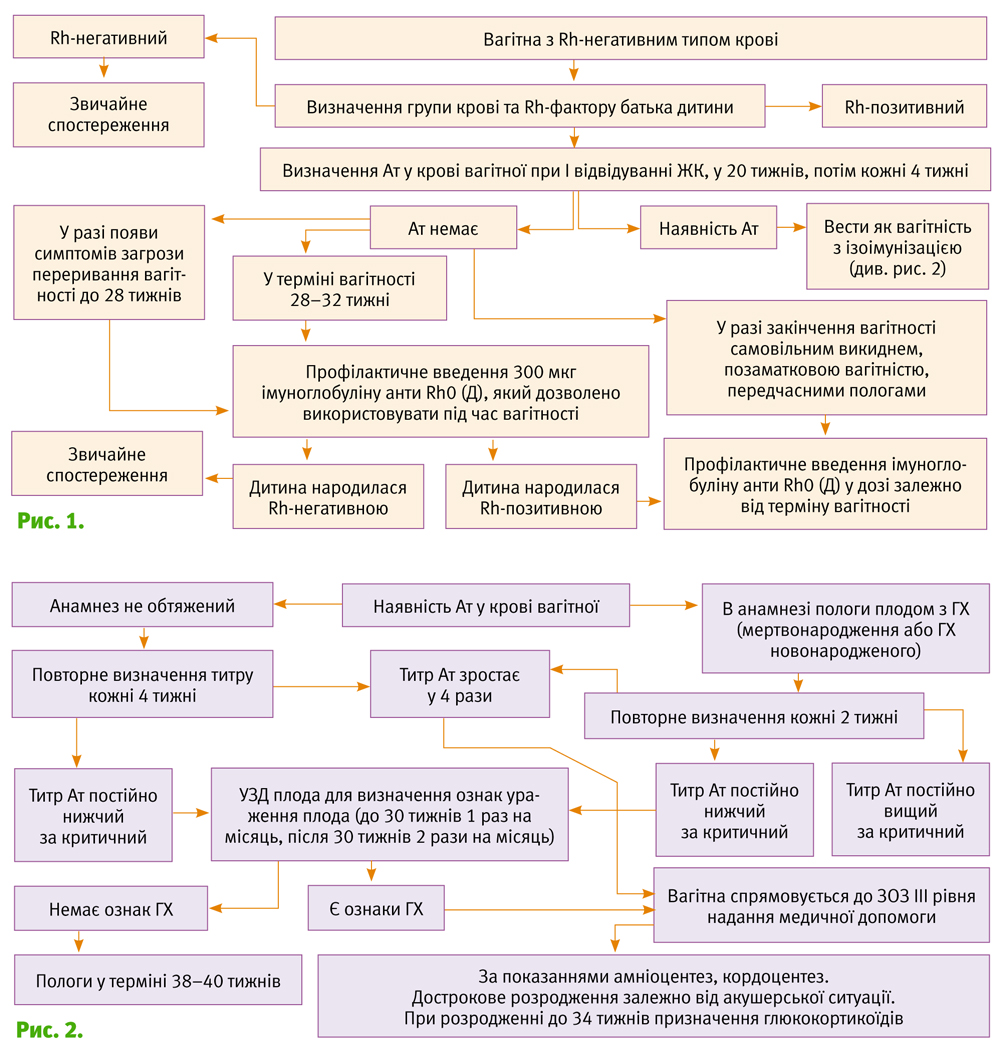
Метою управління материнською резус-аллоімунізацією є виявлення анемічних плодів внутрішньоутробно та лікування їх шляхом внутрішньоматкового замінного переливання або припинення вагітності (шляхом природніх пологів або кесаревого розтину).
Розвиток ультразвуку в 70-ті роки дозволив детально досліджувати плід, а також виконувати інвазивні внутрішньоматкові втручання. Ще у 1961 році Liley розробив прогностичну шкалу для оцінки ступеню тяжкості гемолітичної хвороби плода та ризику внутрішньоутробної анемії, засновану на показниках оптичної щільності білірубіну в навколоплідних водах (вище 450 нм). (Liley A. W. Liquor amnii analysis in the management of the pregnancy complicated by Rhesus sensitization. American J.Obstet. Gynecol. 1961; Liley A.W. The use of amniocentesis and fetal transfusion in erytroblastosis fetalis. Pediatrics. 1965.)
Амніоцентез дозволяє визначити ступінь тяжкості анемії за рівнем білірубіну, присутнього в амніотичній рідині внаслідок гемолізу еритроцитів плода. Але цей метод не надає жодних відомостей про кровотворну реакцію плода, і для контролю за перебігом вагітності зазвичай потрібні послідовні процедури. Недоліками є недостатня точність до 27 тижнів вагітності та складнощі прогнозування тяжкості анемії.
Кордоцентез є єдиним надійним методом прямого визначення концентрації гемоглобіну. Дослідження крові плода, отриманої шляхом кордоцентезу, дозволяє встановити діагноз гемолітичної хвороби та оцінити ступінь тяжкості захворювання та показання щодо проведення внутрішньоутробної гемотрансфузії. Проте це інвазивне втручання пов’язане з такими ускладненнями, як інфекція, кровотеча з пунктованої ділянки пуповини, транзиторна брадикардія, фето-материнська кровотеча, яка може погіршити аллоіммунізацію плода та призвести до його загибелі.
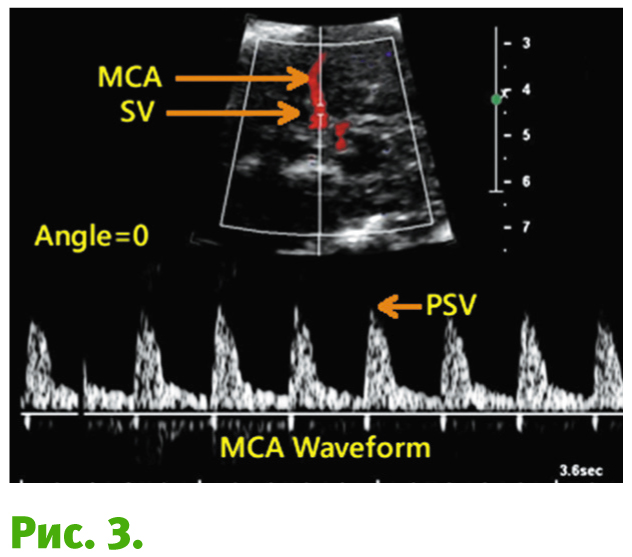 Впровадження неінвазивного тесту на фетальну анемію було метою багатьох дослідників останніх років. Плід адаптується до гемодинамічних змін, і ці компенсаторні зміни можна оцінити за допомогою допплерівського ультразвуку. G. Mari та його команда з Baptist Memorial Hospital-Memphis, США, у 2000 році дослідили, що шляхом вимірювання пікової систолічної швидкості середньої мозкової артерії плоду (MCA PSV) можливо неінвазивним шляхом прогнозувати розвиток фетальної анемії у плодів групи ризику за резус-конфліктом (Mari G. Noninvasive diagnosis by Doppler ultrasonography of fetal anemia due to maternal red-cell alloimmunization. N. Engl. J. Med. 2000) (рис. 3).
Впровадження неінвазивного тесту на фетальну анемію було метою багатьох дослідників останніх років. Плід адаптується до гемодинамічних змін, і ці компенсаторні зміни можна оцінити за допомогою допплерівського ультразвуку. G. Mari та його команда з Baptist Memorial Hospital-Memphis, США, у 2000 році дослідили, що шляхом вимірювання пікової систолічної швидкості середньої мозкової артерії плоду (MCA PSV) можливо неінвазивним шляхом прогнозувати розвиток фетальної анемії у плодів групи ризику за резус-конфліктом (Mari G. Noninvasive diagnosis by Doppler ultrasonography of fetal anemia due to maternal red-cell alloimmunization. N. Engl. J. Med. 2000) (рис. 3).
MCA PSV плода добре корелює з концентрацією гемоглобіну та гематокритом. Цей метод грунтується на тому, що анемічні плоди мають підвищену швидкість кровотоку (гіпердинамічний кровообіг). Переваги вивчення середньо-мозкової артерії, а не інших судин, полягають у тому, що він дозволяє вимірювати швидкість без корекції кута, оскільки в осьової площині кут інсонації MCA близький до 0°, що покращує відтворюваність.
Метод вимірювання пікової систолічної швидкості в середньо-мозковій артерії (PSV MCA) при діагностиці анемії плода різного ступеня тяжкості має практично 100% чутливість та специфічність.
Розрахувати ступінь тяжкості анемії за показниками PSV MCA, а також об’єм гемотрансфузії (в мл), згідно терміну гестації та показників гематокриту плода з гемолітичною хворобою та донора, можна за допомогою online-калькулятора за посиланням https://medicinafetalbarcelona.org/calc/.
З 1982 року стандартом корекції анемії плода є внутрішньоутробна внутрішньосудинна (у вену пуповини) гемотрансфузія під ультразвуковим контролем. На сьогодні і в Україні є медичні центри, що успішно проводять дану маніпуляцію. Інтрасудинна трансфузія – це ефективний метод лікування анемії плода. Її мета – підтримати плід до гестаційного віку, коли розродження може бути безпечним. Під час виконання кордоцентезу в вену пуповини водять еритроцитарну масу, збіднену лейкоцитами і тромбоцитами Rh-негативної 0 (І) групи крові. Набрякова форма супроводжується вираженою гіпоальбумінемією, яка коригується веденням розчину альбуміна разом з еритроконцентратом. В результаті успішної терапії відновлюється онкотичний тиск і вільна рідина з серозних порожнин переходить у кровоносне русло. Об’єм еритроконцентрату та кратність виконання трансфузій залежить від терміну гестації, тяжкості захворювання, рівня гематокрита плода і донора, передбачуваної маси і об’єму циркулюючої крові.
В цілому менеджмент інтраваскулярних трансфузій дає хороші результати. Рівні плодових втрат вищі при тяжкому перебігу захворювання, особливо при гемолітичній хворобі, що виникає рано (до 20 тижнів), у зв’язку з технічними складнощами доступу до пуповини дрібного розміру. У 2007 році госпіталь принцеси Анни, Саусамптон, Великобританія, опублікував свій перший досвід інтраперитонеальної трансфузії. Пацієнти, що були відібрані для даного дослідження, мали попередній обтяжений анамнез та підвищений рівень анти резус-антитіл на час взяття у групу. Рішення щодо трансфузії приймалось на основі даних PSV MCA, як індикатора анемії плода. Найменший термін гестації – 15 тижнів, у плодів зі складностями доступу до судин пуповини процедура проводилась регулярно до тих пір, поки з ростом плода не поліпшились умови доступу до пуповини. Час розродження пролікованих плодів групи — 32–37 тижнів, кількість проведених втручань: від 2 до 4. Попередні дослідження вказують на частоту перинатальних втрат біля 24% після інтраваскулярних втручань в терміні менше 20 тижнів. Інтраперитоніальні трансфузії є безпечними та досить ефективними у випадку розвитку анемії в малому терміні гестації (N. Crawford, R. Parasuraman, S. Boxall, D. T. Howe. Outcomes of severe Rhesus isoimmunisation requiring treatment at £20 weeks gestation managed with early intraperitoneal transfusions. ISUOG, Rome 2016).
Методом профілактики розвитку гемолітичної хвороби є введення антирезусного імуноглобуліну під час вагітності або після пологів.
Анти-D-імунноглобулін – це продукт крові, що містить високий титр антитіл до резус-антигенів еритроцитів. Він отриманий з плазми людини та ефективний у профілактиці активної резус-аллоіммунізації. Можливий шлях введення препарату – внутрішньовенний або внутрішньом’язовий, тривалість дії обох шляхів однакова.
Після внутрішньовенного введення початкові рівні анти-D-антитіл у сироватці крові вище протягом першого тижня, але потім мають аналогічний внутрішньом’язовому введенню рівень (до 3 місяців).
Високий рівень циркулюючих анти-D антитіл може бути корисним, коли відомий термін плодово-материнської кровотечі (наприклад, післяпологовий період, кровотеча в III триместрі – тоді доцільне введення препарату внутрішньовенно), але для антенатальної профілактики достатньо внутрішньом’язової ін’єкції.
Після введення анти-D-імуноглобуліну у жінок стає позитивним скринінг на антирезусні антитіла. Ця реакція зазвичай буде у низькому титрі чи слабореактивна. Зазвичай, проведення тестування після імунізації не рекомендоване. Aнти-D імуноглобулін проникає через плаценту і зв’язується з еритроцитами плоду, не викликаючи гемолізу, анемії або жовтяниці. У дослідженні 20% Rh-позитивних дітей, народжених матерями, які отримали передпологову дозу анти-D імуноглобуліну, демонстрували позитивний «прямий» антиглобуліновий тест, проте їх рівень гемоглобіну та білірубіну не відрізнявся від резус-негативних дітей. Препарати анти-D-імуноглобулінів ніколи не були пов’язані з трансмісивними інфекціями, такими як ВІЛ або гепатити В та С. Всі донори суворо перевіряються.
Післяпологова іммунопрофілактика з використанням анти-D-імуноглобуліну діє у Великобританії з 1969 року. Програма відзначилась вражаючим успіхом: за даними RCOG, смертність, пов’язана з Rh-аллоіммунізацією, знизилася з 46/100 000 народжень в 1969 році до 1,6/100 000 у 1990 році.
Керівні принципи щодо імунопрофілактики RhD впроваджені Британським королівським коледжем акушерів та гінекологів (RCOG) з 1976 року і були переглянуті кілька разів. Останні чинні гайдлайни розроблені спільною робочою групою Британського товариства з гемотрансфузії (BCSH guideline for the use of anti-D immunoglobulin for the prevention of haemolytic disease of the fetus and newborn. Transfusion medicine, 2013) та RCOG (The Use of Anti-D Immunoglobulin for Rhesus D Prophylaxis.RCOG, Green-top Guideline No. 22, March 2011; The Management of Women with Red-Сell Antibodies During Pregnancy. RCOG, Green-top Guideline No. 65, May 2014).
Рекомендації SOGC (Канадського товариства акушерів-гінекологів) перегукуються з настановами британських колег (Prevention of Rh alloimmunisation. SOGC Clinical Practice Guidelines No. 133, September 2003).
- Анти-D Ig у дозі 300 мкг слід вводити внутрішньомязово чи внутрішньовенно протягом 72 годин після пологів несенсибілізованій резус-негативній жінці при пологах резус-позитивним плодом. Додаткова доза анти-D Ig може бути призначена при плодово-материнській кровотечі більше 15 мл плодових еритроцитів (приблизно 30 мл цільної крові).
- Якщо анти-D Ig не вводили протягом 72 годин після пологів або іншої потенційно сенсибілізуючої події, його слід призначити одразу після встановлення такої потреби, протягом 28 днів після пологів чи події.
- Проведення рутинного тесту післяпологових плодово-материнських кровотеч (тест Kleinchauer-Betke) всім резус-негативним матерям не є виправданим.
- Всі резус-негативні вагітні, при невизначеному типі крові плода чи визначеній резус-позитивній його належності мають отримати профілактику 300 мг анти-D Ig в 28 тижнів вагітності (альтернативно, дві дози по 100–120 мг можуть вводитись двічі: в 28 та 34 тижні гестації).
- Всім вагітним жінки (D-негативним або D-позитивним) необхідно провести тест на непрямий антиглобулін («непряма» проба Кумбса) під час першого пренатального візиту, та повторно в 28 тижнів.
Можна запропонувати всім резус-негативним вагітним жінкам Rh-тестування батька дитини для ліквідації непотрібного введення препарату крові (у випадку, якщо факт батьківства точно відомий).
- Вагітним жінкам, що мають слабку експресію D-антигену (так званий «Du-позитивний» або «слабкий D» тип крові) не проводять профілактичне введення анти D-імуноглобуліну.
- Не потрібно повторно вводити передпологову дозу Rh-іммуноглобуліну в 40 тижнів вагітності, за умови, що попередня імунізація проведена не раніше 28 тижня вагітності.
Після введення однієї дози анти-Д-імуноглобіліну, антитіла циркулюють у крові матері протягом 3-х місяців.
- Після викидня, загрози переривання вагітності або індукованого аборту протягом перших 12 тижнів вагітності десенсибілізованим резус-негативним жінкам слід вводити мінімальну дозу анти-D імуноглобуліну (120 мкг).
Після 12 тижнів вагітності їм слід ввести стандартні 300 мкг.
- При перериванні вагітності (аборті) необхідно визначити тип крові та наявність антирезус-антитіл у жінки, але якщо ці результати встигли отримати протягом вагітності, скринінг на антитіла не потрібно повторювати.
- Анти-D імуноглобулін слід також призначити несенсибілізованим резус-негативним жінкам при позаматковій вагітності. Мінімум 120 мкг має бути призначено до 12 тижнів вагітності та 300 мкг – після 12 тижнів.
- При пухирцевому занеску також необхідно призначати анти-D Ig несенсибілізованим резус-негативним жінкам через можливість часткового міхурцевого занеску. Якщо напевно встановлений факт повного міхурцевого занеску – можна утриматись від призначення анти-D імунопрофілактики.
- Проведення інвазивних втручань не протипоказане резус-негативним жінкам, але після втручань є обов’язковою профілактика резус-конфлікту.
При амніоцентезі анти-D імуноглобулін слід вводити в дозі 300 мкг (несенсибілізованим D-негативним жінкам). При біопсії хоріону, проведеній до 12 тиж., анти-D імуноглобулін слід призначити в дозі 120 мкг та в дозі 300 мкг – при проведенні біопсії плаценти після 12 тижнів вагітності. Після кордоцентезу слід вводити 300 мкг анти-D Ig.
- Кількісний тест плодово-материнської кровотечі (тест Kleinchauer-Betke) проводиться при подіях, потенційно пов’язаних з травмуванням та порушенням плодово-маткового бар’єру (наприклад, відшарування плаценти, тупа травма живота, кордоцентез, плацента previa з кровотечею). Існує великий ризик розвитку плодово-материнської кровотечі більше 30 мл у зв’язку з такими подіями, особливо при травмі живота.
- Анти-D 120 мкг або 300 мкг рекомендовано ввести паралельно під час проведення тесту, ще до отримання його результату. Якщо визначений об’єм кровотечі перевищує той, що покривається вже введеною дозою імунглобуліну (відповідно, 6 чи 15 мл еритроцитів плода), додатково слід ввести по 10 мкг анти-D Ig на кожні 0,5 мл еритроцитів. Ризик масивної плодово-материнської кровотечі найвищий при травмі живота.
- Перед веденням препарату має бути отримана інформована згода вагітної.
Згідно рекомендацій Національного інституту здоров’я та клінічного удосконалення Великобританії (NICE 2002, 2008) після АВО та Rh-типування зразка пуповиної крові дитини після пологів, підтвердженого як позитивний, всім попередньо несенсибілізованим резус-негативним жінкам вводиться 500 МО (300 мкг) антиD-імуноглобуліну протягом 72 год. після пологів. Материнські зразки крові направляються на тестування об’єму плодово-материнської кровотечі і додаткова доза імуноглобуліну призначається в залежності від результатів тестування.
Коли при масивній кровотечі під час кесарського розтину має місце аутогемотрансфузія фільтрованих елементів крові (intara-operative cell salvage), резус-негативним, первинно несенсибілізованим жінкам (якщо в пуповинній крові новонародженого визначений резус-позитивний тип крові) водиться щонайменше 1500 МО (900 мкг) антиD імуноглобуліну. Зразок материнської крові направляється на тестування, і в разі підтвердження об’єму більше ніж 30–45 мл плодово-материнської кровотечі при реінфузії, коригується доза імуноглобуліну.
При внутрішньоутробній загибелі плода, коли немає можливості встановити резус-фактор плода, профілактична доза імуноглобуліну вводиться несенсибілізованим резус-негативним жінкам протягом 72 годин від часу загибелі, не очікуючи пологів.
Ключові моменти
Найбільша кількість еритроцитів плода переміщається в кров’яне русло матері (що призводить до найбільшого ризику материнської сенсибілізації) під час пологів (особливо, травматичних) або після переривання вагітності.
Необхідно проводити скринінг усім вагітним жінкам для визначення групи крові, типу Rh-належності, анти-Rh0 (D) та інших антитіл, які можуть спричинити гемолітичну хворобу.
Якщо жінка знаходяться під загрозою ризику виникнення фетального еритробластозу, необхідно моніторити рівні антитіл і періодично проводити вимірювання швидкості кровоплину середньо-мозкової артерії плода.
Лікування гемолітичної хвороби плода – внутрішньоутробна гемотрансфузія, а при важкій анемії – передчасне розродження у терміні від 32 до 35 тижнів гестації, залежно від клінічної ситуації.
Усі жінки, що мають ризик сенсибілізації, потребують введення Анти (D) імуноглобуліну у 28 тижнів гестації та протягом 72 годин після пологів. Додаткове введення антирезусного імуноглобуліну показане при виникненні ускладень перебігу вагітності та проведенні інвазивних втручань.


коментариев