Вагітність є станом, для якого притаманна гіперкоагуляція, і підвищений ризик тромботичних ускладнень існує протягом вагітності і особливо у післяпологовий період. А у жінок з набутою та вродженою тромбофілією додатково підвищується ризик розвитку різноманітних проявів плацентарної дисфункції, в тому числі прееклампсії, синдрому затримки роста плода, передчасного відшарування плаценти
Попередні дані, що отримані за результатами багатьох різноспрямованих рандомізованих досліджень, свідчать про оптимізацію результатів вагітностей у жінок із спадковою або набутою тромбофілією при профілактичному застосуванні антитромботичних препаратів. І, хоча дослідження з цього приводу досі не закінчені, вже з’явилися перші керівництва щодо обстеження і медикаментозної профілактики венозних тромбозів різної локалізації у жінок під час вагітності, пологів та післяпологового періоду. З деякими з них ми і маємо на меті ознайомити наших читачів. Сподіваємось, що наданий матеріал дозволить покращити ведення вагітних та породіль та запобігти несприятливим тромботичним наслідкам.
Тромбофілія є патологічним станом, коли у судинах, переважно у венах, формуються тромби [6, 12]. Часто такий патологічний стан у жінок репродуктивного віку вперше виникає під час вагітності, коли виникає та функціонує третє (плацентарне) коло кровообігу. Нормальний плин вагітності пов’язаний зі змінами механізмів гемостазу, які мають тенденцію до створення протромботичного середовища [4, 8]. Тому ускладнення вагітності та післяпологового періоду у вигляді тромбоемболічної хвороби є основною причиною материнської захворюваності та смертності в усьому світі [4].
Тромбофільні фактори ризику є поширеними у жінок білої раси і виявляються у 15–25% [4]. Оскільки вагітність є набутим гіперкоагулянтним станом, тромбофілія вперше може виявляти клінічні симптоми судинних ускладнень саме під час вагітності [8, 9]. Крім венозних тромбозів та тромбоемболії, під час вагітності для хворих на тромбофілію характерні ускладнення, що пов’язані з плацентарними судинними ускладненнями, такими як втрата плода, прееклампсія, затримка росту плода (ЗРП) і передчасне відшарування нормально розташованої плаценти [2]. Загалом, усі тромбофілічні порушення, що можуть мати місце під час вагітності та післяпологового періоду, можна визначити за окремими типами (табл. 1).
Тяжкі випадки тромбофілії, як правило, спричинені сукупністю декількох факторів. Наприклад, порушення плину крові поєднується із вродженим підвищеним тромбоутворюванням.
Для практичної діяльності лікаря акушера-гінеколога дуже важливим є правильно визначитися із станом жінки, що існує, розрахувати ризик тромбоемболічних ускладнень і своєчасно провести профілактичні заходи. Для досягнення цієї мети пропонуємо ознайомитись із керівництвом South Australian Perinatal Practice Guidelines «Thrombophilia in pregnancy» [2] та Practice Bulletins from the American College of Obstetricians and Gynecologists No. 197: Inherited Thrombophilias in Pregnancy [1], що є у вільному доступі в мережі та мають найсучасніші рекомендації з діагностики та менеджменту набутих та спадкових тромбофілій під час вагітності, пологів та у післяпологовому періоді.
За даними South Australian Perinatal Practice Guidelines «Thrombophilia in pregnancy» [2], тромбофілії є спадковими або набутими станами, які пов’язані з венозною тромбоемболією (ВТЕ), такі як тромбоз глибоких вен і легенева емболія.

Клінічну значущість в акушерській практиці мають такі успадковані тромбофілії:
- Аномалії прокоагулянтних факторів
- Фактор V-Лейденська мутація, що викликає стійкість до активованого білка С (APCR).
- Мутація гена протромбіну (протромбін G20210A).
- Інгібітор активатора плазміногену-1 (PAI-1) генна мутація.
- Недоліки ендогенних білків в каскаді коагуляції
- Протеїн С.
- Протеїн S.
- Антитромбін.
До набутої тромбофілії відноситься антифосфоліпідний синдром (АФС), що виявляється наявністю антифосфоліпідних антитіл до вовчакового антикоагулянта та/або антикардіоліпінових антитіл.
До тромбофілії змішаного генезу (успадкованого та набутого) відноситься гіпергомоцистеїнемія (коли виявляється підвищений рівень гомоцистеїну в плазмі).
Всі узяті разом, успадковані тромбофілії є поширеними, зустрічаються у близько 15% [6]. Вони ускладнюють перебіг близько 1 з 1000 вагітностей. Успадковані та набуті тромбофілії викликають більше половини всіх материнських ВТЕ [6, 14]. Тромбофілії, крім материнських тромбозів, мають внесок у розвиток таких тяжких акушерських ускладнь як:
- Рання внутрішньоутробна затримка обмеження росту, що вимагає розродження у терміні <34 тижнів.
- Мертвонародження.
- Тяжка рання прееклампсія, що вимагає розродження у терміні <34 тижнів вагітності.
- Відшарування плаценти [15].
Низькомолекулярний гепарин (НМГ, LMWH) при вагітності може зменшити ризик зазначених вище акушерських ускладнень. Малі дози аспірину з або без НМГ є основою лікування набутих тромбофілій (наприклад, антифосфоліпідного синдрому) під час вагітності [10].
Діагностичні заходи для визначення набутих та спадкових тромбофілій.
Мають бути застосовані для наступних категорій жінок:
- Вагітних жінок із сімейним анамнезом венозної тромбоемболічної хвороби у родичів 1-го та 2-го ступеня – обстежують тільки на спадкові форми тромбофілії.
- Жінок, що мали періодичні викидні (три або більше у першому триместрі), втрати плода у 12–20 тижнів, анамнез венозного тромбозу до або під час вагітності, мертвонародження, ранню прееклампсію (<34 тижнів вагітності), ранній СЗРП є сенс обстежувати на спадкову та набуту тромбофілію.
Дослідження мають включати наступні тести:
- Вовчаковий антикоагулянт.
- Протеїн С і S.
- Резистентність до активованого протеїну С (APCR).
- Фактор V Leiden.
- Ген протромбіну.
- MTHFR.
- Гомоцистеїн.
- Антикардіоліпінові антитіла.
Таким чином, успадковану схильність можна виявити у 60–70% жінок, які мали тромбоз глибоких вен [12].
Усі жінки, що мають визначену тромбофілію, мають спостерігатися у високодосвідчених акушерів-гінекологів і допомога їм має здійснюватись у закладах ІІ–ІІІ рівня спеціалізованої допомоги.
Найбільше цікавим у South Australian Perinatal Practice Guidelines «Thrombophilia in pregnancy» [2] є те, що критерії спостереження та лікування надані за нозологічними формами.
Менеджмент вагітних, що мають фактор V Leiden
Фактор V Leiden (FVL) визначається у результаті однієї точкової мутації в гені фактору V на точці розщеплення (положення 506), де діє протеїн С. Лейденівська мутація є найпоширенішою причиною активності протеїну C (APCR) [14]. Найбільш економічним та ефективним способом скринінгу на Фактор V Leiden – це перевірка на аномальний фенотип (резистентність до aPC). Гетерозиготний стан цієї мутації виявляється у 20–40% невагітних осіб з анамнезом венозної тромбоемболії [8]. Гомозиготний стан лейденської мутації несе 80-кратний ризик ВТЕ [12].
Ця мутація притаманна 5–15% етнічної європейської популяції і є рідкісною в азіатській або африканській популяції. Вона має наступні пов’язані ризики:
- Враховуючи низьку поширеність ВТЕ під час вагітності, ризик розвитку ВТЕ при безсимптомній лейденській мутації лише 0,2% [7].
- Втрати плода у другому і третьому триместрах.
- Ранні форми СЗРП.
- Спонтанні аборти.
- Ранній початок та тяжкий перебіг прееклампсії.
- Передчасні пологи.
- У порівнянні з не-носіями, FVL-носії мають збільшену кількість патологічних допплерівських показників, включаючи двосторонні ранні дікротичні виїмки у спектрах маткових артерій.
Менеджмент вагітних, що мають мутацію гена протромбіна
Ця мутація нуклеотиду 20210 в гені, що кодує протромбін, призводить до появи високого рівню протромбіну в циркулюючій крові, який є попередником тромбіну [13]. Поширеність цього гену в загальній популяції становить від 2 до 5% [12]. Більш поширеним він виявляється у жінок білої раси. Ця мутація має наступні пов’язані ризики:
- Втричі підвищений ризик тромбозу вен.
- Суперечливим і не доведеним є зв’язок мутації гену протромбіну із раннім дебютом прееклампсії.
- Підвищений ризик СЗРП.
- Підвищений ризик відшарування плаценти.
Оцінку мутації генів протромбіну найкраще проводити за допомогою прямого генетичного аналізу для ідентифікації переходу G20210A [12].
Менеджмент вагітних, що мають мутацію протеїну C і протеїну S із дефіцитом антитромбіну
Протеїн C (ПС) має аутосомно-домінантний тип успадкування. Поширеність дефіциту ПС становить 0,3%. Може бути результатом мутацій протеїну, що визначають два первинних фенотипи:
- Тип I: як імунореактивні рівні білка, так і активність білка C знижені.
- Тип II: імунореактивні рівні є нормальними, але активність протеїну знижується [8].
Доведена відсутність значних фізіологічних змін рівнів протеїну С під час нормальної вагітності. На його рівень сильно впливає наявність системного тромбозу або хірургічного втручання. Рівень ПС знижуються у жінок із ДВЗ- синдромом, захворюваннями печінки та якщо застосовують антагоністи вітаміну К.
Поширеність дефіциту протеїну S (ПS) становить 0,1% і він має три підтипи:
- Тип I: характеризується зниженим рівнем загального і вільного імунореактивного білка і його активності.
- Тип II: характеризується нормальним загальним і вільним рівнем ПS, але його активність знижена.
- Тип III: нормальні загальні імунореактивні рівні ПS, але знижені вільні імунореактивні рівні і його активность внаслідок підвищеного зв’язування з C4b-BP-білком-носієм [14].
Тести на активність ПS є недосконалими, рекомендується проводити їх поза вагітністю та проводити 2 окремі вимірювання поза вагітністю (принаймні 8 тижнів після пологів). Вільний ПS демонструє помітне фізіологічне зниження протягом вагітності. Це зменшення є одним з основних приводів фізіологічного зниження активності ПC. ПС не слід вимірювати під час вагітності.
Пов’язані ризики дефіциту ПС і ПS включають:
- Венозну тромбоемболію (<5% випадків).
- Підвищений ризик мертвонародження.
- Втрату плода (рекурентна для ПS).
- Збільшення випадків прееклампсії, відшарування плаценти і СЗРП.
Дефіцит антитромбіну може виникнути через безліч мутацій. Він є найрідкістнішим і найбільше тромбогенним із усіх спадкових тромбофілій. Його поширеність низька (від 1:1000 до 1:5000) і він має два основні типи:
- Тип I характеризується зниженням рівня і активності циркулюючого імунореактивного білка.
- Тип II характеризується нормальним рівнем імунореактивного білка, але зниженням активності [8].
При неускладненому перебігу вагітності антитромбіновий (АТ) рівень активності не виявляє змін або мaє граничне зниження. Доведено зниження рівню активності антитромбіну у жінок з прееклампсією і синдромом ДВЗ.
Дефіцит антитромбіну має наступні пов’язані ризики:
- Ранні втрати плода.
- Рідко мертвонародження, важку прееклампсію, СЗРП або відшарування плаценти, але
- Жінки з дефіцитом антитромбіну мають особливо високий ризик тромбоемболії.
Дефіцит антитромбіну – це єдина тромбофілія, що завжди потребує тромбопрофілактики під час вагітності та у післяпологовому періоді.
Менеджмент вагітних, що мають антифосфоліпідніий синдром
Антифосфоліпідний синдром (АФС, APS) – це аутоімунне порушення, яке визначається асоціацією судинного тромбозу на тлі вагітності із підвищеними рівнями антифосфоліпідних антитіл (АФЛА), або вовчакового антикоагулянта (ВАК) та/або наявністю антитіл до антикардіоліпіну (AКA) [8]. АФС є найбільш поширеною набутою тромбофілією під час вагітності і переважно вражає молодих жінок [10]. Не всі хворі на АФС матимуть як ВАК, так і AКA; тому тестування рекомендовано на обидва антифосфоліпідні антитіла.
Рекомендовано проводити скринінг жінок для визначення антифосфоліпідних антитіл у разі наступного анамнезу:
- Ранній початок (менше 32 тижнів) прееклампсії та/або СЗРП (особливо якщо є дані про плацентарний інфаркт або більше двох рецидивуючих ранніх втрат плода).
- Антенатальна загибель плода.
- Відшарування плаценти.
Наявність антифосфоліпідних антитіл, особливо у поєднанні із випадком тромбоемболії (артеріальної або венозної), має підвищений ризик плацентарного тромбозу і інфаркту, СЗРП і загибелі плода.
Вовчаковий антикоагулянт присутній у багатьох осіб без захворювання на системний червоний вовчак і пов’язаний з тромбозом, а не гіпокоагуляцією. Діагностика АФС – це виявлення в крові антифосфоліпідних антитіл два або більше разів, принаймні за шість тижнів один від одного.
AФС діагностується також за наявності антикардіоліпінових IgG або IgM антитіл, присутніх у помірному або високому рівні у крові у двох або більше динамічних випадках, принаймні, через шість тижнів. Клінічне значення ізольованого визначення антитіл до антикардіоліпіну невизначене.
Поширеність АФС (наявність ВАК і AКA) у вагітних жінок – приблизно 2% і має наступні пов’язані ризики:
- Звичне невиношування (втрати у терміні менше 10 тижнів вагітності).
- Прееклампсія.
- Тромбоз.
- Спонтанні аборти.
- СЗРП.
- Передчасні пологи.
Для жінок із діагностованим АФС передбачена преконцепційна профілактика. Жінки з АФС повинні бути проінформовані про потенційні ризики і акушерські ускладнення. На етапі підготовки до наступної вагітності варто:
- Підтвердити значні рівні AКA/ВАК.
- Оцінити наявність ознак анемії, тромбоцитопенії, основного захворювання нирок або системного червоного вовчака.
- Призначити жінці малі дози аспірину (100 мг на добу).
- Перевірити антитіла до краснухи та призначити преконцепційну дозу фолієвої кислоти.
- Проконсультувати жінок з АФС, які мали анамнез тромбозу і які знаходяться на тривалому застосуванні варфарину, що їм потрібно буде змінити його на терапевтичну дозу низькомолекулярного гепарину переважно до зачаття і щонайменше протягом двох тижнів після пологів. Варфарин має тератогенний ефект між 6 та 12 тижнем вагітності [10].
Вагітним жінкам з позитивною АКА та/або ВАК слід запропонувати лікування з малими дозами аспірину (100 мг добу) від 12 тижнів вагітності у випадках попереднього анамнезу антенатальної загибелі плода або СЗРП, або на етапі преконцепційної профілактики та раннього терміну вагітності у випадках рецидиву ранніх втрат вагітності.
Моніторинг під час вагітності
- Раннє УЗД в першому триместрі.
- Регулярно перевіряти артеріальний тиск і рівень протеїнурії, щоб виявити ранній початок прееклампсії.
- Провести доплерографічне дослідження кровоплину у маткових артеріях на 20 і 24 тижнях.
- Проводити сканування плода кожні 2–3 тижні у вагітних з ознаками ранньої діастолічної виїмки у маткових артеріях (високий ризик ПЕ та СЗРП).
- Ультразвукове дослідження плода кожні 4 тижні для оцінки росту та обсягу навколоплодових вод (якщо немає порушень кровоплинів у маткових артеріях).
- Розробити (в обговоренні з жінкою) план ведення вагітності, заходи допологового моніторингу стану вагітної і плода та післяпологової допомоги, занести його у відповідні документи.
Медикаментозне лікування АФС
- Аспірин – 100 мг на добу.
- Додати НМГ доцільно, якщо:
- виявляються ВАК, або високопозитивні титри АКА;
- в анамнезі мали місце загибель плода або ознаки інфаркту плаценти і СЗРП. Таких вагітних є сенс консультувати у гематолога.
- Використання кортикостероїдів у жінок з АФС обмежується наявністю тромбоцитопенії або системного червоного вовчака. Необхідно забезпечити регулярний моніторинг глюкози крові для жінок, що довгостроково використовують стероїди.
Менеджмент у пологах
Аспірин можна продовжувати до народження. Низькі дози аспірину не впливають на використання регіональної анестезії під час пологів.
Слід відправити плаценту для гістопатологічного дослідження, якщо є прееклампсія, СЗРП, мало місце попереднє мертвонародження або викидні.
Післяпологовий період
Жінки з анамнезом попереднього тромбозу повинні отримувати низькомолекулярний гепарин (НМГ, LMWH) або варфарин протягом 6 тижнів після пологів. Жінки без попереднього анамнезу тромбозу, які мають інші фактори ризику венозного тромбозу, повинні отримувати післяпологовий LMWH протягом 5 днів. Припинити вживання LMWH, коли міжнародне нормоване співвідношення (МНС, INR) становить >2,0.
Слід заохочувати грудне вигодовування. Навіть варфарин виявляється у грудному молоці мінімально. Слід проконсультувати жінок щодо можливих ризиків розвитку неакушерських розладів, пов’язаних з AФС, та щодо наслідків для майбутніх вагітностей.
Менеджент гіпергомоцистеїнемії
При нормальному плині вагітності рівень гомоцистеїну падає. Гомоцистеїн утворюється із метаболізму амінокислоти метіоніну і у здорових жінок протягом репродуктивного періоду зазвичай циркулює у плазмі крові концентрації 4–7 мкмоль/л [14]. Дієтичні добавки, що містять вітамін B12 і фолієву кислоту та вітамін B6, захворювання шлунково-кишкового тракту, що призводять до порушення всмоктування, метаболічні порушення (ниркова недостатність і хвороби щитоподібної залози), вживання кави та алкоголю впливають на концентрації гомоцистеїну у венозній крові [11]. Існують генетичні поліморфізми інших ферментів, що беруть участь у метаболізмі гомоцистеїну, наприклад метилентетрагідрофолатредуктази (MTHFR) – ферменту, що необхідний для синтезу 5-метил тетрагідрофолата – донора метилу, який потрібний для перетворення гомоцистеїну в метіонін [11].
Гіпергомоцистеїнемія (підвищений рівень гомоцистеїну в плазмі) може бути успадкованою або набутою [15]. Дефекти транссульфурації, або ремітілізації призводять до підвищення концентрації гомоцистеїну в крові, відомого як гіпергомоцистеїнемія. Термолабільний варіант C677T гена MTHFR пов’язаний із схильністю від легкої до помірної гіпергомоцистеїнемії, особливо у присутності дефіциту фолієвої кислоти [11]. Фенотип гіпергомоцистеїнемії більше пов’язаний з високою частотою ранньої прееклампсії, ніж будь-який асоційований генотип, наприклад MTHFR. Тяжка форма гіпергомоцистеїнемії виникає внаслідок надзвичайно рідкісних гомозиготних недоліків ферментів цистатіонін-синтази (CBS) або метилентетрагідрофолатредуктази (MTHFR).
За показниками рівня гомоцистеїну у периферичній венозній крові визначають тяжкість захворювання:
- Тяжка гіпергомоцистеїнемія – >100 мкмоль/л.
- Помірна гіпергомоцистеїнемія – 25–100 мкмоль/л.
- Легка гіпергомоцистеїнемія – 16–24 мкмоль/л.
Гомозиготність 667C-T MTHFR присутня до 11% у популяції етнічних європейців і є провідною причиною легкої і помірної гіпергомоцистеїнемії.
З гіпергомоцистеїнемією пов’язані наступні ризики:
- Рання прееклампсія, відшарування плаценти [11, 15].
- Фетальні дефекти нервової трубки (легка та помірна гіпергомоцистеїнемія).
- Мертвонародження.
- СЗРП.
- Судинні захворювання, наприклад ішемічна хвороба серця.
- Рекурентні ВТЕ (тяжка гіпергомоцистеїнемія).
Не існує послідовного зв’язку між гіпергомоцистеїнемією та рецидивами спонтанних абортів у цілому, але є чіткий зв’язок між гіпергомоцистеїнемією і антенатальною втратою плода.
На етапі преконцепційної підготовки жінки з гіпергомоцистеїнемією повинні бути проінформовані про потенціал для матері та акушерські ускладнення.
Слід порадити жінці зменшити або уникнути умов, що як відомо, збільшують рівні гомоцистеїну, наприклад паління, споживання кави та алкоголю. Слід оцінити наявність ознак порушення функції нирок або гіпотиреозу. Заохотити дотримуватися збалансованої дієти, бо гіпергомоцистеїнемія посилюється недоліками у вітамінах В6, В12 і фолієвої кислоти.
Абсолютно показане преконцепційне вживання фолієвої кислоти. Співвідношення ризик-користь між високим (5 мг) порівняно із низьким (0,5 мг) дозами фолатів на цей час не визначено. Те ж саме справедливо і для додаткового призначення вітамінів В12 і В6.
Антенатальний догляд
- Раннє сканування в першому триместрі, плюс ранній (11–13 тижнів) трансвагінальний скринінг на дефекти нервової трубки у плода.
- Спостереження з регулярними перевірками артеріального тиску і аналізом сечі, щоб виявити ранній дебют прееклампсії.
- Регулярне ультразвукове і доплерографічне дослідження для оцінки росту, фето-плацентарного кровообігу та обсягу навколоплодових вод.
За відсутності доказів, лікування в першу чергу базується на індивідуальному профілі акушерського ризику жінки і часто є емпіричним.
Після пологів доцільно провести гістопатологічне дослідження плаценти.
На відміну від вказаного документа, у резюме керівництва ACOG [1] щодо тромбофілій у вагітних за липень 2018 року наданий дещо інший підхід. За рекомендаціями ACOG [1], тактику лікування і профілактики застосовують після визначення ступеня ризику тромбофілії. На думку автора, доцільно ознайомитись з цими рекомендаціями і обрати для впровадження в практичну діяльність найбільше вдалий варіант.
Рекомендації ACOG стосуються як різних тромбофілій, так і асоціацій із можливими несприятливими результатами вагітності.
- Скринінг на спадкові тромбофілії доцільний у наступних випадках:
- Особиста історія ВТЕ (венозної тромбоемболії) з або без фактору ризику, що повторюється.
Приклади факторів ризику, що повторюються: вагітність або використання оральних контрацептивів.
Приклади факторів ризику, що не повторюються: хірургічне втручання або тривала імобілізація.
- Сімейна історія – є родич першого ступеня зі спадковою тромбофілією високого ступеня.
- Скринінг на спадкову тромбофілію не рекомендується у наступних випадках:
- Антенатальна загибель плода.
- Відшарування нормально розташованої плаценти.
- Прееклампсія.
- Синдром затримки роста плода.
Але у разі рецидиву зазначених ускладнень вагітності або мертвонародження, жінку доцільно протестувати на наявність набутого антифосфоліпідного синдрому (АФС).
- Що доцільно включати в панель скринінгу:
- Фактор V Лейдена, патогенний варіант.
- Протромбін G20210A, патогенний варіант.
- Дефіцит антитромбіну (активність <60%).
- Дефіцит ПS (функціональний аналіз <55%).
- Дефіцит ПС (активність <65%).
- Антифосфоліпідні антитіла (набута тромбофілія).
- Скринінг має бути проведений за умови:
- >6 тижнів від випадку венозної тромбоемболії.
- Жінка повинна бути не вагітною.
- Жінка не повинна отримувати антикоагулянтну або гормональну терапію.
- До тромбофілії високого ризику відносяться:
- Дефіцит антитромбіну;
- Антифосфоліпідний синдром (АФС, АРS).
- Фактор V Лейдена або протромбін G20210A, патогенні варіанти у стані гомозиготності або складної гетерозиготності.
- До тромбофілії низького ризику відносяться:
- Фактор V Лейдена або протромбін G20210A, патогенні варіанти у гетерозиготному стані.
- Дефіцит протеіну С або S.
Методом профілактики венозної тромбоемболії є антикоагулянтна терапія (А).
- Антикоагулянтна терапія у разі тромбофілії низького ризику без особистої історії венозної тромбоемболії до пологів не проводиться, а після пологів показана у профілактичній дозі за наявності додаткових факторів ризику (наприклад, ожиріння, імобілізація, кесарів розтин).
- У разі тромбофілії низького ризику у поєднанні з наявністю випадків венозної тромбоемболії у родича першого ступеня (батьки, брати\сестри, діти) до пологів антикоагулянтна терапія не проводиться або застосовуються профілактичні дози. Після пологів застосовується профілактична антикоагулянтна терапія або проміжна доза НМГ/НФГ.
- У разі тромбофілії низького ризику із єдиним випадком венозної тромбоемболії (без тривалого застосування антикоагулянтів) до пологів показане застосування профілактичної або проміжної дози НМГ/НФГ. Після пологів – післяпологова профілактична антикоагулянтна терапія або проміжна доза НМГ/НФГ.
У разі тромбофілії високого ризику без передуючого випадку венозного тромбозу:
- До пологів – профілактична або проміжна доза НМГ/НФГ.
- Після пологів – післяпологова профілактична антикоагулянтна терапія або проміжна доза НМГ/НФГ.
У разі тромбофілії високого ризику з одним передуючим випадком тромбозу або ураженими родичами першого ступеня, що не отримували тривалу антикоагулянтну терапію:
- До пологів – профілактична або проміжна доза або скоригована доза НМГ/НФГ.
- Після пологів – післяпологова профілактична антикоагулянтна терапія або проміжна доза НМГ/НФГ або скоригована доза НМГ/НФГ протягом 6 тижнів. Терапія має відповідати обраному лікуванню до пологів.
У разі тромбофілії із ≥2 передуючими випадками тромбозу (без довготривалої антикоагулянтної терапії):
- До пологів – проміжна доза або скоригована доза НМГ/НФГ.
- Після пологів – проміжна доза НМГ/НФГ або скоригована доза НМГ/НФГ протягом 6 тижнів, відповідно до обраного лікування до пологів.
У разі тромбофілії із ³2 передуючими випадками тромбозу (з тривалою антикоагулянтною терапією):
- До пологів – скоригована доза НМГ/НФГ.
- Після пологів – відновити довготривалу терапію антикоагулянтами. Оральні препарати можуть бути застосовані в залежності від тривалості терапії, грудного вигодовування та переваг пацієнтки.
Нарешті, хочу зазначити, що для усіх акушерських пацієнтів є підвищений ризик материнської венозної тромбоемболії, особливо у післяпологовий період у разі проведення оперативного втручання у пологах.
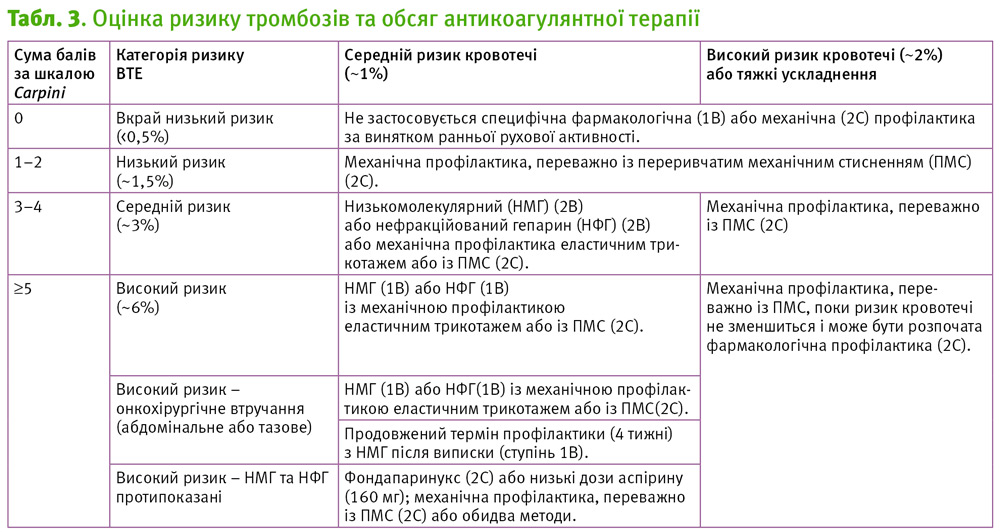
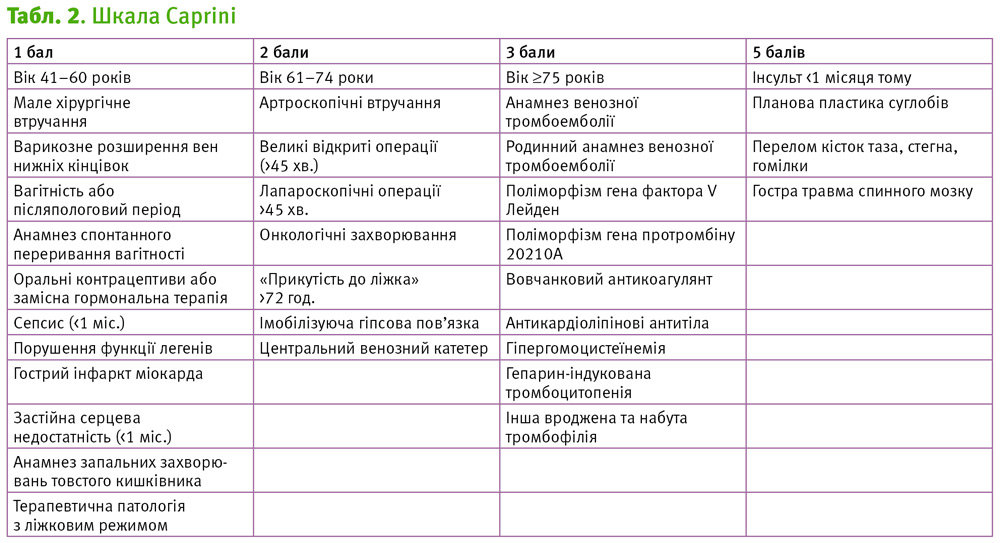
Для розрахунку ризику венозних тромбозів існують різні шкали, найбільше цікавою із них є шкала Caprini [3], що враховує стан вагітності, набуті та спадкові тромбофілії, вживання оральних контрацептивів, що є дуже важливо саме для використання в акушерсько-гінекологічній практиці. Загалом, за цією шкалою оцінюється ризик венозних тромбозів для пацієнтів перед хірургічним втручанням у загальній хірургії, а також в урологічній, гінекологічній, судинній, пластичній та реконструктивній хірургії.
Дані, що отримано, складаються за визначними балами. Оцінка ризику тромбозів та обсяг антикоагулянтної терапії визначається у відповідності до категорії ризику венозної тромбоемболії із урахуванням ризику кровотечі.
На високий ризик тромбозів вказують наступні зміни у гемостазіограмі:
- Рівень фібриногену вищий за 6 г/л;
- Активований частковий термопластичний час (АЧТЧ, АЧТВ) менший за 15–17 секунд. Змінюються також показники тромбінового часу.
- Підвищена концентрація протромбіну. За тромбофілії цей показний вищий за норму (норма 78–142%).
- Концентрація тромбоцитів вище за 180–320х109/л, еритроцитів більше ніж 3.5–55,0х1012/л.
- Підвищена концентрація Д-димера відносно норми по триместрах вагітності. Норма Д-димера у 1 триместрі – 750 нг/мл; у 2 триместрі – 1000 нг/мл, у третьому – 1500 нг/мл.
Ускладнення, що виникає у разі застосування низькомолекулярного гепарину, особливо у терапевтичній дозі – гепариніндукована тромбоцитопенія (ГІТ, НІТ). ГIT може вражати до 3% пацієнтів, які піддаються гепарину. ГIT є дуже рідкісним ускладненням у пацієнтів з низькомолекулярним гепарином (НМГ, LMWH). Більше половини пацієнтів з безсимптомним ГІТ можуть мати утворення аномальних тромбів у наступні 30 днів після початку терапії. Існує два типи ГIT:
- Тип I проявляється протягом декількох днів від початку застосування гепарину. Має доброякісний перебіг і не потребує специфічного лікування або антидоту.
- Тип II проявляється від 5 дня до 3 від початку лікування і являє собою аутоімунний імуноглобулін-опосередкований синдром, пов’язаний з венозним і артеріальним тромбозом. Пацієнтам з діагнозом ХІТ рекомендується проконсультуватися з гематологом і отримати лікування фондапаринуксом [16].
Хоча діагноз ГІТ визначається насамперед за клінічними ознаками, для йог підтвердження використовуються такі лабораторні тести, як ІФА гепарин/ПФ 4, індукована гепарином агрегація тромбоцитів (HIPA) і аналіз вивільнення серотоніну (SRA).
The Pregnancy and Thrombosis Working Group [16] рекомендує припинити вживання препаратів гепарину, якщо кількість тромбоцитів знижується нижче 150 000 або 50% від вихідного рівня під час терапії гепарином або НМГ.
Загалом, при призначенні НМГ рекомендоване визначення рівня тромбоцитів на початку лікування, на 4-у добу терапії, потім кожні 2–3 дні протягом перших двох тижнів лікування і через 3 тижні, для своєчасного визначення ГІТ [ 17, 18].
Також з метою моніторингу ефективності застосування LMWH під час вагітності, за даними декількох окремих досліджень [19, 20], ефективним виявилось визначення активності anti-Factor Xa. Але ці дослідження були ретроспективними та обсерваційними, тому конкретні клінічні рекомендації щодо застосування кратності та критерії визначення активності anti-Factor Xa на теперешній час не визначені.
Враховуючи усі зазначені діагностичні та лікувальні заходи, на думку автора, на сьогодні розроблено досить вдалий арсенал заходів щодо попередження тромботичних ускладнень в акушерській практиці, справа за малим – вдале їх впровадження у практичну діяльність.


коментариев