Незважаючи на поширеність практичного застосування прогестерону у жінок з проблемною вагітністю, доцільність такого лікування з метою запобігання ранньому викидню залишається суперечливою.
У недавньому дослідженні PROMISE автори не виявили позитивного ефекту профілактичного застосування вагінального прогестерону у жінок зі звичними викиднями. У дослідженні брали участь 1568 жінок з трьома і більше викиднями через невідому причину. Прогестерон застосовували не раніше, як з моменту позитивного тесту на вагітність.
Натомість відомо, що результат вагітності суттєво залежить від якості жовтого тіла та готовності ендометрію до імплантації, а отже корекція недостатності жовтого тіла в цей період може мати вирішальне значення, однак даних про ефект від застосування прогестерону, починаючи від фази жовтого тіла, поки що мало.
В нещодавній публікації Mary Stephenson та колег (2017) автори вивчали, як впливає ранній – від початку другої фази – початок терапії мікронізованим прогестероном на вислід вагітності у жінок зі звичними викиднями.
Як виявилося, успішні вагітності у жінок зі звичними викиднями, які приймали прогестерон від постовуляторного періоду, траплялися у 10 разів частіше, ніж у контрольній групі.
Звичні викидні, тобто два і більше викиднів у терміні до 10 тижнів вагітності, є складною проблемою в сучасному акушерстві, яка, на жаль, не має поки що достатньо обґрунтованих терапевтичних опцій. Згідно даних Американської асоціації репродуктивної медицини (ASRM), ця проблема стосується 15–25% усіх вагітностей.
Зі звичним викиднем асоціюється багато чинників, зокрема, генетичних, ендокринних, анатомічних, імунологічних тощо, однак насправді у 50% випадків проблема залишається невизначеною. Тактика ведення жінок зі звичними викиднями характеризується всебічним обстеженням та ретельним спостереженням та підтримкою при наступних вагітностях.
Роль у проблемі звичного викидня чинників, які стосуються ендометрію, завойовує все більший інтерес. Дослідження Burton et al. (2007) засвідчило, що залози ендометрію відіграють вагому роль у розвитку ранньої вагітності. Ці залози функціонують принаймні до 10 тижнів вагітності. Як відомо, глікопротеїд MUC-1 і глікопротеїд А, які утворюються залозами ендометрію, поглинаються фагоцитами плаценти та виконують важливу роль в ранньому розвитку ембріона. Крім того, численні дослідження засвідчили про низькі концентрації MUC-1 в ендометрії жінок зі звичними викиднями, що вказує на низьку активність залоз ендометрію (Hey 1995, Xu 2012).
Прогестерон сприяє секреторній трансформації ендометрію, що дуже важливо для підтримки ранньої вагітності. Часто прогестерон застосовують у жінок зі звичними викиднями емпірично у терміні до 10 тижнів. У кількох дослідженнях вивчали клінічну ефективність вагінального, внутрішньом’язового та перорального застосування прогестерону в поліпшенні перспектив вагітності у жінок з кров’янистими виділеннями в І триместрі та звичними викиднями в анамнезі (Haas 2013, Hussain 2012, Coomarasamy 2011). У відомому кохрейнівському огляді Haas 2013 автори прийшли до висновку, що застосування прогестерону збільшує частку успішних вагітностей у жінок з трьома і більше викиднями в анамнезі. Однак такі дослідження базувалися на гетерогенних когортах, у них застосовували різні способи введення прогестерону, і крім того, застосовували лікування лише з того моменту, коли у жінки вже почалася кровотеча.
У 2015 році Coomarasamy et al. виконали рандомізоване дослідження із застосування вагінального прогестерону у жінок зі звичними викиднями (3 і більше викиднів у І триместрі). Жінки отримували 400 мг мікронізованого прогестерону двічі на день або плацебо. Лікування починали від позитивного тесту на вагітність, але не пізніше 6 тижнів вагітності. Частка успішних пологів у групі лікування становила при цьому 66% порівняно з 63% у групі плацебо. Автори закономірно прийшли до висновку, що застосування прогестерону в І триместрі не поліпшує вислід вагітності у жінок зі звичними викиднями. Однак хоча це дослідження було рандомізованим, його недоліками був пізній початок лікування та високі дози препарату.
Відомо, що підвищення рівня лютеїнізуючого гормону (ЛГ) у період, близький до овуляції, сприяє лютеїнізації зернистих клітин та збільшення утворення прогестерону. Розвиток і дозрівання залоз ендометрію оптимально оцінювати шляхом дослідження молекулярних маркерів. Оскільки маркер розвитку ендометрію n-циклін Е (nCyclin E) у жінок зі звичними викиднями до 10 тижнів звичайно патологічно підвищений, автори зробити припущення, що застосування мікронізованого прогестерону вагінально, починаючи на 3 дні пізніше піку ЛГ, може бути ефективним у поліпшенні висліду вагітності у таких пацієнток.
Матеріали і методи
Пацієнтки
У дослідження увійшли пацієнтки, які брали участь у Чикагській програмі зі звичного викидня. Дані для дослідження отримали з бази даних зі звичного викидня Чикагського університету, яку вів один з авторів. У цю базу даних увійшли усі жінки, які звернулися від липня 2002 до квітня 2012 року з анамнезом звичного викидня, чи інакше двох або більше викиднів через невідому причину (виключали випадки з хромосомними аномаліями) у терміні до 10 тижнів, та яким виконали біопсію ендометрію через 9–11 днів після піку ЛГ і які мали принаймні одну наступну вагітність, яка настала без застосування ліків для поліпшення плідності.

Жінок, у яких виявляли гістологічні відхилення в біоптаті ендометрію (затримку дозрівання, десинхронізацію розвитку залоз, лейкоцитарну інфільтрацію), виключили з дослідження. Лабораторне дослідження пацієнток включало визначення рівнів ТТГ, пролактину, цитогенетичний аналіз обох батьків та дослідження на наявність антифосфоліпідних антитіл (вовчакового антикоагулянту, антикардіоліпінових і IgG, IgM до бета-2-глікопротеїду). Виконували також гістероскопію для оцінки стану порожнини матки.
Критерії відхилень експресії n-цикліну Е
Біопсію ендометрію виконували на 9–11 день після піку ЛГ, який визначала жінка за допомогою домашніх тестів. Ендометрій досліджували гістологічно після фарбування гематоксиліном і еозином, а також виконували гістохімічне дослідження для визначення експресії n-цикліну Е. Таке дослідження виконали у 100 пацієнток.
Результат вважали патологічним, якщо експресія n-цикліну Е перевищувала 20%, при цьому пороговому значенні було максимальне відношення шансів настання вагітності між групами з рівнями експресії вище та нижче порогового. Для визначення оптимального порогового значення використали дані про 118 жінок, які проходили дослідження з приводу неплідності у Єльському університеті.
При цьому частота настання вагітності становила 42% у жінок з рівнем n-цикліну Е £20% та 8% у жінок з рівнем n-цикліну Е >20% (відношення шансів 0,12; 95% ДІ 0,02–0,99, p=0,027).
Стратегія лікування
Пацієнткам призначали наявний на ринку США мікронізований прогестерон (Ендометрин або Прометріум) у дозі 100–200 мг через кожні 12 годин, починаючи від 3 днів після піку ЛГ (початок фази жовтого тіла) і протягом 10 тижнів вагітності. Таке лікування отримували жінки з підвищеною експресією n-цикліну Е (>20%). Деякі жінки з нормальною експресією n-цикліну Е наполягали на призначенні їм вагінального мікронізованого прогестерону, який приймали в таких же дозах.
Жінки з нормальною експресією n-цикліну Е, які не приймали вагінального прогестерону, становили контрольну групу.
Жінкам із підвищеною експресією n-цикліну Е пропонували повторну біопсію ендометрію в першому циклі лікування прогестероном (максимум 200 мг через кожні 12 годин). Морфолог, який оцінював біоптати, не знав, приймає пацієнтка прогестерон чи ні. Водночас враховували й інші чинники, які могли вплинути на оцінку результату.
Наступну вагітність діагностували на основі підвищення рівня b-ХГЛ ³5 мМО/мл у крові, взятій через 1–2 дні після затримки менструації, далі цей аналіз повторювали через тиждень. У 6 тижнів вагітності виконували вагінальну ультрасонографію. Усім жінкам пропонували ретельне спостереження протягом І триместру вагітності, зокрема, трансвагінальну ультрасонографію і візит до лікаря через кожні 1–2 тижні із можливістю невідкладної допомоги протягом 24 годин на добу. Наприкінці І триместру пацієнток скеровували під нагляд місцевих закладів – до акушера-гінеколога або фахівця із материнсько-плодової медицини. Про результат вагітності довідувалися із записів в цих закладах або пологових будинках.
Визначення
Втрата вагітності до 10 тижнів включала викидень (з ідентифікацією ембріона та вимірюванням його куприко-тім’яного розміру), закінчену самовільно вагітність невідомої локалізації та втрату біохімічної вагітності. Згідно рекомендацій Європейського товариства репродукції людини та Групи ембріології ранньої вагітності, біохімічну вагітність визначали як зниження рівня ХГЛ сечі без ультрасонографічного підтвердження вагітності (Kolte, 2015). Гестаційний вік визначали за датою останньої менструації за винятком тих випадків, коли він відрізнявся від гестаційного віку згідно куприко-тім’яного розміру, визначеному в першому триместрі, більш ніж на 3 дні (ACOG Committee Opinion 611б 2014).
Кінцеві точки
Успішною вважали вагітність, яка закінчилася вчасними або передчасними пологами чи тривала в терміні понад 10 тижнів. Вторинним вислідом, який визначали, була поширеність патологічної експресії n-цикліну Е у жінок зі звичними викиднями.
Аналіз даних
Дані дослідження збирали проспективно. Порівнювали демографічні характеристики жінок з нормальною та зміненою експресією n-цикліну Е в залозах ендометрію. Неперервні змінні порівнювали за допомогою t-критерію (стьюдента). Категорійні змінні аналізували за допомогою критерію c2 або точного критерію Фішера. Статистично значущими вважали різницю при двобічному P<0,05.
За допомогою багатофакторної моделі методом оцiночних рiвнянь (Generalized Estimating Equations, GEE) вивчали вплив різноманітних чинників на висліди вагітності.
Зворотний відбір результатів виконали за віком, індексом маси тіла, расою та іншими чинниками, зокрема, навністю транслокацій у батьків, гіпотиреозу, внутрішньоматкових аномалій (зростів, перегородок), антифосфоліпідного синдрому. Жоден із цих чинників не мав статистично значущого значення.
Результати
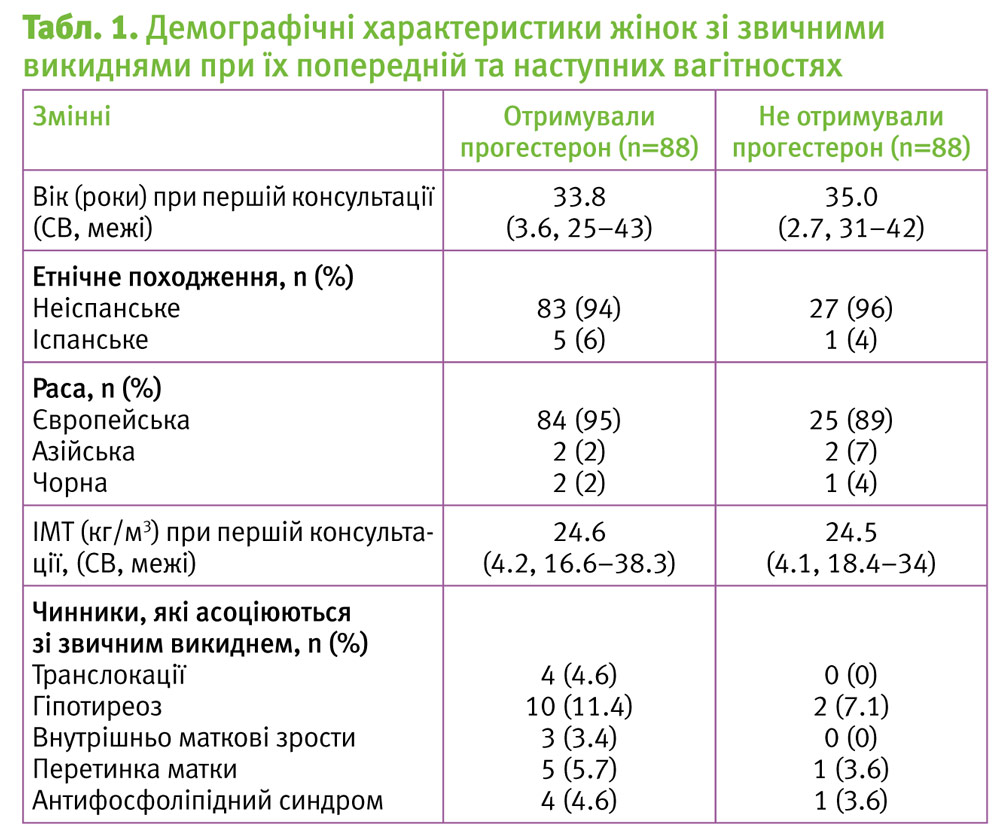
Критеріям включення в дослідження відповідали 116 жінок. В усій когорті було загалом 499 попередніх вагітностей, із яких 425 (85%) закінчилися викиднями в терміні до 10 тижнів. Між групою жінок, які отримували прогестерон, і контрольною групою не було значущих відмінностей у віці, етнічному походженні, індексі маси тіла та інших чинниках (табл. 1).
У 51% жінок (59/116) була патологічно підвищена експресія n-цикліну Е в біоптаті ендометрію, натомість у 49% (57/116) вона була нормальна. Значущих відмінностей у віці, етнічному походженні, індексі маси тіла та інших чинниках між групами жінок з нормальною та підвищеною експресією n-цикліну Е не було.
Усім жінками з підвищеною експресією n-цикліну Е призначили вагінальний мікронізований прогестерон у дозі 100–200 мг через кожні 12 годин, починаючи від 3-го дня після піку ЛГ. У 25 жінок з підвищеним при першій біопсії рівнем n-цикліну Е на фоні такого лікування виконали повторну біопсію, при цьому у 84% (21) випадків рівень n-цикліну Е знизився, а у 16% [4] залишався на попередньому рівні. Трьом із цих чотирьох жінок призначили більшу дозу вагітнального прогестерону (200 мг через кожні 12 годин), ще дві жінки скоригували собі дозу до цього рівня.
Результати вагітностей
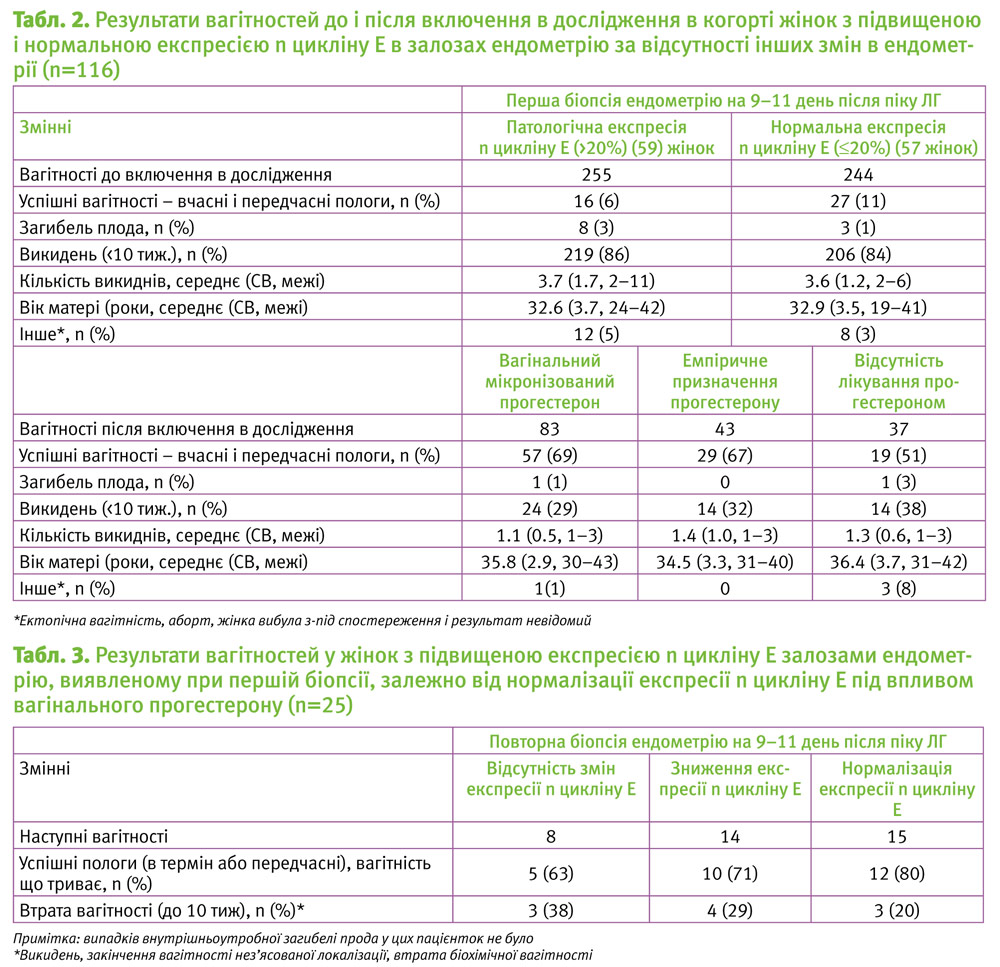
У 59 жінок з підвищеними рівнями n-цикліну Е при початковій біопсії було 255 вагітностей в минулому і далі 83 вагітності при лікуванні мікронізованим вагінальним прогестероном по 100 мг через кожні 12 годин (n=56) або 200 мг через кожні 12 годин (n=27) (табл. 2). Частка успішних вагітностей при цьому значуще збільшилася від 6% (16/255) до 69% (57/83) при лікуванні вагінальним прогестероном та перебуванні у програмі спостереженя. У 25 жінок, які мали повторну біопсію на фоні лікування прогестероном, вислід вагітності поліпшувався поступово водночас зі зниженням експресії n-цикліну Е (табл. 3).
Частка успішних вагітностей у жінок зі звичними викиднями без лікування прогестероном, становила 6%, натомість при застосуванні прогестерону та перебуванні у програмі спостереженя вона збільшилася до 69%, чи більш ніж у 10 разів.
У 57 жінок з нормальною експресією n-цикліну Е при першій біопсії в минулому були 244 вагітності і далі 80 вагітностей (табл. 3). Частка успішних вагітностей на фоні лікування значуще збільшилася від 11% (27/244) до 60% (48/80) (P<.001).
Частина жінок з нормальною експресією n-цикліну Е при першій біопсії (n=28) попросила емпіричного призначення вагінального прогестерону. При цьому було 43 вагітності на фоні лікування 100 мг препарату через кожні 12 годин (n=39) або 200 мг через кожні 12 годин (n=4). Між цими підгрупами не було статистично значущої різниці, зумовленої лікуванням, а частка успішних вагітностей становила відповідно 67% (29/43) та 51% (19/37, Р=0,14).
Загалом протягом дослідження було 163 вагітності у 116 жінок: 126 – на фоні лікування мікронізованим прогестероном (при емпіричному призначенні або через підвищену експресію n-цикліну Е) та 37 вагітностей – без застосування прогестерону. Був один випадок викидня в терміні 15 тижнів у жінки, яка отримувала прогестерон, та один випадок викидня в терміні 12 тижнів у жінки, яка не отримувала прогестерон. Також були 38 випадків викидня у терміні до 10 тижнів у жінок, які отримували прогестерон: 14 – на рівні біохімічної вагітності, 2 – анембріонії, 4 – після візуалізації жовткового мішка і 18 – після візуалізації ембріона. У жінок, які не отримували прогестерон, було 14 викиднів у терміні до 10 тижнів: 5 – на рівні біохімічної вагітності, 1 – анембріонія, 1 – при візуалізації жовткового мішка і 7 – при візуалізації ембріона.
Середній гестаційний вік на момент викидня у жінок, які отримували прогестерон, становив 5,3 тижня порівняно з 5,8 тижня у жінок, які не отримували прогестерон. Середній вік матері був однаковий в обох групах: 35,4 року та 36,4 року.
У 23 випадках викиднів виконали хромосомне дослідження. Співвідношення жіноча-чоловіча стать у втраченого потомства становило 1,09.
У жінок, які отримували прогестерон, частка викиднів з аневплоїдіями становила 47,1% (8/17) порівняно з 33,3% (2/6) у жінок, які не отримували прогестерон, відмінність була статистично незначуща (P=0.66).
Успішних вагітностей було більше у жінок, які отримували прогестерон: 68% (86/126) порівняно з 51% (19/37; P=0.05) зі співвідношенням шансів 2,1 (95% ДI, 1.0–4.4).
При зворотному відборі за віком, індексом маси тіла, расою та іншими чинниками результат не змінювався. Для того, щоб отримати одну додаткову успішну вагітність, треба було призначити прогестерон від початку лютеїнової фази 6 жінкам.
Дискусія
У цьому обсерваційному когортному дослідженні виявили позитивний ефект від застосування вагінального прогестерону від початку фази жовтого тіла у жінок зі звичними викиднями.
Автори припускають, що таке лікування сприяє ліпшому розвитку залоз ендометрію та суттєво поліпшує мікросередовище для раннього розвитку зародка. Хоча молекулярний маркер n-циклін Е має поки що експериментальне значення, а його експресію у жінок з неускладненим виношуванням вагітності у цьому дослідженні не вивчали, результат засвідчують у 84% випадках нормалізацію експресії n-цикліну Е під впливом прогестерону.
Крім того, автори виявили поступове поліпшення результатів вагітностей водночас із нормалізацією експресії n-цикліну Е, тому повторна біопсія ендометрію на фоні приймання прогестерону у першому циклі була доцільною, оскільки давала можливість скоригувати дозу прогестерону у тих жінок, в яких експресія n-цикліну Е залишалася все ж підвищеною, незважаючи на розпочате лікування. Отже, імуногістохімічне дослідження молекулярних маркерів, зокрема n-цикліну Е, надійніше характеризує ендометріальний фактор при звичних викиднях, ніж саме лише патогістологічне дослідження. Для впровадження цього дослідження у практику потрібні проте додаткові дослідження.
Автори виявили, що у жінок зі звичними викиднями в анамнезі та підвищеною експресією n-цикліну Е частка успішних вагітностей при застосуванні прогестерону з початку фази жовтого тіла була вищою. Цікаво, що в жінок зі звичними викиднями та нормальною експресією n-цикліну Е частка успішних вагітностей при застосуванні прогестерону також буда вищою порівняно з такими ж пацієнтками, які не застосовували прогестерон. Автори вважають, що це міг бути ефект плацебо.
З іншого боку, n-циклін Е є лише одним із маркерів розвитку ендометрію, отже, лікування прогестероном могло позитивно впливати на експресію інших маркерів, які в цьому дослідженні не вивчали.
Як відомо, ретельне спостереження і підтримка є вирішальними в успішності вагітності, яка настає у жінки після звичних викиднів. Це пояснює той факт, що в жінок, які не отримували прогестерон, частка успішних вагітностей також була значуще вищою, ніж в минулому.
Позитивний ефект вагінального прогестерону в цьому дослідженні суперечить результатам нещодавнього рандомізованого дослідження PROMISE (Coomarasamy et al. 2015). Це дослідження охоплювало досить гетерогенну когорту пацієнток.
Крім того, у ньому не досліджували стан ендометрію в другу фазу циклу. Початок терапії прогестероном був дуже різний – від моменту позитивного тесту і до 6 терміну тижнів.
У коментарі до цієї публікації Joseph Stanford, Phil Boyle та Paul Carpentier (2016) аргументують відсутність позитивного ефекту від застосування прогестерону, перш за все, надто пізнім початком лікування. Як відомо, коротка фаза жовтого тіла або інші типи недостатності другої фази асоціюються з нижчою частотою настання клінічної вагітності та вищим ризиком викидня.
Отже, корекція другої фази, якщо її розпочати ще до імплантації, може суттєво поліпшити шанси на успішну вагітність.
Автори висловлюють сподівання, що вдасться виконати рандомізоване дослідження із плацебо-контролем, щоб остаточно з’ясувати, чи існує корисний ефект на вислід вагітності від лікування прогестероном з початку другої фази циклу у жінок зі звичними викиднями.
Однак, оскільки мікронізований прогестерон є безпечним і водночас не дуже дорогим лікуванням, автори вже тепер рекомендують на емпіричній засаді застосовувати його у жінок зі звичними викиднями від періоду після овуляції у тих циклах, в яких вони роблять спроби завагітніти.
Крім того, автори висловлюють побажання дальшого дослідження клінічної цінності молекулярних маркерів ендометрію, що дасть змогу визначити, у яких жінок позитивний ефект такої терапії буде найбільш виражений.
У записник клініцисту
- Лікування вагінальним мікронізованим прогестероном від початку другої фази циклу у жінок, які перебували під ретельним спостереженням змогу у 10 разів підвищити частку успішних вагітностей у жінок зі звичними викиднями – від 6 до 69%.
- Початок суплементації прогестерону у ранню лютеїнову фазу дає змогу позитивно вплинути на стан ендометрію на момент імплантації, і в цьому полягає, принаймні частково, механізм поліпшення шансі на успішну вагітність у жінок зі звичними викиднями.
- Молекулярні маркери ендометрію, зокрема, n-циклін Е, можуть стати корисними індикаторами для відбору пацієнток зі звичними викиднями для такої ранньої терапії прогестероном, однак для впровадження їх у практику потрібні дальші дослідження.
- Оскільки мікронізований прогестерон є безпечним і водночас не дуже дорогим лікуванням, доцільно на емпіричній засаді застосовувати його у жінок зі звичними викиднями від початку другої фази в тих циклах, в яких роблять спроби завагітніти.
При цьому важливо, щоб лікування було розпочате не раніше, ніж відбудеться овуляція (наприклад, згідно визначення піку ЛГ за допомогою домашніх тестів).
Перелік літератури знаходиться в редакції.


коментариев