Починаючи з 2006 року, після ліцензування першого покоління вакцин проти вірусу папіломи людини (ВПЛ), з’явилася надія на запобігання раку не лише шийки матки, але й вульви, піхви, порожнини рота, анального проходу, а отже можливості первинної профілактики більшості випадків такого раку. Перше покоління вакцин включало чотиривалентну вакцину проти ВПЛ 6/11/16/18 (Gardasil, MSD) і двовалентну вакцину проти ВПЛ 16/18 (Cervarix, GSK). З 2015 року вакцина другого покоління, вакцина дев’ятикомпонентної ВПЛ 6/11/16/18/31/33/45/52/58 (Gardasil 9, MSD), була ліцензована у Європі (Pils 2015). Тепер щеплення проти ВПЛ виконують у 76 країнах світу. У цьому огляді пропонуємо ознайомитися із найновішими публікаціями, які висвітлюють успіхи та перспективи щеплення проти ВПЛ, зокрема, останніми висновками Європейського Товариства з гінекологічної онкології та Європейської Асоціації кольпоскопії (ESGO–EFC, 2019)
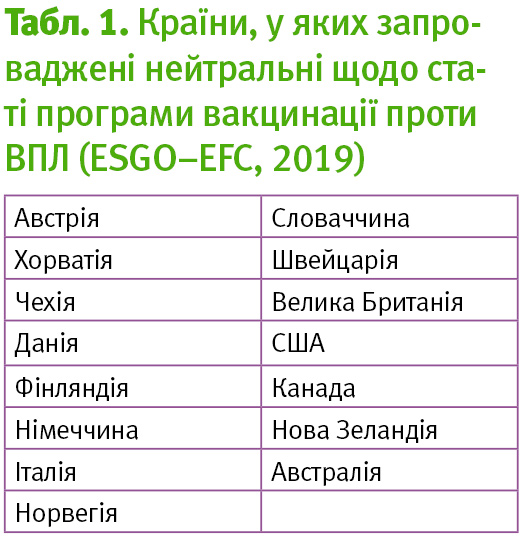
У Європі зареєстрували понад 50 000 нових випадків пов’язаного з ВПЛ раку, включаючи 35 000 випадків раку шийки матки та 10 000 випадків вульварного та вагінального раку (ESGO–EFC, 2019). Ці захворювання пов’язані із ВПЛ. У цій частині світу ВПЛ 16 спричинює 66% інвазивного раку шийки матки та понад 70% інших ракових захворювань, пов’язаних з ВПЛ. За частотою, після ВПЛ 16, йдуть типи HPV 18 і 33 (de Sanjose 2010). Експерти вважають, що за допомогою вакцин другого покоління майже 90% випадкам цих хвороб потенційно можна запобігти. Крім того, із 280 000–540 000 виявлених передракових уражень статевих органів більш ніж 80% можна запобігти вакцинами проти ВПЛ (Hartwig, 2015, Garland, 2018). Підсумки нещодавньої публікації ESGO–EFC представлені у табл. 1.
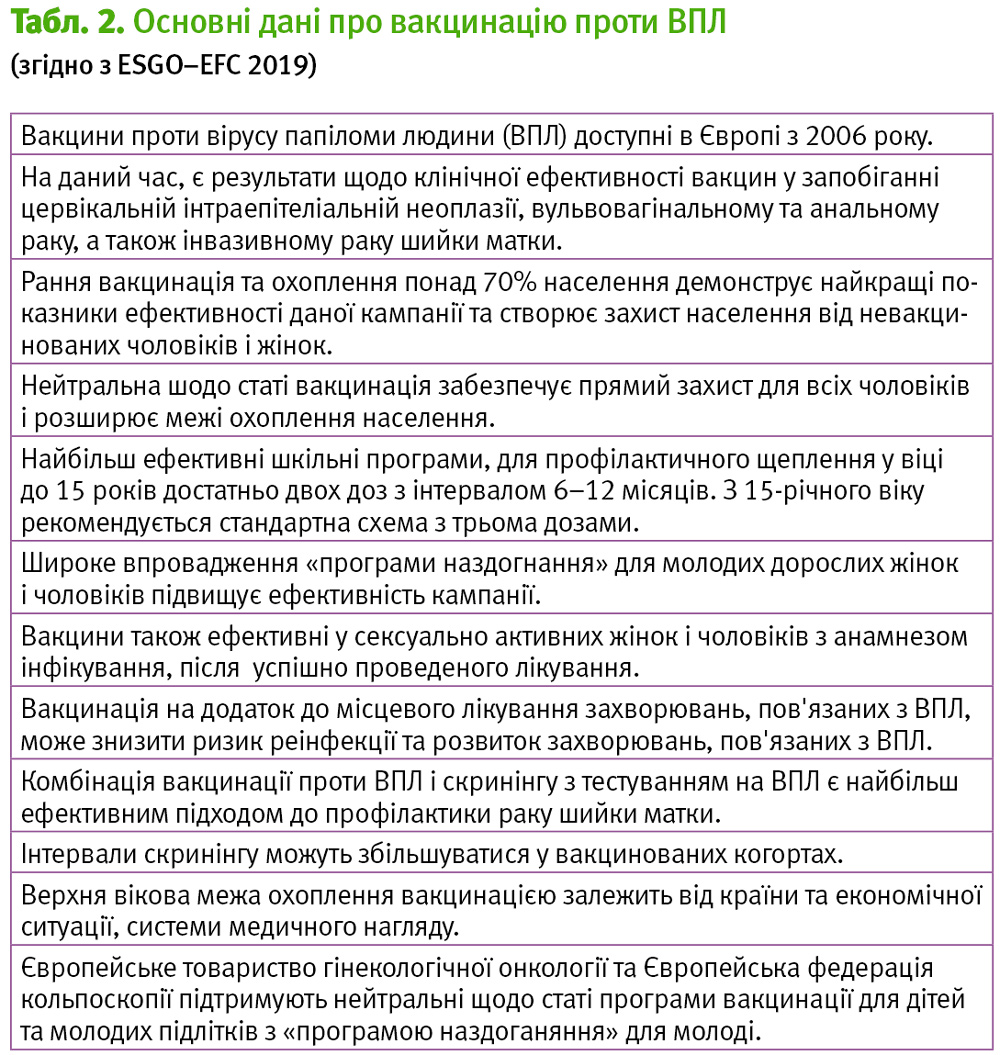
Результати клінічних досліджень
Клінічна ефективність вакцинації
Загалом, усі клінічні дослідження ІІІ фази вакцин проти ВПЛ охоплювали понад 70 тисяч учасників. Позитивний ефект вакцинації оцінили як 95% порівняно з відсутністю вакцинації (позитивним ефектом вакцинації тут вважають відсутність ДНК вірусу відповідних типів у матеріалі з шийки матки та інших органів-мішеней). Такий ефект спостерігали після щеплення молодих жінок віком 15–26 років. Для молодих чоловіків віком 16–26 років ефективність вакцинації оцінювали як 75%. Клінічний ефект спостерігали також у жінок віком 15–45 років (ESGO–EFC, 2019).
Тривалість ефекту
Експерти вважають, що тривалість захисного ефекту вакцинації сягає 10 років і більше. Зокрема, у дослідженні FUTURE II , у якому вивчали динаміку асоційованих із ВПЛ 16/18 патологічних станів, не спостерігали спалаху названих захворювань протягом 10-річного періоду (Kjaer, 2015). У другій фазі досліджень бівалентної ВПЛ-вакцини спостерігали 100% ефективність щеплення протягом періоду 9,3 року (Pils, 2015).
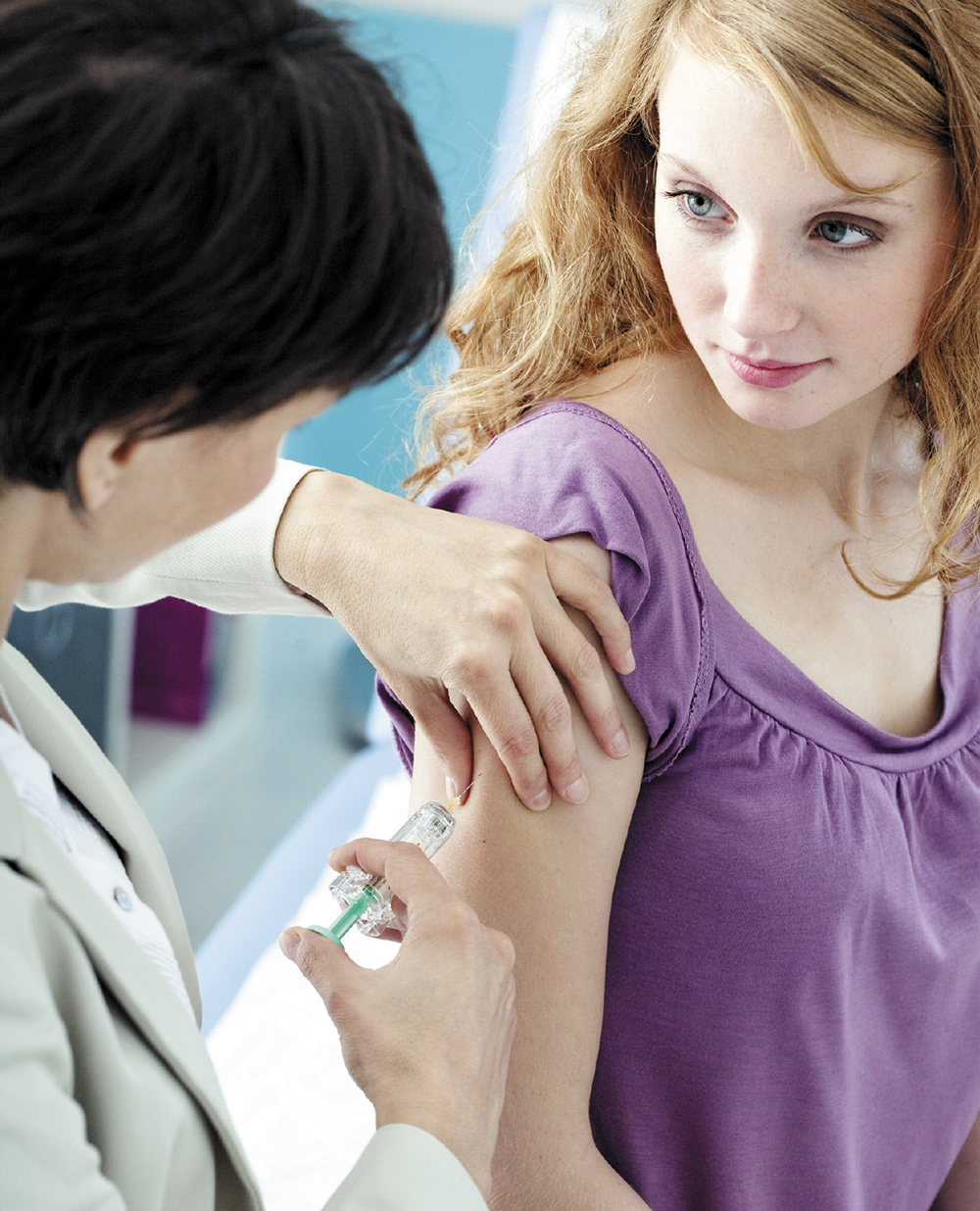
Скільки доз вакцини рекомендують вводити?
Підліткам до 15-річного віку рекомендують вводити дві дози вакцини з інтервалом 6–12 місяців. Для осіб віком понад 15 років рекомендують 3 дози вакцини.
Оскільки імуногенність вакцин зберігається протягом 10 років і більше, потреби ревакцинації загалом не бачать. Однак можливо, що особам, які отримали щеплення давнішими (двовалентними) вакцинами, буде доцільно виконати ревакцинацію новішими вакцини, наприклад, ноновалентною. Рішення про ревакцинацію наразі рекомендують приймати індивідуально в кожному випадку (ESGO–EFC, 2019).
Щеплення проти ВПЛ та захворювання, відмінні від раку шийки матки
Гострокінцеві кондиломи пов’язані з ВПЛ 6 і 11 типів. Пік захворюваності припадає на початок третього десятиліття життя. Поширеність захворювання у популяції оцінюють як 1%. Воно не є загрозливим для життя, проте спричинює суттєвий дискомфорт. Крім того, інфікування ВПЛ, які спричинюють гострокінцеві кондиломи, часто поєднується з високоонкогенними типами ВПЛ (Garland, 2009).
Згідно з дослідженням FUTURE, ефективність щеплення квадривалентною вакциною щодо запобігання гострокінцевим кондиломам становила 99% для жінок віком 16–26 років, які повністю отримали щеплення (групи per protocol). Для групи intention-to-treat (усі жінки, незалежно від того, повністю вони отримали щеплення, чи ні) цей показник становив 82% для жінок, які на момент включення у дослідження не були інфіковані ВПЛ, і 62% для групи, яка охоплювала і інфікованих, і неінфікованих раніше жінок (Dillner, 2010). Ефективність щеплення у запобіганні гострокінцевим кондиломам у чоловіків становила 90% (Giuliano, 2011).
Зростання поширеності інтраепітеліальної неоплазії вульви та інвазивного раку вульви у молодих жінок пояснюють інфікованістю ВПЛ. У старших вікових групах це захворювання має іншу природу та не пов’язане із ВПЛ. Захворювання спричинене в основному ВПЛ 16/18. У згаданому вже FUTURE ефективність щеплення у запобіганні інтраепітеліальній неоплазії вульви становила 100% для когорт per protocol і 79% для intention-to-treat (Dillner, 2010, Pils 2015).
Рак анального каналу трапляється в обох статей, проте частіше буває у жінок. Частіше зустрічається у чоловіків, які мають секс з чоловіками. Припущення про ефективність щеплення щодо запобігання раку анального каналу базується на суттєво меншій інфікованості ВПЛ серед щеплених осіб. Зокрема, із понад 600 щеплених чоловіків (які мали секс з чоловіками) ефективність щодо запобігання інфекції ВПЛ у когорті intention-to-treat була 54%, а в когорті per protocol 75%. У подібному дослідженні у республіці Коста-Ріка відповідні показники становили 62% та 84% через 4 роки після вакцинації (Pils, 2015).
Кого рекомендують щеплювати проти ВПЛ?
Імуногенність вакцин підтвердили від віку 9 років і для дівчат, і для хлопців, а також для жінок віком до 55 років. На основі цих даних Європейське медичне Агентство (EMA) рекомендує вакцинацію від 9-річного віку без верхньої вікової межі.
Національні програми щеплень запроваджені насамперед для дівчат, однак в деяких країнах також і для хлопців (табл. 2). Вакцина ліцензована для дітей від 9-річного віку.
Програми щеплень проти ВПЛ впроваджуються у деяких країнах і для жінок старших вікових груп. Зокрема, це програми «наздоганяння» (catch-up programs) для жінок віком до 26 і навіть до 45 років. Їхньою метою є запобігання реінфікування. Вважають, що такі програми доцільні з точки зору вкладення коштів, хоча ефективність їх менша, ніж щеплення підлітків. Хоча доцільність вакцинації у старшому віці найліпше визначати індивідуально у кожному випадку, експерти вважають, що на рівні популяції такі програми мають сенс у віці до 26 років, натомість для старших вікових груп вони навряд чи економічно доцільні (ESGO–EFC, 2019).
Зрештою, щеплення вважають можливим також для осіб, які перенесли лікування асоційованих з ВПЛ захворювань.
Реальна ефективність
У публікації ESGO–EFC (2019) у висновках про реальну ефективність щеплень спираються на дані популяційних досліджень, виконаних у країнах із широким охопленням вакцинацією: Австралії, Данії, Португалії та Великої Британії.
Зокрема, у Австралії за перші три роки після початку програми щеплення квадривалентною вакциною поширеність HSIL серед молодих жінок зменшилася удвічі (Brotherton, 2011). У Данії цей же показник знизився на 81% (Baldur-Felskov, 2014).
Щеплення бівалентною вакциною у Великій Британії знизило поширеність ВПЛ 18/18 на 82%, а невакцинних штамів ВПЛ 31/33/45 – на 49% (Mesher, 2018).
У Шотландії у популяції дівчат, щеплених у 12–13 років, поширеність HSIL зменшилася на 89% і невакцинних штамів – на 45% (Kavanagh 2017).
У фінському дослідженні Luostarinen et al. (2018), яке охоплювало понад 190 тисяч років-спостережень, вивчали поширеність різних видів асоційованого з ВПЛ раку. При цьому повідомили про 8 випадків інвазивного раку шийки матки, усі з яких виявили у невакцинованій когорті жінок.
Експерти ESGO–EFC оцінюють зниження інфікованості ВПЛ та асоційованої з ним захворюваності як надійне і стабільне, хоча ефективність вакцин щодо інших, ніж вакцинні, типів вірусу менша і короткочасніша.
Чому рекомендують щеплювати хлопців і чоловіків?
Доцільність нейтральних щодо статі програм щеплення від ВПЛ пояснюють кількома аргументами.
Перше, при щепленні лише дівчат захист чоловіків від асоційованих з ВПЛ хвороб залежить винятково від того, чи пройшли вакцинацію їх партнерки. Крім того, експерти висувають такий аргумент, що жодного захисту від щеплення жінок не будуть мати у такому разі чоловіки, які мають секс із чоловіками. При цьому висувають аргументи щодо рівності статей та однакового права на захист від асоційованих із ВПЛ хвороб.
Друге, експерти розраховують на поліпшення охоплення вакциною популяції і швидше формування колективного імунітету, для якого потрібно 70% вакцинованої популяції. Вони розраховують на те, що створення імунітету в чоловіків обмежить циркуляцію ВПЛ від невакцинованої популяції і у такий спосіб буде корисним для жінок. Крім того, експерти стверджують, що такі програми легше сприймаються в суспільстві і викликають менший опір, ніж програми, орієнтовані лише на жінок (ESGO–EFC 2019).
Щеплення жінок із перенесеними раніше захворюваннями, асоційованими із ВПЛ
Вакцинацію проти ВПЛ тепер рекомендують також жінкам і чоловікам, які були інфіковані, але позбулися вірусу. Метою такого заходу є запобігання реінфекції. Експерти вважають, що природний імунітет від ВПЛ є слабшим, ніж поствакцинний. Зокрема, у дослідженні Olsson et al., (2009) вивчали ефективність щеплення квадривалентною вакциною статево активних жінок, які були серопозитивні і ДНК-негативні щодо вакцинних типів ВПЛ. Дослідження охоплювало понад 2,5 тисячі учасниць, а спостереження тривало 40 місяців. У групі плацебо асоційовані з вакцинними типами ВПЛ захворювання шийки матки розвинулися у 8 випадках, а захворювання зовнішніх статевих органів у 7 випадках, тоді як у групі щеплених жінок таких захворювань за період спостереження не було.
Зрештою, експерти вважають можливим щеплення жінок після місцевого консервативного лікування інтраепітеліальної неоплазії шийки матки. Триразове щеплення жінок, інфікованих ВПЛ, вважають нешкідливим. З іншого боку, такі жінки мають високий ризик рецидиву преінвазивного захворювання шийки матки, який оцінюють як 5–10%, а ризик раку шийки матки у них у 2–4 рази вищий, ніж у популяції (ESGO–EFC, 2019). Дані досліджень вакцин 3 фази, а також ретроспективні дослідження дають змогу припускати, що ризик рецидиву HSIL може бути нижчим після вакцинації (Garland 2016, Ghelard 2018). Рішення про щеплення таких пацієнток наразі рекомендують приймати індивідуально. Ретельно це питання будуть вивчати у дослідженні NOVEL, яке розпочали у 2019 році (ESGO–EFC, 2019).
Чи можливе лікування ВПЛ-асоційованих захворювань за допомогою сучасних комерційних вакцин?
Вакцини проти ВПЛ, які є на ринку (Cervarix, Gardasil і Gardasil9), призначені лише для запобігання зараженню ВПЛ. Загалом, вони передбачають створення гуморального імунітету до капсидного білка L1, який відповідає за проникнення вірусу всередину клітини. На вірус, який опинився в клітині, вони не впливають, а отже й не мають лікувального ефекту.
Натомість тривають розробки терапевтичних вакцин, призначених для елімінації вірусу, що вже проник в епітеліальну клітину і активував свій геном. Такі вакцини спрямовані на створення специфічного Т-клітинного імунітету, спроможного атакувати уражені клітини. Однак для практичного застосування такі вакцини поки що недоступні (Chabeda 2018).
Поєднана стратегія вакцинації та скринінгу на ВПЛ
Поєднання щеплення від ВПЛ та скринінгу інфікованості цим вірусом (HPV-FASTER протокол) передбачає вакцинацію жінок віком 9–45 років, незалежно від інфікованості ВПЛ. Згідно з поясненнями експертів, щеплення від ВПЛ повинне захистити неінфікованих здорових жінок, незалежно від попереднього контакту з вірусом. Натомість щеплення інфікованих жінок має мету запобігти реінфекції тим самим типом вірусу (Joura et al., 2019).
Жінкам віком 25–30 років, крім вакцинації, рекомендується також скринінг на інфікованість ВПЛ при першому візиті. Це обстеження базується на даних, що при адекватному спостереженні за жінками з ВПЛ інфекцією ризик раку шийки матки наближається до нуля.
Метою такого протоколу є суттєве зменшення кількості необхідних оглядів у частини жінок, кількість яких можна звести до одного-двох протягом життя. Це поліпшує комплаєнтність та зменшує навантаження на заклади охорони здоров’я, які звичайно перевантажені пацієнтами, що звертаються для профілактичних оглядів.
Таку систему профілактики раку шийки матки пропонують для країн Центральної і Східної Європи, Латинської Америки, Азії і деяких більш розвинутих країн Африки (Bosch, 2016).
Безпечність вакцин
Незважаючи на те, що ESGO–EFC, Світова організація здоров’я та інші авторитетні організації оцінюють вакцини проти ВПЛ як цілком безпечні, сприйняття щеплення у світі через більш ніж десять років після його впровадження не можна описати як дуже позитивне. У недавньому огляді Cervantes et al. (2018) представили підсумки даних щодо побічних ефектів і побоювань, пов’язаних з застосуванням вакцини проти ВПЛ. Вони звертають увагу на низьку охопленість щепленням багатьох країн із різними рівнями економічного розвитку. Як приклад, автори згадують Канаду, де кількість відмов від щеплення дуже висока серед населення і з високим, і з низьким рівнем доходів (Remes et al. 2014).
Ще однією країною із високим рівнем доходів, які не сприйняла щеплення проти ВПЛ, є Японія. У Японії програма імунізації проти ВПЛ тривала всього лише 4 роки і була зупинена у 2014 році. Причиною були повідомлення про випадки хронічного болю та інших ускладнень, які виникали у щеплених осіб (Larson et al. 2014). Незважаючи на висновки експертів про непричетність вакцини до названих ускладнень, уряд Японії вирішив не відновлювати програму щеплень проти ВПЛ на національному рівні.
Побоювання, які гальмують програми вакцинації проти ВПЛ, базуються, перш за все, на недостатній безпеці такої інтервенції. Зокрема, в оглядовій статті Martinez-Lavin звертає увагу на притаманну новим вакцинам (також і проти ВПЛ) спроможність викликати несподівані симптоми, із яких найчастіше трапляються хронічний біль з парестезіями, біль голови, втома і ортостатичні реакції. Крім того, як ускладнення вакцинації проти ВПЛ, повідомляють про синдроми комплексного реґіонарного болю (complex regional pain syndrome (CRPS)), поступальної ортостатичної тахікардії (postural orthostatic tachycardia syndrome (POTS)) та фіброміалгії. При застосуванні вакцин проти ВПЛ ці реакції трапляються частіше, ніж при застосуванні інших вакцин. Причиною цих нечастих, але тяжких реакцій є ураження (демієлінізація) дрібних нервових волокон та дисфункція вегетативної нервової системи. Ці ускладнення трапляються хоч і нечасто, але й не так рідко, щоб ними можна було знехтувати. У 93% випадків такі реакції тривають довше 4 років та спричинюють інвалідність з неспроможністю навчатися чи працювати (Martinez-Lavin 2015). Ще одним прикладом є диспропорційно висока порівняно з очікуваною виробниками вакцин кількість випадків невропатичного болю у щеплених проти ВПЛ у Колумбії (Sanchez-Gomez 2014), що дуже негативно вплинуло на продовження програми вакцинації у цій країні.
У інших працях не виявили асоціації між щепленням проти ВПЛ та названими ускладненнями. Зрештою, Глобальний дорадчий комітет щодо безпеки вакцин (GACVS) та Центр із контролю та профілактики захворювань (CDC) зробили висновок про відсутність зв’язку описаних симптомів (також зареєстрованих в Японії) з вакцинацією проти ВПЛ (Gee et al. 2016). Однак деякі автори рекомендують сприймати ці висновки з обережністю, оскільки йдеться про захворювання та стани, які не мають чітко визначених діагностичних критеріїв, і тому такі ускладнення можуть бути проігноровані (Cervantes et al. 2018).
Побоювання щодо безпеки вакцин стосуються і реакцій на ад’юванти, перш за все алюміній. Відомо, що ці речовини можуть спричинити аутоімунні реакції у схильних до цього осіб. Термін «ASIA» (Autoimmune/inflammatory Syndrome Induced by Adjuvants) описує комплекс соматичних та неврологічних симптомів, які з’являються у перші три тижні після щеплення. Це астенія, біль голови, когнітивна дисфункція, міалгія, синусова тахікардія та висипка на шкірі. Названі симптоми можуть утримуватися довгий час (Palmieri, 2017). Як прояви аутоімунної/запальної реакції на щеплення описані епіглотит, артрит та рідкісне захворювання сітківки (multiple evanescence white dot syndrome) (Cervantes et al. 2018). Є повідомлення про тромбоцитопенію та появу антифосфоліпідних антитіл після щеплення проти ВПЛ. Однак ефекти вакцини не можна пояснити суто ад’ювантами, оскільки ускладнення у групі щеплених осіб траплялися частіше, ніж у групі, яка отримувала тільки ад’ювант (Bizjak et al. 2016).
На закінчення
Згідно припущень експертів, вакцина проти ВПЛ дасть змогу повністю позбутися раку шийки матки та інших захворювань, і досягнути цього вдасться у недалекому майбутньому. Зокрема, у Австралії збираються подолати рак шийки матки у найближчі 20 років. Однак офіційна статистика різних країн поки що засвідчує лише стабілізацію захворюваності на рак шийки матки на тому рівні, якого вдалося досягнути завдяки запровадженню цитологічного скринінгу. Наприклад, згідно з даними Australian Institute of Health and Welfare, цей показник зменшився приблизно удвічі від 1982 до 2002 року і далі стабільно залишається на цьому рівні, незважаючи на ефективне запровадження програми щеплень в останні 10 років. Подібно до цього, проєкт NORDCAN повідомляє про відносну стабільність захворюваності на рак шийки матки у країнах Північної Європи протягом останніх 10 років, де також успішно запровадили програму щеплень проти ВПЛ.
У публікації ESGO–EFC ці дані не коментують. Отже, відповісти на питання, чи зможе вакцинація проти ВПЛ подолати рак шийки матки, можна буде лише у майбутньому.
Література
Pils, S. and Joura, E.A. From the monovalent to the nine-valent HPV vaccine. Clin Microbiol Infect. 2015; 21: 827–833
Joura, Elmar A. et al . Human papillomavirus vaccination: The ESGO–EFC position paper of the European society of Gynaecologic Oncology and the European Federation for colposcopy. European Journal of Cancer, Volume 116, 21 - 26
Bosch, F.X., Robles, C., Diaz, M., Arbyn, M., Baussano, I., Clavel, C. et al. HPV-FASTER: broadening the scope for prevention of HPV-related cancer. Nat Rev Clin Oncol. 2016; 13: 119–132
Cervantes JL, Doan AH. Discrepancies in the evaluation of the safety of the human papillomavirus vaccine. Mem Inst Oswaldo Cruz. 2018;113(8):e180063. doi:10.1590/0074-02760180063
Pils, S. and Joura, E.A. From the monovalent to the nine-valent HPV vaccine. Clin Microbiol Infect. 2015; 21: 827–833
Olsson, S.E., Kjaer, S.K., Sigurdsson, K., Iversen, O.E., Hernandez-Avila, M., Wheeler, C.M. et al.Evaluation of quadrivalent HPV 6/11/16/18 vaccine efficacy against cervical and anogenital disease in subjects with serological evidence of prior vaccine type HPV infection. Hum Vaccine. 2009; 5: 696–704
Brotherton, J.M., Fridman, M., May, C.L., Chappell, G., Saville, A.M., and Gertig, D.M. Early effect of the HPV vaccination programme on cervical abnormalities in Victoria, Australia: an ecological study.Lancet. 2011; 377: 2085–2092
Baldur-Felskov, B., Dehlendorff, C., Munk, C., and Kjaer, S.K. Early impact of human papillomavirus vaccination on cervical neoplasia--nationwide follow-up of young Danish women. J Natl Cancer Inst. 2014; 106: djt460
Mesher, D., Panwar, K., Thomas, S.L., Edmundson, C., Choi, Y.H., Beddows, S. et al. The impact of the national HPV vaccination program in england using the bivalent HPV vaccine: surveillance of type-specific HPV in young females, 2010-2016. J Infect Dis. 2018; 218: 911–921
Kavanagh, K., Pollock, K.G., Cuschieri, K., Palmer, T., Cameron, R.L., Watt, C. et al. Changes in the prevalence of human papillomavirus following a national bivalent human papillomavirus vaccination programme in Scotland: a 7-year cross-sectional study. Lancet Infect Dis. 2017; 17: 1293–1302
Luostarinen, T., Apter, D., Dillner, J., Eriksson, T., Harjula, K., Natunen, K. et al. Vaccination protects against invasive HPV-associated cancers. Int J Cancer. 2018; 142: 2186–2187
Garland, S.M., Paavonen, J., Jaisamrarn, U., Naud, P., Salmeron, J., Chow, S.N. et al. Prior human papillomavirus-16/18 AS04-adjuvanted vaccination prevents recurrent high grade cervical intraepithelial neoplasia after definitive surgical therapy: post-hoc analysis from a randomized controlled trial. Int J Cancer. 2016; 139: 2812–2826
Ghelardi, A., Parazzini, F., Martella, F., Pieralli, A., Bay, P., Tonetti, A. et al. SPERANZA project: HPV vaccination after treatment for CIN2. Gynecol Oncol. 2018; 151: 229–234
Martínez-Lavín M Hypothesis: Human papillomavirus vaccination syndrome--small fiber neuropathy and dysautonomia could be its underlying pathogenesis. Clin Rheumatol. 2015 Jul; 34(7):1165-9.
Chabeda A, Yanez RJR, Lamprecht R, Meyers AE, Rybicki EP, Hitzeroth II. Therapeutic vaccines for high-risk HPV-associated diseases. Papillomavirus Res. 2018;5:46–58. doi:10.1016/j.pvr.2017.12.006
Australian Institute of Health and Welfare 2017. Cancer in Australia 2017. Cancer series no.101. Cat. no. CAN 100. Canberra: AIHW.
http://www-dep.iarc.fr/NORDCAN/english/frame.asp
Guo F, Hirth JM, Berenson AB. Comparison of HPV prevalence between HPV-vaccinated and non-vaccinated young adult women (20-26 years). Hum Vaccin Immunother. 2015;11(10):2337–2344. doi:10.1080/21645515.2015.1066948
Carozzi F, Puliti D, Ocello C, et al. Monitoring vaccine and non-vaccine HPV type prevalence in the post-vaccination era in women living in the Basilicata region, Italy. BMC Infect Dis. 2018;18(1):38. Published 2018 Jan 15. doi:10.1186/s12879-018-2945-8


коментариев