Результати та їхнє обговорення
Імплантація, інвазія трофобласта та плацентація є вкрай важливими процесами, які визначають перебіг і результат вагітності. При недостатності цих процесів виникають такі ускладнення вагітності, як гіпертензивні порушення, синдром втрати плода, передчасне відшарування нормально розташованої плаценти [2, 3, 7, 9, 13, 16].
Провідною патогенетичною ланкою при гіпергомоцистеїнемії (ГГЦ) є дисфункція ендотелію. Дисфункція ендотелію в цьому випадку виявляється у пригнобленні його антикоагулянтних і активації прокоагулянтних властивостей. Біохімічною основою цього процесу є індукований надлишком гомоцистеїну оксидантний стрес, збільшення продукції активних кисневих радикалів і порушення здатності до детоксикації перекисів [1, 4, 5, 7, 8, 14, 15].
На сьогодні дані про частоту ГГЦ у вагітних із загрозою невиношування вагітності та у жінок з обтяженим акушерським анамнезом, концентрації ГЦ під час фізіологічної вагітності, дозування застосування препаратів групи В мають неоднозначну відповідь [12, 13, 16].
Із метою визначення закономірностей у частоті та виразності ГГЦ у пацієнток із загрозою переривання вагітності, а також оцінки патогенетично обґрунтованих способів медикаментозної корекції цього стану ми проводили визначення рівнів гомоцистеїну (ГЦ) за триместрами вагітності, тому що фізіологічною особливістю під час вагітності є його зниження в міру прогресування терміну гестації: для І триместру вагітності нормальним вважався рівень ГЦ <5,6 мкмоль/л, для II триместру <4,3 мкмоль/л, для III триместру <3,3 мкмоль/л (табл. 4).
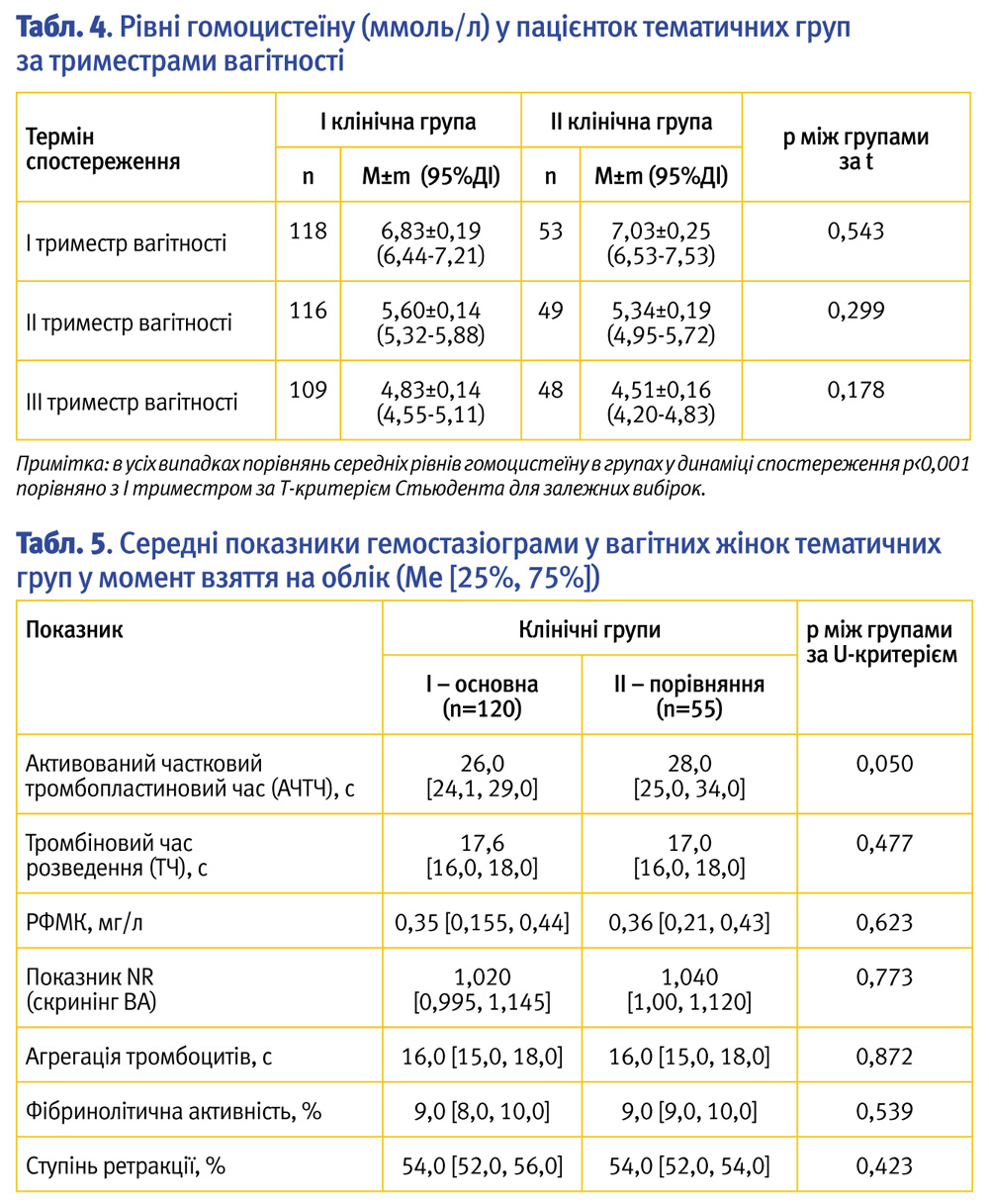
Кількість спостережень за триместрами в групі була різною у зв’язку з втратами вагітності та недоношуванням вагітності під час спостереження.
При вивченні рівнів ГЦ за триместрами вагітності (табл. 4) статистично значущих взаємозалежностей з ІМТ не виявлено (p>0,05).
Привертав увагу той факт, що для І та ІІ триместрів вагітності був характерний підвищений рівень ГЦ порівняно з нормами, що регламентуються. Невідповідність біохімічного маркера нормативним показникам клінічно відображалася на перебігу вагітності. Ці показники у І і ІІ триместрах були вищими в жінок із наявністю випадків втрати вагітності в анамнезі: 7,16±0,19 (95% ДІ: 6,77–7,54) проти 6,45±0,25 (95% ДІ: 5,94–6,95) в І триместрі (р=0,027 за t-критерієм), 5,69±0,14 (95% ДІ: 5,42–5,95) проти 5,15±0,21 (95% ДІ: 4,82–5,48) у ІІ триместрі (р=0,050).
Відповідні коефіцієнти кореляції становили: r=0,160, р=0,036 і r=0,184, р=0,018.
Підвищений рівень ГЦ у І та ІІ триместрах прямо корелював з ускладненим перебігом першої половини вагітності (r= 0,211, p=0,006 і r=0,215, p=0,005 відповідно по триместрах) та загрозою її переривання у другу половину (r=0,183, p=0,022 і r=0,145, p=0,069). Установлений зворотний кореляційний зв’язок між рівнями ГЦ в І та ІІ триместрах вагітності в жінок обох тематичних груп із рівнем вільного естріолу в терміні гестації 16–18 тижнів: r=-0,255, p=0,002 та r=-0,193, p=0,018 відповідно. Це доводило важливість впливу ГЦ на формування повноцінного фетоплацентарного комплексу, а отримані кореляційні залежності – про формування його недостатності.
Виражене зниження вільного естріолу, постійно низька величина або недостатній підйом рівня естріолу, які спостерігалися при підвищенні рівня ГЦ в тематичних жінок, вказували на порушення з боку фетоплацентарної системи. Усе це призводило до формування ризиків виникнення патологічних станів, які пов’язані з порушенням матково-плацентарного і фетоплацентарного кровотоку, а також утрудняють обмін попередників синтезу естрогену між плацентою та плодом, порушують ферментативну активність плаценти, негативним чином впливають на процеси життєдіяльності плоду.
Під час аналізу результатів гемостазіограми, яка досліджувалася в момент взяття на облік (табл. 5), достовірна кореляція з ІМТ була встановлена тільки для показника АЧТЧ (r= -0,193, р=0,010).
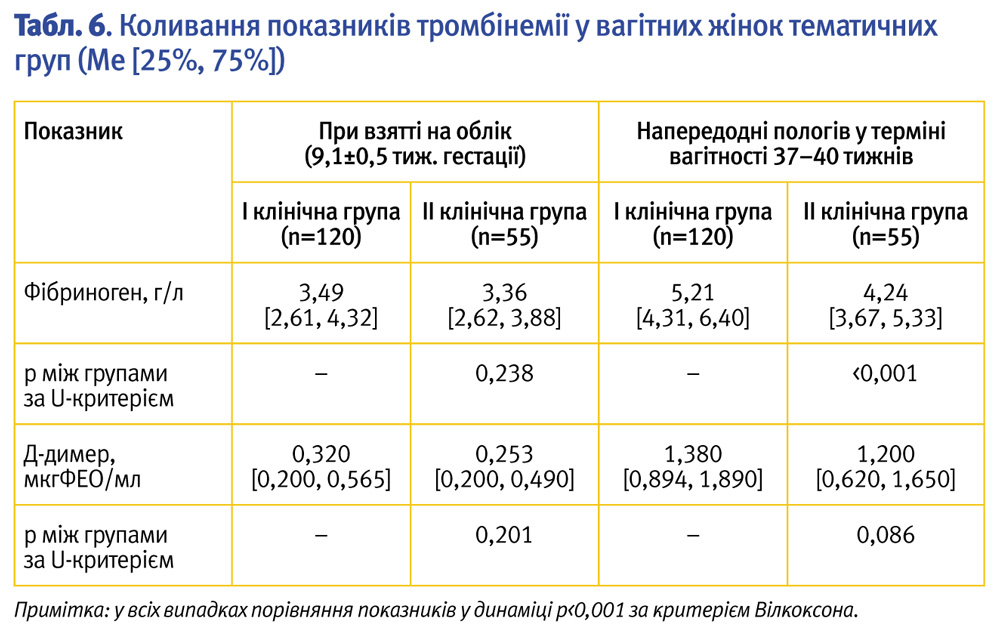
Взаємозв’язок показників гемостазіограми з мутацією генів тромбофілії та фолатного циклу відзначався в парах: АЧТЧ – ген F5-Лейден (r=-0,153, р=0,043), АЧТЧ – ген МТНFR: 1298 (r=0,151, р=0,046), агрегація тромбоцитів – F2-протромбін (r=0,149, р=0,049), агрегація тромбоцитів – ген F13A1 (r=-0,194, р=0,010), показник NR – ген F13A1 (r=0,228, р=0,002), ступінь ретракції – ген F13A1 (r=-0,162, р=0,032), ступінь ретракції – ген МТНFR: 677 (r=0,163, р=0,030).
Коливання рівня Д-димеру та фібриногену, як одних з основних характеристик тромбінемії, які досліджувалися в момент взяття на облік та у ІІІ триместрі вагітності, наведені в табл. 6.
Показники фібриногену і Д-димеру при взятті на облік не залежали від лікування, оскільки тематичні жінки до моменту забору крові не отримували антикоагулянтну й антиагрегантну терапію. Достовірного зв’язку цих показників з ІМТ у початковий період не відзначалося. В останні терміни гестації середній рівень фібриногену в жінок із надмірною масою тіла на 22,9% перевищував такий показник у ІІ клінічній групі (р<0,001), а коефіцієнт кореляції показника з ІМТ становив r=0,270, р<0,001.
Високі рівні Д-димеру в крові вагітної асоціювалися з неповним передлежанням плаценти (r=0,167, р=0,027) й ускладненнями гестації (r=0,185, р=0,032), а в пологах – із затримкою частин посліду (r=0,215, р=0,011). Підвищений рівень фібриногену корелював з ускладненим перебігом другої половини вагітності (r=0,153, р=0,043) та пологів (r=0,323, р<0,001). Зокрема, зростав ризик переривання вагітності (r=0,18, р=0,022), прееклампсії (r=0,179, р=0,036), затримки частин посліду (r=0,283, р<0,001).
За результатами кореляційного аналізу встановлено прямі зв’язки підвищеної концентрації сироваткового фібриногену з мутацією таких генів тромбофілії і фолатного циклу, як: ген F5-Лейден (r=0,199, р=0,011), ген Серпін 1 (r=0,178, р=0,022) і МТRR: 66 (r=0,151, р=0,046). Високі рівні Д-димеру у вагітних жінок асоціювались зі зниженням АЧТЧ (r=-0,154, р=0,049), підвищенням РФМК (r=0,155, р=0,047).
Чинники ризику розвитку невиношування вагітності, хронічної плацентарної дисфункції, прееклампсії досить схожі, тому відсутня можливість достовірного прогнозування розвитку цих станів [6, 9, 10, 11].
Таким чином, наведені вище факти обґрунтували актуальність проведених досліджень: визначення генетичних причин обтяженого акушерсько-гінекологічного анамнезу на генах-кандидатах, що мають відношення до тромбофілії та метаболізму фолієвої кислоти.
Висновки
- Патологічні зміни ендотелію призводять до порушення регуляції судинного тонусу, тромборезистентності судинної стінки, адгезії лейкоцитів і проникності судин, що веде до декомпенсації плацентарної дисфункції, яка клінічно може проявлятися антенатальною загибеллю плоду, синдромом затримки внутрішньоутробного зростання плоду або передчасним відшаруванням нормально розташованої плаценти.
- Жінки з обтяженим акушерсько-гінекологічним анамнезом складають групу ризику розвитку таких гестаційних ускладнень, як загроза переривання вагітності, дисфункція плацентарного комплексу, прееклампсія тощо. Основу патогенезу невиношування вагітності й патологічних станів, пов'язаних з пролонгацією вагітності, складає ембріоплацентарна дисфункція, клінічні прояви якої визначаються генетичним кодом і характером екзо- і ендогенних впливів.
Перелік літератури знаходиться у редакції.

коментариев