Настанова Європейського товариства кардіологів (ESC) (скорочений виклад)
- Легенева емболія (ЛЕ) та вагітність
9.1 Епідеміологія та фактори ризику розвитку легеневої емболії під час вагітності
Гостра ЛЕ залишається однією з провідних причин материнської смертності у країнах з високим рівнем доходу [379, 380]. Наприклад, у Великобританії та Ірландії тромбоз та тромбоемболія були найпоширенішими прямими причинами материнської смертності (смерть внаслідок розвитку вагітності, а не існуючих перед нею станів) протягом трирічного періоду 2013–2015 рр. При цьому смертність становила 1,13 на 100 000 матерів (npeu.ox.ac.uk/mbrrace-uk). Ризик ВТЕ у вагітних підвищений, порівняно з невагітними жінками аналогічного віку; впродовж вагітності він збільшується і досягає пікових значень у післяпологовий період [381]. Базовий показник ризику, пов’язаний з вагітністю, ще більш збільшується за наявності додаткових факторів ризику ВТЕ, куди входить запліднення in vitro: у поперечному дослідженні, отриманому зі шведського реєстру пологів, показник співвідношення ризиків для ВТЕ після запліднення in vitro становив 1,77 (95% ДІ 1,41–2,23) під час вагітності загалом, і 4,22 (95% ДІ 2,46–7,20) протягом І триместру [382]. Інші важливі та поширені фактори ризику включають ВТЕ у анамнезі, ожиріння, захворювання, спричинені прийомом медичних препаратів, невиношування, прееклампсію, післяпологові кровотечі та кесарів розтин. Тому оцінка задокументованих ризиків відіграє важливу роль [383].
Рекомендації, надані у цій настанові, відповідають рекомендаціям, що містяться в Настанові ESC 2018 з менеджменту серцево-судинних захворювань під час вагітності [384].
9.2 Діагностика легеневої емболії під час вагітності
9.2.1 Правила клінічного прогнозування та визначення D-димеру
Діагностика ЛЕ під час вагітності може бути складною, оскільки її симптоми часто перегукуються з симптомами нормальної вагітності. Загальна поширеність підтверджених випадків ЛЕ серед жінок, яких досліджували з приводу цього захворювання, була низькою, між 2 і 7% [385–388]. Рівні D-димеру під час вагітності постійно зростають [389, 390] і у ІІІ триместрі вони перевищують нижній поріг виключення ВТЕ майже у чверті вагітних жінок [390]. Результати мультинаціонального проспективного дослідження менеджменту 441 вагітної жінки, яка надійшла до відділення невідкладної допомоги з клінічними підозрами на ЛЕ свідчать про те, що діагностична стратегія, заснована на оцінці клінічної ймовірності, вимірюванні рівня D-димеру, проведенні ЛАКТ (легеневої ангіографії з використанням комп’ютерної томографії) та КУЗД (компресійного ультразвукового дослідження), дозволяє безпечно виключити діагноз ЛЕ під час вагітності [388]. У цьому дослідженні виключення ЛЕ на основі негативного результату дослідження D-димеру (без візуалізації) було можливим у 11,7% з 392 жінок з невисокою оцінкою можливості ЛЕ перед виконанням тесту (шкала Женеви). Цей показник знижувався до 4,2% у ІІІ триместрі [388]. У подальшому проспективному дослідженні ведення вагітних було оцінено поєднання адаптованого до вагітності алгоритму YEARS з визначенням рівня D-димеру у 498 жінок із підозрою на ЛЕ протягом вагітності. ЛЕ було виключено без виконання ЛАКТ у жінок, які, як вважалось, мали низький ризик ЛЕ, відповідно до комбінації алгоритму та результатів визначення D-димеру. Через 3 місяці лише у одної жінки з ЛЕ, виключеної на основі алгоритму, розвинувся тромбоз підколінної вени (0,21%, 95% ДІ 0,04–1,2). Випадків ЛЕ не спостерігалось у жодної жінки [391].
9.2.2 Методи візуалізації
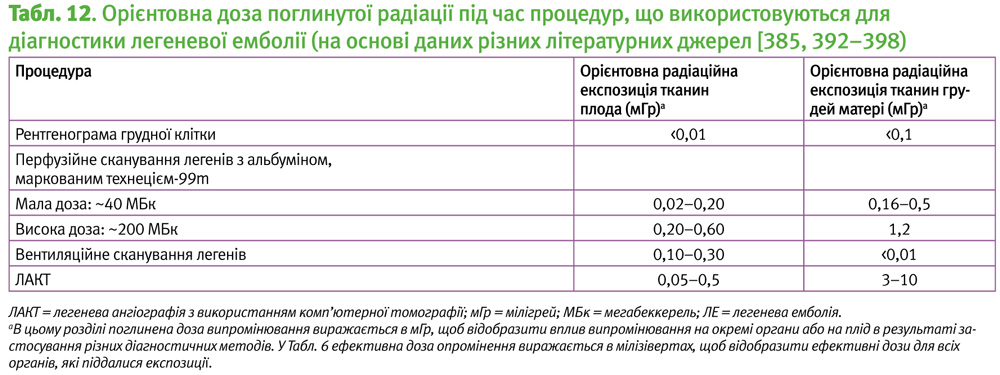
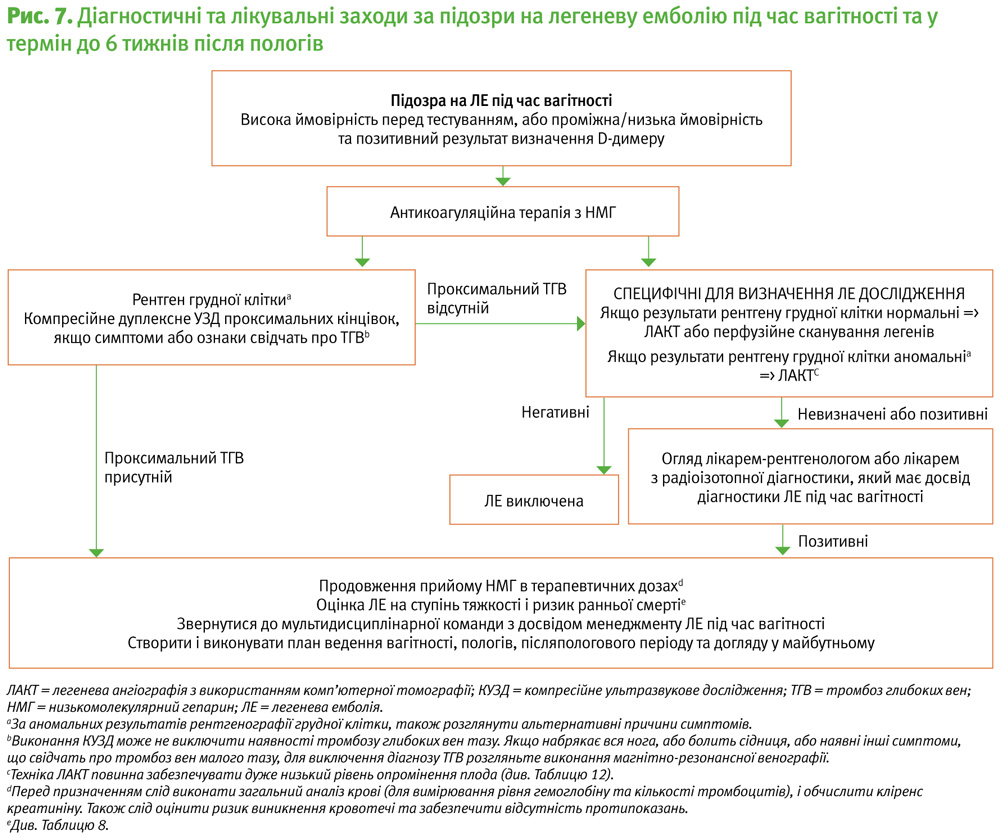
Запропонований алгоритм дослідження за підозр на ЛЕ у жінок під час вагітності або через <6 тижнів після пологів показаний на Рис. 7. При використанні сучасних методів візуалізації рівень радіаційного опромінення як вагітної, так і її плода є низьким (Табл. 12) [385, 392–398]. Під час дослідження В/П (вентиляції/перфузії) та ЛАКТ дози опромінення плода є значно нижчими за поріг, пов’язаний з виникненням ускладнень внаслідок дії радіації (50–100 мЗв) [399, 400]. У минулому повідомлялося, що ЛАКТ викликає опромінення грудей високими дозами [395, 401]; однак технології КТ розвиваються, і зараз існує кілька методів, за допомогою яких можна зменшити радіаційне опромінення без погіршення якості зображення. До них відносяться зменшення анатомічного покриття під час сканування [393]; зниження кіловольт при генерації випромінювання, використання ітеративних реконструктивних методик та зменшення компонента контрастного моніторингу ЛАКТ [392, 393]. Сучасні методи візуалізації ЛАКТ можуть довести середню дозу радіаційного впливу на груди матері до 3–4 мГр (Табл. 12) [392]. Вплив на ризик виникнення раку у матері при використанні сучасних методів ЛАКТ незначний (ризик раку протягом життя збільшується на коефіцієнт 1,0003–1,0007). Таким чином, уникнення виконання ЛАКТ з причини ризику виникнення раку в матері не є виправданим [394].
Нормальні результати перфузійного сканування та негативні результати ЛАКТ виявляються однаково ефективними для безпечного виключення діагнозу ЛЕ під час вагітності, як це пропонується у ретроспективних оглядах серій випадків [385, 386, 402–404]. Непереконливі результати можуть становити проблему (4–33% досліджень) [385, 386, 405], особливо в кінці терміну вагітності [405]. Нещодавнє дослідження, виконане на 24 сайтах у Великобританії, яке складає 15,5 млн. осіб, виявило аналогічний рівень неадекватних або невизначених результатів ЛАКТ та сцинтиграфії. Це дозволяє припустити, що початковий вибір методу візуалізації найкраще визначається локальним рівнем підготовки фахівців та наявністю ресурсів [406].
Застосування для В/П однофотонної емісійної комп’ютерної томографії (ОЕКТ) пов’язане з низьким рівнем опромінення плода і матері та є перспективним у діагностиці ЛЕ під час вагітності [407]. Однак, перед широким включенням цієї методики в діагностичні алгоритми потрібна її подальша оцінка. Для магнітно-резонансної ангіографії (МРА) невідомі наслідки тривалого впливу на плід контрасту на основі гадолінію. У невагітних пацієнток часто отримують технічно неадекватні зображення, а частота непереконливих результатів сканування є високою [140]. Тому використання цієї методики для діагностики наявності або виключення ЛЕ під час вагітності наразі не рекомендується. Застосування традиційної пульмональної ангіографії передбачає значно більшу радіаційну експозицію для плода (2,2–3,7 мЗв), тому її слід уникати під час вагітності [400].
Гіпердіагностика ЛЕ є також потенційно небезпечною і може нести суттєві наслідки для вагітної жінки, включаючи ризик виникнення кровотечі під час пологів, відмову від прийому естрогенних засобів контрацепції та необхідність тромбопрофілактики під час майбутніх вагітностей. Отже, уникнення гіпердіагностики ЛЕ при вагітності є так само важливим, як і непропущення діагнозу ЛЕ.
9.3 Лікування легеневої емболії під час вагітності
Призначення НМГ є методом вибору лікування ЛЕ під час вагітності [384]. На відміну від АВК (антагоністів вітаміну К) та НАВК (неантагоністів вітаміну К), НМГ не проходить крізь плаценту і, отже, не несе ризику виникнення фетальної кровотечі або тератогенності. Більше того, хоча нефракціонований гепарин (НФГ) також є безпечним під час вагітності, НМГ має більш передбачувану фармакокінетику та більш сприятливий профіль ризику [408–411]. Незважаючи на те, що оптимальну дозу НМГ для лікування ЛЕ під час вагітності не оцінювали у жодному РКД, опубліковані в наш час дані свідчать про значення доз, подібні до доз пацієнтів, які не є вагітними, у режимах один раз або двічі на добу, розрахованими на основі маси тіла жінки на початку вагітності [408, 410]. Для більшості пацієнтів, які отримували лікування ЛЕ під час вагітності з використанням НМГ [412, 413], залишається невідомим, чи може мати клінічну користь для коригування дози використання серійних вимірювань активності в плазмі крові антиактивованого фактора згортання.
Важливо враховувати, що: (i) НМГ має передбачуваний фармакокінетичний профіль; (ii) відсутні дані про оптимальні значення рівня анти-активованого фактора згортання, і (iii) аналіз має власні обмеження [414]. Окрім того, немає достовірних даних про клінічні переваги та негативний ефект частого коригування дози НМГ під час вагітності на основі значення маси тіла.
Таким чином, моніторинг анти-активованого фактору згортання X може бути зарезервований для специфічних обставин підвищеного ризику, таких як повторний епізод ВТЕ, порушення функції нирок та екстремальні показники маси тіла.
Застосування НФГ асоціювалось з індукованою гепарином тромбоцитопенією та втратою кісткової маси. Залишається невизначеним питання, чи збільшується ризик втрати кісткової маси при застосуванні НМГ. У нещодавньому обсерваційному когортному дослідженні, у якому мінеральну щільність кісткової тканини вимірювали із застосуванням двоенергетичної рентгенівської абсорбціометрії через 4–7 років після останніх пологів у 152 жінок (92 з яких отримували під час вагітності НМГ у пролонгованому режимі), мінеральна щільність кісток поперекового відділу після врахування дії потенційних спотворюючих факторів була подібною до такої у жінок, які отримували НМГ, та групи контролю. Про випадки остеопорозу або остеопоротичних переломів не повідомлялося [415].
Застосування фондапаринуксу можна розглянути за наявності алергічних або несприятливих реакцій на НМГ, хоча відсутні достовірні дані щодо його ефективності, а також було продемонстровано незначне його трансплацентарне проникнення [416].
АВК проходять крізь плаценту і асоціюються з чітко вираженою ембріопатією протягом І триместру. Прийом АВК у ІІІ триместрі може призвести до розвитку крововиливів у плода та новонародженого, а також до відшарування плаценти. Застосування варфарину може бути пов’язане з розвитком аномалій центральної нервової системи плода протягом всієї вагітності. Призначення НАВК вагітним пацієнткам протипоказане [417].
Ведення пологів потребує особливої уваги. У жінок, які отримують НМГ з терапевтичною метою, слід ретельно планувати пологи у співпраці з багатодисциплінарною командою, щоб уникнути ризику спонтанного їх початку, під час використання антикогуляційної терапії у повному обсязі. У вагітних, які перебували на лікуванні антикоагулянтами, не було повідомлень про випадки виникнення спінальної гематоми після регіональної анестезії. Якщо регіональна аналгезія виконується для жінки, яка отримує НМГ з терапевтичною метою, з моменту введення останньої дози НМГ і до введення спінальної або епідуральної голки повинно пройти ³24 годин (за умови нормальної функції нирок і з урахуванням ризиків, пов’язаних з екстремальною масою тіла).
У ситуаціях високого ризику, наприклад, у пацієнток з недавнім епізодом ЛЕ, їх рекомендується перевести з НМГ на НФГ за ³36 годин до початку пологів. Інфузію НФГ слід припинити за 4–6 год. до передбачуваного часу початку пологової діяльності, перед регіональною анестезією значення активованого часткового тромбопластинового часу повинні бути нормальними (тобто не збільшеними) [418].
Дані щодо оптимальних термінів поновлення лікування НМГ після пологів є обмеженими [419, 420]. Ці терміни будуть залежати від способу розродження та оцінки ризику виничнення тромбозу або кровотечі багатодисциплінарною командою. НМГ не слід призначати через ³4 год. після видалення епідурального катетера; під час прийняття рішення про терміни початку та дозу лікування слід встановити, чи було введення в епідуральний простір травматичним, та враховувати профіль ризику жінки.
Наприклад, введення проміжної профілактичної дози НМГ може бути розглянуте у післяопераційному періоді (після кесаревого розтину), коли пройшло не менше 4 год. після видалення епідурального катетера та з урахуванням інтервалу ³8–12 год. між профілактичною та наступною терапевтичною дозою. Рекомендується тісна співпраця між акушером, анестезіологом та лікуючим лікарем.
Терапію антикоагулянтами слід розпочинати у термін ³6 тижнів після пологів, з мінімальною загальною тривалістю лікування 3 місяці. НМГ та варфарин можна призначати годуючим матерям; застосування НАВК не рекомендується [417].
ЛЕ під час вагітності — рідкісна, але потенційно катастрофічна подія з високим рівнем ризику і загрози життю. Нещодавно проведений систематичний огляд включав 127 випадків тяжкої ЛЕ під час вагітності (і до 6 тижнів після пологів), при яких застосовувались тромболізис, тромбектомія та/або екстракорпоральна мембранна оксигенація (EКMO) [421]. До огляду були включені випадки ЛЕ як високого, так і середнього ризику. 23% жінок зазнали зупинки серцевої діяльності. Зафіксовані показники виживаності становили 94 та 86% після тромболізису та хірургічної тромбектомії відповідно; однак такі сприятливі показники, можливо, були отримані через неточності при написанні звіту. Після тромболізису масивні кровотечі виникали у 18 та 58% випадків, під час вагітності та після пологів відповідно [421]. Загибель плода було зафіксовано в 12 і 20% випадків після виконання тромболізису і тромбектомії відповідно [421]. Тромболітичну терапію не слід застосовувати в перинатальному періоді, за винятком випадків, коли ЛЕ становить небезпеку для життя. Зазвичай НМГ застосовують при інтенсивному лікуванні ЛЕ високого ризику.
Хоча показання до встановлення вагітним фільтрів порожнистої вени (кава-фільтрів) схожі з показаннями для невагітних пацієнтів, (обговорення в Розділі 6), досвід їх використання при вагітності є обмеженим, і ризик, пов’язаний з процедурою, може бути збільшений.
Пропозиції щодо лікування антикоагулянтами ЛЕ у специфічних клінічних ситуаціях, пов’язаних із вагітністю, для яких відсутні переконливі докази наведені у додатковій Табл. 9.
9.3.1 Роль кардіологів у складі мультидисциплінарної команди при лікуванні тромбозів під час вагітності
Мультидисциплінарна команда фахівців повинна співпрацювати під час планування тактики до-, пери- та післяпологового догляду жінок із серцево-судинними захворюваннями, включаючи ЛЕ. Якнайбільше членів цієї команди повинно мати досвід в галузі менеджменту ЛЕ під час вагітності та у післяпологовому періоді. Для ефективної комунікації повинні бути доступними спільно узгоджені і зафіксовані в документації маршрути догляду (якщо терміни дозволяють) (Приклад показаний на Рис. 7).
9.4 Емболія навколоплодовими водами
Емболія навколоплодовими водами (ЕНВ) — рідкісний стан, що виникає під час вагітності або незабаром після пологів. Вона залишається однією з провідних прямих причин материнської смертності (смерть внаслідок розвитку вагітності, а не існуючих перед нею станів) у країнах з високим рівнем доходу [422].
Діагностика ЕНВ є складним завданням, в основному це клінічний діагноз виключення. Поінформованість про ЕНВ, швидка діагностика та проведення агресивних реанімаційних заодів мають вирішальне значення.
ЕНВ характеризується раптовим погіршенням роботи серцево-судинної або дихальної системи невстановленої етіології, що часто супроводжується синдромом дисемінованого внутрішньосудинного згортання [422], і виникає під час вагітності або після пологів [423, 444].
Захворюваність становить приблизно 2–7 випадків на 100 000 пологів, рівень смертності — 0,5–6 смертей на 100 000 пологів [422, 425, 426]. Зафіксовані летальні випадки дуже відрізняються між собою, що відображає проблеми діагностики та рідкісність ЕНВ.
У ретроспективному дослідженні, проведеному в Каліфорнії, яке включало понад 3,5 мільйони пологів, повідомлялось про рівень летальності 13%, як і в інших дослідженнях США та Канади [425]. Аналогічно, в недавно проведеному у Великобританії проспективному популяційному дослідженні з валідованими критеріями включення випадків повідомлялось про рівень летальності 19% [422]. У літературних джерелах останнім часом припускається, що факторами ризику ЕНВ можуть бути наявні серцеві, цереброваскулярні та ниркові розлади, передлежання плаценти, багатоводдя, мертвонародження, хоріоамніоніт, гіпертонічні розлади, інструментальне розродження та кесарів розтин [422, 425].
Терапія при ЕНВ є підтримувальною та ґрунтується на наданні високоефективної екстреної допомоги після розпізнавання та діагностики стану, з оперативним лікуванням кровотеч та коагулопатії [423]. Поінформованість щодо ЕНВ має бути невід’ємною частиною освіти залучених лікарів та алгоритмів дії у невідкладних ситуаціях.
Перелік літератури на сайті
Extempore.info

коментариев