Неонатальний сепсис, перш за все у дітей з дуже малою масою при народженні (ДММТ), є важливою причиною захворюваності та смертності, а також незалежним чинником ризику негативних віддалених наслідків. Кілька попередніх публікацій журналу були присвячені сепсису новонароджених, але вони стосувались, головним чином, раннього неонатального сепсису
Визначення пізнього неонатального сепсису (ПНС)
Термін «неонатальний сепсис» використовується для позначення системного стану бактеріального походження, пов'язаного з гемодинамічними змінами та системними клінічними проявами [1]. Незважаючи на роки досліджень, залишається актуальною проблема його консенсусного визначення.
По-перше, традиційно визначення сепсису потребує виділення патогена зі стерильної в нормі рідини організму. Але існує й поняття «клінічного сепсису» (тобто сепсису з негативною культурою крові або без визначення такої культури). Крім того, клінічна різниця між сепсисом з виявленим патогеном та сепсисом з невідомим патогеном невелика.
По-друге, оскільки клінічні особливості сепсису можуть бути індуковані сильними прозапальними цитокінами, то для опису патології використовується термін «синдрому системної запальної відповіді». Але інвазивні інфекції можуть мати місце у майже асимптоматичних новонароджених.
По-третє, визначення неонатального сепсису ускладнюється існуванням неінфекційних захворювань, що за своїми проявами нагадують сепсис, особливо у недоношених немовлят з ДММТ, а також відсутністю оптимальних діагностичних тестів [1-3].
Згідно часу і способу зараження, ми можемо розрізняти ранній сепсис новонародженого, діагностований протягом перших 72 годин життя (або перших 7 днів життя), і пізній неонатальний сепсис, коли інфекція проявляється пізніше.
При ПНС має місце постнатальне зараження (можлива й інфекція, пов’язана з пологами, але з відстроченими клінічними проявами) [1–3]. Для новонароджених, які потребують тривалої госпіталізації (діти з екстремально малою масою при народженні), визначення ПНС може застосовуватися до будь-якого епізоду сепсису після перших 7 днів життя і до виписки зі стаціонару незалежно від віку на час епізоду (сепсис, що розвивається після тримісячного віку, «дуже пізній») [4].
Частота
Інформація про загальну частоту випадків неонатального сепсису є різною для неонатальних відділень країн з високим рівнем доходу й країн з низьким та середнім рівнем доходу. Повідомляють про частоту від 1–5 до 49–170 випадків сепсису на 1000 живонароджених.
ПНС – це, насамперед, «інфекція, пов’язана з наданням медичної допомоги», ризик розвитку якої зворотньо пропорційний гестаційному вікові (ГВ) і масі при народженні. Згідно даних, представлених в оглядах Cortese F. та співавт. (2016), Stoll BJ та співавт. (2002) частота ПНС серед новонароджених з ГВ 34–37 тиж. становить 6–10%, а при ГВ <25 тиж. – 46% [2, 5].

Фактори ризику ПНС
Отже, найважливіші фактори ризику ПНС – недоношеність і низька маса при народженні, які обумовлюють наявність імунної дисфункції та відсутність трансплацентарно набутих материнських IgG антитіл [1, 2]. Фактором ризику ПНС є необхідність тривалого інтенсивного лікування новонароджених дітей: ендотрахеальна інтубація, тривалий внутрішньовенний доступ та інші інвазивні процедури, які надають інфекційне навантаження, забезпечують портали для входу інфекції або послаблюють бар'єрні механізми (табл. 1) [1, 2]. Джерелами для інфікування є персонал лікарні, члени сім'ї, забруднене обладнання. Забруднення рук є найвагомішим чинником постнатальних інфекцій у немовлят [1, 2]. Нижчий рівень 25-гідроксивітаміну D пов'язаний з раннім початком неонатального сепсису [6].
Мікроорганізми-збудники
Згідно даниз Stoll BJ та співав. (2002) 70% випадків ПНС були обумовлені грампозитивними мікроорганізмами (серед них Coagulase negative staphylocоcci (CoNS) в 48%), грамнегативними збудниками в 18% випадків, і грибкова інфекція мала місце у 12% випадків [5].
Дані досліджень, проведених у Великобританії в 2006–2008 рр. (NeonIN Surveillance Network), показали, що грампозитивні мікроорганізми складають 70% серед збудників сепсису, грамнегативні – 25% і гриби – 5%. Серед грампозитивних мікроорганізмів Coagulase negative staphylocоcci відповідали за 42% інфекцій, Staphylococcus aureus – 10%, Enterococci – 9%, Group B streptococcal – 5%, а інші – 4%. Серед грамнегативних збудників E. coli складала 8%, Klebsiella spp. – 5%, Enterobacter spp. – 5%, Pseudomonas spp. – 3% і інші організми – 4%. Candida spp. була відповідальною за всі грибкові інфекції [3, 10].
Слід відмітити, що поширеність патогенних мікроорганізмів значно відрізняється серед різних країх з помітним вищим ризиком грамнегативних інфекцій в районах з недостатніми ресурсами [1, 11]. Неонатальні дослідження NICHD Neonatal Research Network, (neonatal.rti.org), які вивчали епідеміологію неонатальних інфекцій серед тисяч новонароджених з ДММТ, показали, що хоча серед збудників ПНС й переважали грампозитивні мікроорганізми, смертність дітей від інвазивного кандидозу і грамнегативних інфекцій була у 2–3 разів вищою, ніж від грампозитивних інфекцій [3, 5].
Клінічні симптоми
Клінічні прояви можуть мати діапазон від субклінічної інфекції до серйозних симптомів хвороби. Типові початкові клінічні ознаки та симптоми інфекції у новонароджених представлені у табл. 2.
Початкові симптоми можуть бути нечисленними і включати апное або тахіпное з ретракцією, кректання/стогін, тахікардію. Пізніші ускладнення сепсису представлені респіраторними порушеннями, легеневою гіпертензією, серцевою недостатністю, шоком, нирковою недостатністю, дисфункцією печінки, набряком мозку, тромбозами, крововиливами у наднирники або недостатністю наднирників, дисфункцією кісткового мозку (нейтропенія, тромбоцитопенія, анемія), дисемінованою внутрішньосудинною коагуляцією [1].
Патологічними процесами, які, з одного боку, підвищують ризик розвитку сепсису, а з іншого, можуть імітувати його ознаки, є вроджені вади розвитку, хвороби дихальних шляхів (респіраторний дистресс-синдром, аспірація), некротизуючий ентероколіт, метаболічні захворювання (наприклад, галактозамія) [1].
Додаткова діагностика
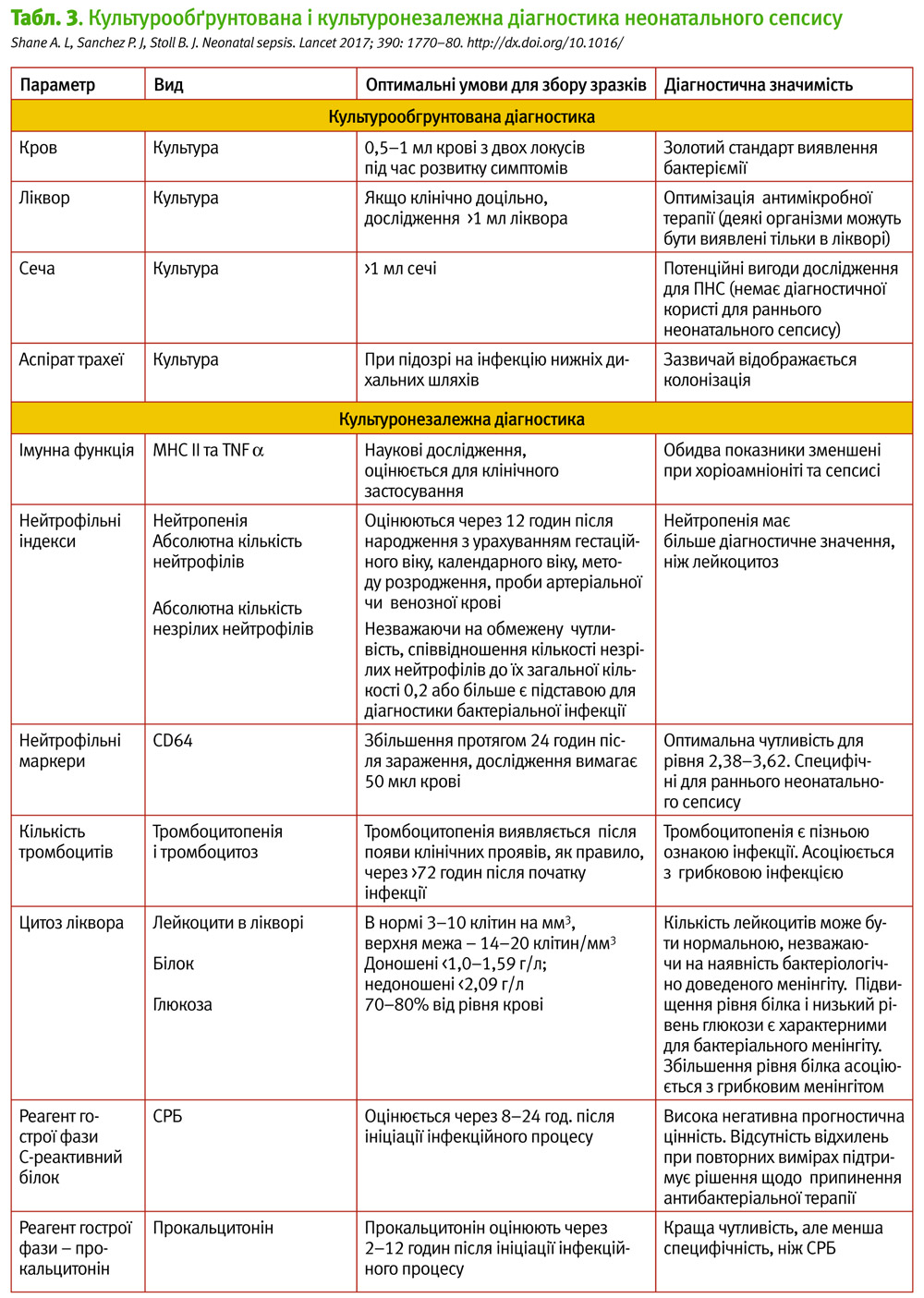
Методи додаткової діагностики включають: мікробіологічні дослідження біологічних зразків (кров, сеча, ліквор, тощо); дослідження рівня запальних біомаркерів сироватки крові (реагенти гострої фази, зміни в аналізах крові, запальні цитокіни); ідентифікацію збудника за допомогою методів молекулярної генетики (ампліфікація цільових фрагментів ДНК/РНК) (табл. 3).
Традиційно неонатальний сепсис повинен бути лабораторно підтвердженим шляхом виділення збудника зі стерильних в нормі середовищ організму (кров, ліквор, сеча, плевральна рідина, тощо). Щоб оптимізувати діагностику, зразки повинні бути адекватного об'єму (для культур крові мінімум 0,5–1 мл, бажано з двох різних локусів), асептично отримані. При використанні різних венозних доступів, культури крові ідеально було б одержати одночасно і з периферичного, і з центрального катетера (для диференціації «периферічної бактеріємії» і катетер-пов'язаних інфекцій крові) [1, 12].
Ідентифікація збудника за допомогою методів молекулярної генетики (ампліфікація цільових фрагментів ДНК/РНК) є надзвичайно чутливою і швидкою технікою, для якої достатньо зразка невеликого об'єму. Але можливою є помилкова ідентифікація в якості збудника технічного бактеріального забруднення.
Діагностичні алгоритми
Експертні групи намагалися розробити алгоритми діагностики ПНС шляхом включення різних комбінацій параметрів клінічного огляду, маркерів запальної відповіді та лабораторних досліджень, але діагностика не була надійною. У дослідженні, яке включало 113 дітей і проводилось у п’яти європейських країнах, прогностична цінність критеріїв для виявлення підтвердженого мікробіологічно ПНС склала 61% [13].
Антибактеріальна терапія – емпірична терапія ПНС
Хоча бажано отримати культури крові перед початком лікування, антимікробна терапія у дітей з проявами сепсису чи септичного шоку не повинна затримуватись для збору аналізів.
По-перше, слід враховувати наявні дані досліджень. Нозокоміальні захворювання у недоношених новонароджених, обумовлені Coagulase negative staphylocоcci, як зазначалось раніше, є відносно поширеними у неонатальних відділеннях країн з високим рівнем доходу, вони пов'язані з довгостроковими порушення неврологічного розвитку. Але інфекції, викликані грамнегативними бактеріями, обумовлюють значно вищий рівень смертності.
Тож у якості емпіричної терапії першої лінії рекомендують використовувати ванкоміцин и аміноглікозид (тривалість лікування залежить від збудника та клінічних проявів). Емпіричний вибір ванкоміцину обумовлюється тим, що переважна більшість ізолятів Coagulase negative staphylocоcci є стійкими до бета-лактамних агентів, включаючи пеніциліназостійкі пеніциліни. Комбінація з використанням аміноглікозиду має переваги через менший ризик формування резистентності [1, 2, 14].
По-друге, при виборі препаратів для емпіричної терапії слід керуватись даними мікробного моніторингу відділень (форми мікроорганізмів, їх резистентність). Тож, альтернативу глікопептиду визначають на підставі місцевих епідеміологічних даних та особливостей клінічного перебігу інфекції [1, 2, 14]. Слід передбачити:
- доцільність використання цефалоспоринів за наявності менінгіту;
- мати на увазі потребу призначення карбапенемів, якщо дитина нещодавно отримувала цефалоспорини 3-ї генерації;
- призначення протигрибкових препаратів профілактично (внутрішньовенно) дітям з масою тіла <1500 г [1, 2, 14].
Неонатологи є одними з найбільших споживачів ванкоміцину, і, цілком можливо, що більша частина цього використання недоцільна. З виникненням резистентності до ванкоміцину серед метицилін-резистентних стафілококів (MRSA) та виділенням Enterococcus faecium з його відомими зв'язками з попереднім призначенням ванкоміцину (ванкоміцин-стійкі ентерококи) стало важливим зменшити використання ванкоміцину. Декілька досліджень у Північній Америці та Європі показали, що зменшення використання ванкоміцину можна досягти безпечно без змін у летальності, тривалості бактеріємії або частоті ускладнень, пов'язаних з ПНС [15, 16, 17].

Romanelli et al. (2016) у своєму дослідженні порівнювали частоту нозокоміальних інфекцій у відділеннях інтенсивної терапії новонароджених (відділення з високою поширеністю Coagulase negative staphylocоcci та низькою – MRSA) серед дітей з високим ступенем ризику (ДММТ, наявність центрального венозного катетера, використання механічної вентиляції, операції та лікування з анти-мікробними препаратами) протягом двох періодів [17]:
- періоду січень 2011 р. – грудень 2012 р., коли ванкоміцин був використаний для емпіричної терапії можливого пізнього сепсису;
- періоду січень 2013 р. – грудень 2014 р., коли оксацилін був препаратом вибору.
Протягом періоду лікування оксациліном відбулось значне зниження числа інфекцій, викликаних Staphylococcus aureus (p=0,008), а також зниження частоти смертей, пов'язаних з ними. Істотних змін у поширеності грамнегативних бактеріальних або грибкових інфекцій не відбулося. Не спостерігалося достовірного збільшення пов'язаної з Coagulase negative staphylocоcci захворюваності та смертності [17].
Karlowicz M. G., et al. (2000) пов'язували попереднє емпіричне використання ванкоміцину з наступним розвитком грамнегативного сепсису [18].
Антибактеріальна терапія – спрямована терапія
Після виявлення збудників і отримання відомостей про їх резистентність, а також з урахуванням локусів інфекції, обираються найбільш відповідні антимікробні препарати (тривалість лікування варіюється від 7 до 21 днів). Лікування припиняється тоді, коли патоген не ідентифікується, не спостерігається жодних ознак і симптомів інфекції [19].
Додаткова терапія
Три рандомізовані контрольовані дослідження, що порівнювали ефективність переливання гранулоцитів і плацебо у 44 немовлят з неонатальним сепсисом, не показали зниження смертності [3, 19].
Рекомбінантні гранулоцитарні фактори (G-CSF і GM-CSF) стимулюють функцію нейтрофілів, однак не запобігають виникненню інфекцій і не зменшують інфекційну летальність, тому клінічне застосування їх не рекомендується ні з метою профілактики, ні для лікування інфекцій у новонароджених [3, 20].
Collaborative Group INIS продемонструвала, що інфузії полівалентного імуноглобуліну G не впливають на короткострокову та довгострокову захворюваність або смертність новонароджених із сепсисом. Проте окремий аналіз результатів лікування підгрупи немовлят з ГВ 26–29 тиж. у цьому дослідженні показав, що використання внутрішньовенних імуноглобулінів у таких дітей вірогідно зменшувало ризик смерті або важкої інвалідності до досягнення віку 2 років (відносний ризик [ВР] – 0,86; 95% ДІ: 0,76-0,98) [3, 14, 21].
Кокранівський огляд десяти рандомізованих контрольованих досліджень вважає, що все ще є недостатньо доказів для підтримки рекомендацій використання внутрішньовенних імуноглобулінів для запобігання смерті новонароджених з клінічним чи бактеріологічно підтвердженим сепсисом [3, 22].
Два рандомізовані контрольовані дослідження за участю 140 новонароджених показали поліпшення виживання серед дітей, які мали бактеріологічно підтверджений сепсис і отримали пентоксифілін. Але необхідні додаткові великомасштабні дослідження, щоб підтверддити цю потенційну вигоду [3, 23].
Стратегії запобігання нозокоміальним інфекціям
В якості стратегій профілактики нозокоміальних інфекцій у новонароджених вказують: використання пробіотиків (доведена ефективність), лактоферину (попередні дані дозволяють припустити, що бичачий лактоферрин у поєднанні з пробіотиками може зменшити частоту ПНС), антистафілококові моноклональні антитіла (не доведена ефективність) [3]. Dermyshi E. та співавт. (2017) опублікували результати досліджень новонароджених дітей (4042 дитини отримували пробіотики і 3945 – група контролю), згідно яких частота пізнього неонатального сепсису при призначенні пробіотиків знижувалась на 12% (відносний ризик [ВР] 0,88, 95% ДІ 0.80–0.97, р=0,01) [24].
Стратегії запобігання нозокоміальним інфекціям включають покращення гігієни рук персоналу, оптимізацію штату та екологічного дизайну неонатальних відділень, ранній початок годування грудним молоком, ретельний догляд за шкірою, обмежене використання інвазивних пристроїв, уніфіковані практики (стандартизація процесів) використання внутрішносудинних катетерів [3, 25, 26].
Практика використання антимікробних препаратів в неонатальних відділеннях впливає на типи мікроорганізмів, відповідальних за неонатальний сепсис, та їх резистентність. Тож, стратегії запобігання нозокоміальним інфекціям потребують оптимізації інфекційного контролю відділень та заходів запобігання формуванню резистентності мікроорганізмів (наприклад, моніторингу тривалості використання антибіотиків) [3].
Довгострокові ризики неонатального сепсису
Діти, які що вижили після неонатального сепсису, мають ризик порушення неврологічного розвитку. Доведено, що постнатальні інфекції обумовлюють ушкодження білої речовини мозку. У 13% немовлят з ГВ <34 тижнів, які мали епізод сепсису, виявляли такі ушкодження (в порівнянні з 4,7% (відносний ризик [ВР] – 3,2; 95% ДІ: 0,8–11,8) тих, які не не мали задокументованого епізоду неонатального сепсису). У 36,4% немовлят, які мали кілька епізодів сепсису, виявляли докази ушкодження білої речовини (в порівнянні з 5% (відносний ризик [ВР] – 10,9; 95% ДІ: 2,5–47,6) немовлят, які мали 1 епізод сепсису або не мали його). Доведено, що сепсис підвищує ризик розвитку церебрального паралічу (відносний ризик [ВР] – 3,23 [95% ДІ: 1,23–8,48], р=0,017) [3, 27–30].
Для підсумку
Неонатальний сепсис продовжує залишатися важливою причиною захворюваності та смертності новонароджених у всьому світі. Причинами вважають відсутність адекватних профілактичних та терапевтичних стратегій в умовах країн з низьким рівнем доходів та збільшення виживання глибоко недоношених новонароджених і їх тривале перебування в неонатальних відділеннях в країнах з високим рівнем доходів [2].
Повний перелік літератури знаходиться у редакції.


коментарів