Емболія амніотичною рідиною (ЕАР) (О88.1. в міжнародній класифікації хвороб Х перегляду) – критичний стан, пов'язаний з вагітністю та пологами, який виникає у разі проникнення елементів навколоплодових вод у кровоплин матері та супроводжується розвитком гострої серцево-легеневої недостатності або зупинкою кровообігу
На сьогодні будь-який випадок кардіо-пульмонального шоку, або як його називають, материнського колапсу у вагітної або породіллі розглядається з точки зору ЕАР та потребує диференційної діагностики.
В США та Великобританії діагноз ЕАР встановлюють в разі виникнення гострої гіпотензії або зупинки серця, гострої гіпоксії, коагулопатії або профузної кровотечі під час пологів або кесаревого розтину, ділятації та евакуації вмісту матки або в межах 30 хв. після розродження, або при загибелі жінки – у разі постмортального виявлення фетальних клітин або волосся плода у легенях матері.
Вперше фатальне ускладнення вагітності та пологів було описане 1926 року Ricardo Meyer, а вже 1941 року Steiner et Laushbaugh виявили скупчення фібрину в легенях жінки, що раптово померла в пологах, та патогенетично пов'язали це явище з розвитком колапсу [1]. Вони назвали це синдромом негайного пологового шоку.
Офіційна статистика щодо частоти цього ускладнення коливається в межах 1 випадок на 8–30 тисяч пологів. Fong A. et al. (2015) зазначають, що частота ЕАР мало відрізняється у різних країнах, при цьому істинна поширеність патології невідома через різні критерії діагнозу. За одними даними, расові та етнічні відмінності в частоті амніотичної емболії відсутні, дослідження, проведені у строкатій за цим критерієм Каліфорнії, виявили зростання ризику патології у темношкірих жінок [2].
Так само суперечливими є дані щодо віку. Національний реєстр випадків ЕАР США наголошує на однаковій частоті цього ускладнення в різному віці. A. Fong et al. (2014) виявили зростання ризику фатальної патології після 39 років, а P. Stein et al. (2009) – після 30 років.
Материнська смертність при ЕАР сягає 80%, щоправда у розвинених країнах світу спостерігають її зниження протягом останніх 20 років. Це можна пояснити збільшенням можливостей надання екстреної допомоги, більш ранньою констатацією діагнозу та реєстрацією нефатальних випадків. З метою дослідження частоти ЕАР та її наслідків Clarke S. в США 1995 року та Tuffnelle D. в Сполученому королівстві 2000 року було створено Національні реєстри цієї патології.
За даними Національного реєстру США, 61% роділь, у яких в пологах розвинулось це ускладнення, помирають, половина із них помирає протягом першої години від його початку. 85% тих пацієнток, що вижили, мають неврологічні розлади. За цим же джерелом, ЕАР є причиною 10% всіх материнських смертей в США. В цілому світі цей показник складає 5–10% [5]. U. Gilbert et al. (1999) доповіли про популяційне дослідження, що його проводили протягом 2 років в Каліфорнії, США, яке охопило понад 1 млн пологів. У 53 роділь розвинулась клінічна картина ЕАР, 14 із них померло (26%), решта 39 пережили тяжку коагулопатію. У Сполученому Королівстві Національний реєстр випадків ЕАР станом на 2015 рік засвідчує 37% материнської смертності, а також тяжкі неврологічні розлади, які розвиваються у 7% жінок, що пережили це ускладнення [6].
ЕАР в усьому світі є однією з провідних причин материнської смертності. В Україні щороку не менше 12–14% всіх пов'язаних з вагітністю та пологами смертей є спричиненими ЕАР [11). В Австралії, за даними N. McDonnal, 14% всіх випадків материнської смертності асоційовані саме з ЕАР [12].
Важливим аспектом є питання неонатальних наслідків ЕАР. Реєстр США повідомляє про 79% випадків виживання новонароджених, реєстр Сполученого Королівства – про 78%. В цілому по світу рівень виживання новонароджених від пологів, що ускладнився ЕАР, складає 70%. Неврологічний розвиток дітей залежить від часу, що минув від перших клінічних проявів захворювання до розродження. Реєстр США свідчить, що не менше 50% таких дітей мають неврологічні розлади, що впливають на їх розвиток, в Сполученому Королівстві – 29%.
Невідомим є питання ризику повторення ЕАР. Описані випадки неускладненого перебігу вагітності та пологів у жінок, що вижили.
- Benson 1993 року так сформулював ставлення до ЕАР. «Розвиток цієї патології є настільки непередбачуваним, наскільки непередбачуваним є її прогноз».
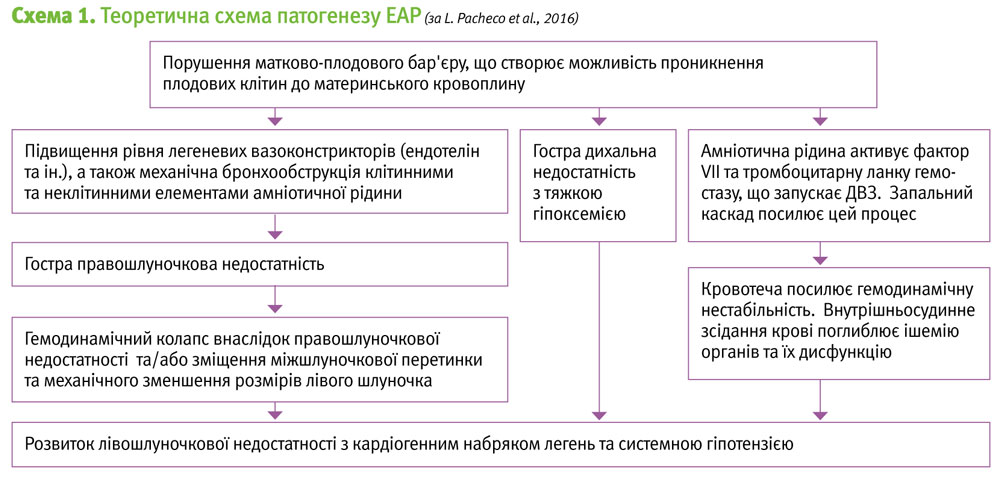
Патогенез ЕАР не є остаточно вивченим. Найбільш поширена концепція розглядає весь каскад фатальних для життя жінки змін як наслідок потрапляння амніотичної рідини та разом з нею клітин плода до материнського кровоплину та розвиток анафілактичної реакцїі.Саме про анафілактичний характер реакції свідчить той факт, що 41% всіх жінок, що загинули внаслідок ЕАР, мали в анамнезі алергічні реакції [11]. Досі розглядають 2 альтернативні шляхи активації патологічної реакції – дегрануляція тучних клітин з викидом високих концентрацій гістаміну та трипсину, а також – запуск системи комплементу. Поодинокі спостереження, у яких одночасно з наданням невідкладної допомоги пацієнтці було визначено концентрації вказаних речовин в сироватці, не дають підстав ні визначити один із патогенетичних механізмів провідним, ні визнати їх паралельними.
Пусковий механізм – потрапляння амніотичної рідини до материнського кровоплину – може відбутись під час пологів (70%), кесарського розтину (19%) та після вагінальних пологів (11%) (Rudra et al., 2009). Описані казуїстичні випадки розвитку ЕАР під час ручного відділення плаценти, амніоцентезу, виконуваного з діагностичною метою, внаслідок абдомінальної травми та навіть при знятті циркулярного шва з шийки матки. Традиційно важають, що це сприяє розвитку ускладнення збільшення внутрішньоматкового тиску відносно системного артеріального тиску. Причинами можуть бути швидкі пологи, неконтрольована індукція пологів, великий плід та багатоплодовість, зниження системного артеріального тиску. Крім того, серед чинників ризику АЕР – врощення плаценти, передчасне відшарування нормально розташованої плаценти (за даними реєстру США, виявлено у 13% всіх випадків ЕАР), ручне відділення плаценти, оперативні пологи, кесарський розтин. У випадку останнього клінічні прояви розвиваються через кілька хвилин після народження дитини. 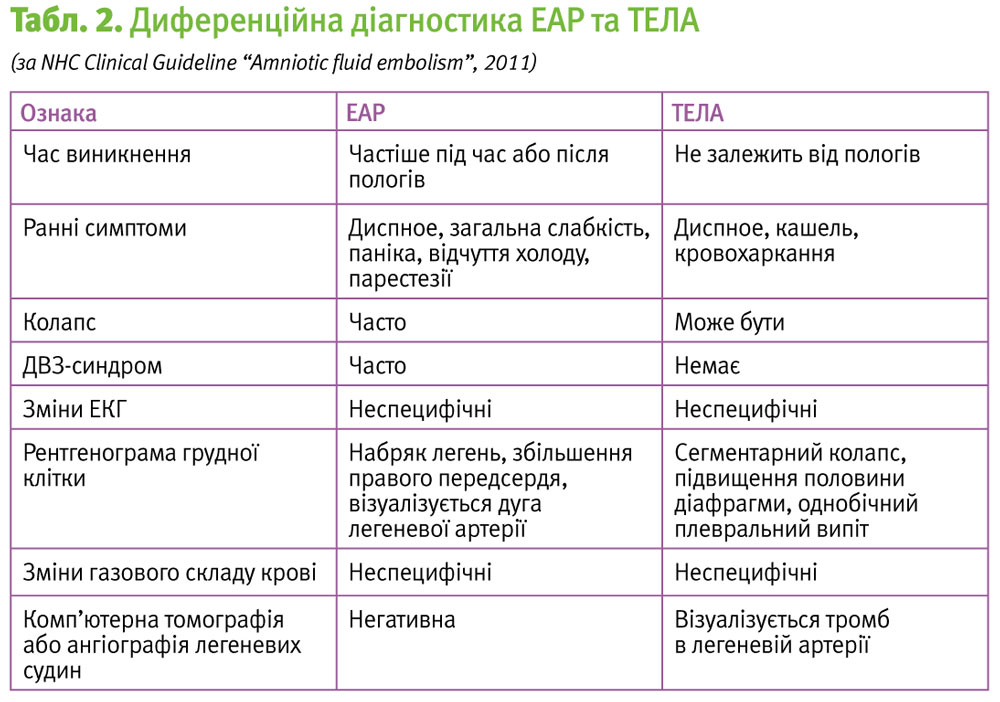
Вважається, що проникнення амніотичної рідини до материнського кровоплину можливе лише після розриву плодових оболонок, проте, за даними США та Сполученого Королівства, у 22% пацієнток із ЕАР плодові мембрани були цілими. 2\3 випадків розриву плодових оболонок були ятрогенними, 1/3 – спонтанними.
Безпосереднім чинником, що провокує транзиторний легеневий вазоспазм, є проникнення амніотичної рідини з елементами плодових клітин, запуск ними арахідонового каскаду. Внаслідок цього розвивається легенева гіпертензія, бронхоспазм, тяжка гіпоксія. Продромальними симптомами є озноб, тремор, відчуття неспокою, тобто дуже неспецифічні симптоми, особливо для післяпологового періоду. Остаточно невідомо, який саме компонент плодових клітин викликає вазоспазм, невідома також роль в цьому процесі материнських біологічно активних речовин.
Саме значення материнських цитокінів та їх спотвореного синтезу було предметом більшості присвячених темі публікацій 90-их років минулого сторіччя. Численні експерименти продемонстрували, що нормальні компоненти навколоплодових вод самостійно не можуть спричинити таку генералізовану реакцію. Clarke S. (1990) передбачив роль меконію, що міститься в амніотичній рідині, у розвитку раптового вазоспазму. Цей транзиторний вазоспазм неможливо зареєструвати, адже абсолютна більшість роділь не має тяжкої серцевої патології, що вимагала би постійного кардіопульмонального моніторингу в пологах.
Внаслідок масивного підвищення опору в малому колі кровообігу розвивається гостра правошлуночкова недостатність, що клінічно проявляється кашлем, ознобом, відчуттям страху. Ця стадія триває хвилини, що значно обмежує можливості діагностики. Наступна лівошлуночкова недостатність з набряком легень проявляється респіраторним дистресом та кардіоваскулярним колапсом. Міокардіальна дисфункція є результатом підвищеного навантаження, гіпоксемії та, можливо – токсичної дії на міокард компонентів амніотичної рідини. У пацієнток, що переживають стадію кардіопульмонального шоку, розвивається гострий ДВЗ-синдром з атонією матки. Причинами розвитку коагулопатії є велика кількість активованих чинників гемостазу ІІ, VII та Х, що містяться в амніотичній рідині, а також її здатність активувати ендогенних ІІ фактор та агрегацію тромбоцитів (Lockwood G. et al., 1991).
Нервова система не може не зазнати впливу респіраторної та гемодинамічної катастрофи, тож навіть на тлі лікування коагулопатії розвиваються судоми та кома.
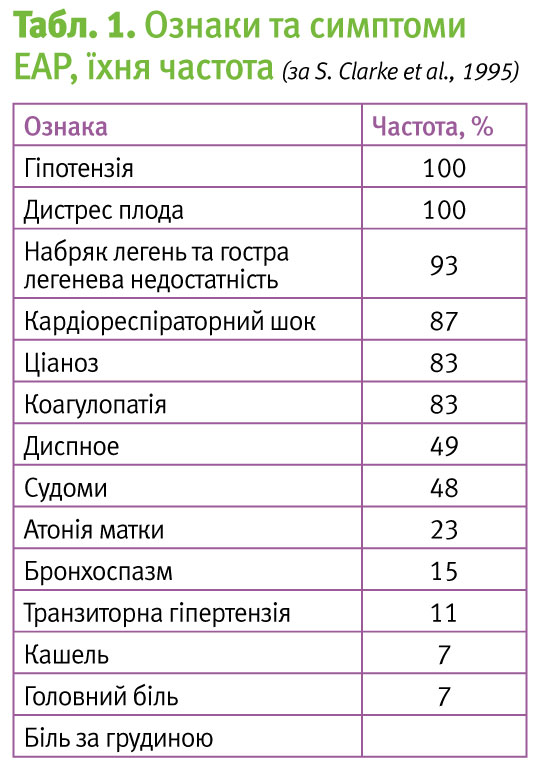
Серед діагностичних критеріїв ЕАР провідне значення мають клінічні, діагноз встановлюється на підставі виключення всіх інших станів, що супроводжуються серцево-легеневою недостатністю. Гіпотензія та дистрес плода – два симптоми, які супроводжують кожний випадок ЕАР.
Зміни електрокардіограми є неспецифічними – тахікардія, гіпертрофія правого шлуночка з підвищеним систолічним його навантаженням (косо зміщена депресія сегменту S-T та негативний зубець Т). Пульсоксиметрія зареєструє катастрофічне зниження сатурації в момент розвитку кардіопульмонального шоку. Виконане рентгенологічне дослідження виявить збільшення правих відділів серця, розширення проксимальної частини легеневої артерії та набряк легень.
Біохімічна коагулограма буде демонструвати тяжку коагулопатію – зменшення числа тромбоцитів, зниження концентрації фібриногену до афібриногенемії, подовження тромбопластинового часу, появу великої кількості продуктів деградації фібрину.
Історично вважають, що патогномонічним симптомом АЕР є виявлення лусок шкіри плода в крові з правого шлуночка або з легеневої артерії. Цей симптом необхідний для підтвердження діагнозу. У разі прижиттєвої діагностики для цього використовують зразок крові, отриманий шляхом катетеризації правого шлуночка. Для точного підтвердження необхідно, щоб таких лусок було багато в зразку, частина із них – оточена нейтрофілами, а також присутні інші елементи навколоплодових вод. 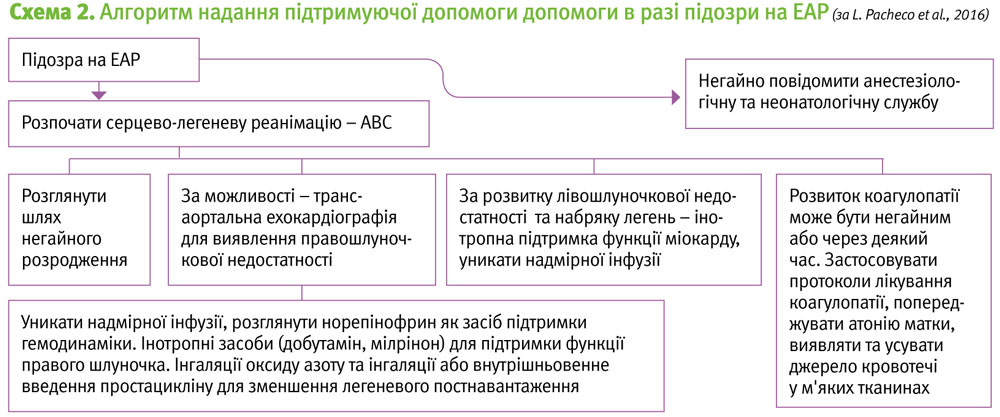
Варто відмітити Sialyl-тест, який становить собою моноклональне імунологічне виявлення антигену – специфічного для респіраторного та гастроінтестинального тракту плода муцину-TKH2. Його частка в меконіальних водах сягає 10%, проте доступний до визначення вміст присутній і в прозорій амніотичній рідині (Oi H. et al., 1993). Так само можливим є визначення в системному кровоплині сполуки цинк-корпопорфірин, що є постійним компонентом меконію. Незважаючи на те, що з часу розробки цих лабораторних маркерів ЕАР минуло вже понад 20 років, широкого поширення в практичному акушерстві вони не здобули.
Clark S. et al. 1995 року, ретельно вивчивши патогенез ЕАР, запропонували концепцію, згідно з якою процес є ближчим до анафілаксії, ніж власне до емболії, та відповідно назву – анафілактоїдний синдром вагітності. Саме в рамках цієї концепції підкреслено, що елементи плодової тканини не є універсальною знахідкою при аутопсії жінок, що мали клінічну картину ЕАР, їх виявляють у 70% випадків посмертного дослідження та в 50% – у разі прижиттєвого дослідження крові із легеневої артерії. Водночас при проведенні популяційних досліджень елементи клітин плодового походження було виявлено в крові породіль, що не мали згаданої клінічної картини. 2002 року Hankins et al. в експерименті на тваринах досліджували виявлення плодових елементів в легенях після ін'єкції амніотичної рідини. З 7 випадків введення меконіальних вод їх компоненти було виявлено у 7 зразках, для прозорих вод – лише у 2 із 8.
Найчастіше диференційний діагноз ЕАР проводять із тромбоемболією легеневої артерії (ТЕЛА). Відрізняє останню біль в грудній клітині, а також час виникнення – переважно у пізньому післяпологовому періоді.

Кардіопульмональний шок також може бути проявом повітряної емболії. Крім болю в грудній клітині, цей стан має специфічну аускультативну ознаку – шум «водяного колеса» в проекції перикарду. Екламптичні судоми та наступна за ними кома є більш поширеним акушерським ускладненням, ніж ЕАР, їх відрізняють супутні гіпертензія, набряки та протеїнурія.
Судоми можуть бути також наслідком токсичної реакції на місцеві анестетики, від ЕАР їх відрізняє чіткий зв'язок із проведенням знеболення. Гостра лівошлуночкова недостатність може розвинутись у вагітної з вродженими або набутими вадами серця, ускладненими серцевою дисфункцією, диференційним критерієм тут виступають саме дані анамнезу. Ціаноз, тахікардія та набряк легень властиві аспірації шлункового вмісту, проте це ускладнення розвивається у пацієнтки в несвідомому стані або в загальному наркозі. Нарешті, кровотечі під час пологів та в післяпологовому періоді також варто диференціювати з ЕАР. Принциповими відмінностями тут є відсутність проявів кардіопульмонального шоку до початку кровотечі. Для виключення всіх інших причин кардіопульмонального шоку необхідно розглянути можливість септичного шоку, анафілаксї, розриву аневризми аорти, інфаркт міокарду.
Таким чином, підставою для діагнозу ЕАР є клінічна картина та виключення всіх інших причин гострої серцево-дихальної недостатності.
Лікування ЕАР наразі носить синдромальний характер, медичну допомогу необхідно почати надавати якомога швидше, вона включає корекцію кардіопульмонального колапсу та коагуляційних розладів.
Ключовими точками успішного надання допомоги при ЕАР є вчасна діагностика, негайна реанімація та розродження. Для визначення глибини гемодинамічних порушень необхідно розпочати моніторинг пульсу та артеріального тиску.
Оптимальним є встановлення центрального венозного катетера, однак здійснювати це слід одночасно із виконанням всіх інших заходів допомоги.
Компоненти висококваліфікованої кардіо-пульмональної реанімації під час вагітності (за L. Pacheco et al., 2016)
- Зовнішній масаж серця/хв.
- Використовувати натискання на грудину з глибиною не менше 2 см.
- Переконатись у поверненні грудини у вихідне положення перед наступним натисканням.
- Мінімізувати перерви між натисканнями.
- Уникати втрати часу на вимірювання пульсу (не більше 5–10 с).
- Утриматись від натискання на грудину зразу після дефібриляції.
- Кожні 2 хв. змінювати виконавця реанімації, щоб попередити втому.
- Змістити матку вліво під час виконання реанімаційних заходів.
Питання розродження визначається гестаційним терміном, а саме – більше 23 тижнів. Це залежить не лише від терміну життєздатності плода, але і від необхідності усунення перетискання нижньої порожнистої вени для покращення гемоциркуляції плода.
Спосіб розродження залежить від акушерської ситуації; якщо оперативні вагінальні пологи неможливі, вдаються до кесарського розтину.
Оптимальним часовим проміжком для виконання такого втручання є 4 хвилини від початку кардіопульмонального шоку. У разі неефективності кардіо-пульмональної реанімації дитина має бути вилучена не пізніше 5 хв. від початку зупинки кровообігу. Для досягнення цього абдомінальне розродження має бути виконане на місці виникненні колапсу! Важливо розпочинати приготування для цього в момент виникнення ознак колапсу [14]. Критичною має бути наявність скальпеля у наборі для надання реанімаційної допомоги.
Оксигенотерапія покликана попередити гіпоксію внаслідок гіпоперфузії тканин, в першу чергу – головного мозку, тобто знизити ризик неврологічних ускладнень. З цією метою можна застосовувати маску, ендотрахеальну трубку, а також вентиляцію з позитивним тиском на видиху, вибір залежить від можливості якомога швидкого початку оксигенації.
Важливим компонентом надання допомоги при ЕАР є інфузійна терапія. Для запобігання посилення перевантаження лівих відділів серця інфузійну терапію можна проводити під контролем трансаортальної або трансезофагальної ехокардіографії, або застосовуючи катетеризацію легеневої артерії.
Для корекції рефрактерної гіпотензії препаратами першої лінії є добутамін та норадреналін через їх позитивний ізотропний ефект та дію на адренозалежні механізми регуляції судинного тонусу.
ДВЗ-синдром розвивається в більшості випадків ЕАР, відмінності полягають у часі розвитку цього ускладнення – від негайного до відтермінованого на кілька годин. У разі масивної кровотечі іншого походження світові рекомендації радять відкласти переливання компонентів крові до отримання результатів лабораторних тестів. Натомість рекомендації SMFM (2016) у разі підозри на ЕАР зазначають доцільність раннього початку так званої «агресивного відновлення ОЦК», що полягає у переливанні еритроцитарної маси, свіжозамороженої плазми та тромбоцитарної маси у співвідношенні 1:1:1. Доцільність такого підходу, який ще має назву «гемостазіологічної реанімації», автори керівництва обґрунтовують блискавичністю розладів системи зсідання, властивих ЕАР, вони мають досить високий рівень доказовості С1.
В кількох описах клінічних випадків ЕАР описано застосування рекомбінантного активованого фактору VII. Незначна кількість таких спостережень не дозволяє говорити про ефективність, проте є дані про зростання ризику тромбозів та мультиорганної недостатності при застосуванні вказаного фактору у пацієнтів із коагулопатією.
Не слід забувати про порушення скоротливої активності матки, для попередження гіпотонічної післяпологової кровотечі в рамках лікування ЕАР застосовують утеротоніки.
Основними способами попередження ЕАР є дотримання показань до розтину плодових оболонок та техніки цієї маніпуляції, уникнення розрізу плаценти під час кесаревого розтину, а також чітке визначення необхідності та дозування посилення пологової діяльності окситоцином.
На завершення наводимо заключні рекомендації клінічного керівництва «Емболія амніотичною рідиною» SMF (Товариства материнсько-плодової медицини) 2016 року.
- Рекомендується (суворі рекомендації, 1С) передбачати ЕАР у всіх випадках кардіопульмонального колапсу у жінок в пологах або ранньому післяпологовому періоді.
- Не рекомендується (1С) застосовувати специфічні діагностичні тести для підтвердження діагнозу ЕАР, орієнтуючись на клінічну картину.
- Рекомендується (1С) негайний початок висококваліфікованої кардіо-пульмональної реанімації у пацієнток з клінічною картиною ЕАР.
- Рекомендується (власний досвід) включення мультидисциплінарної команди за участю анестезіолога та спеціаліста з критичних станів, неонатолога у надання медичної допомоги пацієнткам з підозрою на ЕАР.
- Рекомендується (рекомендації слабкої сили, 2С) негайне розродження пацієнтки з ЕАР, якщо гестаційний термін більше 23 тижнів.
- Рекомендується (1С) проведення адекватної оксигенотерапії та, якщо виникають показання з боку гемодинаміки, застосування вазопресорів та засобів інотропної дії, уникання надмірного обсягу інфузії.
- Рекомендується (1С) раннє дослідження порушень системи зсідання крові, а також ранній початок «агресивної» компенсації її розладів.
Перелік літератури знаходиться у редакції.


коментариев