Диабетическая нефропатия (ДН) – это поражение сосудов почек, возникающее при сахарном диабете (СД), которое сопровождается их замещением плотной соединительной тканью (склероз) и формированием почечной недостаточности.
В последние десятилетия диабетическая нефропатия вышла на первое место по частоте развития терминальной хронической почечной недостаточности, на втором месте – артериальная гипертензия и хронический гломерулонефрит [11].
Являясь специфическим поражением сосудов почек при сахарном диабете, диабетическая нефропатия сопровождается формированием очагового или диффузного гломерулосклероза, терминальная стадия которого характеризуется развитием хронической почечной недостаточности (ХПН).
Диабетическая нефропатия включает диабетический гломерулосклероз, инфекции мочевых путей, а также папиллярный некроз.
В последние годы для характеристики хронического поражения почек у взрослых, в том числе при СД, применяется термин «хроническая болезнь почек» (ХБП). Однако в педиатрической практике данный термин до сих пор не нашел широкого использования. В МКБ-10 диабетическая нефропатия кодируется как Е 10.2 или Е 11.2.
В ряде экономически развитых и развивающихся стран диабетическая нефропатия занимает первое место по потребности в гемодиализе или трансплантации почек, вытеснив на второе и третье места первично-почечные заболевания любой этиологии. Указанная тенденция побуждает исследователей продолжить изучение особенностей возникновения и развития диабетической нефропатии, в том числе и в детском возрасте. [3].
Современные сведения, касающиеся ДН, показывают четкую зависимость возраста дебюта сахарного диабета и частоты развития терминальной стадии почечной недостаточности. При этом поражение почек при так называемом СД молодых является основной причиной инвалидизации и смертности пациентов.
Наряду с возрастом, в котором дебютировал СД, частота ДН также зависит и от длительности заболевания диабетом.
По данным современных исследований, максимальная частота ДН (около 45%) при СД 1-го типа встречается у пациентов в возрасте 11–20 лет. При дебюте СД после 20 лет частота ДН снижается до 30–35%, а при развитии СД в возрасте старше 35 лет частота ДН составляет всего несколько процентов [7].
Вышеизложенное определяет чрезвычайную важность своевременной диагностики, лечения и профилактики диабетической нефропатии у детей и подростков. В ранний период формирования болезни еще возможно предотвратить и (или) отсрочить возникновение и прогрессирование гломерулосклероза путем использования адекватных профилактических и лечебных мероприятий.
По данным Diabetes Control and Complications Trial Research Group (DCCT, 2004) гипергликемия является ведущим патогенетическим механизмом развития ДН. Актуальной и убедительно доказанной является концепция: «без диабета не существует диабетических осложнений», в том числе это касается и диабетической нефропатии [2].
При этом ряд исследователей отмечает, что достаточно часто по мере развития ДН прямая зависимость прогрессирования нефропатии от степени компенсации углеводного обмена исчезает. С течением времени патологический процесс в почках приобретает самостоятельное значение. При этом все большее количество результатов исследований показывает значение дислипидемии в генезе диабетического поражения почек.
Согласно результатам современных исследований, риск развития нефропатии выше у больных с дебютом сахарного диабета в пубертатном возрасте в сравнении с детьми, у которых начало заболевания приходится на возраст до 10 лет [1].
Классификация
Современная классификация ДН утверждена и опубликована в протоколах диагностики и лечения диабетической нефропатии у детей (Приказ № 254 МЗ Украины от 27.04.06 «Про затвердження протоколів надання медичної допомоги дітям за спеціальністю «Дитяча ендокринологія» [4, 13] и предусматривает 5 стадий развития ДН:
I стадия – стадия гиперфункции почек
Первые признаки диабетического поражения почек могут возникать уже в дебюте заболевания. Эта стадия характеризуется увеличением скорости клубочковой фильтрации (СКФ), а также повышением почечного кровотока. Указанные факторы приводят к развитию гипертрофии почек. В этой стадии отмечается нормоальбуминурия (альбумин в моче – менее 30 мг/сутки).
II стадия – стадия начальных структурных изменений в почках
Эта стадия развивается через 2–5 лет от начала сахарного диабета. Отмечается утолщение базальных мембран капилляров клубочков, а также расширение мезангиума. Сохраняется высокая скорость клубочковой фильтрации. В этой стадии сохраняется нормоальбуминурия (<30 мг/сутки).
Первые 2 стадии являются доклиническими.
ІІІ стадия – начинающаяся диабетическая нефропатия
Эта стадия является клинической, то есть впервые устанавливается диагноз ДН. Характеризуется повышением уровня микроальбуминурии (от 30 до 300 мг/сутки), высокой или нормальной скоростью клубочковой фильтрации, а также нестойким повышением артериального давления.
IV стадия – стадия выраженной диабетической нефропатии
Данная стадия обычно диагностируется через 10–25 лет от дебюта сахарного диабета. По мере прогрессирования ДН формируется склероз клубочков. В этой стадии их склероз достигает 50–75%. Развивается высокая протеинурия (более 500 мг/сутки). Характерна стабильная артериальная гипертензия.
V стадия – стадия уремии
Возникает через 15–20 лет от начала сахарного диабета или через 5–7 лет от появления протеинурии. Эта стадия характеризуется тотальным диффузным или очаговым гломерулосклерозом. Характерно снижение СКФ менее 10 мл/в минуту, развивается стойкая артериальная гипертензия, а также нарушение азотвыделительной функции почек (повышение креатинина, мочевины). У ребенка часто развиваются симптомы интоксикации.
План обследования
1) Исследование осадка мочи (эритроциты, лейкоциты).
2) Определение протеинурии (в общем анализе мочи и (или) в суточной моче).
3) Исследование креатинина и мочевины в сыворотке крови.
4) Определение СКФ.
5) Исследование микроальбуминурии (МАУ) трехкратно.
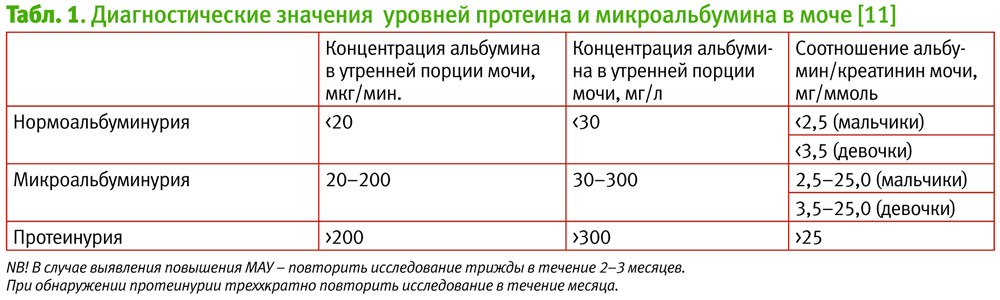
Диагностика
Наиболее ранним методом диагностики ДН является микроальбуминурия (МАУ).
Показания к проведению скрининга МАУ:
1) при выявлении СД 1 типа в раннем детском возрасте – ежегодно с 10–12 лет;
2) при дебюте СД 1 типа в период пубертата – 1 раз в год с момента диагностики заболевания;
3) старт СД 1 типа после пубертата – 1 раз в год через 5 лет от момента диагностики заболевания;
4) у больных с СД 2 типа: 1 раз в год с момента диагностики СД 2 типа.
Наличие повышенной МАУ свидетельствует о ІІІ стадии ДН, которая является единственной обратимой стадией ДН, при условии вовремя назначеной нефропротекторной терапии.
Диагностическое значение имеет только постоянная микроальбуминурия, то есть выявленная трижды на протяжении 2–3 месяцев.
Другие причины повышения МАУ:
1) у подростков в период интенсивного роста;
2) при физических нагрузках;
3) инфекции мочевых путей;
4) фебрильная лихорадка;
5) пороки сердца;
6) декомпенсация СД.
Диагностические значения уровней протеинурии и МАУ представлены в табл. 1.
Ранним маркером поражения почек является внутриклубочковая гипертензия, являющаяся основной причиной развития и прогрессирования ДН. Она диагностируется на основании повышения скорости клубочковой фильтрации (СКФ) болеее 140 мл/мин. Для определения СКФ можно использовать пробу Реберга, представляющую собой определение клиренса эндогенного креатинина за сутки (норма — 80–120 мл/мин.).
Проба Реберга может быть неинформативной при употреблении пищевых продуктов с высоким содержанием белка, в дебюте сахарного диабета и при его декомпенсации [14].
Следует подчеркнуть, что появление периферических отеков, эпизодических или постоянных, является клиническим симптомом, как правило, четвертой стадии диабетической нефропатии у детей и подростков. При этом отеки сопровождаются появленим протеинурии [6, 9].
Алгоритм лечения
Лечение ДН у детей и подростков проводится согласно протоколам диагностики и лечения эндокринных заболеваний у детей и подростков (Приказ №254 МЗ Украины от 27.04.06 г.). В то же время, терапия ДН может осуществляться с использованием современных европейских и американских руководств [5, 8].
Важнейшей задачей терапии ДН является предотвращение поражения почек и (или) предотвращение прогрессирования диабетической нефропатии.
Модификация образа жизни для снижения артериального давления (АД) и риска кардиоваскулярной патологии должна рекомендоваться всем детям и подросткам с ДН.
Назначая лечение в связи с ДН, следует помнить, что именно комплексный терапевтический подход позволяет остановить/затормозить прогрессирование потери функции почек.
Принимая во внимание, что сахарный диабет является самой частой причиной ХПН, антигипертензивные средства с диабетогенными свойствами не могут использоваться как препараты первого ряда при выборе терапии артериальной гипертензии у пациентов с диабетической нефропатией.
Учитывая современные данные, с целью нефропротекции уже на этапе появления инсулинорезистентности следует отдавать предпочтение ингибиторам ангиотензинпревращающего фермента (ИАПФ) или симпатолитикам. При этом важной является рекомендация не использовать в стартовой терапии гипертензии у пациентов с ДН b-блокаторы и тиазидные диуретики [10, 12].
При нормальной экскреции альбумина с мочой у детей с СД с целью нефропротекции основополагающей является рекомендация обеспечения тщательной коррекции углеводного обмена с обеспечением следующих (положений) показателей:
1) целевой уровень HbA1c не выше 7–7,5%;
2) артериальное давление не выше 110/70 мм рт. ст.;
3) холестерин ниже 4,5 ммоль/л.;
4) триглицериды ниже 1,7 ммоль/л.;
В случае обнаружения микроальбуминурии (3 стадия ДН) у детей и подростков с СД необходимо обеспечить следующие мероприятия:
1) Соблюдение диеты с ограничением животного белка (до 0,9–1,2 г/кг в сутки) и соли.
2) Коррекция углеводного обмена (HbA1c менее 7,0 – 7,5%).
3) Коррекция АД (при повышенном – препараты в средне-терапевтических дозах, при нормальном – в минимальных дозах)
- Ингибиторы АПФ продленного действия 1 раз в день вечером (в 17 часов) имеют нефропротекторное действие и на стадии микроальбуминурии позволяют предотвратить протеинурию почти у 55% больных СД.
- Избегать назначения тиазидовых диуретиков и неселективных b-адреноблокаторов, так как указанные препараты повышают инсулинорезистентность и уровни триглицеридов. В то же время большинство b-блокаторов снижают сердечный выброс, ухудшая тем самым почечную гемодинамику.
- Наряду с ингибиторами АПФ, нефропротективное действие имеют и селективные агонисты имидазолиновых рецепторов (моксонидин, физиотенз) – препараты центрального действия. Важно, что эти препараты хорошо переносятся, в том числе детьми, при продолжительном приеме.
4) Коррекция внутрипочечной гемодинамики
- ИАПФ, даже при нормальном АД – в небольших дозах;
- агонисты имидазолиновых рецепторов (моксонидин, физиотенз).
5) Ацетилсалициловая кислота ежедневно, постоянно на ночь: детям старше 12 лет – 325 мг 1 раз в 3 дня или 100 мг.
6) Сулодексид (препарат из группы гликозамингликанов) не действует на свертывающую систему крови, но повышает содержание гепарансульфата в мембранах почечных клубочков, восстанавливает селективную проницаемость почечного фильтра и предотвращает развитие склеротических процессов в почечной ткани. Препарат наиболее эффективен на стадии микроальбуминурии. Назначается в/м 1 раз на протяжении 5 дней, 2 дня перерыва, всего 3 недели; или 10 дней в/м, потом 2 недели в капсулах; или: по 2 капсулы 2 р. (под контролем уровня альбуминурии), через 1 мес. дозу можно увеличить до 3 капсул 2 раза.
Патогенетические механизмы развития ДН и тактика ведения детей и подростков с ДН указаны в табл. 2.
Особенности антигипертензивной терапии при ДН у детей и подростков
Многочисленные исследования, в том числе ALLHAT (Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial) (2005), посвященные применению тиазидоподобного диуретика в качестве антигипертензивного препарата, позволили установить повышение уровня глюкозы натощак на 0,17 ммоль/л. В то же время, при приеме амлодипина отмечалось повышение гликемии на 0,03 ммоль/л, по сравнению с лечившимися лизиноприлом пациентами, у которых уровень сахара крови снизился на 0,08 ммоль/л. В последующем были получены убедительные данные об уменьшении риска развития СД при назначении ИАПФ, БРА ІІ, а карведилол и небиволол признаны безопасными препаратами в лечении метаболического синдрома (МС) [10, 12].
Исследованиями KDOQI (2004) определены основные положения относительно лечения гипертензии у больных с ХБП с акцентом на применении ИАПФ и БРА ІІ. Эти рекомендации предложены для пациентов с 1–4-й стадией ХБП, то есть со скоростью клубочковой фильтрации свыше 15 мл/мин. (креатинин крови меньше 0,528 ммоль/л, согласно приказу МЗ Украины №65/462 от 30.09.03 и креатинин крови меньше 0,44 ммоль/л для детей, согласно приказу МЗ Украины №365 от 20.07.05) (рис. 1, Табл. 3).

Уровень протеинурии в сочетании с показателями АД являются критерием оценки эффективности антигипертензивных препаратов.
Необходимо подчеркнуть, что у подростков, как и у взрослых, ингибиторы АПФ или БРА являются препаратами, которым отдается предпочтение в лечении не только диабетической нефропатии, но и недиабетических поражений почек с наличием протеинурии.
Для подростков с ДН целевым уровнем АД должно являться 110/70 мм рт. ст. Подбор дополнительных препаратов, которые уменьшают кардиоваскулярный риск, для достижения целевого давления должен осуществляться согласно JNC-7 и существующим рекомендациям.
Пациенты с ДН относятся к группе высокого риска по частоте возникновения осложнений фармакологической терапии в сравнении с общей популяцией и, соответственно, должны чаще наблюдаться.

Согласно современным рекомендациям, побочные действия при применении препаратов, которые снижают холестерин, могут возникать из-за сниженной функции почек. Также определено, что лечение протеинурии может быть составляющей терапии дислипидемии [1, 3, 8].
К настоящему времени в нефрологии сформулирован ряд принципов, которых придерживаются в лечении взрослых пациентов с ДН:
- Целевое АД при ДН <120/80 мм рт. ст. или САД <98 мм рт. ст. (жесткий контроль — <125/75 мм рт. ст. и САД <92 мм рт. ст.).
- Протеинурия должна быть минимально возможной или отсутствовать. Срок уменьшения протеинурии в два раза не должен, по возможности, превышать 6 месяцев (J. Redon, 2006).
- Достижение целевого уровня АД и ликвидация протеинурии являются независимыми задачами и предполагают использование всех возможных антигипертензивных средств при соблюдении определенной последовательности.
- Препараты выбора (как правило, в комбинации) в этой последовательности: ИАПФ, моксонидин, селективные антагонисты кальция, селективные b-блокаторы. При этом среди кальциевых блокаторов предпочтение отдается дилтиазему (верапамилу), фелодипину, лерканидипину, среди b-блокаторов — карведилолу (блокатор a- и b-рецепторов), бисопрололу, метопролола сукцинату и небивололу.

ИАПФ на сегодня во всех клинических рекомендациях признаны стартовым препаратом в лечении ДН. Не получено убедительных данных о преимуществах БРА или прямых ингибиторов ренина, как и не признана целесообразной практика повсеместного назначения в нефрологии комбинации ИАПФ + БРА. Выбор конкретного ИАПФ определяется доказательной базой относительно снижения кардиоваскулярной смертности, ренопротекторной эффективности и возможности использования препарата в полной дозе согласно имеющейся у пациента СКФ.
Важно подчеркнуть, что различные ИАПФ неодинаково влияют на циркулирующее и тканевое содержание АПФ. Для длительной терапии наибольшее значение имеет органопротекторные свойства препарата. Так, периндоприл имеет преимущества перед нифедипином (30–60 мг), амлодипином (5–10 мг), атенололом (50–100 мг), небивололом (5–10 мг) и телмисартаном (80–160 мг) в развитии эндотелийзависимой вазодилатации. Механизмы действия ИАПФ определяются их активностью в плазме и тканях. Экспериментальным путем доказана более высокая ингибиция АПФ в сердце, легких и почках, свойственная моэксиприлу, в сравнении с квинаприлом и эналаприлом (A. Torsello еt al., 2003). Согласно современным данным, моэксиприл и квинаприл обладают свойством, с одной стороны, снижать активность тканевого АПФ, с другой – повышают уровни простагландинов І2, то есть дополнительно еще и тормозят образование АПФ. Описанный эффект может приводить к нарушению адаптационной функции кардиомиоцитов с последующим развитием гипертрофии желудочков сердца. В связи с вышеизложенным, индивидуальный подбор ИАПФ является важнейшей составляющей лечения пациентов с ДН.
При назначении ИАПФ следует контролировать уровни калия и креатинина сыворотки крови. Дозу ИАПФ необходимо титровать до целевой или максимально переносимой. Чем выше переносимая доза ИАПФ, тем выше антипротеинурический и, вероятно, антисклеротический эффект. Важно заметить, что препараты с почечным путем выведения (периндоприл, лизиноприл, эналаприл) имеют более выраженный антигипертензивный (и, вероятно, антипротеинурический) эффект. В то же время, препараты с печеночным путем выведения (квадроприл, моэксиприл) более безопасны при значительном снижении СКФ.
Другая группа препаратов — БРА ІІ (сартаны) — также позиционируется для лечения ХБП. Данные ряда исследований свидетельствуют об эффективности сартанов в уменьшении левожелудочковой гипертрофии и снижении сердечно-сосудистой смерти, риска развития инфарктов и инсультов. При этом ренопротекторные свойства сартанов более характерны для высоких доз.
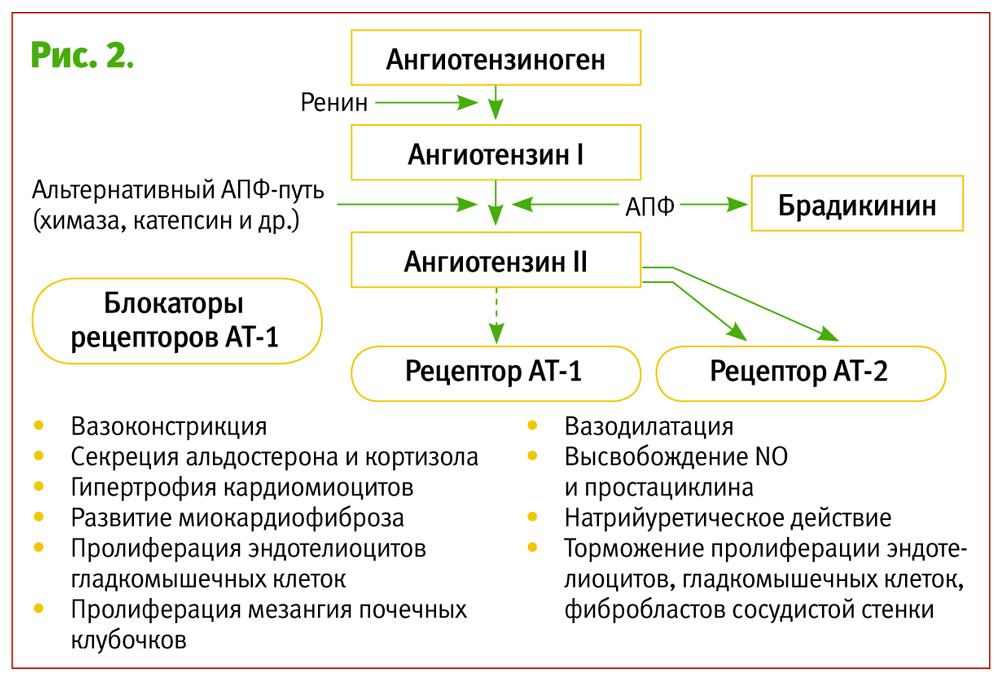
Механизм действия БРА отличается от ИАПФ, количество побочных эффектов у этой группы препаратов не отличается от плацебо (рис. 2). Однако кардиопротекторные свойства БРА уступают таковым ИАПФ, а стимуляция рецепторов 2-го типа не полностью изучена, что следует принимать во внимание в оценке рисков у пациентов с ДН.
Следует подчеркнуть, что эффективность БРА в снижении микроальбуминурии не зависит от полиморфизма ренин-ангиотензинового гена. Как и для ИАПФ, БРА свойственно внутригрупповое разнообразие, в первую очередь связанное с липофильностью/водорастворимостью и степенью выведения почками. По мере прогрессирования ХБП доза сартанов с почечным выведением (кандесартан) и двойным выведением (ирбесартан, валсартан) уменьшается. Только доза телмисартана, на 98% выводящегося печенью, и эпросартана (75%) не корригируется в зависимости от стадии ХБП-ХПН.
Назначая препараты в лечении ХБП, следует помнить, что их взаимодействие может приводить к нежелательным побочным эффектам, например увеличению гиперурикемии и васкулитам (ИАПФ + БРА), а также принимать во внимание плейотропные свойства лекарственных средств, например, антитромбоцитарные эффекты ИАПФ (эналаприл, квадроприл), синергизм в подавлении гиперактивности симпатической системы (теветен + моксонидин или БРА + спиронолактон/эплеренон).
Таким образом, схема лечения ДН при АД более 130/85 мм рт. ст. в настоящее время выглядит таким образом: 1) антигипертензивная, антипролиферативная и антипротеинурическая терапия: ИАПФ (БРА и, возможно, прямые ингибиторы ренина), моксонидин, индапамид или ксипамид (или тиазидный диуретик 12,5–25 мг), или спиронолактон 25 мг (при отсутствии СД), или эплеренон, селективный b-блокатор (небиволол, бисопролол), или карведилол (блокатор a-, b-рецепторов), отдельные антагонисты кальция (фелодипин, лерканидипин); 2) терапия анемии: железосодержащие препараты + эритропоэтинстимулирующий агент; 3) снижение уровня фосфора (при необходимости), кальций-D3, или фосфатбиндер, или цинакальцет, кетостерил, энтеросорбент; 4) антитромбоцитарный препарат (аспирин, клопидогрель, тиклопедин); 5) статины (при выраженной дислипидемии) или современные фенофибраты (при диабетической нефропатии) [16, 17].
При наличии терминальной ХПН, вероятно, целесообразно применение препаратов с преимущественным выведением внепочечным путем, например, схема 3М: моэкс + микардис (теветен) + моксонидин.
Липидоснижающая терапия является составляющей защиты сосудов в коррекции АД и применяется для первичной и вторичной профилактики.
Среди диуретиков предпочтение отдается тиазидоподобным (индапамид, ксипамид) или петлевым (торасемид). Следует помнить, что торасемид имеет лучший в сравнении с фуросемидом профиль по кардиоваскулярным рискам. Однако при терминальной стадии ХПН мочегонный эффект фуросемида более выраженный. Доза индапамида 0,625 или 1,25 мг/сут. для длительного приема, ксипамида — от 10 до 80 мг/сут. (выше при меньшей СКФ!), торасемида — от 5 до 200 мг/сут. (при диабетической болезни почек), фуросемида — от 10 до 500 мг/сутки (при СД). Большие дозы торасемида и фуросемида назначаются по 1–2 дня, затем 1–2 дня перерыв.
Согласно международным руководствам, назначение ИАПФ/БРА не показано при первой стадии ДН. Имеются немногочисленные сведения об использовании олмесартана (или других ИАПФ/БРА) для профилактики перехода первой стадии ДН во вторую при СД 2 типа. ИАПФ/БРА составляют основу ренопротекторной терапии ДН при СД 2 типа. По мере снижения скорости клубочковой фильтрации увеличивается активность симпатической нервной системы, а также утрачивается количество функционирующих нефронов, что определяет необходимость изменения тактики лечения. С целью снижения кардиоваскулярных рисков на фоне нарастания артериальной гипертензии вместо ИАПФ/БРА используют симпатолитики и/или блокаторы кальциевых каналов.
При наличии протеинурии:
- Коррекция углеводного обмена (см выше).
- Низкобелковая диета (животный белок — до 0,8–0,9 г/кг массы тела в сутки, желательна замена животного жира растительным). Разрешается расширение углеводного рациона для покрытия энергозатрат.
- Коррекция АД в постоянном режиме (см выше).
- Препараты выбора – ИАПФ. На этой стадии предупреждают развитие хронической почечной недостаточности (ХПН) у 50–55% больных СД.
- При необходимости комбинации с препаратами других групп: петлевые диуретики (фуросемид, индапамид), блокаторы кальциевых каналов (недигидропиридиновые), препараты центрального действия (моксонидин).
- Коррекция липидного обмена. При повышении холестерина >6,5 ммоль/л и триглицеридов >2,2 ммоль/л – присоединение гиполипидемических средств (преимущественно никотиновой кислоты).
- Сулодексид – внумышечно 1 р./сут. 10 дней, посля чего – по 2–3 капсулы 2 р./сут. в сутки – 14 дней.
- Ибустрин (ингибитор синтеза тромбоксана Н2) – повышает СКФ, снижает суточную протеинурию. 1т х 2 р (400 мг/сутки) – 3 мес.
На стадии ХПН: суточная потребность в инсулине резко снижается.
- Ограничение белка до 0,6 г/кг/сут.
- Для лечения гипертензии – преимущественно применяются препараты с двойным путем элиминации (печень и почки) и непродолжительного действия (с целью предотвращения кумуляции препарата). Назначение ИАПФ на стадии ХПН пролонгирует додиализный период жизни больных СД на 4–5 лет. В случае повышения уровня креатинина более 300 мкмоль/л необходимо применять ИАПФ с особой осторожностью!, рекомендуется комбинированная терапия гипертензии (ИАПФ + петлевые диуретики + антагонисты кальция + препараты центрального действия).
- Лечение почечной анемии (эритропоэтин).
- Коррекция фосфорно-кальциевого обмена.
- Коррекция гиперкалиемии
- Энтеросорбция
- Л-формы аминокислот
- Симптоматическое лечение
- Коррекция кальциево-фосфорного обмена
- При повышении уровня креатинина крови >500 мкмоль/л, снижении СКФ <15 мл/хв. – экстракорпоральные (гемодиализ, перитонеальный диализ) или хирургические методы лечения (трансплантация почек).
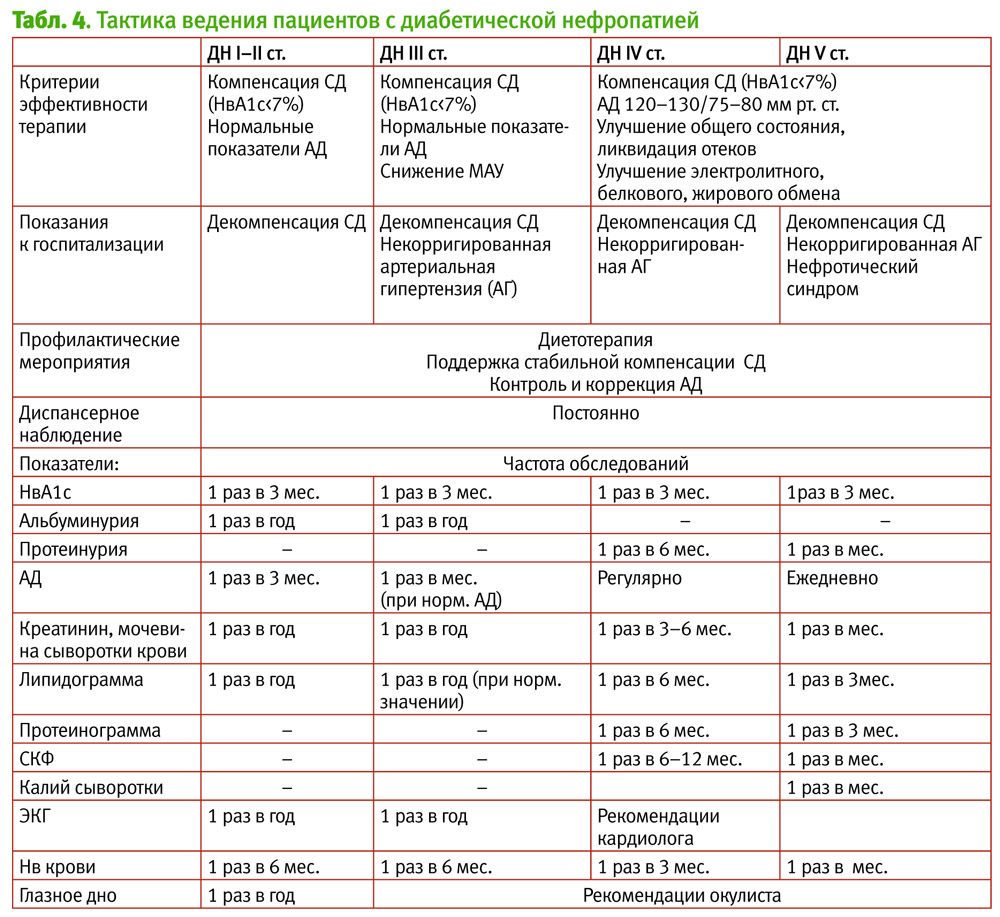
Тактика ведения пациентов с диабетической нефропатией представлена в табл. 4.
В заключении необходимо подчеркнуть, что, несмотря на определенные успехи, достигнутые в диагностике и лечении диабетической нефропатии у детей и подростков, проблема своевременной постановки диагноза и адекватной терапии, а также расширение возможностей профилактики данной патологии, остается чрезвычайно актуальной и значимой.
Полный перечень литературы находится в редакции.


коментариев