 Заболевания щитовидной железы у детей и подростков занимают первое место среди всех эндокринопатий в Украине. Распространенность тиреотоксикоза, по данным МЗ Украины, в 2012 году составила 0,05 на 1000 детей, при этом девочки страдают данной патологией в 10 раз чаще, чем мальчики
Заболевания щитовидной железы у детей и подростков занимают первое место среди всех эндокринопатий в Украине. Распространенность тиреотоксикоза, по данным МЗ Украины, в 2012 году составила 0,05 на 1000 детей, при этом девочки страдают данной патологией в 10 раз чаще, чем мальчики
Несмотря на четко сформулированные клинические признаки синдрома тиреотоксикоза у детей, диагностика его в ряде случаев представляет определенные сложности. Зачастую, наличие у ребенка зоба в сочетании с признаками аутоиммунного поражения щитовидной железы (повышение содержания антител к тиреопероксидазе (АТ-ТПО) в сыворотке крови) ошибочно трактуется врачами как гипертиреоидная стадия аутоиммунного тиреоидита (АИТ) даже при длительной тахикардии, выраженном экзофтальме, глазных симптомах, стойком повышении тиреоидных гормонов и значительном снижении ТТГ (тиреотропный гормон).
В этой связи представляется актуальным описание дифференциально-диагностических критериев тиреотоксикоза у детей.
Синдром тиреотоксикоза – это патологический синдром, который характеризуется определенными клиническими проявлениями в результате повышения содержания тиреоидных гормонов: Т4св. (свободный тироксин, тетрайодтиронин) и Т3св. (свободный трийодтиронин) в крови и тканях. В то же время, под гипертиреозом понимают увеличение содержания тиреоидных гормонов в крови.
Тиреотоксикоз у детей в более чем 90% случаев обусловлен диффузным токсическим зобом. Среди других причин тиреотоксикоза следует иметь в виду гипертиреоидную фазу аутоиммунного тиреоидита, токсическую аденому щитовидной железы, многоузловой токсический зоб, ТТГ-секретирующую аденому гипофиза, йод-индуцированный тиреотоксикоз, транзиторный тиреотоксикоз новорожденных, хронический лимфоцитарный тиреоидит (хашитоксикоз). Необходимо еще раз подчеркнуть, что ДТЗ, так же как и АИТ, является аутоиммунным заболеванием, о чем нередко забывают врачи, устанавливая диагноз.
В случаях предположения о тиреотоксикозе, первоочередным исследованием является определение уровня тиреоидных гормонов. При этом диагностически значимым является повышенный или определяемый на верхней границе нормы уровень Т4св. и Т3св. в крови в сочетании с пониженным уровнем ТТГ.
С целью уточнения причины тиреотоксикоза необходимо проведение УЗ-исследования щитовидной железы, а также определение тиреоглобулина и антитиреоидных антител в крови (АТ-ТПО и антител к рецепторам ТТГ). В случае одновременного повышения тиреоидных гормонов и ТТГ, следует подумать о тиреотоксикозе вторичного (гипофизарного) генеза с последующим проведением визуализации гипофиза.
Антитела к ТПО – антитела к ферменту клеток щитовидной железы, участвующему в синтезе тиреоидных гормонов. Они являются показателем агрессии иммунной системы по отношению к собственному организму. Тиреоидная пероксидаза обеспечивает образование активной формы йода, которая способна включаться в процесс йодификации тиреоглобулина. Антитела к ферменту блокируют его активность, вследствие чего снижается секреция тиреоидных гормонов (T4,T3). Однако АТ-ТПО могут быть только «свидетелями» аутоиммунного процесса. Антитела к тиреопероксидазе – наиболее чувствительный тест для обнаружения аутоиммунного заболевания щитовидной железы. Обычно их появление является первым сдвигом, который наблюдается в ходе развивающегося гипотиреоза вследствие тиреоидита Хашимото. При использовании достаточно чувствительных методов АТ-ТПО обнаруживаются у 95% людей с тиреоидитом Хашимото, и примерно у 85% пациентов с болезнью Грейвса. Обнаружение АТ-ТПО во время беременности говорит о риске развития у матери послеродового тиреоидита и возможном влиянии на развитие ребенка.
Повышение уровня АТ-ТПО выявляется при болезни Грейвса (диффузный токсический зоб), узловом токсическом зобе, подостром тиреоидите (де Кревена), послеродовой дисфункции щитовидной железы, хроническом тиреоидите (Хашимото), идиопатическом гипотиреозе, нетиреоидных аутоиммунных заболеваниях.
Антитела к тиреоглобулину (АТ-ТГ, anti-thyroglobulin autoantibodies) – аутоантитела к белку-предшественнику тиреоидных гормонов. Тиреоглобулин – йодированный белок, из которого образуются тиреоидные гормоны (Т3 и Т4). Он продуцируется в организме только клетками щитовидной железы и накапливается в фолликулах железы в виде коллоида. Небольшие количества тиреоглобулина (пропорциональные общей массе ткани железы и активности стимулирующих влияний ТТГ) поступают в кровь во время секреции тиреоидных гормонов. Низкие концентрации антител к тиреоглобулину обнаруживаются примерно у 10% здоровых индивидуумов.
АТ-ТГ в высоких титрах часто присутствуют у пациентов с аутоиммунными заболеваниями щитовидной железы (30% пациентов с болезнью Грейвса, 85% пациентов с тиреоидитом Хашимото).
Использование АТ-ТГ в целях выявления аутоиммунных заболеваний щитовидной железы целесообразно в йоддефицитных регионах, особенно при обследовании пациентов с узловым зобом.
Определение АТ-ТГ полезно также при мониторинге терапии йодом эндемического зоба, поскольку йодированный тиреоглобулин более иммуногенен.
Высокий уровень АТ-ТГ, как и АТ-ТПО, указывает на риск нарушения функции щитовидной железы, в том числе, тиреоидной дисфункции во время беременности, потенциально опасной для плода, послеродового тиреоидита, возможного поражения щитовидной железы у больных с нетиреоидными аутоиммунными эндокринными заболеваниями и членов семей больных с наследственными органоспецифическими аутоиммунными заболеваниями.
Клинический диагноз при увеличении щитовидной железы формулируется с учетом следующих характеристик:
- Форма увеличения щитовидной железы, наличие либо отсутствие узлов
а) диффузный зоб;
б) узловой зоб.
- Локализация зоба:
а) типично расположенный;
б) частично загрудинный;
в) кольцевой;
г) дистопия.
- Размер зоба:
а) при пальпаторном исследовании;
б) при сонографич. исследовании.
- Функциональное состояние щитовидной железы:
а) эутиреоз;
б) гипотиреоз;
в) тиреотоксикоз.
Диффузный токсический зоб (ДТЗ) (болезнь Грейвса–Базедова) – аутоиммунное заболевание, характеризующееся стойким повышением секреции тиреоидных гормонов, диффузным увеличением щитовидной железы в сочетании с эндокринной офтальмопатией у 50–70% больных.
В 1840 году Базедов подробно описал заболевание и выделил 3 основных симптома: зоб, пучеглазие и тахикардию, не утративших и поныне высокую диагностическую значимость. Впервые ДТЗ у ребенка был описан A. Romberg в 1851 году, который диагностировал у 14-летней девочки зоб, тахикардию и аменорею. В России первое описание тиреотоксикоза у ребенка 5 лет сделано Н. Ф. Филатовым в 1902 году.
Этиология заболевания
- инфекции (после острых детских инфекций, обострения хронического тонзиллита);
- психическая и физическая травма;
- инсоляция;
- врожденная предрасположенность.
Патогенез
Патогенез сложный и до конца не установлен. Общепризнана аутоиммунная теория развития ДТЗ, связанная с появлением в сыворотке крови антител к рецепторам тиреотропина на поверхности клеток щитовидной железы.
Собирательное название всех антител щитовидной железы – тиреостимулирующие иммуноглобулины. Наиболее изученным среди них является длительно действующий тиреостимулятор LATS, предотвращающий связывание антигена с компонентами щитовидной железы (т. н. депрессор функции щитовидной железы). Определенную роль в патогенезе ДТЗ играют гуморальный и клеточный иммунитет.
Важное место также отводится влиянию генетических факторов: ген, обуславливающий изменения в иммунокомпетентной системе, локализован на 6-й хромосоме и тесно сцеплен с антигеном HLA- Dw3. Отмечена также большая частота HLA- B8.
Морфологическая структура щитовидной железы при тиреотоксикозе у детей изучена в меньшей мере, чем у взрослых. Отмечены полиморфизм фолликулов, переход кубического эпителия, выстилающего фолликулы, в цилиндрический, наличие значительных утолщений с одновременным образованием сосочковых выростов в просвете фолликулов.
Клиническая картина
Ранний и постоянный симптом ДТЗ –увеличение щитовидной железы, обычно диффузное (узловой зоб встречается у детей редко). Классификация степеней увеличения щитовидной железы представлена в таблице 1. 
В развитии и течении тиреотоксикоза различают 4 стадии (по Milcu):
I cm., невротическая. Клиника вегетативного невроза с общим повышением возбудимости нервной системы, сердцебиениями при малозаметном увеличении щитовидной железы.
II ст., нейрогормональная. Увеличение щитовидной железы в сочетании с классическими симптомами тиреотоксикоза: трудоспособность, похудание, глазные симптомы.
III ст., висцеропатическая. Поражение внутренних органов с нарушением их функции.
IV cт., кахектическая. Необратимые дистрофия, изменения внутренних органов и систем, выражена общая дистрофия или кахексия, склонность к коматозным состояниям, тиреотоксическим кризам, мерцательной аритмии.
Наиболее распространенные клинические проявления тиреотоксикоза у детей представлены в таблице 2.
Изменения сердечно-сосудистой системы
1) Тахикардия 90–120 уд./мин. (пульсовая волна напоминает таковую при аортальной недостаточности). Сохранение тахикардии во время сна – важный признак при дифференциальной диагностике с тахикардиальным неврозом сердца.
2) Усиление сердечного толчка, тоны сердца часто усилены, четкие, акцент II тона над легочной артерией. При тяжелом тиреотоксикозе тоны сердца резко приглушены!
3) Функциональные сердечные шумы – грубый систолический шум на легочной артерии, на верхушке сердца, в V точке (меняется при перемене положения тела). Иногда – функционально-диастолич. шумы.
4) Размеры сердца чаще смещены влево.
5) АД систолическое повышено (150–170 мм. рт. ст.), диастолическое в норме или понижено.
6) На рентгене талия сердца сглажена, левый желудочек увеличен; для дифференциальной диагностики с митральными пороками используют контрастирование пищевода (отклонение тени контрастированного пищевода отсутствует).
Эндокринная офтальмопатия
- экзофтальм,
- отек орбитальных тканей,
- изменения глазных мышц.
Глазные симптомы при ДТЗ изучены довольно полно. Их известно до 40. Приведем некоторые из наиболее часто встречающихся.
Симптом Дальримпля – широкое раскрытие глазных щелей (придает лицу больного выражение страха, удивления, испуга или ужаса).
Симптом Грефе – запаздывание верхнего века при медленном опускании взора вниз.
Симптом Мебиуса – недостаточность конвергенции.
Симптом Штельвага – редкое и неполное мигание.
Симптом Жоффруа – отсутствие морщин на лбу при взгляде вверх.
Изменения нервной системы и психики
85% детей рано обнаруживают моторное возбуждение и эмоциональную неустойчивость; чрезмерно активны, постоянно находятся в движении, нервные, раздражительные, впечатлительные, неуравновешенные. Быстрая смена настроения со склонностью к агрессии и плаксивости. Снижение памяти, расстройство сна. Головная боль – также один из ведущих симптомов заболевания. Отмечается тремор пальцев вытянутых рук. Возможно наличие хорееформного гиперкинеза (насильственные, типичные, быстрые, толчкообразные движения пальцев рук, головы, сокращения мимических мышц и мускулатуры конечностей). Характерны вазомоторные, секреторные и трофические расстройства: гипергидроз, интенсивный и стойкий дермографизм, кожный зуд, повышение кожной температуры.
Наблюдается общая и мышечная слабость. Поражаются преимущественно проксимальные отделы конечностей, атрофия мышц пояса верхних конечностей. Определяются положительный симптом Мари (тремор пальцев вытянутых рук), тремор всего тела (симптом «телеграфного столба»), гиперрефлексия.
Изменения желудочно-кишечного тракта
- рвота и понос встречаются реже, чем у взрослых;
- повышение аппетита;
- прогрессирующее похудение.
Симптомы надпочечниковой недостаточности
- общая слабость и утомляемость;
- пигментация кожных покровов;
- низкое диастолическое АД.
Отмечается также увеличение лимфоузлов. В крови – лимфоцитоз; нарушение экскреции 17-КС и 17-ОКС.
При ДТЗ снижается антитоксическая и гликогенообразовательная функции печени. Нередко выявляется нарушение углеводного обмена (гипергликемическая сахарная кривая). У части детей наблюдаются изменения скелета (усиленный рост, ускоренное окостенение), в ряде случаев – задержка полового развития.
Диагностика
Диагностика основывается на клинической картине, а также лабораторных методах:
- Rö-логически выявляется опережение костного возраста;
- На ЭКГ определяется высокий вольтаж зубцов, синусовая тахикардия, ускорение AV-проводимости;
- Снижение уровня холестерина;
- Повышение уровня Тз и Т4.
Дифференциальная диагностика
- гиперплазия щитовидной железы в пубертатном периоде, когда она сочетается с функциональными нейровегетативными и вегетососудистыми сдвигами;
- при отсутствии зоба и экзофтальма неверно диагностируют ревматизм или врожденный порок сердца.
Лечение
Наиважнейшей задачей лечения тиреотоксикоза является достижение эутиреоидного состояния, а также купирование симптомов патологии сердечно-сосудистой системы.
Первой линией препаратов в лечении тиреотоксикоза, согласно протоколам по детской эндокринологии (приказ МОЗ Украины №254 от 27.04.2006 г.), являются тиреостатики: тирозол, мерказолил, тиамазол, метизол и др. Начальная доза — 0,3–0,5 мг/кг в сутки в зависимости от тяжести тиреотоксикоза. Доза делится на 2–3 приема. При клиническом улучшении (нормализация пульса, отсутствие клинических проявлений тиреотоксикоза), в среднем через 14–21 день, далее каждые 10–16 дней, дозу снижают на 2,5–5 мг до поддерживающей. Средняя поддерживающая доза — 2,5–7,5 мг/сутки (приблизительно 50% от начальной) – 1 раз в день. Подобную терапию продолжают в течение 1–1,5 лет. Длительность тиреостатической терапии у детей может достигать 2 лет.
Использование настоящей схемы предполагает постоянный контроль за функцией щитовидной железы с соответствующей коррекцией дозы для поддержания эутиреоидного состояния.
На фоне приема препаратов тиамазола могут возникать побочные эффекты: аллергические реакции в виде зудящей кожной сыпи, тошноты, изменений со стороны периферической крови: лейкопении, агранулоцитоза, тромбоцитопении.
Патогенетическую тиреостатическую терапию при тиреотоксикозе сочетают с применением β-адреноблокаторов, которые тормозят активность симпатоадреналовой системы, уменьшая нагрузку на сердце и снижая потребность миокарда в кислороде.
Бета-адреноблокаторы (анаприлин, пропранолол) — первые 4 недели, одновременно с тиреостатиками — 1–2 мг/кг в сутки в 3–4 приема. При нормализации пульса — постепенное снижение дозы до полной отмены препарата (резкое прекращение приема препарата может приводить к «синдрому отмены» с ухудшением состояния).
Совместное использование β-адреноблокаторов с тиреостатиками приводит к более быстрому устранению тахикардии. Кроме этого, применение β-блокаторов способствует уменьшению выраженности потливости, тремора и повышенной возбудимости. Однако необходимо отметить, что β-блокаторы не являются средством этиотропного лечения и должны использоваться только в сочетании с патогенетической (тиреостатической) терапией.
Показания для назначения глюкокортикоидов
- тяжелое течение тиреотоксикоза в сочетании с эндокринной офтальмопатией;
- признаки надпочечниковой недостатночности;
- лейкопения, тромбоцитопения;
- в случае присоединения сопутствующей патологии,
- на фоне стресса – для предупреждения острой надпочечниковой недостаточности.
Назначается преднизолон коротким курсом в средней дозе 0,2–0,3 мг/кг/сутки в 2–3 приема, с постепенным снижением через 7–10 дней на 2,5–5 мг каждые 5–7 дней до полной отмены.
Дополнительные методы лечения: санация очагов хронической инфекции, седативные препараты, витамины, гепатопротекторы.
Длительность терапии, в среднем, 1–2 года; у некоторых больных достигает 3 и более лет. Лечение проводят под контролем анализов крови (при начальной дозе – 1 раз в неделю). При появлении лейкопении назначают стимуляторы лейкопоэза (пентоксил, лейкоген, нуклеинат натрия и др.) в сочетании с преднизолоном. Повторная реакция крови после возобновления лечения требует его прекращения.
Хирургическое лечение показано при тяжелых формах диффузного токсического зоба, не поддающегося консервативной терапии. В предоперационном периоде большое внимание уделяют назначению стероидных препаратов. За 2 недели до оперативного вмешательства назначают преднизолон по 5–10 мг/сутки, по показаниям — за 1–2 дня до операции — гидрокортизон по 25–50 мг в/м, ДОКСА.
Основные принципы субтотальной субфасциальной резекции по О. В. Николаеву
- минимальное травмирование тканей достигается ограничением зоны операции пределами 4-й фасции шеи, которая висцеральным листком покрывает щитовидную железу, а париетальным – прилегающие к ней мышцы;
- минимальная кровопотеря;
- правильное положение больного на операционном столе;
- совершенная анестезия.
Соблюдение этих условий обеспечивает профилактику послеоперационного тиреотоксикоза.
Проводя дифференциальную диагностику тиреотоксикоза, необходимо отметить, что признаки тиреотоксикоза могут появляться также и в начальной стадии аутоиммунного тиреоидита, однако их выраженность и длительность значительно меньше, чем при ДТЗ.
Как правило, продолжительность тиреотоксической стадии АИТ не превышает нескольких недель, редко – до 4–6 месяцев, трансформируясь затем в гипотиреоз. В то же время при ДТЗ симптомы тиреотоксикоза прогрессивно нарастают.
Критерием адекватности терапии тиреотоксикоза у детей является стойкое поддержание нормального уровня Т4св. и ТТГ в течение 1 года после завершения лечения, что расценивается как наступление ремиссии.
В качестве примера поздней диагностики диффузного токсического зоба приводим клинический случай из практики.
Девочка Л. П., 16 лет, поступила в эндокринологическое отделение с жалобами на увеличение щитовидной железы, общую слабость, раздражительность, учащенные сердцебиения, повышение артериального давления.
Болеет в течение 2,5 лет, когда впервые обнаружено увеличение щитовидной железы 1-й степени. При первоначальном определении тиреоидных гормонов выявлено снижение ТТГ до 0,07 МЕ/мл (N 0,23–3,4), повышение Т4св. и Т3св. в 1,5-2 раза, уровень АТ-ТПО составлял 180,1 МЕ/мл (N до 34,0). Эндокринологом по месту жительства был диагностирован аутоиммунный тиреоидит, назначен йодомарин 150 мкг в сутки, который больная получала в течение 6 месяцев. При повторном УЗИ щитовидной железы было выявлено ее увеличение до 2-й степени, снижение уровня ТТГ, повышение Т4св. в 2,5 раза, нарастание в динамике АТ-ТПО. Тогда же впервые мать отметила увеличение глаз у девочки, а также была зарегистрирована артериальная гипертензия в пределах 130–140/60–70 мм. рт. ст., сопровождавшаяся головной болью. Диагноз эндокринолога по месту жительства: аутоиммунный тиреоидит. Рекомендовано продолжить прием йодомарина в той же дозе, дополнительно назначен пумпан. В дальнейшем мать заметила прогрессирующее увеличение глаз у ребенка, наросла раздражительность, плаксивость, появился тремор пальцев рук, сердцебиение. Направлена в клинику для уточнения диагноза и определения тактики лечения.
 При осмотре девочка правильного телосложения, пониженного питания. Рост 169 см, масса тела 46 кг, ИМТ – 16,01 кг/м2. Половое развитие – 5 стадия по Tanner. АД 150/70 мм рт. ст. Кожные покровы розовые, теплые, гипергидроз ладоней, движения суетливые, тремор тела и пальцев рук. Положительные симптомы Мари и «телеграфного столба». Выражен экзофтальм, гиперпигментация и отечность век. Положительные симптомы Жоффруа, Мебиуса, Штельвага, Дельримпля. Область шеи деформирована за счет увеличенной щитовидной железы, консистенция ее при пальпации мягко-эластическая. В легких дыхание везикулярное. Тоны сердца громкие, ритмичные, ЧСС – 120/мин.
При осмотре девочка правильного телосложения, пониженного питания. Рост 169 см, масса тела 46 кг, ИМТ – 16,01 кг/м2. Половое развитие – 5 стадия по Tanner. АД 150/70 мм рт. ст. Кожные покровы розовые, теплые, гипергидроз ладоней, движения суетливые, тремор тела и пальцев рук. Положительные симптомы Мари и «телеграфного столба». Выражен экзофтальм, гиперпигментация и отечность век. Положительные симптомы Жоффруа, Мебиуса, Штельвага, Дельримпля. Область шеи деформирована за счет увеличенной щитовидной железы, консистенция ее при пальпации мягко-эластическая. В легких дыхание везикулярное. Тоны сердца громкие, ритмичные, ЧСС – 120/мин.
Данные лабораторных и инструментальных исследований. Общий анализ крови в пределах нормы. Незначительно повышены уровни трансаминаз и щелочной фосфатазы. Оральный глюкозо-толерантный тест: тощаковая гликемия – 4,6 ммоль/л, через 2 часа – 6,1 ммоль/л. Уровень гормонов: ТТГ – 0,005 МЕ/мл (N 0,27–4,2), Т4св. – 5,13 нг/дл (N 1,1–1,8), Т3св. – 26,59 пг/мл (N 2,3–5,0), АТ-ТПО – 235,7 МЕ/мл (N до 34,0), АТ к рецепторам ТТГ – более 40 МЕ/мл (N до 1,75). ЭКГ: ритм синусовый, 120 в минуту. УЗИ щитовидной железы: диффузные изменения, эхогенность повышена, увеличение объема до 52,3 см3.
На основании анамнестических, клинических, лабораторных и инструментальных данных обследования установлен диагноз: «Диффузный токсический зоб 2 степени, тиреотоксикоз средней тяжести». Назначена терапия тирозолом в стартовой дозе 25 мг в сутки в сочетании с анаприлином 50 мг в сутки, которая проводилась в течение 3-х недель с последующим постепенным снижением дозы обоих препаратов и отменой, в дальнейшем, анаприлина. На фоне проводимой терапии достигнуты признаки клинико-лабораторного эутиреоза. В настоящее время продолжает получать поддерживающую дозу тирозола – 5 мг в сутки. Через 6 месяцев от начала терапии объем ЩЖ уменьшился вдвое, нормализовались уровни тиреоидных гормонов (ТТГ – 0,8 МЕ/мл, Т4св. – 1,6 нг/дл), уменьшился объем щитовидной железы до 16,4 см3.
Таким образом, данный случай демонстрирует пример поздней диагностики диффузного токсического зоба, который ошибочно рассматривался как тиреотоксическая стадия аутоиммунного тиреоидита.
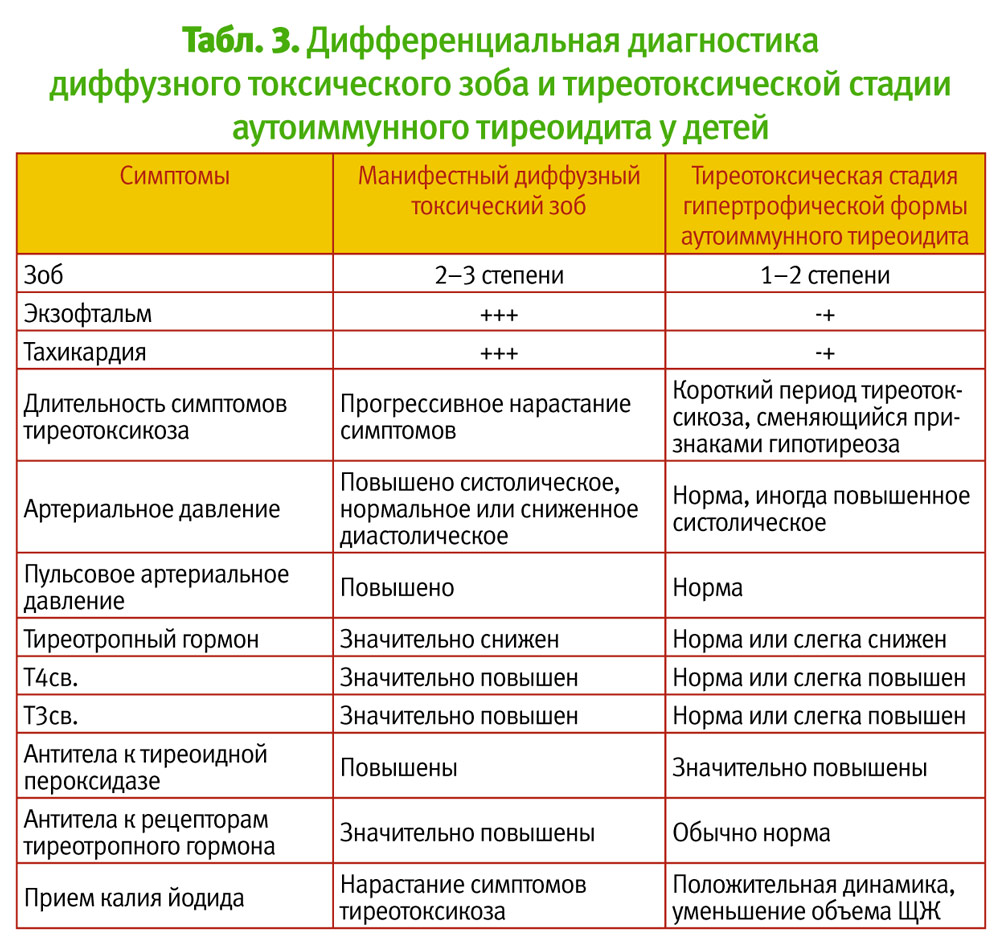
Учитывая ряд сложностей в постановке диагноза тиреотоксикоза, нами предложена схема дифференциальной диагностики диффузного токсического зоба и тиреотоксической стадии АИТ (см. таблицу 3).
Важно отметить, что, клинически значимыми антитиреоидными антителами при тиреотоксикозе являются: АТ-ТПО, однако, их определение целесообразно только в случаях нарушенной функции ЩЖ. При этом повышение их титра позволяет высказать предположение об АИТ – болезни Хашимото. При ДТЗ титры АТ-ТПО, как правило, ниже, чем при АИТ. Определение содержания АТ-ТПО в динамике нецелесообразно, так как они не обладают прогностической ценностью.
Что касается антител к рецепторам ТТГ, то их повышение весьма характерно для ДТЗ, что может явиться одним из ведущих лабораторных критериев для диагностики тиреотоксикоза. Кроме того, определение уровня АТ к рецепторам ТТГ в динамике позволяет оценить прогноз в условиях проведения и после окончания тиреостатической терапии (определение риска рецидива этого заболевания).
Выводы
- Проведение дифференциальной диагностики тиреотоксикоза у детей предполагает оценку, прежде всего, длительности и выраженности клинико-лабораторных симптомов, таких как зоб, экзофтальм, тахикардия, которые типичны для диффузного токсического зоба. При этом признаки тиреотоксикоза, наблюдаемые в начальной стадии аутоиммунного тиреоидита, менее выражены, нежели при диффузном токсическом зобе.
- Повышение уровня антител к тиреоидной пероксидазе характерно не только для аутоиммунного тиреоидита, но и для диффузного токсического зоба, ввиду аутоиммунного генеза последнего.
- Повышенный уровень антител к рецепторам тиреотропного гормона является одним из наиболее важных диагностических критериев диффузного токсического зоба, наряду со снижением тиреотропина и повышением уровней свободного тироксина и свободного трийодтиронина.


коментариев