Новый консенсус EASD/ADA и рекомендации ADA 2015
2015–2016 годы ознаменовались появлением обновленных клинических руководств по диагностике и лечению сахарного диабета (СД) – консенсуса Европейской ассоциации по изучению СД (EASD) и Американской диабетической ассоциации (ADA), а также рекомендаций ADA, которые традиционно пересматриваются ежегодно. Какие существенные изменения претерпели эти согласительные документы?
Ежегодное обновление доказательной базы по диагностике и лечению пациентов с сахарным диабетом позволяет Американской диабетической ассоциации (ADA) достаточно часто пересматривать свои клинические рекомендации по ведению пациентов с СД и вносить своевременные рекомендательные коррективы.
Ключевые изменения настоящей редакции руководства Американской диабетической ассоциации касаются нескольких положений по диагностическим критериям СД и тактике ведения пациентов.
Необходимо отметить, что произошло обновление и формата стандартов. В новой редакции они опубликованы в виде единого документа, в то время как в старой это была подборка отдельных документов.
Остановимся подробнее на основных положениях, касающихся диагностики и терапии СД.
СД можно разделить на следующие основные категории:
- Диабет 1 типа (результат разрушения b-клеток, что, как правило, приводит к абсолютному дефициту инсулина).
- Диабет 2 типа (прогрессирующее снижение секреции инсулина на фоне инсулинорезистентности).
- Гестационный сахарный диабет (ГСД) (сахарный диабет диагностирован во втором или третьем триместре беременности, не является (в строгом смысле) явным сахарным диабетом).
- Специфические типы диабета вследствие других причин, в том числе моногенные синдромы диабета (например, диабет новорожденных и диабет взрослого типа у молодых, MODY-тип), болезней экзокринной части поджелудочной железы (такие как муковисцидоз), медикаментозно- или химически-индуцированный диабет (например, при лечении ВИЧ/СПИДа или после трансплантации органов).
Согласно современным материалам Американской диабетической ассоциации, определены категории повышенного риска развития СД (см табл. 1).
В качестве диагностического критерия уровень HbA1c должен составлять, в соответствии с современными рекомендациями, ³6,5% (48 ммоль/моль).
Рекомендуется определение HbA1c с использованием метода, сертифицированного в соответствии с National Glycohemoglobin Standardization Program (NGSP) или International Federation of Clinical Chemists (IFCC) и стандартизованного в соответствии с референсными значениями, принятыми в Diabetes Control and Complications Trial (DCCT).
Нормальным считается уровень HbA1c до 6,0% (42 ммоль/моль).
В случае отсутствия симптомов острой метаболической декомпенсации диагноз сахарного диабета должен быть поставлен на основании двух цифр, находящихся в диабетическом диапазоне, например дважды определенный HbA1c или однократное определение HbA1c + однократное определение уровня глюкозы.
В обновленных рекомендациях при СД у детей целевой уровень HbA1с должен составлять менее 7,5% для детей любого возраста.
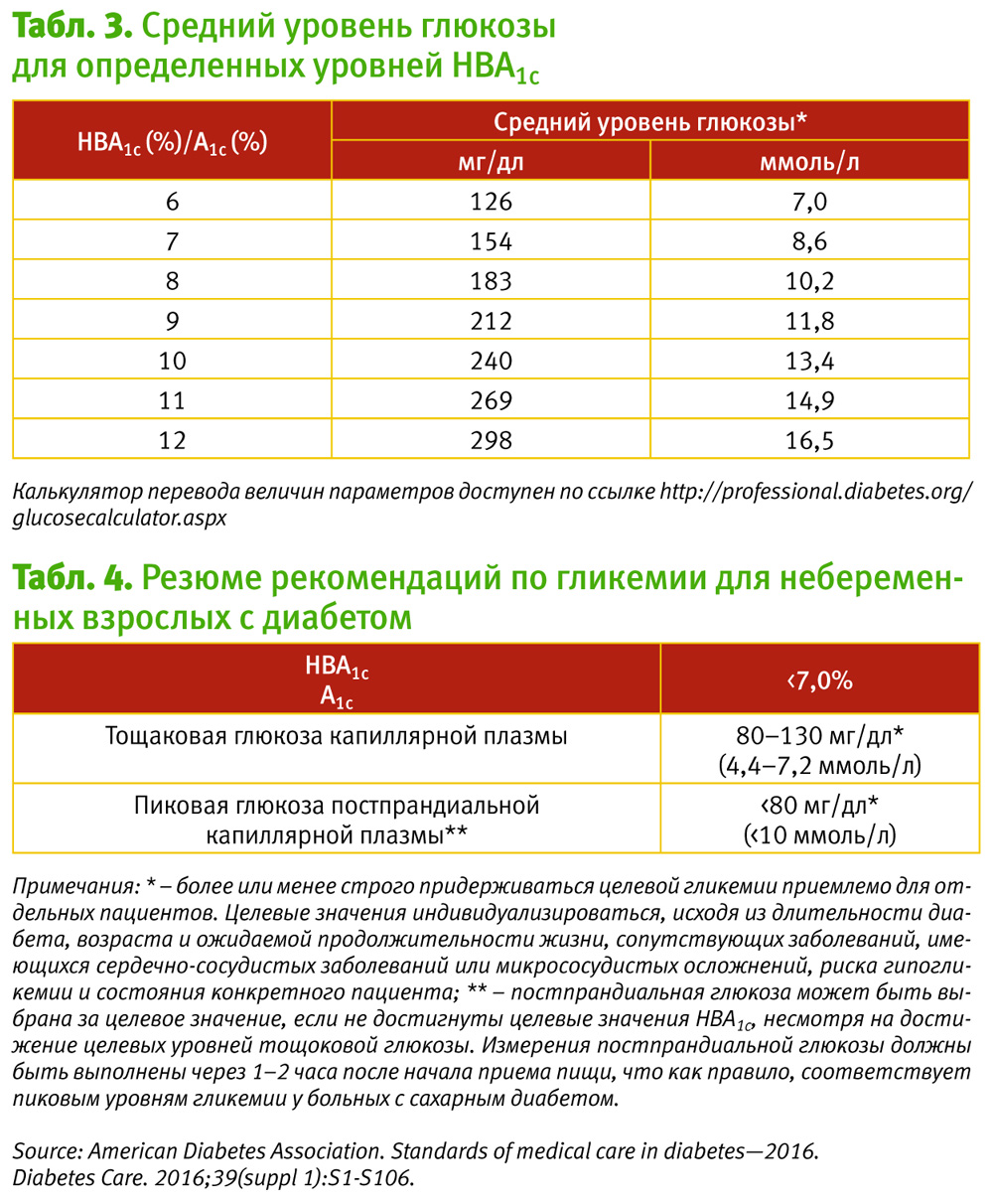
Что касается тощаковой гликемии, то целевые уровни гликемии натощак изменены с 70–130 мг/дл до 80–130 мг/дл с целью отражения новых данных по сравнению средних уровней глюкозы крови с показателем гликозилированного гемоглобина (табл. 2).

СД 2 типа
Проведение теста для выявления СД 2 типа у бессимптомных пациентов следует считать целесообразным для взрослых любого возраста, имеющих избыточный вес или страдающих ожирением (ИМТ ³25 кг/м2 или ³23 кг/м2 для американцев азиатского происхождения) и имеющих один или более из дополнительных факторов риска сахарного диабета. Для всех пациентов, особенно имеющих повышенную массу или ожирение, тестирование должно начинаться в возрасте 45 лет. (B)
Если анализы в норме, повторное тестирование целесообразно по крайней мере 1 раз в 3 года. (С)
Для выявления СД использование значений HbA1c, ГПН или двухчасовой глюкозы плазмы крови в нагрузочном тесте с 75 г глюкозы является приемлемым. (B)
У пациентов с СД необходимо выявление и, при необходимости, лечение других факторов риска сердечно-сосудистых заболеваний (ССЗ). (B)
Необходимость проведения тестов для выявления СД 2 типа должна рассматриваться у детей и подростков, имеющих избыточную массу тела или ожирение, а также для тех, у кого имеется 2 и более риск-факторов развития диабета. (Е)
Целевые значения гликемии HbA1с
- Проводить определение HbA1c по крайней мере два раза в год пациентам, у которых достигнуты цели лечения (и тех, кто имеет стабильный контроль гликемии). (Е)
- Проводить определение HbA1c ежеквартально пациентам, чья терапия изменилась или у которых не достигнуты целевые значения гликемии. (Е)
- Использование выборочного определения HbA1c дает возможность более своевременного изменения лечения. (Е)
- Снижение уровня HbA1c ниже или около 7%, как известно, уменьшает частоту микрососудистых осложнений сахарного диабета, а в случае реализации такого подхода в ближайшие сроки от дебюта СД демонстрирует долгосрочное снижение макрососудистых заболеваний. Таким образом, для многих небеременных взрослых HbA1c <7% является разумным целевым значением. (B)
Было бы разумно предлагать более жесткие целевые значения HbA1c (например, <6,5%) для отдельных пациентов, если эти значения могут быть достигнуты без выраженной гипогликемии или других побочных эффектов лечения. К таким пациентам могут быть отнесены люди, имеющие малую длительность диабета, получающие лечение только путем модификации стиля жизни или метформином, ожидаемую большую продолжительность жизни или не имеющие существенных сердечно-сосудистых заболеваний. (C)
Менее жесткие целевые значения HbA1c (например, <8%) могут быть целесообразными для пациентов с тяжелой гипогликемией в анамнезе, ограниченной продолжительностью жизни, выраженными микро- или макрососудистыми осложнениями, наличием выраженных сопутствующих заболеваний и для тех, кто давно страдает сахарным диабетом, у кого трудно достичь целевого значения гликемии, несмотря на самоконтроль диабета, достаточный контроль глюкозы и эффективные дозы нескольких сахароснижающих препаратов, включая инсулин. (B)
Коррекция гипергликемии при СД 2 типа: обновление консенсуса EASD/ADA-2015
Свой последний консенсус по коррекции гипергликемии у пациентов с сахарным диабетом 2 типа ADA и EASD опубликовали в 2012 г. Он существенно отличался от предыдущего согласительного документа 2009 г. и поэтому был представлен как новый консенсус, а не обновление. Ключевым посылом предыдущего консенсуса стал пациент-ориентированный подход к ведению больных СД 2 типа, подразумевающий индивидуализацию целей и схем терапии, а также максимальное привлечение пациентов к принятию клинических решений.
Проанализировав накопленную к тому времени доказательную базу и отметив недостаток прямых сравнительных исследований сахароснижающих препаратов, эксперты ADA и EASD консенсус 2012 г. сделали не таким директивным, как предыдущие. Он дает достаточно большую свободу врачу в выборе сахароснижающих средств и их комбинаций (табл. 3, 4).
Принцип ориентированности на пациента сохраняется и в обновленном консенсусе. Следует подчеркнуть, что это не новый согласительный документ, а обновление консенсуса 2012 г. с включением в него некоторых новых данных, полученных в недавних клинических исследованиях. Кардинальных изменений не претерпели ни подход к определению целей терапии, ни алгоритм лечения.
Стратегии лечения
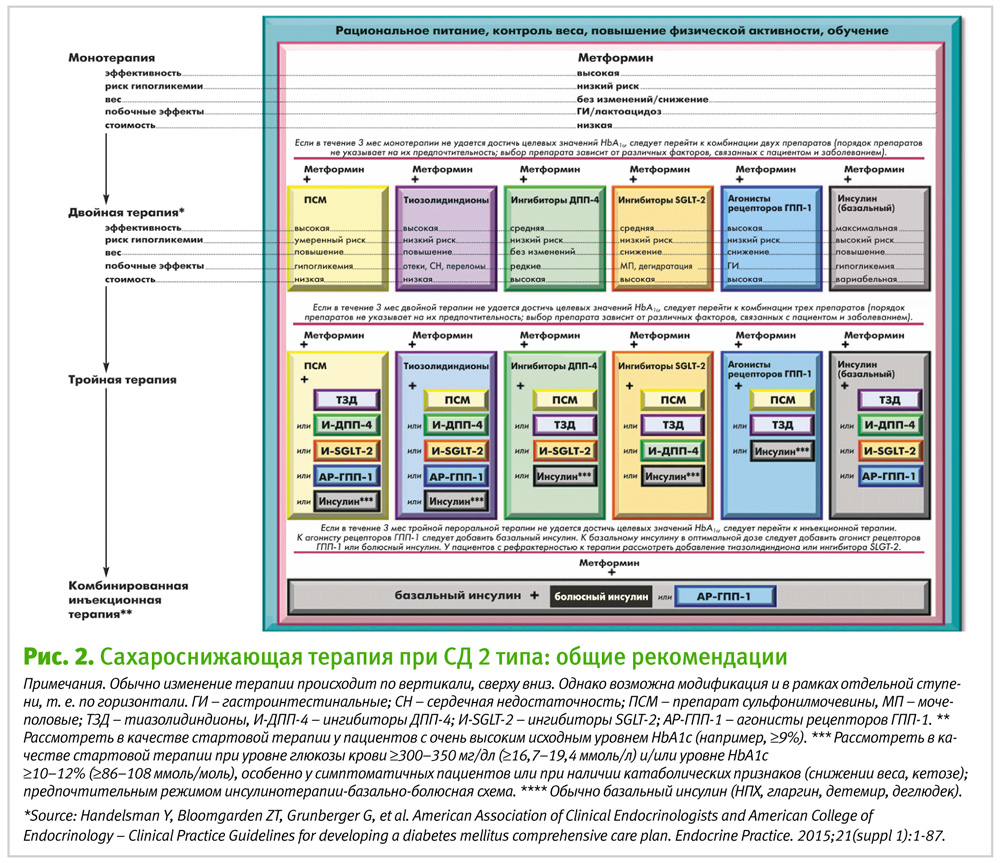
Метформин сохраняет свои позиции в качестве оптимального средства стартовой монотерапии и базового препарата в комбинированных схемах лечения сахарного диабета 2 типа. Ключевое место метформина в алгоритме лечения СД 2 типа, по данным экспертов во всем мире, обусловлено его благоприятным профилем безопасности, нейтральностью в отношении массы тела, потенциальным благоприятным влиянием на сердечно-сосудистые исходы и, что немаловажно, относительно низкой стоимостью.
В обновленном консенсусе подчеркивается необходимость смягчения ограничений по применению метформина при нарушении функции почек с целью более широкого применения этого важного лекарственного средства у пациентов со стабильной хронической болезнью почек легкой и средней тяжести. Многие практикующие врачи считают целесообразным назначение метформина даже при расчетной скорости клубочковой фильтрации (СКФ) <45–60 мл/мин./1,73 м2 с возможной коррекцией дозы в зависимости от степени снижения почечного клиренса. Критерий прекращения приема препарата – снижение СКФ до <30 мл/мин./1,73 м2. Применение метформина у пациентов с хронической болезнью почек требует тщательного мониторинга функции почек.
Метформин, если не противопоказан и хорошо переносится, является предпочтительным начальным фармакологическим средством для лечения диабета 2-го типа. (А)
У пациентов с впервые выявленным сахарным диабетом 2-го типа и наличием выраженных симптомов и/или значительно повышенным уровнем глюкозы в крови или HbA1c рассмотрите вопрос о назначении инсулинотерапии (с дополнительными медикаментозными средствами или без них). (Е)
Если при использовании инсулинонезависимой монотерапии в максимально переносимой дозе не удается достичь и поддерживать целевой уровень Hb A1с в течение 3 месяцев, добавьте второй пероральный препарат, агонист рецептора GLP-1 или базальный инсулин. (А)
Пациентоориентированный подход должен быть использован для выбора фармакологического препарата. На принятие решения о выборе препарата влияют его эффективность, стоимость, возможные побочные эффекты, масса тела пациента, сопутствующие заболевания, риск гипогликемии и предпочтения пациентов. (Е)
В современных рекомендациях целевой уровень диастолического артериального давления был повышен с 80 до 90 мм рт. ст., в то время как целевой показатель систолического АД остался прежним.
Эксперты ADA пересмотрели рекомендации по применению статинов у лиц с СД с целью их согласования с рекомендациями Американского колледжа кардиологии (ACC) и Американской ассоциации сердца (AHA). Как и в рекомендациях ACC/AHA, в новом руководстве ADA сделан акцент на применении статинов, исходя из профиля риска, а не показателей липопротеинов низкой плотности.
На основании последних исследований по терапии СД экспертами принята директива об обязательном применении статинов практически всем пациентам с сахарным диабетом. Исключением в этом вопросе являются лица в возрасте моложе 40 лет без других сердечно-сосудистых факторов риска и кардио-васкулярных заболеваний. По мере необходимости проводится мониторинг уровня липидов для оценки приверженности лечению. Показан ежегодный мониторинг уровня липидов у пациентов в возрасте моложе 40 лет, которые еще не начали прием статинов.
В отличие от рекомендаций ACC/AHA, эксперты ADA не настаивают на обязательном применении калькулятора сердечно-сосудистого риска.
В современных рекомендациях изменены граничные значения индекса массы тела (ИМТ) при проведении скрининга на предиабет и диабет среди лиц азиатского происхождения – 23 кг/м2 вместо предыдущих 25 кг/м2. Это изменение базируется на полученных недавно данных о повышении риска развития предиабета и диабета у лиц азиатского происхождения при меньших значениях ИМТ по сравнению с общей популяцией.
В отношении физической активности в обновленном документе пациентам с СД рекомендуется не проводить в сидячем положении более 90 мин. подряд. При необходимости длительной работы в сидячем положении необходимо периодически вставать и делать небольшую разминку.
Интересно, что эксперты ADA настоятельно не рекомендуют курение больным СД и не поддерживают применение электронных сигарет как альтернативы обычному курению либо способу облегчения зависимости.
Были добавлены рекомендации по проведению иммунизации против пневмококковых заболеваний у лиц пожилого возраста.
И, наконец, была выделена отдельная секция по ведению пациенток с сахарным диабетом во время беременности, которая обобщает информацию, ранее содержавшуюся по разным разделам.
Цели терапии
Контроль гликемии остается главным фокусом в ведении пациентов с СД 2 типа. Однако он всегда должен осуществляться на фоне комплексной программы по снижению кардиоваскулярного риска, включающей отказ от курения и внедрение других принципов здорового образа жизни, контроль артериального давления, липидоснижающую и в некоторых случаях – антиагрегантную терапию.
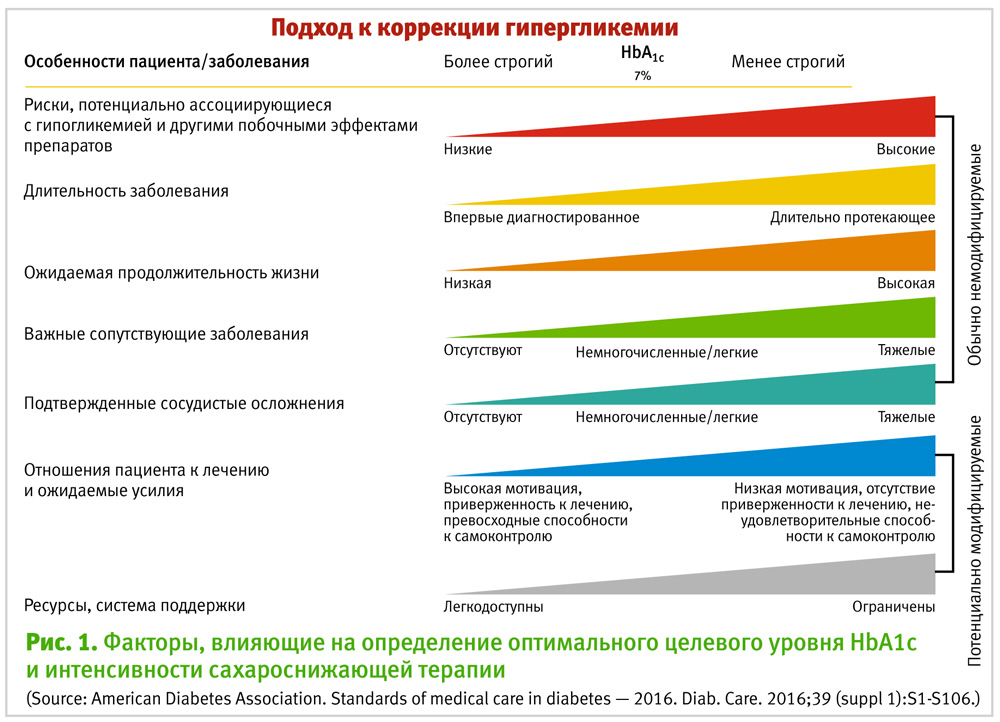
В консенсусе ADA/EASD подчеркивается необходимость индивидуализации лечения СД 2 типа с сохранением баланса между преимуществами контроля гликемии и его потенциальными рисками, с учетом побочных эффектов сахароснижающих препаратов (особенно гипогликемии), возраста и общего состояние здоровья пациента.
Основным обновлением этого рисунка в 2015 г. стало разделение факторов на потенциально модифицируемые и немодифицируемые.
Такие факторы, как отношение пациента к лечению и прилагаемые им усилия, доступ к ресурсам здравоохранения и системам поддержки, уникальны тем, что могут значительно улучшаться (или ухудшаться) с течением времени. Медицинским работникам следует поддерживать приверженность пациентов к терапии с помощью образовательных мероприятий, а также стараться оптимизировать медицинскую помощь с учетом финансовых возможностей пациента. Другие же факторы, такие как возраст, ожидаемая продолжительность жизни, сопутствующие заболевания, риски и последствия, связанные с побочными эффектами препаратов, более-менее постоянны. Стандартный целевой уровень HbA1c 7% был помещен в верхнюю часть рисунка в качестве некоторой опорной точки для определения степени интенсивности терапевтических вмешательств.
Терапевтические возможности
Самым существенным изменением в этом разделе стало появление нового класса сахароснижающих средств – ингибиторов натрийглюкозного котранспортера 2 типа (SGLT2). Результаты проведенных до настоящего времени исследований показали, что препараты этого класса снижают уровень HbA1c в среднем на 0,5–1% по сравнению с плацебо. Их механизм действия заключается в подавлении натрийглюкозного котранспортера 2 типа (SGLT2) в проксимальных канальцах нефронов, что приводит к снижению реабсорбции глюкозы и повышению ее экскреции с мочой до 80 г/день. Важно подчеркнуть, что благодаря инсулиннезависимому механизму действия ингибиторы SGLT2 могут применяться на любой стадии СД 2 типа, в том числе при значительном снижении секреции инсулина. Дополнительные потенциальные преимущества ингибиторов SGLT2 включают умеренное снижение массы тела (примерно 2 кг со стабилизацией в течение 6–12 мес.) и устойчивое снижение систолического и диастолического артериального давления (примерно 2–4/1–2 мм рт. ст).
Среди побочных эффектов ингибиторов SGLT2 отметим, в первую очередь, повышение частоты урогенитальных инфекций, которые вполне предсказуемы, исходя из механизма действия этих препаратов. Кроме того, ингибиторы SGLT2 следует применять с осторожностью у пожилых лиц, а также у пациентов любого возраста, принимающих диуретики или имеющих признаки гиповолемии, поскольку характерный для этих препаратов диуретический эффект может вызвать дегидратацию.
Некоторые изменения были внесены в описание тиазолидиндионов. В частности, после получения результатов недавних исследований были развеяны опасения относительно повышения риска рака мочевого пузыря на фоне их приема (в частности, пиоглитазона). Но в то же время, в консенсусе подчеркивается, что применение глитазонов может приводить к повышению массы тела, появлению периферических отеков, увеличению частоты сердечной недостаточности и риска переломов, преимущественно у женщин.
Несколько расширились представления о преимуществах и рисках ингибиторов дипептидилпептидазы-4 (иДПП-4). На основании результатов обсервационных исследований на эти препараты возлагались большие надежды в отношении снижения риска макроваскулярных осложнений диабета. Однако два масштабных контролируемых клинических испытания по изучению эффективности и безопасности саксаглиптина и алоглиптина показали, что иДПП-4 не оказывают существенного влияния на общий сердечно-сосудистый риск, то есть не повышают и не снижают его. Следует, правда, отметить, что продолжительность этих исследований была относительно небольшой (1,5–2 года), поэтому эти выводы касаются средне-, а не долгосрочной перспективы.
В консенсусе отмечено, что в группе иДПП-4 было зарегистрировано повышение частоты госпитализаций по поводу сердечной недостаточности. Еще длятся несколько исследований по изучению эффективности и безопасности иДПП-4, и до получения их результатов у пациентов с сердечной недостаточностью данный класс препаратов следует использовать с осторожностью или вообще не применять.
Что касается панкреатической безопасности иДПП-4, то в консенсусе отмечено, что недавние результаты нескольких крупных контролируемых исследований не показали статистически значимого повышения частоты патологии поджелудочной железы на фоне терапии иДДП-4.
В тех случаях, когда метформин противопоказан или имеется его непереносимость, может быть использован один из препаратов второй линии.
Стартовая комбинированная терапия с применением метформина и препарата второй линии может обеспечить более быстрое достижение целевых значений HbA1c, чем последовательная интенсификация терапии. Такой подход может быть рассмотрен у пациентов с исходным уровнем HbA1c, значительно превышающим целевой, у которых достижение контроля с помощью монотерапии маловероятно. Разумным критерием для такого назначения является уровень HbA1c ³9% (³75 ммоль/моль). Но поскольку в настоящее время преимущества более быстрого достижения целевых значений HbA1c (в течение недель и даже месяцев) не доказаны, своевременное последовательное назначение препаратов считается приемлемой альтернативой даже у пациентов с исходно высоким уровнем HbA1c при условии тщательного мониторинга.
Что касается комбинированной двойной и тройной терапии, то врачу предоставляется достаточная свобода выбора, однако требуется знание преимуществ и рисков доступных сегодня сахароснижающих средств, чтобы сделать оптимальный выбор в каждом конкретном случае.
К сожалению, у некоторых пациентов гликемический контроль остается неудовлетворительным даже при использовании комбинации трех сахароснижающих препаратов. В таких случаях следует рассмотреть назначение базального инсулина, который обычно применяется в комбинации с метформином и иногда с дополнительным препаратом.
Если и такая схема лечения не обеспечивает контроль гликемии, в консенсусе было рекомендовано добавление от 1 до 3 инъекций аналога инсулина быстрого действия перед приемами пищи.
В консенсусе-2015 уделено значительно большее внимание ведению пациентов с поздними стадиями СД, у которых бывает сложно достичь контроля гликемии. В частности, предлагается новый подход – комбинация агонистов рецепторов глюкагоноподобного пептида-1 (как короткодействующих, так и более новых лекарственных форм для применения один раз в неделю) с базальным инсулином.
В нескольких недавних исследованиях была показана эквивалентная или даже несколько более высокая эффективность такой комбинации по сравнению с добавлением прандиального инсулина при более низкой частоте гипогликемических состояний и снижении массы тела.
Агонисты рецепторов ГПП-1 являются предпочтительными для больных с более выраженным ожирением и которые плохо переносят режим многократных инъекций инсулина. Пациентов, которые не ответили адекватно на добавление к базальному инсулину агонистов рецепторов ГПП-1, следует перевести на прандиальный инсулин в составе базально-болюсной схемы инсулинотерапии. У некоторых пациентов следует рассмотреть добавление ингибиторов SGLT-2, что может улучшить контроль гликемии и снизить потребность в инсулине, особенно при ожирении и выраженной инсулинорезистентности, нуждающихся в высоких дозах инсулина.
Более старым вариантом является добавление тиозолидиндионов (обычно пиоглитазона), которые также обладают инсулиносберегающим эффектом и могут приводить к дополнительному снижению уровня HbA1c, но при этом способствуют прибавке веса, вызывают задержку жидкости и повышают риск развития сердечной недостаточности. Таким образом, на данной стадии заболевания тиозолидиндионы можно применять в низких дозах и только при условии тщательного мониторинга пациента.
Определенную роль при очень высоких ежедневных дозах инсулина, играют концентрированные инсулины, позволяющие уменьшить объем инъекции. Однако их назначают с осторожностью при тесном взаимодействия с пациентом. При невозможности достижения целевых уровней гликемии, несмотря на использование сложных схем лечения, стоит пересмотреть целевые показатели HbA1c или же (у пациентов с морбидным ожирением) рассмотреть возможность применения бариатрической хирургии.
Переход из педиатрической во взрослую службу
При переходе подростков во взрослую службу медицинские работники и их семьи должны осознавать многочисленные сложности (B) и готовить развивающихся подростков по крайней мере за 1 год до этого перехода. (E). Как педиатры, так и работники взрослой медицинской службы должны оказывать содействие в обеспечении всесторонней поддержки и обращения к соответствующим ресурсам подростковой и взрослой помощи. (B) 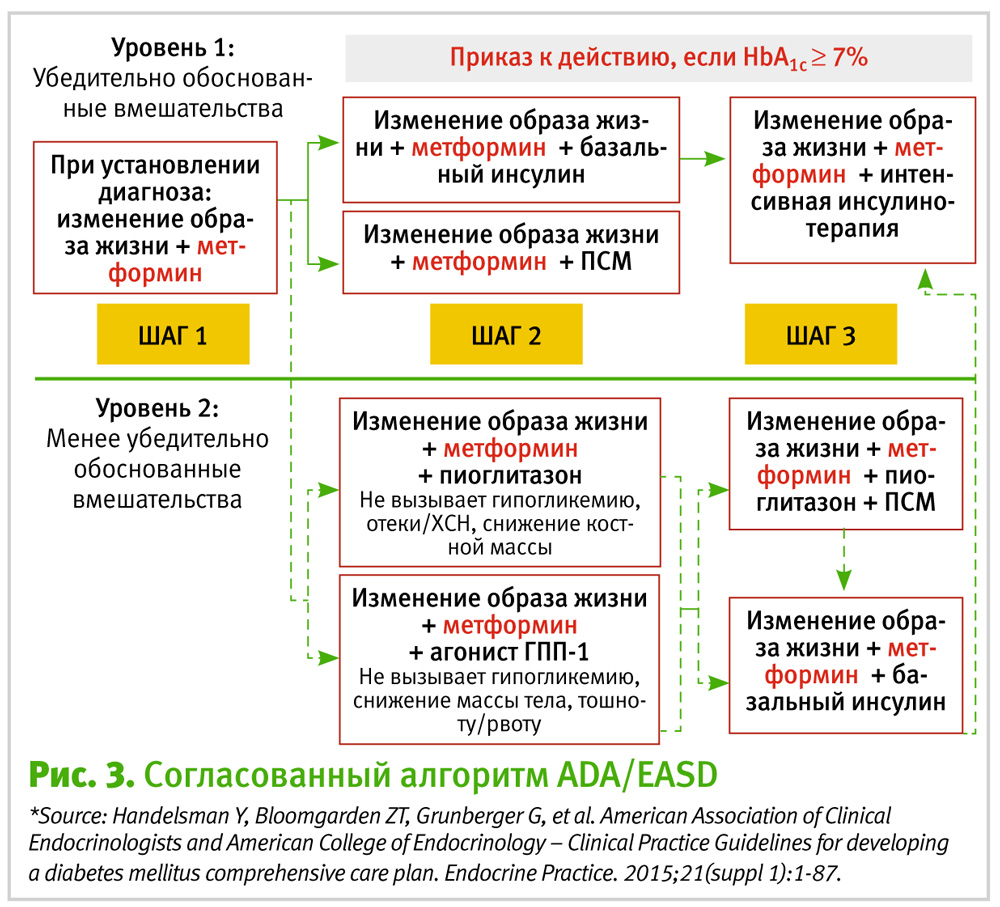

коментариев