
«План анестезии без плана последующей анальгезии является несостоятельным…» Jage J.
Проблема острой послеоперационной боли присутствует на протяжении всего времени существования хирургии и, к сожалению, не теряет своей актуальности. Почему так происходит? Возможно, потому что в раннем послеоперационном периоде перед врачом на первом месте стоят такие задачи как стабилизация гемодинамики, инфузионно-трансфузионная терапия, энтеральное и парентеральное питание, антибиотикотерапия. На этом фоне боль кажется второстепенной проблемой, неизбежной неприятностью, с которой можно смириться.
Такой подход привел к тому, что сегодня лечение острой послеоперационной боли не может быть признано адекватным, причем эта проблема актуальна не только для нашей страны.
По данным Национального центра статистики здравоохранения США, от острой послеоперационной боли ежегодно страдает более 4,3 миллионов американцев, 50% из них считают послеоперационное обезболивание неадекватным.
В 2010 г. в Германии прошло исследование качества послеоперационного обезболивания, участие приняли 25 клиник (2252 пациента). Данные были опубликованы в журнале Dtsch Arstebl Int, исследователи пришли к выводу, что боль средней и высокой интенсивности в покое испытывали 29,5% пациентов, а при активации – более 50%, при этом 55% всех пациентов не были удовлетворены качеством обезболивания [1].
В 2013 году вышла статья в журнале Anesthesiology «Pain Intensity on the First Day after Surgery». Проведена оценка боли в 1-е сутки после операции у более 50 тысяч пациентов из 105 клиник Германии. Авторы пришли к выводу, что как это ни удивительно, но самая высокая интенсивность боли была отмечена после операций «низкой» травматичности – холецистэктомии, аппендэктомии, геморроидэктомии и т. п. Травматичность этих операций недооценивается докторами, следовательно, пациентам уделяется мало внимания [2]. В этой же работе приводится рейтинг самых «болезненных» операций (самые высокие оценки послеоперационной боли для 174 хирургических вмешательств): 4-е место — открытая миомэктомия; 9-е место — кесарево сечение; 27-е — открытая субтотальная гистерэктомия; 57-е — операции по поводу внематочной беременности; 75-е — вагинальная гистерэктомия.
Для сравнения: 118-е — открытая резекция легкого, 120-е — гастрэктомия тотальная или субтотальная, 163-е — радикальная простатэктомия.
Можно сделать вывод, что тема послеоперационного обезболивания в гинекологии актуальна. Учитывая частоту оперативных вмешательств на матке, мы можем только представить масштабы этой проблемы.
Миома матки занимает около 30% в структуре всей гинекологической патологии. По данным D. Barlow (2010), гистерэктомия выполняется в 76,8% случаев диагностированной миомы матки, чаще у женщин в пременопаузе. Гистерэктомия – самое частое хирургическое вмешательство в США – 5:1000 населения в год (>500 000 операций в год); в Швеции – 2,1:1000 в год; в Дании – 1,8:1000 в год [3].
Неадекватный контроль боли в послеоперационном периоде:
- удлиняет период активизации пациентки и увеличивает время пребывания в ПИТ и стационаре;
- увеличивает частоту регоспитализаций;
- повышает риск и частоту инфекционных осложнений;
- резко повышает риск развития хронического болевого синдрома.
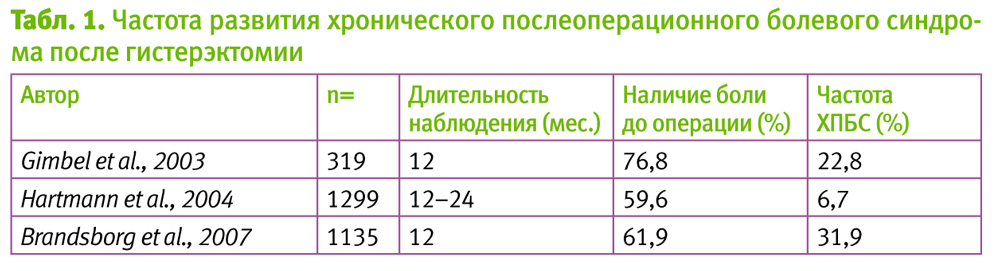
Острая послеоперационная боль может стать хронической, мы должны четко понимать эту связь: чем выше интенсивность боли в раннем послеоперационном периоде, тем выше вероятность ее хронизации!
Факторы риска хронического послеоперационного болевого синдрома:
1) наличие боли до операции;
2) молодой возраст;
3) женский пол;
4) травматичный хирургический доступ (повреждение значительного количества нервных волокон);
5) неадекватная анестезия во время операции;
6) неадекватное обезболивание в раннем послеоперационном периоде.
Большинство из перечисленных факторов риска хронизации боли присуще гинекологическим операциям.
Основные причины неадекватного обезболивания (Meissner W et al., 2001) [4]:
1) организационные проблемы 62,5%;
2) дефицит времени медперсонала 61,9%;
3) отсутствие мотивации 38,8%;
4) несоблюдение принципа мультимодального лечения боли 37,7%;
5) трудности оценки боли 37,0%;
6) недостаток знаний медперсонала 30,1%.
В данной статье мы поговорим только об одной причине неадекватного обезболивания в послеоперационном периоде, а именно несоблюдении принципа мультимодального лечения боли.
Мультимодальная аналгезия – предусматривает одновременное использование двух или более анальгетиков, обладающих различными механизмами действия и позволяющих достичь адекватного обезболивания при минимуме побочных эффектов [5]. Основой мультимодального подхода является применение совместно с перацетамолом, опиатами и НПВС методов региональной анальгезии.
Важнейшая роль тканевого воспаления в механизмах центральной сенситизации, а следовательно, и в формировании хронической боли является показанием для обязательного включения в схему лечения послеоперационной боли НПВП. За счет подавления воспалительного ответа на хирургическую травму НПВП препятствуют развитию сенситизации периферических ноцицепторов. Можно утверждать, что НПВП являются средствами патогенетической терапии боли (Овечкин А. М., 2000).
По данным опроса, проведенного независимой компанией в 2004 году среди врачей хирургических специальностей в ряде крупных городов Украины, наиболее часто назначаемым инъекционным анальгетиком для послеоперационного обезболивания является метамизол – 34% (анальнин). Второе место по частоте назначения (20%) занимает промедол. Для сравнения, аналогичный опрос, проведенный среди участников конгресса «Евроанестезия–2005» (Вена, июнь 2005 г.), дал следующие результаты: 1) морфин — частота назначения 73%; 2) парацетамол для внутривенного введения — 61%.
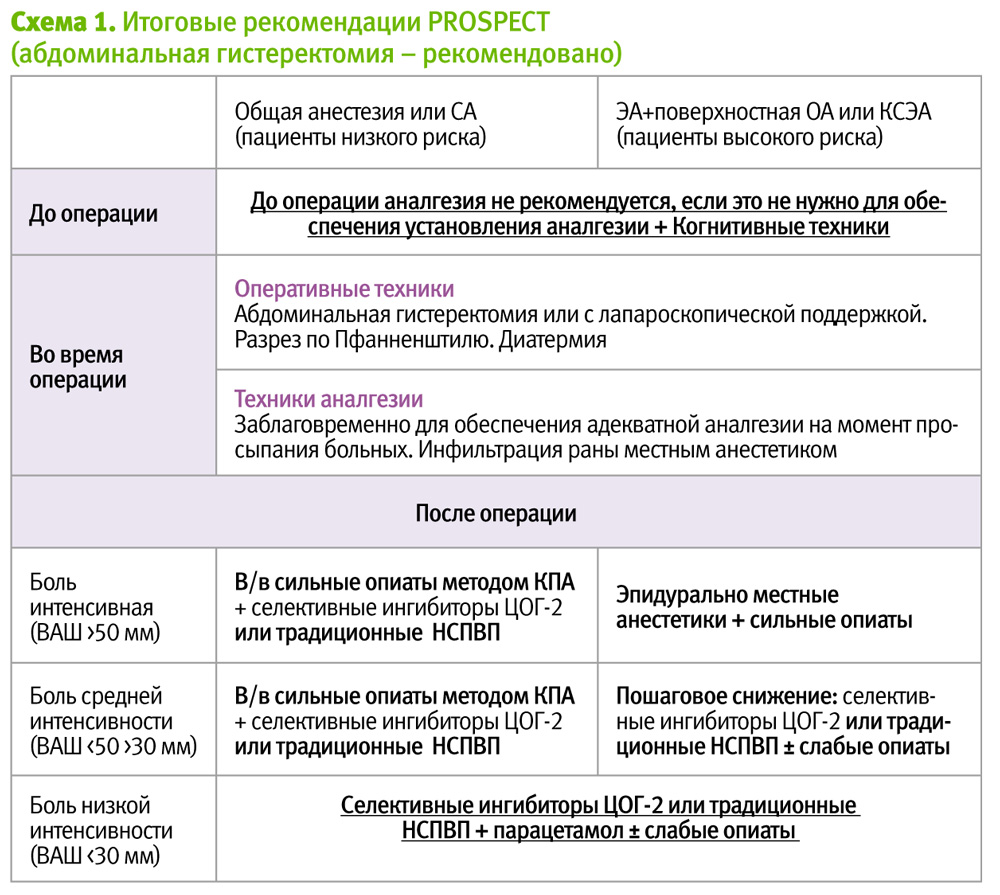
Рабочая группа PROSPECT (procedure specific postoperative pain management) – это уникальное сотрудничество хирургов и анестезиологов, возглавляемое профессором анестезиологом Francis Bonnet на основе систематизированных обзоров литературы (Cochrane protocol), Medline & EMBASE, 1966–2008, пришли к выводам, которые представлены в виде итоговых рекомендаций (схема 1).
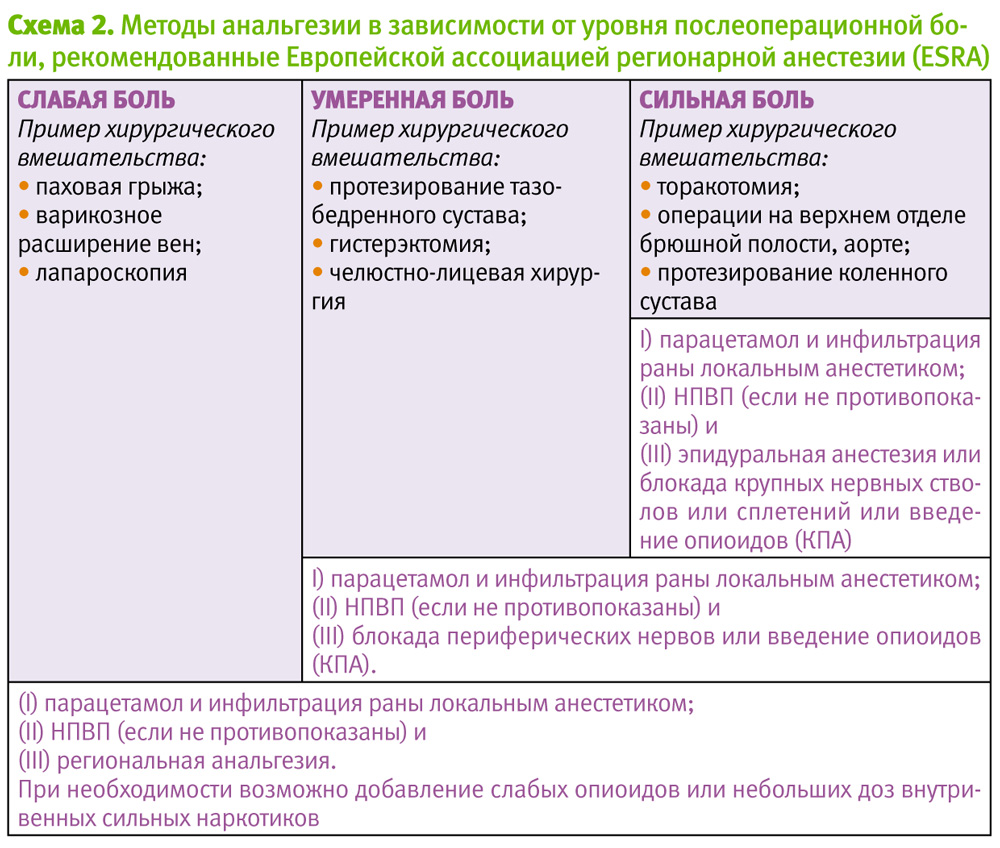
В послеоперационном периоде возможны различные варианты обезболивания в зависимости от вида анестезии, травматичности операции и течения послеоперационного периода. На схеме 2 представлены рекомендации Европейской ассоциации регионарной анестезии.
Обратите внимание, в рекомендациях Европейской ассоциации регионарной анестезии парацетамол рекомендуется при всех уровнях боли! Внутривенный парацетамол является эффективным препаратом для лечения острой боли (доказательства I уровня, Кокрановская база данных). Сочетание НПВП с парацетамолом повышает эффективность обезболивания (доказательства I уровня). Потребность в опиоиде на фоне базовой послеоперационной аналгезии парацетамолом снижается на 30–50% (рис. 1).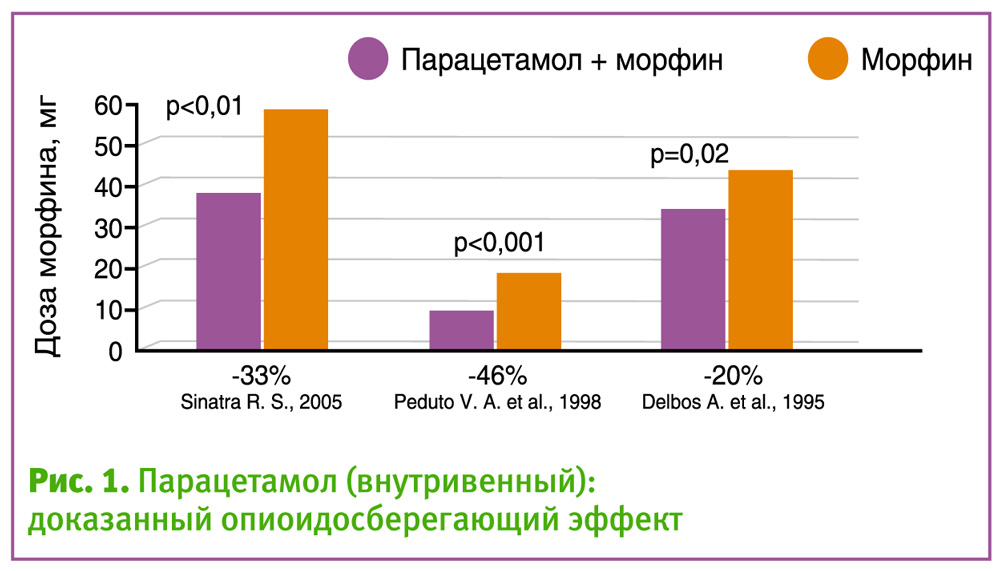
Механизм действия парацетамола отличается от НПВП. По сравнению с опиоидами и НПВП соответственно, парацетамол не имеет эндогенных рецепторов и практически не подавляет активность циклооксигеназы на периферии. Появляется все больше доказательств центрального антиноцицептивного эффекта парацетамола. Вероятные механизмы его включают: а) подавление активности ЦОГ-2 в ЦНС (профилактика развития вторичной гиперальгезии); б) подавление активности ЦОГ-3 (существование которой предполагается и которая, видимо, обладает селективной чувствительностью к парацетамолу); в) усиление активности нисходящих тормозных серотонинергических путей.
Парацетамол препятствует продукции простагландина на уровне клеточной транскрипции, т. е. независимо от уровня активности ЦОГ; является эффективным анальгетиком, потенциал которого лишь несколько уступает стандартным дозам морфина или НПВП.
С точки зрения патофизиологии острой боли оптимальным считается введение 1-й дозы НПВП за 30–40 минут до кожного разреза (принцип предупреждающей анальгезии, pre-emptive). Такая методика позволяет существенно снизить интенсивность боли и потребность в послеоперационном назначении опиоидных анальгетиков.
В настоящее время не существует идеального анальгетика или метода лечения острой послеоперационной боли.
Приблизиться к решению проблемы адекватности послеоперационного обезболивания можно лишь, реализуя в клинике концепцию мультимодальной анальгезии, предусматривающей одновременное назначение двух и более анальгетиков и/или методов обезболивания, обладающих различными механизмами действия и позволяющих достичь адекватной анальгезии при минимуме побочных эффектов. Мультимодальная анальгезия в настоящее время является методом выбора послеоперационного обезболивания. Ее базис — назначение неопиоидных анальгетиков (НПВП и парацетамол), которое у пациентов с болями средней и высокой интенсивности сочетается с использованием опиоидных анальгетиков и методов регионарной анальгезии. Выбор той или иной схемы мультимодальной анальгезии определяется травматичностью хирургического вмешательства.
Как работаем мы (операция – абдоминальная экстирпация матки, анестезия – севофлюран 2–2,5об% + фентанил):
- До операции: за 30–40 мин в/в НПВП, мы отдаём предпочтение декскетопрофену, также можно использовать кеторолак или лорноксикам.
- Во время: за 30 мин до окончания в/в 1 г парацетамола в течение 15 мин.
- После: базисный препарат – внутривенный парацетамол, в суточной дозе до 4 г. Если обезболивания недостаточно, то назначается НПВП (50 мг каждые 8–12 ч.). При отсутствии необходимого эффекта мы применяем опиоидные анальгетики (морфин).
Цель, которую мы преследуем: пациентка должна проснуться после операции без боли (ВАШ не больше 3).
Выводы
- Для уменьшения частоты побочных эффектов опиоидов и НПВП целесообразно использовать принципы мультимодальной аналгезии.
- Использование pre-emptive аналгезии потенцирует действие средств для наркоза и уменьшает потребность в опиоидах в п/о периоде.
- Регионарная анестезия в том или ином варианте (инфильтрация краев раны, блокада нервов и сплетений, спинальная или эпидуральная анестезия) должна присутствовать в обязательном порядке.
- Парацетамол – обязательный компонент мультимод



коментарів