
ПРИРОДНОЕ РЕШЕНИЕ СЕРЬЕЗНЫХ ЖЕНСКИХ ПРОБЛЕМ
Уважаемые коллеги! Нам посчастливилось жить в эпоху перемен и прогресса. Однако каждый день Вы можете наблюдать истинные последствия нашего прогресса — «настоящую эстрогеновую женщину с избытком веса и женской красоты и букетом дисгормональных нарушений». Естественно, мы обсуждаем вопросы лечения с нашими пациентами, стараемся прислушаться к их пожеланиям. В первую очередь говорим об оптимизации образа жизни как о главном лечебном факторе. Ставим во главу угла безопасность назначаемых препаратов и удобство их использования. Однако очень часто забываем о наших добрых, проверенных веками помощниках — лекарственных растениях, которые заслуживают почетное место в терапии дисгормональных нарушений, особенно в репродуктивном периоде женщины.

Наиболее частой причиной снижения или утраты фертильности являются доброкачественные гормонозависимые заболевания репродуктивной системы женщины (мастопатия, миома матки, эндометриоз, гиперплазия эндометрия, кистозные новообразования яичников), стремительно распространяющиеся среди популяции и охватывающие всё более молодые возрастные группы. Пролиферативные заболевания гениталий занимают второе место в структуре гинекологической заболеваемости, уступая первенство лишь воспалительным процессам. На сегодняшний день не существует единого подхода к интерпретации этиологических и патогенетических факторов риска развития дисгормональных новообразований, причин может быть множество:
- нарушения в работе гипоталамо-гипофизарной системы;
- нарушения выработки гормонов щитовидной железой, яичниками, надпочечниками;
- иммунный дисбаланс;
- генетическая предрасположенность;
- метаболические нарушения;
- аутопаракринные нарушения и нарушения регуляции ангиогенеза;
- нарушения запрограммированной гибели клеток (процессов апоптоза);
- местные воспалительные или травматические изменения;
- нарушения функции печени и т.д.
Все вышеперечисленные факторы приводят к диссонансу в работе гипоталамо-гипофизарно-яичниковой системы в организме женщины с исходом формирования абсолютной или относительной гиперэстрогении на фоне снижения концентрации прогестерона. Общность патогенеза подтверждается и тем, что у одной пациентки достаточно часто одновременно выявляются сразу несколько дисгормональных проблем. Так, ДЗМЖ в 60–90% случаев сочетаются с лейомиомой матки, эндометриозом, гиперплазией эндометрия и и другими дисгормональными состояниями женской репродуктивной сферы.
Дисбаланс женских половых гормонов обеспечивает пролиферативные процессы в эндометрии и в железистой ткани молочных желез. Дефицит прогестерона может быть обусловлен нарушением процессов овуляции, а к относительному избытку различных фракций эстрогенов приводят и сбои в метаболизме половых стероидов. Например, при гиперандрогенном синдроме, ожирении мы можем наблюдать истинную эстрогенемию, поскольку андрогены под влиянием ароматазы превращаться в эстрон. Также еще одним из этиологических факторов гиперэстрогении является нарушение функции печени, где происходит распад эстрогенов вследствие конъюгации их с глюкуроновой кислотой. Нарушение утилизации эстрогенов в печени приводит к хронической гиперэстрогении и тем самым способствует развитию гиперпластических процессов.
В действительности синдром абсолютной эстрогенной доминантности встречается достаточно редко, и чаще всего в гинекологической практике мы сталкиваемся с синдромом относительной эстрогенизации.
Однако в последнее время научными исследованиями доказано, что решающая роль в возникновении гиперпролиферативных гинекологических заболеваний принадлежит не абсолютной концентрации гормонов в плазме крови, а состоянию рецепторов в органах репродуктивной системы женщины. Ведь известно множество ситуаций, когда на фоне высокого уровня эстрогенов, прогестерона или пролактина в плазме крови, женщины были абсолютно здоровыми, и, наоборот, при обнаружении каких-либо новообразований уровень гормонов в кровяном русле не превышал предельно допустимые цифры. Но неоспоримым является факт, что количество гормональных рецепторов в репродуктивных органах коррелирует с пролиферативной активностью, а преобладание числа эстрогеновых рецепторов над прогестероновыми следует считать маркером канцерогенеза. Так, даже гиперпролактинемия вызывает ДЗМЖ путем увеличения количества эстрогеновых рецепторов в ткани молочной железы, что провоцирует пролиферацию и развитие мастопатии.
Исходя из этого, следовало бы каждой женщине с гипепролиферативными процессами определить состояние рецепторного аппарата в пораженном органе и назначить соответствующую терапию. Но мы с вами знаем, что ни один этический комитет не позволит нам произвести оперативную диагностику при диффузном процессе, а в тех ситуациях, когда есть прямое показание для биопсии, не всегда удается выполнить данную манипуляцию из-за материального положения пациенток или технического оснащения лечебного учреждения. Поэтому традиционно лечение дисгормональных гиперпролифертивных заболеваний, строго регламентированное приказами МОЗ Украины №676 от 31.12.2004 и №582 от 15.12.2003, базируется на применении «тяжелой артиллерии» — гормональных препаратов. Понятно, что оба приказа требуют обновления в связи с появлением новых научных исследований и новых фармакологических средств, но говорить о некоем золотом стандарте лечения мы вряд ли сможем даже после пересмотра этих протоколов. Ведь в действительности, несмотря на общность патогенеза, лечебная тактика всегда будет зависеть от множества дополнительных факторов:
- возраста женщины;
- ее репродуктивных планов;
- наличия сопутствующей соматической патологии;
- клинической симптоматики и степени ее выраженности;
- месторасположения, размеров и других характеристик лейоматозных узлов или эндометриоидных очагов, или кист и т.д.;
- личных убеждений женщины относительно допустимости и приемлемости тех или иных методов и форм лечения.
Исходя из данных об огромной причастности эстрогеновых рецепторов в развитии пролиферативных процессов в женском организме, казалось бы, огромный потенциал имеют антиэстрогенные препараты — SERM, действующие как тканеспецифические антагонисты эстрогена: тамоксифен (Там) и торемифен (Тор). Однако их применение ограничено серьезными побочными эффектами со стороны внутренних органов и неблагоприятными последствиями для здоровья женщины, поэтому они используются в основном только для лечения злокачественных гормонозависимых опухолей. Единственным оружием в руках гинеколога в отношении гиперпролиферативных процессов остаются синтетические гестагены и ГнРГ. Но самая большая проблема, связанная с гормональной терапией, заключается в том, что у большинства пациенток достигнутый в относительно короткие сроки успех от ее применения после отмены препаратов сменяется столь же быстрым появлением рецидива заболевания, что вынуждает врачей проводить многократные курсы терапии или прибегать к оперативному лечению. Особенно часто рецидивирование гиперпластических заболеваний репродуктивной сферы наблюдается в том случае, когда у женщины имеется не одна, а сразу несколько таких патологий, то есть тогда, когда ей ставится диагноз «гиперпластический синдром».
Фармацевтический прогресс — это прекрасно, но иногда важно остановиться, оглянуться и понять, что сама болезнь может быть вызвана спецификой современной жизни. Не зря появился термин «болезни цивилизации». Не исключено, что дисгормональные пролиферативные процессы — заболевания из этого ряда. Именно болезни цивилизации лучше других поддаются лечению простыми вещами: сменной образа жизни, питания, физической активности, фитотерапией и т.д. Обязательное условие — сама пациентка должна захотеть изменить свою жизнь.
Исходя из сложившихся к настоящему времени представлений о природе пролиферативных заболеваний, нормализация гормонального гомеостаза заключается в:
- приведении в равновесие эмоциональной сферы;
- стабилизации метаболических процессов в клетках;
- поддержании на должном уровне работы иммунной системы;
- поддержании полноценного функционирования печени и т.д.
Не следует сразу же прибегать к синтетической гормональной коррекции, следует попробовать возможности природного восстановления гормонального равновесия или хотя бы их сочетание, с минимальным вмешательством гормональных препаратов. Если обратиться к истокам медицинских знаний, то использование смесей лекарственных трав уходит корнями в вековую историю, и такой «комплексный» способ помощи больным доказывал свою дееспособность на протяжении многих тысячелетий.
Фитотерапия завоевала сердца украинских женщин своей безопасностью, отсутствием неприятных побочных эффектов, возможностью совместить в одном флаконе несколько эффектов. Особое место среди таких лекарственных средств занимает наш отечественный лекарственный препарат комплексного действия Tazalok™, который доказал свою эффективность в лечении гиперполиферативных дисгормональных заболеваний. Именно этот препарат всесторонне изучался в ведущих клиниках Украины и подтвердил свою высокую эффективность в лечении предменструального синдрома, дисменореи, ДЗМЖ, гиперплазии эндометрия. Tazalok™ также показал высокий профиль безопасности и был отмечен пациентками как удобный в применении.
Tazalok™ содержит смесь лекарственного растительного сырья нашего ареала: корень лабазника шестилопастного, свежий корень петрушки кудрявой, свежий корень сельдерея, траву подмаренника настоящего, траву ленка настоящего и цветки календулы. Каждый растительный компонент обладает собственной гаммой полезных свойств, однако в целом вся комбинация дарит препарату поистине уникальные эффекты.
Особое открытие прошлого года — подтверждение антиэстрогенной и антипролиферативной активности Tazalok™ в исследовании профессора А. Г. Резникова. Полученные данные позволяют назвать Tazalok™ природным антиэстрогенным препаратом (фито-SERM) и могут объяснить один из механизмов его действия относительно нормализации эстроген-прогестинового равновесия в организме женщины.
Однако не следует забывать, что Tazalok™ оказывает комплексное действие, которое обусловлено синергическими эффектами входящих в его состав селективных фитомолекулТМ: нормализует ритмичность секреции и соотношение гонадотропных гормонов, регулирует лютеиновую фазу, устраняет гормональный дисбаланс между эстрадиолом и прогестероном, оказывает выраженное действие на ткани молочной железы, яичников, матки, проявляет антипролиферативные и противовоспалительные свойства, снижает продукцию простагландинов и устраняет мышечный спазм, способствует размягчению капсулы кистозных образований и снижению их напряжения за счет активной резорбции содержимого кист, обладает выраженным противоотечным действием.
Благодаря такому мультифакторному воздействию практически на все возможные звенья патогенеза дисгормональных пролиферативных состояний, мягкому и безопасному воздействию на организм женщины, Tazalok™ влияет как на причину заболевания, так и на симптомы, и может быть рекомендован как монотерапия или в составе комплексного лечения большинства заболеваний женской половой сферы. В очередной раз спираль развития науки обращается к силе растений во имя здоровья Женщины.


БЕЗОБЛАЧНЫЙ РАССВЕТ НОВОЙ ЖИЗНИ
Говорят, что у счастливой женщины два имени – Любимая и Мама. Что же делать, когда на пути к рождению долгожданного маленького чуда, единственная улыбка которого может украсить любой пасмурный день, возникают трудности и преграды? Как можно получить уникальную должность, не предполагающую перерывов на обед, отпуск и плохое настроение, но приносящую радость, – право быть мамой?
В настоящее время выделяют множество причин невынашивания беременности (НБ) и преждевременных родов (ПР): стресс, курение, ожирение или низкая масса тела, вагинальное кровотечение, инфекционные заболевания, дефицит прогестерона, прием оральных контрацептивов за 30 дней до зачатия, депрессия и др.
В исследовании Poston (2009) было установлено, что у женщин с низким уровнем прогестерона в слюне в период между 24-34-й неделями беременности повышался риск ПР. Кроме того, значимое снижение концентраций указанного гормона в слюне выявлялось у 100% пациенток, роды у которых произошли до 34-й недели.
Прогестерон неоспоримо является главным гормоном беременности, с помощью которого женщины на протяжении всей истории человечества вынашивали плод. В настоящее время не вызывает сомнений целесообразность нормализации уровня прогестерона во всех клинических ситуациях, сопровождающихся дефицитом данного гормона: прогестероновая недостаточность не только создает предпосылки для НБ и ПР, но и обусловливает повышение риска развития рака молочной железы, тромбоэмболий у матери, а также может иметь негативные последствия для здоровья новорожденного.
Выделяют натуральные и синтетические гестагены.
К натуральным (идентичным эндогенному гормону) относится прогестерон в любой лекарственной форме, в том числе микронизированный прогестерон, масляный раствор прогестерона, все остальные являются синтетическими, так как они не идентичны эндогенному прогестерону, их формула изобретена, такое вещество не синтезируется в организме женщины во время или вне беременности.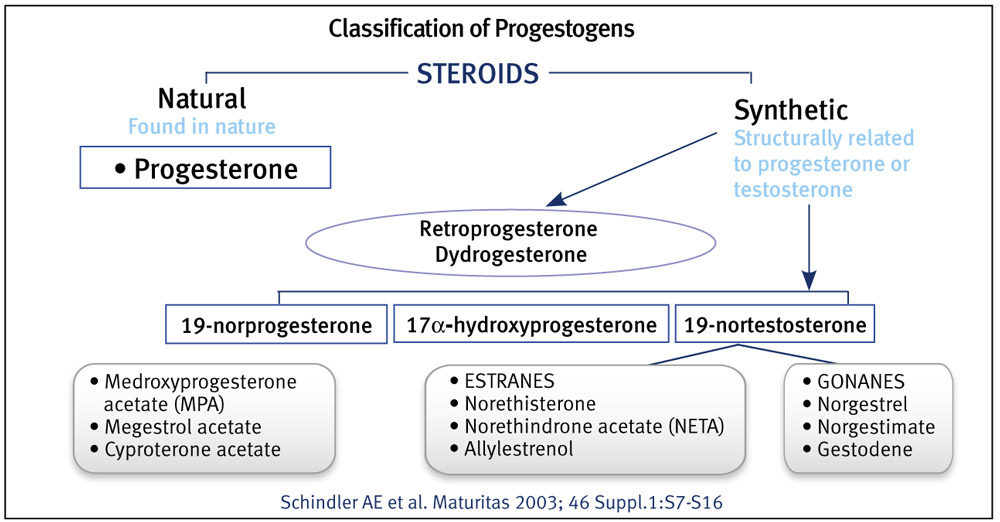
Прошлое: ошибки, о которых хочется забыть, – это опыт, который следует учесть
Беременность – это состояние, требующее максимально взвешенной и объективной оценки возможных рисков и преимуществ назначения лекарственных средств, поскольку на кону не только здоровье будущей мамы, но и жизнь малыша. Истории известен не один печальный пример последствий приема непроверенных лекарственных препаратов.
Одним из наиболее трагичных событий ХХ века стала так называемая талидомидная катастрофа. Менее чем за 6 лет вследствие применения беременными женщинами талидомида, позиционировавшегося как «безопасный снотворный препарат», на свет появились более 8 тыс. детей с тяжелыми пороками развития (отсутствием верхних и нижних конечностей, ушных раковин, дефектами глаз и мимической мускулатуры), психическими нарушениями (аутизмом, эпилепсией, замедлением умственного развития и др.). По данным W. Lenz, около 40% детей не дожили до своего первого дня рождения. Впоследствии выяснилось, что для возникновения тяжелейших аномалий у ребенка было достаточно приема будущей мамой 1 таблетки талидомида в I триместре беременности.
Второй волной «шоковой терапии» для человечества стали отдаленные последствия рутинного использования в акушерской практике диэтилстильбэстрола для здоровья новорожденных: спустя 16-20 лет у девушек, рожденных матерями, во время беременности принимавшими данный препарат, возникали злокачественные опухоли влагалища и шейки матки, влагалищный аденоматоз, у юношей наблюдались тяжелые нарушения сперматогенеза, гипоплазия и индурация капсул яичек, кисты придатков яичек. За период с 1948 по 1971 г. только в США диэтилсильбэстрол получили около 3 млн беременных, в Европе их количество составило 4 млн.
Парадоксально, но именно препарат, о способности которого «предупреждать аборт, выкидыш и преждевременные роды» и «возможности принимать для профилактики во время беременности» гласили рекламные слоганы, стал, по образному выражению специалистов, «медицинским кошмаром» и «бомбой замедленного действия с часовым механизмом» и привел к возникновению новой нозологии – ранее в перечне известных заболеваний рак влагалища не фигурировал. Точное число пострадавших неизвестно, приблизительные масштабы трагедии можно оценить на примере Бостона: здесь было зарегистрировано 380 случаев возникновения нарушений, ассоциированных с приемом указанного лекарственного средства.
Детей, рожденных от матерей, получавших аллилэстренол (туринал) в 1980-1990 г., называют туриналовым поколением. Последствия приема этого препарата обозначают понятием «функциональный тератогенез»: у многих из появившихся на свет без видимых отклонений детей по достижению половой зрелости возникли нарушения со стороны нервной системы (необъяснимая безосновательная агрессия, раздражительность и др.), репродуктивной системы (поликистоз, бесплодие), расстройства психики (поведенческие аномалии), нарушения слуха и зрения. Самое удивительное, что и сейчас, введя в поисковик слово «туринал», можно обнаружить в его показаниях угрожающий аборт и четко прописанную схему дозирования. Но еще больше можно найти огромное количество форумов, на которых матери, принимавшие аллилэстренол во время беременности, делятся своими проблемами и задают вопросы врачам, на которые сложно ответить.
 Настоящее: не нужно создавать проблемы завтра, используя препараты с недоказанной долгосрочной безопасностью сегодня
Настоящее: не нужно создавать проблемы завтра, используя препараты с недоказанной долгосрочной безопасностью сегодня
Можно понять женщину, имеющую в анамнезе несколько случаев НБ, в своем желании стать мамой. «Я готова на все», – говорит она лечащему врачу. Однако не слишком ли высока цена подобной беспечности и неосторожности в использовании препаратов для сохранения беременности? Можно ли избежать безальтернативных решений? Какими возможностями компромисса располагает современная медицина?
О том, каких принципов следует придерживаться при назначении гестагенов в настоящее время, рассказывает доцент кафедры клинической фармакологии, фармакотерапии и скорой медицинской помощи Московского государственного медико-стоматологического университета (РФ), кандидат медицинских наук Елена Ивановна Вовк.
– Когда гестагены были синтезированы, казалось, что наконец-то медицина получила настоящую панацею от лютеиновой недостаточности. Тем не менее, по мере развития и усовершенствования технологий пришло осознание, что препараты этого класса – не только не панацея, но и далеко не самый оптимальный метод лечения указанной патологии.
Таким образом, синтетические гестагены – это некий компромисс для женщин, когда существовала только масляная форма прогестерона и не было других альтернатив его применения.
За прошедшие десятилетия технологии по производству препаратов прогестерона пережили настоящую революцию, разработка микронизации прогестерона предоставила человечеству возможность выбора. Благодаря инновационной форме микронизированного прогестерона у врачей и женщин появилась возможность использовать натуральный прогестерон в виде капсул, которые могут применяться как перорально, так и интравагинально, а широкий спектр синтетических гестагенов оставить для применения в гинекологической практике.
В настоящее время накоплены доказательства эффективности и прогестерона, и синтетических гестагенов. Вопрос безопасности в отношении прогестерона менее актуален, поскольку препарат эквивалентен эндогенному гормону, однако касательно гестагенов он стоит достаточно остро. Почему? С фармакологической точки зрения синтетические гестагены – это вещества с иным строением молекулы, с высоким сродством к рецепторам, что значимо изменяет систему сигнальной информации по отношению к стероидам в каждой клетке организма – не только в матке, но и в печени, центральной нервной системе.
В специальной литературе встречаются данные, свидетельствующие, что применение синтетических гестагенов увеличивает андрогенную стимуляцию плода, представляющую особенно актуальную проблему для плода женского пола. Второй момент гораздо ближе к понятным для практического врача терминам: применяя синтетические гестагены, не имея всей суммы метаболитов эндогенного прогестерона, мы не получаем нейропротекторного и анксиолитического действия, так как прогестерон является предшественником ряда нейростероидов в головном мозге, так необходимых для физиологического сохранения беременности.
Кроме того, в отличие от натурального прогестерона, гестагены не позволяют контролировать стимуляцию организма матери ее собственными андрогенами, избыток которых при беременности приводит к таким тяжелым последствиям как гестационная гипертензия и сахарный диабет.
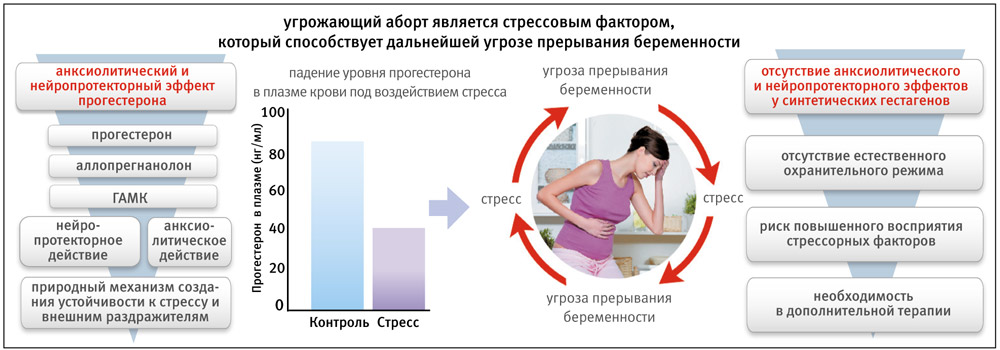
Угроза прерывания беременности сама по себе – мощный стрессовый фактор, который является ведущей причиной НБ. Роль прогестерона во время беременности – создание повышенного порога устойчивости к стрессовым факторам и нейтрализация обусловленного стрессом высокого тонуса матки. Микронизированный прогестерон, как аналог природного, обладает выраженным токолитическим действием и, в отличие от синтетических гестагенов, накопил огромный зарубежный опыт и доказательную базу в профилактике преждевременных родов, войдя в международные протоколы. Замещение прогестерона гестагенами, не имеющими важных природных метаболитов, также не способно обеспечить необходимое для сохранения беременности нейропротекторное и анксиолитическое действие и, безусловно, увеличивает риск прерывания беременности на поздних сроках, поскольку женщина, нервная система которой не находится в состоянии охранительного торможения, не может обеспечить плоду полный физиологический покой.
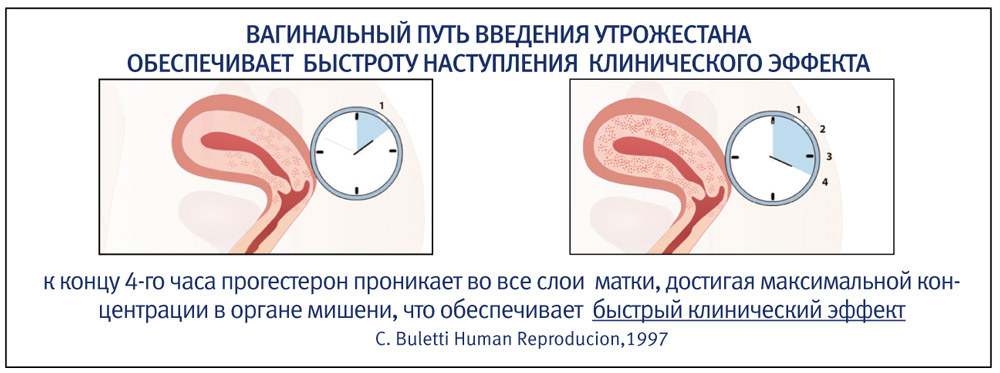
У синтетических гестагенов существует еще одна важная для беременности особенность – у них нет характерной для прогестерона природной антиальдостероновой активности. На фоне терапии гестагенами из организма беременной женщины плохо выводится избыточный натрий – еще одна причина для задержки жидкости и высокого риска гестационной гипертензии.
Таким образом, очевидно, что безопасность применения гестагенов для сохранения беременности не может соответствовать требованиям современной медицины, и мне не понятно, почему некоторые врачи до сих пор стоят перед выбором: какой препарат назначить – гестаген или прогестерон, который оказывает эффективное и безопасное сохраняющее действие на беременность и ограждает организм будущей мамы от осложнений беременности. Зачем нужно сомневаться в выборе, если мы можем обеспечить адекватную и физиологичную поддержку беременности, применяя микронизированный прогестерон? Зачем, имея в арсенале безопасный и действенный препарат, обеспечивающий физиологическое течение беременности, «обкрадывать» организм и матери, и плода по всей совокупности положительных эффектов прогестерона?
Общая идеология современного здравоохранения по сравнению с таковой в 1980-е годы радикально изменилась. Сегодня специалисты в меньшей степени ориентируются на эффективность (эффективных молекул много) – на первый план выходит вопрос безопасности эффективных средств. Именно безопасность лекарственного средства должна стать приоритетом, предопределяющим наш выбор в каждом конкретном случае, требующем обеспечения гормональной поддержки лютеиновой недостаточности. С этой точки зрения тактики использования синтетических гестагенов для поддержания беременности нам нужно оставить в ХХ веке. В ХХI веке врачи имеют возможность использовать безопасные лекарственные средства, в частности микронизированный прогестерон Утрожестан.
Классик медицины Парацельс писал: «Природа терпелива, она прощает многое, что человек по неразумению своему делает во вред своему здоровью, но терпение природы небезгранично». Я хочу призвать специалистов не создавать проблем для будущих поколений. Помните: применяя лекарства с недоказанной долгосрочной безопасностью сегодня, вы оставляете будущим мамам и их детям меньше шансов на здоровое завтра.
Будущее – результат наших усилий
Очевидно, что при выборе терапии для сохранения беременности желательно применение лекарственных средств, максимально приближенных к молекулам, синтезирующимся в организме беременной, таких как Утрожестан (Besins Healthcare) – натуральный микронизированный прогестерон. Среди преимуществ препарата выделяют:
- быстрое наступление клинического эффекта;
- адресную доставку прогестерона в орган-мишень (матку);
- наличие перорального и вагинального путей введения;
- возможность применения на этапах прегравидарной подготовки, угрожающего аборта и преждевременных родов.
Кроме того, Утрожестан -- единственный прогестерон в Украине, разрешенный для применения в третьем триместре беременности.
По материалам газеты «Здоровье Украины»
Детальніше
ВІД ПОЛІТИКИ ДО ПРАКТИКИ: дослідження процедури тестування на ВІЛ-інфекцію вагітних жінок в Україні
 Станом на 1 січня 2011 року в Україні було офіційно зареєстровано понад 182 000 випадків ВІЛ-інфекції серед громадян України, у тому числі 37 000 захворювань на СНІД , у тому числі 21 000 випадків смерті від захворювань, зумовлених СНІДом. За підрахунками експертів, в Україні проживає близько 360 тисяч людей, віком від 15 років і старше, інфікованих ВІЛ. Цей показник є одним з найвищих в європейському регіоні і на початок 2010 року становив 1,33% дорослого населення. Позаяк кількість випадків передачі ВІЛ-інфекції гетеросексуальним шляхом зростає (45% від усіх випадків передачі в 2010), відповідно, частка жінок серед усіх ВІЛ-позитивних осіб зростає теж і становить 44%. У цій ситуації в Україні було схвалено законодавчі норми стосовно планового тестування на ВІЛ-інфекцію вагітних жінок у період медичного обстеження до пологів. Досі не зрозуміло, наскільки ці нормативні документи виконуються на практиці та забезпечується захист прав жінок.
Станом на 1 січня 2011 року в Україні було офіційно зареєстровано понад 182 000 випадків ВІЛ-інфекції серед громадян України, у тому числі 37 000 захворювань на СНІД , у тому числі 21 000 випадків смерті від захворювань, зумовлених СНІДом. За підрахунками експертів, в Україні проживає близько 360 тисяч людей, віком від 15 років і старше, інфікованих ВІЛ. Цей показник є одним з найвищих в європейському регіоні і на початок 2010 року становив 1,33% дорослого населення. Позаяк кількість випадків передачі ВІЛ-інфекції гетеросексуальним шляхом зростає (45% від усіх випадків передачі в 2010), відповідно, частка жінок серед усіх ВІЛ-позитивних осіб зростає теж і становить 44%. У цій ситуації в Україні було схвалено законодавчі норми стосовно планового тестування на ВІЛ-інфекцію вагітних жінок у період медичного обстеження до пологів. Досі не зрозуміло, наскільки ці нормативні документи виконуються на практиці та забезпечується захист прав жінок.
З метою вивчення цих питань HealthRight у період з жовтня 2009 по червень 2010 року провів практичне дослідження щодо досвіду жінок, які проходили тестування на ВІЛ протягом періоду вагітності в одній із областей України, що має один з найвищих рівнів поширеності ВІЛ-інфекції. Компоненти дослідження: 1) проведення напівструктурованих інтерв’ю з 25 медичними працівниками та 60 вагітними жінками, які проходили тестування протягом останніх 60 днів; 2) глибинні інтерв’ю зі збором свідчень 30 ВІЛ-позитивних жінок про їхній досвід протягом року після тестування на ВІЛ у період вагітності.
Головні висновки інтерв’ю з вагітними жінками:
- Інформована згода. Більшість жінок (68%) повідомили про те, що вони заповнювали та підписували форму про надання згоди на проходження тестування на ВІЛ. Проте 18% жінок повідомили про свою усну, а не письмову згоду. Певна кількість жінок не мали чіткого уявлення, на що вони погоджуються.
- Добровільність тестування. Не зважаючи на процедуру поінформованої згоди, лише 53% жінок розуміли, що тестування є добровільним; на додаток, декілька жінок висловили відчуття, що насправді вони не мали вибору щодо проходження тестування через відповідну практику медичних закладів.
- Конфіденційність інформації. Майже чверть жінок (23%) повідомили, що їхнє тестування на ВІЛ або наступне повідомлення про/використання результатів тесту було проведено в умовах, які порушували процедуру конфіденційності. У той час, як більшість повідомляли, що їх особисто не турбувало питання конфіденційності, деякі ВІЛ-позитивні жінки описували ситуації, коли результати тесту надавалися роботодавцю або повідомлялися медичними працівниками іншим медичним працівникам та/або пацієнтам.
- Якість та зміст консультування. Якість та зміст консультування значно відрізнялися серед опитаних жінок. Тільки у 20% запитали під час передтестового консультування, чи був у них досвід ризикованої поведінки, та тільки у 5% – під час післятестового консультування. Проте жінки повідомляли, що загалом вони були задоволені консультуванням перед проходженням тесту. Післятестове консультування для жінок, які отримали ВІЛ-негативний результат, було мінімальним. Натомість, певна кількість ВІЛ-позитивних жінок повідомляли про стан шоку після отримання результатів та неспроможність засвоїти багато інформації стосовно наступних кроків та направлень до інших закладів.
- Стигма та дискримінація, пов’язана з ВІЛ-позитивним статусом. Чотири з семи опитаних ВІЛ-позитивних жінок описували свій досвід, коли вони зіштовхувалися з проявами стигми та дискримінації у закладах охорони здоров’я після отримання ними позитивного статусу. Три жінки повідомили про те, що їм порадили перервати вагітність. Декілька жінок описали, як вони спостерігали чи зазнавали дискримінаційного або принижуючого поводження під час переймів та пологів з огляду на ВІЛ-позитивний статус.
- Оплата послуг. Декілька жінок повідомляли про те, як їх просили оплатити послуги чи медичні засоби, які мали б бути безкоштовними під час тестування на ВІЛ протягом вагітності.
- Перенаправлення. Тільки 53% жінок була надана інформація про місцеві СНІД-центри чи організації, що надають послуги ЛЖВ.
Головні висновки інтерв’ю з медичними працівниками:
- Інформована згода, добровільність та конфіденційність. Здебільшого медичні працівники були одностайними у своїх твердженнях щодо дотримання практики отримання поінформованої згоди, захисту конфіденційності, надання консультацій тощо. Водночас медичні працівники висловили змішані почуття, чи взагалі є доречним розголошувати ВІЛ-статус пацієнта іншим особам.
- Повідомлення про ВІЛ-позитивний статус. Частина медичних працівників (17%) відчували дискомфорт у ролі консультанта, особливо у випадку, коли мали повідомити пацієнта про позитивний результат тестування на ВІЛ.
- Ресурси. Усі медичні працівники скаржилися на недостатню кількість часу для надання детальних консультацій пацієнтам під час тестування на ВІЛ і зазначали про брак інформаційних матеріалів для поширення серед пацієнтів.
- Перенаправлення. Медичні працівники з великих міст зазначали, що вони мало знають про організації, в які можна перенаправляти ВІЛ-позитивних жінок для отримання подальших послуг та підтримки, в той же час медичний персонал із невеликих міст про такі організації знав краще.
Згідно з висновками дослідження, припускається, що більшості з жінок послуги з консультування та тестування на ВІЛ були запропоновані на рівні мінімальних вимог українського законодавства. Розбіжності між давнішими свідченнями та більш нещодавніми інтерв’ю дають підстави стверджувати, що практичні процеси щодо тестування на ВІЛ і лікування ВІЛ-позитивних вагітних жінок продовжують поліпшуватися в Україні. Проте обидві сукупності висновків вказують на те, що можна зробити значно більше для захисту прав вагітних жінок під час і після тестування на ВІЛ для забезпечення доступу ВІЛ-позитивним жінкам до послуг з підтримки з метою захисту їхнього здоров’я та добробуту як протягом періоду вагітності, так і після пологів.
Результати даного дослідження вказують на потребу покращення надання послуг, а також на потребу адвокаційних заходів задля забезпечення практичного виконання законодавства та зменшення стигми й дискримінації в Україні.
Повна версія звіту за дослідженням доступна на сайті www.healthright.org.ua
Детальніше
ДОПОМІЖНІ РЕПРОДУКТИВНІ ТЕХНОЛОГІЇ: НОВІ ОБМЕЖЕННЯ
21 лютого 2012 року Верховною Радою України прийнято в першому читанні проект Закону України про внесення змін до деяких законодавчих актів України щодо обмежень у використанні допоміжних репродуктивних технологій (реєстр. № 8282).
Законопроектом передбачається внесення змін до статті 123 Сімейного кодексу України від 10.01.2002 № 2947-III та статті 48 Закону України «Основи законодавства України про охорону здоров’я» від 19 листопада 1992 р. № 2801-ХІІ.
Так, із прийняттям вказаного законопроекту планується ввести наступні обмеження у використанні допоміжних репродуктивних технологій:
- Вік повнолітньої жінки, щодо якої застосовується штучне запліднення та імплантація ембріона, не повинен перевищувати 49 років на день перенесення ембріонів. У виключних випадках вікове обмеження для жінки може бути збільшено на підставі висновку комісії, утвореної органом центральної виконавчої влади у сфері охорони здоров’я.
- Допоміжне (сурогатне) материнство може здійснюватись лише іноземним громадянам тих країн, де ця процедура дозволена законодавством.
- Умовами проведення допоміжного (сурогатного) материнства є відсутність безпосереднього генетичного зв’язку дитини з допоміжною (сурогатною) матір’ю та генетичний зв’язок принаймні з одним із майбутніх батьків.
Редакція журналу «З турботою про Жінку» звернулась до Миколи Леонідовича Аряєва, чл.-кор. НАМН України, д. м. н., професора, проректора Одеського національного медичного університету, зав. кафедри педіатрії, неонатології та біоетики, та Олени Бабич, медичного адвоката, партнера Юридичної компанії «Бабич, Сисоєнко і Партнери» з проханням прокоментувати зазначений проект.
Коментар М. Л. Аряєва
 Безумовно, будь-які кроки щодо належного правового регулювання медико-біологічної сфери є позитивними за умови широкого попереднього обговорення необхідності прийняття закону, його суті, цілей і завдань. Негативним прикладом недостатньої реалізації такого принципу є існуюча законодавча база в галузі трансплантології, після прийняття якої були суттєво обмежені можливості проведення трансплантації органів і тканин в Україні.
Безумовно, будь-які кроки щодо належного правового регулювання медико-біологічної сфери є позитивними за умови широкого попереднього обговорення необхідності прийняття закону, його суті, цілей і завдань. Негативним прикладом недостатньої реалізації такого принципу є існуюча законодавча база в галузі трансплантології, після прийняття якої були суттєво обмежені можливості проведення трансплантації органів і тканин в Україні.
Концептуально обговорення тієї чи іншої проблеми, що стосується медико-біологічної сфери, має декілька вимірів: суто професійний, екстраюридичний (деонтологічний), юридичний (правовий) та етичний (біоетичний).
З нашої точки зору, передбачені законодавством зміни у Сімейному кодексі України та Законі України «Основи законодавства України про охорону здоров'я» не порушують умови професійної діяльності у галузі репродуктивної медицини.
У той же час обмеження можливості застосування методу допоміжного (сурогатного) материнства лише іноземними громадянами тих країн, де ця процедура дозволена законодавством, може стати об'єктом деонтологічної оцінки тому, що стосується професійних кодексів і норм взаємин між фахівцями, а також між фахівцями, пацієнтами та їх родичами. Пропоновані обмеження умов надання медичної допомоги іноземним громадянам можуть мати певні негативні економічні наслідки для вітчизняних клінік, що використовують допоміжні репродуктивні технології і для України в цілому. Причина полягає в позбавленні конкурентних переваг на ринку медичних послуг для вітчизняних лікувальних закладів у порівнянні з країнами, в яких не передбачено такого правового обмеження.
Дуже важливою є правова оцінка такого обмеження з точки зору його відповідності положенням Конституції України. Йдеться про заборону дискримінації в питаннях народження дітей і використання методів лікування або вирішення проблем у репродукційній сфері за ознаками проживання на означеній території тієї чи іншої держави і виходячи із законодавства іншої країни. У ст. 26 Конституції зазначено, що «іноземці та особи без громадянства, що перебувають в Україні на законних підставах, користуються тими самими правами і свободами, а також несуть такі самі обов'язки, як і громадяни України, за винятками, встановленими Конституцією, законами чи міжнародними договорами України».
Ретельної правової оцінки потребує встановлення вікового обмеження 49 років для жінки, щодо якої застосовується штучне запліднення та імплантація ембріона. Виникає необхідність законодавчого визначення, які саме випадки в цьому контексті вважаються винятковими. Потрібне законодавче закріплення процедури роботи комісії, яка може дозволити збільшити вікове обмеження для жінки та порядок ініціювання її скликання лікувальним закладом, пацієнтом або іншими особами.
Етична оцінка законопроекту лежить в площині міжгалузевої дисципліни — біоетики. Остання виникла як етична відповідь на неконтрольоване впровадження новітніх медико-біологічних технологій, за допомогою яких людина почала претендувати на контроль власної еволюції і покращення своєї природи за власним розумінням (!). Біоетичні складнощі аналізу проблеми допоміжних репродуктивних технологій загальновідомі через різні причини — соціальні, релігійні, моральні. У багатьох країнах світу застосування сурогатного материнства заборонено законом.
Очевидний факт успішного становлення і динамічного розвитку біоетики в Україні наглядно відображає прихильність нашого суспільства принципам демократичної побудови держави, міжнародної інтеграції та захисту прав особистості.
Не випадково починаючи з 2011–2012 учбового року викладання біоетики і біобезпеки стало обов'язковим на усіх факультетах вищих медичних навчальних закладів у країні.
З біоетичної точки зору необхідність прийняття закону має достатнє обґрунтовування. «Конвенцією ООН про права дитини» встановлено зобов'язання всіх держав, що її ратифікували, захищати дитину від дискримінації, в тому числі й на підставі статусу та походження дитини. Конвенція вимагає здійснення боротьби з незаконним переміщенням дітей та захисту від усіх форм фізичного, психологічного, сексуального насильства, відсутності піклування чи недбалого і брутального поводження та експлуатації. Для виконання міжнародних зобов'язань в Україні прийнятий Закон «Про Загальнодержавну програму «Національний план дій щодо реалізації Конвенції ООН про права дитини» на період до 2016 року».
Законодавче врегулювання захисту прав дітей, народжених в результаті застосування допоміжних репродуктивних технологій, зокрема з використанням сурогатного материнства, слід розглядати як один із заходів, спрямованих на забезпечення вищезазначеного завдання. На жаль, останнім часом Україна фігурує у скандальних справах, пов'язаних з порушенням прав дітей, народжених внаслідок використання технології сурогатного материнства. Проблема полягає в тому, що дітей, які народжені сурогатною матір'ю в Україні для іноземців, не визнають у країнах, де репродуктивні технології заборонені законом. За такими обставинами батьки вдаються до незаконних способів, зокрема використовуючи контрабандний шлях вивозу дітей за межі України. Долю такої дитини не може відстежити жодна країна.
Іншою ціллю законопроекту є збереження здоров'я сурогатної матері під час вагітності та пологів, повноцінний розвиток дитини при її виношуванні шляхом обмеження віку повнолітньої жінки, щодо якої застосовується штучне запліднення та імплантація ембріона, 49 роками на день перенесення ембріонів.
В обґрунтуванні необхідності прийняття Закону не зазначений ще один привід для обмеження віку пацієнтки, щодо якої застосовується штучне запліднення. В інтересах майбутньої дитини треба враховувати середню тривалість життя, яка в Україні менше, ніж такий показник в економічно розвинутих країнах. У той самий час слід мати на увазі, що визначені ВООЗ інтервали репродуктивного віку (15–49 років) і оптимальний період для запліднення (20–35 років) мають загальний характер і не враховують індивідуальну ситуацію повною мірою.
Законопроект не порушує основні принципи біоетики: добродіяння, незаподіяння шкоди, поваги до автономії та соціальної справедливості. Разом з тим він потребує деталізації та доопрацювання деяких вищезгаданих положень, що стосуються обмежень за ознаками місця проживання і віку.
Позитивною рисою законопроекту є чітке визначення походження дитини, народженої в результаті застосування допоміжних репродуктивних технологій (ст. 123 Сімейного кодексу України). Біоетичний сенс нової редакції статті полягає в захисті майбутньої дитини від дискримінації, стигматизації та наслідків правової невизначеності.
Важливе біоетичне навантаження має зміна ст. 48 Закону України «Основи законодавства України про охорону здоров'я». Вона регламентує умови генетичного зв'язку дитини з сурогатною матір'ю та майбутніми батьками: «Умовами проведення допоміжного (сурогатного) материнства є відсутність безпосереднього генетичного зв'язку дитини з допоміжною (сурогатною) матір'ю та генетичний зв'язок принаймні з одним із майбутніх батьків». Така реакція цілком відповідає біоетичним принципам і правилам, і надає ясну відповідь на питання можливості використання в програмі штучного запліднення та імплантації повністю донорських репродуктивних клітин.
Законопроект «Про обмеження в застосуванні репродуктивних технологій» в цілому відповідає стратегії забезпечення загальнодержавного пріоритету охорони материнства і дитинства в Україні. Зазначена стратегія першочергову увагу приділяє вдосконаленню нормативно-правової бази охорони дітей у порівнянні з нормами міжнародного права, а також посиленню державного контролю й захисту дітей від жорстокого поводження, насилля й експлуатації.
Можливість широкого обговорення Законів України в процесі їх прийняття є принциповою ознакою демократичної побудови та розвитку громадського суспільства. З іншого боку, можливість попередньої різносторонньої оцінки може суттєво впливати на якість законотворчості.
Удосконалення законодавства у сфері допоміжних репродуктивних технологій є вагомим внеском у подальший розвиток перинатології в нашій країні в межах Національного проекту України «Нове життя — нова якість в охороні материнства і дитинства». Створення системи регіональних перинатальних центрів орієнтовано на об'єднання зусиль ВООЗ, ЮНІСЕФ, Міжнародної асоціації акушерів і гінекологів, Міжнародної асоціації педіатрів та міністерств охорони здоров'я окремих країн щодо глобального зниження дитячої смертності до рівня 5 на 1000 дітей, народжених живими, і майже повного запобігання материнської смертності.
На закінчення хотілося б зазначити, що законопроект, безперечно, не вирішує більшості проблемних питань щодо застосування допоміжних репродуктивних технологій. Цей напрям медицини потребує комплексного підходу і подальшого професійного, юридичного, екстраюридичного і біоетичного моніторингу. З правової точки зору юридичне регулювання застосування допоміжних репродуктивних технологій доцільно здійснити шляхом прийняття окремого закону.
Коментар Олени Бабич
 Тема застосування допоміжних репродуктивних технологій, а особливо методу так званого сурогатного материнства, за останні декілька років набула в Україні чималої популярності. Вперше увага до цієї теми була викликана скандальним випадком із громадянкою Сполучених Штатів Америки, яка декілька років тому намагалась вивезти дитину, народжену сурогатною матір’ю в Україні. Ця дитина, до речі, так і залишилась в Україні. Минулорічна історія із громадянами Франціі, що намагалися нелегально вивезти дітей народжених в Україні, в результаті застосування методу сурогатного материнства, теж не залишилась поза увагою.
Тема застосування допоміжних репродуктивних технологій, а особливо методу так званого сурогатного материнства, за останні декілька років набула в Україні чималої популярності. Вперше увага до цієї теми була викликана скандальним випадком із громадянкою Сполучених Штатів Америки, яка декілька років тому намагалась вивезти дитину, народжену сурогатною матір’ю в Україні. Ця дитина, до речі, так і залишилась в Україні. Минулорічна історія із громадянами Франціі, що намагалися нелегально вивезти дітей народжених в Україні, в результаті застосування методу сурогатного материнства, теж не залишилась поза увагою.
Активне висвітлення цих випадків ЗМІ певною мірою змусило законодавця врегулювати деякі питання сфери допоміжних репродуктивних технологій на законодавчому рівні. Одним із таких намагань і є вищезгаданий законопроект.
Безумовно, будь-які кроки щодо належного правового регулювання сфери медицини є однозначно позитивними, але прийняття даного законопроекту, на думку автора, за відсутності законодавчого закріплення механізму застосування нововведених норм, матиме певну низку проблем їх практичного застосування.
Необхідно звернути увагу, що законодавець встановлює вікове обмеження 49 років для жінок, які намагаються завагітніти за допомогою штучного запліднення, а не тільки за допомогою методу сурогатного материнства. Тобто після настання цього віку жінка позбавлена права на застосування допоміжних репродуктивних технологій.
Так, щодо можливості у виняткових випадках збільшення вікового обмеження для жінки, щодо якої застосовується штучне запліднення, на підставі висновку комісії, утвореної органом центральної виконавчої влади у сфері охорони здоров’я. Виникає необхідність законодавчого закріплення процедури роботи такої комісії, зокрема порядку її утворення і роботи, визначення кола осіб, які можуть ініціювати її скликання – лікувальний заклад, безпосередньо пацієнт, інші особи, і, головне, які саме випадки, в даному контексті, вважаються винятковими.
Встановлення можливості застосування методу допоміжного (сурогатного) материнства лише іноземним громадянам тих країн, де ця процедура дозволена законодавством, є досить суперечливим.
По-перше, чинне законодавство України не містить визначення поняття допоміжного (сурогатного) материнства. Так, ч. 2 статті 123 Сімейного кодексу України регулює питання походження дитини, народженої в результаті застосування допоміжних репродуктивних технологій шляхом перенесення в організм іншої жінки ембріона людини, зачатого подружжям. По-друге, у разі прийняття даного положення, постає необхідність створення та оприлюднення переліку іноземних країн, в яких повністю або частково заборонено застосування допоміжних репродуктивних технологій. Ведення такого переліку, скоріш за все, має бути покладено на орган центральної виконавчої влади у сфері охорони здоров’я – Міністерство охорони здоров’я України.
Одним із позитивних моментів даного законопроекту є намагання закріпити умови генетичного зв’язку дитини з допоміжною (сурогатною) матір’ю та майбутніми батьками. Адже на сьогодні в чинному законодавстві дане питання досі залишається не врегульованим. В цьому контексті одним із основних є питання обов’язковості генетичної спорідненості дитини і майбутніх батьків, генетичної спорідненості дитини із сурогатною матір’ю та можливості використання в таких програмах лікування, повністю донорських репродуктивних клітин.
Наостанок хотілось би зазначити, що даний законопроект звичайно не вирішує більшості проблемних питань сфери застосування допоміжних репродуктивних технологій, адже ця сфера медицини потребує комплексного підходу при її правовому регулюванні шляхом прийняття окремого закону.
ДетальнішеАКУШЕРСТВО, ОСНОВАННОЕ НА ДОКАЗАТЕЛЬСТВАХ
Тест Клейхауэра-Бетке
Тест Клейхауэра-Бетке (Kleihauer-Betke) — анализ крови, используемый для вычисления количества фетального гемоглобина, передающегося в кровоток матери от плода. Это исследование, как правило, необходимо у резус-отрицательных матерей для определения дозы Rh0 (D) иммуноглобулина (RhIg) с целью предотвращения образования резус-антител у матери и профилактики резус-конфликта у резус-положительного ребенка, а также для подтверждения фетально-материнской трансфузии как причины мертворождения.
Тест Клейхауэра-Бетке (КБ) является стандартным методом расчета фетально-материнской трансфузии. Он основан на разнице в устойчивости фетального гемоглобина к кислоте по сравнению с гемоглобином взрослого человека. Из крови матери готовят стандартный мазок крови и подвергают кислотной ванне. Вследствие этого из эритроцитов устраняется гемоглобин А (adult-гемоглобин), фетальный гемоглобин остается. Дальнейшее окрашивание мазка позволяет увидеть розовые фетальные эритроциты (содержащие фетальный гемоглобин), в то время как эритроциты взрослого выглядят как обесцвеченные тени. В дальнейшем подсчитывается 2000 эритроцитов и вычисляется процент фетальных и материнских клеток.
По сравнению с другими, более дорогими и технологически сложными методиками, такими как проточная цитометрия, КБ-тест – простой и в то же время достаточно чувствительный метод для обнаружения фетально-материнской трансфузии. Чувствительность данного теста составляет 95–96%. Ложноположительный результат теста может быть вызван заболеванием матери, которое вызывает стойкое повышение фетального гемоглобина, например серповидно-клеточной анемией. Ошибки подсчета могут привести к ложноотрицательному результату теста, если фетально-материнская трансфузия составляет менее 5 мл. В то же время стандартные методики, доступные в большинстве лабораторий, показывают, что существует чрезвычайно низкая вероятность появления ложноположительного или ложноотрицательного результата при более значительной фетально-материнской трансфузии.
Использование метода
Применяется для оценки тяжести фетально-материнской трансфузии, в частности для подтверждения фетально-материнской трансфузии (ФМТ) как причины мертворождения. Для определения причинно-следственной связи между положительным тестом на ФМТ и внутриутробной гибелью плода должен быть вычислен объем плодовой кровопотери. Для этого необходимо учесть следующие данные:
1) размер фетальных эритроцитов в 1,22 раза больше, чем эритроцитов взрослых;
2) у теста КБ, как известно, есть средний показатель успешности (94–96%) в обнаружении эмбриональных эритроцитов;
3) у женщин во время беременности средний объем материнских эритроцитов составляет приблизительно 1800 мл;
4) средний гематокрит плода 50%, а у мертворожденных средний объем крови составляет 150 мл/кг массы.
Эти данные могут быть применены для получения формулы:
ПФК=(3200)*(ФК)/(ММ)*(МК)
Где ПФК — это процент фетальной кровопотери; ФК — число эритроцитов плода; МК — число материнских эритроцитов; ММ — масса мертворожденного плода в килограммах.
Подтверждение мертворождения (пример использование расчетной формулы)
Предположим, что КБ-тест представлен общим количеством эритроцитов, равным 5000, из них являются эмбриональными эритроцитами 200 (ФК). Далее предположим, что вес мертворожденного плода равен 2,0 кг. Тогда мы пришли бы к заключению, что процент потерянной крови плодом приблизительно (ПФК):
ПФК= (3200)*(ФК)/(ММ)*(МК) = (3200)*(200)/(2,0)(4800)=200/3=66,667
Итак, плод потерял 66,667% (две трети) крови из-за фетально-материнского кровотечения. Как известно, мертворождение очень вероятно при ПФК, равном или большем 20% ОЦК при острой кровопотере. Следовательно, в этом примере мы подозревали бы фетально-материнское кровотечение как причину мертворождения. Однако, так как тест КБ ничего не говорит нам относительно скорости фетально-материнского кровотечения, это означает, что невозможно полностью коррелировать положительный тест КБ и ПФК с мертворождением. Тем не менее во многих случаях при использовании дополнительной информации, например факта наследственных осложнений беременности, мы можем наблюдать чрезвычайно высокий положительный коэффициент корреляции r ~ +1,000 между фетально-материнским кровотечением и мертворождением.
Эмбриональные проблемы обнаружения ФМТ
Так как у эмбриональных и материнских клеток крови одна и та же продолжительность жизни в материнском кровотоке, возможность получить информативный результат теста КБ существует в течение определенного промежутка времени после мертворождения. Так, если мать и плод несовместимы по системе АБО, крайне важно максимально быстро выполнить тест КБ после мертворождения, поскольку эмбриональные эритроциты будут устранены из материнского кровотока и тест КБ станет менее чувствительным для оценки фетально-материнского кровотечения. Дискутабельным остается вопрос относительно ложноположительных результатов теста. Нужно помнить, что если предполагается кесарево сечение и предварительный забор крови не будет сделан, ложноположительный результат будет получен в 2% случаев.
Сравнение эффектов раннего и отсроченного пережатия пуповины у недоношенных новорожденных
У недоношенных новорожденных отсрочка пережатия пуповины на 60–120 секунд ассоциируется с меньшей частотой необходимости переливания крови и меньшей частотой внутрижелудочковых кровоизлияний.
Комментарий БРЗ ВОЗ. Автор: Ceriani Cernadas J.M., 2007.
Резюме доказательных данных
Основной целью данного обзора стала оценка краткосрочных и отдалённых результатов плацентарной трансфузии с учётом времени пережатия пуповины и/или положения новорожденного относительно уровня плаценты, и/или выдавливания крови из пуповины в случае рождения детей в сроке менее 37 недель гестации. Отсроченное пережатие пуповины определяется как пережатие пуповины на 60–120 секунде после рождения.
Масштабы проблемы
Пережатие пуповины обычно осуществляется сразу же или в течение первой минуты после рождения ребёнка. Нет никаких научно обоснованных данных в поддержку данной методики, которая, скорее всего, основывается среди других причин на уверенности, что отсроченное пережатие пуповины негативно отражается на здоровье новорожденных вследствие плацентарной трансфузии. Это мнение поддерживается ограниченным числом небольших обсервационных испытаний, большинство из которых были проведены в 1960-е и 1970-е гг. Эти испытания указывали на большую частоту патологии сердечной и дыхательной систем и гипербилирубинемии у новорожденных с отсроченным пережатием пуповины. Более поздние рандомизированные контролируемые исследования, вошедшие (и исключённые) в данный обзор не выявили никаких негативных или опасных последствий этой методики. Несмотря на ограничения испытаний, указанные в обзоре, высока вероятность того, что отсроченное пережатие пуповины является безопасной методикой, хотя и требуется соблюдать некоторую осторожность (см. ниже). Основным преимуществом отсроченного пережатия пуповины является то, что постнатальная плацентарная трансфузия способствует увеличению количества красных кровяных телец и запаса железа у новорожденных. Это особенно справедливо для недоношенных детей, так как они подвержены многим воздействиям, увеличивающим риск возникновения серьёзной патологии. Анемия новорожденных, связанная с преждевременными родами, является часто возникающей проблемой, оказывающей значительное влияние на клинические исходы, особенно в условиях ограниченных ресурсов.
У недоношенных новорожденных существует три основные причины анемии: физиологические механизмы, сопутствующие преждевременным родам; неонатальные заболевания или патология; и, что наиболее важно, частый забор крови для лабораторных анализов во время интенсивной терапии. Несмотря на определённые стратегии, направленные на снижение числа трансфузий, большинству недоношенных детей, рождённых в сроке менее 32 полных недель гестации, выполняется по меньшей мере одно переливание крови. Проблемы, связанные с анемией у недоношенных новорожденных, а также с её лечением (переливание крови), многочисленны и могут быть достаточно опасны. Анемия замедляет процесс нормального роста и способствует недостаточному усвоению питания у большинства недоношенных детей с очень низкой массой тела при рождении, пребывающих на стационарном лечение в течение длительного времени. Анемия также нарушает процесс выздоровления при дыхательной патологии (в частности при бронхолегочной дисплазии), врождённой сердечной патологии и бактериальных инфекциях. С другой стороны, кровь и продукты крови для переливания могут представлять значительную опасность в плане передачи инфекции или других заболеваний, особенно в условиях ограниченных ресурсов.
Применимость результатов
Результаты данного Кокрановского обзора применимы к условиям с ограниченными ресурсами. Важно помнить о том, что существуют определённые ситуации, в которых желательно выполнить пережатие пуповины в течение нескольких первых секунд после рождения, независимо от условий. При внутриутробной асфиксии и дистрессе плода происходит больший перенос крови из плаценты к плоду до наступления родов, таким образом, отсроченное пережатие пуповины может быть не показано в этих случаях. Это, однако, не относится к ситуации, когда дистресс плода возникает на позднем этапе родов (второй период родов). В этом случае выполнение отсроченного пережатия пуповины не противопоказано, согласно наблюдениям Liderkamp et al. [8]. Наоборот, в такой ситуации приток крови на первой минуте может способствовать более эффективной реанимации недоношенных новорожденных с низкой оценкой по шкале Апгар при рождении. Другие ситуации, в которых не рекомендуется выполнять отсроченное пережатие пуповины, включают резус-конфликт, внутриутробную задержку роста или диабет у матери.
Применение вмешательства
В Аргентине испытание, осуществлённое при поддержке ЮНИСЕФ и изучавшее наиболее благоприятное время пережатия пуповины, было проведено в 31 родильном доме. Точное время пережатия пуповины было зафиксировано в 3738 случаев родов. Среднее время выполнения пережатия пуповины составляло 25 секунд в общей популяции и 10 секунд в группе новорожденных с массой тела при рождении менее 2500 г (Carroli G., личный контакт). Основываясь на этих данных, был предпринят рад шагов по распространению методики отсроченного пережатия пуповины не позднее первой минуты после рождения среди доношенных новорожденных с основной целью увеличить запас железа в организме новорожденных и предупредить возникновение анемии в течение первых месяцев жизни. С такой же целью ЮНИСЕФ решил поддержать разработку рандомизированных контролируемых испытаний по оценке возможных рисков для новорожденного и его матери при проведении этой процедуры. В целом 276 пар «мать — новорожденный» путем случайного выбора были распределены на три группы с учётом различного времени пережатия пуповины: в течение первых 15 секунд (раннее пережатие пуповины), на первой минуте и на третьей минуте (обе группы значились как группы с отсроченным пережатием пуповины).
Испытание показало, что отсроченное пережатие пуповины повышает гематокрит в течение первых 6 часов жизни в физиологических пределах и не приводит ни к каким рискам ни у матери, ни у новорожденного. Также отсроченное пережатие пуповины значительно снижает частоту неонатальной анемии, определяемой как значение венозного гематокрита менее 45% [12]. В результате второй фазы испытания (ещё не опубликованного), оценивающего содержание гемоглобина и ферритина у детей в шестимесячном возрасте, было обнаружено, что уровень ферритина значительно выше в группе с отсроченным пережатием пуповины, даже после контроля смешивающих параметров.
Литература
- Mercer J.S., McGrath M.M., Hensman A., et al. Immediate and delayed cord clamping in infants born between 24 and 32 weeks: a pilot randomized controlled trial. Journal of Perinatology 2003;23:446–472.
- Oh W., Lind J., and Gessner I.H. The circulatory and respiratory adaptation to early and late cord clamping in neonate infants. Acta Paediatrica Scandinavica 1966;55:17–25.
- Oh W., Wallgren G., Hanson J.S., and Lind J. The effects of placental transfusion on respiratory mechanics of normal term neonate infants. Pediatrics 1967;40:6–12.
- Saigal S., and Usher R.H. Symptomatic neonatal plethora. Biology of the Neonate 1977;32:62–72.
- Yao A.C., Lind J., and Vuorenkoski V. Expiratory grunting in the late clamped normal neonate. Pediatrics 1971;48:865–870.
- Saigal S., O'Neill A., Surainder Y., Chua L.B., and Usher R. Placental transfusion and hyperbilirubinemia in the premature. Pediatrics 1972;49:406–419.
- Yao A.C., and Lind J. Placental transfusion. American Journal of the Diseases of the Childhood 1974;127:128–141.
- Linderkamp O., Nelle M., Kraus M., and Zilow E.P. The effect of early and late cord-clamping on blood viscosity and other hemorheological parameters in full-term neonates. Acta Paediatrica 1992;81:745–750.
- Van Rheenen P., Brabin B.J. Late umbilical cord-clamping as an intervention for reducing iron deficiency anaemia in term infants in developing and industrialised countries: a systematic review. Annals Tropical Paediatrics 2004;24:3–16.
- Flod N.E., Ackerman B.D. Perinatal asphyxia and residual placental volume. Acta Paediatric Scandinavian 1971;60:433.
- Yao A., Lind J. Blood volume in the asphyxiated term neonate. Biology of the Neonate 1972;21:199.
- Ceriani Cernadas J.M., Carroli G., Otaño L., Pellegrini L. et al. Effect of timing of cord clamping on postnatal hematocrit values and clinical outcome in term infants. A randomized controlled trial. Pediatric Research 2004;55:462.
Инъекция в пупочную вену при задержке отделения плаценты
Инъекция физраствора с окситоцином в пупочную вену эффективна в лечении задержки плаценты.
Комментарий БРЗ.
Автор: Purwar M.B. ВОЗ, 2009.
Резюме доказательных данных
В лечении задержки плаценты инъекция физраствора в вену пуповины (с сокращающими средствами или без них) сравнивалась с выжидательной тактикой с одной стороны и с инъекцией в вену пуповины другого раствора с другой стороны. В сравнении с тактикой ожидания инъекция физраствора с окситоцином продемонстрировала снижение частоты отделения плаценты вручную, но эта разница была статистически погранично несущественной (ОР: 0,86; 95% ДИ 0,72–1,01). В сравнении с введением только одного физраствора введение физраствора с окситоцином продемонстрировало статистически существенное снижение частоты ручного отделения плаценты (ОР: 0,79; 95% ДИ 0,69–0,91). Сравнение физраствора плюс простагландин с физраствором плюс окситоцин не обнаружило статистически значимой разницы по вышеуказанным показателям.
Масштабы проблемы
Ежегодно в мире умирает 585 000 женщин в связи с беременностью и родами, и 99% этих смертей происходят в развивающихся странах [1]. Около 25% случаев материнской смертности в азиатских странах связаны с кровотечением во время беременности, родов или в послеродовом периоде. Из них почти 30% связаны с послеродовым кровотечением. А 15–20% из общего числа случаев материнской смертности в результате послеродового кровотечения (ПРК) связаны с задержкой плаценты [2]. Частота случаев задержки плаценты составляет 0,8–1,2% от всех родов [2]. В современной практике отделение плаценты вручную применяется, если она не рождается через полчаса после рождения ребенка. Отделение плаценты вручную сопряжено с риском травмы, кровотечения, резусной аллоиммунизации, послеродовой инфекции и анестезиологических осложнений. В целом, на уровне оказания первичной помощи нет такой инфраструктуры, которая бы включала операционные и анестезиологов. Поэтому менее инвазивная и недорогая форма лечения была бы предпочтительнее для снижения необходимости в выполнении операции по отделению плаценты вручную.
Практическая осуществимость вмешательства
Для проведения данной манипуляции необходимо подготовить шприц объемом 20 мл, 10 ЕД окситоцина и 40 мл физраствора. При диагностике задержки отделения последа и отсутствии признаков наружного кровотечения необходимо растворить 10 ЕД окситоцина в 40 мл физиологического раствора и ввести струйно в пупочную вену, после чего наложить зажим выше места инъекции и продолжить выжидательную тактику до десяти минут. В случае отсутствия признаков самостоятельного отделения последа рекомендовано перейти на ручное его отделение.
Сложности с внедрением этой манипуляции связаны с уровнем подготовленности персонала по выполнению инъекций в пупочную вену. Окситоцин и физраствор, как правило, есть в наличии во всех ЛПУ первичного и вторичного уровня оказания помощи.
Литература
- WHO and UNICEF. Revised 1990 estimates of maternal mortality WHO/FRH/MSM/96.1. 1996.
- Daftary S.N. and Nanawati M.S. Management of Postpartum Haemorrhage. In: Principals and practice of Obstetrics and Gynaecology for Postgraduates. FOGSI Publication. Eds. Buckshee K, Patwardhan VB, and Soonawala R.P. Jaypee Brothers Medical Publishers, New Delhi:1996.
Применение сульфата магния среди женщин с угрозой преждевременных родов для нейропротекторного эффекта на плод
Антенатальная терапия сульфатом магния среди женщин с угрозой преждевременных родов снижает риск возникновения нейрологических нарушений у их новорожденных. Несмотря на то что сульфат магния является безопасным препаратом, рамки его дозировки очень ограничены. Таким образом, женщины, получающие сульфат магния с целью нейропротекторного эффекта для новорожденного, должны находиться под тщательным наблюдением во время лечения.
RHL Commentary by Lumbiganon P. ВОЗ, 2009.
Введение
Преждевременные роды и низкая масса тела новорожденного при рождении являются серьёзными проблемами здравоохранения в развивающихся странах. У недоношенных детей по сравнению с доношенными имеется более высокий риск развития таких нейрологических проблем, как церебральный паралич и нарушение когнитивной функции. Риск нейрологических проблем увеличивается с уменьшением гестационного возраста на момент родов, особенно среди детей с очень низкой массой тела при рождении (ОНМТР). В 1993 году Ho с коллегами [2] оценили распространённость и структуру отклонений в нервном развитии среди детей двух лет с ОНМТР, наблюдавшихся в трёх малазийских детских учреждениях. Среди 150 новорожденных с ОНМТР, включённых в это исследование, 82 дожили до двухлетнего возраста, из которых у 77 была произведена оценка нервного развития. Функционально у 24 (31%) детей были обнаружены умеренные или тяжёлые отклонения. Другое исследование, насчитывающее 2036 детей, проведённое в Южной Африке, показало, что уровень инвалидизации среди новорожденных с ОНМТР составляет 60 на 1000 (95% ДИ 50–71). Наиболее частыми отклонениями были умеренные нарушения восприятия или обучения (17 на 1000), церебральный паралич (10 на 1000) и потеря слуха (10 на 1000) [3]. Проспективное когортное исследование, проведённое в Малайзии, по оценке заболеваемости среди новорожденных с ОНМТР показало, что среди детей с ОНМТР значительно более высок риск церебрального паралича (ОШ 8,6; 95% ДИ 2,0–77,6) и нейросенсорной потери слуха (ОШ 12,0; 95% ДИ 1,7–513,6) [4].
Цель данного Кокрановского обзора заключалась в оценке влияния сульфата магния как нейропротекторного препарата при назначении женщинам, угрожаемым по преждевременным родам.
Методы
Всего 5 испытаний соответствовали критериям включения в обзор. Они насчитывали 6145 детей, рождённых у женщин группы риска по преждевременным родам вследствие преждевременного начала схваток, преждевременного дородового излития околоплодных вод, преэклампсии или эклампсии. Группы сравнения в этих испытаниях включали женщин, получивших сульфат магния по сравнению с плацебо или отсутствием лечения. В 4 из 5 испытаний первичная цель назначения женщине лечения сульфатом магния заключалась в защите новорожденного от возможных неблагоприятных нейрологических последствий преждевременных родов. В одном из испытаний (испытание Magpie) сульфат магния назначался женщине для предупреждения эклампсии, но также были оценены результаты для новорожденных.
Результаты
Антенатальная терапия сульфатом магния, назначаемая женщинам, угрожаемым по преждевременным родам, значительно снизила риск развития церебрального паралича у их детей (ОР 0,68; 95% ДИ 0,54–0,87; 5 испытаний; 6145 новорожденных). Также наблюдалось существенное снижение частоты нарушений основной двигательной функции (ОР 0,61; 95% ДИ 0,44–0,85; 4 испытания; 5980 новорожденных). Во всех 5 исследованиях дети, рождённые у женщин, вошедших в исследование в сроке менее 34 недель гестации и получивших сульфат магния, характеризовались сниженным риском развития церебрального паралича (ОР 0,69; 95% ДИ 0,54–0,88; 5 испытаний; 5357 новорожденных) по сравнению с теми, кто не получил лечения или получил плацебо.
Четыре исследования сообщили о применении кортикостероидов у более чем 50% женщин, угрожаемых по преждевременным родам. Анализ этих 4 исследований отдельно не изменил выводы (ОР 0,67; 95% ДИ 0,53–0,86; 4 испытания; 4493 новорожденных). Не наблюдался статистически значимый эффект терапии сульфатом магния у женщин, угрожаемых по преждевременным родам, на неонатальную смертность или другие нейрологические показатели.
Отмечались более высокие уровни малых побочных эффектов со стороны матери в группе сульфата магния, но значительного увеличения осложнений со стороны матери не наблюдалось.
Обсуждение
Сульфат магния безопасен только в рамках определённых дозировок, а превышение его дозы может приводить к серьёзным осложнениям, включая угнетение дыхания и остановку сердца у матери. Одно крупное исследование [6] сообщило, что назначение сульфата магния при строгом соблюдении протокола не приводило к большей частоте осложнений по сравнению с плацебо, даже в условиях ограниченных ресурсов. Учитывая, что при недостаточных ресурсах даже умеренные отклонения в развитии могут иметь серьёзные последствия для благополучия ребёнка, применение сульфата магния с нейропротекторной целью для новорожденного потенциально может быть очень полезным во всех отношениях, несмотря на риск возникновения осложнений со стороны матери.
Литература
- Paneth N., Hong T., Korzeniewski S. The descriptive epidemiology of cerebral palsy. Clinics in Perinatology 2006; 33:251-67.
- Ho J.J., Amar H.S.S., Mohan A.J., Hon T.H. Neurodevelopment outcome of very low birth weight babies admitted to a Malaysia nursery. Journal of Paediatrics and Child Health 1999; 35:175-80.
- Couper J. Prevalence of childhood disability in rural KwaZulu-Natal. South African Medical Journal 2002; 92:549-52.
- Boo N.Y., Ong L.C., Lye M.S., Chandran V., Teoh S.L., Zamratol S., et. al. Comparison of morbidities in very low birthweight and normal birthweight infants during the first year of life in a developing country. Journal of Paediatrics and Child Health 1996; 32:439-44.
- Doyle L.W., Crowther C.A., Middleton P., Marret S. Magnesium sulphate for women at risk of preterm birth for neuroprotection of the fetus. Cochrane Database of Systematic Reviews 2007; Issue 3. Art. No.:CD004661; DOI: 10.1002/14651858.CD004661.pub2.
- 6. Altman D., Carroli G., Duley L., Farrell B., Moodley J., Neilson J., Smith D.; Magpie Trial Collaboration Group. Do women with pre-eclampsia, and their babies, benefit from magnesium sulphate? The Magpie Trial: a randomised placebo-controlled trial. The Lancet 2002;359:1877-1890.
ВИПАДОК УСПІШНОГО ВЕДЕННЯ ВАЖКОЇ ЕКСТРАГЕНІТАЛЬНОЇ ПАТОЛОГІЇ
Вагітна З., 30 років, жителька Черкаської області, 12.03.2011 р. доставлена до відділення екстрагенітальної патології КЗ «Обласна лікарня – центр екстреної медичної допомоги та медицини катастроф» Черкаської обласної ради з Центральної районної лікарні зі скаргами на головний біль, слабкість та болі у верхніх та нижніх кінцівках, затерпання обличчя, язика, передньої черевної стінки до рівня молочних залоз, часткове порушення ковтання, неможливість повністю зімкнути очі.
З анамнезу відомо, що 13.02.2011 жінка захворіла на гостре респіраторне захворювання. Вагітність друга. Передбачувані пологи перші. Об’єктивно: гіперстенічної статури, підвищеного харчування. Пульс 88 уд/хв, АТ 160/110 мм рт. ст., температура тіла 37,0OС.
Неврологічний статус: парез лицевих нервів з обох боків; сухожильні рефлекси, сила м’язів верхніх і нижніх кінцівок, больова чутливість різко знижені.
Діагноз при надходженні «Підгострий інфекційно-алергічний (вірусний, післягрипозний) енцефаломієлополіневрит Гієна-Барре з в’ялим прогресуючим тетрапарезом та бульбарними розладами. Вагітність 19 тижнів».
При обстеженні в слині вагітної виявлено вірус Епштейн-Барра.
У терміні 24–25 тижнів вагітності до основного захворювання приєднується гестаційний пієлонефрит. На фоні основного захворювання виникає атонія кишківника, наростають явища гострої дихальної недостатності ІІІ ступеня. Стан вагітної вкрай тяжкий. Проведена трахеотомія. Вагітна переведена на режим штучної вентиляції легень, на якому перебувала протягом шести днів. Трахеостомічна трубка видалена через 13 днів після постановки.
На 26–27 тижнях вагітності у жінки виникла вертеброгенна лівобічна люмбоішиалгія.
Вагітній проведено клініко-лабораторне обстеження, МРТ головного мозку, МРТ грудного відділу хребта, МРТ поперекового відділу хребта, люмбальна пункція, рентгенографія органів грудної порожнини, ехокардіографія, УЗД органів черевної порожнини, УЗД плода. Стан плоду, згідно з обстеженнями, залишався задовільним.
Лікування: біовен-моно, ацикловір, нуклео-ЦМФ, калімін, сорбілакт, L-лізін есценат, дексаметазон, алокін, фуросемід, аспаркам, допегіт, актовегін, магнія сульфат, мільгама, пентоксіфілін, цефепін, флуканазол, лазерне опромінювання крові, плазмоферез, гіпербарична оксигенація, фізпроцедури.
31.05.2011 з діагнозом «Вагітність 31 тиждень. Гостра демієлінізуюча радікулополіневропатія (синдром Гієна-Барре) з тетрапарезом, відновний період. Остеохондроз поперекового відділу хребта, лівобічна люмбоішиалгія, стадія ремісії» вагітна виписана додому під нагляд дільничного акушера-гінеколога та невролога.
Повторно вагітна поступила до відділення екстрагенітальної патології 07.07.2011 у терміні вагітності 37–38 тижнів. У жінки зберігався в’ялий тетрапарез: легкий в руках, помірний в ногах. Пересувалася обмежено, з ходунцями.
Враховуючи важку екстрагенітальну патологію, 18.07.2011 проведено плановий кесарський розтин. Народився хлопчик вагою 3770,0 г, зростом 55 см, з оцінкою за шкалою Апгар 9–10 балів, без видимих вад розвитку. На п’яту добу після пологів породілля разом з дитиною виписана додому.
На цей час у жінки відновилась рухова активність у верхніх та нижніх кінцівках.
Дитина розвивається згідно з віковими нормами.
Мнение эксперта
Евгений Петренко
Синдром Гийе́на-Барре может представлять как существенную угрозу для жизни двух организмов — матери и ребенка, так и существенную клиническую проблему для медицинских работников.
Острая воспалительная демиелинизирующая полирадикулоневропатия — синдром Гийена-Барре (СГБ) — острая аутоиммунная воспалительная полирадикулоневропатия, проявляющаяся вялыми парезами, нарушениями чувствительности, вегетативными расстройствами. Данная патология — одно из наиболее тяжелых заболеваний периферической нервной системы и самая частая причина острых периферических параличей. СГБ в трети случаев требует проведения всего комплекса мероприятий интенсивной терапии, включая ИВЛ.
Терминология
Заболевание впервые было описано французским неврологом Ландри в 1859 году, а впоследствии детально исследовано его соотечественниками Гийеном, Барре и Штролем в 1916 году. Исторически сложившиеся терминологические разногласия привели к тому, что в настоящее время существует не менее восьми названий болезни. При этом следует подчеркнуть, что синдром Ландри, синдром Гийена-Барре, синдром Гийена-Барре-Штроля, синдром Ландри-Гийена-Барре, синдром Ландри-Гийена-Барре-Штроля, острый полирадикулоневрит, острая постинфекционная полинейропатия, острая воспалительная демиелинизирующая полинейропатия, — синонимы одного заболевания. Имевшиеся ранее представления о том, что синдром Ландри — заболевание с обязательно неблагоприятным течением, связанное с поражением бульбарной и дыхательной мускулатуры, а синдром Гийена-Барре — «доброкачественный» вариант синдрома Ландри без вовлечения в процесс дыхательной мускулатуры, в настоящее время пересмотрены, и эти состояния признаются как единое по своей природе заболевание. В МКБ 10-го пересмотра заболевание входит как синдром Гийена-Барре, и именно так его необходимо обозначать при постановке диагноза.
Эпидемиология
Частота встречаемости составляет в среднем 1–2 человека на 100 тысяч населения. У подавляющего большинства больных отмечается быстрое и практически полное восстановление, но в трети случаев развиваются нарушения дыхания, требующие проведения ИВЛ; у 5–22% пациентов отмечаются остаточные явления; в 3–10% случаев наблюдаются рецидивы и от 5 до 33% больных с тяжелыми формами заболевания умирают.
Этиология и патогенез
За 1–3 недели до проявления заболевания у большинства пациентов отмечают признаки инфекции желудочно-кишечного тракта или дыхательных путей. Основными провоцирующими агентами считаются Campylobacter jejuni (обнаруживаются в трети случаев СГБ, риск развития СГБ повышается примерно в 100 раз) и цитомегаловирус (до 15% случаев). Установлена определенная связь СГБ и с вирусом Эпштейн-Барра (около 10% случаев). Вероятно, перенесённая инфекция запускает аутоиммунную реакцию по принципу клеточной мимикрии. Эту же роль могут играть вакцинация, оперативные вмешательства, травмы периферических нервов. Аутоиммунная реакция против антигенов шванновских клеток и миелина приводит к отёку, лимфоцитарной инфильтрации и сегментарной демиелинизации корешков спинномозговых и черепных нервов. Реже атаке подвергаются антигены аксонов периферических нервов (при аксональном варианте синдрома).
Классификация МКБ-10 — G61.0
Различают следующие клинические варианты СГБ:
- Острая воспалительная демиелинизирующая полиневропатия — наиболее частая, классическая форма
- Острая моторная аксональная невропатия
- Острая моторно-сенсорная аксональная невропатия
- Синдром Миллера-Фишера — сочетание арефлексии, мозжечковой атаксии, офтальмоплегии при слабовыраженных парезах
Клиническая картина
Заболевание характеризуется относительно симметричной мышечной слабостью (вялый парез), которая типично начинается в проксимальных отделах мышц ног и через несколько часов или дней распространяется на руки. Часто слабость сопровождается парестезиями пальцев стоп и кистей. Иногда слабость в первую очередь возникает в руках или одновременно в руках и ногах. Повышается содержание белка в спинномозговой жидкости (начиная со 2-й недели заболевания). В тяжелых случаях возникают параличи дыхательных и краниальных мышц, главным образом мимических и бульбарных. Нередки боли в спине, плечевом и тазовом поясе, иногда иррадиирующие по ходу корешков, симптомы натяжения. Часто отмечаются выраженные вегетативные нарушения: повышение или падение артериального давления, ортостатическая гипотензия, синусовая тахикардия, брадиаритмия, преходящая задержка мочи. Интубация или отсасывание слизи могут спровоцировать резкую брадикардию, коллапс и даже остановку сердца. Достигнув пика, симптоматика стабилизируется (фаза плато длится 2–4 недели), а затем начинается восстановление, которое может продолжаться от нескольких недель до 1–2 лет. Смерть возможна от дыхательной недостаточности, связанной с параличом дыхательного или бульбарного центров, пневмонии, тромбоэмболии лёгочных артерий, остановки сердца, сепсиса, но благодаря современным методам интенсивной терапии, прежде всего ИВЛ, летальность в последнее десятилетие снизилась до 5%.
Лабораторные методы исследования
Состав спинномозговой жидкости при СГБ в первые дни болезни чаще всего в пределах нормы, но ее белок имеет четкую тенденцию к повышению после первых 5–7 суток, обычно достигая максимума к 3–4-й неделе. В ряде случаев не исключено резкое увеличение концентрации белка в ликворе уже спустя 2–3 суток после начала СГБ. Более чем 50 мононуклеарных лейкоцитов в ликворе или наличие в нем полиморфно-ядерных лейкоцитов исключают диагноз «СГБ».
Электромиография (ЭМГ) — наиболее чувствительный параклинический метод в диагностике СГБ. При ЭМГ выявляются признаки как деструкции миелина, так и аксональной дегенерации.
Диагностические критерии СГБ (ВОЗ, 1993)
А. Признаки, необходимые для постановки диагноза СГБ:
- Прогрессирующая мышечная слабость более чем в одной конечности
- Сухожильная арефлексия
Б. Признаки, поддерживающие диагноз СГБ (в порядке значимости):
- Прогрессирование: симптомы и признаки двигательных нарушений развиваются быстро, но прекращают нарастать к концу 4-й недели от начала заболевания
- Относительная симметричность поражения
- Чувствительные нарушения
- Черепные нервы: характерно поражение лицевого нерва
- Восстановление: обычно начинается через 2–4 недели после прекращения нарастания заболевания, но иногда может задерживаться на несколько месяцев. Большинство больных хорошо восстанавливаются
- Вегетативные нарушения: тахикардия, аритмии, постуральная гипотензия, гипертензия, вазомоторные симптомы
- Отсутствие лихорадки в начале заболевания (небольшое число больных имеют лихорадку в начале заболевания из-за интеркуррентных инфекций или по другим причинам). Лихорадка не исключает СГБ, но ставит вопрос о возможности другого заболевания
- Изменения цереброспинальной жидкости, поддерживающие диагноз
- Белок после первой недели заболевания повышен или повышается в дальнейшем
- Клеточный состав: число мононуклеарных лейкоцитов 10 или меньше. В случае повышения числа клеток больше 20 необходимо пристальное внимание; диагноз неправомочен при числе клеток выше 50.
Признаки, вызывающие сомнения в диагнозе:
- Выраженная сохраняющаяся асимметрия двигательных нарушений
- Сохраняющиеся нарушения функций сфинктеров
- Нарушения функций сфинктеров в начале заболевания
- Более чем 50 мононуклеарных лейкоцитов в ликворе
- Наличие полиморфно-ядерных лейкоцитов в ликворе
- Четкий уровень чувствительных нарушений
Лечение
Даже в лёгких случаях к синдрому Гийена-Барре в острой фазе следует относиться как к неотложному состоянию ввиду опасности быстрого развития тяжелой дыхательной недостаточности или нарушения сердечного ритма. Обязательна срочная госпитализация больных в отделения интенсивной терапии. В фазе прогрессирования — почасовое наблюдение за состоянием больного с оценкой дыхательной функции, сердечного ритма, артериального давления, состояния бульбарной мускулатуры, тазовых функций. Ранние признаки дыхательной недостаточности: ослабление голоса, необходимость делать паузы для вдоха во время разговора, выступание пота на лбу и тахикардия при форсированном дыхании, ослабление кашля. При бульбарном параличе бывают необходимы интубация и введение назогастрального зонда. Плазмаферез и иммуноглобулин внутривенно, способные ускорять восстановление и уменьшать остаточный дефект, особенно целесообразны в фазе прогрессирования (обычно в первые 2–3 недели от начала заболевания). Кортикостероиды не улучшают исход заболевания. В целях профилактики тромбоза глубоких вен голени (при плегии в ногах) назначают малые дозы гепарина или низкомолекулярный гепарин (фраксипарин). При парезе мимической мускулатуры необходимы меры по защите роговицы (закапывание глазных капель, повязка на ночь). Большое значение имеют ранние реабилитационные мероприятия, включающие массаж, лечебную гимнастику, другие физиотерапевтические процедуры (парафиновые аппликации, магнитотерапия, радоновые и сероводородные ванны, электростимуляция и другие).
Прогноз
Полное восстановление — в 70% случаев, у 15% больных сохраняются выраженные остаточные параличи, вызывающие инвалидизацию. В 2–5% развивается рецидив и формируется хроническая рецидивирующая полиневропатия.
Список литературы находится в редакции
Детальніше