
СПОКОЕН МАЛЫШ - ДОВОЛЬНА МАМА
 Современный рынок товаров по уходу за грудными детьми стремительно развивается. Появились многие инновационные аксессуары, облегчающие повседневную жизнь с малышом. Расширяется и выбор сосок-пустышек — оригинальные формы, дизайн, способы использования. Несмотря на современные рекомендации, ограничивающие использование пустышек у детей, находящихся на грудном вскармливании, мамы сохраняют приверженность к этому традиционному детскому аксессуару
Современный рынок товаров по уходу за грудными детьми стремительно развивается. Появились многие инновационные аксессуары, облегчающие повседневную жизнь с малышом. Расширяется и выбор сосок-пустышек — оригинальные формы, дизайн, способы использования. Несмотря на современные рекомендации, ограничивающие использование пустышек у детей, находящихся на грудном вскармливании, мамы сохраняют приверженность к этому традиционному детскому аксессуару
Действительно, многие «подобные эффекты» применения пустышки обусловлены не пустышкой как таковой, а ее неправильной, нефизиологичной для малыша формой. Поэтому хорошо, если врач-педиатр, наблюдающий ребенка, поможет маме не растеряться в существующем разнообразии детских товаров и принять оптимальное для здоровья и развития крохи решение.
В интересах ребенка
Продукция под торговой маркой BABY-NOVA™ производится заводами NOVATEX GmbH (Германия) почти три десятилетия. Ассортимент товаров широк — это аксессуары для кормления, гигиеническая продукция, а также игрушки. Вся продукция выполнена из высококачественных пищевых полимеров, разрешенных к использованию в странах Европы. Строгий контроль товаров марки BABY-NOVA™ на соответствие мировым стандартам качества позволяет добиваться их безусловной безопасности для ребенка. Тесное взаимодействие производственных мощностей BABY-NOVA™ с научно-исследовательскими лабораториями и клиниками Германии позволяет использовать передовые разработки ученых, а также оперативно реагировать на практические пожелания врачей-педиатров, гастроэнтерологов, детских ортодонтов, логопедов и психологов. Благодаря удобству и привлекательному фирменному дизайну эта продукция популярна не только в Европе, но также в США. Руководство компании подчеркивает, что достижение успеха было обусловлено качеством, ориентированностью на потребителя и честностью на рынке.
Компания BABY-NOVA™ выпускает товары, необходимые повседневно. Благодаря официальному дистрибьютору в Украине, корпорации «Европродукт», полная линия продуктов по уходу за малышами уже хорошо знакома и отечественным потребителям. Самым популярным товаром, согласно результатам опросов, в течение многих лет остается пустышка BABY-NOVA™.
Пустышка: использовать правильно — ребенку на пользу
 Детям, находящимся на грудном вскармливании, в наше время не принято предлагать пустышку: этот пункт прописан в действующих клинических протоколах по уходу за здоровым ребенком — как в Украине, так и в зарубежных странах. Причина такой «дискриминации» — возможное снижение у малыша желания сосать грудь. Тем не менее, речь идет не о строгом запрете, а о рекомендации; опыт многих матерей показывает, что при условии правильного выбора пустышки и умеренного по времени ее использовании качество прикладывания к груди не страдает. Сосательный рефлекс далеко не у всех детей, находящихся как на грудном вскармливании, так и на искусственном, ограничивается временем сосания груди и бутылочки. Поэтому им пустышка периодически необходима для удовлетворения сосательного рефлекса в первые недели и месяцы жизни, для расслабления, успокоения, облегчения засыпания.
Детям, находящимся на грудном вскармливании, в наше время не принято предлагать пустышку: этот пункт прописан в действующих клинических протоколах по уходу за здоровым ребенком — как в Украине, так и в зарубежных странах. Причина такой «дискриминации» — возможное снижение у малыша желания сосать грудь. Тем не менее, речь идет не о строгом запрете, а о рекомендации; опыт многих матерей показывает, что при условии правильного выбора пустышки и умеренного по времени ее использовании качество прикладывания к груди не страдает. Сосательный рефлекс далеко не у всех детей, находящихся как на грудном вскармливании, так и на искусственном, ограничивается временем сосания груди и бутылочки. Поэтому им пустышка периодически необходима для удовлетворения сосательного рефлекса в первые недели и месяцы жизни, для расслабления, успокоения, облегчения засыпания.
Как правильно выбрать пустышку? Прежде всего, она должна быть анатомической формы. Установлено, что гармоничное развитие челюстно-лицевого аппарата в раннем детстве влияет на здоровье ребенка в целом. Исследования подтверждают, что большинство ортодонтических и многие стоматологические проблемы, нарушения речи и патология носового дыхания во взрослом возрасте — в буквальном смысле родом из детства. Однако не стоит забывать, что еще в недавнем прошлом все используемые соски и пустышки обладали нефизиологическими свойствами. Их невозможно даже сравнивать с современными ортодонтическими пустышками!
Ваша любимая пустышка
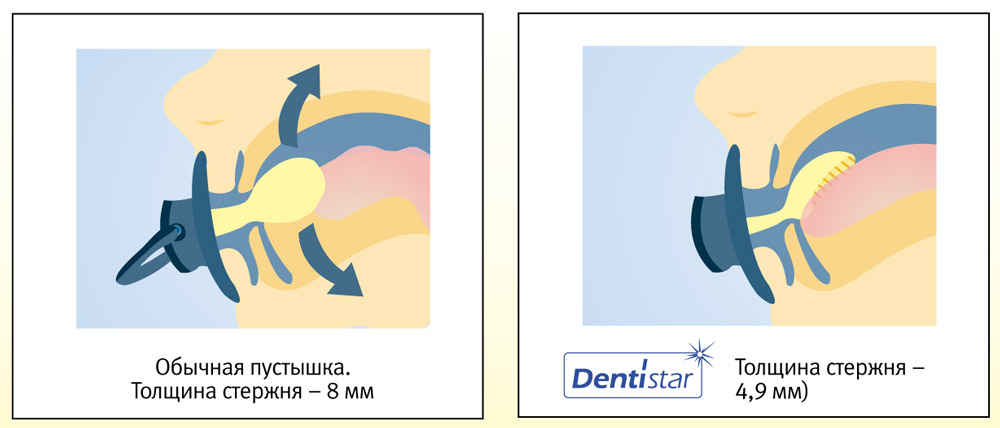 В 2009 году компания BABY-NOVA™ представила украинским потребителям первую в мире стоматологическую соску Dentistar. Новая модель пустышки разработана в тесном сотрудничестве с учеными и врачами; она не просто физиологична, но также способствует профилактике ортодонтических нарушений у детей в молочном прикусе. Преимущества Dentistar обсуловлены ее объективными свойствами:
В 2009 году компания BABY-NOVA™ представила украинским потребителям первую в мире стоматологическую соску Dentistar. Новая модель пустышки разработана в тесном сотрудничестве с учеными и врачами; она не просто физиологична, но также способствует профилактике ортодонтических нарушений у детей в молочном прикусе. Преимущества Dentistar обсуловлены ее объективными свойствами:
- Тонкий стержень обеспечивает минимальное давление на челюсти малыша при сосании.
- Свободное расположение языка достигается наличием вогнутости в нижней части соски, благодаря чему соска прижимается к нёбу. Язык в этом случае занимает естественное положение — точно как при сосании материнской груди!
- Ступенька в стержне — дополнительная особенность, «работающая» на достижение естественного соотношения плоскостей верхней и нижней челюстей.
Чтобы у малыша с рождения формировался правильный прикус, а впоследствии прекрасная улыбка, важно правильно подбирать размер соски BABY-NOVA™:
1 – рекомендуется для малышей первых недель и месяцев жизни, у которых еще не появились зубки;
2 – рекомендуется детям после полного прорезывания первого зуба (во втором полугодии жизни).
Под маркой BABY-NOVA™ выпускаются ортодонтические пустышки не только традиционной, всем привычной формы, но также пустышки без кольца, которые во всем мире используются во время сна ребенка (чтобы он не мог случайно вытянуть соску изо рта). Все пустышки BABY-NOVA™ имеют яркий и запоминающийся дизайн, и поэтому порадуют малыша в качестве развивающих элементов его среды.
Консультируя мать, педиатр обязан напомнить ей о гигиенических аспектах применения пустышки: перед первым употреблением изделие необходимо прокипятить в течение нескольких минут; в первые недели жизни малыша пустышку часто моют и обдают кипяченой водой. Пустышку из латекса, как правило, нужно менять 1 раз в 3 месяца.
BABY-NOVA™: выбрать лучшее для малыша
 Когда обстоятельства складываются так, что грудное вскармливание невозможно, малышу необходим докорм. Очевидно, что в случае перевода ребенка на смешанное или искусственное вскармливание родителям крохи предстоит совместно с педиатром выбирать не только адаптированную молочную смесь, но и бутылку с соской. Подобный выбор неизбежен и для родителей малышей на грудном вскармливании — когда в 6 месяцев наступает время введения прикорма (одно из первых блюд — жидкая каша) и дополнительного питья.
Когда обстоятельства складываются так, что грудное вскармливание невозможно, малышу необходим докорм. Очевидно, что в случае перевода ребенка на смешанное или искусственное вскармливание родителям крохи предстоит совместно с педиатром выбирать не только адаптированную молочную смесь, но и бутылку с соской. Подобный выбор неизбежен и для родителей малышей на грудном вскармливании — когда в 6 месяцев наступает время введения прикорма (одно из первых блюд — жидкая каша) и дополнительного питья.
BABY-NOVA™ предлагает широкий выбор бутылочек и сосок для допаивания и кормления грудных детей. Бутылочки, которые выпускаются двух размеров (объемом 125 и 250 мл) изготовлены из традиционного прочного стекла или экологичного, сертифицированного пластика. Бутылочку можно подобрать на любой вкус — классическую или с держателем удобной формы, с разноцветным декоративным покрытием.
Соски BABY-NOVA™ выпускаются в удобных блистерах по две штуки и представлены в трех вариантах:
- для чая, воды, компота, сока;
- для грудного молока или его заменителей;
- для густой пищи (например, каши).
Все они имеют противоколиковый клапан.
Практичность сосок BABY-NOVA™ и выгодное отличие от аналогичной продукции других компаний заключается в том, что соски BABY-NOVA™ подходят для большинства бутылочек других производителей.
Многие родители задают педиатру вопрос: «Какую соску лучше выбрать — латексную или силиконовую?». Правильным будет ответ: «И то, и другое вполне приемлемо. Важно присмотреться к ребенку и понять его желания». При этом врач может кратко перечислить свойства латекса (натуральный продукт на растительной основе, мягкий и нежный по структуре, пластичный и прочный «на укус», но при этом хуже переносит длительную термическую обработку, легко поддается воздействию ферментов слюны и в результате меняет форму, приобретает шероховатость поверхности, из-за чего подвергается повышенной колонизации микроорганизмами). И свойства силикона (синтетический материал, несколько плотнее латекса, не впитывает и не удерживает запахи, нейтрален на вкус и особо устойчив к воздействию высоких и низких температур, ферментов слюны, поэтому не деформируется).
Помимо сосок и пустышек, компания BABY-NOVA™ выпускает широкий ассортимент всевозможных аксессуаров, предметов для кормления, ухода за ребенком и различных полезных мелочей. У кормящих матерей популярна продукция BABY-NOVA™, содействующая грудному вскармливанию — это всевозможные накладки на соски (облегчающие прикладывание малыша к груди), молокоотсос, удобные гигиенические прокладки для груди.
BABY-NOVA™ — одна из немногих компаний в мире, ассортимент которой включает все необходимые товары по уходу за детьми в возрасте от 0 до 3 лет. Вся продукция BABY-NOVA™ имеет премиальное качество, в то время как цена ее благодаря политике компании-дистрибьютора остается доступной для украинской семьи с любым уровнем достатка.
Детальніше
КОРМЛЕНИЕ ГРУДЬЮ: о чем еще нужно помнить на старте
 Врачам, ежедневно работающим с кормящими грудью женщинами и их детьми, хорошо известно, что если с самого начала у мамы и малыша что-то пошло не так, как должно быть, потом ситуацию исправить очень трудно. Статистика безжалостна: глобальный мониторинг ВОЗ указывает на то, что только 39% новорожденных во всем мире получают исключительно грудное вскармливание в возрасте до четырех месяцев
Врачам, ежедневно работающим с кормящими грудью женщинами и их детьми, хорошо известно, что если с самого начала у мамы и малыша что-то пошло не так, как должно быть, потом ситуацию исправить очень трудно. Статистика безжалостна: глобальный мониторинг ВОЗ указывает на то, что только 39% новорожденных во всем мире получают исключительно грудное вскармливание в возрасте до четырех месяцев
К сожалению, большинство женщин, прекращающих кормить грудью в первые три месяца после родов, делают это по банальной причине – они не получают должной поддержки в первую очередь от нас, специалистов. Кому-то из врачей не хватает времени разобраться в проблеме, с которой столкнулась женщина, кому-то – терпения, а кому-то – знаний. Но ведь не стыдно не знать, стыдно не учиться, а врачи, как известно, учатся не до старости, а до смерти. Поэтому мы предлагаем некоторые теоретические и практические моменты, связанные с налаживанием кормления грудью, которые иногда не так очевидны, но очень важны «на старте».
Хорошо известно, что в первые месяцы после родов лактация – почти полностью гормонозависимый процесс. Контролируют выработку и выделение молока множество гормонов, но две главные партии в этом действе играют пролактин и окситоцин.
Как работает пролактин
Когда ребенок сосет грудь, сенсорные импульсы от соска поступают в мозг. В ответ на них гипофиз выделяет пролактин, который поступает в кровь и заставляет специальные клетки лактоциты вырабатывать молоко.
Сильнее всего повышается уровень пролактина через 30 минут после кормления — в 10–20 раз по сравнению с уровнем до начала кормления. Молоко, выработанное под воздействием этого пролактина, ребенок будет сосать в следующий раз. В текущее кормление ребенок высасывает молоко, которое уже есть в груди плюс то молоко, которое вырабатывается в процессе кормления. Из этого следует, что если ребенок будет сосать больше, у матери будет больше молока. Следовательно, частое сосание груди способствует выработке молока.
Если у матери двойня, и оба ребенка сосут грудь – она будет «работать» на двоих детей. Если ребенок прекращает сосать, грудь вскоре перестает вырабатывать молоко.
Напомним также, что ночью пролактина вырабатывается больше. Поэтому ночные кормления должны быть в обязательном порядке, чтобы мать смогла создать «запасы».
Некоторые люди полагают, что для того, чтобы у матери вырабатывалось молоко, она должна лучше питаться, больше пить, больше отдыхать или принимать лекарства. Конечно, очень важно, чтобы мать получала достаточно еды и питья, но это НЕ поможет ей вырабатывать больше молока, если ребенок не сосет грудь или сосет недостаточно.
Теория рецепторов пролактина
Пролактин необходим для того, чтобы молоко синтезировалось. На клеточных стенках лактоцитов есть рецепторы, которые позволяют клеткам реагировать на пролактин. Если рецепторов нет – клетка будет нечувствительна к гормону, какой бы высокой ни была его концентрация в крови.
Исследования De Carvalho et al (1983); Hinds & Tindale-Biscoe (1982); Zuppa et al (1988) показали, что частые кормления в первые недели после родов, когда уровень пролактина еще очень высок сам по себе и еще больше повышается после кормлений, приводят к образованию большего количества рецепторов к пролактину на поверхности лактоцитов. Это происходит благодаря тому, что срабатывает положительная обратная связь: выше уровень пролактина – больше образуется рецепторов. Большее количество рецепторов означает, что клетки становятся более чувствительными к пролактину.
Сразу же после родов уровень гормона пролактина очень высок. После полутора-двух месяцев жизни ребенка его уровень значительно падает, по-прежнему повышаясь после кормлений (рис. 1). При этом ребенок получает все необходимое ему молоко, тот же объем, что и раньше, просто основными регулирующими факторами становятся степень и частота опорожнения груди, так называемый аутокринный контроль.
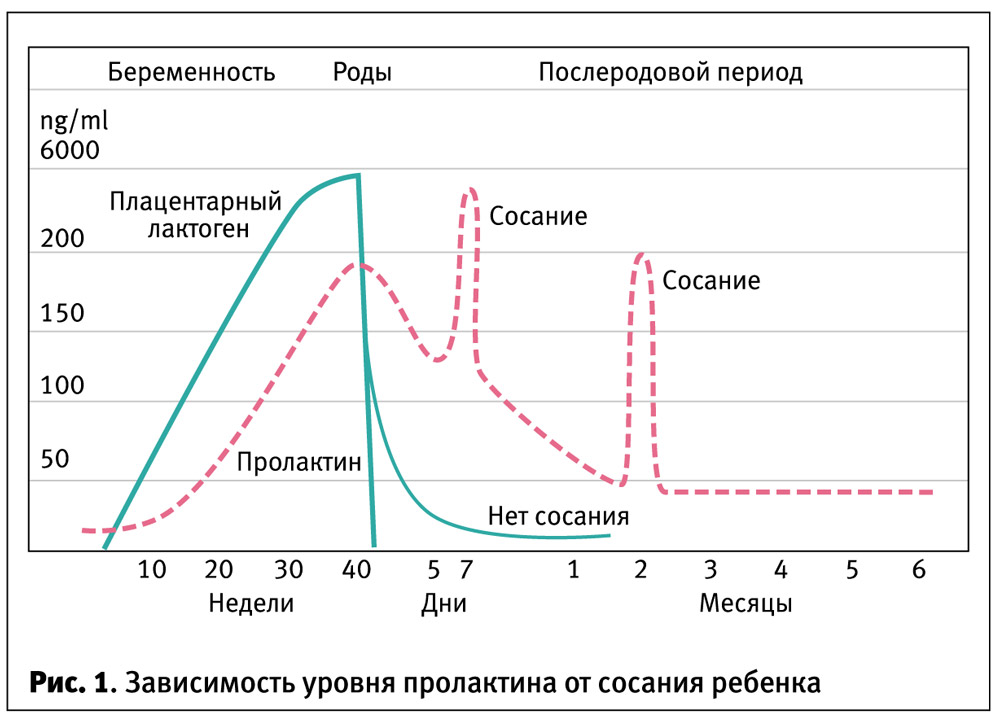
Таким образом, можно сделать очень важный вывод: длительная успешная лактация зависит от того, заложилось ли у кормящей женщины адекватное количество рецепторов к пролактину. Поэтому очень важно не ограничивать частоту и длительность кормлений.
Хотя часть женщин может «на волне» высокого пролактина, обусловленного родами, успешно последовать ошибочным советам ввести режим, это может привести к сложностям с количеством молока позже, когда уровень пролактина упадет. Эксперты Lisa Marasco и Jan Barger пишут в своей статье в Breastfeeding Abstracts (May 1999, v.18, 4, pp. 28-29): «Мы обнаружили, что многие женщины успешно кормят детей по расписанию в первые месяцы после родов. Но через 3–4 месяца после родов среди кормящих по расписанию наблюдается необычно высокий показатель нехватки молока. Это видно по снижению набора веса ниже допустимых норм среди детей, которых кормят по временному режиму, необходимости докорма и/или вынужденному прекращению кормления, потому что дети предпочитают быстрый напор молока из бутылки медленному напору молока из груди». Об этом свидетельствует и статистика, приведенная в самом начале этой статьи.
Практические рекомендации: как помочь матери поддерживать достаточный уровень пролактина
- прикладывайте ребенка так часто, как он просит;
- правильно прикладывайте ребенка к груди, НЕ давайте ему пустышку и другие заменители соска;
- кормите его так долго, как он захочет;
- кормите и днем, и (это особенно важно!) ночью.
При чем здесь пустышка, спросите вы? Как было сказано выше, сосание груди вызывает скачок уровня пролактина у матери. Когда ребенок сосет пустышку, грудь не получает сигнал от ребенка, что надо вырабатывать молоко. Уровень пролактина у матери не повышается. Это сосание – холостой выстрел: ребенок затратил энергию, подал сигнал – но этот сигнал не будет иметь необходимого эффекта. Кроме того, сосание пустышки сопряжено и с другими нежелательными последствиями, но об этом в другой раз.
Длительная успешная лактация зависит от того, заложилось ли у кормящей женщины адекватное количество рецепторов к пролактину
Окситоцин – гормон, отвечающий за выделение молока
Пролактин и окситоцин работают в паре. Это очевидно: пролактин простимулировал лактоциты, молоко образовалось, теперь очередь окситоцина – молоко должно выделиться из груди.
Отрицательного давления, создаваемого в полости рта ребенка при сосании и сцеживающих движений язычка ребенка недостаточно, чтобы извлечь молоко из сложной системы чрезвычайно тонких протоков. Этому будут препятствовать силы поверхностного натяжения. Поэтому сама грудь помогает ребенку получать молоко.
Когда ребенок сосет грудь, в мозг матери поступают сенсорные импульсы от соска. В ответ задняя доля гипофиза выделяет в кровь гормон окситоцин (окситоцин вырабатывается в супраоптическом и паравентрикулярном ядрах гипоталамуса и затем транспортируется в заднюю долю гипофиза, где депонируется и выделяется в кровь).
Окситоцин в крови заставляет сокращаться миоэпителиальные клетки, окружающие альвеолы и мелкие протоки. В результате молоко начинает течь по направлению из альвеол к большим протокам под ареолой и далее к выводящим протокам соска. Это молоко высасывает ребенок во время кормления.
Окситоциновый рефлекс запускается не только в ответ на сосание. Он может сработать еще до того, как ребенок начинает сосать – в ответ на мысли матери о ребенке, его запах, издаваемые ребенком звуки, когда мать знает, что пришло время кормления.
Если окситоциновый рефлекс работает неэффективно, у ребенка могут быть трудности с получением молока. Можно подумать, что грудь перестала вырабатывать молоко. Тем не менее, молоко в груди вырабатывается, но не вытекает.
Еще одно важное свойство окситоцина заключается в том, что он способствует сокращению матки после родов. Это помогает снизить риск кровотечения, но иногда вызывает боль в матке и прилив крови во время кормления в первые несколько дней после родов. Эти болевые ощущения могут быть довольно сильными.
Уровень окситоцина в крови во время кормления не постоянен, он изменяется волнообразно. После выброса окситоцина в кровь в ответ на сосание или другой адекватный стимул, его уровень падает уже через несколько минут. Соответственно, поток молока из груди то усиливается (что говорит о том, что в данный момент в крови высокий уровень окситоцина), то ослабевает (уровень окситоцина уменьшился). Наблюдая за кормлением ребенка, можно увидеть, что он то сосет медленно, глубоко, активно глотает молоко, то посасывает грудь быстро и легко, то опять начинает глотать. Как правило, окситоциновый рефлекс, отвечающий за выделение молока, срабатывает несколько раз за кормление.
У разных пар «мать–ребенок» и даже у одной и той же пары в разные кормления рефлекс окситоцина срабатывает различное количество раз. Как показали исследования группы Питера Хартманна (с применением ультразвука), разные дети высасывают различное количество молока в одно срабатывание рефлекса (рис. 2). Были зарегистрированы кормления, когда рефлекс срабатывал всего один раз и ребенок высасывал большой объем молока, насыщался и выпускал грудь. Также были кормления, когда рефлекс молока срабатывал неоднократно, дети получали небольшую порцию молока с каждым новым срабатыванием.
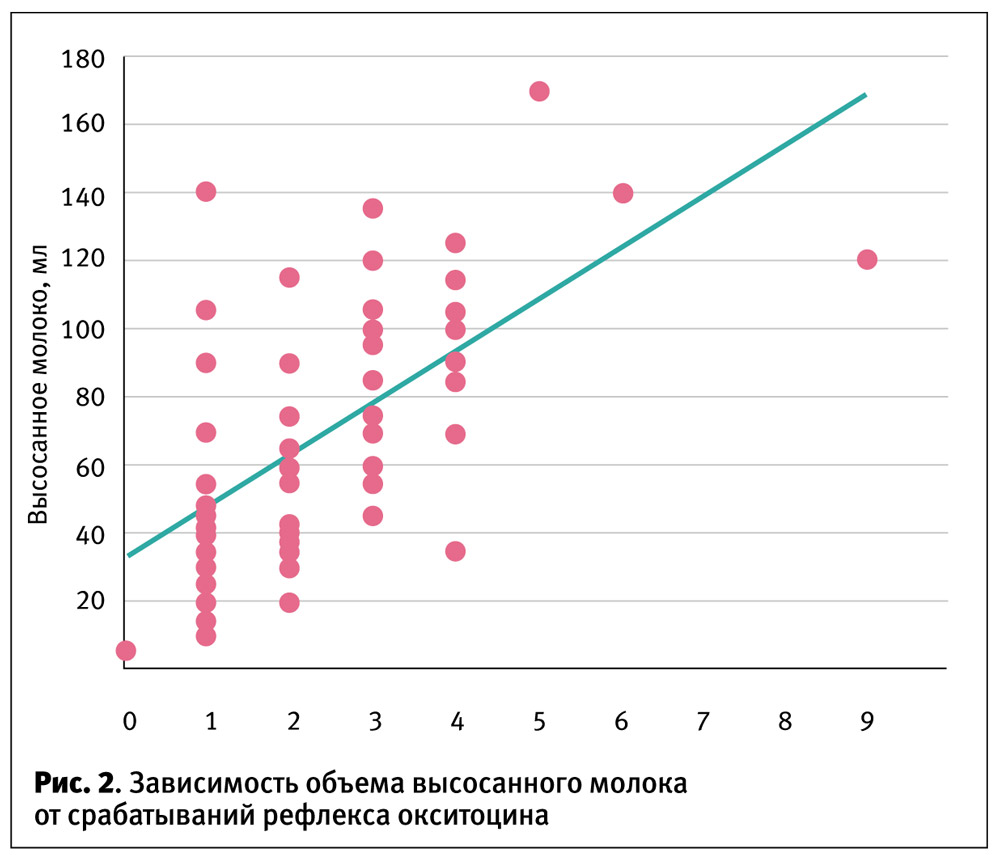
Бытует мнение, что ребенок за первые 5 минут высасывает 90% молока, находящегося в груди, поэтому не имеет смысла держать его у груди существенно дольше. Однако данное исследование показывает, что на самом деле это далеко не всегда не так, и необходимо ориентироваться на аппетит ребенка, давать ему возможность самому отпустить грудь, иначе есть риск, что ребенок недополучит нужное ему количество молока. Ведь каждая пара «мать–ребенок» уникальна.
Также важно понимать, что фраза «ребенок сосет грудь как пустышку», описывающая сосание, при котором ребенок держит во рту грудь и редко глотает молоко, очень опасна для мам, особенно на этапе становления лактации. Эта фраза подрывает уверенность матери в себе и своих инстинктах. Каждое последующее срабатывание рефлекса окситоцина все менее ощутимо для матери и когда кому-то кажется, что ребенок «сосет грудь как пустышку», на самом деле молоко может попадать к малышу. Важно помнить и то, что такое «непитательное» сосание, т. е. легкое быстрое посасывание в перерывах между срабатываниями рефлекса выделения молока из груди, способствует выработке новой порции окситоцина, тем самым обеспечивая больше молока в данное кормление, а также повышает уровень пролактина, стимулируя выработку молока для следующего кормления, а кроме того, успокаивает ребенка, стабилизируя его дыхание, температуру и сердцебиение.
Практические рекомендации: как помочь матери поддерживать высокий уровень окситоцина
Рефлекс окситоцина более сложен, чем рефлекс пролактина. На него могут оказывать влияние мысли, эмоции и чувства матери. Положительное мышление, например, чувство радости материнства или любви к ребенку, и чувство уверенности в том, что грудное молоко лучшее для ребенка, способствуют окситоциновому рефлексу и вытеканию молока. Такие ощущения, как прикосновения к ребенку, образ ребенка, звук детского плача также способствуют работе этого рефлекса.
Однако отрицательные эмоции, например, боль, беспокойство, сомнение в том, что у женщины достаточно молока, могут приостановить действие рефлекса и прекратить вытекание молока. К счастью, этот эффект обычно носит временный характер.
Необходимо, чтобы ребенок был все время рядом с матерью, чтобы она могла его касаться, видеть, отвечать ему. Если мать и ребенок разлучаются между кормлениями, окситоциновый рефлекс у матери будет работать не так эффективно.
Поэтому так важно в работе с женщинами помнить об их чувствах. Очень важно в нужную минуту успокоить мать и вселить в нее уверенность. Ведь от психологического комфорта мамы напрямую зависит успех кормления.
Ингибиторы в грудном молоке
Секреция грудного молока также контролируется самой молочной железой. Если ребенок перестает сосать одну грудь, но продолжает сосать вторую, то в первой груди молоко постепенно перестает вырабатываться, тогда как во второй секреция молока продолжается. При этом и окситоцин, и пролактин поступают в обе груди в одинаковых количествах.
В самом грудном молоке имеется вещество, которое замедляет его выработку, своеобразная «встроенная защита» от переполнения. Это вещество назвали «фактор – ингибитор лактации» или просто «ингибитор». Чем больше грудь остается наполненной, тем медленнее вырабатывается в ней новое молоко. Это помогает защитить молочную железу от отрицательных последствий переполнения. Выработка молока может полностью прекратиться, если молоко из груди не удаляется долго. Это очевидно необходимо в случае, если ребенок умирает или прекращает сосать грудь по другим причинам.
При опустошении груди путем сосания или сцеживания вместе с молоком удаляется и ингибитор. Благодаря этому синтез молока идет быстрее и за единицу времени молочная железа вырабатывает больше молока. Чем более опорожнена грудь, тем быстрее вырабатывается в ней новое молоко. Теперь становится понятным, почему:
- для увеличения выработки молока рекомендуется не накапливать молоко, а наоборот, прикладывать ребенка к груди как можно чаще и давать обе груди в кормление;
- если ребенок перестает сосать одну грудь, она перестает вырабатывать молоко;
- если ребенок больше сосет из одной груди, в этой груди вырабатывается больше молока, и она становится продуктивнее и больше другой;
- лактацию можно остановить только в одной груди (иногда необходимо для медицинских вмешательств).
Для того, чтобы секреция молока не прекращалась, грудь должна опустошаться. Здоровый ребенок в состоянии сам регулировать секрецию молока у матери, так что молока вырабатывается именно столько, сколько ему нужно в данный момент. Иногда дети сосут чаще, при этом скорость выработки молока увеличивается. Бывают периоды, когда дети прикладываются к груди реже, тогда скорость выработки молока замедляется.
Если ребенок по какой-то причине не может прикладываться к груди, молоко надо сцеживать, чтобы обеспечить продолжение лактации. Это очень важный момент.
Для эффективного выделения молока необходимо правильное прикладывание
Молоко хорошо поступает к ребенку, если он удобно расположен у груди и глубоко захватил не только сосок, но и значительный участок ареолы. В этом случае комбинация сцеживающих движений язычка и нижней челюсти ребенка, а также изменения давления в ротовой полости ребенка не травмируют грудь, а вызывают активное срабатывание рефлекса у матери и позволяют ребенку эффективно высасывать поступающее молоко. У разных пар «мать–ребенок» могут быть свои излюбленные положения для кормления. Поэтому женщинам может потребоваться квалифицированная помощь при выборе правильного положения ребенка у груди и прикладывания.
«Большинство детей, которые медленно прибавляют или теряют в весе, делают это не потому, что у их матерей мало молока, а потому, что ребенок не получает того молока, которое есть у матери» Д-р Джек Ньюмен, MD, FRCPC
Кроме того, детям не следует давать бутылки и пустышки. Если ребенка начали кормить из бутылки до того, как грудное вскармливание наладилось, это может нарушить эффективность сосания. Ребенок сосет бутылку и пустышку не так, как грудь, он учится другим движениям и другой технике сосания. Рот у ребенка, сосущего соску, закрыт, он использует десны для того, чтобы добывать молоко из бутылки. Даже те дети, которых начинают кормить из бутылки через несколько недель, могут испытывать трудности с сосанием.
Неправильно приложенный ребенок не может эффективно высасывать молоко из груди, поэтому у матери могут возникнуть нагрубание и застой молока. Из-за того, что ребенок не может эффективно высасывать молоко, он может компенсировать это увеличением длительности и/или частоты кормлений. Мать может характеризовать это как «постоянно висит на груди». При этом ребенок может быть беспокойным, плакать и недостаточно набирать вес. Кроме того, если грудь не опустошается эффективно в течение длительного времени, выработка молока уменьшается.
Практические рекомендации: как помочь матери правильно приложить ребенка к груди
- При консультировании и помощи матери в кормлении грудью очень важно проверить наличие ВСЕХ ЧЕТЫРЕХ признаков правильного прикладывания ребенка к груди: рот широко открыт, нижняя губа вывернута наружу, больше ареолы видно над верхней губой ребенка, подбородок прижат у груди. Если хотя бы один отсутствует, нельзя говорить, что ребенок правильно приложен к груди. Кроме этого, важным признаком того, что ребенок приложен правильно, являются ощущения матери – кормление должно быть комфортным для нее.
- Не давайте ребенку никаких имитаторов груди. Если ребенок нуждается в докорме, то его нужно давать любым альтернативным способом (ложка, шприц, чашка), но только не с помощью соски. Лучше всего докармливать ребенка с помощью системы докорма у груди.
Используй или потеряй!
Часто матери, которые беспокоятся, что их ребенок не получает достаточно молока, получают ошибочные советы «накопить молоко к кормлению», «подождать, пока грудь наберется». На самом деле это может привести к снижению лактации. Для того, чтобы ребенок получил больше молока, следует рекомендовать обратное – более частые кормления. Необходимо предостерегать матерей от «накапливания» молока.
Пищевые рефлексы новорожденного
Природа позаботилась не только о рефлексах матери, обеспечивающих ребенка молоком, но и том, чтобы ребенок был готов его получить. Какие же пищевые рефлексы имеются у новорожденного?
Ребенок запрограммирован природой на мягкий переход от внутриутробной жизни к внеутробной. После рождения у ребенка включается запрограммированное поведение, и ребенок начинает искать источник пищи – материнскую грудь. Именно аппетит ребенка регулирует количество молока у матери. Это так называемый закон «спроса и предложения». Поэтому если прикладывать ребенка к груди тогда, когда он демонстрирует признаки голода, и не ограничивать длительность кормлений, ребенок отрегулирует выработку молока оптимальным образом.
У ребенка имеются три основных рефлекса, задействованных в питании – поисковый, сосательный и глотательный. Когда что-либо касается губ или щеки ребенка, он открывает рот и поворачивает голову в поисках этого объекта. Он высовывает язык вперед и вниз. Это называется «поисковый рефлекс». Как правило, ребенок находится «в поисках» груди. Когда что-либо касается неба ребенка, он начинает сосать. Это – сосательный рефлекс. Когда рот ребенка наполняется молоком, он его глотает. Это – глотательный рефлекс. Все эти рефлексы функционируют автоматически, ребенку не нужно ничему учиться.
Практические рекомендации: как определить готовность ребенка к кормлению
Своим поведением ребенок дает матери понять, что он готов к кормлению. Сначала он начинает ерзать, проявлять беспокойство, делать сосательные движения, засовывать пальцы в рот. Если он спит, то можно заметить быстрые движения глаз, при этом он может издавать тихие звуки, похожие на вздохи. Это ранние признаки готовности к кормлению и это оптимальное время для того, чтобы предложить ему грудь. В этом случае ребенок будет более терпелив у груди, его легче будет правильно приложить, при этом он будет сосать дольше и активнее. Если же мать упустит эти ранние признаки или будет ждать, когда малыш начнет плакать, то в таком случае крик и беспокойство могут утомить его, ему будет сложнее правильно захватить грудь, он может травмировать сосок и сосать неэффективно. При этом ребенок может быстро утомиться и заснуть раньше, чем насытится. Никто не может хорошо выполнять свою работу, если голоден и расстроен. Ребенок лучше возьмет грудь, будет дольше и эффективнее сосать, если мама не будет ждать плача.
Нормальный ритм кормления новорожденного – кормление сериями
 Ритм кормления новорожденного ребенка отличается от ритма кормления ребенка в возрасте, например, одного месяца. Было замечено и описано в литературе, что новорожденные сосут в течение короткого времени, затем отпускают грудь, а через 15–30 минут снова могут проявить признаки готовности к кормлению. После нескольких кормлений новорожденный засыпает на более долгое время.
Ритм кормления новорожденного ребенка отличается от ритма кормления ребенка в возрасте, например, одного месяца. Было замечено и описано в литературе, что новорожденные сосут в течение короткого времени, затем отпускают грудь, а через 15–30 минут снова могут проявить признаки готовности к кормлению. После нескольких кормлений новорожденный засыпает на более долгое время.
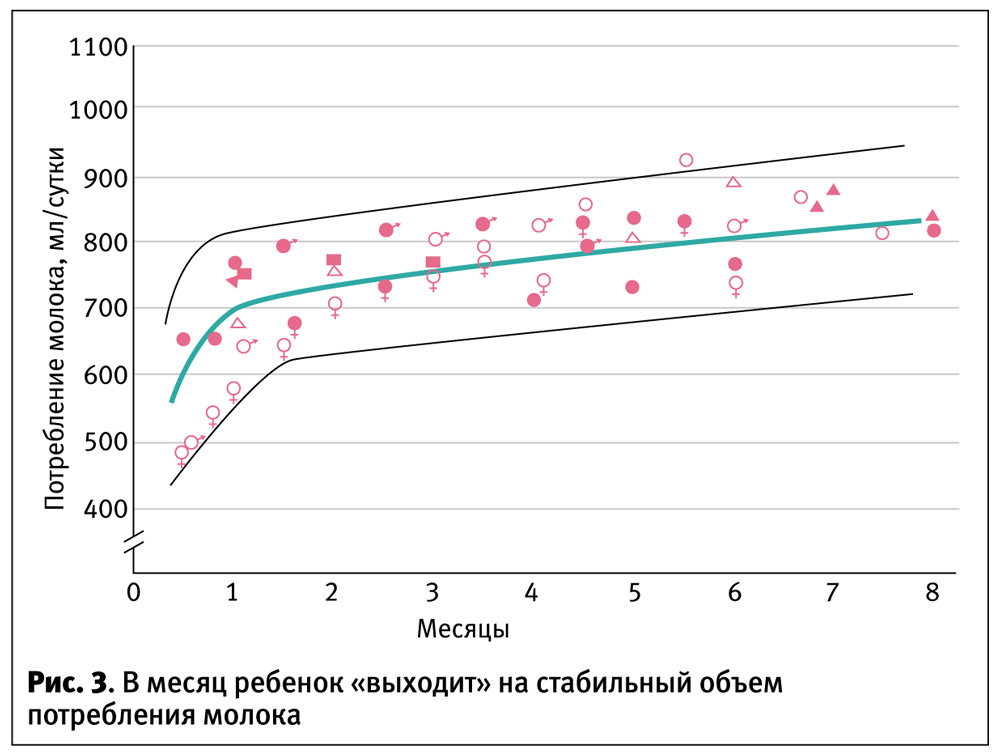
Поскольку вместимость желудка новорожденного очень невелика, ему не нужно большое количество пищи – ребенок может съесть до 5 мл молозива на одно кормление в первый день. В первые 24 часа после родов ребенок высасывает небольшое количество молозива, приблизительно до 37 мл за сутки. Секреция молока увеличивается постепенно в первые 36 часов, а после – резко возрастает в следующие 49–96 часов. К пятому дню объем выработки молока может достичь 400–500 мл в сутки. К месяцу младенцы в среднем потребляют 750±150 мл молока в сутки. Этот объем медленно увеличивается до около 800 мл в день к шести месяцам, причем цифра может варьировать в пределах от 550 до 1150 мл. Как показано на рис. 3, объединяющем результаты нескольких исследований, суточный объем молока, потребляемого здоровыми детьми на грудном вскармливании, в интервале от 1 до 6 месяцев почти не меняется. Этим дети на грудном вскармливании отличаются от искусственников, которые съедают все большие объемы молока с возрастом. После того, как в рацион ребенка вводятся другие продукты, суточный объем молока постепенно снижается.
Секреция грудного молока напрямую зависит от потребностей ребенка. В разные кормления в течение дня ребенок потребляет молоко в различном объеме. Аппетит ребенка не постоянен: в одно кормление он высасывает больше, в другое – меньше. Кормление сериями и длительное кормление – обычные компоненты грудного вскармливания. Матери должны быть готовы к быстрому росту детей в возрасте 3, 6 и 12 недель. В такие периоды дети могут просто «висеть» на груди, и жизнь матери на 3–4 дня превращается в сплошную кормежку. Через несколько недель после родов грудь становится мягче и меньше. По мере того, как устанавливается лактация, ощущения в груди могут меняться.
Сталкиваясь с перечисленными явлениями, да и вообще с какими-либо проблемами в процессе грудного вскармливания, матери часто начинают сомневаться в своей способности кормить грудью. Поэтому им очень важно получить квалифицированную поддержку и достоверную информацию.
Литература
- UNICEF Global Database on Breastfeeding Indicators as of March 2006. http://www.childinfo.org/areas/breastfeeding/countrydata.php.
- Infant and Young Child Feeding Counselling: An Integrated Course. Trainer’s Guide, WHO 2006.
- Jan Riordan, Breastfeeding and Human Lactation. Third edition, 2005.
- Оптимальное вскармливание новорожденных в родовспомогательных учреждениях. Проект «Здоровье матери и ребенка», 2011.

ГІПОТЕРМІЯ: нові можливості у лікуванні асфіксії
Частота перинатальної асфіксії, за даними ВООЗ, становить ~1–1,5% у більшості неонатальних центрів і зазвичай залежить від гестаційного віку і маси тіла при народженні [S. Shankaran, 2010]. У розвинених країнах частота виникнення асфіксії середнього та тяжкого ступеня у дітей складає 1–2 випадки на 1000 пологів у терміні більше 37 тижнів; приблизно 25% новонароджених помирають у відділеннях інтенсивної терапії та 40% немовлят, які вижили, мають ДЦП, інші – різного ступеня неврологічні розлади [N. J. Robertson, 2011].
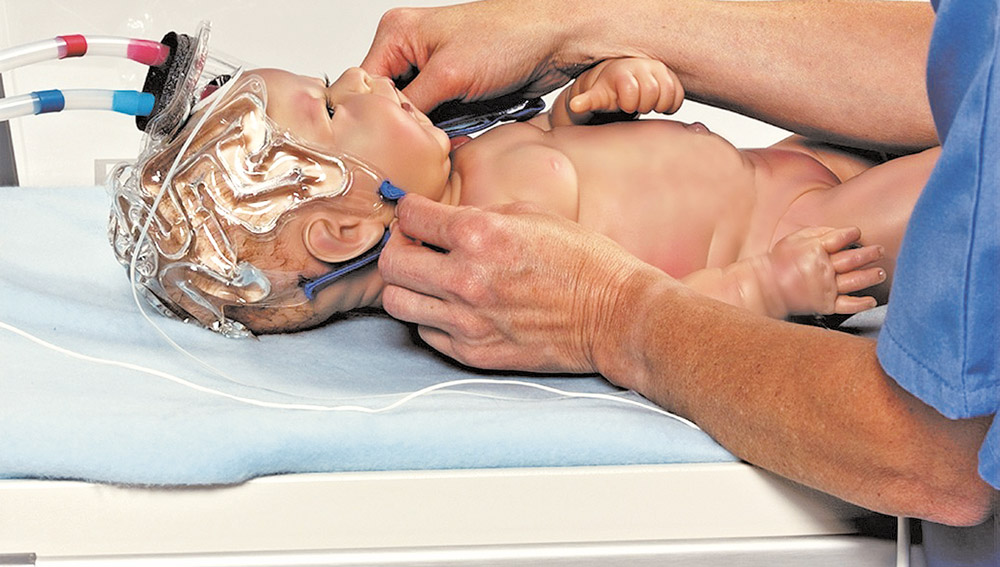
Асфіксія трапляється у 9% дітей з гестаційним віком до 36 тижнів і у 0,5% дітей, чий гестаційний вік перевищує 36 тижнів [М. Л. Аряєв, 1999; Л. О. Безруков, 2000; О. С. Рубіна, 2009; Savman Karin, 2007]. Гіпоксично-ішемічна енцефалопатія (ГІЕ) – патологія перинатального періоду, яка характеризується ушкодженням головного мозку внаслідок асфіксії та діагностується невдовзі після пологів.
На даний час у світі вивчаються питання щодо ефективної нейропротекції у немовлят, що перенесли асфіксію [J. M. Perlman, 2006; S. Prakesh, 2006, D. Azzopardi, 2008].
На сьогоднішній день відсутнє специфічне медикаментозне лікування з доведеною ефективністю, яке попереджає та зменшує ступінь ураження головного мозку при ГІЕ. Але у цьому напрямку ведуться дуже цікаві дослідження: застосування блокаторів кальцієвих каналів – неуспішні (G. Simbruner. Семінар з неонатології, Зальцбург, 2002 рік); щодо застосування антикольвульсантів проведено сім рандомізованих досліджень. Жодне з них не продемонструвало переконливого зниження ризику летальності або важкого ураження нервово-псіхічного розвитку; мета-аналіз, що об’єднував п'ять досліджень, не продемонстрував зниження ризику смерті та важкого ураження нервово-психічного розвитку, або ж комбінованого показника смерті чи важкого ураження нервово-психічного розвитку. На сьогодні протисудомна терапія у доношених немовлят безпосередньо після перенесеної асфіксії не може рекомендуватися як стандартна клінічна практика, за винятком лікування пролонгованих або частих приступів судом [Evants D. J. 2010]. Щодо застосування еритропоетину, результати досліджень показали, що призначення рекомбінантного еритропоетину є безпечним та покращує неврологічний прогноз у віці 18 місяців у пацієнтів з ГІЄ середнього ступеню [Yvonne W., 2012]. Щодо застосування аллопурінолу у новонароджених з важкою асфіксією наявні дані неостаточні. Не доведено, що алопурінол забезпечує клінічно значиму користь для новонароджених з ГІЄ [Joepe J. Kaandorp 2011]. Інфузія сульфату магнезії після народження є безпечною і може покращити короткотривалий прогноз у немовлят з важкою асфіксією [Ichiba H., 2008].
Одним із загальновизнаних є метод лікувальної гіпотермії [F. William, 2010]. Дана методика використовується у науковому медичному світі протягом 10 останніх років [Gianluca Lista, 2004; K. Blomgren, 2006; D. Azzopardi, 2007; Deirdre M. Murray, 2009]. Виявлено дію гіпотермії на функціональну активність органів та систем: на склад газів крові [F. Groenendaal, 2009]; стан мозкового кровоплину [R. Laptook, 2001]; гемодинамічні ефекти [C. M. Gebauer, 2005]; фармакокінетику лікарських засобів тощо [Н. Porter, 2008].
Є декілька досліджень, які продемонстрували ефективність комбінованої терапії: фенобарбіталу та охолодження [Meyn D. F., 2010]. Щодо застосування ксенону та охолодження у немовлят, народжених у асфіксії [Michael Fries, 2010], певні надії покладаються на поєднання медикаментозної терапії (зокрема, застосування магнезії, еритропоетину та ксенону) з лікувальною гіпотермією. Однак, на сьогоднішній день доказова база відсутня.
Запропоновано два методи, якими можна досягнути нейропротективного ефекту: тотальне охолодження тіла та краніоцеребральна гіпотермія з помірним системним охолодженням [Jacobs, 2008]. У новонароджених головний мозок продукує до 70% усієї енергії, тому краніоцеребральна гіпотермія може бути більш фізіологічною. Побічні дії охолодження мінімізуються з використанням краніоцеребральної гіпотермії у порівнянні з тотальним охолодженням тіла [Gunn A. J., 1998]. Але теоретичні моделі охолодження демонструють зменшення температури глибоких структур головного мозку при зниженні температури ядра тіла нижче 34ОС, так що можна зробити припущення, що при зменшенні температури ядра тіла, впроваджуючи метод тотального охолодження тіла, ми досягнемо більшого зниження температури глибоких структур головного мозку [Zhou W. H., 2003, Azzopardi D., 2008].
Деякі аспекти гіпотермії залишаються дуже дискусійними. Невідомо, як швидко (протягом перших 6 годин життя) необхідно розпочати гіпотермію; який рівень гіпотермії є необхідним та безпечним; якому методу надати перевагу – краніоцеребральній гіпотермії чи тотальному охолодженню тіла; скільки повинна тривати гіпотермія; чи застосовувати додаткові медикаменти під час гіпотермії; чи включати дітей у лікувальну гіпотермію до 6 годин життя, чи можливе проведення повторних курсів охолодження немовлят, народжених з важкою асфіксією. Огляд методів гіпотермії показав значне зменшення несприятливого неврологічного прогнозу у дітей, народжених у асфіксії [Tagin et al., Cochrane 2012].
Критерії ідентифікації новонароджених, яким показано проведення краніоцеребральної гіпотермії, складаються з наступних показників [Azzopardi D., 2008]. Гіпотермії підлягають новонароджені, які мають ознаки асфіксії важкого ступеня у пологах і наявні наступні ознаки, які складаються з трьох груп: А, В і С (табл. 1).
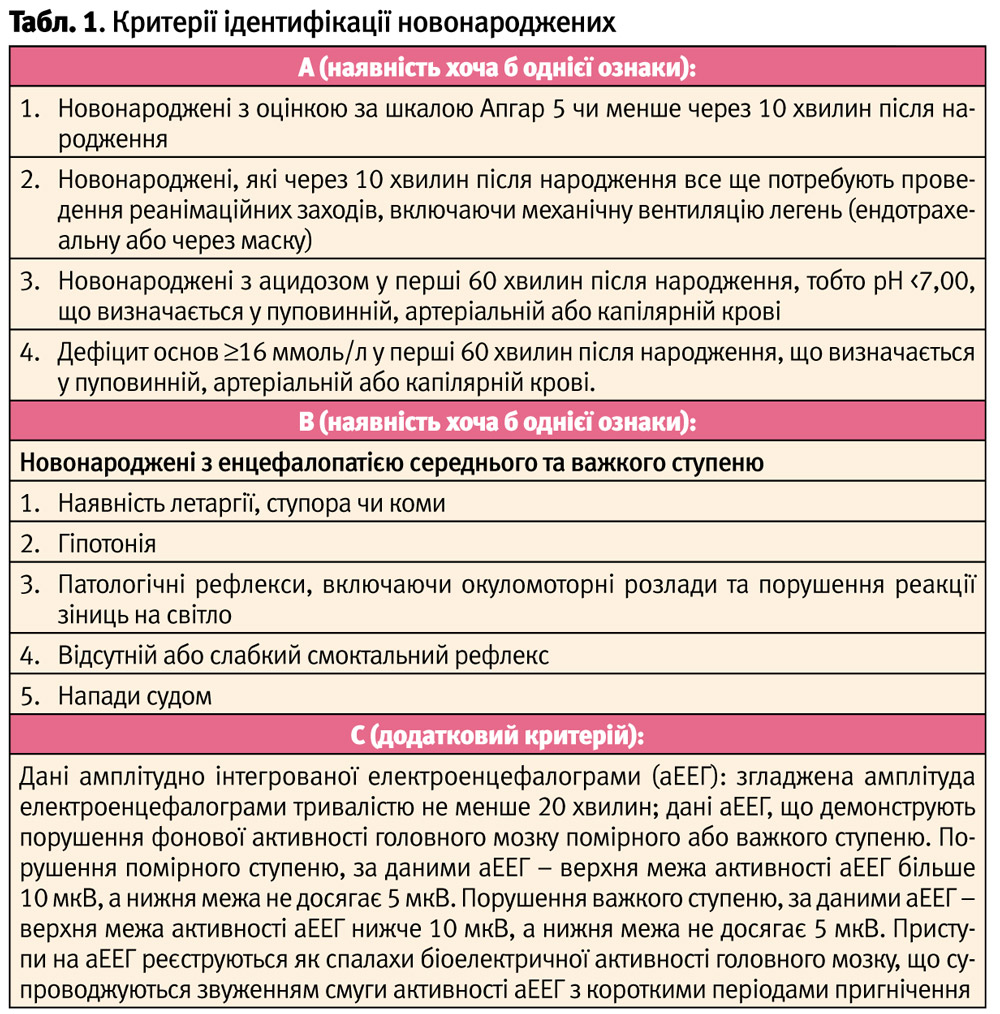
При виконанні критеріїв: А+В та С (додатковий критерій) рекомендується розпочати охолодження протягом 6 годин після народження.
Протипоказання:
- Атрезія прямої кишки.
- Ознаки травми голови, тріщин черепа, що сприяли внутрішньочерепному крововиливу.
- Вага при народженні менше 1800 г.
Застосування краніоцеребральної гіпотермії (Cool-Cap) на теренах України можливе при застосування системи OLYMPIC Cool-Cap (Olympic Medical Inc., США). Система забезпечує охолодження голови при незначній системній гіпотермії з одночасним променевим нагрівом решти тіла. OLYMPIC Cool-Cap забезпечує циркуляцію води через шапочку, яка входить до її комплекту, та підтримує задану лікарем температуру цієї води. Пристрій обладнано монітором, на який виводяться фізіологічні значення температури пацієнта (включаючи ректальну). Виходячи із значення ректальної температури, лікар налаштовує температуру води, яка циркулює у шапочці. Необхідно утримувати таку температуру води у шапочці, щоб ректальна температура новонародженого складала 34,5ОС±0,5ОС (34,0ОС … 35,0ОС).
Відділення інтенсивної терапії новонароджених Житомирського обласного перинатального центру впроваджує дану методику з 2008 року. Загалом терапію провели 53 новонародженим. Починаючи з 2012 року, спільно з Донецьким перинатальним центром, розпочато роботу щодо вивчення ефективності комбінованого застосування гіпотермії та еритропоетину (робота триває).
З 2008 по 2012 рік на базі Житомирського перинатального центру спільно із Львівським Національним медичним університетом імені Данила Галицького проведено дослідження ефективності застосування гіпотермії у немовлят з важкою асфіксією. Проведено клініко-лабораторну характеристику пацієнтів у порівняльному аспекті між двома клінічними групами: основну групу склали 36 немовлят з асфіксією, які отримували краніоцеребральну гіпотермію. До групи порівняння включено 33 новонароджених, які отримували лікування в умовах нормотермії. Загальна кількість дітей, які досягли віку 12–18 місяців, склала по 29 у групі гіпотермії та в групі нормотермії.
Лікування немовлят проводили згідно з протоколом МОЗ України «Про затвердження клінічного Протоколу з первинної реанімації та післяреанімаційної допомоги новонародженим» від 08.06.2007 року.
Під час проведення краніоцеребральної гіпотермії призначали фентаніл або морфін у постійній інфузії у такому дозуваннІ: фентаніл – 3 мкг/кг/маси тіла/годину, морфін – 0,05–0,2 мг/кг маси тіла, що забезпечувало відсутність больової реакції на охолодження шкіри голови. Під час сеансу охолодження можливий розвиток набряку скальпу, обличчя, явища зникають після закінчення процедури охолодження. Кожні 12 годин проводили інспекцію скальпу з метою оцінки стану шкіри голови. Застосування опіоїдів припиняли після зігрівання пацієнта. Підтримка гемодинаміки здійснювалась комбінуванням симпатоміметиків дофаміну та добутаміну, титрування доз проводилося у залежності від її показників. Під час сеансу зігрівання пацієнта ретельно дотримувалися протоколу – покроково збільшували температуру променевого обігрівача з інтервалом 0,1°С. Більш тривале та покрокове зігрівання – головна мета під час процедури прогріву немовляти після сеансу охолодження.
Особливості коливання температур у немовлят під час гіпотермії
Вивчаючи особливості динамічної зміни температур під час краніоцеребральної гіпотермії, необхідно зазначити, що у 73,1% немовлят було розпочато охолодження протягом 3 годин після народження. Кількість немовлят з ректальною температурою >35,0°С – 1:13. Кількість немовлят з ректальною температурою <34,0°С – 1:5 (частота випадків більше припадала на індукцію гіпотермії). Відмічалася стабільність ректальної температури під час 72-годинного періоду охолодження: 34,5±0,6°С, температура шкіри відповідно – 36,4±0,7°С.
Вивчений вплив звуження періоду початку охолодження на формування неврологічного прогнозу. Вивчався взаємозв’язок між часом охолодження – у межах перших 6 годин життя – та можливістю формування тяжких неврологічних розладів та летальності у віці 12–18 місяців. Статистична обробка даних проводилася методом логістичної регресії. Встановлено відсутність взаємозв’язку між звуженням часу початку охолодження (до 6 годин) та формуванням несприятливого неврологічного прогнозу (p=0,99).
Встановлено відсутність взаємозв’язку між часом досягнення бажаного діапазону та формуванням несприятливого неврологічного прогнозу (p=0,52).
Висновки дослідження
- При проведенні краніоцеребральної гіпотермії у новонароджених, які народилися у стані тяжкої асфіксії, спостерігається сприятливий прогноз нервово-психичного розвитку у віці 12–18 місяців, якщо за даними аЕЕГ амплітуда верхньої межі аЕЕГ ≥25µV (OR 1,1, 95% ДІ: 0,99–1,24; чутливість 55,0%, специфічність 100%, ППЗ 100%, НПЗ 50%).
- У новонароджених, що народилися у стані асфіксії тяжкого ступеня, поява циклу сну–бадьорості (SWC) до 144 годин життя асоціюється зі сприятливим прогнозом (OR 0,97, 95% ДІ: 0,94–0,99; чутливість 95,0%, специфічність 62,5%, ППЗ 93,3%, НПЗ 50%). Відновлення патерну непостійно нормальної активності до 148,8 годин вказує на сприятливий неврологічний прогноз у немовлят з тяжким перинатальним гіпоксично-ішемічним ураженням ЦНС, які отримали краніоцеребральну гіпотермію (чутливість 57,1%, специфічність 100,0%, ППЗ 100,0%, НПЗ 85,7%).
- При проведенні краніоцеребральної гіпотермії у новонароджених, що перенесли асфіксію важкого ступеня, спостерігали зменшення рівня іонізованого кальцію у порівнянні з групою немовлят у нормотермії, яка більш виражена на першу добу: 0,69 [0,35–1,2] та 1,07 [0,28–1,5] ммоль/л.
- У новонароджених під час охолодження виявлено більш виражену схильність до зниження кількості тромбоцитів (199,5±40,5 Т/л) у порівнянні з немовлятами групи нормотермії (231,6±72,9 Т/л), (р=0,05), що не супроводжувалося більшою частотою геморагічного синдрому (відповідно 2 (5,6%) проти 2 (6,1%); р=0,67).
- Проведення краніоцеребральної гіпотермії супроводжується нижчою ЧСС (118,6±9,0 уд./хв.) під час сеансу охолодження, ніж за умов ведення дітей в умовах нормотермії (133,1±8,3 уд./хв.). Також встановлена більш виражена залежність немовлят від симпатоміметичних засобів на 2–3 добу під час краніоцеребральної гіпотермії.
- При звуженні часового коридору початку охолодження у межах перших 6 годин життя у новонароджених, які перенесли асфіксію тяжкого ступеня, не встановлений позитивний вплив на частоту розвитку та наслідки перинатального гіпоксично-ішемічного ураження ЦНС (OR 0,92, 95% ДІ: 0,47–1,74, p=0,79). Встановлено, що швидші темпи зігрівання не погіршували неврологічний прогноз порівняно з повільнішими темпами (OR 1,29, 95% ДІ: 0,38–4,36, p=0,68).
- У немовлят з групи гіпотермії з тяжким гіпоксично-ішемічним ураженням ЦНС у віці 12–18 місяців відмічено зниження летальності у порівнянні з групою нормотермії (відповідно 6,9% проти 31,0%, р=0,041). У 12–18 місяців у групі дітей після краніоцеребральної гіпотермії виявлено тенденцію до зниження комбінованого показника (летальності та важких неврологічних розладів) у порівнянні з немовлятами групи нормотермії (31,0 та 51,7% відповідно, р=0,18). У дівчат, які зазнали охолодження після народження, відмічається наявність тенденції щодо більш сприятливого неврологічного розвитку у порівнянні з хлопчиками (RR 1,63 (95% ДІ: 0,94–2,89), р=0,08 та RR 1,17 (95% ДІ: 0,53–2,52), р=0,69).
Практичні рекомендації
- В умовах перинатальних центрів, пологових будинків 2-го рівня та пологових відділень, у немовлят з тяжкою асфіксією та наявністю тяжкої або середньо-тяжкої гіпоксично-ішемічної енцефалопатії доцільно розпочинати краніоцеребральну гіпотермію у перші 6 годин після народження при наявності протоколу проведення охолодження (згідно критеріїв, запропонованих NICHD).
- Рекомендується використовувати моніторинг аЕЕГ до застосування гіпотермії (перші 20 хвилин життя), під час та після гіпотермії для своєчасної діагностики та прогнозування стану новонароджених з гіпоксично-ішемічним ураженням ЦНС.
- При проведенні аЕЕГ-моніторингу у новонароджених з тяжкою асфіксією після народження, амплітуда верхньої межі аЕЕГ ³25 µV, а також поява SWC до 144 годин, відновлення DNV-патерну до 148,8 годин, може свідчити про сприятливий неврологічний прогноз у віці 12–18 місяців.
- Дітям, яким проводиться краніоцеребральна гіпотермія, необхідно визначати рівень тромбоцитів у перші 72 години охолодження, а також рівень іонізованого кальцію. При зниженні концентрації іонізованого кальцію у першу добу життя у немовлят, які отримують краніоцеребральну гіпотермію, рекомендовано призначати препарати кальцію з розрахунку 200–300 мг/кг/добу (2,0–3,0 мл/кг 10% розчину кальцію глюконату) під контролем кальціємії. Зниження рівня кількості тромбоцитів до 199,5±40,5 Т/л не потребує корекції.
- При проведенні краніоцеребральної гіпотермії новонародженим з асфіксією тяжкого ступеню призначаються симпатоміметики: дофамін та добутамін від 10 до 20 мкг/кг/хв з метою утримання середнього артеріального тиску у межах 45–47 мм. рт. ст. та збереження адекватного діурезу.
Застосування краніоцеребральної гіпотермії безпечне та сприяє поліпшенню неврологічного статусу у немовлят з важким гіпоксично-ішемічним ураженням ЦНС, усі дослідження демонстрували значне зменшення тяжких неврологічних ускладнень та летальності, NNT 6–8 (Tagin et al., Cochrane 2012). Не було зафіксовано жодних ускладнень у немовлят, які отримували лікувальну гіпотермію. Під час проведення охолодження необхідно дуже обережно підтримувати ректальну температуру у межах бажаного діапазону: під час краніоцеребральної гіпотермії — 34–35°С, під час тотального охолодження тіла — 32–33°С, а також запобігати її флуктуації. Немає різниці впливу на прогноз між методами охолодження: краніоцеребральна гіпотермія RR 0,77 (95% ДІ: 0,65–0,93), тотальна гіпотермія RR 0,75 (95% ДІ: 0,66–0,85), (Tagin et al., Cochrane 2012).
Лікувальна гіпотермія безпечна за умови виконання у спеціалізованих центрах та ефективна у середньостроковій перспективі.
Ефективність комбінованого впливу (гіпотермія та ксенон, гіпотермія та еритропоетин) знаходиться на етапі вивчення.
ДетальнішеК ВОПРОСУ О ЛЕЧЕНИИ ЖЕЛЕЗОДЕФИЦИТНЫХ АНЕМИЙ У ДЕТЕЙ
Анемии – это одна из самых частых и разнообразных по этиологии и патогенезу группа заболеваний у детей. Это связано с тем, что гемопоэз чутко реагирует на различные неблагоприятные факторы как эндогенного, так и экзогенного характера
Наиболее распространенными среди данной патологии являются железодефицитные состояния, характеризующиеся снижением содержания гемоглобина вследствие дефицита железа в организме при нарушении его поступления, усвоения или патологических потерь. По данным Всемирной организации здравоохранения (ВОЗ), у 20% населения земного шара выявляют железодефицитную анемию (ЖДА). Согласно официальным статистическим данным, в Украине этой патологией страдает 20–30% женщин детородного возраста и 2–3% детей, причем среди детей раннего возраста ЖДА встречается в 21–30% случаев.
Причины столь частого возникновения ЖДА у детей разнообразны.
В первую очередь они обусловлены антенатальными факторами, такими как нарушение маточно-плацентарного кровообращения, фето-материнское и фето-плацентарное кровотечение, синдром фетальной трансфузии при многоплодной беременности, недоношенность, многоплодие, глубокий и длительный дефицит железа в организме беременной женщины, преждевременная или поздняя перевязка пуповины, интранатальное кровотечение вследствие травматических акушерских вмешательств или аномалии развития плаценты и сосудов пуповины. Железодефицитное состояние может быть обусловлено повышенной потребностью в железе у недоношенных новорожденных, а также у детей во втором полугодии жизни. Недостаточное количество железа в пище, которое может быть связано с искусственным вскармливанием коровьим или козьим молоком, а также несбалансированным питанием, при котором в рационе ребенка отсутствуют полноценные источники железа (мясо, печень), также является причиной развития ЖДА. Хронические заболевания кишечника, синдром мальабсорбции, а также значительные и длительные геморрагические маточные кровотечения у девочек пубертатного возраста приводят к повышенным потерям железа и развитию железодефицитного состояния. ЖДА может быть также следствием нарушения обмена железа в организме, нарушения транспорта и утилизации железа при гипо- и атрансферинемии, энзимопатии, аутоиммунных процессах, а также недостаточной резорбции железа в пищеварительном тракте (пострезекционные и агастральные состояния).
Выделяют следующие стадии развития ЖДА (ВОЗ, 1977):
- прелатентная, при которой наблюдается истощение тканевых запасов железа, однако показатели крови в норме и клинических проявлений нет;
- латентная, когда в организме имеется дефицит железа в тканях и уменьшение его транспортного фонда, но при этом показатели крови в норме. На этой стадии клиническая картина обусловлена трофическими нарушениями, которые развиваются вследствие снижения активности железосодержащих ферментов и проявляются сидеропеническим синдромом: эпителиальные изменения кожи, ногтей, волос, слизистых оболочек, искажение вкуса, обоняния, нарушение процессов кишечного всасывания и астеновегетативных функций, снижение местного иммунитета. Лабораторно эта стадия характеризуется нормальным содержанием гемоглобина (Hb) при уменьшении фонда депонированного железа, определяемого по снижению значений сывороточного ферритина (СФ) – менее 12 мкг/л. ЖДА в латентной стадии, как правило, является случайной находкой при диспансеризации, скрининге или обследовании детей по другому поводу.
- стадия явной ЖДА характеризуется более выраженным истощением тканевых резервов железа и механизмов компенсации его дефицита. На этой стадии отклонения от нормы показателей крови зависят от степени тяжести процесса. Наблюдаются клинические проявления в виде сидеропенического синдрома и общеанемических симптомов, которые обусловлены анемической гипоксией: тахикардия, приглушенность тонов сердца, систолический шум на верхушке сердца, одышка при физических нагрузках, бледность кожи и слизистых оболочек, особенно хорошо заметная при осмотре конъюнктивы нижнего века, артериальная гипотония, астено-невротические нарушения. Также при осмотре ребенка можно выявить следующие неспецифические симптомы, которые в совокупности с результатами лабораторных данных могут помочь в постановке диагноза ЖДА: сглаженные сосочки языка, придающие ему яркий малиновый цвет, тусклость и ломкость волос, истончение ногтей и их ложкообразная вогнутость (койлонихия), извращение вкуса (геофагия, пакофагия и др.), снижение мышечного тонуса, особенно сфинктеров, сопровождающееся у маленьких детей недержанием мочи и стула при кашле, смехе, чихании.
Выраженность анемической гипоксии зависит не только от уровня гемоглобина, но и от быстроты развития анемии и от компенсаторных возможностей организма. В тяжелых случаях развивается синдром метаболической интоксикации в виде снижения памяти, субфебрилитета, головной боли, утомляемости, гепатолиенального синдрома и др. Длительно протекающий дефицит железа способствует снижению иммунитета, задержке психомоторного и физического развития детей.
В соответствии с уровнем гемоглобина, ЖДА разделяют на степени тяжести:
- легкую – Hb 110–91 г/л;
- среднюю – Hb 90–71 г/л;
- тяжелую – Hb 70–51 г/л;
- сверхтяжелую – Hb 50 г/л и менее.
Установление диагноза «железодефицитная анемия» в типичных случаях не представляет особых трудностей: для этого требуется анализ крови с определением уровня гемоглобина, эритроцитов, морфологических изменений эритроцитов, цветового показателя и определение показателей метаболизма железа («железного статуса»).
Критериями верификации ЖДА, согласно рекомендациям Рабочей Группы по Анемиям ВОЗ и ЮНЕСКО, являются:
- снижение значений Hb<110 г/л (у детей от 2 месяцев до 5 лет);
- изменение эритроцитарных индексов (RDW, MCH, MCV, MCHC);
- снижение СФ<12 мкг/л.
При этом кривая распределения эритроцитов по объему (RDW) расширяется и становится >15% (анизоцитоз); в то же время уменьшается содержание Hb в эритроците (MCH) <28 пг (гипохромия), средний объем эритроцитов (MCV) <70 фл (микроцитоз) и средняя концентрация Hb в эритроците (MCHC) <30 г/л (анизо- и пойкилоцитоз).
Параметры железного статуса при ЖДА изменяются следующим образом: значения СФ и железа сыворотки (ЖС) снижаются (соответственно <12 мкг/л и <10 мкмоль/л), а значения ОЖСС и трансферрина (Тф) – увеличиваются (соответственно >70 мкмоль/л и >2,6 г/л).
Основные принципы лечения ЖДА регламентированы «Протоколом лечения анемий у детей», утвержденным Приказом МЗ Украины №9 от 10.01.2005 г.:
- обязательно назначаются препараты железа, поскольку восполнить запасы железа одной диетотерапией невозможно;
- препаратами выбора являются железосодержащие средства для орального применения;
- не принимаются препараты железа одновременно с продуктами питания или другими лекарственными средствами, уменьшающими всасывание железа.
В то же время, при назначении препаратов железа необходимо отдавать предпочтение препаратам, которые содержат вещества, усиливающие абсорбцию железа, например, аскорбиновой кислоте;
- доза железа и продолжительность терапии зависят от степени тяжести анемии;
- обязателен контроль эффективности терапии препаратами железа путем проведения гемограммы с исследованием содержания ретикулоцитов на 10–14 день лечения и определение концентрации ферритина в сыворотке крови один раз в два месяца.
Суточные терапевтические дозы пероральных препаратов железа при ЖДА средней и тяжелой степени составляют:
- до 3 лет — 3–5 мг/кг/в сутки элементарного железа;
- от 3 до 7 лет — 50–70 мг/сутки элементарного железа;
- старше 7 лет — до 100 мг/сутки элементарного железа.
Терапия железом осуществляется до нормализации уровня гемоглобина с дальнейшим уменьшением дозы на 1/2.
Длительность лечения обычно составляет 6 месяцев, а для детей недоношенных – в течение 2 лет для пополнения запасов железа в организме.
У детей старшего возраста поддерживающая доза назначается курсом 3–6 месяцев, у девочек пубертатного возраста – в течение года прерывисто – каждую неделю после месячных.
Выбор препарата
Важным аспектом использования оральных железосодержащих препаратов является соотношение их эффективности и безопасности.
На сегодняшний день на украинском рынке существует большое количество препаратов железа, которые можно условно разделить на две группы, действующими веществами которых являются ионные (солевые, полисахаридные) и неионные соединения железа. Более безопасными считаются несолевые (неионные) ферропрепараты, что обусловлено их химической структурой, представленной гидроксид-полимальтозным комплексом трехвалентного железа (ГПК-Fe3+). Гидроксид-полимальтозный комплекс препятствует высвобождению свободных ионов железа, с которыми связаны осложнения и нежелательные последствия терапии солевыми железосодержащими препаратами.
Целесообразно назначать препараты трехвалентного железа благодаря их оптимальному всасыванию и отсутствию побочных эффектов
 Резорбция железа из ГПК-Fe3+ приближена к абсорбции гемового железа: комплекс полимальтозы с железом непосредственно переносится на трансферрин (Тф), связывается с ним, после чего депонируется в тканях в виде ферритина. Неионная структура ГПК-Fe3+ и активный транспортный механизм всасывания предохраняют организм от избытка свободных ионов металла, поскольку железо не подвергается окислению.
Резорбция железа из ГПК-Fe3+ приближена к абсорбции гемового железа: комплекс полимальтозы с железом непосредственно переносится на трансферрин (Тф), связывается с ним, после чего депонируется в тканях в виде ферритина. Неионная структура ГПК-Fe3+ и активный транспортный механизм всасывания предохраняют организм от избытка свободных ионов металла, поскольку железо не подвергается окислению.
При этом сохраняются физиологические процессы саморегуляции: по мере восполнения депо железа всасывание металла прекращается по принципу «обратной связи», что полностью исключает риск развития оксидативного повреждающего воздействия, а также возможность передозировки и отравления.
Эти данные были убедительно подтверждены результатами многолетних исследований по оценке эффективности и безопасности использования различных по химической структуре ферропрепаратов – сульфатных солей железа (СфЖ) и гидроксид-полимальтозного комплекса трехвалентного железа (ГПК-Fe3+), входящего в состав препарата Мальтофер (Вифор, Швейцария), проведенных в России на базе ГБОУ ВПО РНИМУ им. Н. И. Пирогова Минздравсоцразвития РФ, ФГБУ «Гематологический научный центр» Минздравсоцразвития РФ и трех детских клинических больниц.
В ходе этих исследований было показано, что в процессе лечения как солевые, так и препараты на основе ГПК-Fe3+ показали высокую эффективность в отношении восполнения запасов железа (содержание Hb, СФ), нормализации транспортного фонда (Тф) и значений основного регуляторного белка – гепсидина. Однако имелись достоверно значимые различия в отношении практически всех исследованных показателей в пользу препарата ГПК-Fe3+ (Мальтофер) по восстановлению емкостных фондов железа, где процессы восстановления положительного баланса железа были более выраженными.
Выводы
Таким образом, при выборе препарата для проведения ферротерапии у детей предпочтение следует отдавать тем лекарственным средствам, которые обладают высокой терапевтической эффективностью и хорошей переносимостью, не вступают во взаимодействие с пищей или лекарствами, имеют широкий диапазон безопасности с минимальным риском развития случайной передозировки. Именно таким требованиям отвечает оригинальный препарат Мальтофер (Вифор, Швейцария).
В нем удачно сочетаются уникальные свойства, обеспечивающие высокую антианемическую активность, удобство приема, минимальное число нежелательных явлений и, что немаловажно, ценовую доступность, что позволяет минимизировать затраты на лечение.
Многообразие лекарственных форм (в частности, капли и сироп) позволяет применять препарат абсолютно во всех возрастных группах, начиная с периода новорожденности.
Детальніше
ВЫЗДОРОВЛЕНИЕ АМЕРИКАНСКОГО РЕБЕНКА ОТ ВИЧ ОБНАДЕЖИВАЕТ И СТАВИТ НОВЫЕ ВОПРОСЫ
 Недавно в США было сделано сенсационное заявление о первом случае выздоровления ребенка от ВИЧ-инфекции. Это дает новые надежды на то, что в ближайшее время эта опасная инфекция будет успешно поддаваться лечению во всем мире. Однако ученые говорят, что потребуется еще много исследований и намного более чувствительная диагностика, прежде чем эта надежда воплотится в действительность.
Недавно в США было сделано сенсационное заявление о первом случае выздоровления ребенка от ВИЧ-инфекции. Это дает новые надежды на то, что в ближайшее время эта опасная инфекция будет успешно поддаваться лечению во всем мире. Однако ученые говорят, что потребуется еще много исследований и намного более чувствительная диагностика, прежде чем эта надежда воплотится в действительность.
В июле 2010 г. в штате Миссисипи родилась ВИЧ-инфицированная девочка, в течение 30 часов после родов ее лечили агрессивной ВИЧ-терапией, которая затем продолжалась в течение 18 месяцев. Она получала три препарата – зидовудин, ламивудин и невирапин – вместо стандартной монотерапии невирапином, потому что диагноз ВИЧ был установлен у матери только после родов.
Затем девочка не наблюдалась в течение длительного периода, во время которого, как сообщила ее мать, она не получала лечение.
Позже было обнаружено, что ребенок излечен от инфекции. Об этом на Конференции по ретровирусам и оппортунистическим инфекциям в Атланте заявила команда исследователей во главе с доктором Деборой Персо, вирусологом Университета Джонса Хопкинса в Балтиморе.
«С клинической точки зрения это означает, что если пролечить инфицированного ребенка антиретровирусными препаратами сразу же после родов, то появляется возможность, по сути, вылечить ребенка» – сообщил доктор Стивен Дикс, исследователь ВИЧ/СПИД из Калифорнийского Университета в Сан-Франциско.
Лечение ВИЧ-инфицированных беременных является лучшим способом предотвращения ВИЧ-инфекции у их детей, говорят эксперты, но даже в богатых ресурсами странах, таких как Соединенные Штаты, каждый год 100–200 младенцев рождаются с ВИЧ, а во всем мире каждый день рождается 1 000 инфицированных младенцев, особенно в развивающихся странах. Для этих детей данные результаты могут оказать значительное влияние на их будущее.
Мишель Сидибе, исполнительный директор Объединенной программы Организации Объединенных Наций по ВИЧ/СПИД, известной как UNAIDS, сказал, что эти новости вселяют большую надежду на то, что лечение ВИЧ у детей возможно, но это также подчеркивает необходимость исследований и инноваций особенно в области ранней диагностики.
http://www.medscape.com/viewarticle/780275
ДетальнішеРАННИЙ ПРИЕМ АНТИБИОТИКОВ МОЖЕТ ПОВЫШАТЬ РИСК ВОЗНИКНОВЕНИЯ ПИЩЕВОЙ АЛЛЕРГИИ
Согласно результатам большого исследования «случай–контроль», воздействие антибиотиков на организм ребенка в течение первого года жизни связано с повыфшенным риском возникновения пищевой аллергии. Риск особенно велик у тех детей, которые получили несколько курсов антибиотиков. Такие результаты были представлены исследователями на последней сессии ежегодного собрания Американской академии аллергологии, астмы и иммунологии.
Детям, которые участвовали в исследовании, наиболее часто назначались антибиотики пенициллинового ряда и цефалоспорины. По данным этого исследования, у детей в возрасте от 7 до 12 месяцев вероятность возникновения пищевой аллергии после курса антибиотикотерапии была выше, чем у детей первого полугодия жизни. Это связано с тем, что в 7–12 месяцев ребенку вводятся новые виды пищи.
Кроме того, было замечено, что риск пищевой аллергии возрастал с увеличением количества курсов антибиотикотерапии. При одном или двух курсах антибиотиков существенного возрастания риска пищевой аллергии не было замечено, но при трех и четырех курсах отношение шансов стало значительным и достигло наивысшего значения для пяти курсов и более (отношение шансов 2,15).
По мнению исследователей, полученные результаты подтверждают гипотезу, которая состоит в том, что изменение нормальной кишечной флоры, происходящее после приема антибиотиков, может способствовать увеличению частоты проявления пищевой аллергии у детей. Нормальная иммунологическая реакция кишечника, включая взаимодействие с разнообразным микробиомом, способствует развитию пищевой переносимости.
http://www.pediatricnews.com/single-view/early-antibiotics-may-up-food-allergy-risk/f65f4b42a23b03c06edf81a8329de515.html
Детальніше