 В раннем детском возрасте нейтропении встречаются достаточно часто, и хотя в большинстве случаев протекают легко и не подлежат лечению, все же требуют своевременного выявления, проведения дифференциальной диагностики и определения оптимальной тактики ведения пациентов.
В раннем детском возрасте нейтропении встречаются достаточно часто, и хотя в большинстве случаев протекают легко и не подлежат лечению, все же требуют своевременного выявления, проведения дифференциальной диагностики и определения оптимальной тактики ведения пациентов.
В настоящее время существует как проблема гиподиагностики нейтропений, так и проблема «гиперопеки» пациентов с нейтропенией. Гиподиагностика связана с тем, что медработник, оценивающий общий анализ крови, не подсчитывает абсолютное число нейтрофилов, а выявленные изменения трактует как «относительный лимфоцитоз». Часто за этим следует «диагноз» — «лимфатико-гипопластический диатез», и склонность ребенка к частым инфекциям объясняется именно этой «аномалией конституции».
С другой стороны, если у ребенка раннего возраста выявляется нейтропения, то это нередко сопровождается назначением множества анализов (особенно любимы педиатрами анализы на TORCH-инфекции), различными ненужными ограничениями (отказ от прививок, запрет на посещения детских коллективов) и бесконтрольным назначением антибиотиков, что закономерно порождает серьезное беспокойство родителей.
В связи с этим понимание основных механизмов развития и причин нейтропений, возникающих в раннем детском возрасте, принципы их дифференциальной диагностики и подходов к лечению и диспансерному наблюдению пациентов важны для медицинских работников первичного звена, оказывающих помощь детскому населению.
Патофизиология
Жизненный цикл нейтрофилов составляет около 15 дней. Большая его часть проходит в костном мозге. Костномозговой пул нейтрофилов представлен активно делящимися (миелобласты, промиелоциты, миелоциты) и созревающими (метамиелоциты, палочкоядерные и сегментоядерные нейтрофилы) клетками. Особенностью нейтрофилов является способность значительно увеличивать свою численность, когда это необходимо, как за счет ускорения клеточного деления, так и за счет «рекрутирования» созревающих и зрелых клеток.
В отличие от других клеток крови в сосудистом русле, нейтрофилы проводят там всего около 6–8 часов, но при этом составляют самую большую группу циркулирующих лейкоцитов. В сосудах лишь половина нейтрофилов находится в движении, остальные обратимо прилипают к эндотелию. Эти пристеночные или маргинальные нейтрофилы представляют собой запасной пул зрелых клеток, которые в любой момент могут быть вовлечены в инфекционный процесс.
В тканях нейтрофилы проводят еще меньше времени, чем в крови. Здесь они обеспечивают свое клеточное действие или погибают. Основная функция нейтрофилов — защита от инфекции (преимущественно бактериальной) — реализуется посредством хемотаксиса, фагоцитоза и уничтожения микроорганизмов.
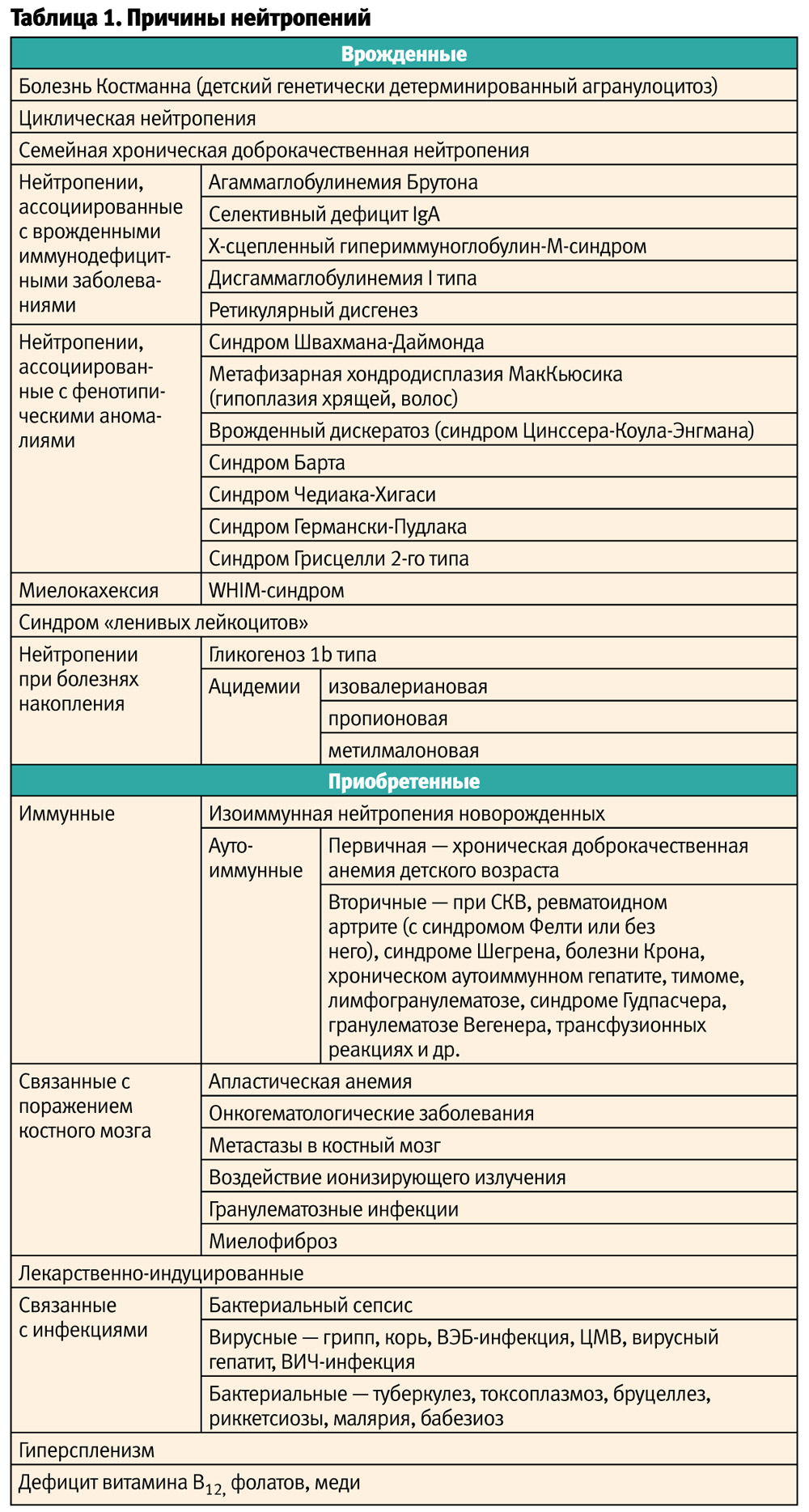
Нейтропения может возникнуть вследствие уменьшения любого из пулов нейтрофилов: при снижении интенсивности образования новых клеток в костном мозге, нарушении созревания нейтрофилов в костном мозге, повышенном разрушении нейтрофилов в крови и тканях, а также при перераспределении нейтрофилов в кровяном русле (повышенная маргинация нейтрофилов — псевдонейтропения). Основные причины нейтропений представлены в таблице 1.
Диагностика нейтропении базируется на подсчете абсолютного числа нейтрофилов в периферической крови. Для этого общее количество лейкоцитов нужно умножить на суммарный процент нейтрофилов (сегментоядерных и палочкоядерных) и разделить на 100.
О нейтропении говорят при снижении абсолютного числа нейтрофилов в периферической крови менее 1000/мкл у детей первого года жизни и менее 1500/мкл у детей старше 1-го года.
Термин «агранулоцитоз» используется в случае практически полного отсутствия нейтрофилов в крови — менее 100/мкл.
Тяжесть течения нейтропении определяется количеством нейтрофилов в периферической крови. При легкой (1000–1500/мкл) и средней степени тяжести (500–1000 мкл) нейтропении клинические проявления могут отсутствовать или же отмечается некоторая склонность к острым респираторным инфекциям, которые протекают нетяжело.
Снижение уровня нейтрофилов менее 500/мкл (тяжелая нейтропения) может сопровождаться развитием повторных бактериальных инфекций. Чаще всего инфекции затрагивают слизистые оболочки (афтозный стоматит, гингивит, средний отит) и кожу (импетиго, склонность к нагноениям ран, царапин и т.д.). Нередко отмечается поражение перианальной зоны и промежности. При этом для пациентов с нейтропенией при локальных инфекциях характерна слабо выраженная местная реакция, но, как правило, всегда присутствует лихорадка.
При уровне нейтрофилов менее 200/мкл высок риск развития серьезных, в том числе жизнеугрожающих, бактериальных инфекций и сепсиса. Риск развития тяжелой инфекции прямо пропорционален длительности нейтропении и обратно зависит от абсолютного числа нейтрофилов в крови. Так, при уровне нейтрофилов менее 100/мкл в течение 3–4 недель риск развития бактериальной инфекции приближается к 100%. Развитие тяжелых вирусных и паразитарных инфекций для больных с нейтропенией нехарактерно, в то время как грибковая суперинфекция встречается довольно часто на фоне массивной антибиотикотерапии.
Дифференциальная диагностика нейтропений в раннем детском возрасте
Наиболее часто у детей раннего возраста встречается хроническая доброкачественная нейтропения детского возраста (ХДНДВ). Она возникает чаще всего во втором полугодии жизни, хотя крайние значения возраста начала заболевания составляют 3–30 месяцев, длится оно более 6 месяцев и спонтанно проходит через несколько лет (как правило, к 4–5 годам). Данное заболевание не является наследственным. Уровень нейтрофилов редко опускается ниже 500/мкл, при рождении уровень нейтрофилов (если он определялся) — нормальный.
Инфекции, связанные с данным вариантом нейтропении, обычно протекают нетяжело и проходят самостоятельно. Характерны инфекции верхних дыхательных путей, острый средний отит, инфекции кожи, стоматиты, гингивиты. Может отмечаться лихорадка без явного очага инфекции. Инфекции хорошо поддаются лечению антибиотиками. Сепсис и пневмония редки. Несмотря на то что инфекционные заболевания у детей с хронической доброкачественной нейтропенией могут возникать чаще, чем у здоровых детей, на рост и развитие детей они не влияют (хотя некоторые исключения встречаются).
Во время инфекционных заболеваний уровень нейтрофилов обычно повышается, но к моменту выздоровления вновь возвращается к исходным значениям. Костный мозг у детей с ХДНДВ с нормальным или повышенным цитозом, морфология его в норме или может отмечаться нарушение созревания миелоидных предшественников, как правило, на поздних стадиях.
В настоящее время считается, что ХДНДВ является приобретенной первичной аутоиммунной нейтропенией, механизм развития которой сходен с таковым при идиопатической тромбоцитопенической пурпуре (ИТП). Известно, что развитие ИТП ассоциировано с вирусной инфекцией и иногда иммунизацией. Играют ли эти факторы роль в генезе ХДНДВ, пока не известно. В некоторых исследованиях была показана связь между ХДНДВ и парвовирусной инфекцией В19. При ХДНДВ в крови обнаруживаются антитела класса IgG к HNA1 (человеческий нейтрофильный антиген-1) и, реже, к нейтрофильным гликозилированным изоформам FC гамма RIIIb (CD 16b). Система человеческих нейтрофильных антигенов включает антигены HNA1-HNA5 групп. Чаще всего, как уже было сказано, антитела вырабатываются к антигенам HNA1, которые представлены NA1, NA2, SH-антигенами.
При уровне нейтрофилов менее 200/мкл высок риск развития серьезных бактериальных инфекций и сепсиса
Первичную аутоиммунную нейтропению следует отличать от вторичных аутоиммунных нейтропений. В первом случае нейтропения является единственным проявлением, в то время как вторичные аутоиммунные нейтропении развиваются на фоне системных аутоиммунных заболеваний, инфекций и злокачественных неоплазий.
Аутоиммунная нейтропения, которая выявляется у ребенка старшего возраста, как правило, всегда является вторичной и не должна рассматриваться как аналог ХДНДВ. Ее клиническое течение не отличается доброкачественностью. Часто вторичная аутоиммунная нейтропения сочетается с аутоиммунной гемолитической анемией и тромбоцитопенией, обнаружением в крови антифосфолипидных антител и оказывается проявлением системной красной волчанки, синдрома Фелти, синдрома Шегрена и других СКВ-подобных заболеваний. Поэтому в старшей возрастной группе при наличии аутоиммунной нейтропении всегда нужно искать другие аутоиммунные процессы. У детей же раннего возраста аутоиммунная нейтропения обычно является первичной, вторичные варианты крайне редки.
Другим вариантом иммунной нейтропении у детей раннего возраста может быть изо- и аллоиммунная нейтропения, развивающаяся у новорожденных вследствие воздействия на нейтрофилы материнских антинейтрофильных антител. Патогенез данного заболевания сходен с таковым при гемолитической болезни новорожденных. Сенсибилизация чаще всего происходит к NA1- и NA2-антигенам. Изоиммунная нейтропения встречается приблизительно у 3% новорожденных и может проявляться лихорадкой, развитием инфекции мочевых путей, целлюлита, пневмонии и сепсиса. Нейтропения обычно длится 7 недель.
ХДНДВ необходимо дифференцировать с врожденными и наследственными нейтропениями, которые представляют собой большую разнородную группу и, как правило, протекают тяжелее.
Болезнь Костманна (детский генетически детерминированный агранулоцитоз, тяжелая наследственная нейтропения) характеризуется развитием в первые месяцы жизни рецидивирующих бактериальных инфекций, особенно в ротовой полости и перианальной области, на фоне резкого снижения уровня нейтрофилов в крови (0–500/мкл). Механизм развития заболевания до конца не выяснен, предполагается дефект созревания предшественников нейтрофилов в костном мозге. Конкретный генетический дефект не установлен. Тип наследования — аутосомно-рецессивный. У некоторых пациентов на фоне лечения гранулоцитарным колониестимулирующим фактором (Г-КСФ) может развиться миелодиспластический синдром или острая миелобластная лейкемия, что объясняется наличием дополнительных мутаций, чаще всего в гене рецептора Г-КСФ. Пациенты, отвечающие на лечение Г-КСФ, должны получать его пожизненно. Прогноз серьезный.
Циклическая нейтропения характеризуется периодически возникающей нейтропенией, сопровождающейся лихорадкой, поражением кожи или слизистых оболочек. Первые проявления, как правило, возникают на 1-м году жизни, реже — в старшем возрасте. Снижение уровня нейтрофилов в крови практически до нуля наблюдается со средней периодичностью в 21 день (12–35 дней), нейтропения сохраняется в течение 3–5 дней, а затем лейкограмма восстанавливается. Наряду с циклическими изменениями количества нейтрофилов, у 70% пациентов отмечаются циклические колебания количества моноцитов, а у 20% — эозинофилов. Пик моноцитоза и эозинофилии приходится на окончание периода нейтропении. Нейтропении предшествует значительное сокращение пула созревающих нейтрофилов в костном мозге вследствие ускоренного апоптоза. На пике нейтропении содержание клеток нейтрофильного ряда в костном мозге нормальное или повышенное. Тип наследования — аутосомно-доминантный, иногда — аутосомно-рецессивный. В генезе заболевания имеют значение мутации в гене ELA2.
Прогноз относительно благоприятный — с возрастом проявления заболевания ослабевают. Однако примерно у 10% пациентов отмечается тяжелое течение заболевания с развитием жизнеугрожающих инфекций. Лечение заключается в ежедневном введении Г-КСФ.
Семейная хроническая доброкачественная нейтропения — заболевание с аутосомно-доминантным типом наследования, наблюдающееся у западных европейцев, африканцев и йеменских евреев. Пациенты обычно бессимптомны, риск инфекций низок. Никакого лечения не требуется.
Нейтропения может сопровождать врожденные иммунодефицитные заболевания: агаммаглобулинемию Брутона, селективный дефицит IgА, Х-сцепленный гипериммуноглобулин-М-синдром и дисгаммаглобулинемию І типа. При ретикулярном дисгенезе нейтропения сочетается с лимфоцитопенией и агаммаглобулинемией (комбинированный иммунодефицит).
Синдром Швахмана-Даймонда характеризуется нейтропенией средней или тяжелой степени, экзокринной недостаточностью поджелудочной железы, хондродисплазией, нанизмом, рецидивирующими инфекциями и диареей. Манифестирует в раннем возрасте. Смертность составляет 15–25%. Тип наследования — аутосомно-рецессивный. Большинство случаев синдрома Швахмана-Даймонда вызвано мутациями в гене SBDS. Точная функция этого гена до конца не выяснена, однако известно, что он вовлечен в синтез рибосом и процессинг РНК. Лечение нейтропении состоит во введении Г-КСФ.
Метафизарная хондродисплазия МакКьюсика (гипоплазия хрящей, волос) — аутосомно-рецессивное заболевание, в основе которого лежит дефект гена RMRP, локализованного в 9-й хромосоме, кодирующего РНК-компонент рибонуклеазы процессингового комплекса митохондриальной РНК (RNase MRP). Нейтропения средней и тяжелой степени. Кроме того, имеет место клеточный иммунодефицит, макроцитарная анемия, а также нанизм с преимущественным укорочением конечностей, тонкие редкие светлые волосы, дисплазия ногтей, гипопигментированная кожа, мальабсорбция, пороки развития ЖКТ, умеренная платиспондилия, поясничный лордоз, расширение хрящевых отделов рёбер, брахидактилия, искривление ног, гипермобильность суставов, ограничение разгибания в локтевых суставах. Отмечается склонность к развитию злокачественных опухолей, особенно лимфом. Лечение гематологических нарушений — пересадка костного мозга.
Определение титра антител к NA1 и NА2 в сыворотке крови ребенка и матери может быть полезным для подтверждения диагноза изоиммунной нейтропении
Врожденный дискератоз (синдром Цинссера-Коула-Энгмана) характеризуется задержкой умственного развития, поражением кожи, ее придатков и слизистых оболочек вследствие патологического ороговения эпителия (дистрофия ногтей, гипотрихоз ресниц, закупорка слезных протоков, лейкоплакия слизистой оболочки полости рта, пойкилодермия и др.), панцитопенией и клеточным иммунодефицитом. Гематологическая картина напоминает таковую при врожденной апластической анемии Фанкони. Тип наследования — обычно X-сцепленный рецессивный, хотя существуют и аутосомно-доминантные и аутосомно-рецессивные формы этого заболевания. Х-сцепленная форма связана с мутациями в гене DKC1, который кодирует дискерин, нуклеарный белок, связанный с рибонуклеопротеиновыми частицами. Аутосомно-доминантная форма связана с мутациями в другом гене, TERC, который является частью теломеразы. Пациенты с этим расстройством имеют более короткие теломеры, чем в норме. Лечение гематологических нарушений — Г-КСФ, ГМ-КСФ (гранулоцитарно-макрофагальный КСФ) и пересадка костного мозга.
Синдром Барта — рецессивное, X-сцепленное заболевание, характеризующееся развитием в раннем возрасте кардиомиопатии, скелетной миопатии, повторными инфекциями, нанизмом и нейтропенией средней или тяжелой степени.
Синдром Чедиака-Хигаси — аутосомно-рецессивное заболевание, при котором нейтропения сочетается с альбинизмом, прогрессирующими неврологическими нарушениями, геморрагическим синдромом. Характерны повторные инфекции, особенно гингивиты. Во многих клетках, в том числе и гранулоцитах, определяются специфические лизосомальные гранулы. Лечение — пересадка костного мозга.
Сочетание нейтропении и альбинизма характерно также для синдрома Германски-Пудлака и синдрома Грисцелли 2-го типа.
У пациентов с синдромом Германски-Пудлака кроме того наблюдается тенденция к кровотечениям, дисморфизм лица, задержка развития, фиброз легких, повышенная частота бактериальных инфекций (в том числе как следствие нейтропении).
Синдром Грисцелли 2-го типа — редкая разновидность первичных гемофагоцитарных лимфогистиоцитозов, которые возникают обычно в первые 2 года жизни. Основные клинические проявления — лихорадка, рефрактерная к антибактериальной терапии, гепатоспленомегалия, поражение ЦНС, альбинизм, панцитопения, гипофибриногенемия, гипертриглицеридемия.
Mиелокахексия характеризуется умеренной нейтропенией и повторными инфекциями. При этом заболевании вследствие ускоренного апоптоза и сниженной экспрессии bcl-x в предшественниках нейтрофилов отмечаются множественные дефекты функций нейтрофилов, укорочение их жизни и задержка их высвобождения из костного мозга. Характерен аномальный вид ядер нейтрофилов — гиперсегментация, нити хроматина между сегментами, пикноз, а также вакуолизация цитоплазмы. Лечение — Г-КСФ.
Миелокахексия наблюдается также при синдроме WHIM (warts, hypogammaglobulinemia, infections and myelokathexis). При данном синдроме отмечается комбинированный иммунодефицит (нейтропения, лимфоцитопения, гипогаммаглобулинемия), обуславливающий повышенную склонность к бактериальным и вирусным инфекциям, особенно к папилломавирусной инфекции, проявляющейся множественными бородавками на руках и ногах. В основе заболевания — мутация в гене CXCR4 с аутосомно-доминантным типом наследования.
Синдром «ленивых лейкоцитов» — заболевание неизвестной природы с тяжелой нейтропенией и резким угнетением хемотаксиса нейтрофилов. Морфология костного мозга и предшественников нейтрофилов нормальная. Однако в ответ на стимуляцию не происходит увеличения количества нейтрофилов, миграция в очаг воспаления (тест «кожного окна») не наблюдается. В наибольшей степени хемотаксис угнетен у костномозговых нейтрофилов. Прогноз относительно благоприятный.
При метаболических расстройствах могут отмечаться нейтропении разной степени тяжести. Эти расстройства включают гликогеноз 1b типа и различные ацидемии (изовалериановая, пропионовая и метилмалоновая).
Приобретенные нейтропении, кроме уже упоминавшихся ХДНДВ и изоиммунной нейтропении, в раннем детском возрасте встречаются значительно реже, чем у детей старшего возраста и взрослых. В качестве дифференциальных диагнозов имеет смысл рассматривать:
- нейтропению, вызванную приемом лекарственных препаратов;
- гиперспленизм;
- ВИЧ-инфекцию, туберкулез.
При проведении дифференциальной диагностики следует также помнить о транзиторных нейтропениях, возникающих на фоне инфекций, чаще всего вирусных. Продолжительность таких нейтропений редко превышает 1–2 недели и в среднем составляет 3,3 дня.
Таким образом, диагностическая тактика при выявлении нейтропении у ребенка раннего возраста может быть следующей:
1) исключение транзиторного характера нейтропении (связь с недавно перенесенной вирусной инфекцией, повторное исследование через 1–2 недели);
2) поиск признаков, которые исключают возможность ХДНДВ:
- тяжелое течение заболевания (частые бактериальные инфекции, лихорадочные состояния, нарушения физического развития и др.);
- наличие жизнеугрожающих инфекций в анамнезе;
- уровень нейтрофилов менее 200/мкл с рождения;
- гепато- или спленомегалия;
- геморрагический синдром.
Если ни одного из этих признаков нет, то наиболее вероятный диагноз — ХДНДВ. Если в наличии хотя бы один — следует искать другие причины нейтропении.
Характер и объем лабораторных обследований у ребенка с нейтропенией зависит не столько от степени выраженности нейтропении, сколько от частоты и степени тяжести связанных с ней инфекций.
Для детей с ХДНДВ важным моментом является документация продолжительности нейтропении более 6 месяцев, отсутствие других изменений в гемограмме, а также повышение уровня нейтрофилов в период интеркуррентных инфекций.
Минимальная диагностическая программа при изолированной нейтропении также включает определение уровня иммуноглобулинов в крови.
Пункция костного мозга может потребоваться для исключения других заболеваний.
Рутинно определять у детей с ХДНДВ в крови уровень антинейтрофильных антител необходимости нет, так как выявить их удается не у всех. С другой стороны, при подозрении на вторичную аутоиммунную нейтропению эти тесты, как и определение других аутоантител, должны проводиться. Определение титра антител к NA1 и NА2 в сыворотке крови ребенка и матери может быть полезным для подтверждения диагноза изоиммунной нейтропении.
При врожденных нейтропениях может потребоваться генетическое исследование.
Ведение пациентов раннего возраста с ХДНДВ предусматривает, в первую очередь, разъяснение сути проблемы родителям, чтобы избежать ненужного беспокойства с их стороны. Рекомендуют уделять больше внимания гигиене полости рта ребенка для профилактики стоматита, гингивита. Профилактические прививки проводятся согласно календарю, рекомендуют также прививать детей дополнительно от гриппа, пневмококковой и менингококковой инфекции. В подавляющем большинстве случаев ХДНДВ иных мер не требуется.
Антибактериальные препараты назначаются только при выявлении у ребенка очага бактериальной инфекции, а также при наличии нейтропении и лихорадки без явного очага инфекции.
При частых рецидивах бактериальной инфекции предлагают проводить профилактику триметопримом/сульфометаксазолом, однако дозы, длительность курса, эффективность и безопасность данного метода изучены не были.
Частые повторные инфекции, резистентные к терапии антибиотиками, а также определенные формы врожденных нейтропений (см. выше) — показания для применения Г-КСФ и внутривенных иммуноглобулинов.
Глюкокортикоиды способны повышать уровень нейтрофилов. Однако применение их при нейтропениях может быть оправдано лишь в случае неэффективности всех остальных методов, и в целом является скорее исключением, чем правилом. Категорически не рекомендуется назначать глюкокортикоиды детям с неосложненной ХДНДВ с целью коррекции уровня нейтрофилов.
Литература
- John E Godwin. Neutropenia. — Режим доступа: http://emedicine.medscape.com/article/204821-overview
- Susumu Inoue. Pediatric Autoimmune and Chronic Benign Neutropenia. — Режим доступа: http://emedicine.medscape.com/article/ 954781-overview
- Шиффман Ф. Дж. Патофизиология крови. Пер. с англ. — М.-СПб.: «Издательство БИНОМ» — «Невский диалект», 2000. — С.123-134, 293-300.
- Гематология детского возраста: Руководство для врачей / Под ред. Н. А. Алексеева. — СПб.: «Гиппократ», 1998. — С. 500-526.
- Ратманова Г. А., Руссова Т. В., Кузнецова О. В. и др. Нейтропении в педиатрической практике // Вопросы диагностики в педиатрии. — 2009, Т. 1. — №2. — С. 69-72.


коментарів