Дефицит железа – наиболее распространенный пищевой дефицит в мире. Около 30% населения земного шара имеет железодефицитную анемию (ЖДА), хотя большая часть этих людей проживает в развивающихся странах. Но даже в социально благополучных обществах недостаток железа испытывают 9–10% детей в возрасте 12–36 месяцев, а у трети из них дефицит железа прогрессирует до ЖДА
Наиболее часто железодефицит развивается вследствие недостаточного поступления железа с пищей. В организме доношенного новорожденного содержится приблизительно 0,5 г железа, у взрослого – 5 г. Чтобы обеспечить такой прирост запасов железа, в организм ребенка ежедневно на протяжении первых 15 лет жизни должно поступать 0,8 мг железа, а с учетом суточных потерь – 1 мг. Поскольку из пищи абсорбируется менее 10% железа, то содержание железа в суточном рационе должно быть не менее 8–10 мг. Молоко, которым вскармливаются дети на первом году жизни, содержит около 1 мг/л железа. При этом если из коровьего молока и молочных смесей усваивается не более 10% железа, то из грудного молока железо всасывается в 4–6 раз эффективнее.
Таким образом, на 1-м году жизни одно лишь молоко не может обеспечить потребности ребенка в железе. В течение первых 6–9 месяцев жизни недостаточное поступление железа с пищей компенсируется наличием у ребенка его запасов. У детей, родившихся с низкой массой тела и детей с перинатальными потерями крови запасы железа могут истощаться раньше – к 4 месяцам. В таких случаях отсроченное пережатие пуповины и обеспечение грудного вскармливания могут улучшить ферростатус ребенка и снизить риск развития железодефицита. Так или иначе, алиментарный генез дефицита железа у доношенного ребенка младше 6 месяцев и у недоношенного младше 4 месяцев маловероятен.
Наиболее часто ЖДА, обусловленная нерациональным вскармливанием, развивается в возрасте 9–24 месяцев и редко – в более старшем возрасте. После истощения запасов основным источником железа становится твердая пища.
В этом возрасте основная причина дефицита железа – употребление в пищу продуктов с низким его содержанием – в первую очередь, цельного коровьего молока. Употребление ребенком старше 6 месяцев более 700 мл цельного коровьего молока в день – фактор возможного железодефицита.
При этом имеет значение не только низкое содержание железа в молоке, но и возможность повреждения слизистой оболочки кишечника термолабильными белками коровьего молока, такими как бычий альбумин, вследствие чего происходит потеря крови через кишечник. Колит, индуцированный белками цельного коровьего молока, не имеет отношения к аллергии на белок коровьего молока, т. е. не опосредован иммунными механизмами, а также не связан с ферментативными нарушениями (лактазной недостаточностью). Эта реакция ЖКТ на коровье молоко встречается исключительно в раннем возрасте, преимущественно на первом году жизни и не характерна для детей старше 2 лет.
Кровопотеря всегда должна рассматриваться в качестве потенциальной причины ЖДА, особенно у детей старшего возраста и у детей первых 4–6 месяцев жизни. Потери крови через ЖКТ могут иметь место при пептических язвах, дивертикуле Меккеля, полипах, гемангиомах кишечника, а также воспалительных заболеваниях кишечника. У детей раннего возраста, как уже упоминалось, скрытые потери крови могут быть вызваны колитом от употребления цельного коровьего молока. В таких случаях ЖДА развивается раньше или может быть более выраженной, чем ожидается при обычном алиментарном дефиците железа. Кроме того, скрытая кровопотеря может иметь место при хронической диарее, глистной инвазии (некоторые нематодозы), инфекции Helicobacter pylori, иногда – при легочном гемосидерозе.
Около 2% девочек пубертатного периода имеют ЖДА, в значительной мере обусловленную менструальными потерями крови на фоне бурного роста. А среди беременных или родивших девушек-подростков ЖДА встречается более чем в 30% случаев.
У большинства детей клинические проявления ЖДА отсутствуют. Именно поэтому целесообразно проводить скрининг на ЖДА у детей раннего возраста. Согласно Протоколу медицинского наблюдения здоровых детей до трех лет, принятому в Украине, всем детям в возрасте 9 месяцев проводится определение уровня гемоглобина в крови, а у детей из групп риска это исследование может проводиться и в более ранние сроки.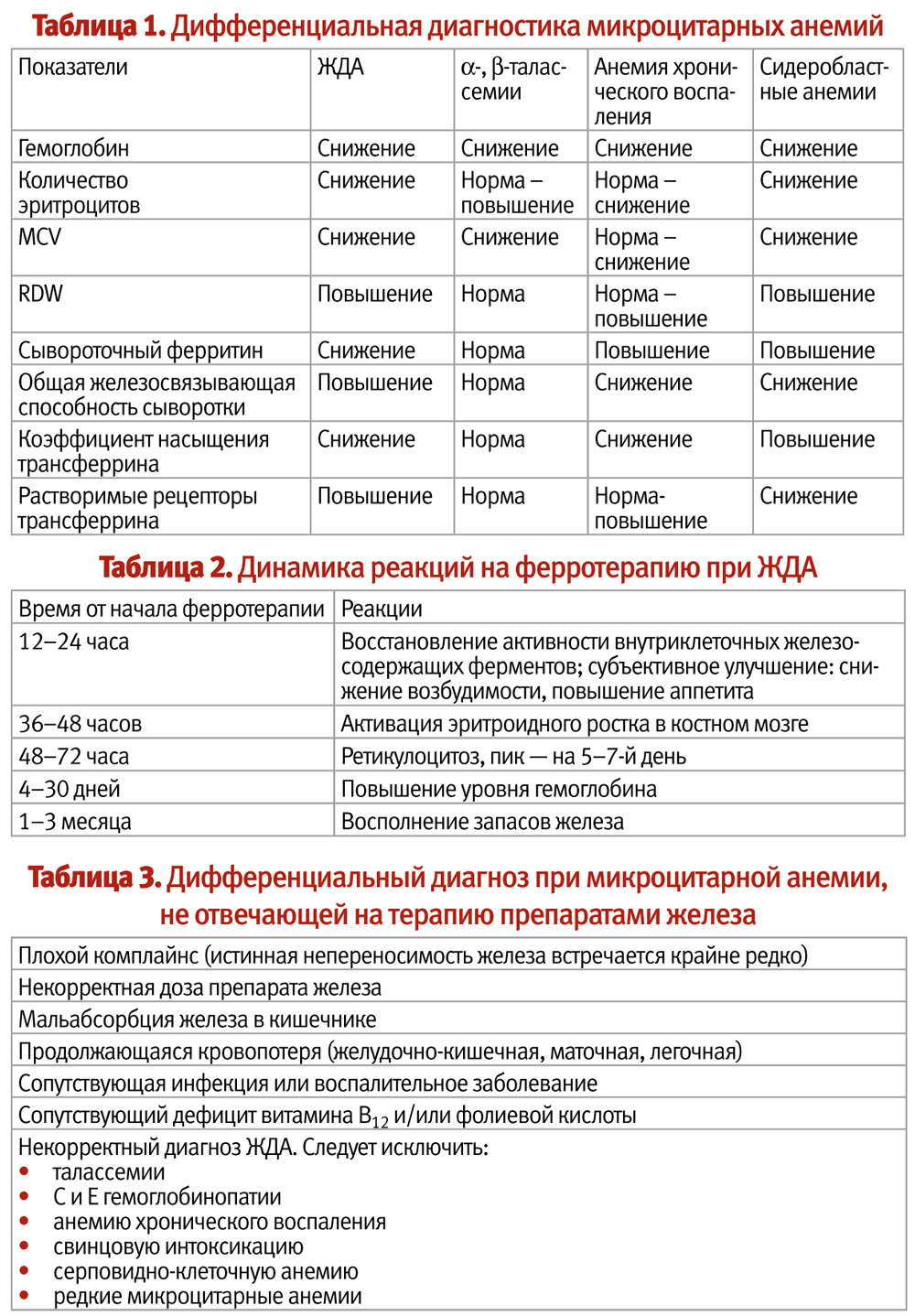
Бледность – наиболее важный клинический признак анемии – при ЖДА, как правило, проявляется, когда уровень гемоглобина снижается до 70–80 г/л. Наиболее показательно побледнение ладоней, ногтевых лож и конъюнктив. Родители часто не замечают бледности ребенка из-за типичного для ЖДА медленного снижения уровня гемоглобина.
При уровнях гемоглобина в пределах 60–100 г/л компенсаторные механизмы (увеличение уровня 2,3-дифосфоглицерата и сдвиг кривой диссоциации кислорода), могут быть настолько эффективными, что других признаков анемии, кроме некоторой раздражительности, не отмечается. И лишь при снижении концентрации гемоглобина до 50 г/л и менее, появляется анорексия, утомляемость, сонливость, а также систолический шум при аускультации сердца. При дальнейшем падении уровня гемоглобина наблюдается тахикардия. Повышение минутного объема кровотока в условиях гипоксии может привести к развитию сердечной недостаточности.
Дефицит железа имеет и негематологические системные проявления. Так, у детей раннего возраста нарушения психомоторного развития могут появиться даже раньше, чем анемия. Есть сведения, что после устранения дефицита железа полного восстановления функций ЦНС не происходит, что придает еще большее значение своевременной диагностике и коррекции железодефицита.
Извращение аппетита, проявляющееся желанием есть непищевые вещества (мел, землю и т. д.) и пагофагия – желание есть лед – являются другими системными признаками дефицита железа. Из-за извращения аппетита дети могут поедать вещества, содержащие свинец, что может привести к сопутствующей свинцовой интоксикации, которая сама по себе способствует развитию анемии (сидеробластной).
Диагностика ЖДА обычно не представляет трудностей. Изменения со стороны красной крови при ЖДА включают:
- снижение уровня гемоглобина и количества эритроцитов;
- микроцитоз (уменьшение MCV);
- гипохромию или снижение среднего содержания гемоглобина в эритроците (МСН) и средней концентрации гемоглобина в одном эритроците (МСНС);
- анизо- и пойкилоцитоз или увеличение RDW.
Следует учитывать, что объем эритроцитов изменяется с возрастом. У новорожденных показатель MCV находится в диапазоне 105–120 фл, у детей в возрасте 6 мес.–6 лет — 70–74 фл, 7–12 лет — 76–80 фл, у взрослых — около 80 фл. Нижнюю границу нормального показателя MCV можно рассчитывать по формуле «70 + количество лет». Т. е., у ребенка 3 лет в норме средний объем эритроцита не должен быть меньше, чем 73 фл.
Показатели белой крови не изменяются, нередко отмечается тромбоцитоз.
Обязательно проводится исследование кала на скрытую кровь.
Если анализ крови выполнен в полном объеме и в нем наличествуют все типичные для ЖДА изменения (гипохромная микроцитарная анемия с ретикулоцитопенией и анизоцитозом, нормальное или повышенное содержание тромбоцитов, нормальные показатели лейкоцитов), то лабораторного подтверждения дефицита железа не требуется. В других ситуациях, например, когда анализ крови неполный, присутствуют другие осложняющие клинические факторы, анемия тяжелая или не отвечает на ферротерапию, показано изучение ферростатуса ребенка.
Биохимическим подтверждением наличия дефицита железа является:
- снижение уровня сывороточного ферритина;
- снижение уровня сывороточного железа;
- повышение общей железосвязывающей способности сыворотки (сывороточного трансферрина);
- снижение коэффициента насыщения трансферрина.
Дифференциальный диагноз при ЖДА проводят с другими микроцитарными анемиями (a- или b-талассемия, гемоглобинопатии, сидеробластные анемии), а также с анемией хронического воспаления (табл. 1).
Лечение ЖДА, в первую очередь, подразумевает назначение препаратов железа. Одной лишь диетой восполнить дефицит железа невозможно. Быстрое восстановление уровня гемоглобина в ответ на адекватную дозу препаратов железа – характерная особенность ЖДА (табл. 2). Эффективность дополнения препаратов железа какими-либо витаминами, металлами или другими веществами в настоящее время убедительно не доказана.
Суточная терапевтическая доза составляет 3–6 мг/кг элементного железа. В настоящее время используют 2 группы пероральных препаратов железа: 1) препараты, содержащие соли двухвалентного железа и 2) препараты, содержащие гидроксид полимальтозный комплекс железа (ІІІ) (ГПК Fe3+).
Выгодным отличием препаратов 2-й группы является содержание железа в неионной форме, что существенно снижает риск неблагоприятных реакций со стороны ЖКТ и улучшает переносимость препарата. Кроме того, при использовании железа в виде гидроксид-полимальтозного комплекса ниже риск перенасыщения организма железом, его всасывание мало зависит от приема пищи и сопутствующей медикаментозной терапии. Таким образом, препараты на основе ГПК Fe3+ по эффективности, не уступающей ионным формам ферросодержащих препаратов, имеют гораздо лучшие показатели безопасности и переносимости, что, безусловно, повышает приверженность пациентов лечению.
Парентеральное введение железа не имеет никаких преимуществ по эффективности перед оральной терапией, при этом дорого и намного более опасно. Поэтому парентерально препараты железа назначаются только в случаях мальабсорбции или абсолютной непереносимости оральных форм.
Рекомендуемая в настоящее время длительность ферротерапии после нормализации уровня гемоглобина согласно принятому в Украине Протоколу (Приказ МЗ Украины №9 от 10.01.2005) — 3–6 месяцев в дозе в два раза меньше терапевтической. В зарубежных руководствах (Nelson Textbook of Pediatrics, 19th Edition, 2011) принято продолжать ферротерапию после нормализации уровня гемоглобина в полной терапевтической дозе в течении 8 недель. В случае недостаточной эффективности терапии препаратами железа следует рассмотреть возможность наличия отягощающих состояний или альтернативных диагнозов (табл. 3).
Рекомендации по коррекции питания обязательно дополняют ферротерапию. Девушкам с нарушениями менструального цикла назначается соответствующее лечение.
Дефицит железа гораздо легче и дешевле предотвратить, чем потом лечить его последствия.
Переливание крови может понадобиться только в случаях, когда анемия сопровождается застойной сердечной недостаточностью или является следствием серьезной кровопотери.
Основными мерами профилактики дефицита железа является сохранение грудного вскармливания, по меньшей мере, до 1 года, своевременное введение прикорма с употреблением продуктов, богатых железом. Дети на искусственном вскармливании должны получать обогащенные железом (12 мг/л) адаптированные смеси. Цельное коровье молоко не должно использоваться для вскармливания детей младше 1 года, а после года его суточное количество в рационе не должно превышать 600–700 мл. ![]()


коментарів