
ЕТИКА В АКУШЕРСТВІ ТА ГІНЕКОЛОГІЇ (ЧАСТИНА 2)
В епоху бурхливого технологічного прогресу для збереження рівноваги у суспільстві важливою є система моральних цінностей, що регулює стосунки між людьми. Ця потреба реалізується і у взаєминах лікаря та пацієнта, що лежить в основі медичної етики. Активно кооперуючись з медичним правом, медична етика є невід'ємною частиною діяльності лікаря. Читачеві пропонується огляд публікації*, що присвячена основам медичної етики та особливостям її в акушерстві та гінекології
Реалізація етичних принципів гуманності та поваги до автономії в акушерській практиці
Дотримання етичних принципів гуманності та поваги до автономії в акушерській практиці є значно більш складною задачею, ніж у гінекологічній. Очевидно, що вони мають істотний вплив на зобов'язання лікаря – приймаючи рішення про обстеження та лікування вагітної, лікар з огляду на максимальну користь, керується принципом гуманності, водночас врахування власних поглядів жінки на стан свого здоров'я вимагає від лікаря дотримання принципу поваги до автономії. Через недостатній розвиток центральної нервової системи плода не може йти мови про його цінності та переконання, а отже, немає підстав стверджувати про його бачення власних інтересів та про принципи поваги до його автономії. Права плода не прийнято враховувати при прийнятті рішень в акушерській практиці, хоча позиція про права ненародженої дитини наразі є дуже популярною в суспільному та політичному життя США та інших країн. Не викликає заперечень, що лікар зобов'язаний враховувати інтереси плода, і отже діяти, виходячи з позицій гуманності стосовно нього, але лише розглядаючи плід як пацієнта. Через важливе значення для акушерської клінічної практики, етична концепція плода як пацієнта вимагає особливо детального розгляду [4].

Етична концепція плода як пацієнта
Етична концепція плода в якості пацієнта є вкрай необхідною складовою прийняття рішення в акушерській практиці. Бурхливий прогрес діагностичних можливостей та стратегій покращення перинатальних наслідків також заохочують розвиток цієї концепції. Клінічне її значення полягає у тому, що розглядаючи плід як пацієнта, ми можемо застосовувати до нього безпосереднє консультування як рекомендовану форму участі його у прийнятті рішення для досягнення максимальних переваг, в той час, як не вважаючи плід пацієнтом, ми вдаємося до непрямого консультування, яке є припустимим, але не рекомендованим. Тим не менш, не завжди лікарі впевнені, чи можна сприймати плід як пацієнта. Нижче буде наведено підхід до вирішення цієї невизначеності, заснований на визначенні особистісних або інших моральних якостей плода. Оскільки показаний підхід не завжди є абсолютною відповіддю на це складне морально-юридичне питання, нами сформульовано альтернативний підхід, який є більш переконливим.
Незалежний моральний статус плода
Найбільш поширений підхід тлумачення плода у якості пацієнта передбачає показати незалежний моральний статус плода. Незалежний моральний статус плода означає, що одна або більше властивих плоду характеристик, незалежних від вагітної та інших чинників, генерують та обґрунтовують етичні зобов'язання щодо нього з боку матері та лікаря.
Багато із притаманних плоду властивостей було запропоновано на роль фактору незалежності, в тому числі момент зачаття, імплантації, розвиток центральної нервової системи та власне народження. Не дивно, що існують значні розбіжності між етичними аргументами щодо того моменту, коли плід набуває незалежного морального статусу. Момент зачаття, безперечно, ключовий у процесі утворення нового життя – злиття двох геномів гамет створює основу нового генотипу, сукупності нових властивостей. Втім, на думку N. Ford (1988), утворена зигота ще не проявила властивостей життя, тому про людську істоту варто говорити лише після імплантації.
Інші вважають, що незалежний моральний статус набувається поступово, тобто існують певні його ступені. Ще дехто вважає, хоч часто і приховує таку точку зору, що плід не має незалежного морального статусу протягом свого перебування в утробі [22, 23].
Незважаючи на постійно зростаючу кількість богословської та філософської літератури з цього питання, вона не містить єдиного авторитетного посилання на час появи незалежного морального статусу плода. Це не дивно, оскільки відсутній єдиний методологічний підхід у всіх теологічних та філософських течій, залучених у безкінечну дискусію, а без нього отримання остаточної відповіді, яка б влаштувала всіх, неможливе. Така відповідь мала би розв'язати одвічний диспут між філософськими та теологічними школами, стала б неймовірною за значенням культурною та інтелектуальною подією.
Іншими словами, наразі поняття незалежного морального статусу плода не має стабільного та клінічно апробованого значення – позаяк етична концепція розглядання плода у якості пацієнта не має ґрунтуватись на спірних твердженнях про незалежний моральний статус плода. Ми відмовились від цих марних спроб зрозуміти етичну концепцію плода як пацієнта з точки зору незалежного етичного його стану, і звернулись до альтернативного підходу, що дає можливість ідентифікувати унікальне значення плода як пацієнта та клінічні наслідки вибору прямого та непрямого консультування.
Залежний моральний статус плода
Наш підхід до обґрунтування етичної концепції плода у якості пацієнта починається з визнання, що бути пацієнтом не означає мати незалежний моральний статус. Певною мірою, бути пацієнтом означає можливість отримання вигоди від клінічної майстерності лікаря. Точніше кажучи, людську істоту без незалежного морального стану доцільно розглядати як пацієнта, якщо дотримані дві умови: 1) істоту надано лікарю, і 2) існують клінічні втручання, що можуть бути надійно ефективними та дати результат, а саме домінування переваг над шкодою у питанні людського життя [24]. Таке розуміння етичної концепції плода як пацієнта ми називаємо залежним моральним статусом плода.
Автори стверджують, що зобов'язання, засновані на принципі гуманності стосовно плода, мають право на існування, лише коли очікується, що плід пізніше набуде незалежного морального статусу в якості дитини та особистості [4].
Іншими словами, плід є пацієнтом, коли є представленим до медичного втручання, діагностичного чи лікувального, очікуваним результатом якого є отримання переваг, які домінують над можливою шкодою для дитини та особистості, що проявить себе пізніше, у ранньому дитинстві. Етичне значення концепції плода як пацієнта, таким чином, залежить від зв'язків, встановлених між плодом та подальшим набуттям ним незалежного морального статусу.
Життєздатний плід як пацієнт
Однією із таких ланок є життєздатність плода. Втім, сам цей термін варто розглядати як з позицій біологічного, так і технологічного поняття. Спираючись на обидві фактори, життєздатним вважають плід, який може існувати поза утробою матері та набути, таким чином, незалежного морального статусу. Коли плід життєздатний, тобто, коли він досяг достатнього рівня зрілості, щоб вижити в неонатальному періоді і набути незалежного морального статусу, навіть із наданням необхідної технічної підтримки, і коли він представлений до лікаря, його можна вважати пацієнтом.
Життєздатність є функцією як біологічного індивідуального розвитку, так і біомедичних технологічних можливостей. Останні є різними у різних частинах світу. Як наслідок, у світі на даний час не існує консенсусу щодо мінімального, критичного для виживання гетаційного віку. У Сполучених Штатах, як ми вважаємо, життєздатним є плід після 24 гестаційних тижнів [25, 26].
Якщо плід є пацієнтом, проведення консультування з огляду на безпосередні його інтереси (прямого консультування) є етично виправданим. У клінічній практиці пряме консультування щодо інтересів плода включає наступне: рекомендації проти переривання вагітності; рекомендації проти неагресивного ведення вагітності або рекомендації щодо агресивного її ведення. У цьому контексті агресивне ведення вагітності передбачає активний нагляд за станом плода, проведення токолізу або кесарського розтину у разі необхідності, за наявності показань – пологи в умовах центру високоспеціалізованої медичної допомоги. На противагу, неагресивна тактика ведення вагітності виключає будь-які втручання. Проводячи пряме консультування, варто взяти до уваги наявність та ступінь тяжкості вад розвитку плода, екстремальну його недоношеність та інтереси, пов'язані зі станом здоров'я самої вагітної.
При прийнятті клінічного рішення в акушерській практиці дуже важливо розуміти, що сила прямого консультування та його значення залежить від наявності та тяжкості аномалій. Як правило,чим більш важкою є вада розвитку плоду, тим менше доцільності у прямому консультуванні в інтересах плода. Зокрема, коли несумісну з життям аномалію, як, наприклад, аненцефалію, діагностовано з упевненістю, відсутні жодні засновані на принципі гуманності підстави для втручання. Ці пацієнти вмирають і консультування, таким чином, варто вважати непрямим, в його основі лежить обговорення вибору між перериванням вагітності та неагресивною тактикою, або прямим консультуванням, але зосередженим навколо аспектів материнського здоров'я [27].
На противагу цьому, переривання вагітності у ІІІ триместрі за наявності синдрому Дауна або ахондродисплазії з етичної точки зору не є обґрунтованим, тому що майбутня дитина має високі шанси рости та розвиватись як людська істота [28, 29].
Пряме консультування щодо інтересів плода у випадку екстремальної недоношеності є доцільним за умови життєздатності плода. Зокрема, це стосується плодів із гестаційним терміном 24–26 тижнів («ледве життєздатних плодів»), народжені у цей термін діти мають значний показник виживання, але водночас і високі показники смертності та захворюваності. Ці показники захворюваності та смертності зростають у разі застосування неагресивної акушерської тактики, водночас агресивне ведення вагітності може сприятливо впливати на результат. Таким чином виявляється, що агресивна тактика ведення вагітності є більш доцільною з точки зору дотримання принципу гуманності стосовно «ледве життєздатного плода».
Вищезазначене стосується випадків вагітності з терміном менше 26 тижнів. Зрозуміло, що пряме консультування є ще більш виправданим у пізніших термінах, коли екстремально недоношений плід є життєздатним.
Таке пряме консультування є доречним, лише коли воно засноване на документально підтвердженій ефективності того чи іншого медичного втручання щодо відповідного показання з боку плода. Наприклад, таку ефективність не було продемонстровано для рутинного кесарського розтину як способу розродження в екстремально малі терміни.
Будь-яке пряме консультування щодо інтересів плода повинне балансувати у рамках принципів гуманності стосовно плода, гуманності стосовно матері та поваги до автономії матері.
Таке балансування має враховувати у тому числі і те, що ризик від медичного втручання для здоров'я жінки може бути обґрунтованим лише у випадку надійних доказів потенційної переваги для життєздатного плода або майбутньої дитини.
Унікальною особливістю акушерської етики є те, що дотримання принципу поваги до автономії вагітної пацієнтки у деяких випадках може вплинути на представлення життєздатного плода до лікаря.
Очевидно, що будь-яка стратегія прямого консультування щодо потенційної користі для плода, яка враховує і зобов'язання щодо інтересів здоров'я вагітної, завжди є відкритою для конфлікту між рекомендаціями лікаря і протилежним автономним рішенням пацієнтки. Такий конфлікт легше попередити, ніж розв'язати, попередження його найкраще досягнути у процесі отримання інформованої згоди шляхом діалогу протягом всієї вагітності, доповненого за необхідності переговорами та шанобливим переконанням [30].
Плід, що ще не досяг життєздатності, як пацієнт
Єдиним зв'язком, що можливий між плодом, що не досяг життєздатності, та майбутньою дитиною, є вільне рішення жінки. Адже жодні технологічні чинники не можуть забезпечити переходу такого плода у статус дитини. Отже, такий перехід можливий тільки за рішення жінки визнавати пацієнтом її плід, що ще не досяг життєздатності. Такий плід не можна визнавати пацієнтом без свідомого відповідного рішення жінки. Вагітна жінка є вільною утриматись або визнати пацієнтом свого плода, що ще не досяг життєздатності, один раз визнавши, – відмовитись.
Таким чином, представлення такого плода, що ще не досяг життєздатності, до лікаря, є функцією вільного вибору жінки [4]. Консультування пацієнтки щодо подальшого ведення її вагітності, коли плід ще не досяг життєздатності, є непрямим, включає вирішення питання стосовно пролонгування або переривання вагітності, якщо жінка відмовляється надати плоду статус пацієнта. Якщо ж вона у врегульованому порядку підтверджує статус свого плода як пацієнта, чинності набуває принцип гуманності стосовно інтересів плода та стає можливим пряме консультування.
Так само, як для життєздатних плодів, таке консультування повинно враховувати наявність та тяжкість аномалій плоду, екстремальну недоношеність та інтереси здоров'я самої вагітної. Коли пацієнтка не впевнена у наданні плоду статусу пацієнта, автори пропонують розглядати плід як такий, що тимчасово має статус пацієнта. Це виправдовує прямі консультування проти поведінки, яка може завдати значної та необоротної шкоди плоду, наприклад, токсикоманії, особливо алкоголю, поки жінка не приймає рішення, чи надавати плоду статусу пацієнта.
З-поміж іншого, непряме консультування доречно у випадку «ледве життєздатного плода», з гестаційним терміном 22–23 тижнів, для якого є поодинокі повідомлення про виживання новонародженого [25, 26, 31]. На наш погляд, агресивну акушерську та неонатальну тактику в таких випадках варто розглядати як клінічне дослідження, а не стандарт медичної допомоги. Немає необхідності отримувати від жінки згоди на визнання її плода, що ще не досяг життєздатності, пацієнтом, оскільки ефективність агресивної тактики ще потребує доказів [26].
Ембріон у пробірці, як пацієнт
Концепція плода, що ще не досяг життєздатності, стосується також ембріонів у пробірці. На перший погляд, ембріон у пробірці завжди є представленим до уваги лікаря, тому автоматично може вважатись пацієнтом. Тим не менше, для дотримання принципу гуманності всі медичні втручання повинні мати доведену потенційну ефективність.
Нагадаємо, що з точки цього принципу, сприйняття плода у якості пацієнта визначається незалежним його моральним статусом. Тобто доцільність будь-якого втручання залежить від того, чи стане ембріон в пробірці у майбутньому життєздатним. В іншому випадку не можна говорити про жодну перевагу такого втручання. Ембріон може досягнути життєздатності лише пройшовши етап клітинного поділу в пробірці, трансфер, імплантацію та подальший внутрішньоутробний розвиток до досягнення сумісного з життям терміну. Процес досягнення життєздатності відбувається лише у природних умовах, і, отже, повністю залежить від рішення жінки про статус плода (ів) у якості пацієнта. Чи досягне ембріон з пробірки стану життєздатності, чи матиме медичне втручання на ньому переваги, залежить від автономного рішення жінки відмовитись, підтвердити, або, одного разу підтвердивши, відмовитись визнавати плід, що ще не досяг життєздатності, пацієнтом, що і є головним результатом даної концепції.
Таким чином, доцільніше розглядати ембріон в пробірці як плід, що ще не досяг життєздатності, ніж як життєздатний плід. Як наслідок, розглядати ембріон (и) з пробірки у якості пацієнта варто лише тоді, коли жінка, в матку якої перенесено його, надає йому такого статусу. Таким чином, консультування щодо передімплантаційної діагностики повинне бути непрямим, адже жінка може обрати відмову від імплантації аномальних ембріонів. Ці ембріони не мають статусу пацієнтів, тому відсутні підстави для прямого консультування. Обов'язково слід надати інформацію про прогноз для успішної вагітності, можливість прийняття або відмови від рішення про селективну редукцію залежно від кількості ембріонів. При проведенні консультування з приводу кількості ембріонів, що їх буде перенесено, слід користуватись лише науково доведеними даними [32].
Три концепції справедливості
Етична проблема справедливості виникає за умови обмеження ресурсів. Справедливість вимагає, щоб у процесі розподілу ресурсів кожен отримував те, на що заслуговує. Різні концепції справедливості по-різному підходять саме до поняття «те, що заслуговує». Ми прагнемо справедливого розподілу благ, тобто доступу до ресурсів, та обтяжень, тобто ризиків, що є результатом відсутності такого доступу.
Утилітаризм є теорія справедливості, що в основі проблеми встановлює прагнення досягти максимального блага для максимальної кількості людей у царині розподілу дефіцитних ресурсів. Тому для успішного керівництва та прийняття щоденних рішень утилітаризм вимагає врахування найбільшого блага.
Для суспільства в цілому досить важко, якщо взагалі можливо, визначити, що є найбільшим благом. Значення утилітаризму полягає у балансі – пошуку такого розподілу благ та тягарів, щоб нерівномірність цього розподілу не спричинила нерівності між людьми, тобто несправедливості.
Критики утилітаристів підкреслюють цю нерівність, яка є результатом розподілу благ та тягарів [33].
Для подолання цієї проблеми було розроблено два інші підходи.
Першим із них є концепція лібертаріанства, покликана усунути явища тиранії, властиві чистому утилітаризму. Зокрема, лібертаріанство було розроблене для надання пріоритету індивідуальної свободи і прав власності, коригуючи потенційно можливе домінування багатих класів у політичній царині та у сфері управління державою.
Лібертаріанці стверджують, що на ринку, який по-різному оцінює різні послуги та продукти та надає рівні можливості для розвитку талантів, ті, хто надає послуги, які більше цінуються, справедливо заробляє більше, ніж ті, хто надає менш популярні (необов'язково при цьому менш цінні) послуги. Кожна людина має право сама розпоряджатись заробленими у таких ринкових умовах коштами, що і є проявом головного лібертаріанського принципу – права на власність. Лібертаріанство підкреслює рівність у процесі, а не у розподілі результатів.
Третя концепція – егалітарної справедливості, яку було розроблено для захисту вразливих і знедолених членів суспільства, що можуть опинитись незахищеними в процесі утилітарного розподілу дефіцитних ресурсів. Такий підхід попереджає несправедливість розподілу в аспекті надмірного тягаря для тих, хто менш здатний захистити себе.
Ці три концепції, як і інші концепції справедливості, продовжують перебувати у стані незавершеної боротьби між собою [34]. Що стосується літератури з питань медичної етики, то вона у більшості своїй перебуває під впливом концепції рівномірних можливостей (варіант лібертаріанства) та захисту більш вразливої частини суспільства (елемент егалітарної справедливості). Тим не менше, не можна сказати, що один із принципів чинить домінуючий вплив на політику охорони здоров'я у Сполучених Штатах. Ця відсутність концептуально-послідовної політики є давньою рисою американської системи охорони здоров'я. Зокрема, в Сполучених Штатах актуальною є проблема створення загального права охорони здоров'я (де б домінував принцип лібертаріанства) та селективних систем, наприклад, надання медичної допомоги особам літнього віку (Medicare), малозаможним прошаркам населення (Medicaid), кваліфікованим працівникам певної галузі.
Перелік літератури знаходиться у редакції.
Підготувала Олександра Загородня.
Детальніше
Мини-MBA по гинекологии. Модуль 4. Проблемы переходного возраста. 18 сентября 2015 года. Лектор: Михаил Медведев
Учимся властвовать над временем
18 сентября мы провели очередной мастер-класс. Наша задача – не только указать врачам новые творческие направления, осветить разнообразные аспекты традиционных тем, но и открыть новые имена, представить новую генерацию экспертов в области акушерства и гинекологии.
В этот раз мастер-класс провел профессор Днепропетровской медицинской академии Михаил Медведев, который открыл участникам все тонкости переходного возраста женщины! Почему мы пригласили именно этого спикера (и как оказалось, не ошиблись, судя по многочисленной аудитории)?
Во-первых, он обладает знаниями и большим практическим опытом. Во-вторых – умеет делиться этим опытом с коллегами.
За 8 часов участники мероприятия смогли не только познакомиться с передовыми зарубежными практиками, услышав ценное мнение эксперта, но и активно поучаствовать в дискуссии.
Разумеется, тет-а-тет общение с экспертом не заменит никакая статья.
Поэтому не упускайте возможность посещать наши образовательные сессии!
Посмотреть и скачать все фото: goo.gl/0qZVzp

Детальніше

ВЕДЕННЯ ЖІНОК З НИЗЬКИМ РІВНЕМ PAPP-A БЕЗ ХРОМОСОМНИХ АНОМАЛІЙ
 Шановні читачі! Пропонуємо вам практичне керівництво з перинатології, видане у Південній Австралії 2014 р.* Це керівництво надає поради загального характеру і підготовлене для заохочення і полегшення стандартизації та узгодженості клінічної практики з використанням міждисциплінарного підходу. Керівництво засноване на оглядах і опублікованих доказах та думках експертів
Шановні читачі! Пропонуємо вам практичне керівництво з перинатології, видане у Південній Австралії 2014 р.* Це керівництво надає поради загального характеру і підготовлене для заохочення і полегшення стандартизації та узгодженості клінічної практики з використанням міждисциплінарного підходу. Керівництво засноване на оглядах і опублікованих доказах та думках експертів
Вступ
- Всім жінкам у І триместрі повинен бути запропонований Комбінований скринінг між 9 і 14 тижнями вагітності, з адекватним консультуванням перед його проведенням.
- До скринінгу входить виконання комплексу заходів: вимірювання у сироватці крові матері рівня вільного бета-хоріонічного гонадотропіну людини (ВБ-ХГЛ) і асоційованого з вагітністю протеїну-А плазми (РАРР-А) на 9–13+6 тижні вагітності, поряд з вимірюванням товщини комірцевого простору (ТКП) у мм за даними УЗД на 11–13 тижні вагітності, поєднанні з фоновими ризиками, такими як вік, вага матері та термін гестації, ці вимірювання дозволяють зробити оцінку ризику для плода з синдромом Дауна або трисомією за 18 хромосомою [1].
- У випадку вагітності підвищеного ризику можуть бути запропоновані пренатальне діагностичне тестування за допомогою виконання біопсії хоріона або амніоцентезу.
РАРР-А
- РАРР-А є глікопротеїном великого розміру, продукується плацентою і децидуальною оболонкою. Вважають, що він чинить вплив на кілька функцій, включаючи:
- запобігання розпізнання плоду імунною системою матері;
- мінералізацію матриксу;
- розвиток кровоносних судин.
- Низький рівень РАРР-А відповідає недостатній ранній плацентації і може призвести до несприятливих наслідків вагітності, таких як [2, 3]:
- невиношування у другому
триместрі; - затримка росту плода;
- внутрішньоутробна загибель плода;
- передчасні пологи;
- прееклампсія.
- Під час вагітності після застосування ДРТ при скринінгу у І трим. рівень РАРР-А є зниженим, що призводить до збільшення ймовірності отримання хибнопозитивних результатів і необхідності проведення біопсії ворсин хоріона/амніоцентезу.
Низькі рівні РАРР-А можуть вказувати на порушення імплантації на ранніх термінах після застосування деяких видів ДРТ [4].
- Аномальні рівні РАРР-А визначаються, як концентрації РАРР-А у сироватці крові матері <5-го процентилю, зі збільшенням частоти несприятливих акушерських результатів при перетині межі нижче цього рівня [5].
- Хоча ризик ускладнень вагітності збільшується, коли РАРР-А <5-го процентилю, рівень РАРР-А менше 1-го процентилю свідчить про особливо значний ризик для вагітності [6].
Примітка. Точна маса тіла матері повинна бути встановлена після отримання результату скринінгу в І триместрі, тому що вона чинить істотний вплив на концентрацію РАРР-А.
Дослідження FASTER5
- Дослідження з оцінки ризику у І та ІІ триместрі (FASTER).
- Проспективне багатоцентрове дослідження Американського національного інституту здоров'я дитини і розвитку людини (невибрана популяція дослідження – 34411 учасників).
- Низький рівень РАРР-А є найбільш поширеним маркером несприятливого результату вагітності.
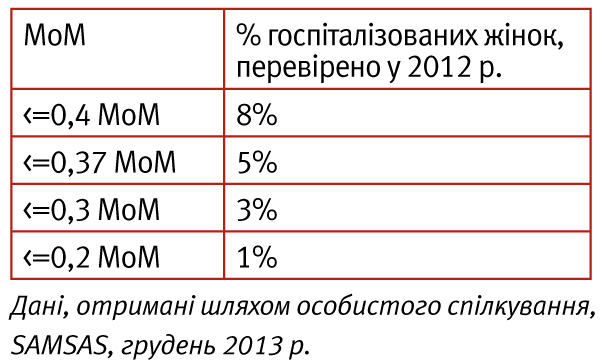
- Низький рівень РАРР-А у дослідженні FASTER був визначений як <5-го проц. У дослідженні FASTER це відповідало 0,4 MoM. Однак, 5-й проц., за даними SAMSAS, становить 0,37 MoM і є нижнім рівнем релевантності для Південної Австралії.
- Показники рівня обернено пропорційні до реакції.
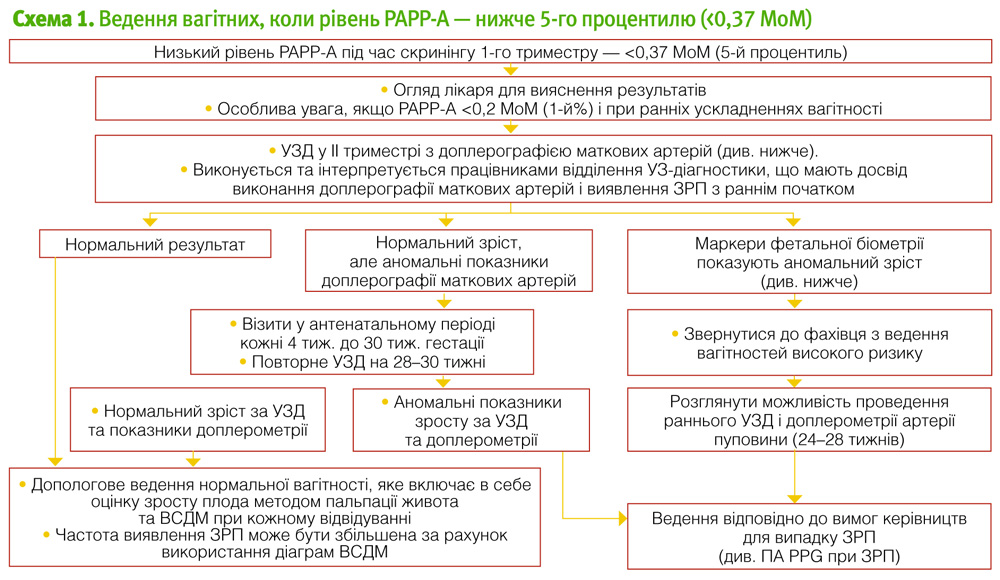
PAPP-A <5-го процентилю (див. табл. 1) 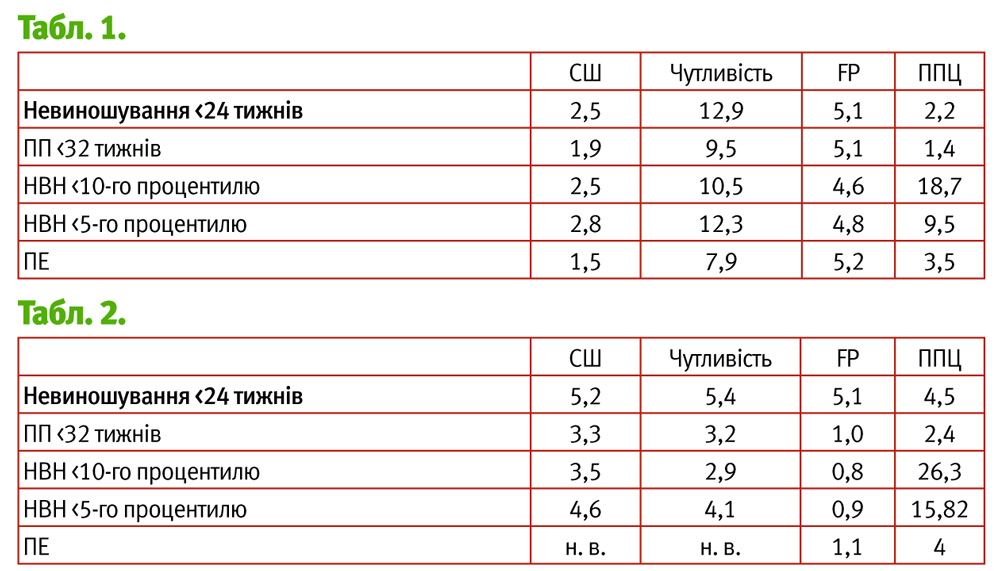
- Підвищений ризик внутрішньоутробної загибелі плоду. Переважно на ранніх термінах.
- ППЦ для втрати вагітності <24 тижнів – 2,2.
- ППЦ для втрати вагітності >24 тижнів – лише 0,6.
- Підвищений ризик ЗРП (ВН <10-го процентилю).
- ППЦ майже 20%.
- Показник помилково-позитивних результатів на рівні 5% для всіх несприятливих подій з іншими скринінговими тестами І триместру.
РАРР-А <1-го процентилю (див. табл. 2)
- ППЦ для втрати вагітності <24 тижнів – 4,5.
- ППЦ для втрати вагітності >24 тижнів лише – 0,8.
- НВН <10-го процентилю – ППЦ 26,3.
- НВН <5-го процентилю – ППЦ 15,8.
- Якщо результати УЗД в другому триместрі були нормальними у жінок з аномальним рівнем РАРР-А, тільки у 4,8% з них у третьому триместрі було діагностовано гіпотрофію плода (95% НПЦ).
- Однак, коли УЗД у другому триместрі показало ознаки ЗРП, ці пропорції склали 38,9%.
Чутливість і ППЦ
- Низький рівень РАРР-А має низьку чутливість для передбачення несприятливого результату вагітності.
- Однак, ці асоціації існують в нижній частині графіку розподілу РАРР-А.
- Більшість вагітних жінок з такими несприятливими результатами не мають низького рівня PAPP-A.
- Крім того, вимірювання PAPP-A має низьку позитивну прогностичну цінність, лише невелике число пацієнтів з низьким PAPP-A насправді мали несприятливий результат вагітності.
- 89% жінок мали нормальний результат при PAPP-A <0,2 MoM [7].
Дослідження SAMSAS
- При визначенні процентилів, рекомендується, за можливості, використовувати місцеві дані.
Терміни дослідження
- Виконання УЗД у ІІ триместрі дає можливість проведення подальшого скринінгу ЗРП і, таким чином, відповідного ведення вагітної.
- При прийнятті рішення про акушерське ведення до пологів, акушерська команда повинна знати, на якому терміні вагітності почався аномальний ріст плода за допомогою ранніх скринінгових тестів за межами нормального часового діапазону.
- Кілька досліджень, проведених серед жінок з низьким сироватковим рівнем PAPP-A у першому триместрі показали аномалії росту від початку другого триместру.
Фетальна біометрія
- Фетальна біометрія за допомогою УЗД визначення морфології може продемонструвати маркери обмеження зростання плода [8]. Поєднання низьких значень PAPP-A і ранного обмеження росту плода збільшує ризик несприятливих наслідків вагітності майже в шість разів [9].
- Маркери біометрії плода у ІІ триместрі для аномального росту повинні використовуватися в поєднанні з РАРР-А <5-го проц., щоб визначити цю популяцію високого ризику.
- ОМП (оцінювана маса плода) <2,5 проц. під час вагітності [8].
- Середні показники віку за даними фетальної біометрії УЗД більше, ніж на 7 днів менші, ніж точно встановлені терміни (за датою останньої менструації і УЗД на 12 тиж.).
- Cпіввідношення окружності голови (ОГ) до окружності живота (ОЖ) >90-го проц. для гестаційного віку.
Доплерографія маткових артерій
- Доплерографія маткових артерій під час досліджень морфології дозволяє зробити подальшу стратифікацію ризику ЗРП у жінки з низьким рівнем РАРР-А [10].
<1-го процентилю MOM ≤0,2 MoM
- При екстремальних рівнях фетоплацентарних протеїнів (<1-го проц.).
- 20% жінок мали аномальні показники при доплерівському дослідженні маткових артерій (у порівнянні з 5% у загальній популяції) на 22–24 тижні вагітності.
- 65% жінок з екстремальними рівнями фетоплацентарних білків і аномальними показниками допплерометрії маткових артерій мали несприятливий результат вагітності (низька вага при народженні, гіпертензія, передчасні пологи або викидні) в порівнянні з 34% з нормальними даними доплерометрії маткових артерій.
Ведення
- Відповідно до останніх даних SAMSAS, критичний рівень, після якого ризик зростає, повинен бути встановлений на 5-му процентилі (0,37 MoM).
- Підтвердження точної маси тіла матері за даними SAMSAS (високий ІМТ буде штучно занижувати PAPP-A MoM). Якщо дані про відповідну масу тіла матері відсутні, слід звернутись до SAMSAS за правильними даними, а потім потрібно буде уточнити результат.
- Жінок, які мають низький рівень PAPP-А під час скринінгу І триместру, практичний лікар, який призначив тест повинен проконсультувати про ризик ускладнень вагітності, пов'язаних з низьким PAPP-A.
- Жінки з РАРР-А <1-го проц. потребують особливої уваги через ризик викидня у ІІ триместрі. Вважається, що вони повинні проходити обстеження лікарем на 16–17 тижні для аускультації серцебиття плода.
УЗД у другому триместрі
- УЗД у ІІ триместрі з приводу дослідження морфології плода, як правило, проводиться на 19 тиж. вагітності.
- Направлення до відділення діагностики повинне включати інформацію про результат скринінгу у І трим. зі вказанням рівня PAPP-A <5-го процентилю (0,37 MoM).
- Працівники відділення діагностики повинні мати досвід виконання та інтерпретації результатів доплерометрії маткової артерії і незначних порушень біометрії плода, як описано вище.
- Для вагітностей з рівнем PAPP-A <5-го процентилю (0,37 MoM) УЗД з метою дослідження морфології повинне включати в себе оцінку результатів доплерометрії маткових артерій.
Ультразвукова доплерометрія маткових артерій11
Аномальні дані доплерометрії:
- Середній Rl (лівої і правої) >0,70.
- Середній Rl (лівої і правої) >0,65. з однобічною діастолічною виїмкою.
- Двобічні виїмки.
Дані УЗД дозволяють встановити розміщення плаценти
- Центральне, переднє або заднє.
- Праве латеральне.
- Ліве латеральне.
Будь-які ранні аномалії росту
- ОЖ <10-го процентилю.
- Середній вік за даними УЗД більше, ніж на 7 днів відрізняється від встановлених термінів.
Нормальні дані УЗД у ІІ триместрі
- Якщо дані УЗД у ІІ триместрі є нормальними, слід заспокоїти жінку, що ймовірність несприятливого результату є приблизно такою, як і для популяції без аномалій. Жінка вимагає рутинного спостереження за зростом плода:
- Під час кожного допологового візиту вимірювати висоту стояння дна матки (ВСДМ) і відмічати його на графіку ВСДМ.
- Вимірювання ВСДМ повинне проводитись від верхньої частини дна до фіксованої точки на верхньому краї лобкового симфізу. Вимірювання виконується вздовж осі плода, використовуючи нееластичну рулетку5.
- ЗРП підозрюється, коли результати вимірювання є меншими 10-го процентилю для терміну вагітності або коли на графіку результати вимірювання ВСДМ перетинають лінію процентилів у зворотному напрямку.
- Діагностична точність може бути поліпшена за рахунок використання спеціалізованих графіків зросту [12, 13].
- Якщо не вдається точно виміряти ВСДМ (наприклад, жінка має високий індекс маси тіла), корисним може бути застосування УЗД для калібрування ВСДМ на близько 28–30 тижні гестації.
- Для отримання додаткової інформації див. керівництво з клінічної оцінки обмежень зросту плода.
- Якщо клінічний зріст відповідає нормальному для даного терміну вагітності, немає жодних показань до ранньої індукції пологів, і термінові пологи проводяться за нормальними акушерськими показаннями.
Нормальний зріст і аномальні показники доплерографії маткових артерій під час УЗД ІІ триместру
- Слід розглянути виконання УЗД на 28–30 тижні вагітності, щоб оцінити зріст плоду, дані доплерівського дослідження артерій пуповини та індекс навколоплідних вод (ІНВ).
- Якщо під час цього УЗД діагностується ЗРП, для подальшого ведення слід звернутись до керівництва з клінічного ведення вагітності при ЗРП.
- Якщо ріст є симетричним і відстежується паралельно до лінії процентилів, ризик ЗРП зменшується до рівня фонового ризику, і, отже, жінка може отримувати стандартне допологове ведення, як описано вище.
Аномальний зріст і нормальні показники доплерографії маткових артерій під час УЗД ІІ триместру
- Ці жінки перебувають у групі підвищеного ризику розвитку ЗРП із раннім початком і загибелі плоду.
- Слід розглянути виконання УЗД на 24–28 тиж. вагітності, щоб оцінити зріст плоду, дані доплерівського дослідження артерій пуповини та ІНВ.
- Якщо є стійкі ознаки ЗРП із раннім початком, для подальшого ведення слід звернутись до керівництва з клінічного ведення вагітності при ЗРП.
- Якщо графік зросту повертається до нормального, частота УЗД може бути зменшена, або ці дослідження навіть можуть припинитись.
Аномальний ріст і аномальні показники доплерографії маткових артерій під час УЗД ІІ триместру
- Ці жінки перебувають у групі підвищеного ризику розвитку ЗРП із раннім початком і загибелі плоду. Їх ведення повинне здійснюватись разом з фахівцем акушером, що має досвід ведення вагітностей високого ризику.
- УЗД для вимірювання росту, допплерометрії та ІНВ проводиться у 24–26 тижнів.
- Якщо є стійкі ознаки ЗРП із раннім початком, для подальшого ведення слід звернутись до керівництва з клінічного ведення вагітності при ЗРП.
- Якщо графік зросту повертається до нормального, частота УЗД може бути зменшена, або ці дослідження навіть можуть припинитись.
Гіпертензивні розлади
- Жінки з низьким рівнем PAPP-A та аномальними показниками доплерографії маткових артерій схильні до ризику прееклампсії з раннім початком.
Цих жінок без будь-яких інших факторів ризику після 20 тижнів вагітності слід оглядати частіше. Вони повинні відвідувати лікаря, принаймні, кожні 4 тижні до 30 тижнів вагітності, і частіше, якщо помічені ознаки прееклампсії.
Перелік літератури знаходиться у редакції.
 Коментар експерта
Коментар експерта
За рекомендаціями та роз’ясненнями, як ці рекомендації можна адаптувати до української практики, ми звернулися до головного лікаря ОКУ «Міжобласний центр медичної генетики і пренатальної діагностики» (м. Кривий Ріг), Заслуженого лікаря України Миколи Петровича Веропотвеляна
Багато лікарів в Україні використовують цей фактор у клінічній практиці як предиктор потенційних ускладнень та несприятливого висліду вагітності, проте! До сьогодні немає єдиного керівництва чи рекомендацій щодо тактики ведення вагітності в таких умовах.
Запропоноване до розгляду практичне керівництво перинатологів штату Південної Австралії – алгоритм ведення вагітності з рівнем РАРР-А нижче 5-го процентиля, котрий передусім націлений на ранню діагностику ЗРП з раннім початком. Певним чином він впорядковує дії спеціаліста, та по суті являє собою селективний варіант допплерингу (деякий час в минулому десятиліття цей метод широко пропагувався в світі у якості додатку до масового пренатального УЗ-скринінгу в II триместрі).
У наданому керівництві зазначено: «УЗД у ІІ триместрі з приводу дослідження морфології плода, як правило, проводиться на 19 тижні вагітності»; в той же час, не конкретизуючи коли саме, авторами пропонується у 2-му триместрі вагітності проводити допплерометрію маткових артерій для вагітностей з рівнем PAPP-A <5 процентилю (0,37 МоМ) у І триместрі. Оцінюючи цю рекомендацію, слід прийняти до уваги той факт, що у 18–20 тижнів гестації спостерігається значна доля хибнопозитивних результатів при оцінці кровотоку в маткових артеріях.
Подальша схема претанальної детекції ЗРП базується лише на УЗ-фетальній біометрії та допплерометрії матково-планцентарного та плодово-плацентарного артеріального кровотоку. Що не є вичерпним!
Вже не перший рік для для диференціювання плодів, конституційно малих для свого терміну гестації, і плодів із ЗРП та прогнозування наслідків цих вагітностей, успішно використовується оцінка церебро-плацентарного співвідношення (індексу). На жаль, цей показник не знайшов свого місця у представленому алгоритмі.
Згідно керівництва, жінок з низьким рівнем PAPP-A та аномальними показниками допплерографії маткових артерій, як схильних до розвитку прееклампсії з раннім початком, рекомендується з 20 по 30 тиждень оглядати частіше (кожні 4 тижні), але окрім аускультації серцебиття плоду та виміру висоти дна матки, мова ні про що інше не йдеться. При цьому автори самі підкреслюють, що вимірювання PAPP-A має низьку позитивну прогностичну цінність і радять особливо прискіпливо ставитися до вагітних жінок з показником PAPP-A нижче 0,2 МоМ.
Для звуження кола вагітностей з високим ризиком зазначених акушерських ускладнень, на мій погляд, доцільно додати в алгоритм обстеження інші біохімічні маркери – плацентарний фактор росту (placental growth factor – PIGF), зниження його рівня також асоціюється із ЗРП та прееклампсією. Цей показник можна визначати як у I (11–14 тиж.), так і в II (16–20 тиж.) і III (30–34 тиж.) триместрах вагітності. З цією ж метою з кінця II та в III триместрі можна досліджувати рівень екскреції такого білка, розчинної fms-подібної тирозинкінази-1 (SFLT-1) та інших біохімічних маркерів (АФП, ХГЛ), що у комплексі істотно підвищує чутливість виявлення патології.
Що стосується представленого керівництва, то вже у першому абзаці вступу виникає питання відносно методології проведення скринінгу. Вимірювання біохімічних маркерів (PAPP-A, β-ХГЛ) у сироватці крові проводиться у терміні 9–14 тижнів, а ТКП (за даними УЗД) – на 11–14 тижні. Питання: а як саме без УЗД з 9 по 11 тиждень можна точно визначити термін вагітності, куприково-тім’ячковий розмір? Також є неприпустимим, щоб між виміром БХ-маркерів та ТКП пройшло 2 тижні, а не одна доба (максимум три), як допускає FMF.
Особливу увагу читачів звертаю на вказані в алгоритмі порогові значення рівня РАРР-А – менше 0,37 МоМ! Це дуже «делікатний» момент, котрий вимагає роз’яснень. Автори документу представляють результати двох масштабних досліджень і звертають увагу на те, що в них різні рівні РАРР-А, що відповідають формулюванню «нижче 5 процентиля». Отже, згідно результатів «рідного» дослідження SAMSAS (Південна Австралія), релевантний показник екскреції РАРР-А нижче 5 процентиля відповідає 0,37 МоМ, в той же час, за результатами дослідження, виконаного у «нерідній» популяції в США FASTER, він становить 0,4 МоМ.
Цей факт чітко підкреслює недопустимість прямого переносу цих порогових значень на українську популяцію. Питання не лише в етнічних особливостях (оскільки ці рекомендації стосуються одного штату, з високою вірогідністю можу припустити, що дослідження були виконані за єдиним стандартом в одній мережі лабораторій). Для коректного трактування цього критерію необхідно знати, яким методом проводився біохімічний тест (імуноферментним чи імуно-хемілюмінісцентним або імунофлюоресцентним, що впливає на рівень чутливості тесту), на якому аналізаторі та з застосуванням яких реагентів (аналітів).
В Україні більшість комерційних лабораторій виконує панель пренатального скринінгу на автоматичних аналізаторах «IMMULITE» («Siemens», Німеччина) – твердофазний імуно-хемілюмінісцентний аналіз, і звичайних «відкритих» БХ-рідерах – твердофазний ІФА. Лише одиничні лабораторії виконують ці дослідження згідно рекомендацій FMF – на автоматичних аналізаторах «KRYPTOR» («BRAHMS», Німеччина) – імунофлюоресцентний аналіз з відкладеною в часі ампліфікованою прихованою емісією за унікальною технологією TRACE, та «ROSHE» («COBAS», Швейцарія), «Perkin Elmer» («Delfia», США ) з відповідними реагентами.
Все перераховане не дозволяє нам отримати однозначну відповідь щодо порогового значення РАРР-А. Найправильніше було би провести пілотне дослідження у наших субпопуляціях вагітних з використанням регламентованих реагентів.
Подібне пілотне дослідження (окрім PAPP-A, β-ХГЛ, включало визначення PLGF та SFLT-1) нещодавно було проведене Донецькими колегами (проф. Арбузова С. Б., проф. Ніколенко М. І.).
Тож, якщо взяти до уваги наші реалії, я б рекомендував брати до уваги результати лише потужних акредитованих лабораторій з нижнім пороговим значенням РАРР-А менше 5 процентилю.
А для підвищення ефективності ранньої доклінічної діагностики ЗРП, прееклампсії (вагітним з групи ризику, тобто з РАРР-А нижче порогового), рекомендував би повторне визначення РАРР-А у ІІ триместрі (16–20 тиж.) і при повторних показниках РАРР-А <0,4МоМ, окрім допплерометрії у 22–24 тиж. гестації, у 25–30 тиж. варто провести оцінку відношення екскреції PLGF/SFLT-1 (антиангіогенного/ангіогенного факторів) + контрольну допплерометрію (в т. ч. з оцінкою CPI, за потреби – з використанням on-line калькуляторів, рекомендованих експертами FMF). Все це дозволить нам суттєво підвищити прогностичну цінність цих тестів в діагностиці вищезгаданих ускладнень вагітності, і звичайно, покращити перинатальні наслідки у групі вагітних високого ризику.
Детальніше
СЕРКЛЯЖ НА ПІДСТАВІ ФІЗИКАЛЬНОГО ОБСТЕЖЕННЯ. Систематизоване ревю та мета-аналіз
 Тлумачення перекладача
Тлумачення перекладача
Особисто мені вперше потрапив на очі мета-аналіз, який має суттєві відмінності від раніше проведених та надрукованих досліджень у цій сфері. Різниця полягає у основному критерії, взятому за основу. Найчастіше в літературі зустрічається аналіз ефективності ургентного та терапевтичного серкляжів, накладених на підставі двох основних критеріїв: ознак істміко-цервікальної недостатності, виявлених під час УЗД, та історії втрат попередніх вагітностей у ІІ триместрі.
Даний мета-аналіз проводить оцінку ефективності серкляжу, накладеного на підставі фізикального обстеження в пацієнток при вагітності 14–27 тижнів. Цервікальна дилатація була суттєвою та складала від 0,5 до 5 см в окремих дослідженнях, з високою частотою наявності пролабування плодового міхура. Пацієнтки, які мали лише виміряне при УЗД вкорочення шийки матки без дилатації, з аналізу виключені.
Інші критерії виключення були різноманітні та доволі жорсткі, що дозволяє вважати похибку мінімальною, а висновки, зроблені на підставі аналізу, – достовірними.
Таким чином, йдеться про крайній варіант ургентного серкляжу (вочевидь, має сенс назвати його «екстремальним»), ефективність якого, зазвичай, на підставі хибних уявлень та відсутності доказової бази, ставиться під сумнів. Автори аналізу підходять до висновків вкрай обережно та одним з головних чинників успіху заходів з накладення такого «екстремального» серкляжу вважають коректний відбір пацієнтів.
Мета аналізу
Оцінити ефективність серкляжу, накладеного у ІІ триместрі при дилатації шийки матки на підставі аналізу та систематизації надрукованих досліджень. До аналізу залучені дослідження з вивчення лікування істміко-цервікальної недостатності шляхом накладання серкляжу. Пошук досліджень, надрукованих від 1966 до 2014 рр., проводився через пошукові ресурси MEDLINE, EMBASE, Scopus, Clinical Trials.gov, Web of Science, a також базу Cochrane.
Цервікальна недостатність, що раніше трактувалася як неспроможність, визначається як безболісна дилатація цервікального каналу за відсутності перейм або кровотечі в ІІ триместрі вагітності, що трапляється приблизно в 1% всіх вагітностей. Про накладання цервікального серкляжу при дилатації шийки або у випадку попередніх втрат у ІІ триместрі вперше доповів Shirodkar V. ще у 1950 р.
Накладання шва за наявності дилатації визначається як «невідкладне», або ургентне, або «призначене за результатами обстеження» і користь такої невідкладної допомоги для збереження вагітності залишається невизначеною.
Оптимальні оцінка та менеджмент асимптомних пацієнтів з цервікальною дилатацією залишаються суперечними. Існує лише одне рандомізоване дослідження з оцінки серкляжу при даному сценарії, воно включає лише 23 пацієнти, 7 з яких вагітні двійнею. Кілька нерандомізованих досліджень порівнювали наслідки вагітності в жінок з серкляжем та очікувальний менеджмент у випадку цервікальної дилатації у ІІ триместрі.
Метою даного ревю був систематизований огляд літератури з подальшою можливістю порівняння та комбінації результатів для отримання найбільш достовірного висновку щодо ефективності серкляжу.
Відбір досліджень
Для включення дослідження мало порівняти серкляж та очікувальну тактику у вагітних з визначеною під час фізикального обстеження дилатацією шийки від 0,5 см та більше при вагітності 14–27 тижнів. Дослідження, що оцінювали показання для серкляжу на підставі визначеної при УЗ-дослідженні ВКОРОЧЕНОЇ, ПРОТЕ ЗАКРИТОЇ шийки були виключені з мета-аналізу! Ступінь дилатації у дослідженнях коливався від найменшого 0,5–1 см (Pereira et al., 2008; Curti et al., 2012; Aoki et al., 2013) до 5 см (Novy et al., 2001; Ventolini et al., 2009), більшість дослідженнь припускали пролабування плодового міхура.
Критеріями виключення були: порушення цілісності плодових оболонок, кровотеча, наявність інфекції, пологи. Окремі дослідження категорично виключали пацієнток, що мали випадки самовільного переривання вагітності у ІІ триместрі, серкляж у попередню вагітність, маткові аномалії, багатоплодові вагітності, вади розвитку плоду, операції на шийці у минулому.
Зменшення гетерогенності було проведене для мінімізації похибки. Якість кожного дослідження перевірялася двома дослідниками. Метод Кокрейн для оцінки похибки був використаний для рандомізованих контрольованих та когортних досліджень. Дизайн досліджень, схожість лікування та контрольних груп були проаналізовані для оцінки ризику похибки у наступних характеристиках: акушерський анамнез, гестаційний вік при встановленні діагнозу, ступінь дилатації при діагностиці, субклінічні прояви інфекції, використання антибіотиків та токолізу.
Якщо дослідження демонструвало значну статистичну різницю у паритеті, історії передчасних пологів або втрат ІІ триместру – вважалося, що ймовірність похибки була значною. Різниця гестаційного віку в 1 тиждень або у 1 см для дилатації на момент встановлення діагнозу між групами серкляжу та контролю передбачала значний ризик похибки. Якщо дослідження вказувало на маркери запалення або історію передчасних пологів – значна різниця підвищувала похибку. Коли токоліз або призначення антибіотиків розпочиналися одночасно в обох групах – похибка вважалася низькою. Коли початок був різним – була продемонстрована статистично достовірна різниця.
Результати
На підставі аналізу 6314 цитувань та абстрактів були відібрані когортні та рандомізовані дослідження, що порівнюють накладання серкляжу з очікувальним менеджментом у жінок з цервікальною дилатацією при вагітності 14–27 тижнів. 17 з них, на перший погляд, відповідали критеріям включення, проте надалі 7 досліджень були виключені з аналізу через методологічні помилки та складнощі.
Таким чином були відібрані 10 досліджень: одне рандомізоване, два проспективних когортних та сім ретроспективних когортних. З 757 жінок в 485 (64%)був накладений серкляж, у 272 (64%) менеджмент був очікувальний. Описання хірургічної процедури та навколоопераційного періоду наведені в табл. 1.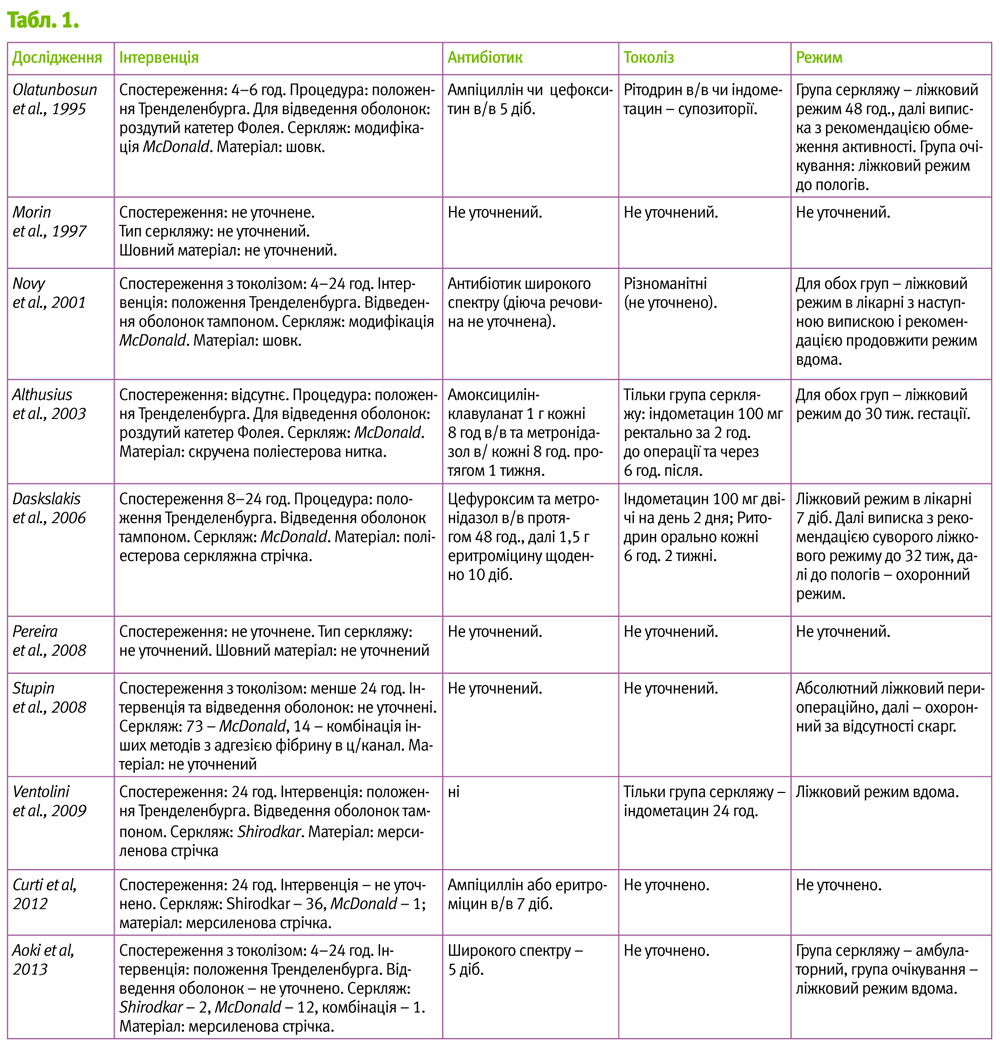
У рандомізованому дослідженні виявлена низька похибка відбору.
Всі пацієнтки отримували рутинно периопераційно індометацин, проте у групі «ліжкового режиму» – ні. Пацієнтки обох груп отримували 1 г амоксициліна клавуланату внутрішньовенно кожні 6 год. та 500 мг метронідазолу в/в кожні 8 год. Ймовірність похибки у дослідженні підвищується через призначення індометацину.
Групи серкляжу та очікування були однакові по відношенню до віку вагітної, паритету, анамнезу попередніх передчасних пологів. В дослідженні Pereira et al. відмічено значно більшу частоту попередніх втрат вагітності ІІ триместру в групі серкляжу.
Діагностика цервікальної дилатації у групі серкляжу була в середньому на 1 тиждень раніше, ніж у групі очікування, проте не було достовірної різниці між ступенем дилатації в обох групах. Маркери інфекції та запалення визначалися в 3 групах, більша кількість лейкоцитів була в групі очікування (9,76/мл проти 14,73/мл, середня різниця 4,97, 95% СІ 2,25–7,69). Плодові оболонки були видимі або пролабували в усіх пацієнток в усіх дослідженнях (за винятком дослідження Pereira, де у 56% пацієнток групи серкляжу міхур не візуалізувався). Три дослідження порівнювали ступінь пролапсу, не виявлено суттєвої різниці. Двійні виключені в 6 дослідженнях, включені – в 2 та в 2 – не ідентифіковані.
Використання амніоцентезу, токоліза та антибіотикотерапії були подібними в обох групах. Після виключення з аналізу двох досліджень, в яких використовувався амніоцентез, первинні наслідки та виживання новонароджених все ж були значно більшими в групі серкляжу (69,7% проти 50,3, 95% CI 1,06–2,05). Техніка шва: два дослідження використовували техніку Широдкар, в трьох техніка не визначена. Решта використовували шов по Макдональду або його модифікацію. Накладання серкляжу асоціювалося із значним пролонгуванням вагітності (середнє значення 33,98 діб, 95% СІ 17,88–50,08), а також більшим гестаційним віком на момент пологів (в середньому на 4,62 тижні, 95% СІ 3,89–5,36). Серкляж пов’язаний зі значним зменшенням частоти пологів у 24–28 тижнів (8% у порівнянні з 37% контролю, RR 0,23 95% СІ 0,13–0,41, а також передчасних пологів до 34 тижнів (50 проти 82%, RR 0,55, 95% СІ 0,38–0,80) та більшою вагою новонароджених (середня різниця 1028 г, 95% СІ 714–1341). Частота живонароджень склала 71% у групі серкляжу проти 43% в контрольній групі (RR 1,65 95% СІ 1,19–2,28).
Інтраопераційний розрив оболонок трапився в 4,1% випадків, розрив шийки матки – в 7,9%, проте подібні дані для групи очікування не наведені. Частота випадків відшарування плаценти, передчасного (післяопераційного) розриву оболонок та хоріонамніонітів викладена непослідовно та варіабельно.
Дискусія
Статті, включені в даний мета-аналіз, лімітовані у кількості, проте варіабельні у якості та дизайні досліджень, незважаючи на те, що була виявлена різниця у наслідках вагітності…
Аналіз підтвердив попередні висновки про те, що серкляж, накладений на підставі фізикального дослідження, асоціюється зі статистично достовірним збільшенням рівня неонатального виживання та значною пролонгацією вагітності, якщо порівнювати з неоперативною інтервенцією. Серкляж призводить до значного покращення усіх вторинних наслідків.
Раніше вважалося, що серкляж, накладений на підставі фізикального обстеження, може більш-менш тривало пролонгувати вагітність лише по відношенню до екстремально передчасних пологів. Наведений мета-аналіз продемонстрував, що очікувальна тактика більш ніж чотирикратно підвищує ризик пологів між 24 та 28 тижнями. У дослідженні Pereira et al. запропоновано бімодальний розподіл гестаційного віку на момент пологів у групі серкляжу. Цей розподіл припускає існування різних підгруп з більш та менш сприятливими наслідками вагітності, що може бути викликано наявністю, наприклад, субклінічної інфекції. Найбільшою лімітацією аналізу була якість досліджень – субоптимальний дизайн може збільшувати похибки та впливати на висновки.
Потенціал для похибки відбору існує та пов’язаний з відсутністю рандомізації розподілу. Ані серкляж, ані очікувальний менеджмент не мають очевидно збільшеного ризику несприятливих наслідків. Цервікальна дилатація, пролабування плодового міхура, акушерський анамнез, ознаки інфекції є факторами, що корелюють із наслідками серкляжу. Значна різниця була виявлена в значенні гестаційного віку на час виявлення дилатації та, відповідно, накладенні серкляжу (22,8 тиж. для групи очікування та 21,7 тиж. для групи серкляжу). Накладання серкляжу у більш ранні терміни асоціюється із покращенням наслідків вагітності. Існує також можливість похибки внаслідок лікування, а також акушерських та неонатальних інтервенцій (фетальний моніторинг, оперативні пологи, реанімація новонароджених). Неонатальні наслідки були викладені несистемно, відсутні дані про віддалені наслідки у дитинстві.
Незважаючи на певну лімітацію, послідовність знахідок у включених в аналіз дослідженнях, субаналізах та опублікованих серіях випадків визнана задовільною. Для отримання найдостовірніших висновків необхідні проспективні РКД для попереднього визначення найкращих кандидатів для накладання серкляжу. До надання подальших доказів, серкляж, накладений на підставі фізикального обстеження, слід вважати ефективним у правильно відібраній групі пацієнтів.
Детальніше
ВЕДЕННЯ РОЗРИВІВ ПРОМЕЖИНИ ІІІ ТА ІV СТУПЕНЯ (ЧАСТИНА 2)
 Шановні колеги! Вашій увазі надаються рекомендації Королівського коледжу акушерів та гінекологів з діагностики, ведення та лікування розривів промежини третього і четвертого ступеня (акушерські травми анального сфінктера, далі АТАС). Належним чином підготовлені акушери-гінекологи, більш ймовірно, можуть забезпечити оптимальне лікування травм анального сфінктера на високому рівні та сприяти скороченню масштабів захворюваності
Шановні колеги! Вашій увазі надаються рекомендації Королівського коледжу акушерів та гінекологів з діагностики, ведення та лікування розривів промежини третього і четвертого ступеня (акушерські травми анального сфінктера, далі АТАС). Належним чином підготовлені акушери-гінекологи, більш ймовірно, можуть забезпечити оптимальне лікування травм анального сфінктера на високому рівні та сприяти скороченню масштабів захворюваності
- Вибір шовних матеріалів
6.1 Які шовні матеріали повинні бути використані для хірургічного лікування розривів зовнішнього анального сфінктера
Для ушивання аноректальної слизової оболонки повинен використовуватись шовний матеріал 3-0 на основі поліглактину, тому що він призводить до меншого подразнення і дискомфорту, ніж матеріал на основі полідиоксанону (ПДС). (D) При ушиванні м'язів ЗАС і/або ВАС, з еквівалентними результатами використовуються або монофіламентний шовний матеріал, такий як ПДС 3-0, або сучасні плетені матеріали, такі як поліглактин 2-0. (B)
Детальніше
ПЕРЕЛИВАННЯ КРОВІ В АКУШЕРСЬКІЙ ПРАКТИЦІ (ЧАСТИНА 2)
 Шановні колеги! Вашій увазі надаються клінічні рекомендації Королівського коледжу акушерів та гінекологів щодо належного використання продуктів крові в акушерській практиці та обговорюються стратегії підвищення рівня гемоглобіну під час пологів, а також зведення до мінімуму втрат крові
Шановні колеги! Вашій увазі надаються клінічні рекомендації Королівського коледжу акушерів та гінекологів щодо належного використання продуктів крові в акушерській практиці та обговорюються стратегії підвищення рівня гемоглобіну під час пологів, а також зведення до мінімуму втрат крові
- Ведення акушерських кровотеч з використанням компонентів крові
6.1 Компоненти крові, які можуть бути використані при акушерській кровотечі.
6.1.1 Використання еритроцитарної маси.
Детальніше