ИСКУССТВО ДЕЛИТЬСЯ ОПЫТОМ
Мы уверены на все 200%, что вы сделаете правильный выбор, посетив мастер-класс по невынашиванию беременности. Чтобы стать экспертом в этом вопросе, надо посвятить этому многие годы упорного труда. Ксения Хажиленко и Светлана Шиянова имеют огромный практический опыт и готовы поделиться секретами успеха со своими коллегами. Знакомьтесь: один из наших спикеров – Ксения Хажиленко
Тема невынашивания для Вас была осознанным выбором?
— Конечно. Этим вопросом я активно заинтересовалась более 10 лет назад, с тех пор веду специализированный прием.
Для того, чтобы досконально разбираться в проблеме, мне, помимо основной специальности, пришлось углубиться (специализироваться) в генетику, ультразвуковую диагностику, овладеть гистероскопией, изучить иммунологию репродукции и гемостазиологию.
Мне повезло, – я работаю в клинике, стимулирующей саморазвитие и профессиональный рост.
Невынашивание – задача со многими неизвестными, Вы нашли ее решение?
— Универсального решения нет. Каждый раз перед тобой уникальная пара, к которой ты подбираешь ключик, используя знания, опыт и логику клинического мышления. И еще – только глупец считает, что он знает (нашел) все.
Как Вы приобретали свой клинический, преподавательский опыт?
— Клинический опыт приобретается методом проб и ошибок. Особенность моей специальности такова, что цена ошибки очень высока, поэтому все время пытаюсь снизить ее вероятность, поглощая и анализируя очень большое количество информации.
При этом я не сижу на сундуке приобретенных знаний, а с удовольствием делюсь ими с тем, кому это надо.
Кого Вы пригласите на мастер-класс? И какие секреты раскроете?
— Очень хочу видеть врачей, которые болеют за пациентов, ибо без искреннего желания помочь таким парам ничего не получится. Секреты? Если я раскрою их сейчас, то это уже не секреты. А если серьезно: секреты в нашем деле – это чей-то конденсированный опыт. Обмениваясь им, мы становимся богаче. Обещаю не жадничать.
Детальніше
ГІПЕРТЕНЗИВНІ РОЗЛАДИ ПІД ЧАС ВАГІТНОСТІ (Частина 2)
Даний документ «Гіпертензивні розлади під час вагітності» було розроблено Цільовою групою з вивчення гіпертензивних розладів під час вагітності: James M. Roberts, MD, Chair; Phyllis A. August, MD, MPH; George Bakris, MD; John R. Barton, MD; Ira M. Bernstein, MD; Maurice Druzin, MD; Robert R. Gaiser, MD; Joey P Granger, PhD; Arun Jeyabalan, MD, MS; Donna D. Johnson, MD; S. Ananth Karumanchi, MD; Marshall Lindheimer, MD; Michelle Y. Owens, MD, MS; George R. Saade, MD; Baha M. Sibai, MD; Catherine Y. Spong, MD; Eleni Tsigas; і колектив Американського коледжу акушерів і гінекологів: Gerald F. Joseph, MD; Nancy O'Reilly, MHS; Alyssa Politzer; Sarah Son, MPH та Karina Ngaiza. Copyright © Американський коледж акушерів і гінекологів.
Доповідь Цільової групи Американського коледжу акушерів і гінекологів*
Шановні колеги! Пропонуємо вам практичне керівництво, яке було підготовлене Комітетом з акушерської практики і затверджене Виконавчим комітетом і Радою Товариства акушерів-гінекологів Канади. Ця практична настанова була затверджена у вересні 2013 року на заміну настанові, опублікованій у серпні 2001 року
(Початок у № 5 (53) 2014)
Рекомендації цільової групи
- пропонується ретельний моніторинг жінок з гестаційною гіпертензією або прееклампсією без обтяжливих факторів, з наступною оцінкою симптомів матері, рухів плода (самостійно жінкою, щодня), серійних вимірювань АТ (два рази на тиждень), оцінки кількості тромбоцитів, рівня печінкових ферментів (протягом тижня).
Якість доказів: Середня
Сила рекомендацій: Кваліфіковані
- Для жінок з гестаційною гіпертензією пропонується моніторинг АТ, принаймні один раз на тиждень, з оцінкою протеїнурії амбулаторно і додатковим щотижневим вимірюванням АТ у домашніх умовах або амбулаторно.
Якість доказів: Середня
Сила рекомендацій: Кваліфіковані
- Для жінок з легкою формою гестаційної гіпертензії або прееклампсією при постійному систолічному АТ менше 160 мм рт. ст. і діастолічному АТ 110 мм рт. ст., використання антигіпертензивних препаратів не обов'язкове.
Якість доказів: Середня
Сила рекомендацій: Кваліфіковані
- Для жінок з гестаційною гіпертензією або прееклампсією без обтяжливих факторів суворий ліжковий режим не є обов'язковим .1, 2
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Цільова група визнала, що для окремих жінок можуть бути показані різні рівні спокою, у домашніх умовах або лікарні. Попередні рекомендації не поширювалися на поради стосовно загальної фізичної активності і ручної роботи або роботи в офісі.
- Жінки можуть бути госпіталізовані з іншою метою, ніж дотримання ліжкового режиму, наприклад, для спостереження за станом матері і плода. Втім, цільова група вирішила, що госпіталізація для спостереження за станом матері та плода вимагає значних ресурсів та необхідні подальші дослідження для вивчення її доцільності з формулюванням відповідних рекомендацій.
- Для жінок з прееклампсією без обтяжливих факторів пропонується використання УЗД для оцінки розвитку плода і максимально ранньої діагностики порушень його стану.
Якість доказів: Середня
Сила рекомендацій: Кваліфіковані
- Якщо докази затримки росту плода виявлено у жінок з прееклампсією, рекомендується проведення оцінки стану фетоплацентарного комплексу, яка включає доплерометрію кровоплину у артерії пуповини у якості доповнення до фетометрії.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Для жінок з легкою формою гестаційної гіпертензії або прееклампсією без обтяжливих факторів і без показань до розродження у терміні менше 37 тижнів вагітності пропонується вичікувальна тактика з моніторингом стану матері і плода.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
Усі вищеперераховані рекомендації відповідають положенням НКП.
- Для жінок з легкою формою гестаційної гіпертензії або прееклампсією без обтяжливих факторів у терміні 37 тижнів вагітності пропонується розродження, а не продовження спостереження.
Положення НКЛ у разі прееклампсії легкого ступненя надають перевагу вичікувальній тактиці до настання пологової діяльності. Спонтанний початок пологів є пріорітетним у таких вагітних.
Якість доказів: Середня
Сила рекомендацій: Кваліфіковані
- Для жінок з прееклампсією з систолічним АТ менше 160 мм рт. ст. і діастолічним АТ менше 110 мм рт. ст. і без симптомів з боку матері не показане рутинне призначення сульфату магнію для профілактики еклампсії.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
НКЛ передбачає початок лікування прееклампсії з підвищенням значення діастолічного АТ до 100 мм рт. ст., що відповідає прееклампсії середньої тяжкості.
- Для жінок з тяжкою прееклампсією у терміні вагітності після 34 тижнів, а також у випадках нестабільного стану матері або плода, незалежно від терміну вагітності, рекомендується якнайшвидше розродження після стабілізації.
У НКЛ дану рекомендацію сформульовано як визначення тяжкої прееклампсії показанням до негайного розродження.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Для жінок з тяжкою прееклампсією у терміні вагітності меншому, ніж 34 тижні при стабільному стані матері та плода, рекомендується продовження вагітності лише в умовах стаціонару, який достатньо забезпечений ресурсами для інтенсивної терапії матерів та новонароджених.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Для жінок з тяжкою прееклампсією при вичікувальній тактиці ведення вагітності у терміні 34 тижні або менше, рекомендується призначення кортикостероїдів для прискорення дозрівання легенів плода.
Якість доказів: Висока
Сила рекомендацій: Ефективні
- Для жінок з прееклампсією і тяжкою гіпертензією під час вагітності (стійкий систолічний АТ не менше 160 мм рт. ст. або діастолічний не менше 110 мм рт. ст.), рекомендується застосування антигіпертензивної терапії.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Протеїнурія та її зростання не є вирішальним чиником при прийнятті рішення про дострокове розродження.
Якість доказів: Середня
Сила рекомендацій: Ефективні
Як вже зазначено вище, зростання протеїнурії до значень, що відповідають прееклампсії більш тяжкого ступеня, є критерієм встановлення відповідного діагнозу, за умови появи ознак тяжкої прееклампсії постає питання про розродження.
- Для жінок з тяжкою прееклампсією і життєздатним плодом рекомендується розродження після стабілізації стану матері. Вичікувальна тактика не рекомендується.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- У випадках тяжкої прееклампсії вагітним у стабільному стані з життєздатним плодом з гестаційним терміном менше 34 тижні та одним із нижчевказаних чинників рекомендується пролонгування вагітності на 48 годин з одночасним проведенням кортикостероїдної профілактики синдрому дихальних розладів.
- передчасний розрив плодових оболонок;
- початок пологової діяльності – латентна фаза першого періоду пологів;
- зниження рівня тромбоцитів (менше 100 000/мкл);
- стабільно аномальні концентрації ферментів печінки (які в два і більше разів перевищують верхню межу нормальних значень);
- затримка внутрішньоутробного росту плода (менше п'ятого процентиля);
- тяжкий ступінь маловоддя (індекс амніотичної рідини менше 5 см);
- реверсний кінцевий діастолічний кровоплин під час доплерівських досліджень пупкової артерії;
- вперше виявлена дисфункція нирок або збільшення ступеню ниркової дисфункції.
Більшість із перелічених чинників є показанням до негайного розродження без проведення курсу стероїдної терапії, як то реверсний діастолічний кровоплин, визначений за допомогою доплерометрії, латентна фаза першого періоду пологів на тлі прееклампсії, дисфункція печінки та нирок, критичне зниження рівня тромбоцитів, згідно із положеннями НКП.
Якість доказів: Середня
Сила рекомендацій: Кваліфіковані
- У терміні вагітності менше 34 тижнів за життєздатного плода та прееклампсії тяжкого ступеня розродження проводять негайно після стабілізації стану при наявності наступних ускладнень:
- неконтрольована тяжка гіпертензія;
- еклампсія;
- набряк легенів;
- відшарування плаценти;
- ДВЗ-синдром;
- відсутні ознаки покращення стану плода;
- загибель плода під час пологів.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Кесарський розтин не є оптимальним методом розродження для вагітних із тяжкою прееклампсією. При виборі способу розродження варто враховувати гестаційний вік плода, його передлежання, статус шийки матки і стан матері і плода.
Якість доказів: Середня
Сила рекомендацій: Кваліфіковані
У НКП дані рекомендації надано більш детально – а саме: за наявності прееклампсії середнього ступеня та зрілих пологових шляхів проводять амніотомію з наступним пологозбудженням, за незрілих – підготовку їх місцевими препаратами простагландинів, відсутність ефекту від останньої є показанням до КР. За тяжкої прееклампсії та зрілих пологових шляхів рекомендована амнітомія з наступним пологозбудженням, за незрілих – КР.
- Жінкам з еклампсією рекомендується парентеральне призначення сульфату магнію.
Якість доказів: Висока
Сила рекомендацій: Ефективні
- Жінкам з тяжкою прееклампсією рекомендується інтра- та постнатальне призначення сульфату магнію для запобігання розвитку еклампсії.
Якість доказів: Висока
Сила рекомендацій: Ефективні
- Для жінок з прееклампсією, яким проводиться кесарський розтин, рекомендується безперервне інтраопераційне парентеральне введення сульфату магнію для запобігання розвитку еклампсії.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Для жінок з HELLP-синдромом, по досягненню плодом гестаційного віку його життєздатності, рекомендується здійснення розродження відразу після первинної стабілізації стану матері.
Якість доказів: Висока
Сила рекомендацій: Ефективні
- Для жінок з HELLP-синдромом у терміні вагітності 34 тижнів та більше, рекомендується здійснення розродження відразу після первинної стабілізації стану матері.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Для жінок з HELLP-синдромом, починаючи від гестаційного віку життєздатності плода, до повних 34 тижнів, передбачається розродження з затримкою протягом 24–48 годин, за умови стабільного стану матері та плоду, щоб завершити курс кортикостероїдів3.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
У рандомізованих контрольованих дослідженнях для спроби поліпшення стану матері та плода використовувались кортикостероїди. У цих дослідженнях не було одержано доказів поліпшення загальних результатів для матері і плода (хоча це було запропоновано в обсерваційних дослідженнях). Рандомізовані дослідження надали докази підвищення кількості тромбоцитів під час лікування кортикостероїдами. Якщо у певних клінічних умовах необхідним є підвищення кількості тромбоцитів, призначення кортикостероїдів може бути виправданим.
- Для жінок з прееклампсією, яким необхідна аналгезія у пологах для проведення кесарського розтину, і за клінічної ситуації, що дозволяє мати достатньо часу для підготовки анестезії, рекомендується застосування нейроаксіальної (або спінальної чи епідуральної) анестезії.
Якість доказів: Середня
Сила рекомендацій: Ефективні
У НКП відсутній розділ, присвячений веденню HELLР-синдрому.
- Використання інвазивного моніторингу гемодинаміки не покращує надання медичної допомоги вагітним із тяжкою прееклампсією
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Для жінок з діагностованою гестаційною гіпертензією, прееклампсією або поєднаною прееклампсією передбачається, що лікарський контроль АТ чи інші елементи амбулаторного спостереження слід виконати не пізніше 72 годин після пологів і повторити протягом 7–10 днів після пологів або раніше при появі відповідних симптомів.
Якість доказів: Середня
Сила рекомендацій: Кваліфіковані
- Інструкції, що їх надають при виписці із стаціонару всім жінкам, а не лише тим, що перенесли прееклампсію, повинні містити інформацію про ознаки і симптоми прееклампсії, а також про важливість звертання до медичних працівників при появі таких симптомів.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Жінкам, які звертаються у післяпологовому періоді з приводу вперше виявленої гіпертензії, що асоціюється з головними болями або погіршенням зору, або прееклампсії з тяжкою артеріальною гіпертензією, показаним є парентеральне введення сульфату магнію.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Породілям, у яких після пологів зберігається артеріальна гіпертензія зі значенням систолічного АТ 150–159 мм рт. ст. та діастолічного АТ 100–119 мм рт. ст., виміряного двічі з інтервалом 4–6 годин, рекомендовано антигіпертензивну терапію. При значеннях систолічного АТ 160 мм рт. ст. або діастолічного АТ 110 мм рт. ст. і вище, лікування слід розпочати на підставі одного вимірювання протягом 1 години.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
Ведення жінок з попередньо діагностованою прееклампсією
Жінки, у яких попередня вагітність ускладнилась прееклампсією, повинні отримати консультації та оцінки перед їх наступною вагітністю. Таке консультування варто проводити при першому післяпологовому зверненні до лікаря, але вкрай важливим є його проведення в рамках планування наступної вагітності.
Під час преконцепційного візиту слід переглянути анамнестичні дані попередньої вагітності і обговорити прогноз для майбутньої. Жінок слід заохочувати до відповідних змін способу життя, що впливають на модифіковані чинники ризику, як то зменшення ваги і підвищення фізичної активності.
За необхідності, слід оцінювати поточний стан здоров'я, у тому числі із залученням лабораторних методів. Обсяг обстеження слід розширити за наявності хронічної гіпертензії або цукрового діабету, а також ретельно обговорити можливий вплив таких станів на перебіг вагітності та розвиток плода. Перед настанням вагітності необхідно переглянути перелік ліків, що їх приймає пацієнтка, та модифікувати способи введення. Рекомендована фолієва кислота. Якщо при попередній вагітності прееклампсія стала причиною передчасного розродження або дві або більше із попередніх вагітностей супроводжувались розвитком прееклампсії, рекомендованим на преконцепційному етапі є прийом низьких доз аспірину. З настанням наступної вагітності у ранньому терміні слід виконати УЗД для визначення її терміну. Жінкам, що мають прееклампсію в анамнезі, мають частіше відвідувати лікаря. Вкрай важливим є доступне інформування вагітної про ознаки і симптоми прееклампсії і про те, коли і як звернутись до свого лікаря.
Рекомендації цільової групи
- Для жінок з прееклампсією під час попередньої вагітності пропонується преконцепційне консультування і оцінка.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
Хронічна гіпертензія у поєднанні з прееклампсією
Хронічна гіпертензія (яка передувала вагітності), має особливу актуальність, у першу чергу, з огляду на необхідність диференціювання її з прееклампсією. При першому виявленні підвищеного АТ необхідно виключити «гіпертонію білого халата» та ті захворювання, що спричинюють вторинну гіпертензію. Для визначення можливості виношування вагітності та подальшої тактики лікування потрібно вивчити наявність та ступінь ураження органів-мішеней, при виборі лікарських засобів враховувати доказові дані про несприятливий вплив на плід надмірного зниження АТ.
Вкрай серйозною проблемою є вчасна діагностика прееклампсії, накладеної на хронічну гіпертензію – стан, який зазвичай пов'язаний з несприятливими результатами для матері та плоду. Існують рекомендації щодо спостереженя за вагітними, у яких прееклампсія не має тяжкого перебігу (тільки з гіпертензією і протеїнурією), та щодо медичних втручань за вагітності, що ускладнилась проявами тяжкої прееклампсії.
Рекомендації цільової групи
- Для жінок з ознаками, що вказують на вторинну гіпертензію, пропонується звернення до лікаря, який має досвід у лікуванні гіпертензії.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Для вагітних жінок з хронічною гіпертензією пропонується використання домашнього моніторингу АТ.
Якість доказів: Середня
Сила рекомендацій: Кваліфіковані
- Для жінок з підозрою на «синдром білого халата» пропонується застосування амбулаторного моніторингу АТ для підтвердження діагнозу до початку антигіпертензивної терапії.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Не рекомендується зменшення ваги і застосування дієти з дуже низьким вмістом натрію (менше 100 мг-Екв/г) для лікування хронічної гіпертензії під час вагітності.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Для жінок з хронічною гіпертензією, які продовжують працювати та мають стабільні значення АТ, під час вагітності рекомендуються помірні фізичні навантаження.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Для вагітних жінок з персистуючою хронічною гіпертензією з систолічним АТ 160 мм рт. ст. або вище чи діастолічним АТ 105 мм рт. ст. або вище, рекомендується антигіпертензивна терапія.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Для вагітних жінок з хронічною гіпертензією та систолічним АТ менше 160 мм рт. ст. або діастолічним АТ менше 105 мм рт. ст. і без ознак пошкодження органів-мішеней, застосування фармакологічної антигіпертензивної терапії не передбачене.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Для вагітних жінок з хронічною гіпертензією, які отримують антигіпертензивні препарати, передбачається, що рівні АТ повинні підтримуватись між значеннями 120 мм рт. ст. систолічного і 80 мм рт. ст. діастолічного тиску, а також 160 мм рт. ст. систолічного і 105 мм рт. ст. діастолічного тиску, відповідно.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Для початкового лікування вагітних жінок з хронічною гіпертензією, яким потрібне медикаментозне лікування, серед всіх інших антигіпертензивних препаратів рекомендується застосування лабіталолу, ніфедипіну або метилдопи.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Для жінок з неускладненою хронічною гіпертензією під час вагітності не рекомендується використання інгібіторів ангіотензин-перетворюючого ферменту, блокаторів рецепторів ангіотензину, інгібіторів реніну і антагоністів мінералокортикоїдних рецепторів.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Для жінок репродуктивного віку з хронічною гіпертензією не рекомендується використання інгібіторів ангіотензин-перетворюючого ферменту, блокаторів рецепторів ангіотензину, інгібіторів реніну і антагоністів мінералокортикоїдних рецепторів за відсутності вагомих причин, таких як наявність ниркової недостатності з протеїнурією.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Для жінок з хронічною гіпертензією, які мають високий ризик несприятливих наслідків вагітності (з раннім початком прееклампсії у анамнезі та передчасними пологами у терміні менше 34 тижнів вагітності, або прееклампсією під час двох або більш попередніх вагітностей), пропонується призначення щоденного прийому низьких доз (60–80 мг) аспірину, починаючи з кінця першого триместру4.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Мета-аналіз популяції більш, ніж 30000 жінок у рандомізованих дослідженнях використання аспірину для запобігання прееклампсії вказує на невисоку ефективність цього заходу стосовно зниження частоти та тяжкості прееклампсії. Водночас, результат мета-аналізу не дозволяє виключити можливий негативний вплив на плід. Зважаючи на питання материнської безпеки, є виправданим обговорення застосування аспірину з урахуванням індивідуального ризику.
- Для жінок з хронічною гіпертензією пропонується використання УЗ-дослідження для скринінгу затримки внутрішньоутробного розвитку плода.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Якщо докази затримки росту плода діагностуються у жінок з хронічною гіпертензією, рекомендується проведення оцінки фетоплацентарного комплексу, яка включає доплерометрію кровоплину у артерії пуповини як доповнення до антенатальної діагностики.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Для жінок з хронічною гіпертензією і без додаткових ускладнень з боку матері та плоду, не рекомендується розродження у термін до 38 тижнів вагітності.
Якість доказів: Помірна
Сила рекомендацій: Ефективні
- Для жінок з прееклампсією, за вичікувальної тактики ведення вагітності у термін менше 34 тижнів, рекомендується введення кортикостероїдів для прискорення дозрівання легенів плода.
Якість доказів: Висока
Сила рекомендацій: Ефективні
- Для жінок з хронічною гіпертензією та прееклампсією з обтяжливими факторами, рекомендується інтра- та постнатальне призначення сульфату магнію для запобігання розвитку еклампсії.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Для жінок з поєднаною прееклампсією без обтяжливих факторів і стабільному стані матері та плоду, рекомендується вичікувальна тактика до 37 тижнів вагітності.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
- Розродження відразу після стабілізації стану матері рекомендується незалежно від гестаційного віку або закінчення кортикостероїдної терапії для жінок з прееклампсією, ускладненою одним з таких факторів:
- неконтрольована тяжка гіпертензія;
- еклампсія;
- набряк легенів;
- відшарування плаценти;
- синдром дисемінованого внутрішньосудинного згортання;
- відсутні ознаки покращення стану плода.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Для жінок з поєднаною прееклампсією з обтяжливими факторами у терміні вагітності менше 34 тижнів і стабільним станом матері та плоду, рекомендується продовження вагітності лише в умовах достатнього забезпечення ресурсами інтенсивної терапії матерів і новонароджених.
Якість доказів: Середня
Сила рекомендацій: Ефективні
- Для жінок з прееклампсією з обтяжливими факторами не рекомендується вичікувальна тактика після 34 тижнів вагітності.
Якість доказів: Середня
Сила рекомендацій: Ефективні
Серцево-судинні захворювання у літньому віці у жінок з прееклампсією в анамнезі
Інформація, накопичена за останні 10 років, свідчить, що жінка, яка зазнала прееклампсії під час вагітності, знаходиться у групі підвищеного ризику розвитку серцево-судинних захворювань у літньому віці. Це збільшення ризику лежить у діапазоні від подвоєння ризику (для всіх випадків), до восьми-дев'ятикратного збільшення для жінок з прееклампсією, які народили до 34 тижнів вагітності.
Американська асоціація кардіологів визнала цей факт і нині рекомендує, щоб анамнез вагітності був включений до оцінки ризику ССЗ у жінок. Врахування того, що у жінки під час вагітності була прееклампсія, може допомогти виявленню жінок, які раніше не належали до групи ранньої оцінки ризику і потенційного втручання.
Однак, невідомо, чи буде цей факт цінним доповненням до попередньої інформації. Якщо так, то чи буде достатньо для сучасних рекомендацій з оцінки факторів ризику для жінок даних анамнезу, оцінки способу життя, тестування на метаболічні порушення і, можливо, запальних захворювань у віці 40 років, щоб забезпечити надання всієї інформації, якщо не буде враховано захворювання на прееклампсію під час вагітності? Може, проведення такої оцінки було б цінним у більш молодому віці жінок, які перенесли прееклампсію під час вагітності? Якщо ризик був визначений раніше, які втручання (крім модифікації способу життя) потенційно будуть корисними і чи буде це мати значення? Чи існують фактори ризику, які можуть бути встановлені саме під час вагітності, крім звичайних факторів ризику? Необхідні подальші дослідження, щоб визначити, як скористатися інформацією, що стосується прееклампсії і розвитку ССЗ у літньому віці. У даний час цільова група обережно рекомендує зміни способу життя (підтримання нормальної ваги, збільшення фізичної активності, відмову від паління) і припускає можливість використання даного чинника в виділенні жінок високого ризику розвитку ССЗ.
Рекомендації цільової групи
- Для жінок з прееклампсією в анамнезі, які народили до 37 тижнів вагітності або які мають рецидиви прееклампсії в анамнезі, пропонується щорічна оцінка АТ, індексу маси тіла, ліпідного та глікемічного профілю5.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
Незважаючи на явні докази зв'язку між прееклампсією і ССЗ у літньому віці, їх значення і відповідний графік оцінки ще не сформовані. Медичні працівники та пацієнти повинні прийняти це рішення на основі їх власного судження щодо цінності додаткової інформації у порівнянні з витратами і незручностями.
Навчання пацієнтів
Навчання пацієнтів і медичних працівників має ключове значення для успішної діагностики і лікування прееклампсії. Медичні працівники повинні інформувати жінок у пренатальному та післяпологовому періоді про ознаки і симптоми прееклампсії та підкреслювати важливість контактів з лікарями. Навчання пацієнтів повинне бути доповнене навчанням щодо використання стратегій успішної передачі цієї інформації жінкам з різним рівнем знань у питаннях охорони здоров'я. Рекомендовані стратегії для полегшення цього процесу включають у себе використання простих зрозумілих слів, достатнього часу для неквапної розмови з ілюстрацією ключових питань графічною інформацією, і з проханням підтримки зворотного зв'язку, щоб пересвічитись, що пацієнтка (або її партнер) розуміють, про що йде мова.
Рекомендації цільової групи
- Передбачається, що медичні працівники передають інформацію про прееклампсію у контексті допологового та післяпологового догляду, використовуючи перевірені у питаннях здоров'я методи комунікації.
Якість доказів: Низька
Сила рекомендацій: Кваліфіковані
Рекомендації щодо науково-експериментальних досягнень
Протягом останніх 10 років відбулись суттєві зрушення у розумінні причин розвитку прееклампсії. За допомогою клінічних досліджень було отримано достатньо даних, щоб проводити терапію. На сьогодні ясно, що прееклампсія є мультисистемним захворюванням, яке чинить вплив на всі органи і системи, і воно має набагато більше проявів, ніж високий артеріальний тиск і ниркова дисфункція. Основною причиною розвитку прееклампсії виступає стан плаценти. Саме після народження плаценти симптоми прееклампсії починають зменшуватись. Крововилив у плаценту виглядає як імунологічно ініційовані зміни функції трофобласта. Зниження інвазії трофобласта призводить до невдалого ремоделювання спіральних артерій, через які відбувається перфузія плаценти. У результаті зниження перфузії і збільшення швидкості кровоплину у міжворсинчатому просторі порушується процес дифузії між материнським та плодовим кровообігами. Зміни функції плаценти призводять до генералізованого ангіоспазму у матері внаслідок можливої дії первинних медіаторів, у тому числі стресу: окисного і ендоплазматичного ретикулума, та запалення, а також вторинних медіаторів, до яких входять модифікатори функцій ендотелію та ангіогенезу. Таке розуміння патофізіології прееклампсії не передбачає існування предикторів або превенторів розвитку прееклампсії, а також шляхів поліпшення прогнозування та ранньої діагностики. Це призвело до необхідності зміни оцінки даної концепції, з підвищенням уваги до того, що, можливо, прееклампсія є не одним захворюванням, а синдром може включати кілька патофізіологічних підгрунть.
Клінічні дослідження показали підходи до терапії, які є ефективними (наприклад, розродження для жінок з гестаційною гіпертензією та прееклампсією без обтяжуючих факторів на 37 тижні вагітності) або неефективними (застосування вітамінів С і Е для попередження прееклампсії). Однак, лише кілька клінічних рекомендацій можуть бути класифіковані як «ефективні», тому що існують величезні прогалини у доказовій базі, на якій базується терапія. Ці прогалини у знаннях формують основу для дослідження рекомендацій щодо проведення терапії у майбутньому.
Висновок
Цільова група надає науково обгрунтовані рекомендації щодо ведення пацієнтів із артеріальною гіпертензією під час вагітності і після пологів. Рекомендації оцінюються як ефективні або кваліфіковані на основі даних про ефективність проти доказів потенційної шкоди. У всіх випадках остаточне рішення приймається лікарем і пацієнтом після розгляду обгрунтування рекомендацій залежно від цінностей і суджень конкретного пацієнта.
Інформацію, що міститься у даному документі, не слід розглядати як зібрання жорстких правил. Керівні принципи носять загальний характер і призначені для їх адаптації до різних ситуацій, з урахуванням потреб і ресурсів конкретного регіону, установи або практичних потреб. Зміни та інновації, які покращують якість догляду за пацієнтами, повинні заохочуватись, а не обмежуватись. Метою цих керівних принципів є забезпечення надійної основи, на якій можуть бути побудовані місцеві норми надання медичної допомоги.
Матеріал підготувала
Олександра Загородня.
Детальніше

ШКОЛА РЕФОРМАТОРІВ

Літня школа «Управління у трансформованій системі охорони здоров’я в Україні» 2014
18–22 червня 2014 року в Карпатах відбулася перша в Україні літня школа для керівників у сфері охорони здоров'я «Управління в трансформованій системі охорони здоров’я в Україні».
Цю навчальну подію спільно ініціювали Школа охорони здоров’я Національного університету «Києво-Могилянська академія» та україно-швейцарська Програма «Здоров’я матері та дитини»
Проект підтримали авторитетні міжнародні організації – Світовий банк, Всесвітня організація охорони здоров’я (ВООЗ), Дитячий Фонд ООН ЮНІСЕФ, Швейцарський інститут охорони здоров’я та тропічної медицини, а фінансове забезпечення надало Швейцарське бюро співробітництва в Україні. Одним з офіційних партнерів виступило Міністерство охорони здоров'я України – учасники отримали залікові бали підвищення кваліфікації, а сертифікати були підписані особисто міністром.
Місія Літньої школи – стимулювати процеси модернізації та реформування системи охорони здоров'я в Україні шляхом створення платформи для навчання та спілкування тих медичних керівників, які готові підтримувати зміни у галузі. За словами Наталії Рябцевої, співорганізаторки проекту, ідея школи у тому, щоби створити в медичній спільноті критичну масу людей, яка була би налаштована на проведення реальних реформ. «Про них зазвичай багато говорять, але на практиці зміни викликають відторгнення, особливо у медичного співтовариства. Тому ми прагнемо поступово, з року в рік, формувати групу ініціативних керівників на всіх рівнях, які би перейнялися ідеєю реформ і стали їх провідниками, кожен на своєму робочому місці», — зазначила пані Рябцева.
Цьогоріч через революційні та військові події в Україні організаторам було складно провести повноцінну кампанію із залучення учасників. Незважаючи на це, всього за три тижні на 20 місць було отримано 43 заявки, з яких Вчена рада та організатори відібрали учасників із 12-ти регіонів України, у тому числі з АР Крим. Більшість учасників представляли державні медичні установи, решта ж – приватні заклади, громадські організації та органи управління у галузі охорони здоров'я.
Викладачів організатори запрошували за принципом поєднання українського та міжнародного досвіду, практичної та експертної діяльності, роботи у медичній галузі та поза нею. Радо погодилися викладати на Літній школі такі експерти як Паоло Беллі (провідний економіст Світового банку), Андрій Гук (фахівець із організації охорони здоров’я України), Віктор Галайда (експерт із фінансування галузі охорони здоров’я), Аксель Хоффманн та Мартін Рааб (експерти Швейцарського інституту охорони здоров’я та тропічної медицини), Катерина Булавінова (медичний експерт ЮНІСЕФ) та інші фахівці.
Програма Літньої школи була побудована за принципом «від загального – до часткового». Спершу розглядалися питання організації систем охорони здоров’я в цілому, реформи та зміни у них. Окремо йшлося про систему охорони здоров’я України. Після цього учасники прослухали низку тем, корисних на рівні управління медичним закладом, – управління людськими ресурсами, управління якістю, інформаційні технології тощо. Для інтеграції усіх знань учасники виконували практичний проект на прикладі реальних організацій. Завдання полягало у тому, щоб запропонувати проект змін для закладу охорони здоров’я, а одна з груп взялася до написання такого проекту стосовно системи охорони здоров’я України.
Однією з найбільш гарячих тем цьогорічної Літньої Школи стали неформальні платежі пацієнтів, тобто та винагорода від пацієнта надавачу медичної допомоги, яка не обліковується у формальних каналах фінансування медичної допомоги. Наявність неформальних платежів в системі охорони здоров’я є відчутною на всіх рівнях надання медичної допомоги (на рівні амбулаторної та стаціонарної допомоги), на рівні системи охорони здоров’я, на рівні закладу, а також в усіх сферах управління: людськими, фінансовими, інформаційними та іншими ресурсами. 
Змальовуючи особливості дискусії про неформальні платежі, неможливо не згадати один з найважливіших акцентів змістовного наповнення Літньої Школи: результат-орієнтована управлінська діяльність. А саме, основою побудови системи охорони здоров’я повинні бути ті результати, яких вона прагне досягти: постановку мети (місії та візії), або окреслення бажаного результату, ефекту, у відповідності до якої плануються та реалізовуються заходи, спрямовані на досягнення таких результатів. Тобто метою має бути не збільшення фінансування чи запровадження соціального медичного страхування, чи ж закупівля надсучасного обладнання, а, скажімо, зниження смертності від неінфекційних захворювань, а особливо від хвороб системи кровообігу та від онкологічних захворювань. І вже згідно з бажаними цілями та принципами потрібно обирати ті системи заходів, які здатні посприяти їх досягненню. Проте, результат-орієнтована діяльність системи та закладів є більш успішною за умов прозорості, надійності управлінської (та медичної) інформації й орієнтації на економічну ефективність. А неформальні платежі як непрозорий, хоч і певною мірою «управлінський» засіб перешкоджає реалізації поставленої надмети, оскільки робить медичну допомогу менш доступною, якісною та економічно неефективною.
Яким чином існування неформальних платежів може перешкоджати досягненню поставлених завдань? Звертаючись до прикладу з організації надання медичної допомоги, варто зауважити, що неформальні платежі пацієнтів здебільшого переважають у спеціалізованій та стаціонарній медичній допомозі. Тоді як зміцнення потужностей первинної ланки медичної допомоги сприяє ефективному використанню ресурсів у системі охорони здоров’я.
Таким чином, система, яка побудована на тіньових платежах, зіштовхується з величезним спротивом надавачів медичної допомоги на перехідному етапі, коли змінюються акценти й надається більша вага первинній медичній допомозі, що супроводжується оптимізацією спеціалізованої та стаціонарної допомоги.
Зміцнення потужностей первинної медико-санітарної допомоги відбувається значно складніше в умовах, коли надавачі медичної допомоги не зацікавлені бути залученими до первинної ланки через недоотримання потенційних прибутків: офіційні доходи в первинній допомозі все одно лишаються суттєво меншими, аніж сукупний дохід, включаючи неформальну частину, в спеціалізованій допомозі.
Існує безліч доказів того, що значне поширення неформальних платежів перешкоджає належному здійсненню:
- управління людськими ресурсами – лікарі не мотивовані комплексною системою, заснованою як на фінансових, так і на інших стимулах, наприклад, можливостями професійного зростання, а їхня професійна поведінка відображає наявність чи відсутність неофіційної оплати з кишені пацієнта;
- управління якістю та ефективністю медичної допомоги – лікарі схильні надавати таку допомогу, яка призводить до більших неформальних доходів, аніж таку, що доведено сприяє кращим клінічним результатам тощо. Замість того, щоб керуватися принципом «Ми робимо не те, що Ви хочете, а те, що Вам потрібно», відбувається зворотня ситуація. Наприклад, основним мотивом для здійснення кесаревого розтину стають не клінічні покази, а побажання породіллі.
Під час дискусії, яка мала місце у Літній Школі, деякі учасники та гості наголошували на тому, що неформальні платежі пацієнтів є невід’ємною частиною функціонування теперішньої системи. Так, дійсно, неформальні платежі пацієнтів виконують дуже важливу для суспільства функцію – допомагають тримати на рівні виживання хронічно недофінансовану медичну допомогу. Заклади та лікарі знаходять у неформальних платежах ту винагороду, яку вони недоотримали від держави, тоді як пацієнти завдяки неформальним платежам мають можливість отримати «кращу» медичну допомогу. Проте немає жодних доказових даних про те, що неформальні платежі справді покращують якість медичної допомоги для пацієнта. Єдине, що гарантують неформальні платежі, – це надання медичної допомоги як такої; однак жодного контролю якості не відбувається. Можновладці так само покладаються на неформальні сплати, що дає їм можливість не приймати непопулярні рішення.
Однак з точки зору системи, а не її окремих елементів, неформальні платежі відіграють вкрай негативну функцію: неефективно використовуються ресурси (людські, фінансові, інформаційні тощо), не відбувається інвестування в систему надання медичної допомоги, втрачається довіра до закладів охорони здоров’я, що негативно позначається на здоров’ї населення.
Окрім того, в українських реаліях немає чіткого розподілу понять «споживач» та «платник» та відповідальності між ними: часто «споживач» послуги змушений сам за неї платити. Це призводить до того, що медична допомога стає менш доступною, а її споживання може призвести до зубожіння пацієнта та його родини.
Беззаперечно, успішність управлінських систем не виключає неформальних відносин, які завжди існують поряд з формальною системою відносин. Однак, коли формальні механізми – в силу їхньої слабкості чи інших причин – підміняються неформальними, які формують хребет системи управління, це може призвести до непередбачуваних негативних наслідків як для системи, так і для здоров’я. За бажання змінити наявний стан речей та запровадити цивілізоване управління галуззю, орієнтоване на досягнення ефективного результату, потрібно працювати не над реалізацією короткострокових цілей (наприклад, пошук джерел фінансування медичної допомоги сьогодні), а над досягненням довгострокових цілей (наприклад, зниження смертності).
Однак слід врахувати, що найбільший виклик на цьому шляху – повернути втрачений формальний хребет… І все ж таки, за умов політичної волі до вирішення цих питань, Україна вже сьогодні готова до запровадження багатьох заходів щодо модернізації галузі, таких як перехід від утримання потужностей до контрактування закладів охорони здоров’я, запровадження механізмів економічної мотивації лікарів, ведення повноцінної масштабної підготовки сімейних лікарів та менеджерів у галузі охорони здоров’я.
Хоча проблема неформальних платежів торкається не лише галузі охорони здоров’я, корені проблеми знаходяться у значно ширшому соціально-політичному контексті: економічному розвитку, верховенстві закону, ефективності уряду, боротьбі з корупцією, цінностями та рівнем освіченості суспільства, мораллю. Але радикальні політичні зміни, які відбулися і продовжують відбуватися в Україні в 2014 році, серед них – формування громадянського суспільства, дають підстави вважати подальше визначення шляху системи охорони здоров’я багатосекторальним. Очевидно, що за короткий час Літньої школи організатори не могли дати керівникам повноцінну освіту з організації охорони здоров’я чи окремих управлінських дисциплін. Однак учасники отримали уявлення про те, що таке організація сучасної цивілізованої системи охорони здоров’я, яким є шлях до цієї системи, і як виглядає управління окремим закладом у ній.
Висока оцінка Літньої школи від учасників, викладачів, партнерів та донорів Школи підтвердила наміри організаторів продовжувати розвивати проект у наступні роки. У 2015 році заплановано розвинути як формат, так і масштаб Літньої школи. Наприклад, навчання окремим темам буде поглиблене завдяки переходу на формат дво-триденних курсів. Розшириться і аудиторія – крім керівників закладів організатори планують навчати державних управлінців. Зважаючи на широкий резонанс та популярність проекту, ще у 2014 році буде відкрито ранню реєстрацію на Літню Школу 2015. Про деталі можна буди дізнатися у журналі «PROМенеджмент в охороні здоров'я», а також на сторінках соціальних мереж facebook.com/read.pro та www.facebook.com/hct.summer.school.
 Есма Аджієва, акушер-гінеколог, координатор з впровадження Програми в АР Крим
Есма Аджієва, акушер-гінеколог, координатор з впровадження Програми в АР Крим
«На мій погляд, код успіху першої в Україні Літньої школи управлінців закладений у самій назві – управління в трансформованій системі охорони здоров'я. Про що це говорить? Про те, що, по-перше, ми розуміємо, що система охорони здоров'я в Україні повинна трансформуватися, вона буде трансформуватися і в ній вже відбуваються істотні зміни. І другий момент – те, що цими змінами потрібно однозначно управляти. І що мені особливо сподобалося у презентації Паоло Беллі, коли він говорив, що результат теж потрібно планувати і коли ми після презентації задавали питання, як нам це успішно зробити командою, він відповів: «Неможливо просто взяти і реалізувати досвід якої-небудь успішної країни в Україні». Тобто це просто, але разом з тим неможливо з тієї причини, що у кожної країни різні демографічні, культурні та економічні складові. І з цього випливає, що у нас попереду дуже багато важкої, але вдячної роботи в плані трансформування системи охорони здоров'я, і що мене дуже радує, так це те, що спілкуючись з колегами протягом цих кількох днів, я розумію, що у нас великий ресурс кваліфікованих, молодих, освічених фахівців, які готові вчитися, змінюватися самі і змінювати систему на краще. І тепер я в це вірю!
Якщо говорити про мої стартові відчуття і досвід командної роботи, то якщо ти знайомий з командою і разом з нею працюєш, це одне, а коли збираються разом люди з різних міст і регіонів, з різним статусом і розумінням ситуації, і треба за дуже короткий проміжок часу видати результат, це досить складно. Але я розумію, що склад учасників взагалі і нашої команди зокрема підібрався настільки гармонійно, що за невеликий проміжок нашої спільної роботи ми дуже швидко стали просуватися вперед, оскільки ми анонсували тематику (а ми взяли для себе досить високу планку «Стратегія розвитку системи охорони здоров'я»), і до нас приєдналися зацікавлені особи, а не працювали просто за принципом віртуального поділу на кілька груп.
 Олег Петренко, перший заступник генерального директора універсальної клініки «Оберіг».
Олег Петренко, перший заступник генерального директора універсальної клініки «Оберіг».
«Нам треба виходити за межі тих повсякденних обов’язків, які ми виконуємо у своїх медичних закладах, для того, щоб побачити і відчути, чим живе реальне середовище. І ця Школа унікальна тим, що сюди збираються люди з різним менеджерським досвідом, з різними поглядами. Це справжній генератор ідей, який урівнює людей за цінностями, і кожен учасник обов’язково стане агентом змін. Приватному сектору тут теж є чому навчитися. Протягом цих днів тут було згенеровано дуже багато нового. У мене, до речі, теж з’явилося декілька ідей, які я планую втілити по приїзді додому, і це дуже надихає».
Детальніше

ЗАНАДТО ПІЗНО МАТИ ДІТЕЙ?
Уроки з природних плідних популяцій

Too Old to Have Children? Lessons From Natural Fertility Populations
Human Reproduction Volume 29(6):
1304-1312, June 2014
www.medscape.com/viewarticle/825760; автори: Marinus J. C. Eijkemans, Frans van Poppel, Dik F. Habbema, Ken R. Smith, Henri Leridon, Egbert R. te Velde.
Переклад Олексія Соловйова
Питання для вивчення
Чи можливо створити вікову криву, що вказуватиме на вік, після якого жінки є застарими біологічно для відтворювання?
Підсумкова відповідь
Ми створили криву, спираючись на розподіл плідних популяцій жінок за їх віком при останніх пологах після природного запліднення, що віддзеркалює вік жінок, після якого вони стають занадто старими мати дітей.
Що є вже відомим
Середній вік при останніх пологах (ВОП) для жінок склав приблизно 40–41 роки у розбіжностях популяцій природних вагітностей. Це дозволяє припустити, що після того настає занепад чарівної універсальної вікозалежної системи плідності. Проте, мало відомо про розподіл ВОП жінок. Тим більше, що у вік сучасного контролю дітонародження неможливо оцінити залежний від віку розподіл ВОП.
Бракує доступної інформації, котра могла б допомогти розібратися тим парам, які «дивляться в очі» затримці з народженням дітей.
Дизайн дослідження, розмір, тривалість
Це дослідження є переглядом точно визначених історичних даних щодо популяцій з природними вагітностями, де одночасно вивчався розподіл віку жінок при останніх пологах.
Відібрані дослідження використовували ретроспективний когортний дизайн, де жінки спостерігалися щодо їх віку впродовж репродуктивного періоду.
Учасники/матеріали, методи
Ми підготували такий аналіз великої кількості даних щодо популяцій із природною плідністю, який може бути виконаним паралельно через усі популяції з використанням загального набору критеріїв відповідності.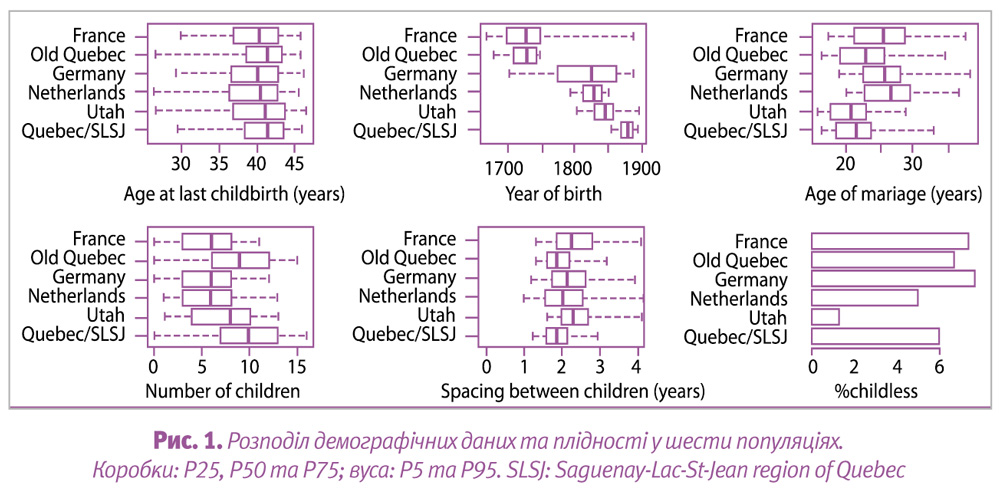
Дані щодо ВОП та розладнаних змінних величин представлені графіком коробок з вусами, які позначають розподіл 5-го, 25-го, 50-го, 75-го та 95-го перцентилів віку при останніх пологах для кожної популяції (рис. 1).
Аналіз включає криві очікування Kaplan–Meier для віку при останніх пологах для кожної популяції (рис. 2). 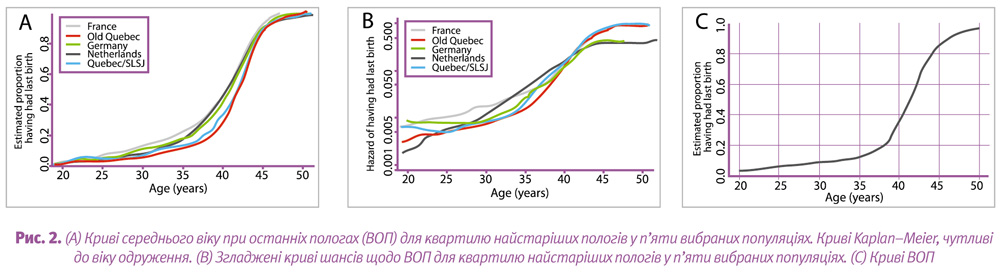
Криву шансів для ВОП одержано шляхом накладання згладжених кривих кожної популяції й одержання найменших шансів для часового періоду принаймні 5 років. Цю криву найменших шансів потому було перетворено у функцію накопичувального розподілу, що представила зведену криву кінця біологічної плідності. Ця крива ґрунтувалася на даних трьох із шести популяцій, які мали найменші шанси завершення плідності.
Основні результати та роль шансу
Ми відібрали шість популяцій природної плідності, що охопили 58 051 жінок, які відповідали визначеним критеріям. Попри те, що ці популяції представляють історично різні періоди часу, розподіл віку при останніх пологах є вражаюче подібним. Крива завершення плідності, що вказує на <3% жінок, які мали свої останні пологи у віці 20 років, означає, що майже 98% були здатні мати принаймні одну дитину після цього віку.
Зведена крива завершення плідності повільно піднімається від 4,5% у 25 років до 7% у 30 років, 12% у 35 років та 20% у віці 38 років. Після цього крива різко підвищується до понад 50% у 41 рік, майже до 90% у віці 45 років і практично досягає 100% у віці 50 років.
Обмеження, причини для застережень
Можна сперечатися, що ці історичні дані плідності не підходять для нашого часу; проте, віково-залежне завершення плідності є подібним для сучасних популяцій і відповідним до проявів, що ми спостерігаємо у жінок, лікованих донорською інсемінацією.
Більше того, ми зазначаємо: щодо репродуктивного віку, малоймовірно, аби такий консервативний біологічний процес з високим ступенем успадкування міг би значно змінитися впродовж століття чи двох.
Ширші наслідки одержаних даних
Ми стверджуємо, що віково-залежну криву ВОП можна використовувати під час консультації пар, які бажали б мати дітей у майбутньому. Наші дані кидають виклик необґрунтованому песимізму щодо можливості природного запліднення у віці понад 35 років.
Детальніше

КОНТРОЛИРУЕМЫЕ РИСКИ И СТРАТЕГИЯ ПРОФИЛАКТИКИ ПРЕЖДЕВРЕМЕННОЙ ПОТЕРИ БЕРЕМЕННОСТИ
Низкая эффективность наших усилий в решении проблемы ранних потерь беременности и преждевременных родов (ПР) явилась предпосылкой для научной гипотезы, рассматривающей невынашивание как инструмент естественного отбора. Это находит подтверждение в случаях прекращения развития беременности на предимплатационном и раннем имплантационном периодах вследствие генетических повреждений (гаметопатии и эмбриопатии). Сохранение такой аномальной беременности нежелательно и нецелесообразно, поэтому медикаментозная поддержка беременности до 8 недель в случаях угрозы ее невынашивания отраслевыми регламентирующими документами не предусматривается. Но даже если принять априори, что причиной выкидышей в ранних сроках являются в 50–70% случаев различные летальные хромосомные абберации, то возникает вопрос, а как поступать с остальными 30% беременных с клиническими симптомами угрозы ее прерывания, причины которого могут быть иными (анатомическими, иммунологическими, инфекционными, гормональными и др.)?
В рамках дискуссии по данной проблеме позвольте напомнить о некоторых хорошо известных фактах. Имплантация зародыша в слизистую оболочку матки происходит на 7-е сутки после оплодотворения и с этого момента, по сути, уже начинается биологический процесс формирования плаценты, поэтому последующие 2–3 недели после имплантации определяют дальнейшую судьбу беременности. Нарушение имплантации оплодотворенной яйцеклетки и процесса формирования тесного взаимодействия трофобласта с децидуальной оболочкой матки, вследствие которых происходит поверхностная, субэпителиальная плацентация с анатомической и функциональной неполноценностью межворсинчатого пространства, является основной причиной нарушения трансплацентарного обмена кислорода и питательных субстратов, плацентарной дисфункции, невынашивания, дистресса и задержки роста плода, преэклампсии и антенатальной гибели плода.
Знание этих рисков сформировало ключевую проблему профилактики невынашивания беременности — прицельное наблюдение и оказание помощи беременным групп риска. Однако, попытки создания рациональных систем отбора беременных в группы риска, а также определения перечня самих критериев риска пока не дали желаемого результата в улучшении статистических показателей здоровья и воспроизводства населения, оставляя актуальным вопрос: «Насколько реально влияет формирование групп риска по невынашиванию на популяционные показатели исходы беременности?».
Вопрос далеко не риторический, поскольку общая теория рисков сегодня находится в центре внимания всех сфер деятельности человека и является одной из самых дерзких реформ в сознании человечества: как можно поставить под контроль будущее. Медицинская наука в этом вопросе не исключение и методология оценки риска и профилактические технологии рассматриваются в качестве глобального фактора улучшения здоровья и качества жизни человека. Обычно риск рассматривают как опасность возникновения неблагоприятных последствий, относительно которых неизвестно: наступят они или нет. В акушерстве этот процесс имеет свою особенность, так как контекст подразумевает оценку двойного риска, как для матери, так и ее будущего ребенка. Именно поэтому сегодня в акушерстве возникла насущная проблема изменения стратегии риск-менеджмента, которая должна заключаться не только в формировании групп риска с ограниченными элементами управления рисками в условиях неопределенности, а и в возможности направленного выбора варианта поведения в ситуации, когда имеется возможность оценить предполагаемый результат. Очевидно, что если присутствует возможность оценить предполагаемый результат, то ситуация не такая уж неопределенная.
Нами предлагается в порядке эксперимента ревизия известных на сегодня принципов отбора факторов риска, в частности, невынашивания беременности, и введение такого понятия как «контролируемые» риски.
Под контролируемыми рисками мы подразумеваем риски, которые:
- часто встречаются в популяции;
- легко опознаются (доступная диагностика);
- в арсенале врача имеется возможность несложного их мониторинга,
- имеются проверенные способы их коррекции.
Оценка рисков с вышеуказанных позиций позволяет не только конкретно объективизировать мероприятия по предупреждению их последствий в каждом индивидуальном случае, но и охватить, прежде всего, тот контингент беременных, которые формируют популяционные показатели. Указанный подход имеет и экономический аспект, поскольку можно говорить и о значительном сокращении расходования материальных и человеческих ресурсов на поиск и профилактику неуправляемых, неконтролируемых рисков на современном этапе.
К примеру, сегодня в число факторов рисков невынашивания зачислены анатомические различные причины (аномалии развития, опухоли, ИЦН), некоторые иммунологические причины, связанные с антифосфолипидным синдромом, тромбофилиями, гистосовместимостью, которые не по всем параметрам соответствуют категории контролируемых рисков. Некоторые из перечисленных факторов риска, например, анатомические, имеют невысокую частоту в популяции (1–3%), что объясняет сложность проведения популяционных исследований, имеют нечеткие скрининговые критерии, профилактика их во время беременности имеет ограниченные возможности или невозможна как таковая, а случаи успешного сохранения беременности мало влияют на популяционные статистические показатели. То же касается некоторых иммунологических причин (2–5%) спонтанной преждевременной потери беременности – АФС, тромбофилии, антигены HLA, гистосовместимость. Исключением из данной группы является иммуноконфликтная беременность по резус-фактору и системе АВО, профилактика которой прописана в национальном протоколе.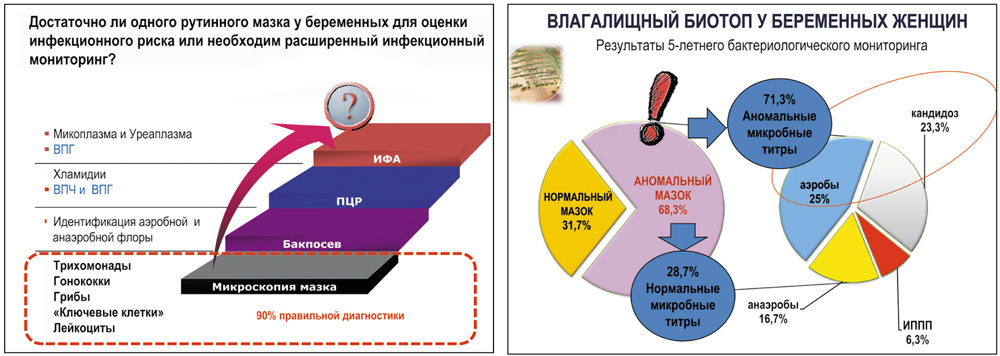
В то же время, воспалительно-инфекционные заболевания наружных женских половых органов широко распространены в популяции беременных и в структуре причин спонтанных потерь беременности, по мнению разных авторов, занимают от 12 до 95%. Доказано, что инфекции, передаваемые половым путем (вагинальный кандидоз, бактериальный вагиноз) являются причинами децидуального эндометрита и хорионамнионита, а значит, непосредственно влияют на процесс имплантации и нарушения развития беременности. Инфекции репродуктивного тракта легко диагностируются, их профилактика и терапия, а также мониторинг результатов этих мероприятий несложны. Поэтому инфекционные факторы риска потери беременности оптимально подходят под понятие контролируемых рисков.
Казалось бы, в вопросе половой инфекции во время беременности нет особых проблем, диагностика и лечение большинства из них прописана соответствующими клиническими протоколами (приказ МОЗ №582). Однако, данный протокол регламентирует деятельность врача в основном у гинекологического контингента пациентов. В отношении же ведения беременных с признаками инфекции репродуктивного тракта возникает сразу несколько принципиальных вопросов.
Как поступать, если у беременной отсутствуют признаки воспаления влагалища, а в мазках из влагалища идентифицированы патогенные или избыточный пул условно-патогенных возбудителей?
- Достаточно ли в качестве скрининга оценки биоценоза влагалища у беременных только бактериоскопического исследования содержимого влагалища (мазка)?
- Как поступать при признаках вагинальной инфекции в сроках до 8 недель беременности, т. е. в период эмбриогенеза и органогенеза?
- Как быть в случае выявления вагинальной инфекции смешанной этиологии, которая у беременных сегодня встречается в 2–3 раза чаще, чем моноинфекция, и лечение которой не прописано клиническими протоколами?
- Нужна ли у беременных профилактическая санация перед родами?
Современные технологии ведения беременности, направленные на снижение акушерской агрессии, сокращение скрининговых и профилактических программ у беременных женщин, большинство этих вопросов просто игнорирует, но ведь от этого они не становятся менее актуальными. Прежде всего, это касается отказа от скрининговых программ по выявлению так называемой группы TORCH-инфекций. Главным аргументов стал тезис, что поскольку мы не можем эффективно лечить эту группу инфекций, нет необходимости и проводить их диагностику.
Можно ли при таком подходе быть уверенным в том, что простое бактериоскопическое исследование мазков ответит на все наши вопросы касательно оценки биоценоза влагалища беременных?
Да, с одной стороны, квалифицированно проведенное бактериоскопическое исследование мазков из влагалища дает 90% диагностики, особенно когда встречаются находки патогенов (гонококк, трихомонада) или «ключевые клетки» как косвенные признаки бактериального вагиноза, но в целом мазок не дает представления о количественном и качественном составе микрофлоры влагалища, а отсутствие повышенного количества лейкоцитов часто свидетельствует не нормоценозе, а о возможном баквагинозе.
Современная наука о микробиоценозе регламентирует его объективную оценку как инструмент профилактики дисбиоза и различных инфекционных осложнений, располагает методами количественной ПЦР-диагностики качественного и количественного состава микробиоты влагалища (Фемофлор-8 и Фемофлор-16), позволяющими выявить степень тяжести дисбиоза от легкого до тяжелого, подходы к лечению и профилактике которых могут быть различными. На наш взгляд, беременная женщина заслуживает такого внимания и нуждается в доступности современных технологий оценки здоровья.
Безусловно, при выраженном дисбиозе лечение должно проводится антибиотиками с антианаэробным эффектом, но следует помнить, что подобная терапия, как и любая антибиотикотерапия, неизбежно приводит с еще большему нарушению биоценоза влагалища и риску развития кандидозной инфекции.
Подобный сценарий исхода терапии предусматривает необходимость использования в схемах лечения бактериального вагиноза и антикандидозной профилактики с использованием антимикотических препаратов.
При легком и умеренном дисбиозе более рационально использовать современные местные пробиотики, которые обладают не только антагонистической активностью к безусловным патогенам и условно-патогенной флоре, но и позволяют быстро восстановить доминантный пул лактобацилл.
Такая градация подходов к терапии бактериального вагиноза дает возможность избежать полипрагмазии, рецидива заболевания и развития кандидоза.
В своей практике в лечении легкого и умеренного дисбиоза влагалища у беременных мы отдаем предпочтение пробиотику Лактожиналь, который содержит штамм лактобактерий (L. casei rhamnosus Lcr 35), выделенных из биотопа влагалища здоровых женщин. Это так называемый «трибиотик», который содержит не только лактобактерии, но и пребиотик (питальную среду), и постбиотик – продукты их жизнедеятельности (молочная кислота) для более быстрого и стойкого восстановления нарушенного баланса микрофлоры.
Эффект Лактожиналя проявляется уже в первые часы его использования и обусловлен быстрым снижением рН благодаря экзогенной донации молочной кислоты, обеспечивающей оптимальные условия для размножения как экзогенным, в составе культуры пробиотика, так и собственным лактобактериям. 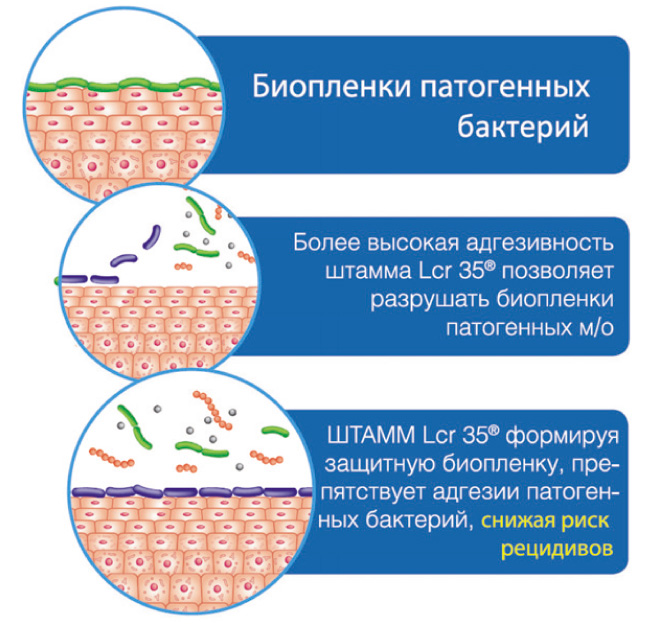
Доказано, что штамм пробиотика Лактожиналь L. casei rhamnosus Lcr 35 обладает высокими адгезивными свойствами и способностью разрушать патогенные микробные биопленки, создавая собственную биопленку из сахаролитических микроорганизмов.
Благодаря этому свойству, пробиотик Лактожиналь способен в течение 6 часов полностью подавить рост главного возбудителя БВ – Gargnerella vaginalis, а в течение 30 часов ингибировать рост Candidа albicans, которая у беременных часто вызывает развитие кандидозного вульвовагинита.
В нашей клинике подтверждена высокая эффективность Лактожиналя в лечении легкого и умеренного бактериального вагиноза у беременных в следующих дозах: 1 капсула 2 раза в день на протяжении 7 дней или 1 капсула 1 раз в день 14 дней.
Следует отметить, что штамм L. casei rhamnosus Lcr 35 в составе пробиотика Лактожиналь обладает природной антибиотикорезистентностью и устойчивостью к противогрибковым препаратам (метронидазол, клиндамицин), что позволяет использовать его параллельно с антибактериальной терапией выраженного дисбиоза и кандидозной инфекции и, таким образом, избежать развития кандидозной суперинфекции и рецидива заболевания благодаря быстрому восстановлению нормального биоценоза после курса терапии.
Не менее распространенным в популяции фактором риска невынашивания беременности, который можно отнести к контролируемым рискам, является дефицит прогестерона, который по данным разных авторов, является причиной выкидышей в 12–30% случаев. Диагностика прогестероновой недостаточности во время беременности не представляет трудности, группы риска женщин, у которых можно предположить ее наличие, подробно изложена в клинических протоколах (приказ МОЗ №624): привычное невынашивание; беременность, наступившая на фоне НЛФ; индуцированная беременность, вылеченное эндокринное бесплодие; беременность, наступившая в результате вспомогательных репродуктивных технологий. 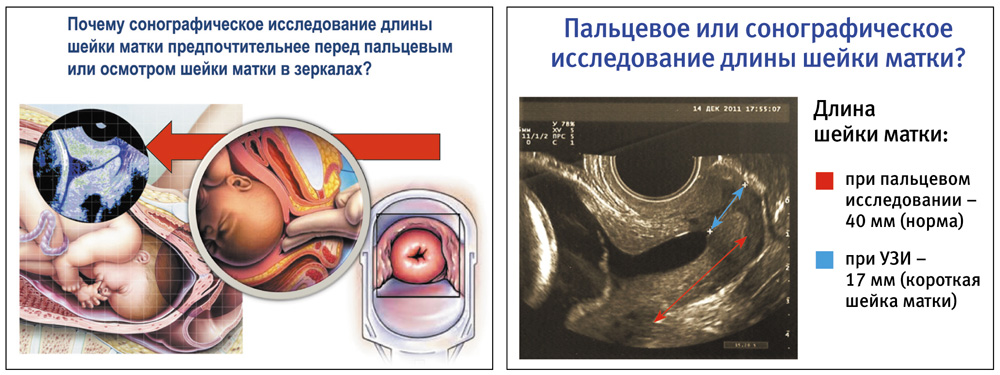
Следует помнить, что до 10 недель беременности источником прогестерона является исключительно желтое тело. При этом его функционирование контролируется эмбриональным ХГЧ, вырабатываемым трофобластом. В более поздние сроки беременности функцию выработки прогестерона берет на себя плацента. Поэтому во время беременности не работают обычные петли обратной связи и регуляция синтеза прогестерона яичниками не находится под контролем гипоталамуса и гипофиза посредством тропных гормонов ФСГ и ЛГ.
В этой связи, при недостаточности прогестерона у беременной донация экзогенного прогестерона является единственным путем его коррекции, а все предостережения относительно угнетения тропных гормонов гипофиза экзогенным прогестероном являются необоснованными.
Интересен также факт, что только биоидентичный прогестерон способен адекватным образом опознаваться клеточной сигнальной системой в организме человека. 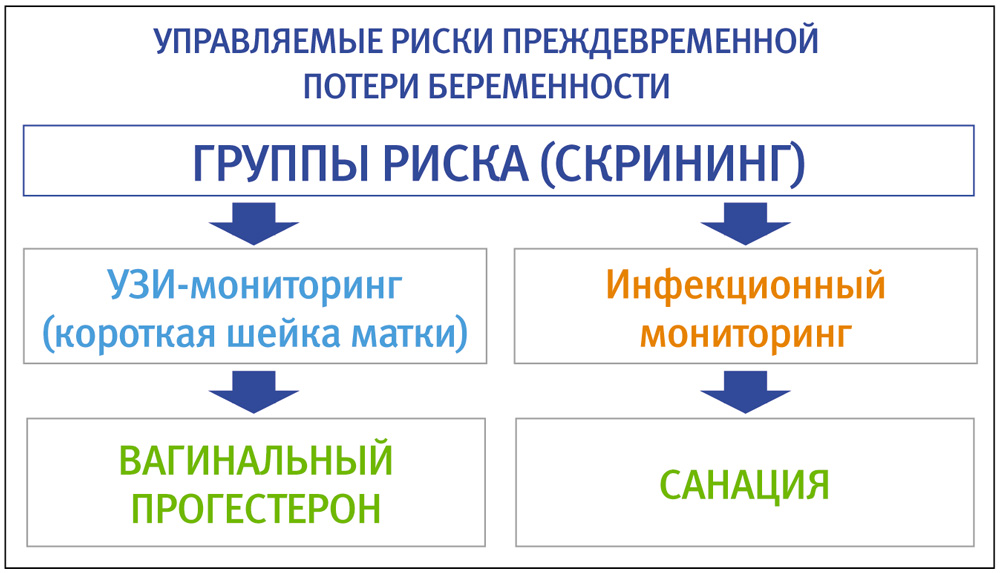
В процессе опознавания и активации системы гормон-рецептор внутриклеточными мессенжерами и сигнальными белковыми молекулами происходит считывание не только количества аминокислот в молекуле прогестерона, но и его уникальной пространственной конфигурации, что в конечном итоге обеспечивает адекватные геномные эффекты, обеспечивающие нормальное развитие беременности.
Одним из проявлений дефицита прогестерона на поздних сроках беременности является синдром бессимптомной короткой шейки матки (КШМ), которая ассоциируется с высоким риском преждевременных родов (Уровень доказательности I-А).
Согласно мнению международных экспертов, сонографическое измерение длины шейки матки трансвагинальным датчиком представляет собой объективный метод оценки риска спонтанного наступления ПР, особенно в случае отсутствия других признаков. При этом за длину шейки матки принимается расстояние от внутреннего до наружного зева по проекции шеечного канала, которая в норме составляет 35–46 мм. Короткой шейкой матки общепринято считается уменьшение ее длины менее 30 мм.
Доказано, что при длине шейки матки менее 30 мм ПР наблюдаются в 10% случаев, а при укорочении менее 20 мм – у каждой третьей беременной с подобной несостоятельностью шейки матки.
Сегодня исследование длины шейки матки для оценки вероятности наступления ПР должно стать основным скрининговым методом, частью стандартной регламентированной сонографической процедуры во II триместре беременных (18–22 недели) на врожденные пороки развития. Почему пальцевое исследование и осмотр шейки матки зеркалах для диагностики короткой шейки матки уступает сонографическому ее исследованию? Суть в том, что укорочение шейки матки идет первоначально за счет раскрытие внутреннего зева и образования так называемой воронки (фанел), образуемой вклиниванием плодного пузыря в просвет шеечного канала, диагностика которых возможна только при трансвагинальном сонографическом исследовании.
Переходя к вопросам лечения невынашивания беременности на ранних сроках и при КШМ, следует отметить, что в настоящее время стандартов терапии этой патологии не существует. Однако накоплен достаточный международный опыт, обобщенный в соответствующих рекомендациях по ведению беременных с КШМ, результаты которого обсуждались не раз как на международных, так и отечественных научно-практических форумах.
Мы в своей практике, следуя этим рекомендациям, используем следующие схемы терапии угрозы НБ: при болях внизу живота натуральный микронизированный прогестерон (Утрожестан) назначается интравагинально в дозе 200–400 мг/сутки. При болях внизу живота, сочетающихся с кровянистыми выделениями, стартовая доза составляет 400 мг/сутки, к ее увеличению до 600 мг обычно прибегают при отсутствии терапевтического эффекта от предыдущей дозы прогестерона. В практической деятельности нам нередко приходится прибегать и к максимальной суточной дозе (800 мг), которая назначается при значительных кровянистых выделениях из половых путей. Можно отметить, что уменьшение размеров ретрохориальных гематом в таких случаях происходит у 2/3 беременных уже через 7–10 дней назначения Утрожестана.
В случае диагностики КШМ в сроках 18–22 недели, Утрожестан профилактически назначаем интравагинально в дозе 200 мг на ночь до 36 недели и 6 дней беременности. В ряде случаев такая терапия является вторым этапом сохраняющей беременность терапии, когда беременным с признаками НЛФ Утрожестан назначался в первом и втором триместрах беременности.
Веские доводы в защиту прогестерона предъявила сама эволюция человека, которая создала и определила именно прогестерон как гормон беременности, а не другое вещество для обеспечения беременности.
Вряд ли нам когда-либо удастся создать искусственно более совершенное средство для сохранения беременности, так не лучше ли рационально использовать то, что уже создано природой и находится в его ареалах. В этом отношении, препарат натурального прогестерона Утрожестан, безусловно, является лидером среди прогестинов и самым назначаемым прогестероном в мире, согласно опросу экспертов в области бесплодия и сохранения беременности.
В резюме хотим отметить, что формирование понятия «контролируемые факторы риска и рациональное управление рисками», в том числе и медикаментозными средствами, стало объективно необходимым условием успешной беременности в современных, порой сложных, условиях жизнеобеспечения, а также ключевым фактором медицинской сферы деятельности, направленной на предотвращение преждевременной потери беременности.
Детальніше

ВОЗМОЖНОСТИ КОРРЕКЦИИ СИМПТОМОВ ГОРМОНАЛЬНОГО ДЕФИЦИТА ПОСЛЕ КОМПЛЕКСНОГО ЛЕЧЕНИЯ ОНКОЗАБОЛЕВАНИЙ МОЛОЧНОЙ ЖЕЛЕЗЫ И ЖЕНСКИХ ПОЛОВЫХ ОРГАНОВ
 Проблема сохранения качества жизни пациенток после различных методов комбинированного лечения онкопатологии давно носит междисциплинарный характер. Применение антиэстрогенов является непременным компонентом такой терапии у женщин. В последнее время широкое применение селективных препаратов этой группы позволило снизить неблагоприятные побочные эффекты гормонального дефицита. Разнообразные аспекты применения торемифена явились поводом обсуждения врачей различных специальностей на конференции, которая проходила в конце мая 2014 г. в Риме
Проблема сохранения качества жизни пациенток после различных методов комбинированного лечения онкопатологии давно носит междисциплинарный характер. Применение антиэстрогенов является непременным компонентом такой терапии у женщин. В последнее время широкое применение селективных препаратов этой группы позволило снизить неблагоприятные побочные эффекты гормонального дефицита. Разнообразные аспекты применения торемифена явились поводом обсуждения врачей различных специальностей на конференции, которая проходила в конце мая 2014 г. в Риме
Гормональная перестройка в условиях климактерия провоцирует формирование целого ряда вегетососудистых, нейропсихических и обменно-дистрофических нарушений. Ее формирование на фоне хирургических потерь и медикаментозных методов антиэстрогеновой коррекции носит стремительный характер.
У большинства пациенток, пролеченных по поводу онкопатологии женской репродуктивной сферы, климактерический синдром (КС) протекает атипично. Кроме того, резкое снижение гормонального фона у таких пациенток характеризуется более выраженной клинической симптоматикой вегето-сосудистых нарушений: приливами тяжелой степени тяжести, мигренеподобной головной болью, расстройствами сна, эмоциональной неустойчивостью с тревожным синдромом. Для таких пациенток характерно быстрое развитие артериальной гипертензии, изменение липидного спектра крови, ИБС, инсульта, инсулинорезистентности. Клинический опыт показывает, что КС приводит к ухудшению течения соматических заболеваний. Все это требует назначения «терапии сопровождения» у женщин с гормональной недостаточностью после лечения онкозаболеваний молочной железы и женских половых органов. Бесспорно, заместительная гормональная терапия (ЗГТ) для этих пациенток противопоказана. И именно в таких случаях используют альтернативные методы лечения.
Альтернативные методы – это методы терапии климактерических нарушений, обладающие подобным с гормональной терапией механизмом действия, но не вызывающие отрицательных побочных влияний (пролиферативной активности в матке, молочной железе, повышения тромбогенного потенциала крови). В данном случае, большое внимание уделяется назначению натуральных средств – фитогормонов и фитоэстрогенов.
Фитогормоны (экстракт цимицифуги, дудника китайского) – природные вещества, не обладающие эстрогенным действием, но положительно влияющие на симптомы менопаузы. Фитогормоны воздействуют на гипоталамус, подавляя пульсирующее высвобождение лютеинизирующего гормона (ЛГ), снижают выброс серотонина, нормализуют активность центра терморегуляции и обладают органной селективностью.
Также у таких пациенток перспективным является использование фитоэстрогенов. Фитоэстрогены – вещества растительного происхождения, функционально близкие к эстрадиолу, что позволяет им связываться с эстрогеновыми рецепторами и оказывать эстрогенный эффект.
Основное преимущество фитоэстрогенов заключается в том, что они способствуют устранению последствий дефицита эстрогенов: раннего старения женщины и климактерического синдрома, не повышая при этом риск развития онкологических заболеваний, за счет угнетения пролиферации клеток, особенно атипически измененных, а также стимуляции их апоптоза.
Комплексные препараты, содержащие фитогормоны и фитоэстрогены, имеют высокую клиническую эффективность и воздействуют на все звенья патогенеза заболевания. Эти свойства реализованы в негормональном фитокомплексе «Лайфемин» (Универсальное агенство «Про-Фарма», Украина), который производится на основе стандартизированных растительных экстрактов «NATUREX»(Франция).
Состав препарата представляет комбинацию соединений экстрактов из шишек хмеля (120 мг) – Lifenol, корневища цимицифуги рацимозы (30 мг), корня пуэрарии лопастной (50 мг), корня дудника китайского (50 мг), дикого ямса (70 мг) и порошка жемчужного кальция (60 мг)
Lifenol – стандартизованный экстракт хмеля (производство «NATUREX», Франция), по функциональным свойствам близок к эстрогену, проявляет выраженное эстрогенное действие.
Экстракт корня пуэрарии лопастной содержит изофлавоны, которые, кроме эстрогенной активности, обладают еще выраженным антиоксидантным действием, он также способствует вазодилатации и нормализации артериального давления.
На сегодняшний день доказано, что фитоэстрогены хмеля и пуэрарии обладают самым мощным эстрогенным действием. Однако при применении фитопрепаратов с высокой эстрогенной активностью возникает вопрос опасности развития гиперпластических процессов.
Поэтому и оправдано наличие дикого ямса в препарате «Лайфемин», который не только предотвращает развитие атеросклероза, обладает спазмолитическим, вазодилатирующим действием, но и обеспечивает защиту матки и молочной железы от патологической пролиферации.
На базе Донецкого регионального центра охраны материнства и детства было проведено обследование 96 женщин, страдающих симптомами гормонального дефицита после комплексного лечения онкозаболеваний молочной железы и женских половых органов.
Клинические проявления КС у обследованных женщин включали:
- раздражительность 70,8%;
- плаксивость 56,%;
- депрессию 65,6%;
- приливы 93,7%;
- потливость 94,7%;
- эмоциональную лабильность 78,1%.
Модифицированный менопаузальный индекс (ММИ) составил в среднем 48,5±11,2 балла, что указывало на наличие КС средней и тяжелой степени тяжести у данных пациенток.
Урогенитальные расстройства отмечались у 54 (56,3%) пациенток, сексологические жалобы на недостаточность и снижение сексуального желания – у 75%, диспареуния – у 59,4% женщин. Отмечено значительное повышение рН влагалища до 6,5–7,3. Индекс вагинального здоровья Бахмана составил 3,3±0,7 балла, что указывало на преобладание умеренной атрофии слизистой влагалища.
Через 6 месяцев применения препарата «Лайфемин» ММИ составил 25,3±2,5 балла. Уровня эмоционального комфорта достигли 71,9% женщин.
Произошло уменьшение показателей рН до 5,4–6,3 и индекс вагинального здоровья составил 3,6±0,4 балла, а улучшение любрикации у 50% пациенток привело к увеличению частоты половых контактов.
Анализ качества жизни через 6 месяцев лечения показал положительную динамику самочувствия, уменьшение частоты вазомоторных, психоэмоциональных и урогенитальных симптомов.
Комплексное влияние «Лайфемин» на организм женщины обусловлен потенцирующим действием всех биологически активных экстрактов и проявляется в значительном уменьшении проявлений климактерического синдрома, нормализации работы нервной системы, повышении стрессоустойчивости, улучшении работы сердечно-сосудистой системы.
Полученные положительные результаты назначения растительного комплекса «Лайфемин» являются основанием для его практического применения и могут быть надеждой для больных и врача при наличии противопоказаний для ЗГТ. Применение фитокомплекса «Лайфемин», который содержит эстроген-гестагенные компоненты, гарантирует отсутствие гиперпластических процессов в матке и молочной железе у таких пациенток, даже при длительных схемах применения.
Детальніше
