
МІКРОНІЗОВАНИЙ ПРОГЕСТЕРОН У ТЕРАПІЇ ЗАГРОЗИ ПЕРЕДЧАСНИХ ПОЛОГІВ
Ефективність комбінованого застосування сублінгвальної та вагінальної форм.
Передчасними вважають пологи зі спонтанним початком, прогресуванням пологової діяльності та народженням плода масою >500,0 г у термінах вагітності від 22 до 36 тиж. + 6 діб [4]. У перебігу передчасних пологів (ПП) виділяють 2 етапи: загроза передчасних пологів та власне передчасні пологи, що почалися. Приділяючи увагу попередженню та терапії передчасних пологів, акушери-гінекологи, насамперед, намагаються вчасно профілактувати та лікувати загрозу ПП.
Фармакокінетика і фармакодинаміка прогестерону, а отже, і вивчені ефекти залежать від способу введення препарату. За внутрішньом'язового шляху введення спостерігаються надфізіологічні плазмові концентрації прогестерону. Пероральне застосування виявляє швидке підвищення плазмових концентрацій з подальшим поступовим їх зниженням. Крім того, за цих способів уведення має місце ефект першого проходження гормону через печінку з утворенням декількох біологічно активних метаболітів.
 За вагінального введення досягають стабільних плазмових концентрацій і постійних концентрацій у тканинах – так званий ефект першого проходження через матку із спрямованим впливом на ендометрій; крім того, спостерігають мінімальний ризик виникнення системних ефектів. Сублінгвальна форма дає змогу досягти найшвидшого ефекту, відсутній первинний метаболізм гормону у печінці, а отже не втрачається його концентрація і, таким чином, ця форма введення має найменш тривалий період напіввиведення [1, 3]. Хоча слід відмітити, що фундаментальних досліджень застосування сублінгвальної форми мікронізованого прогестерону в разі загрози передчасних пологів не проводилося.
За вагінального введення досягають стабільних плазмових концентрацій і постійних концентрацій у тканинах – так званий ефект першого проходження через матку із спрямованим впливом на ендометрій; крім того, спостерігають мінімальний ризик виникнення системних ефектів. Сублінгвальна форма дає змогу досягти найшвидшого ефекту, відсутній первинний метаболізм гормону у печінці, а отже не втрачається його концентрація і, таким чином, ця форма введення має найменш тривалий період напіввиведення [1, 3]. Хоча слід відмітити, що фундаментальних досліджень застосування сублінгвальної форми мікронізованого прогестерону в разі загрози передчасних пологів не проводилося.
На сьогодні, за нашими даними, оптимальною є наступна комбінація різних форм введення прогестерону: лікування у гострому періоді доцільно починати із сублінгвальної форми, а після регресу клінічної симптоматики та досягнення відповідної для даного терміну вагітності концентрації гормону в плазмі крові, за відсутності проявів кольпіту, варто перевести пацієнтку на вагінальну форму.
У ході дослідження R. Romero і співавт., 2012, встановлено, що на тлі застосування вагінального мікронізованого прогестерону ризик передчасних пологів у терміні до 33 тижнів знизився на 42%, крім того, достовірно знизилися показники частоти захворюваності/смертності новонароджених, розвитку респіраторного дистрес-синдрому, потреби у штучній вентиляції легенів та ін. [9].
Метою нашої роботи було вивчити ефективність застосування сублінгвальної та вагінальної форм препарату мікронізованого прогестерону (Лютеїна, Адамед, Польша) у комплексній терапії загрози передчасних пологів.
Матеріали та методи
У дослідженні приймали участь 60 вагітних із загрозою передчасних пологів у терміні вагітності 22–30 тиж., які були госпіталізовані та отримали терапію на клінічних базах кафедри акушерства та гінекології №1 НМАПО імені П. Л. Шупика.
Усі пацієнтки були розподілені на 2 групи:
І-а група – 30 вагітних, які протягом першої доби отримували магнезіальну токолітичну терапію: MgSO4 25% 20 ml + Sol. NaCl 0,9% 200 ml; гормональну терапію – сублінгвальну форму мікронізованого прогестерону (МП) (Лютеїна) 100 мг ч/з 6 год., тричі, разом з третім прийомом сублінгвальної форми вагітні вводили вагінальну форму МП – 100 мг; системну протизапальну терапію – ректальні свічки з диклофенаком 50 мг два рази на добу. На другу добу вагітні отримували магнезіальну токолітичну терапію: MgSO4 25% 20 ml + Sol. NaCl 0,9% 200 ml; гормональну терапію – вагінальну форму МП – 150 мг два рази на добу; системну протизапальну терапію – ректальні свічки з диклофенаком 50 мг два рази на добу. На третю добу вагітні отримували гормональну терапію – вагінальну форму МП – 150 мг два рази на добу; комбінований препарат магнію лактату дигідрату (470 мг) та піридоксину гідрохлориду (5 мг) по 2 таблетки три рази на добу; системну протизапальну терапію – ректальні свічки з диклофенаком 50 мг два рази на добу. На 4–7 добу вагітні отримували гормональну терапію – вагінальну форму МП 100 мг два рази на добу; комбінований препарат магнію лактату дигідрату (470 мг) та піридоксину гідрохлориду (5 мг) по 2 таблетки три рази на добу; системну протизапальну терапію – ректальні свічки з диклофенаком 50 мг за наявності больових відчуттів.
ІІ-а група – 30 вагітних, які протягом перших двох діб отримували магнезіальну токолітичну терапію: MgSO4 25% 20 ml + Sol. NaCl 0,9% 200 ml; гормональну терапію – 2,5% розчин масляного прогестерону 2 мл з внутрішньом'язовим шляхом введення один раз на добу; системну протизапальну терапію – ректальні свічки з диклофенаком 50 мг три рази на добу. На третю добу вагітні отримували гормональну терапію – 2,5% розчин масляного прогестерону 2 мл з внутрішньом'язовим шляхом введення один раз на добу; комбінований препарат магнію лактату дигідрату (470 мг) та піридоксину гідрохлориду (5 мг) по 2 таблетки три рази на добу; системну протизапальну терапію – ректальні свічки з диклофенаком 50 мг два рази на добу. На 4–7 добу вагітні отримували гормональну терапію – 2,5% розчин масляного прогестерону 1 мл з внутрішньом'язовим шляхом введення один раз на добу; комбінований препарат магнію лактату дигідрату (470 мг) та піридоксину гідрохлориду (5 мг) по 2 таблетки три рази на добу; системну протизапальну терапію – ректальні свічки з диклофенаком 50 мг за наявності больових відчуттів.
Усі пацієнтки обох груп отримали профілактику РДС плода – 24 мг дексаметазону в/м (6 мг ч/з 12 годин 4 рази).
Відміну гормональних препаратів прогестерону проводили з 8-го дня поступово, під контролем УЗД, відповідно до клінічного стану вагітної. У разі виявлення вкорочення шийки матки до 20 мм та більше, ми рекомендували вагітним продовжити прийом вагінальної форми МП (50–100 мг два рази на добу) до 34 тижнів вагітності з подальшим поступовим зниженням дози та відміною препарату.
Результати та їх обговорення
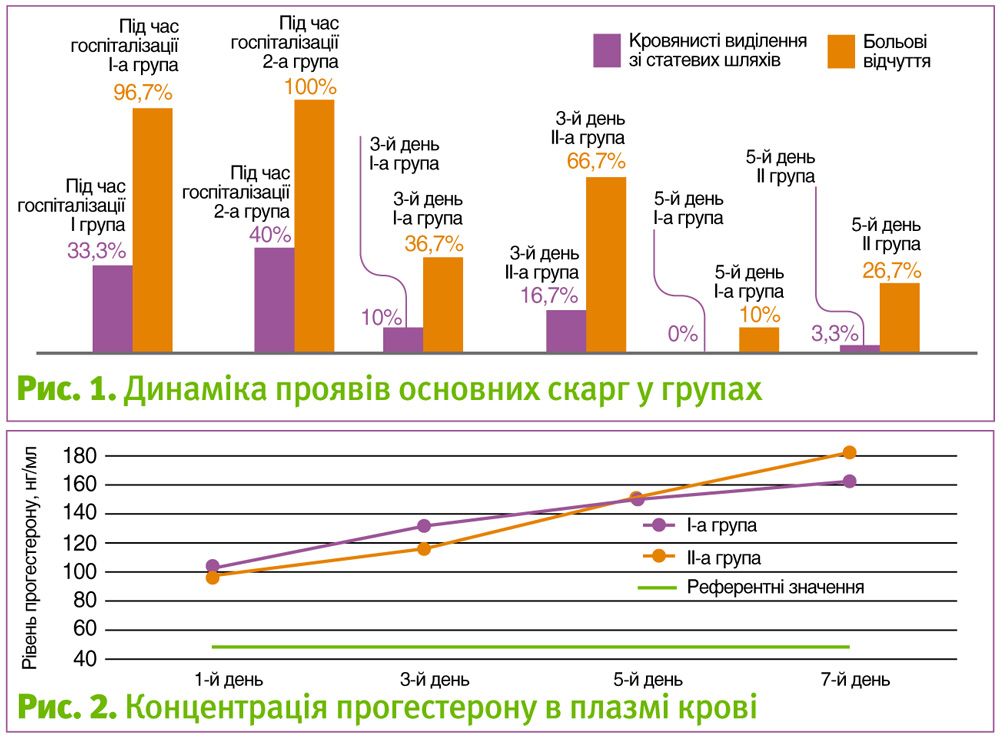
Під час госпіталізації практично всі вагітні в обох групах дослідження скаржилися на ниючі та/чи переймоподібні болі внизу живота та/чи попереку, у І-й групі мажучі кров’янисті виділення зі статевих шляхів спостерігали 33,3% вагітних, цей показник достовірно не відрізнявся в ІІ-й групі дослідження і становив 40,0% (Рис. 1).
У процесі лікування ми спостерігали швидший регрес клінічної симптоматики у І-й групі дослідження. Так, на 3 добу лікування больові відчуття відзначали 40% жінок, в той же час у ІІ-й групі цей показник був достовірно вище (р<0,01) і становив 66,7%. Отримані результати ми пов’язуємо зі швидкою дією сублінгвальної, а потім підтримуючою дією вагінальної форм МП, порівняно з помірними темпами всмоктуванням масляного прогестерону із сідничного м’яза. На 5-ту добу клінічна симптоматика зберігалася у 10,0% вагітних І-ї групи та 26,7 пацієнток ІІ-ї групи. На 7-му добу скарги у пацієнток обох групи були відсутні.
Середні рівні концентрації прогестерону на момент госпіталізації в обох групах дослідження не мали достовірних відмінностей. Під час лікування була помічена цікава тенденція: рівні прогестерону в ІІ-й групі на 3-тю добу мали менший приріст, ніж в І-й групі, проте на 5-ту та 7-му добу саме в ІІ-й групі ми фіксували вищі рівні концентрації прогестерону у плазмі крові (Рис. 2). Отримані результати можна пояснити більш тривалим всмоктуванням масляного прогестерону саме за внутрішньом’язового введення з подальшим створенням пікової концентрації у плазмі крові, в той час як вагінальна форма МП забезпечує первинне проходження та пікову концентрацію гормону в матці.
Під час проведення біохімічного дослідження крові рівні показників печінкових проб (АЛТ, АСТ, загальний білірубін, непрямий білірубін, загальний білок) та коагулограми (АЧТЧ, фібриноген, фібрин, тромбіновий час) в обох групах дослідження знаходилися у рамках референтних значень, а отже можна стверджувати, що порушення функції печінки були відсутні у всіх жінок обох груп.
Основними УЗ-ознаками ефективності проведеної терапії вважали відсутність прогресування вкорочення шийки матки, збільшення діаметру внутрішнього вічка та зникнення гіпертонусу матки. У І-групі на третю добу у 6,7% довжина шийки матки зменшилася до 20–25 мм, а у 3,3% діаметр внутрішнього вічка збільшився >3 мм. У другій групі ці показники були дещо гіршими, так у 13,4% довжина шийки матки становила менше 25 мм, а у 10,0% шийка матки стала коротша за 20 мм. На 5-ту та 7-му добу ми не спостерігали прогресування клінічної симптоматики у І-й групі пацієнток, проте в ІІ-й групі кількість жінок з довжиною шийки матки 15–20 мм збільшилася ще на 10,0%. Вищу ефективність та швидший ефект лікування у І-й групі можна пояснити унікальною властивістю саме вагінальної форми МП накопичуватися безпосередньо у тканинах, протидіяти скороченням матки та зберігати структуру шийки матки.
Під час подальшого спостереження було встановлено, що у жінок І-ї групи пологи в терміні 37 тиж. та більше відбулися в 83,3%, зокрема в терміні 40–42 тиж. у 16,7%. З них 16,7% вагітних були розроджені шляхом кесаревого розтину в зв’язку з дистресом плода у пологах – 10%, передчасним відшаруванням нормально розташованої плаценти – 3,35%, дистоцією шийки матки в пологах – 3,35%. Передчасний розрив плодових оболонок (ПРПО) спостерігали в 20,0% випадків.
У ІІ-й групі пологи в терміні доношеної вагітності відбулися у 53,3%, розродження шляхом кесаревого розтину відбулося в 10% у зв’язку з дистресом плода в пологах. ПРПО спостерігали в 23,3%.
За шкалою Апгар на першій хвилині новонароджені І групи мали оцінку 6,4+1,6, ІІ групи – 6,1+1,9; на п’ятій хвилині новонароджені І групи мали оцінку 7,5+1,5 балів, ІІ групи – 7,0+1,8 балів.
Передчасні пологи у І-й групі спостерігали у 16,7% жінок у термінах 32–37 тижнів, пологи перебігали консервативно, новонароджені були оцінені на І-й хвилині в 5,0+1,0 балів та на 5-й хвилині в 6,0+1,0 балів за шкалою Апгар. У ІІ-й групі передчасні пологи спостерігали достовірно частіше (p<0,05) – у 46,7% пацієнток, у термінах 30–37 тиж., у 26,7% жінок були проведені консервативно, оперативне розродження проведено в зв’язку з передчасним відшаруванням плаценти у 2-х випадках. Новонароджені були оцінені на І-й хвилині в 4,0+1,0 балів та на 5-й хвилині в 6,0+1,0 балів за шкалою Апгар.
Отримані результати вказують на кращі перинатальні перспективи у пацієнток, які отримували комбіновану терапію загрози передчасних пологів сублінгвальною та вагінальною формами МП (Лютеїна), порівняно з вагітними, які отримували внутрішньом'язові ін’єкції 2,5% масляного розчину прогестерону.
Під час дослідження, завдячуючи висококваліфікованій роботі медичного персоналу, ми не спостерігали побічних ефектів та ускладнення терапії в обох групах дослідження.
Висновки
- Використання сублінгвальної форми мікронізованого прогестерону та препаратів магнію у період вираженої клінічної симптоматики загрози передчасних пологів дозволяє отримати максимально швидкий терапевтичний ефект та запобігти подальшому прогресуванню структурних змін з боку шийки матки.
- Комплексна терапія загрози передчасних пологів з використанням сублінгвальної та вагінальної форм МП (Лютеіна), препаратів магнію, нестероїдних протизапальних препаратів має високу ефективність терапевтичної дії та може бути рекомендована для широкого використання у родопомічних закладах.
- Застосування вагінальної форми МП (Лютеїна) у терапії загрози передчасних пологів та в якості вторинної профілактики передчасних пологів у жінок з вкороченою шийкою матки (менше 20,0 мм) достовірно зменшує частку передчасних пологів та покращує перинатальні наслідки.
Перелік літератури
знаходиться у редакції.
Детальніше

ВПИСАТЬСЯ В МАТРИЦУ!
30 октября мы провели Профи-Лаб «Встречи профессионалов: беременность, роды, послеродовой период». Это уже третье мероприятие такого масштаба, организованное нашим журналом
Цель таких встреч – собрать украинских врачей, а также известных зарубежных ученых и практиков для обсуждения общих проблем, с которыми сталкиваются представители акушерского сообщества.
В этот раз мы пригласили легенду мирового акушерства, автора методики проведения кесарева сечения, признанную во всем мире, – Майкла Старка.
Участники встречи с огромным интересом слушали выступление метра – человека, биография которого отображает целую эпоху в мировой медицине.
Мы очень рады, что нам удалось успешно реализовать тот формат конференции, который мы задумывали.
Это и настоящие дискуссии, и участие представителей смежных специальностей, и создание непринужденной атмосферы общения участников.
В общем, настоящая встреча профессионалов – людей неравнодушных, стремящихся выйти за рамки повседневности.
Такие встречи приносят ощущение того, что ты являешься частицей общей матрицы, которая объединяет профессионалов в разных странах мира. Нам бы очень хотелось, чтобы такие же чувства испытывали все участники!
И, по традиции, предлагаем вам посмотреть фотоотчет с места событий.
Эти и другие фото с мероприятия: https://goo.gl/wKeQkx
Детальніше

МАЙКЛ СТАРК: ЛЮДИНА, КОТРА ЗМІНИЛА ВСЕ
 Майкл Старк (Michael Stark), Prof. hc, Dr. med.
Майкл Старк (Michael Stark), Prof. hc, Dr. med.
1983–2000 – медичний директор, керівник відділення акушерства та гінекології клініки Misgav Ladach (Єрусалим);
2002–2010 – керівник гінекологічного напрямку Групи госпіталів «Helios» (Німеччина, Австрія);
З 2011 – науковий керівник Європейського проекту телехірургії Telelap Alf-х, Sofar SpA (Мілан);
З 2004 – Президент NESA – Нової Європейської академії хірургії (Берлін).
- Розробив і продовжує вдосконалювати авторську методику проведення кесарського розтину, визнану в усьому світі.
- На чолі NESA впроваджує нові методи оптимізації хірургічних процедур, зокрема, шляхом використання природних отворів тіла.
- Керує розробкою нових хірургічних стандартів якості.
- Пропагує передачу знань таноу-хау до країн з обмеженими ресурсами.
Трапляються люди, що добре працюють руками. Рідше – ті, хто влучно формулює думки. Один весь вік проживає одну й ту саму захоплюючу історію, інший кожним кроком завойовує новий обрій. Тих, хто поєднує у собі все згадане, зустрінеш нечасто.
З ними не хочеться говорити, лише слухати. Не сперечатися, лише наслідувати. Просто бути поруч – вже це одне виправдовує існування. Дива трапляються. Така людина сьогодні перед нами.
Наступного дня після виступу пана Старка на Профі-Лабі з акушерства нам вдалося взяти у нього чудове інтерв'ю – неквапливе, дружнє, доброзичливе. Чим більше ми спілкувалися під час прогулянки вулицями Києва, тим несподіванішою та багатограннішою особистістю поставав перед нами Майкл Старк – дивовижна чіткість мислення, гумор, абсолютна впевненість у собі разом з цілковитою відкритістю до нової інформації.
Як громадянин Ізраїлю, він пройшов 5 воєн, був поранений. З глибоким співчуттям слухав про наш Майдан, війну, внутрішніх переселенців, військові госпіталі, і у якийсь момент сказав, що світ дуже мало робить для України.
Велике щастя – спілкуватися з людьми, біографії яких відображають цілі епохи, а світогляд та знання – цілий світ.
Професоре Старк, Ви якось зауважили, що візит до України для Вас є особливою подією.
Майкл Старк: Це насправді так. Моя сім’я родом з Чернівців. Батьки жили там за Австрії і фактично до другої світової. Декілька років тому мав нагоду відвідати це чудове місто, знайти старовинний будинок – помешкання батьків, навіть побачити фортепіано, на якому грала мати. Старша сестра виїхала з передвоєнної Буковини останньою, але все пам’ятає і навіть спромоглася скрізь мене поводити.
Втім, насправді дивовижною історією є доля моєї тещі, яка у серпні 1939 року в складі баскетбольної команди Білостоку приїхала до Києва на змагання. А 1-го вересня Німеччина напала на Польщу і шлях до повернення було перетято. Усі її рідні були згодом знищені. Вона ж, студентка-медик, жила при інституті, де, паралельно з навчанням, працювала прибиральницею. За два роки війна пришла до Києва. Інститут перевели на Урал. У 1947 разом із маленькою донькою та чоловіком-військовим, якого намагалися заарештувати без пояснень, була вимушена тікати до США через північний схід. Згодом теща стала відомим у світі лікарем, довго працювала в Нью-Йорку, об’їздила весь світ, але щиро вважала Київ найкращим містом на планеті.
Ваша операція стала свого роду новою класикою в акушерстві. Як це воно – бути класиком?
М. С: Я насправді не вважаю себе якоюсь видатною особистістю. Просто завжди був дуже допитливим. Все, що зробив, походило з глибокого переконання у відсутності чітких догм, зокрема в медицині. Ми живемо в мінливому світі, ніщо не закарбоване в камені. Навіть, коли так здається.
Мене завжди цікавило, що ж за тим каменем? І я намагався зрозуміти сутність речей. Завжди бентежили ситуації, де єдиною підставою для виконання певних дій була винятково традиція і жодних інших підстав.
Окрім того, мене захоплює інтердисциплінарність. Я маю на увазі не тільки запозичення акушерства у хірургії чи урології. Безліч корисних ідей можна взяти з архітектури, музики, механіки. Все, що є тим чи іншим видом мистецтва, – інтердисциплінарне. Ми просто маємо бути більш уважними до світу і краси.
Ви говорите про небезпечність традицій, а чи є традиції корисні?
М. С: Є традиції, які важливо залишати незмінними. Наприклад, народна музика чи обрядові святкування. Однак, коли йдеться про питання життя й смерті, традиції повинні контролюватися. Царицею царів на сьогодні є доказова медицина. Якщо комусь вдалося довести, що наявна традиція – добре, варто її підтримувати. Але дуже часто ми спростовуємо їхню доцільність, і тоді не слід боятися змін!
Традиція не може бути аргументом, а винятково основою для порівняння. Трапляються, ясна річ, і корисні традиції. Наприклад, аспірин. Якщо б його вигадали сьогодні – нікому б на думку не спало його застосовувати: викликає шлункові кровотечі, порушує агрегацію тромбоцитів, казна що! FDA ніколи б не допустила цього неподобства. Однак, у зв’язку з багаторічним традиційним використанням сьогодні ми маємо чудовий препарат. І навпаки, зашивання очеревини. Це – традиція і ніхто до сьогодні не здатний науково довести користь од неї. Накладання швів на підшкіру – теж традиція, і теж шкідлива.

Існують багато модифікацій вашого методу кесарського розтину, як ви ставитеся до цього?
М. С: Я абсолютно впевнений, що усе має базуватися на доказах. Якщо хтось доведе, що той чи інший крок операції має бути змінений – сьогодні ж модифікую свою методику. На жаль, більшість модифікацій радше мають на меті тішення ego та самоствердження. Довести доцільність модифікації доволі складно, тому що для цього необхідно проводити абсолютно стандартизовані операції. Такі прийнятні для всіх і водночас доказово обґрунтовані стандарти створити непросто, однак, за ними майбутнє. Таким чином, покажіть мені, що в проспективному рандомізованому дослідженні ви довели переваги вашої модифікації – і я потисну вам руку. Але до цих пір цього не сталося.
Як ви ставитеся до кесарського розтину за вимогою жінки?
М. С: Я би не хотів забиратися в хащі законодавства. Є безліч країн, де така операція може бути легально проведена за вимогою. Мені б хотілося поговорити про медичні аспекти. Я палкий прибічник природних пологів і не проводжу кесарський розтин без показань. Можна зробити блискучу операцію, але якщо у вас не було показань – скоєно шкоду. Маємо пам’ятати: Primum non nocere.
Річ у тім, що пологи є вкрай важливими для новонародженого. Вони стимулюють правильну роботу дихальної системи, фінальне дозрівання легеневої тканини. Під час пологів відбувається колонізація кишківника новонародженого материнським біотопом, який залишається з ним на все життя, захищаючи від хвороб та онкозахворювань. Тому слід говорити з жінками, пояснювати переваги природних пологів. І переважна більшість погодиться з вашими аргументами.
Вертаючись до питань законодавства. Якщо жінка рішуче налаштована мати кесарський розтин, вона його отримає. Тобто, все одно знайдеться такий лікар, який так чи інакше її прооперує. Але це питання часу, нервів, якості виконання операції. Лікарю доведеться брехати, встановлюючи показання. Тому моя думка: законодавчо це повинно бути доступним, але слід вимагати від лікарів чесного ставлення до своєї роботи. Гарним кроком у деяких країнах було зменшення платні лікарю за проведений кесарський розтин у порівнянні з природними пологами, це в короткий термін призвело до зменшення кількості операцій.
Як ви ставитеся до планових кесарських розтинів?
М. С: Я великий противник такого підходу. Коли ви маєте показання до ургентного кесарського розтину – зробіть його негайно. Але, якщо показання дозволяють відкласти операцію – завжди дочекайтеся початку переймів. У цьому терміні мати буде готовою до народження, молочні залози – для лактації, дитина посилатиме природні сигнали про необхідність народження, цервікальний канал стане прохідним, нижній сегмент сформується та витончиться. Майже всі діти, народжені за таким принципом, будуть функціонально зрілими. Якщо ви робите плановий кесарів розтин, ви часто робите його за два тижні до моменту, коли б насправді ця дитина мала народжуватися.
У нас переважна більшість лікарів та адміністраторів протестують проти такого підходу. Мовляв, у такий спосіб ми переводимо операції з планових до категорії ургентних, а вдень безпечніше проводити оперативні втручання.
М. С: О, ні! Це величезна глупість. В акушерстві має бути так: якщо госпіталь не здатний надати 100% кваліфіковану допомогу цілодобово, він не має права займатися акушерством. Це абсолютно неважливо, коли відбудеться операція – вдень чи вночі, якість надання допомоги має бути однаковою. Хіба о третій ранку не може поступити жінка з відшаруванням чи випадінням петель пуповини?
Можливо, ми боїмося, що вночі в пологовому будинку недостатньо персоналу або недостатньо персоналу найвищої кваліфікації?
М. С: Це не аргумент. Можливо, слід мати меншу кількість госпіталів, але укомплектованих винятково професіоналами високого рівня. Уявляю собі ситуацію: ніч, відшарування, ДВЗ-синдром, а ви їй: «агов, жіночко, негайно припиніть кровити, бо нам треба викликати досвідченого лікаря для вашого лікування!».
Якщо б ви надавали рекомендацію головному лікарю, як контролювати рівень кесарських розтинів, на чому б ви зупинили увагу?
М. С: Нещодавно я консультував один госпіталь у Франції, рівень кесарських розтинів в якому сягав 26%. Єдиною порадою, яку я надав, було впровадження обов’язкової «другої думки» щодо прийняття рішення про розтин. При чому другий лікар ставив свій підпис під рішенням або дозволяв вказати його в консиліумі. Через 2 місяці кількість кесаревих розтинів зменшилася до 16%.
Чесно кажучи, в Україні така практика є рутинною, у нас існує потреба у трьох підписах для виконання операції. Але у лікарів розповсюджена, так би мовити, висока «колегіальність» щодо прийняття таких рішень. І, насправді, знайти однодумця не так вже й важко.
М. С: Це не аргумент. У моєму всесвіті для цього є дуже гарне слово. Це слово – «злочин». Якщо я колись дізнаюся, що хтось із лікарів бодай раз мені збрехав, не щодо «з ким провів ніч», а щодо медичних питань, він вилетить з лікарні у той же день. Ми називаємо це «нульовою толерантністю».
Якщо ви дивитеся на показники кесарських розтинів, що може свідчити на користь того, що їхня кількість у закладі є зависокою?
М. С: Є таке правило: «лікарі повинні завжди говорити правду». Те що ви кажете, є надто бентежним. Якщо призначаються неправильні показання до кесарського розтину, то чи проводяться за правильними показаннями інші операції? В хірургії із цим не жартують. Показання мають бути абсолютно істинними. Тому слід знаходити правильних людей і правильно з ними працювати.
І, ясна річ, позбавлятися оцієї пострадянської системи «каральної статистики». Боятися показників, приховувати реальність – це значить ніколи не знайти шляхів вирішення проблеми. Це тупцювання на місці, що у сьогоднішньому світі означає регрес.
Як часто слід проводити аналіз показників кесаревих розтинів?
М. С: Постійно! Такі речі проводяться щоденно. Так само як і контроль виконання. Ви можете обговорювати рутинні випадки на ранкових засіданнях. Якісь цікаві ситуації можна виносити на детальне обговорення на лікарняних конференціях.
Ви релігійна людина?
М. С: Ні. Як я можу, коли бачу, що відбувається з цим світом? Якщо ви вірите в еволюцію, ви не можете вірити в Бога. Тому що, виходячи з усіх релігій, людина була одразу створена такою, як вона є. А я вірю в еволюцію. Інша справа, що існує безліч речей, яких ми не розуміємо. У ХVI сторіччі Браге розробив теорію про гравітацію, вивчаючи Коперника. Пізніше Ньютон лише розширив його вчення. Ми знаємо, що сила гравітації Землі – триліони тонн, але мені вдається переважити усю гравітацію одним пальцем, піднімаючи ось цю серветку. Зорі за міліарди світлових років від нас притягують і навіть певним чином сторіччями утримують наші думки, як Земля утримує місяць. І чому це відбувається, ніхто не може пояснити напевне.
Скоріше за все, існують інші виміри, які ми не бачимо. І ось для всього, що ми не можемо осягнути, створюється ореол божественності. Але все змінюється.
Сто п’ятдесят років тому лорд Кельвін писав, що літак – це абсурд, що він ніколи не зможе літати, оскільки набагато важчий за повітря. Пізніше, десятиріччями, поважні вчені говорили про неможливість польоту ракети до космосу, через вакуум, який його наповнює. Сьогодні ми надсилаємо апарати на Марс.
Тобто, чим більше ми маємо знань, тим більше рішень можемо знайти. І не варто у всьому звинувачувати Господа. Якщо він все ж таки є, мені було б дуже цікаво спитати, де він був під час Голокосту або коли почалася війна у вашій країні. Втім, я дуже поважаю вірян і у мене насправді все добре з толерантністю. Наприклад, маю дуже релігійного онука. Ми з ним прекрасно ладимо.
Професоре, ми живемо в час швидких змін і спостерігаємо їх ледь не щодня. Що буде з людством завтра?
М. С: Дозвольте говорити лише про гінекологію. Дійсно, коли я закінчив університет, ніхто не знав штучного запліднення, пересадки серця, ультразвукової діагностики, ендоскопії. Все це винайдено у мій час. Прорив відбуватиметься за двома напрямками: генетика і робототехніка. Ми станемо машинозалежні.
Комп’ютерні технології до певної межі швидко падатимуть у ціні. Закон Мура: удвічі більше інформації, менша ціна (емпіричне спостереження засновника Intel Гордона Мура 1965 року про те, що кількість елементів інтегральної схеми комп'ютера щодва роки буде подвоюватись при аналогічному здешевленні. До сьогодні закономірність справджується. – прим. ред.).
Буде менше відкритих операцій, для втручань все більше застосовуватимуться природні отвори. Будемо працювати в малому тазі через Дугласів простір і проводити операції на жовчному міхурі через ротову порожнину. Відбуватиметься глибока спеціалізація лікарів, що добре і водночас погано. Матимемо спеціалістів з ендометріозу, з онкопатології яєчників, з раку шийки матки.
Я везунчик, оскільки навчався в ті античні часи, коли усіх навчали всьому. Тому мені байдуже – читаю я доповідь з онкології чи перинатології. Однак, такі динозаври скоро відійдуть. І залишиться лікар по мітральному клапану. Чудесно! Ніхто не впорається із ним краще, однак, якщо раптом паралельно виникне проблема у «правому серці» – слід буде запрошувати іншого вузького спеціаліста. Така тенденція.
Ви згадували прогрес у генетиці, що саме вас тішить або бентежить?
М. С: У першу чергу, зміниться структура патологоанатомічного розтину. Більше не буде гематоксилін-еозину, лише вивчення патології на рівні клітин, генома. Думаю, років через 20–30 років рак теж будуть лікувати не хіміотерапією, а генетичними методами.
Одного я дуже боюся – тотальної передімплантаційної діагностики. Тому що штучний відбір призведе до відсутності природного. Це стане кінцем еволюції, оскільки ми не зможемо надати планеті достатню варіабельність виду, яка необхідна для виживання.
Адже еволюція все ще триває. Наприклад, ви знаєте про синдром «суперчоловіка» XYY? Це не те щоб подарунок долі, однак, вони мають неабияку витривалість, чудові успіхи в спорті. На сьогодні все більше жінок з таким каріотипом у плода обирають переривання вагітності, у зв’язку з певними особливостями характеру та розвитку таких дітей. Але ми не знаємо, можливо, це нове еволюційне вікно, яке б мало у майбутньому призвести до компенсації виду. А ми його зачиняємо.
Ми не знаємо, як виглядатиме людство через 10 000 років. Можливо, це буде зовсім інший фенотип. Риби майже не змінилися за останні 2,5 міліона років. Можливо, вони знайшли свою оптимальну форму. Людство ж постійно змінюється, причому зміни набагато швидші за очікувані. Приміром, 10 000 років тому на планеті майже не було блакитних очей або лактозної інтолерантності. Ми були набагато меншого розміру, навіть королі, які мали вдосталь їжі. Тобто це не питання харчів, люди реально збільшуються, і ніхто не знає чому: радіація чи інші невідомі сили. Багато чого не знаємо, тому й мусимо бути допитливими. Я не впевнений навіть, що ми добре розуміємо закони фізики. Закон Гейзенберга свідчить, що об’єкт може бути водночас і часткою, і енергією. Тобто ми насправді не розуміємо: існує він у нашому вимірі чи ні.
І взагалі, об’єкт існує винятково, якщо існує спостерігач.
М. С: Саме так, отже ви зараз завдячуєте мені своїм існуванням!
Спасибі, професоре, Ви абсолютно праві. Саме, дякуючи таким як ви, ми – люди, досі існуємо і маємо право так називатися.
Бесіду вели Віктор Ошовський, Тетяна Тихомирова та Людмила Чуприна.
ДетальнішеДИНАМИКА КЛИНИЧЕСКИХ СИМПТОМОВ
Коррекция антиоксидантной недостаточности у женщин с диффузной мастопатией при использовании растительного препарата мастодинон.
Доброкачественные заболевания молочных желез широко распространены у женщин репродуктивного возраста, при этом наиболее частым клиническим проявлением мастопатии является периодический болевой синдром [4, 7]. Изучение патогенеза мастопатии позволило внедрить в практику современные эффективные методы лечения больных, основанные на коррекции гормональных и метаболических нарушений [4].
Ранее было установлено, что наряду с гормональными нарушениями, при дисгормональной мастопатии отмечается активация процессов пероксидации липидов и антиоксидантная недостаточность (то есть оксидативный стресс), в частности, устойчивый дефицит восстановленного гоглутатиона [3]. Восстановленный глутатион является составной частью всех звеньев системы детоксикации ксенобиотиков, выполняет связующую роль между элементами этой системы, принимает участие в регуляции ее активности.
Степень выраженности перекисного окисления липидов (ПОЛ) отражают концентрации его молекулярных продуктов: малонового диальдегида, диеновых конъюгатов гидроперекисей, кетодиенов и триенов (вторичные молекулярные продукты ПОЛ), а также ТБК-активных продуктов пероксидации (продуктов, взаимодействующих с 2-тиобарбитуровой кислотой).
О состоянии антиоксидантной системы можно судить по величине показателя антиокислительной активности сыворотки крови, активности ее ферментативного звена (в частности, супероксиддисмутазы – СОД). Кроме того, о снижении антиокислительной защиты могут свидетельствовать низкие уровни токоферола, ретинола и аскорбата. Оксидативный стресс – один из универсальных механизмов развития многих патологических состояний, в том числе пролиферативных заболеваний, и коррекция антиоксидантной недостаточности рассматривается как патогенетически оправданный метод терапии [2]. В связи с этим представляется перспективным изучение антиоксидантных свойств лекарственных средств растительного происхождения. В некоторых исследованиях [6] была показана антиоксидантная активность растений рода Vitex, к которому принадлежит Vitex agnus castus – основной компонент препарата Мастодинон, который зарегистрирован в России для лечения больных мастопатией.
Вышеизложенное определило цель исследования: установить характер изменений параметров пероксидации липидов и показателей антиоксидантной защиты, а также оценить динамику масталгии при применении растительного препарата Мастодинон у пациенток с диффузной мастопатией.
Материал и методы исследования
В исследовании принимали участие 43 пациентки с диффузной мастопатией, средний возраст которых составил 38,83±1,85 года.
Дизайн исследования
Проспективное нерандомизированное сравнительное исследование в параллельных группах. Критериями включения пациентов в исследование являлись: репродуктивный возраст (от 18 до 45 лет), наличие диффузной мастопатии, отсутствие узловой мастопатии (все пациентки были проконсультированы маммологом), злокачественных новообразований, декомпенсированных психических, неврологических, сердечно-сосудистых, эндокринных заболеваний средней и тяжелой степеней тяжести, инфекционных болезней, острых заболеваний желудочно-кишечного тракта и мочевыделительной системы, а также обострений хронических заболеваний.
В основную группу, в которой применяли растительный препарат Мастодинон в виде монотерапии по 1 табл. 2 раза в сут. в течение 3 мес., вошли 30 пациенток. Группу контроля составили 13 пациенток, отказавшихся от лечения. Группы были сопоставимы по возрасту (38,8+1,85 и 38,6±1,32 года соответственно), анамнезу и клиническим проявлениям диффузной мастопатии (р>0,05).
В работе были использованы общеклинические, инструментальные, лабораторные методы исследования.
Интенсивность боли оценивалась пациентками при помощи визуально-аналоговой шкалы (ВАШ) [5] за 3 дня до начала менструации. Шкала имела длину 100 мм, где отсутствие боли соответствовало 0 мм, «невыносимая боль» – 100 мм. Интенсивность боли интерпретировалась следующим образом: до 30 мм – слабая, от 30 мм до 60 мм включительно – умеренная, более 60 мм – сильная.
Ультразвуковое исследование молочных желез проводили с использованием аппаратов Toshiba 140A и 340A (Япония).
Диеновые конъюгаты (ДК), кетодиены (КД) и сопряженные триены (СТ) определяли спектрофотометрически на аппарате СФ-56.
Содержание КД и СТ выражали в условных единицах (у. е.), ДК – в мкмоль/л.
ТБК-активные продукты пероксидации липидов определяли методом спектрофлуорофотометрии после нагревания пробы в кислой среде и связывания образующегося при этом малонового диальдегида (МДА) с тиобарбитуровой кислотой (ТБК), что приводит к формированию окрашенного комплекса.
Интенсивность флуоресценции регистрировали на спектрофлуорофотометре Shimadzu RF-1501.
Концентрацию МДА выражали в мкмоль/л.
Определение активности СОД проводили на спектрофлуорофотометре Shimadzu (RF-1501) при l=320 нм. Активность СОД выражали в у. е.
Антиокислительную активность (АОА) сыворотки крови определяли на спектрофотометре СФ-56 и выражали в у. е. оптической плотности, при исследовании ее использовали модельную систему, представляющую собой суспензию липопротеидов желтка куриных яиц.
 Определение a-токоферола и ретинола проводили флуориметрически, в качестве внешнего стандарта использовали D,L-a-токоферол фирмы «Serva» и Аll-trans-retinol фирмы «Sigma».
Определение a-токоферола и ретинола проводили флуориметрически, в качестве внешнего стандарта использовали D,L-a-токоферол фирмы «Serva» и Аll-trans-retinol фирмы «Sigma».
Содержание a-токоферола и ретинола выражали в мкмоль/л.
Определение аскорбиновой кислоты проводили спектрофотометрическим методом (при длине волны 520 нм), концентрацию аскорбиновой кислоты выражали в мкмоль/л.
Измерения восстановленного и окисленного глутатиона проводили на спектрофлуорофотометре Shimadzu (RF-1501) при lеx=350 нм и lеm=420 нм.
Методы статистического анализа
Для сравнения качественных показателей в несвязанных выборках применялся критерий c2 или точный критерий Фишера, в связанных выборках использован критерий Мак-Немара. При оценке значимости различий количественных показателей в несвязанных выборках использован критерий Мана-Уитни, в связанных – Уилкоксона. Различия считали статистически значимыми при р<0,05.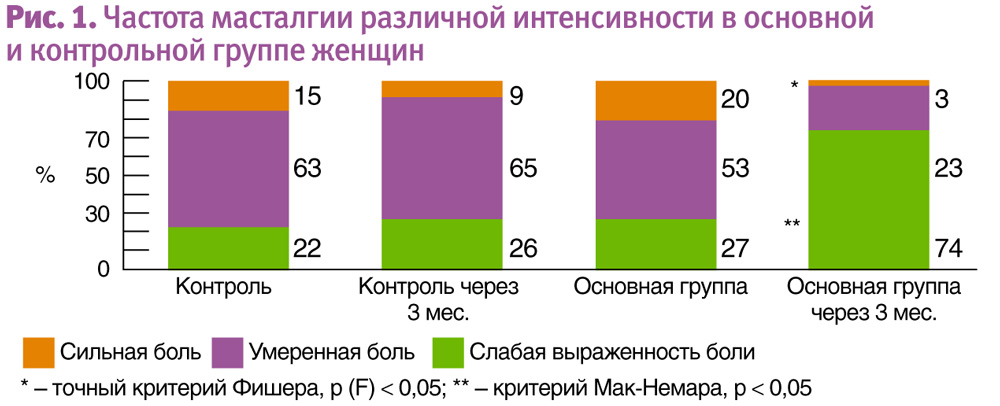
В работе соблюдались этические принципы, предъявляемые Хельсинской Декларацией Всемирной медицинской ассоциации (World Medical Association Declaration of Helsinki, 1964, 2000). Все пациентки до включения в исследование подписывали информированное согласие. Исследование было одобрено локальным этическим комитетом Научного центра проблем здоровья семьи и репродукции человека.
Результаты исследования
При динамической оценке частоты и интенсивности масталгии в основной и контрольной группах женщин были получены следующие результаты: в группе женщин, которые принимали Мастодинон в течение 3 мес., статистически значимо уменьшилась частота выраженной масталгии с закономерным возрастанием регистрации слабо выраженной боли. В группе контроля существенных различий зарегистрировано не было (см. рис. 1).
При количественной оценке исходных показателей боли, значимых различий в основной и контрольной группах не обнаружено, а в динамике (через 3 мес. терапии) существенные изменения отмечены только в основной группе женщин (табл. 1). Полученные результаты согласуются с данными исследований [4, 8], свидетельствующими о клинической эффективности препаратов, содержащих экстракт Vitex Agnus Castus, при диффузной мастопатии.
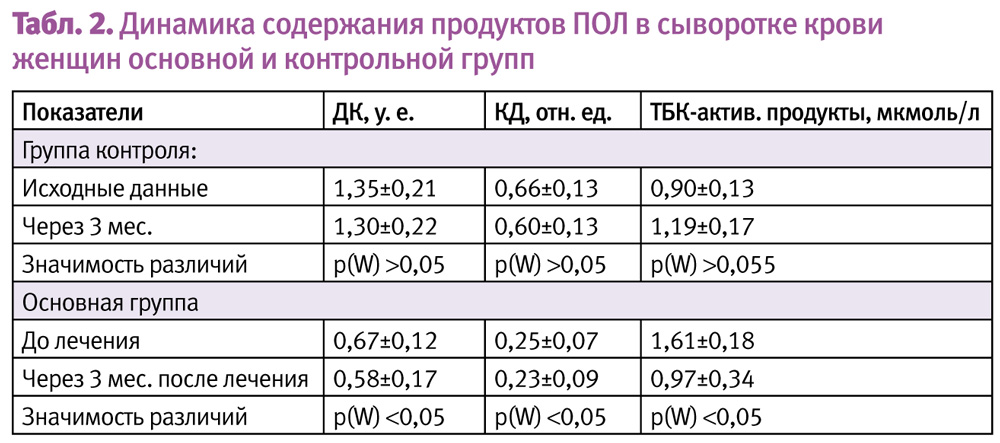 В основной и контрольной группах женщин определяли продукты ПОЛ и ряд антиоксидантов. Как видно из табл. 2, при применении в течение 3 мес. Мастодинона отмечено статистически значимое снижение концентраций как ДК, так и КД и ТБК-активных продуктов ПОЛ. В контрольной группе значимых различий не отмечено.
В основной и контрольной группах женщин определяли продукты ПОЛ и ряд антиоксидантов. Как видно из табл. 2, при применении в течение 3 мес. Мастодинона отмечено статистически значимое снижение концентраций как ДК, так и КД и ТБК-активных продуктов ПОЛ. В контрольной группе значимых различий не отмечено.
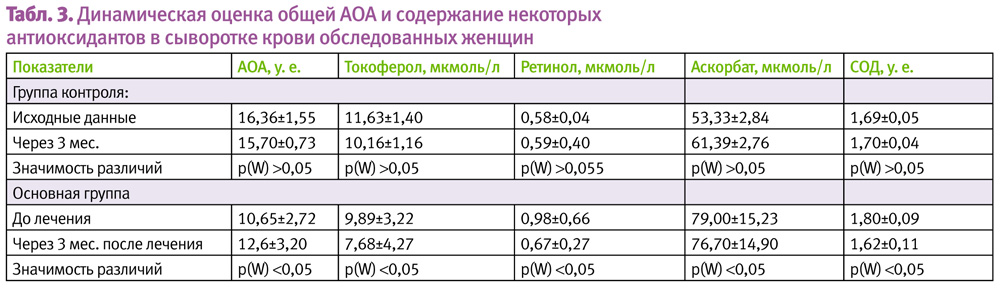
Одновременно в основной группе в отличие от контрольной в динамике наблюдалось увеличение АОА сыворотки крови (табл. 3).
При этом уровень жирорастворимых витаминов (ретинола, токоферола), а также содержание аскорбата и активность СОД у пациенток основной группы незначительно (в пределах референтных значений) снижались.
В то же время у пациенток, получавших Мастодинон, в динамике лечения зарегистрировано снижение соотношения окисленного и восстановленного глутатиона с 1,12±0,06 до 0,99±0,41 (p(W)<0,05), что, по-видимому, и определило увеличение общей АОА сыворотки крови на фоне применения Мастодинона.
Заключение
При использовании у женщин с диффузной мастопатией в течение 3 мес. растительного препарата Мастодинон в отличие от группы контроля отмечено значимое уменьшение проявлений болевого синдрома по ВАШ с существенным уменьшением частоты выраженной масталгии.
Положительная динамика клинических симптомов мастопатии в основной группе женщин ассоциирована с уменьшением содержания в сыворотке крови продуктов ПОЛ (ДК, КД и ТБК-активных продуктов пероксидации) на фоне снижения соотношения окисленного и восстановленного глутатиона и увеличения общей АОА сыворотки крови. В группе контроля существенных изменений процессов пероксидации липидов и состояния антиоксидантной системы не зарегистрировано.
Полученные результаты дают основание для дальнейшего изучения антиоксидантных свойств растительного препарата Мастодинон, которые, наряду с другими механизмами, могут обусловливать его клиническую эффективность при диффузной мастопатии.
По материалам журнала Акушерство и гинекология №8/2012.
Детальніше
СУЧАСНІ ПОГЛЯДИ НА ПАТОГЕНЕЗ ПЕРЕДЧАСНОЇ ПОЛОГОВОЇ ДІЯЛЬНОСТІ (ЧАСТИНА 1)
 Материнський організм є зовнішнім середовищем для ембріону, що розвивається, тому стан здоров'я матері закладає сценарій здоров'я плода на все життя.
Материнський організм є зовнішнім середовищем для ембріону, що розвивається, тому стан здоров'я матері закладає сценарій здоров'я плода на все життя.
За даними A. Beverly (2004), до 25% передчасних розроджень є індукованими за показаннями з боку матері або плода, 30% зумовлені передчасним розривом плодових оболонок. Понад половині всіх ПП передує стадія хибних перейм, коли скорочення матки призводять до структурних, але зворотних змін шийки матки, не відбувається розриву плодових облонок та порушення стану плода. На цій стадії можливим та ефективним є проведення токолітичної терапії, спрямованої на пригнічення передчасної скоротливої діяльності матки. Водночас S. Liong et al. (2013) підкреслюють, що значна частина ПП відбувається на тлі сприятливого та неускладненого перебігу вагітності.
Чинники ризику та маркери прогнозування передчасних пологів
ПП мають багато загальновідомих чинників ризику, до яких належать соціальні фактори, фактори соматичного та акушерського анамнезу, інфекційний процес, аутоімунні розлади, істміко-цервікальна недостатність.
Розроблено численні прогностичні маркери ПП, визначенням яких можна виділити вагітних високого ризику ще до появи клінічних проявів передчасної пологової діяльності. До таких маркерів належать амбулаторне вивчення та реєстрація скоротливої діяльності матки, концентрація естріолу в плазмі, сечі, слині, вміст муцину-16 тощо, виявлення у вагінальних виділеннях фетального фібронектину. Проте значення ЗПП для рівня ранньої неонатальної смертності та стану здоров'я новонароджених вимагають вивчення їх патогенезу та діагностичних маркерів.
Одним із новітніх маркерів прогнозування ПП є сироваткова концентрація муцину-16. 1999 року Tayyar M. et Tutus A. вперше опублікували дані про недоцільність визначення біохімічних маркерів раку яєчників при вагітності через значне спотворення їх значень гестаційними цитокіновими змінами.
Зростання концентрації сполуки, відомої в лабораторній діагностиці як СА-125 – онкомаркер яєчників, є ознакою фізіологічного перебігу вагітності, оскільки основним місцем його утворення є ендотеліальні клітини, кількість яких прогресивно збільшується з гестацією (Mazor M., 2006).
Натомість запропоновано розглядати муцин-16 як маркер неоангеогенезу, зростання концентрації якого вказує на позитивний прогноз вагітності. Так, Y. Xie et al. (2014) проаналізували можливість застосування комбінації даних концентрації муцину-16 та ультразвукових характеристик жовтого тіла для визначення прогнозу вагітності. Чутливість такого тесту склала 81,1%, за умови зниженого вмісту муцину-16 на ранніх термінах вагітності високим є ризик її переривання у першому триместрі.
Про роль запалення як типового біологічного процесу в прогресі пологової діяльності свідчать останні відомості в галузі молекулярної генетики. Виділено специфічний ген S100A9 із локалізацією в імунокомпетентних клітинах та ендотеліоцитах та передбачено його значення в якості фактора хемотаксису в стромі шийки матки. Скупчення лейкоцитів та макрофагів – клітин із здатністю продукувати ПГ в цервікальній стромі виявлено як при ПП, так і при фізіологічних пологах [5].
Незаперечним етіологічним чинником ПП є інфекційний процес, локалізований в хоріоні або органах репродуктивної системи. Так, статистичні дослідження Klein L. (2005) показали, що половина всіх ПП є зумовленою саме інфекційним запальним процессом. M. K. Campbell et al. (2005), аналізуючи когортне дослідження, присвячене прогностичним чинникам ПП в термінах 22–36 тижнів, з'ясували, що у термінах 28–36 тижнів такими маркерами є зниження концентрації материнського адренокортикотропного та кортикотропін рилізинг-гормонів. У термінах 22–27 тижнів найбільш вагомим прогностичним чинником автори вважають лейкоцитоз периферійної крові, пояснюючи це роллю інфекції у походженні передчасної пологової діяльності у ці терміни. R. Mehta (2006), проаналізувавши залежність стану новонароджених від патологічних змін у плаценті, дійшов висновку, що у термінах 22–27 тижнів у плацентах домінують ознаки хоріоамніоніту, а після 28 тижнів – ознаки порушеного плацентарного кровообігу (тромби, фібринові відкладення).
- Vasheghani et al. (2007) виявили підвищену концентрацію ферритину в цервікальному слизі у вагітних, у яких в подальшому відбулись ПП. Враховуючи найбільш виражену залежність між вмістом ферритину в цервікальному слизі та розвитком спонтанних ПП в термінах 22–24 тижні, автори пропонують застосування цього результату в якості додаткового предиктора ЗПП.
Антифосфоліпідний синдром та його вплив на перебіг вагітності
Одним із сучасних пояснень багатьох ускладнень вагітності розглядають антифосфоліпідний синдром (АФС). АФС – мультисистемне захворювання, якому властива циркуляція антифосфоліпідних антитіл (АФА), артеріальні та/або венозні тромбози, тромбоцитопенія та звичне невиношування вагітності [10].
Вперше клінічні дані про зв'язок АФА та тромбозів було сформульовано в 50-х роках ХХ сторіччя, а вже в 70-х роках було описано асоційований із АФА механізм невиношування вагітності [11]. Тривалий час симптомокомплекс мав паралельну назву синдрома G. Hughes, який разом із співавторами вперше описав його 1986 року [10].
2002 року в рамках Міжнародної конференції в м. Терміна (Італія), АФС надано статус системного процесу, оскільки в його основі лежить утворення аутоантитіл до фосфоліпідних детермінант більшості органів та тканин. На думку деяких дослідників, АФС є більш системним захворюванням, ніж системний червоний вовчак [12].
За даними Е. Л. Насонова (2004), розповсюдженість АФС у популяції коливається від 0 до 14%, що відповідає виявленню АФА серед здорових людей, високий титр антитіл виявляється в 0,2%. Показник зростає серед хворих на запальні, аутоімунні та інфекційні захворювання, онкологічних хворих, на фоні прийому лікарських препаратів, тобто у випадках вторинного АФС. Зв’язок між виявленням ВА та звичними втратами вагітності вперше описаний 1954 року J. Beamont. Частота цього синдрому у жінок із ПП складає 10–25%. (V. Branch, 2003).
На сьогодні існує багато досліджень, спрямованих на розкриття патофізіологічних механізмів переривання вагітності, обумовленого циркуляцією АФА [15, 16]. Більшість теорій сходяться на тому, що АФА зв’язуються з мембранними фосфоліпідами тромбоцитів та ендотеліальних клітин, що призводить до підвищеної агрегації тромбоцитів, зменшення ендогенної антикоагулянтної активності, зниження фібринолізу [17].
Важливу роль у патогенезі тромбозів при АФС надають кофактору з'єднання АФА із відповідним фосфоліпідом – b2 глікопротеїну (b2ГП). Саме залежність від b2ГП відрізняє ідіопатичні (первинні) АФА від вторинних, що можуть мати інфекційне походження, ускладнювати онкологічні захворювання тощо [18]. b2ГП є потужною противагою реалізації процесів тромбоутворення, саме тому його зв'язування із антитілами блокуючої дії поглиблює гіперкоагуляцію (О. Б. Яременко, 2007).
Унікальна система комплексного функціонування трьох ендотеліальних поверхонь – ендотелію судин матки, ендотелію трофобласту та фетального ендотелію – створює умови для реалізації АФС та прояву тромботичних розладів.
У І триместрі вагітності мають місце викидні та загибель морфологічно нормального плода, в патогенезі яких на перше місце виходять тромбоз плацентарних судин, фібриноїдний некроз, їхній гострий атероз, наслідком чого стає різке виражене зниження кровотоку в плаценті [20].
Цим пояснюють також невдалі спроби ектстракорпорального запліднення у жінок із АФА [21].
У хворих із звичним невиношуванням вагітності виявляють високу концентрацію ß2-ГП на поверхні трофобласту, що узгоджується із кофакторною теорією патогенезу АФС.
Саме з циркуляцією АФА пов'язують випадки внутрішньоутробної загибелі морфологічно нормального плода [22], ПВНРП [23]. C. Clark at al. (2010), вивчаючи перебіг вагітності у 86 пацієнток з підтвердженим серологічно діагнозом АФС, виявили, що у 24% із них пологи відбулись до 37 гестаційних тижнів, для порівняння, серед групи контролю частота ПП склала 9,8%.
Останнім часом науковці схильні розширювати можливості негативної дії АФА на вагітність. Так, Mulla M. et al. (2009) показали значне зростання титру прозапальних ІЛ у пацієнток із втратою вагітності в першому триместрі, підкресливши можливу патогенетичну роль цього чинника у ґенезі невиношування.
Тромбофілічні стани та їх значення в ґенезі акушерських ускладнень
Ролі вроджених тромбофілічних станів у ґенезі акушерських ускладнень свого часу було присвячено надзвичайно багато публікацій. Так, С. Б. Чечуга (2009) у своїх дослідженнях поширеності гіпергомоцистеїнемії в акушерській практиці, з'ясувала, що частота вказаної тромбофілії у жінок із ПП досягає 40%, часто поєднуючись із АФС. Серед вроджених тромбофілій гіпергомоцистеїнемія є найбільш поширеною, головні патологічні зрушення при ній спостерігаються в сфері обміну метіоніну.
Амінокислота метіонін є важливим компонентом білкового метаболізму ссавців, оскільки ії активна форма – S-аденозилметіонін – є донором метильної групи у сотні реакцій трансметилювання, кінцевим продуктом якої є гомоцистеїн. Відновлення гомоцистеїну до метіоніну каталізується ферментом метіонінсинтетазою, що є кобаламінзалежним ензимом, відновлення активності якого здійснюється ферментом 5-метилгідрофолат-гомоцистеїнметитрансферазредуктазою (MTRR).
Поліморфізм цього гену вивчено досить детально – від клінічно німих мутацій до найбільш поширеного варіанту, коли в 66 положенні нуклеотидний залишок аденін є заміненим на гуанін.
Саме ця мутація призводить до функціональної неповноцінності гену – недостатньо активного відновлення метіонінтрансферази, наслідком чого є накопичення в плазмі неметильованого гомоцистеїну. Останній чинить на організм токсичний вплив, що в першу чергу реалізується на поверхні ендотелію.
Ушкодження нормальної структури мембран ендотелію призводить до активації системи коагуляції та реалізації власне того патогенетичного механізму, що і визначає гіперкоагуляційні прояви. Крім того, підвищена концентрація гомоцистеїну порушує метилювання, що відбувається у процесі неоангіогенезу, впливаючи на імплантацію, інвазію цитотрофобласту, створюючи передумови до плацентарної дисфункції та пізнього гестозу [27].
Слід зазначити, що значне підвищення рівня гомоцистеїну в сироватці (понад 500 µМ) реєструють при дефекті ферменту цистатіонін-b-синтетази, монозиготна форма якої трапляється вкрай рідко. Гіпергомоцистеїнемія, що є наслідком дефекту ферментів трансметилювання, є вторинною та значення її не перевищують 50 µМ, часом її навіть важко визначити на рівні цілого організму, проте вже концентрація амінокислоти 15–20 µМ є визнаним незалежним чинником ризику серцево-судинних захворювань [28].
Маючи невелику молекулярну масу, гомоцистеїн, як і інші амінокислоти, долає плацентарний бар'єр, спричинює розлади метилювання центромер хромосом, що порушує їх розходження у процесі мітозу. Накопичення в ембріоні клітин з неповноцінним хромосомним набором призводить до активації апоптозу та загибелі плода [29].
Крім безпосередньої ушкоджуючої дії на стінку судини, гомоцистеїн та його неприродно високі концентрації чинять вплив власне на утворення ниток фібрину, зв'язуючись із тріольними групами певних амінокислот.
У результаті згусток фібрину містить більш короткі та, водночас, більш розгалужені нитки, що робить структуру більш компактною та більш стійкою до дії фібринолітичних чинників (Lauricella A et al., 2002).
Саме такою, прокоагуляційною дією гомоцистеїну, тривалий час намагались пояснити підвищення ризику ішемічної хвороби серця та інших форм атеросклерозу у носіїв мутантних генів, що визначають обмін метіоніну.
Втім, останнім часом було показано, що дію гомоцистеїну не варто спрощувати. Так, Y. Asunama et al. (2008) показали, що ізольовано від впливу на процеси зсідання крові, високий рівень амінокислоти чинить стимулюючий вплив на синтез клітинами ендотелію прозапальних цитокінів. З проміж інших, таку дію було показано стосовно ІЛ-8 та ІЛ-6 [32]. A. Desai et al. (2001) в експерименті показали, що культура смугастих клітин м'язевої стінки при дії на неї гомоцистеїну в концентрації 250 µМ експресує велику кількість ІЛ-8, активність цитокіну та тривалість виділення була значно більшою, ніж при дії на таку ж культуру визнаних стимуляторів прозапальної відповіді – ІЛ-1, ліпополісахариду бактеріальної клітинної стінки тощо.
Чинники і прогностичні можливості генних мутацій
За даними A. Wilson et al. (1999), як гомозиготна, так і гетерозиготна форма мутантного гену MTRR асоційована з вірогідним зростанням ризику spina bifida. P. Bosco et al. (2003) проаналізували вплив мутації 66 A-G на ризик народження у жінки дитини із трисомією 21. Після виключення впливу вікового та інших мутагенних чинників авторами встановлено, що відносний ризик формування синдрому Дауна є 6,7 у гомозигот та 3,5 у гетерозигот.
- Engel et al. (2006) доповіли про зростання відносного ризику ПП до 2,0 у білих жінок, що є носіями мутантного гену 66 A-G MTRR, у чорних жінок такої залежності виявлено не було.
Ще одним ферментом, залученим до процесів метилювання та фолатного обміну, належить метилентетрагідрофолатредуктаза (MTHFR) – ензим, що каталізує перетворення 5,10-метилентетрагідрофолата в 5-метилгідрофолат. Останній виступає одним із косубстратів у реакції перетворення гомоцистеїну на метіонін. Описано понад 100 можливих мутацій гену, що кодує вказаний фермент, втім серед найбільш значимих – заміна цитозину у положенні 677 на тимін.
За даними S. Hustard et al. (2007), середні концентрації гомоцистеїну внаслідок зниженої функціональної активності ферменту (він за такої мутації набуває термолабільності) зростають до 10,4 µM у гетерозигот та 13,3 µM – у гомозигот. Така мутація є не найбільш поширеною внаслідок незначної (власне нефатальної) її реалізації – протягом внутрішньоутробного розвитку не відбувається елімінації гомозиготних форм. За даними R. Mogk et al. (2000), 7% новонароджених є гомозиготами за цим дефектним геном.
Крім значного зростання частоти вад розвитку – незрощення верхньої щелепи, дефектів нервової трубки (Reyes-Engel A. et al, 2002), гомо- та гетерозиготний стан мутантного гену асоціюються із підвищеним ризиком серцево-судинних захворювань, тромботичних ускладнень (P. Kelly et al., 2002) та навіть шизофренії (J. Muntjewerff et al., 2006).
Дискутабельними є результати широкомасштабних досліджень стосовно частоти прееклампсії у разі носійства даного гену – S. Sohda et al. ще 1997 року опублікували дані про зростання ризику такого ускладнення та збільшення його тяжкості, натомість G. Kobashi (2000) надав протилежні дані. Щоправда, останнє дослідження було проведено в Японії, де досить істотним є вплив особливостей харчування на розвиток пізнього гестозу, а саме – високий вміст поліненасичених жирних кислот у раціоні, мембранопротекторна дія яких відома, та самі автори говорять про неможливість екстраполяції цих даних на інші популяції.
Ще одним варіантом поліморфізму гену ферменту MTFHR є заміна цитозину на аденін у положенні 1298. Саме за такої мутації найбільш вираженим є ризик тромботичних ускладнень. Вивчаючи поширеність різних мутацій генів фолатного обміну серед пацієнтів молодого віку із тромботичними ускладненнями, K. Ozturk et al. (2012) виявили, що понад 60% із них є носіями саме такої мутації у гомо-чи геторозиготній формі.
Численними дослідженнями, як багатоцентровими, так і когортними, показано зростання ризику невиношування за носійства такої мутації.
Одні автори наголошують на майже трикратному зростанні ризику мимовільного викидня у разі носійства однієї із описаних мутацій MTFHR, незалежно від гомо- або гетерозиготної форми.
Дослідники пропонують використовувати рівень сироваткового гомоцистеїну для прогнозування ризику невиношування [42]. Проте абсолютно маловивченим залишається питання ролі поліморфізму генів фолатного обміну в генезі передчасної пологової діяльності. Доступні дані протирічать один одному, оскільки передчасна скоротлива активність матки є багатокомпонентним процесом, реалізацію якого не можна пояснити лише діями генної мутації.
Загалом друга декада ХХІ сторіччя означилась пошуком молекулярно-генетичних чинників ризику ПП. Так, X. Wing et al. у своєму огляді 2001 року лише перелічили гени, які, за різними літературними джерелами, є асоційованими із спонтанним передчасним розродженням. Серед них – поліморфізм генів ензимів детоксикації – глутатіон-S-трансфераз – родини ферментів. Ця група ензимів відіграє важливу роль у процесах зв'язування гідрофобних сполук із глутатіоном, що призводить до інактивації токсичних властивостей продуктів обміну.
На підставі біохімічних, імунологічних та структурних властивостей, групу ферментів поділяють на класи, що позначають грецькими літерами. Серед найбільш поширених та клінічно значимих класів – q-глутатіон-S-трансфераза (GSTT), µ-глутатіон-S-трансфераза (GSTM) та w-глутатіон-S-трансфераза (GSTP) [44].
Головна функція ферментів полягає у зв'язуванні із глутатіоном субстанцій – продуктів І фази антиоксидантного стресу, що регулюється родиною ензимів цитохром-450 [45]. Значне посилення кровоплину та активація обмінних процесів, що є властивими вагітності, значно посилюють навантаження на родину глутатіон-трансфераз, проявляючи їх часткову функціональну неспроможність внаслідок поліморфізму генів, що їх кодують.
Серед найбільш вивчених мутацій – делеція генів GSTT та GSTM, що може бути у гомозиготному та гетерозиготному стані, а також мутація гену GSTP, що полягає в заміщенні аденозину на гуанін у положенні 313. Частота поліморфізму вказаних мутацій в популяції сягає, за даними A. Sharma et al. (2013), 15–16% разом у гомо- та гетерозиготній форм.
Враховуючи участь процесу відновлення глутатіону в більшості біохімічних реакцій організму, неважко пояснити вивчення поліморфізму генів глутатіон-S-трансферази у різних галузях медицини.
Так, Л. А. Сивак та співавт. (2013), вивчивши молекулярно-генетичні механізми хіміотерапії раку грудної залози, показали зростання токсичності протипухлинних препаратів у пацієнток із поліморфізмом гену GSTP. Показано роль неспроможності ферментів цієї родини у схильності до розвитку лімфолейкозу [47], токсичного ураження печінки при застосуванні нестероїдних протизапальних засобів, у тому числі – ацетилсаліцилової кислоти [48] тощо.
Що стосується ролі поліморфізму генів вказаної родини у ґенезі передчасної пологової діяльності, то цьому питанню присвячено багато досліджень, втім жодне із них не надає конкретного механізму передчасної скоротливої активності матки, ПРПО та не вираховує можливості застосування цього чинника в якості прогностичного маркера. Це може бути пов'язано і з відмінностями в даних, так M. Quinzio et al. (2008) просто перераховують мутантну форму GSTP та нульову форму GSTM серед виявлених ними генетичних прогностичних чинників ПП. S. Liong et al. (2013) обчислили відносний ризик ПП за умови носійства виключно GSTP 313 A-G як 0,8, проте не слід забувати про існування у кожної вагітної унікальної комбінації чинників генетичного походження, що можуть вплинути на несприятливий перебіг гестації.
З огляду на роль поліморфізму генів в патогенезі ПП на значну увагу заслуговують також повідомлення про більшу частоту та тяжкість розвитку БЛД у недоношених новонароджених, що є носіями вказаних генів.
Розглядають роль і інших генних мутацій в якості чинника ризику передчасної пологової діяльності. Так, K. Ryckmann et al. (2010), вивчивши геномні моделі прогнозування ПП, показали, що найбільш продуктивними у цьому сенсі є мутація гену рецептора простагландина E3 (PTGER3) для матері та мутація гену параоксидази 1 для новонародженого.
Повний перелік літератури знаходиться у редакції.
Продовження у наступному номері.
Детальніше

СИЛА ПРИРОДЫ
21–24 октября в Праге (Чехия) состоялся 11 Конгресс Европейского Общества Гинекологии (Congress of the European Society of Gynecology), в котором приняли участие, по официальным данным, около 2500 делегатов из различных стран и континентов – Европы, Америки, Австралии, Великобритании, Ближнего Востока, Азии
Конгресс был посвящен актуальным вопросам всех областей репродуктивного здоровья: проблемам материнской и перинатальной заболеваемости и смертности, невынашиванию, преждевременным родам, ведению беременности на фоне эндокринопатий. Были представлены доклады по вопросам гинекологической эндокринологии, менопаузы; по репродуктивным технологиям, в том числе современным методам оперативного лечения. Проводились секционные заседания по современным методам контрацепции, сексуальному здоровью, детской и подростковой гинекологии.
Отдельно проходила секция с докладами, посвященными онкологическим рискам: диагностике и профилактике фоновых состояний, рассматривались редкие клинические случаи онкопатологии женских репродуктивных органов.
На секционном заседании, посвященном проблемам ранней диагностики и профилактики онкологических заболеваний, были представлены доклады по проблеме диагностики вируса папилломы человека (ВПЧ), ведению пациентов с фоновыми заболеваниями, ведущей причиной которых признано наличие ВПЧ.
Докладчик из Великобритании Суварна Махаваркар (кафедра акушерства и гинекологии Royal Devon and Exeter Hospital) представила данные о корреляции «пограничных» результатов цитологических исследований шейки матки с тяжелыми формами дисплазий. Пациенткам проводилось исследование на наличие ВПЧ, кольпоскопическое исследование, биопсия при неблагоприятных результатах кольпоскопии, а также петлевая электроэксцизия шейки матки в случаях дисплазий средней и тяжелой степени. По данным британского госпиталя, дисплазии тяжелой степени встречаются только у 20% женщин, имевших «пограничные» результаты цитологических исследований шейки матки. Однако, подобный контингент заслуживает особого наблюдения, проведения кольпоскопических исследований, обследования на наличие ВПЧ, биопсии шейки матки при сомнительных результатах кольпоскопии.
Доклад группы авторов из Франции послужил дополнительным доказательством роли ВПЧ в онкопатологии кишечника, наряду с дисплазиями шейки матки у женщин. Исследование выполнено совместно Институтом Пастера, университетом Сорбонна, госпиталем Mourier, отделением проктологии Groupe Hospitalier Diaconesses (Париж). Под наблюдением находились ВИЧ-инфицированные женщины, у которых, на фоне иммуносупрессивного состояния, развиваются диспластические процессы шейки матки, вызванные вирусом папилломы человека, а также часто встречается онкопатология кишечника.
 Докладчик Изабель Хеард (Isabelle Heard, Институт Пастера) представила данные об обследовании женщин, имевших клинические признаки дисплазий шейки матки, на наличие ВПЧ в мазках не только с поверхности шейки матки, но также из прямой кишки. Пациентки, имевшие положительные результаты ВПЧ из кишечника, направлялись на обследование к проктологу. Выявлена высокая степень корреляции поражений шейки матки, вызванных ВПЧ 16 типа, и дисплазий слизистой кишечника средней и тяжелой степени, у одной из 171 обследованных женщин обнаружен рак прямой кишки. Рекомендовано всех женщин с дисплазиями шейки матки обследовать на наличие дисплазий кишечника, вируса папилломы человека в мазках из слизистой кишечника, проводить цитологическое исследование слизистой кишечника, направлять на консультацию к проктологу.
Докладчик Изабель Хеард (Isabelle Heard, Институт Пастера) представила данные об обследовании женщин, имевших клинические признаки дисплазий шейки матки, на наличие ВПЧ в мазках не только с поверхности шейки матки, но также из прямой кишки. Пациентки, имевшие положительные результаты ВПЧ из кишечника, направлялись на обследование к проктологу. Выявлена высокая степень корреляции поражений шейки матки, вызванных ВПЧ 16 типа, и дисплазий слизистой кишечника средней и тяжелой степени, у одной из 171 обследованных женщин обнаружен рак прямой кишки. Рекомендовано всех женщин с дисплазиями шейки матки обследовать на наличие дисплазий кишечника, вируса папилломы человека в мазках из слизистой кишечника, проводить цитологическое исследование слизистой кишечника, направлять на консультацию к проктологу.
Вопросам профилактики и терапии диспластических состояний женской репродуктивной системы на фоне вирусной инфекции был посвящен доклад доцента кафедры перинатологии, акушерства и гинекологии ХМАПО Виктории Владимировны Бобрицкой «Онкопротекторная терапия заболеваний, ассоциированных с ВПЧ и ВПГ».
В докладе была подчеркнута роль папилломавирусной инфекции как причинно-следственной связи предопухолевых заболеваний, в том числе не только женской, но и мужской репродуктивной системы. Вирус простого герпеса (ВПГ) потенцирует диспластические эффекты вируса папилломы, кроме того, вирусные ассоциации являются проявлением иммуносупрессивных состояний организма, что, в свою очередь, может приводить к неблагоприятному онкологическому прогнозу заболеваний. Определяющими факторами являются тип вируса и формы существования (клинические проявления), иммунный статус, генетическая предрасположенность, гормональный статус, прочие инфекции.
Рекомендовано обследование на наличие ВПЧ и ВПГ следующему контингенту женщин:
- Женщины репродуктивного возраста, имеющие субъективные и/или объективные симптомы, связанные с репродуктивным трактом.
- Женщины репродуктивного возраста, у которых цитологически и/или гистологически выявлена цервикальная интраэпителиальная неоплазия II, III степени.
- Женщины репродуктивного возраста, у которых цитологически на протяжении 1 года выявляли цервикальную неоплазию I ст.
- Для контроля качества лечения цервикальной интраэпителиальной неоплазии различной степени, лейкоплакии, псевдоэрозии.
- При кольпоскопической картине гиперкератоза и лейкоплакии.
- При длительно незаживающих эрозиях после ДЭК.
- При наличии полипов шейки матки и их рецидивах.
- При наличии плоских и остроконечных кондилом наружных половых органов.
- При половом контакте с партнером, имеющим кондиломы наружных половых органов.
- Женщинам, имевшим репродуктивные потери.
- В случаях планирования беременности.
- При наличии нескольких половых партнеров.
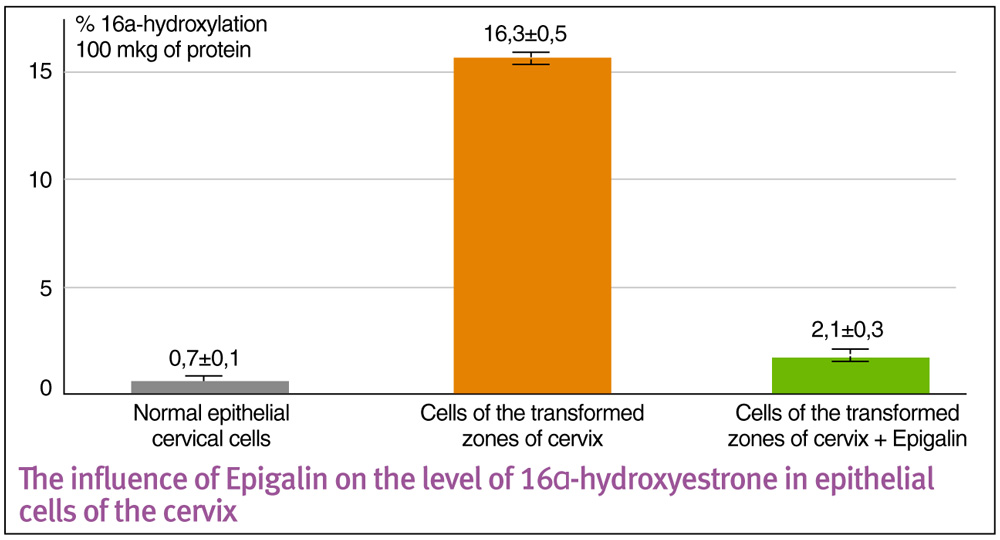
 ДНК вируса внедряется в ДНК клетки, повреждая геном; клетка начинает активно синтезировать белки Е6/Е7, что сопровождается значительной супрессией местного иммунитета. Чрезвычайно важным является соотношение метаболитов эстрадиола: 2-ОНE (2-гидроксиэстрон)/16a-OHE (16-альфа-гидроксиэстрон) как биомаркера развития патологической клеточной пролиферации в эстроген-чувствительных тканях.
ДНК вируса внедряется в ДНК клетки, повреждая геном; клетка начинает активно синтезировать белки Е6/Е7, что сопровождается значительной супрессией местного иммунитета. Чрезвычайно важным является соотношение метаболитов эстрадиола: 2-ОНE (2-гидроксиэстрон)/16a-OHE (16-альфа-гидроксиэстрон) как биомаркера развития патологической клеточной пролиферации в эстроген-чувствительных тканях.
Препаратом выбора с целью онкопротекции может служить сочетание индол-3-карбинола с эпигаллокатехин-3-галлатом (в Украине – препарат Эпигалин®).
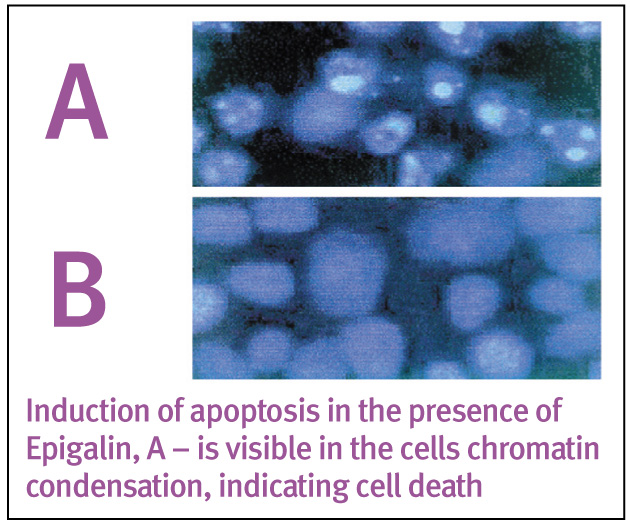
Механизм действия индол-3-карбинола предусматривает блокирование продукции агрессивных метаболитов эстрогенов, нейтрализацию факторов патологического клеточного роста, индукцию апоптоза.
Кроме того, индол-3-карбинол обладает способностью коррекции генетического дефекта синтеза белка BRCA1 и других белков-супрессоров опухолевого роста. Следует отметить, что эффект действия индол-3-карбинола является дозозависимым – не менее 400 мг в сутки, а применение данной дозировки в течение 4 недель достоверно снижает содержание канцерогенных метаболитов.
Эпигаллокатехин-3-галлат является индуктором апоптоза, блокирует продукцию провоспалительных цитокинов, угнетает неоангиогенез. Последнее свойство чрезвычайно важно, поскольку в основе патогенеза гиперпластических процессов лежит патологическая васкуляризация, что зачастую является дифференциально-диагностическим признаком развития гиперпластических процессов репродуктивных органов. Суточная доза эпигаллокатехина-3-галлата – не менее 90 мг.
Проводилось исследование результатов терапии клинических проявлений папилломавирусной инфекции (дисплазии шейки матки I–II ст., кондиломы шейки матки, половых органов) в сочетании с герпетической инфекцией с применением индол-3-карбинола 400 мг и эпигаллокатехин-3-галлата 90 мг (Эпигалин® 2 капсулы в сутки) в течение 3 месяцев с пациентками, получавшими только общепринятые схемы терапии.
После электрохирургического удаления патологических образований пациенткам назначался валацикловир по супрессивной схеме (1 г в сутки в 2 приема, до 6 месяцев), местно комплексные фитосуппозитории с гиалуроновой кислотой и индол-3-карбинол в сочетании с эпигаллокатехин-3-галлатом (Эпигалин®), в основной группе – 90 человек – принимали Эпигалин® по 1 капсуле 2 раза в сутки до 6 месяцев. Группа сравнения 35 человек получала аналогичную базисную терапию без индол-3-карбинола с эпигаллокатехином-3-галлатом.
Результаты терапии: в основной группе нормализация иммунного статуса через 2–3 месяца, отсутствие рецидивов герпетических и папилломатозных высыпаний, отсутствие патологических цитологических результатов – дискератоза, койлоцитоза, характерных для папилломавирусной инфекции, отрицательные результаты ПЦР исследования на наличие ВПЧ до 75% через 3 месяца, до 95% – через 6 месяцев.
Кроме того, наблюдалась положительная динамика результатов кольпоскопических исследований – регрессия дисплазии I ст. у 12% пациенток. В то время, как в группе сравнения отрицательные результаты ПЦР ВПЧ через 3 месяца только у 12% пациенток, через 6 месяцев – у 15%, что может быть связано с процессами самоэлиминации ВПЧ. ВПГ в основной группе – отрицательные результаты 45% через 3 мес., и 67% через 6 месяцев, в группе сравнения – соответственно 34% и 52% результатов.
Таким образом, индол-3-карбинол с эпигаллокатехин-3-галлатом (Эпигалин®) является эффективным иммуномодулирующим, онкопротекторным препаратом, который может использоваться в комплекскном лечении клинических и субклинических форм вирусных инфекций, генитальных неоплазий.
Механизмы позитивного влияния препарата на инфектологическую составляющую патологических процессов подлежат дальнейшему изучению, наука не стоит на месте и Украина готова к демонстрации своих достижений на Европейской медицинской арене.
Детальніше
