
МОВА ЕКГ. Доброякісні варіанти чи аномалії, що загрожують життю?
Шановні читачі!
В цьому номері ми започаткували принципово нову для нас рубрику-тренінг.
Мабуть ви погодитесь, що навчатись, розв'язуючи різноманітні задачі, буває набагато цікавіше, ніж слухати лекції та читати статті. У нашій рубриці ви знайдете клінічні завдання з докладними аргуметованими відповідями. І все це буде забезпечено якісними ілюстраціями. Сподіваємось, що рубрика сподобається нашій шановній аудиторії. Будемо вдячні вам за відгуки та пропозиції щодо тематики наступних тренінгів.
.
Упорядник розділу Тіна Бордій
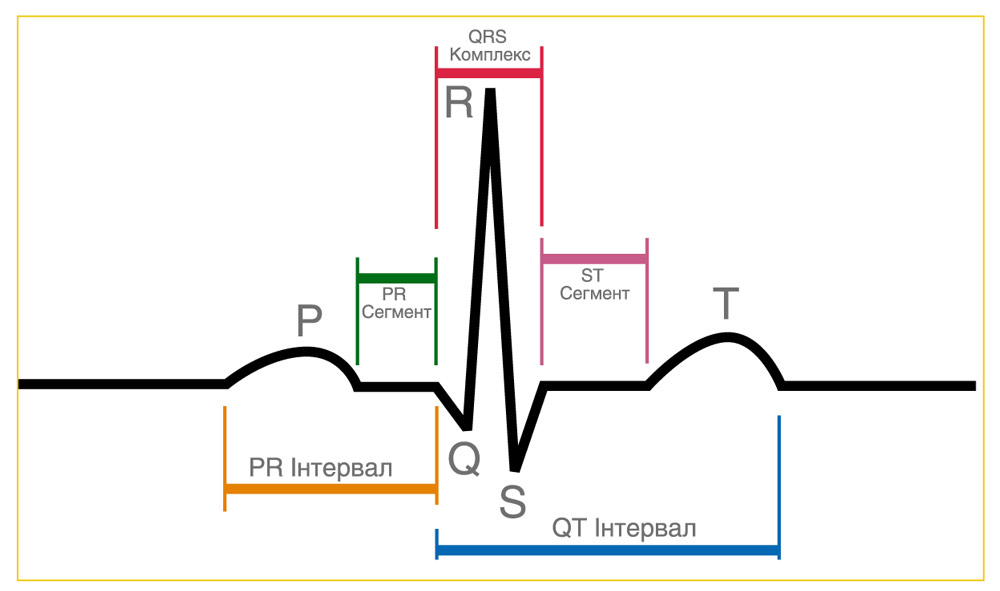 Хоча більшість лікарів знайомі з нормальними межами інтервалів ЕКГ для дорослих, слід нагадати, що у педіатрії нормальні значення можуть відрізнятися. Популяційні дослідження допомогли сформулювати загальноприйняті нормальні значення для дітей різного віку, які можуть бути референсними при тлумаченні ЕКГ. Однак, навіть маючи ці значення, поставити діагноз може бути складно. Варіації ЕКГ зустрічаються у дітей в залежності від віку та статі, проте при більшості патологічних станів вони виходять за межі норми. Подивіться, чи можете ви визначити: ЕКГ у наступних випадках є доброякісними варіантами норми або приводом для занепокоєння?
Хоча більшість лікарів знайомі з нормальними межами інтервалів ЕКГ для дорослих, слід нагадати, що у педіатрії нормальні значення можуть відрізнятися. Популяційні дослідження допомогли сформулювати загальноприйняті нормальні значення для дітей різного віку, які можуть бути референсними при тлумаченні ЕКГ. Однак, навіть маючи ці значення, поставити діагноз може бути складно. Варіації ЕКГ зустрічаються у дітей в залежності від віку та статі, проте при більшості патологічних станів вони виходять за межі норми. Подивіться, чи можете ви визначити: ЕКГ у наступних випадках є доброякісними варіантами норми або приводом для занепокоєння?
Зображення надані Wikimedia Commons.

ДЕФИЦИТ ЖЕЛЕЗА У РЕБЕНКА И ЕГО ИНТЕЛЛЕКТ – ЕСТЬ ЛИ ВЗАИМОСВЯЗЬ? (ЧАСТЬ 2)

Вопросы, беспокоящие родителей
В номере №5 (50) 2014 нашего журнала уважаемые читатели ознакомились с наиболее частыми вопросами, которые возникают у родителей и педагогов о взаимосвязи дефицита железа у детей первых лет жизни с показателями нервно-психического развития. В этой части сообщения приведены ответы на наиболее частые вопросы родителей, педагогов и подростков о влиянии дефицита железа на показатели когнитивных функций, уровень интеллекта, поведенческого развития, взаимосвязи этого состояния с формированием личности школьников
Дефицит железа (ДЖ) остается одной из важнейших проблем здравоохранения во всем мире. Железодефицитное состояние (ЖДС) отмечено у 4–5 млрд. людей на планете, из них около 30% страдают собственно железодефицитной анемией (ЖДА). ЖДА являйся наиболее распространенным заболеванием крови, составляя до 90% всех анемий в детском возрасте.
Длительный ДЖ приводит к задержке физического и нервно-психического развития ребенка, влияет на иммунную систему, ухудшает работу сердечно-сосудистой системы, желудочно-кишечного тракта, работу эндокринных желез, вызывает астеновегетативные проявления, нарушаются процессы тканевого дыхания, что вызывает дистрофические процессы в тканях организма. Но особенно чувствителен к ДЖ мозг ребенка. Прослеживается четкая взаимосвязь ДЖ с показателями когнитивных функций, поведенческими показателями, взаимосвязь с формирование личности школьника.
Интеллект подростка. Есть ли взаимосвязь с дефицитом железа?
Как мы указывали ранее, железо в тканях головного мозга участвует в генерации импульсов в нервных синапсах, в процессах миелинизации нервных волокон, оказывает влияние на функции гипоталамуса. В случае недостатка железа снижается количество и чувствительность допаминовых рецепторов Д2. Это ведет к нарушению метаболизма допамина в нервных синапсах, в результате чего уменьшается стимулирующий эффект на следующую клетку и сокращается количество проходящих импульсов.
Серия экспериментальных исследований ученых США и Канады (A. B. Bruner, et al., 1996; B. Lozoff et al., 2006; K. L. Ward et al., 2007 и др. продемонстрировала, что ДЖ в нейронах сопровождается снижением дофаминергической активности, влияет на процесс передачи нервных импульсов. В итоге, это может привести к изменению поведенческих реакций, познавательных функций, негативно повлиять на способность к обучению и память. Кора головного мозга играет основную роль в таких процессах как внимание, память, перцептивное сознание, мышление, речь. У животных с ДЖ наблюдаются метаболические и структурные изменения в коре головного мозга, которые отвечают за эквиваленты некоторых из указанных функций. В этих же исследованиях было продемонстрировано, что при ДЖ снижается содержание липидов и белков в миелине. Дефекты миелинизации на раннем этапе развития мозга сохраняются во взрослом возрасте, несмотря на последующее восполнение запасов железа.
Особенно чувствительна к ДЖ гиппокамп – центральная структура памяти, отвечающая за опознание, пространственную память, переход из кратковременной памяти в долговременную. В эксперименте на молодых животных было доказано, что эта структура мозга весьма чувствительна к раннему ДЖ.
В большой серии клинических исследований продемонстрирована четкая взаимосвязь ДЖ с показателями когнитивных функций, поведенческими показателями, взаимосвязи этого состояния с формированием личности школьника. Как показали в своих исследованиях R. D. Baker et al. (2010) – даже спустя 5–6 лет после ЖДА, перенесенной в возрасте 12–24 месяцев, у детей отмечается задержка умственного и моторного развития, а также возникают трудности с обучением.
M. Tucker., Н. Н. Sandstead, J. G. Penland et al., (2006) и другие исследователи продемонстрировали, что у школьников, страдающих ЖДА, значительно снижается способность к концентрации внимания, они быстро утомляются, у них снижается индекс интеллекта. Исследователи проанализировали данные 32 исследований с участием 7089 детей (в основном, в странах с низким и средним уровнем дохода). Результаты исследования показали, что у детей с ЖДА, получающих ежедневно препараты железа (как в лечебной, так и в дозе ликвидации латентного ДЖ), были выставлены более высокие оценки их когнитивных функций по сравнению с исходными показателями.
У большой когорты детей, получавших ферротерапию по поводу ЖДА, было проведено девять исследований с участием 2355 детей. Суть исследования: регистрация IQ-баллов у школьников, страдающих ЖДА до начала ферротерапии, на фоне лечения; определение взаимосвязи этого показателя с длительностью терапии препаратами железа; эффективность терапии препаратами двухвалентного и трехвалентного железа (гидроксид-полимальтозного комплекса трехвалентного железа – ГПК-Fe3+). Авторы этих исследований констатировали, что на фоне ферротерапии отмечено повышение IQ, но более позитивные сдвиги были при применении гидроксид-полимальтозного комплекса трехвалентного железа (на 12% выше по сравнению с исходным уровнем). У группы детей, которым проводилась длительная курсовая терапия железом, регистрировались более высокие показатели IQ, чем у детей группы сопоставления, у которых ферротерапия была кратковременной.
Какая терапия железодефицитных анемий у детей школьного возраста является наиболее оптимальной?
Терапия ЖДА и ЖДС у детей различных возрастных групп должна быть комплексной и базироваться на четырех принципах: нормализация режима и питания ребенка; возможная коррекция причины ЖДС; назначение препаратов железа; поддерживающая терапия.
Терапия ЖДА препаратами железа является очень важным этапом лечения. Выбору препарата для коррекции анемии придается особое значение, поскольку длительность лечения может составлять от нескольких недель до многих месяцев. При этом важна не только эффективность препарата железа, но и отсутствие побочных эффектов и осложнений. Актуальна так же приверженность к проводимой терапии.
При проведении терапии ЖДА, используют препараты железа, которые разделены на две группы:
1) ионные железосодержащие препараты (солевые соединения железа);
2) неионные соединения, к которым относятся препараты, представленные гидроксид-полимальтозным комплексом трехвалентного железа.
Характеристика препаратов этих групп, перечень побочных эффектов приведены в І части сообщения («ЗТД №5 (50) 2014).
Главными требованиями, предъявляемыми к препаратам железа для приема внутрь, используемым в детской практике, являются: достаточная биодоступность; высокая безопасность; хорошие органолептические характеристики; лекарственные формы, удобные для пациентов всех возрастов. Этим критериям в наибольшей степени отвечают препараты железа на основе гидроксид-полимальтозного комплекса трехвалентного железа (Мальтофер и др.).
Средняя терапевтическая доза препаратов железа у детей от 3 до 7 лет по элементарному железу составляет 50–70 мг в сутки, старше 7 лет — 80–100 мг в сутки. При этом применение препаратов железа на основе ГПК-Fe3+, в частности препарата Мальтофер, не требует постепенного увеличения дозы. Также Мальтофер не взаимодействует с другими лекарственными препаратами или компонентами пищи.
Длительность терапии определяется врачом. В среднем на этапе устранения анемии она составляет не менее 1,5–2 месяцев. Этап терапии насыщения (ликвидации латентного ДЖ) должен проводиться не менее 3–6 месяцев, как правило, в дозе 50% от дозы этапа устранения анемии.
Ранее существовала точка зрения, что дети, в первую очередь подростки, склонные к периодическим незначительным кровопотерям, при нормальном гемоглобине не нуждаются в поддерживающей ферротерапии. Какое современное состояние этого вопроса?
Необходимо проводить поддерживающую ферротерапию для сохранения нормального уровня всех фондов железа, несмотря на транзиторные его потери.
Кто же нуждается в поддерживающей ферротерапии? Это девочки-подростки с гиперполименореей, которым необходимо назначать препараты железа не менее 7 дней после каждой менструации. Трехвалентные препараты железа показаны при периодических кровотечениях, зачастую микрокровотечениях из ЖКТ. Препараты железа назначаются ситуационно на протяжении 7–10 дней, при необходимости курсы ферропрепаратов рекомендованы ежемесячно. Доза препарата железа на этом этапе подбирается индивидуально, но в большинстве случаев составляет от 50% до 100% от стартовой дозы.
В индивидуально подобранной поддерживающей терапии ЖДА (как по дозе, так и по длительности приема) могут нуждаться подростки с опережающими общепринятыми стандартами физического развития, в случаях высокой физической активности (регулярные занятия спортом).
Кроме того, этим пациентам необходимо не менее 3–6 месяцев в году назначать витаминно-минеральные комплексы, в состав которых входит элементарное железо. Длительность этого этапа лечения ЖДА носит индивидуальный характер. Такая тактика поможет не только ликвидировать ЖДА, но и предупреждает возникновение в будущем ЖДС.
Профилактика железодефицитной анемии осуществляется только алиментарным путем или возможна в сочетании с приемом препаратов железа, витаминотерапией?
Действительно, рациональное питание в сочетании с витаминно-минеральными комплексами во многих случаях является хорошим защитным барьером против железодефицитных состояний и ЖДА.
Важнейшим фактором профилактики ДЖ является сбалансированное питание. Для детей раннего возраста в первую очередь важно грудное вскармливание. Грудное молоко не только содержит железо в высокой биодоступной форме, но и повышает абсорбцию железа из других продуктов, употребляемых одновременно с ним. Однако, интенсивные обменные процессы у грудных детей приводят к тому, что к 5–6-му месяцу жизни антенатальные запасы железа истощаются даже у детей с благополучным перинатальным анамнезом. Это происходит у детей, которые вскармливаются грудным молоком, а также и при вскармливании адаптированными молочными смесями, обогащенными железом. Для ребенка первого года жизни очень важно своевременное введение прикорма, введение в рацион мяса, особенно телятины, гречневой и овсяной круп, фруктовых и овощных пюре, кисломолочных продуктов, отваров шиповника и сухофруктов.
В более старшем возрасте у детей группы риска по ДЖ в рационе, кроме вышеуказанных продуктов, должны быть богатые железом мясные субпродукты (свиная печень, говяжий язык), твердые сорта сыра, яичный желток, бобы, кунжут, морская капуста, рыба, грецкий орех, яблоки, морковь, персики, шпинат, и др.
Следует помнить, что аскорбиновая, лимонная, янтарная и яблочная кислоты, фруктоза, сорбит и ряд других компонентов усиливают всасывание железа. Абсорбцию железа тормозят фитаты, фосфаты, танин, кальций, этилендиаминтетрауксусная кислота, используемая в качестве консерванта, антацидные препараты, тетрациклины.
Для детей, перенесших в раннем возрасте ЖДА, а также в группе риска по ДЖ необходимы длительные прогулки на свежем воздухе, нормализация сна, благоприятный психологический климат, профилактика острых респираторных вирусных инфекций, ограничение повышенной физической нагрузки.
Однако ряд детей входят в группу высокого риска возникновения ЖДА, это недоношенные дети; малыши, рожденные от многоплодной беременности, при осложненном течении беременности, наличии у матери анемии, особенно II, III степени тяжести; при наличии у пациентов стойкого дисбактериоза, выраженной пищевой аллергии; в случае опережения общепринятых стандартов физического развития. В таких случаях рекомендовано назначение профилактических доз препаратов железа, а также витаминотерапия (аскорбиновая кислота, витамины группы В и др.).
Какая тактика врача при назначении профилактических доз железа детям различных возрастных групп?
Следует помнить, что ферротерапия проводится не только на различных этапах лечения ЖДА, но и является составной частью профилактики ЖДС. Так, профилактика ЖДС, согласно отечественных протокольных рекомендаций (2005), начинается с антенатального периода. Женщинам со 2-ой половины беременности назначают препараты железа или поливитамины, обогащенные железом. При повторной или многоплодной беременности обязателен прием препаратов железа на протяжении 2-го и 3-го триместра. Согласно рекомендаций ВОЗ (2001) все беременные на протяжении 2–3 триместра должны получать 60 мг железа/сутки.
Постнатальная профилактика проводится у детей, входящих в группу высокого риска развития ЖДА. В эту группу входят: все недоношенные дети; дети, рожденные от многоплодной беременности и при отягощенном протекании второй половины беременности; дети с дисбиозами кишечника, пищевой аллергией; дети, которые находятся на искусственном вскармливании, особенно с первых месяцев жизни; дети, которые растут с опережением общепринятых стандартов физического развития.
Постнатальная профилактика ЖДС в Украине проводится согласно протокольных рекомендаций 2005 г., которые предусматривают регулярную диагностику риска реализации ЖДА в декретированных группах детей, а также назначение профилактических доз препаратов железа (0,5–1 мг/кг/сутки) в течение 3–6 месяцев, особенно в холодный период времени года.
В Украине на протяжении ряда лет при проведении профилактического лечения ЖДА широко используют гидроксид-полимальтозный комплекс трехвалентного железа – Мальтофер в дозе 0,5–1 мг/кг/сутки на протяжении 3–6 месяцев. У недоношенных детей эти курсы могут быть проведены на протяжении первых двух лет жизни.
В заключении наших сообщений хотелось бы привести точку зрения экспертов ВООЗ (2002): если распространенность железодефицитной анемии превышает 30% среди населения страны, то эта проблема выходит за рамки медицинской и требует принятия решения на государственном уровне. ![]()

АУТОИММУННЫЙ ПОЛИЭНДОКРИННЫЙ СИНДРОМ
Аутоиммунный полиэндокринный синдром (аутоиммунный полигландулярный синдром, синдром полигландулярной недостаточности) — аутоиммунное заболевание, объединяющее поражение нескольких эндокринных органов.
МКБ-10 — E31.0; МКБ-9 — 258.1.
Различают 3 разновидности аутоиммунного полиэндокринного синдрома (АПС):
- Аутоиммунный полиэндокринный синдром 1 типа (АПС-1)
- Аутоиммунный полиэндокринный синдром 2 типа (АПС-2)
- Аутоиммунный полиэндокринный синдром 3 типа (АПС-3)

КАК ЛЕЧИТЬ РИНИТ У РЕБЕНКА?

На сегодняшний день частота распространения заболеваний носа и околоносовых пазух у детей составляет 28–30% среди всех заболеваний верхнего отдела дыхательных путей. Известно, что общее число вирусов, вызывающих ОРВИ, достигает 180 и на их долю приходится примерно 95% всех случаев поражения верхних дыхательных путей у детей. Основной причиной возникновения ОРВИ являются риновирусы (до 80%); наиболее тяжелые ОРВИ вызываются вирусами гриппа
ОРВИ является системным заболеванием, при котором воспаление слизистой оболочки носит генерализованный характер. Заболевание характеризуется отеком слизистой, который вызывает затруднение носового дыхания, и патологической секрецией. Кроме того, у детей до 1 года отмечается нарушение сна, проблемы с глотанием, отказ от грудного вскармливания, в некоторых случаях может даже развиться дыхательная недостаточность. У детей младшей возрастной группы на первый план выходят симптомы общей интоксикации: повышение температуры; беспокойство, плаксивость, отказ от еды; насморк, кашель; проблемы со стулом. Нарушение дыхания при ОРВИ может привести к повышению внутричерепного давления и раздражению мозговых оболочек.
Стандарты лечения ринита
В соответствии с рекомендациями EPOS (Европейские стандарты риносинуситов у взрослых и детей, составленные с позиций доказательной медицины), выделяют 3 основных терапевтических подхода в лечении ринита: первый – элиминационный – является основным в лечении и профилактике воспалительных заболеваний верхних дыхательных путей и включает увлажнение, очищение полости носа от инородных агентов, разжижение и удаление вязкого секрета; второй подход связан с применением назальных деконгестантов, третий – с проведением противовоспалительной терапии.
Назальные деконгестанты – важный компонент комплексного лечения ринита. Они устраняют отек слизистой оболочки носа и снижают назальную секрецию. Прием антиконгестантов при заложенности носа избавляет от серьезной проблемы – нарушения дыхания.
Особо остро проблема возникает в младенческом возрасте, т. к. связана с процессом кормления. Однако некоторые специалисты стараются избегать назначения назальных деконгестантов, поскольку применение может быть неконтролируемым и привести к возникновению побочных эффектов. Очень частой причиной отказов является риск передозировок по причине сложного дозирования препаратов этой группы.
Детальніше
УКРАЇНО-ШВЕЙЦАРСЬКА ПРОГРАМА «ЗДОРОВ’Я МАТЕРІ ТА ДИТИНИ»
Нові підходи до організації охорони здоров’я.
Досягнення. Досвід впровадження. Рекомендації
 У розвитку медицини в Україні важливу роль відіграє діяльність міжнародних організацій та проектів, які приходять у країну з сучасними концепціями та ідеями щодо вдосконалення медичних послуг. З початку 2000-х років завдяки міжнародній співпраці було створено та впроваджено багато корисних та ефективних інструментів, підходів і продуктів, які ґрунтуються на доказових практиках і, водночас, адаптовані до українських реалій.
У розвитку медицини в Україні важливу роль відіграє діяльність міжнародних організацій та проектів, які приходять у країну з сучасними концепціями та ідеями щодо вдосконалення медичних послуг. З початку 2000-х років завдяки міжнародній співпраці було створено та впроваджено багато корисних та ефективних інструментів, підходів і продуктів, які ґрунтуються на доказових практиках і, водночас, адаптовані до українських реалій.
Один із таких міжнародних проектів — україно-швейцарська програма «Здоров’я матері та дитини», яка впроваджується в Україні за фінансової підтримки Швейцарської Конфедерації вже понад 15 років. За цей час напрацьовано величезний досвід у різних сферах: навчання медичного персоналу та керівників закладів охорони здоров’я, розробка навчальних матеріалів, клінічних протоколів, інформаційних матеріалів для лікарень та пацієнтів, здійснення якісного моніторингу діяльності медичних закладів, використання інформаційно-комунікаційних технологій тощо. Багато продуктів та напрацювань офіційно затверджені (наказами МОЗ України) та визнані на національному рівні (наприклад, частина навчальних матеріалів включена до освітніх програм НМАПО ім. П. Л. Шупика та медичних університетів).
Детальніше
ЛЮДИ ТА МАНЕКЕНИ Симуляційне навчання
 Безпека пацієнта – чи не найважливіший компонент якості медичної допомоги. Водночас, тільки у США, за недавніми оцінками, лікарські помилки щорічно призводять до загибелі понад 200 тисяч людей і завдають серйозної шкоди здоров’ю ще в 10–20 разів більшої кількості пацієнтів [1]. Для порівняння: в автокатастрофах щорічно гине 30–35 тисяч американців. Таким чином, шанс померти від неправильних дій лікаря значно більший, ніж ризик загинути від помилки водія на дорозі
Безпека пацієнта – чи не найважливіший компонент якості медичної допомоги. Водночас, тільки у США, за недавніми оцінками, лікарські помилки щорічно призводять до загибелі понад 200 тисяч людей і завдають серйозної шкоди здоров’ю ще в 10–20 разів більшої кількості пацієнтів [1]. Для порівняння: в автокатастрофах щорічно гине 30–35 тисяч американців. Таким чином, шанс померти від неправильних дій лікаря значно більший, ніж ризик загинути від помилки водія на дорозі
Зменшенню кількості лікарських помилок сприяють різні фактори. Серед них — нові підходи до медичної освіти, які дозволяють медичному персоналу вчитися та практикуватися і на чужих помилках, і на власних, не ризикуючи при цьому життям і здоров’ям пацієнтів. Саме таким підходом є симуляційне навчання.
Трохи історії
Ще у другій половині XVIII сторіччя видатна французька акушерка Анжеліка дю Кудре розробила акушерські тренажери у натуральний розмір, відомі під назвою «машини мадам дю Кудре» [2]. Вони були зроблені з тканини та шкіри, начинені справжніми людськими кістками і системою дерев’яних розпірок і ременів, які формували торс та імітували пружність родових шляхів і промежини.
Спеціальні губки всередині манекену могли випускати рідини, які нагадували кров та навколоплідні води, а лялька дитини мала ніс, вушка і відкритий рот, куди можна було вставляти пальці, щоб легше було витягати плід при неправильному передлежанні. За королівським дорученням, у 1760–1783 роках мадам дю Кудре об’їхала майже усю Францію і навчила акушерській справі близько 4 тисяч акушерок і 500 хірургів та лікарів (якими на той час могли бути лише чоловіки). Але потім у Франції розпочалися бурхливі часи, символом яких стали, на жаль, не «машини дю Кудре», а «машини доктора Гільйотена».
Сучасна історія симуляційного навчання у медицині почалася лише у 1960-ті роки. На знаменитому манекені Resusci Anne («обличчя, яке цілували найбільше разів за усю історію людства»), сконструйованому норвезьким фабрикантом пластикових іграшок Асмундом Лаердалем, мільйони людей навчилися робити серцево-легеневу реанімацію. Почався випуск тренажерів, призначених для навчання анестезіологів, кардіологів та лікарів інших спеціальностей.
Пізніше, завдяки розвитку комп’ютерної техніки та мікроелектроніки, з’явилися складні високотехнологічні манекени, які дозволяють розкрити справжній потенціал симуляційного навчання. Нарешті, у 1994 році було створено SESAM – Європейську асоціацію з симуляції у медицині, яка щорічно проводить великі міжнародні конференції [3].
Детальніше