
PLENTY OF CALORIES OVERLOADING SUBCUTANEOUS TISSUE: ЗМІНА ПАРАДИГМ*
 * За матеріалами доповідей із V з’їзду гінекологічної ендокринології, Криниця, Польща, 19–21 березня 2015 року: Romuald Debski «PCOS u nastolatki», Magdalena Sendrakowska «Hirsutyzm» та «Zaburzenia metaboliczne w PCOS»
* За матеріалами доповідей із V з’їзду гінекологічної ендокринології, Криниця, Польща, 19–21 березня 2015 року: Romuald Debski «PCOS u nastolatki», Magdalena Sendrakowska «Hirsutyzm» та «Zaburzenia metaboliczne w PCOS»
Синдром полікістозних яєчників (СПКЯ) (в англомовній літературі PCOS – PolyCystic Ovary Syndrome) описали Штейн і Левенталь у 1935 році, отже, саме тепер відмічаємо його 80-річний ювілей.
Однак цей термін вже давно піддається критиці експертів, оскільки він не відображає сучасних уявлень про патогенез цього стану і дезорієнтує лікаря у виборі лікування.
Перенесення акцентів з гінекологічної ланки на метаболічну неминуче потребує пошуку адекватнішої термінології.
Один із варіантів — «синдром надміру калорій, який перевантажує жирову тканину» (Plenty of Calories Overloading Subcutaneous tissue) — зосереджує увагу на патогенезі названого стану та спонукає до раціонального вибору у його лікуванні та профілактиці.
Звідки взялася ця проблема?
У походженні СПКЯ відіграють роль генетика (дуже вперте успадкування інсулінорезистентності) та умови життя, починаючи з внутрішньоутробного періоду.
Відомо, що надмірна вага матері під час вагітності є найінформативнішим предиктором наміру ваги у дитини. У свою чергу, вага при народженні є сильним чинником ризику надмірної ваги, починаючи з дитинства. Це стосується і немовлят з надто великою масою тіла (можливий вплив гестаційного діабету матері – звертаємо увагу також на спадковість!), і з надто низькою масою при народженні, особливо якщо вона не відповідає гестаційному віку.
Має значення і тип харчування у періоді немовляти (грудне вигодовування чи штучне) та вміст у ньому білка, оскільки, як відомо, споживання більшої кількості білка «програмує» організм на більшу масу тіла.
Типова кандидатка на СПКЯ — дівчинка, яка народилася недоношеною і з малою для гестаційного віку масою тіла, яку вигодовують сумішами із високим вмістом білка і яка завдяки цьому швидко росте і набирає вагу.Загалом, ключовим моментом у патогенезі СПКЯ є інсулінорезистентність, яка спричинює гіперандрогенію. Зазвичай інсулінорезистентність спричинена елементарним переїданням та низькою фізичною активністю.
Слід зауважити, що найвагомішу роль тут відіграє накопичення внутрішньочеревної жирової тканини, чи так зване абдомінальне ожиріння, яке трапляється навіть при нормальному індексі маси тіла.
У свою чергу, гіперандрогенія спричинює добре відомі клінічні прояви: вугрі, жирність шкіри і волосся, гірсутизм, розлади менструального циклу. До того ж, гіперандрогенія сприяє збільшенню маси тіла, що ще більше посилює інсулінорезистетність, отже, у такий спосіб замикається «хибне коло» цієї патології.
Пацієнтки групи ризику
Важливо виявити дівчаток, у яких може розвинутися СПКЯ, якомога раніше, оскільки запобігти розвитку цього стану можна лише за умови впровадження заходів у дуже ранньому віці.
Важливі анамнестичні дані, які вказують на можливість розвитку названого стану, це:
- Сімейний анамнез (надмірна вага/діабет у матері, надмірна вага, діабет чи АГ у батька, ранні серцево-судинні захворювання та цукровий діабет у близьких родичів тощо).
- Дитинство та пубертатний період:
- гестаційний вік та маса тіла при народженні;
- тип вигодовування (штучне/грудне);
- приріст ваги в дитинстві;
- вік пубархе, телархе і менархе (звичайно статеве дозрівання починається у 8–9 років).
- Особливості менструальних циклів:
- аменорея;
- олігоменорея;
- дисфункційні кровотечі.
Звичайно СПКЯ розвивається у дівчат з надмірною вагою, низькою масою тіла при народженні, проявами метаболічного синдрому і раннім статевим дозріванням. Такі діти потребують поглибленого обстеження, схема якого представлена далі (табл. 1):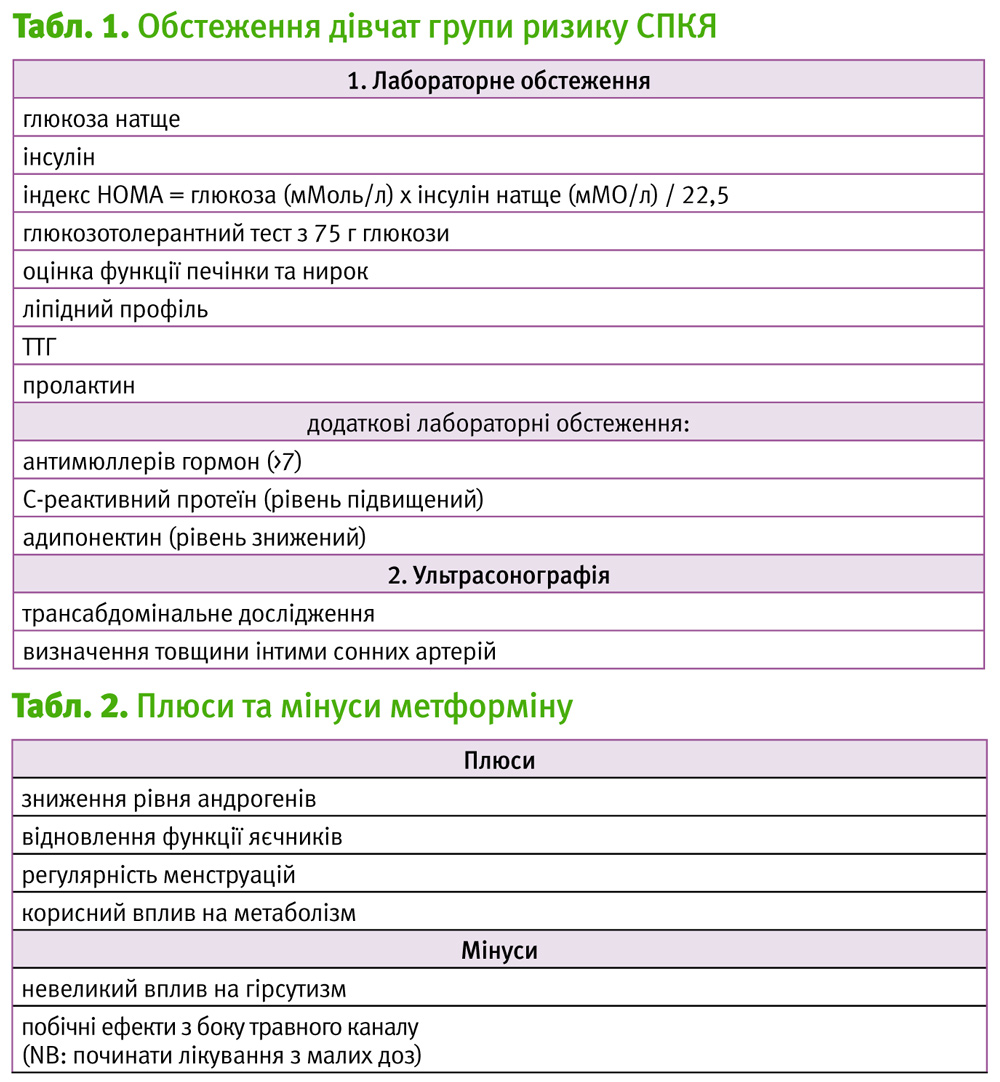
Зазвичай, рівень інсуліну у здорових молодих людей не повинен перевищувати 8 мМО/л, при навантаженні – 60 мМО/л; рівні глюкози не відрізняються від загальноприйнятих. Варто зауважити, що інколи при виконанні глюкозотолерантного тесту рівні глюкози після навантаження є надзвичайно низькими. Суттєве зниження рівня глюкози звичайно спричинене великим викидом інсуліну у відповідь на потрапляння в організм глюкози.
Незважаючи на відсутність офіційних настанов, це слід брати до уваги, оскільки такі пацієнтки можуть бути чутливі до загальноприйнятого при СПКЯ лікування, зокрема, дієтологічних інтервенцій (див. попередні числа ЗТЖ).
Ультрасонографічне дослідження
Дослідження через передню черевну стінку, яке звичайно виконують у дівчаток, має нижчу інформативність порівняно з традиційним у гінекології трансвагінальним дослідженням. Звичайно воно утруднене ще й надмірною вагою пацієнтки.
Дослідження товщини інтими сонних артерій
У 1990-х роках товщину intima media (сумарна товщина tunica interna + tunica media) почали застосовувати як індикатор серцевого ризику та його динаміки, оскільки дослідження засвідчили про кореляцію між цим показником і субклінічною стадією серцево-судинних захворювань. У 2007 році американське товариство ехокардіографії запропонувало офіційні настанови щодо вимірювання товщини інтими сонних артерій, оскільки це дослідження недороге, неінвазивне і не створює дискомфорту для пацієнта. Вважають, що його техніку легко опанувати; необхідною передумовою є лише наявність відповідного датчика для дослідження судин.
У цілком здорових дівчат яєчники часто мають вигляд, який відповідає діагностичним критеріям СПКЯ, однак це не означає, що у них дійсно є цей стан. Замість того, щоб рахувати дрібні фолікули у яєчниках (що, зрештою, не має жодного практичного значення), доцільніше прикласти датчик до шиї пацієнтки і оцінити товщину intima media сонних артерій. Це дає реальне уявлення про її серцевий ризик, зумовлений СПКЯ, та спрямовує у правильному напрямку щодо вибору лікування.
Лікування
Із урахуванням того, що СПКЯ характеризується різними фенотипами, пріоритетні напрямки лікування визначають індивідуально.
Зокрема, для пацієнток з надмірною вагою першочерговим завданням є зниження маси тіла. Слід зауважити, що порогове значення індексу маси тіла (ІМТ) залежить від віку: якщо для дорослих це понад 25 кг/м2, то для дівчат-підлітків — 23 кг/м2. Найефективнішою є нормалізація маси тіла ще до статевого дозрівання, що, в принципі, дає змогу запобігти розвитку симптомів СПКЯ.
Водночас слід пам’ятати, що у пацієнток із гіперандрогенією, яка вже розвинулася, корекція маси тіла буває складною, проте полегшується при одночасному з дієтою та фізичною активністю застосуванні метформіну.
Переваги і недоліки метформіну наведені у табл. 2. Слід пам’ятати, що для запобігання небажаним ефектам з боку травного каналу доцільно розпочати лікування з малих доз (500 мг/добу у два прийоми), збільшуючи їх малими кроками що кілька днів до приблизно 2000 мг/добу. Інколи пацієнтки ліпше переносять пролонговані форми цього препарату.
Застосування метформіну вважають вибором першої лінії у пацієнток із нормальною масою тіла. Додавання оральних контрацептивів до метформіну не має корисних ефектів і не повинно застосовуватися з лікувальною метою.
Продовження – у наступному номері.
Детальніше
ЛЮДИ ЧИ БОГИ?
LUDZIE CZY BOGOWIE?
- У допологовій (пренатальній) діагностиці зокрема, та у медицині плода взагалі, практично щодня доводиться стикатися з питаннями життя та смерті. Аби самому не впасти в легку ілюзію «вершителя доль» та примусити батьків не скидати з себе відповідальності за долю власної дитини, досить часто доводиться собі та їм нагадувати, що лікарі є людьми, а не богами.
- Якось була на прийомі замінна українська мати, яка виношує дитину польській родині, разом з, власне, генетичними батьками. Останні подарували мені книжку, що, в продовження нашої колишньої з родиною розмови, якраз і має назву «ЛЮДИ ЧИ БОГИ / LUDZIE CZY BOGOWIE». Книжка дістала в Польщі вже 2-ге видання, містить 27 розмов з найвідомішими польськими лікарями (автори – Dariusz Kortko та Krystyna Bochenek, видавництво AGORA SA, належить до порад Biblioteka Gazety Wyborczej).
- Слід знати, що У СЕРЕДНЬОМУ поляки є набагато ближчими ментально до українців, ніж будь-хто инший з народів-сусідів, включно з росіянами. Умовно кажучи, такими приблизно й були б українці, якби дістали менший нищівний тиск з боку російської імперії впродовж століть. Більше того, оскільки Польща входила до складу «соціалістичного табору» та СЕВ («Савєта Еканамічєскай Взаімапомащі»), організація медицини й науки в них за радянських часів була майже як близнюки-брати подібною до української.
Але останніми понад 20-ма роками, оскільки суспільство не тупцювало на одному місці, розмірковуючи, треба бути «з розумними чи з красівимі»J, Польща здійснила вражаючи кроки у розвитку політики й економіки, науки й медицини. Тому, НА МІЙ ОСОБИСТИЙ ПОГЛЯД, саме у поляків слід навчатися, як перебудовувати українське суспільство, науку та медицину.
- Відповідно, передбачаю, що на підставі викладеного вище можна сподіватися на цікавість та зрозумілість змісту книжки «ЛЮДИ ЧИ БОГИ» українським читачам, як «уже вихідцям», так і «ще не вихідцям» з радянського минулого/сьогоденного. Тому на шпальтах е-сторінки «Фонду Медицини Плода, Україна» у Facebook та часопису «З Турботою про Жінку» оприлюднюватимемо цитати з книжки.
- Сама ідея такої книжки є цікавою для наслідування, і було б добрим, якби хтось із новинарів українських ЗМІ взявся за подібний проект!
Стор. 10. Dariusz Kortko:
«Впродовж кількох років розмовляли з лікарями, бо не могли погодитися з оскарженнями, що вони неуважні, перевтомлені, у сталій погоні за грошима, неморальні, втратили співчуття. «Уринковані», затоплені в процедурах, контрактах, лічать на касі пункти за лікування. Що збагатилися, і помітно – побудували будинки, їздять ліпшими автівками, відпустки проводять у теплих краях. Пацієнт є клієнтом.
Розпитували: всі, більшість чи дехто? Хто то є великим лікарем? На яку нагороду можна розраховувати і як миритися з поразками? Звідки черпають зразки, хто для них є майстром?
Нагороджували нашу цікавість. Оповідали про найінтимніші справи, часто були ті зізнання дуже зворушливими. Охоче розмовляли о сенсі страждання, хвороби та смерті, з якою так часто мали зустрічатися.
Майже всі підтверджували, що наше покоління виперло смерть зі свідомості. О смерті не розмовляє, відмовляє їй у праві буття, немає для неї місця в нашому світі. Замріялися навіть, щоби її лікувати. Проте смерті не відсунути, хоч би ми того не хотіли, йде з нами через життя.»
Стор. 24. Проф. Kornel Gibiński (1915-2012), надзвичайний терапевт і гастроентеролог:
…пан викладає, пише до престижних медичних видань, усі рахуються з думкою пана. Для кількох поколінь лікарів пан є авторитетом...
– Ніхто не читає того, що пишу.
– Чому пан так каже? Якби не читали, то не замовляли б наступних текстів.
– Кажу, що не читають. Роками проголошую те саме, а всі поводяться так, якби перший раз о тим чули… Нікого не зачаровує те, що кажу… Наприклад, роками нагадую, що мало робимо, аби забезпечити гідну смерть умираючій людині. Багато зусиль іде на рятування новонароджених, на покращення комфорту пологів, на забезпечення плода й мами. Зважають на життя, а що зроблено для помирання? Ніц!
Люди помирають усамітнені, бо немає кому ними зайнятися. Нема родини, бо родина працює. Шпиталь виписує, бо вже нічого не може зробити; не хочуть марнувати ліжка та псувати статистику. Нерідко видно бажання позбавитися хворого, і людина відходить в трагічних умовах. А як приходить у світ, то має такий комфорт. Чому відхід не трактувати так само? Це ж такий самий пункт життя, як і прихід у світ. Чому ж не потрактувати його з подібним піклуванням?… Сучасним підходом постають хоспіси,.. щоби иншим запевнити гідніший, спокійніший відхід. Людям, які потерпають від самотности, своєї безпорадности, а не лише тому, що «болить»…
– Чому так?
– Недооцінюємо, яку велику вагу в контакті з иншою людиною грає здібність співчуття. То джерело лікарського покликання, адже співчуття, вразливість до страждання є основою медицини. Чому лікар допомагає пацієнтові? Бо прагне полегшити страждання…
…Треба більше піднімати питання, на що слід витрачати гроші, які є: на рятування від смерти чи на задоволення потреб сотень тисяч людей?… Почали ми лікувати смерть, а то нонсенс, бо смерти не уникнути. Йдеться о передчасній смерті. Якби не було хвороби, люди би передчасно не вмирали. О тим ідеться…»
Детальніше
КРАСНУХА: ОСОБЛИВОСТІ ПЕРЕБІГУ У ДОРОСЛИХ. КЛІНІЧНА ЛЕКЦІЯ (Ч. 2)
 Вроджена краснуха
Вроджена краснуха
Вроджена краснуха розвивається у плода, якщо вагітна переносить гостру (первинну) інфекцію. Спектр вад розвитку у плода визначається терміном гестаційного періоду, в який вагітна перенесла інфекцію.
При інфікуванні в більш пізні терміни вагітності (13–16 тижні та пізніше) частота розвитку дефектів у внутрішньоутробно інфікованих немовлят знижується, але певна небезпека зберігається аж до ІІІ триместру.

Існувала думка, що плід, інфікований вірусами, в тому числі краснухи, втрачає здатність до створення інтерферону – досить значного захисного фактору.
Однак доведено, що інфікований плід зберігає здатність створювати a-інтерферон вже з 7-го тижня розвитку [Lebon P. et al., 1985].
Багатофакторний несприятливий вплив на плід, який чинить вірус краснухи, не може бути навіть частково нейтралізований материнськими антитілами: IgM через плаценту не проходять.
Частота інфікування плода значною мірою визначається терміном вагітності у момент зараження: у перші 8 тижнів вона становить 60–100%; на 9–12 тижні — 15–50%; після 12 тижнів — 7–12%. Якщо внутрішньоутробне зараження відбулося у більш пізні терміни, то створені власні IgM виявляються при народженні та зберігаються протягом перших 6–8 місяців життя дитини (іноді довше). Таким чином, наявність у новонароджених специфічних антитіл класу IgM – показник перенесеної внутрішньоутробної краснухи.
Вроджена краснуха характеризується тріадою Грегга:
- Катаракта (помутніння кришталика) одно- або двобічне, часто супроводжується мікрофтальмом.
- Пороки серця (незарощення артеріальної протоки, стеноз легеневої артерії, ураження клапанного апарату або якої-небудь серцевої перегородки);
- Глухота.
Поряд з цими трьома ознаками, можуть бути інші вади розвитку: низька маса при народженні, тромбоцитопенічна пурпура, гепатоспленомегалія, катаракта (і мікрофтальмія) та інші.
Стійкі (постійні) вроджені пошкодження плоду формуються переважно у разі зараження у I триместрі вагітності. Хромосомні порушення, як правило, виявляють вже після народження дитини, у процесі його росту і розвитку. Транзиторні порушення у плода характерні для більш пізнього періоду. Чим раніше відбулося зараження, тим більш грубі, а нерідко і комбіновані порушення виникають у плода. Описано порушення слухового апарату, які призводять до глухоти, затримки розвитку зубів і кісток скелета (в тому числі черепа – «вовча паща»), аномалії нирок, «заяча губа», мікроцефалія. У разі внутрішньоутробного інфікування плода тривало зберігається стан пригніченого імунітету (клітинного та гуморального), що також негативно впливає на ріст і розвиток дитини.
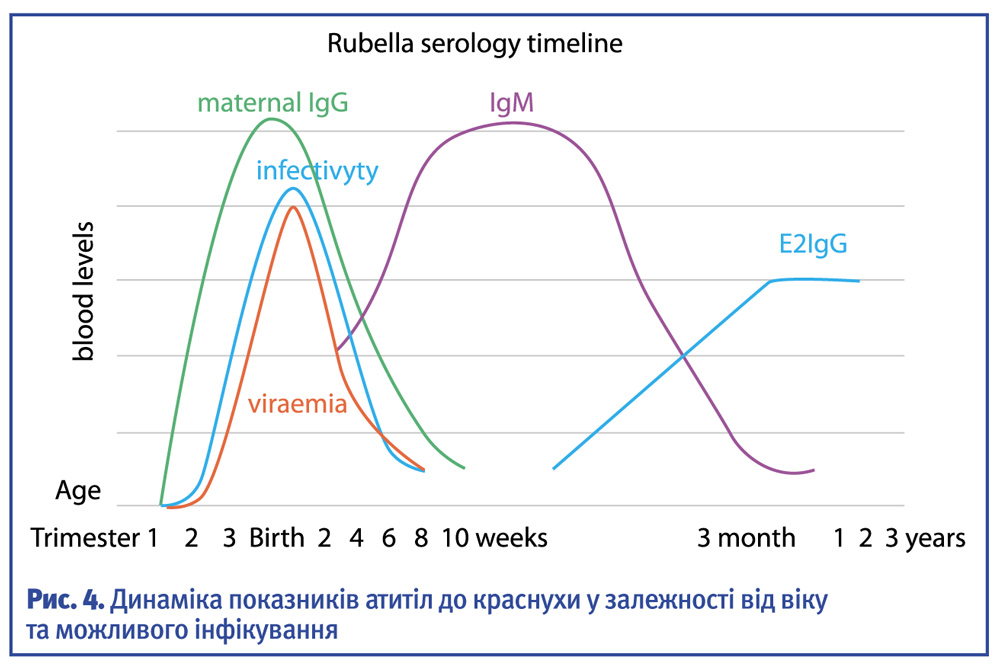
Діагностика краснухи
- Діагноз клініко-епідеміологічний, грунтується на характері висипу, терміні його появи, одномоментності висипань і локалізації, епідемічної ситуації.
- Вірусологічний метод – спрямований на виявлення самого вірусу, метод ефективний лише у певні терміни: дослідження крові та фекалій доцільні у період перебування вірусу в крові від 7 до 14 дня інфікування (до появи висипу); виділення з носоглотки доцільно брати за наявності висипів.
- Серологічні методи – визначають наявність віруснейтралізуючих антитіл за допомогою РНГА та РН, а також визначають класоспецифічні антитіла IgG, M і А за допомогою ІФА. Ці методи використовують у 1–2 день після появи висипу і на 20 добу.
Лікування
Хворі на краснуху підлягають ізоляції до 5-го дня з моменту появи висипу. У дитячому колективі вводять карантин на 21 добу після ізоляції останнього хворого. Контактні хворі можуть відвідувати дитячі колективи до 10-ої доби, а з 11-ої до 21-ї їх ізолюють у домашніх умовах.
Специфічного лікування не розроблено, тому використовують:
- Ліжковий режим протягом 3–7 днів;
- Повноцінне харчування, з урахуванням вікових особливостей;
- Загальногігієнічні заходи;
- Дезінтоксикаційна терапія – рясне пиття;
- Часте провітрювання приміщень.
- Симптоматична терапія (відхаркувальні – певна група застосовується при певному характері кашлю, тобто не можна застосовувати одночасно відхаркувальні та протикашльові), муколітики, жарознижуючі, анальгетики);

Тактика щодо контактних вагітних
Обстеженню на краснуху підлягають жінки, в яких відмічаються зміни загального стану, короткочасна лихоманка, будь-який висип на шкірі, гостре збільшення лімфатичних вузлів. У таких жінок визначають наявність специфічних IgM, низькоавідних IgG або наростання титрів IgG в динаміці, що свідчить про гостре захворювання.
Якщо такі зміни діагностуються у 1-му триместрі вагітності, то необхідно вирішувати питання про її переривання. У разі відсутності лабораторних ознак гострої інфекції необхідне спостереження за вагітною протягом 20 днів з повторним її обстеженням у зазначені строки. За серонегативнми вагітними здійснюється спостереження протягом всієї вагітності.
При інфікуванні жінки у 2–3-му триместрі вагітності необхідне спостереження за нею з використанням, за можливості, методу ПЛР, РНК-гібридизації у біоптаті ворсинок хоріону або вірусологічного дослідження амніотичної рідини, ультразвукового дослідження, доплерографічного обстеження судин плода та пуповини, визначення альфа-фетопротеїну. З успіхом проводиться пряме визначення антигена краснухи та РНК у зразку біоптатів хоріоїдної ворсинки чи специфічного IgM у крові плода, отриманої зі зразка черезшкірної умбілікальної крові.
Діти, що народилися від матерів, які в період вагітності хворіли на краснуху чи були в контакті з хворим на краснуху, підлягають диспансерному спостереженню не менше 7 років з обов’язковим регулярним оглядом педіатра, окуліста, отоларинголога, невролога. Введення імуноглобуліну з метою профілактики краснухи неефективне.
Профілактика
Специфічна профілактика краснухи здійснюється переважно живими вакцинами. Добре себе зарекомендували вакцини, отримані з використанням атенуйованого штаму вірусу краснухи Wister RА 27/3, які стимулюють не лише гуморальну, але й секреторну імунну відповідь. Антитіла з’являються через два–три тижні після вакцинації, імунітет формується у 95% щеплених осіб і зберігається напруженим упродовж 15–20 років.
«Живі» вакцини не можна застосовувати під час вагітності, оскільки при їх введенні виникає короткотривала вірусемія, а це може призвести до ураження плода та народження дитини із синдромом вродженої краснухи. Вагітність можна планувати не раніше, як через три місяці після проведеного щеплення.
На світовому ринку найбільш відомими вакцинами із використанням атенуйованого штаму Wister RА 27/3 є моновакцини: «Рудивакс» (Франція), «Ервевакс» (Бельгія), вакцина виробництва Інституту сироваток Індії та тривакцини: «ММR» (Нідерланди), «Пріорикс» (Бельгія), «Тримовакс» (Франція) і комбінована вакцина виробництва Інституту сироваток Індії. До складу тривакцин також входять вакцини проти кору та паротитної хвороби.
Специфічна профілактика краснухи здійснюється живою вакциною у віці 12–15 місяців з подальшою ревакцинацією в 6 років, а дівчатам — ще і в 15 років.
Д. Клоерті та Е. Старк (2002) рекомендують серонегативних жінок, які не інфікувалися під час вагітності, імунізувати проти краснухи відразу після пологів. Жінкам, які отримали вакцинацію проти краснухи, не рекомендується грудне вигодовування новонародженого.
Діти з СВК повинні розцінюватися як потенційно небезпечне джерело інфекції для оточуючих. У відношенні до них необхідно застосовувати відповідні протиепідемічні заходи. З метою своєчасної діагностики СВК та попередження поширення краснухи серед населення, доцільно всіх новонароджених з вродженими вадами обстежувати на маркери захворювання. Згідно з рекомендаціями ВООЗ, діти з підозрою на СВК чи клінічним проявом СВК повинні госпіталізуватися у спеціально організовані в регіонах медичні установи, створені на базі стаціонарів, в яких надається допомога дітям з вродженими вадами (серцево-судинна хірургія, офтальмологія, неврологія, інтенсивна терапія новонароджених).
Висновок
Таким чином, боротьба з краснухою, попередження розвитку СВК є важливою ланкою поліпшення показників перинатальної захворюваності та смертності. Особливо гостро стоїть питання про необхідність введення масової вакцинації проти краснухи серед дівчаток-підлітків і молодих жінок.
Перелік літератури знаходиться у редакції.
Детальніше
ЗДОРОВ’Я МАТЕРІ ТА ДИТИНИ ЗАВЖДИ НА ЧАСІ
Науково-практична конференція та Пленум акушерів-гінекологів України – 2015. Секційне засідання «Медицина плода: актуальні та щоденні питання»
Стрес матері під час вагітності: наслідки для плода та новонародженого
О. Д. Щуревська, к. мед. н., каф. акушерства, гінекології та медицини плода НМАПО ім. П. Л. Шупика
Доповідь Оксани Дмитрівни була присвячена темі, яка, на жаль, з огляду на політико-економічну ситуацію в нашій країні залишається надто актуальною – «Стрес матері під час вагітності: наслідки для плода і новонародженого».
Спікер детально висвітлила проблему стресу під час вагітності, загальні механізми його дії і «критичні терміни» гестації, а також віддалені наслідки перенесеного перинатального стресу для емоційного, психічного і фізичного здоров’я людини.
Зокрема, спираючись на дані світової наукової літератури та власний професійний досвід, лікар зосередила увагу колег на необхідності замислюватися про віддаленні наслідки перенесеного матір’ю стресу для новонародженого та його здоров’я у дорослому віці: «Стреси та депресії вагітності можуть бути етіологічними чинниками загрози її переривання і впливати на розвиток емоційної сфери внутрішньоутробної дитини та стан її нервової системи. Г. І. Брехман вказує, що перинатальний стрес може бути фактором ризику розвитку шизофренії та біполярного афективного розладу в майбутньої дитини. Крім того, негативні емоції матері під час ускладнень вагітності можуть впливати на зміни з боку серцево-судинної системи пренейта.
У генетиці описують поняття «материнського ефекту», яким позначають вплив матері на потомство. Не дивлячись на те, що генетичний «заряд» передається потомству від матері та батька, все ж саме материнський вплив вважається більш значимим. Окрім соматичного статусу жінки, характеру ускладнень перебігу даної вагітності, має значення також емоційний стан жінки протягом вагітності, адже внутрішньоутробний плід на своєму дещо примітивному рівні здатен чути, відчувати, переживати, чомусь навчатись – все це формує його відношення у подальшому до життя, до себе і оточуючих.
До групи високого ризику щодо розвитку соматичних, неврологічних і психічних розладів відносяться недоношені новонароджені. Існує чимало факторів виникнення таких розладів, у тому числі, безпосередня причина передчасних пологів, гестаційний вік, загальна морфо-функціональна незрілість органів і систем, тривале перебування у лікувальних закладах тощо.
Отже стан матері та матково-плацентарного комплексу під час вагітності відіграють значну роль у всіх аспектах розвитку плода і низці ключових моментів розвитку мозку майбутньої дитини, які надалі проявляються після народження протягом усього подальшого життя.
Численні дослідження впливу внутрішньоутробного періоду на розвиток людини, формування особистості, емоційне і фізичне здоров’я дали поштовх для розвитку нового напрямку науки під назвою «fetal programming» – програмування плода. У рамках даного напрямку зазначають, що віддалені наслідки впливу тих чи інших факторів під час вагітності можуть проявитися через десятиріччя (!) після народження, і їхній ефект буде настільки сильним, що його неможливо уявити і спрогнозувати.
На сьогодні висловлюються різні точки зору стосовно пренатального досвіду людини, проте аналіз ранніх і сучасних досліджень свідчить, що психіка і фізичне здоров’я дитини починають формуватись ще у допологовий період.
Дослідження у психіатричному реєстрі Єрусалиму 88 829 пацієнтів 1964–1976 років народження, що народилися у жінок, які у розпал арабо-ізраїльської війни у червні 1967 року («Шестиденної війни») були на 2-му місяці вагітності, виявило їхню вищу захворюваність на шизофренію протягом наступних 21–33 років.
Шизофренія була описана майже 100 років тому як група розладів, для яких характерні відхилення у сприйнятті реальності або її відображенні. Дотепер залишається не з’ясованим питання щодо причин цього захворювання, проте увагу багатьох учених дедалі більше привертають перинатальні фактори. Так, Г. І. Брехман у 2010 р. зазначив: «Беручи до уваги значення генетичних, нейробіологічних, соціально-психологічних, інфекційних факторів, ми хотіли б підтримати ідею важливої ролі у виникненні шизофренії і біполярного афективного розладу пренатальних психотравм, пов’язаних з глибокими переживаннями матері під час вагітності і пологів. Наразі більшість учених визнають несприятливий вплив емоційного стресу матері на результат вагітності і пологів, а також на стан внутрішньоутробного плода і новонародженого. Крім того, визнано, що стрес має потенціал модулювати імунну систему. Дослідження впливу материнського стресу під час вагітності на імунні функції у потомства почали досліджувати відносно недавно, при цьому було встановлено підвищені рівні у пуповинній крові IgE, що, своєю чергою, вважається фактором ризику атопії в дитинстві. Також встановлено, що вагітні жінки з психо-соціальними стресами мають збільшені сироваткові рівні прозапальних цитокінів, які пов’язують з алергією у подальшому житті їхнього потомства».
Новий погляд на індукцію пологів в інтересах плода
 С. І. Жук, д. мед. н., проф., зав. кафедрою акушерства, гінекології та медицини плода НМАПО імені П. Л. Шупика
С. І. Жук, д. мед. н., проф., зав. кафедрою акушерства, гінекології та медицини плода НМАПО імені П. Л. Шупика
Значну частину своєї доповіді Світлана Іванівна присвятила роз’ясненню необхідності підняття цього питання, яка обумовлена, на її думку, недостатньою увагою лікарів у випадках, коли мова йде про патології, пов’язані з плодом: «Коли у майбутньої мами виникає невідкладний стан (кровотечі, емболії, прееклампсії тощо), лікар діє досить швидко і професійно, проте цього не відбувається у так званих «сумнівних станах» з боку плода. Саме тому потрібно робити акцент на внутрішньоутробних невідкладних станах плода, які на сьогодні вже досить докладно висвітлені в науковій медичній літературі.
Кафедра акушерства, гінекології та медицини плода займається вивченням цих сумнівних станів плода: діагностикою, причинами їх виникнення тощо. Зовсім скоро будуть надані нові нормативні документи стосовно моніторингу внутрішньоутробного стану плода для вчасного виявлення загрозливого стану і надання ефективної медичної допомоги у таких випадках.
Відомо, що найбільші перинатальні втрати виникають на етапі розродження. На жаль, наразі не має чітких рекомендацій щодо алгоритму дій у разі виникнення тяжкого стану плода. Звичайно, є документи щодо дистресу плода, але дистрес – це не тільки гострий процес. Сьогодні закордонні колеги вже використовують такий термін як «хронічний дистрес». Ще точніше назвати цей стан «хронічним стражданням» плода. Отже обов’язково потрібно мати чіткі рекомендації, як розроджувати таку вагітну. На жаль, кесарів розтин (КР) не став тим ідеальним методом, на який так сподівалися. Відомо, що КР може мати (і для жінки, і для дитини) ряд ускладнень як під час операції, так і у віддаленому післяопераційному періоді.
Крім того, наразі достеменно відомо, що постійно зростаючий відсоток КР не впливає на зменшення показників перинатальної захворюваності та смертності. Натомість констатується погіршення стану здоров’я дитини безпосередньо під час оперативного розродження і після КР. До слова, сам КР може бути причиною перинатального стресу, адже у такому випадку, процес дозрівання плода просто не встигає відбутися, тож адаптаційні можливості у таких діток знижені, що проявляється, як правило, респіраторними розладами (через порушення ендогенної та механічної підготовки легень) та досить серйозними проблеми з імунітетом. Згідно висновку експертів ВООЗ (2014 рік), ефект зниження материнської і перинатальної смертності зростає при збільшенні частоти КР на 10% від всіх пологів, тоді як подальший ріст абдомінальних розроджень вже не впливає на зазначені показники.
Крім того, у дітей, народжених за допомогою КР, відзначається підвищений ризик аутоімунних, алергічних захворювань (таких загрозливих як цукровий діабет I типу, бронхіальна астма, хвороба Крона, розсіяний склероз тощо). Отже, володіючи такою інформацією, чи можна залишатися адептом КР? Потрібно відзначити, що нині відбувається так би мовити, натуралізація акушерства ХХI століття. Переживши і переосмисливши акушерську агресію, сьогодні ми схиляємось до природніх методів розродження жінки. Однак це потрібно робити надзвичайно вміло і з урахуванням усіх індивідуальних особливостей пацієнтів.
2014 року з’явилося нове керівництво ВООЗ «Індукція пологів». Даний документ було покладено в основу клінічних протоколів у всіх країнах світу, у тому числі, і вітчизняного Уніфікованого клінічного протоколу первинної, вторинної (спеціалізованої) та третинної (високоспеціалізованої) медичної допомоги «Преіндукція та індукція пологів».
Протокол вже опубліковано на сайті асоціації акушерів-гінекологів України. Отже, кожен спеціаліст має змогу ознайомитися з ним і висловити свої критичні зауваження та пропозиції, аби максимально удосконалити цей документ. Зрештою, ми всі в цьому зацікавлені», – зауважила професор Жук.
Світлана Іванівна спинилася на основних принципах застосування передіндукції та індукції пологів, викладених у Настанові.
Вона також зосередила увагу присутніх на інших важливих практичних аспектах, як, наприклад, застосування окситоцину. З приводу останнього, професор рекомендувала уважно ознайомитися з монографією С. Л. Воскресенського.
«Менінгомієлоцелє: антенатальний догляд в українських реаліях»
 Л. Г. Назаренко, проф., зав. кафедрою генетики та медицини плода ХМАПО
Л. Г. Назаренко, проф., зав. кафедрою генетики та медицини плода ХМАПО
Лариса Григоріївна нагадала колегам, що існує три форми spina bifida, кожна з яких має різну ступінь тяжкості етіології та епідеміології цієї патології. Зокрема, менінгомієлоцелє є найбільш важкою формою дефекту і при використанні терміну «Spina bifida» зазвичай мається на увазі саме ця форма.
У своїй доповіді професор детально висвітлила важливі аспекти діагностики, сучасні можливості лікування та профілактики хвороби: «Щодо етіології, за сучасними уявленнями, такій патології сприяє комбінація генетичних привнесених факторів. Відомо, що частота дефектів розвитку нервової трубки коливається від 1:500 до 1:2000 живих новонароджених у різних регіонах світу і етнічних групах населення, складаючи в середньому 1:1000. Однак, якщо у сім'ї батьків або найближчих родичів зустрічалися випадки народження дітей з дефектами нервової трубки, то ймовірність появи дитини з дефектом зростає до 2–5%. Це ж стосується народження другої дитини, якщо перша народилася з дефектом (ризик близько 5%). Насторожуючим моментом у цьому плані також є спонтанні аборти (викидні), передчасні пологи, дитяча смертність у сім'ї та у родичів.
Тому генетична схильність до появи дитини з дефектом нервової трубки є основним показником включення вагітної у групу високого ризику. До зовнішніх чинників, що сприяють появі дефекту розвитку нервової трубки, відносяться:
- радіація (проживання у районах, забруднених радіонуклідами, робота з джерелами радіаційного випромінювання);
- токсичні речовини хімічного походження (нафтопродукти, добрива, пестициди і т. д.);
- застосування жінкою до вагітності та в перші її місяці протисудомних препаратів;
- висока температура тіла або застосування гарячих ванн на початку вагітності;
- цукровий діабет та ожиріння;
- незбалансоване харчування, дефіцит вітамінів і особливо фолієвої кислоти.
Виявлення одного, а тим більше, кількох з цих факторів є підставою для включення вагітної у групу високого ризику народження дитини з дефектом розвитку нервової трубки.
Також важливе значення останнім часом приділяється оральним контрацептивам. Доведено, що препарати, що містять менше 50 мкг естрогену, можуть порушувати генетику обміну метіоніну фолатного циклу.
Спікер також звернула увагу на важливість ранньої діагностики та вчасного хірургічного лікування Spina bifida, що, за сучасними стандартами, мають бути виконані якомога раніше – ще у внутрішньоутробному періоді: «Вперше про такі операції ми почули 2011-го року, під час Конгресу неонатологів в Уругваї, коли наші закордонні колеги презентували результати своєї десятирічної роботи з цього напрямку. Маю зазначити, що і тоді вже було зрозуміло, і, тим більше, зараз, що тільки така тактика є ефективною, адже якість життя прооперованих діток разюче відрізняється від тих, кому таке лікування не проводиться. Щодо українських реалій, мусимо визнати, ми не маємо чітких статистичних даних щодо частоти менінгомієлоцелє, натомість, в Україні є як мінімум три належно підготовлені команди (у Києві, Одесі та Харкові), готові виконувати фетоскопічні операції з цього приводу», – наголосила Лариса Григорівна.
Амніотична рідина: точність діагностики потребує постійного навчання
 Є. І. Парпалей, доц. кафедри акушерства, гінекології та медицини плода НМАПО ім. П. Л. Шупика
Є. І. Парпалей, доц. кафедри акушерства, гінекології та медицини плода НМАПО ім. П. Л. Шупика
Доповідь стосувалася вагітних з патологіями кількості навколоплідної рідини та принципів їх раціонального супроводу. Насамперед, лікар наголосив на важливості правильної оцінки кількості навколоплідної рідини: «Спеціалісту з певним досвідом роботи це зробити нескладно, за допомогою УЗД, визначаючи індекс амніотичної рідини тощо. Натомість, наприклад, при діагностиці маловоддя, залишається досить високий відсоток хибнопозитивних результатів», – зауважив спікер.
Саме тому, на його переконання, сьогодні існує гостра необхідність у подальшому удосконаленні знань і практичного досвіду українських спеціалістів – проведенні більшої, аніж ми маємо на сьогодні, кількості різноманітних тренінгів, інтенсивного симуляційного навчання, майстер-класів для акушерів-гінекологів з сучасних методів пренатальної діагностики (зокрема, УЗД-діагностики).
Прогнозування прееклампсії у першому триместрі вагітності: що на часі?
О. І. Соловйов, к. мед. н., зав. відділом медицини плода Клініки «Надія», Київ
Тема – надзвичайно актуальна, адже, за словами доповідача: «В Україні, як у всьому світі, основною причиною перинатальної смертності залишаються пізні акушерські ускладнення вагітності, які призводять до дистресу плода, внутрішньоутробної загибелі плода, передчасного народження дитини та асфіксії новонародженого.
У спецвипуску медичного часопису The Lancet за 2005 р. (The Lancet. Neonat. Survival, March 2005), присвяченому проблемам перинатології, на величезному світовому статистичному матеріалі по 147 країнах світу визначено, що очікувана пряма причина малюкових смертей лише у 7% випадків пов’язана із природженими вадами розвитку та ХА, натомість 27% припадає на передчасні пологи, 23% – на асфіксію; 75% всіх ранніх неонатальних смертей спричинені саме асфіксією та недоношеністю. Тим не менше, переважна більшість скринінгових (просівних) УЗ- та БХ-досліджень І та ІІ триместрів має на меті саме пошук ХА та вад розвитку плода. На оцінку акушерських ризиків звертається значно менше уваги. Останнім часом у просівних дослідженнях І триместру використовуються такі ехографічні ознаки: товщина КП, наявність кісток носа, розміри верхньої щелепи, кут обличчя, показники кровотоку через тристулковий клапан та у венозній протоці плода; а також БХ-маркери: PAPP-A, b-ХГЛ.
Вперше поєднання БХ та УЗ просівних досліджень І триместру для пошуку ХА були запроваджені у Великій Британії в 1990 роки. Найбільше за обсягом дослідження (8514 вагітностей) серед здійснених у США із використанням маркерів І триместру, показало високий (79%) рівень виявлення ХА при 5% хибнопозитивних результатів. Для визначення найбільш раціонального та ефективного способу пошуку ХА було проведене дослідження FASTER (First and Second Trimester Evaluation of Risk trial, 2003), в якому порівнювались просівні дослідження І і ІІ триместрів та їх сукупні поєднання. Дослідження проводилось у 15 центрах США з грудня 1999 по грудень 2002 рр., дані оцінювались проспективно; доведено, що поєднане використання УЗ- та БХ-ознак І триместру дозволяє ефективно знаходити синдром Дауна.
Також виявлено, що при змінених БХ та УЗ ознаках вагітність частіше протікала із акушерськими ускладненнями. Вважається, що такі акушерські ускладнення як прееклампсія, гіпертензія вагітності, передчасні пологи та синдром затримки внутрішньоутробного розвитку плода (СЗВУРП) мають спільний етіопатогенетичний механізм, одним із основних етапів якого є порушення інвазії трофобласту і перебудови спіральних судин матки. Ці процеси активного проникнення трофобласту в спіральні артерії, що супроводжуються заміщенням ендотелію клітинами цитотрофобласту і знищенням м’язових клітин судинної стінки, за рахунок чого знижується опір кровоплину в басейні маткових артерій, починаються наприкінці І триместру вагітності і відбуваються за активної участі імунних клітин децидуальної оболонки. Порушення цього етапу розвитку можуть мати певні УЗ та БХ ознаки.
Публікацій про можливість використання УЗ та БХ маркерів ППД для прогнозування вже в І триместрі розвитку пізніших акушерських ускладнень наразі небагато, і не можна вважати ці питання розглянутими й вирішеними. У першу чергу це стосується значення допплерометрії кровоплину маткових артерій, об’ємних показників вмісту плодового міхура; зв’язку змінених УЗ і БХ маркерів з пізнішими акушерськими ускладненнями вагітності при підтвердженій відсутності ХА плода», – наголосив лікар. Він також дав декілька важливих рекомендацій – практичний алгоритм, що сприятиме втіленню у життя підходу «Плід як пацієнт», залученню до співпраці ще на допологовому етапі (за необхідності) неонатологів та членів самої родини для оптимізації перинатальної допомоги дітям.
«Внутрішньоутробні інфекції – невидимий ворог: ізолюємо та нейтралізуємо»
 В. І. Ошовський, к. мед. н., каф. акушерства, гінекології та медицини плода НМАПО ім. П. Л. Шупика:
В. І. Ошовський, к. мед. н., каф. акушерства, гінекології та медицини плода НМАПО ім. П. Л. Шупика:
«Сучасний лікар має у своєму арсеналі досить широкий спектр методів дослідження на наявність інфекції під час вагітності: окрім клінічного, методи, що дозволяють оцінити стан фетоплацентарної системи; мікробіологічні та серологічні дослідження; ПЦ-діагностика, яка дозволяє встановити не тільки факт наявності інфекції, але і її збудник; ми знаємо і враховуємо всі відомі фактори ризику, але…
Попри стрімкий розвиток діагностичних можливостей, інфекції залишаються на першому місці серед причин перинатальних втрат не тільки в Україні, а й у світі (це висновок на підставі аналізу статистики у 193-х країнах світу). Постає логічне питання: чому? Насправді (і в цьому з нами згодні наші західноєвропейські колеги), кількість антенатальних втрат від інфекцій дещо перебільшена.
Вивчаючи дані з багатьох країн світу, зокрема, і України, ми дійшли невтішного висновку: інфекції є таким собі «цапом відбивайлом», завдяки якому легко чимало приховати, у тому числі, неадекватні дії медичного персоналу. Так, інфекцію буває важко запідозрити, підтвердити, але не можна списувати все на інфекції.
Тож, нам всім потрібно багато працювати у над тим, аби вчасно виявляти хворобу, вчасно розпочинати лікування, але тільки тоді, коли це насправді потрібно! Адже дуже важливо, аби лікар, що призначає вагітній жінці, наприклад, антибіотикотерапію, замислювався над такими питаннями: призначення стосується лікування тільки жінки? І якими можуть бути віддалені наслідки для плода від такого лікування?
Безумовно, є випадки, коли антибіотик доводиться призначати вагітній, але на це мають бути дуже серйозні підстави, тож таке рішення має бути виваженим і обережним.
Іншими словами, ми робимо тільки усвідомлені і ефективні кроки, в правильному напрямку і в правильний час. Цього правила потрібно дотримуватися як у діагностиці, так і в лікуванні.
За правило потрібно взяти також наступне: якщо під час вагітності була підозра на гостре інфікування, акушер-гінеколог просто зобов’язаний забезпечити адекватну наступність з неонатологом. Адже, виписавши такого новонародженого на третю добу, ми ризикуємо приректи його на інвалідність або навіть смерть», – наголосив спікер.
«Материнський дзеркальний синдром»
 М. П. Веропотвелян, гол. лікар Криворізького міжобласного центру медичної генетики і пренатальної діагностики
М. П. Веропотвелян, гол. лікар Криворізького міжобласного центру медичної генетики і пренатальної діагностики
«Для багатьох лікарів акушерів-гінекологів, у тому числі, вітчизняних, за цією назвою криється суцільне задзеркалля: причини патології, сучасні можливості її лікування тощо залишаються «в тіні».
Mirror syndrome або материнський дзеркальний синдром (МДС) – рідкісний стан, що характеризується вираженою водянкою плода як імунної, так і неіммунної етіології, що супроводжується також полісерозитом (водянкою) матері. Частота, з якою зустрічається МДС, не встановлена.
МДС вперше був описаний John William Ballantyne у 1882 р. Але за 130 років, що минуло з тих пір, у літературі описано трохи більше 100 спостережень МДС, у т. ч. під епонімом с. Баллентайн та іншими різними назвами у перекладі з англомовної літератури: материнський набряковий синдром, псевдотоксемія, потрійний набряк, токсемія вагітності, гострий гестоз ІІ трим. вагітності, раптова рання прееклампсія. Хоча етіологія МДС точно не встановлена, відомі стани, при яких він найчастіше розвивається: резус-ізоіммунізація (29%), фето-фетальний трансфузійний синдром (ФФТС), синдром зворотної артеріальної перфузії (18%), вірусні інфекції (16%), ВПР плода (переважно серцеві аномалії, аритмії, пухлини плоду і плаценти (37,5%). Серед аномалій, що призводять до синдрому, описані випадки аневризми вени Галена, аномалія Ебштейна, крижово-куприкова тератома, хоріангіома плаценти, у патогенезі яких в результаті гіперволемії і порушення внутрішньосерцевої гемодинаміки виникає серцево-судинна недостатність, а надалі – водянка плода і розвиток клініки МДС. Описано випадок розвитку МДС після внутрішньоутробної дилятації стенозованого клапана аорти у плода.
Зазвичай клініка МДС розвивається в період з 22,5 до 27,6 тижнів гестації. Клінічна картина у матері крім водянки (80–100%), може супроводжуватися помірною гіпертензією (57–78%) і протеїнурією (20–56%), помірною анемією (46,4%), підвищенням рівня печінкових ферментів (19,6%), сечової кислоти і креатиніну (25%), олігурією (16,1%), головним болем і порушеннями зору (14,3%), тромбоцитопенією (7,1%).
У половині спостережень може розвиватися прееклампсія. Однак, наявність всіх симптомів спостерігається не у всіх випадках. Обов'язковим проявом МДС вважається водянка (полісерозит) матері, що ускладнюється набряком легенів в 21,4%. У більшості спостережень природний перинатальний результат несприятливий. Антенатальна смерть настає в 56% випадків, в той же час описані нечисленні спостереження спонтанного зникнення клінічної картини МДС у матері і плоду при інфекційній природі синдрому, викликаній парвовірусом В19, селективної редукції одного найбільш ураженого плоду при ФФТС, а також після терапевтичної корекції тахіаритмії плода. Описаний випадок успішного результату з неімунною водянкою внаслідок крижово-куприкової тератоми. Клінічна картина МДС у матері зазвичай зникає за 4,8–13,5 днів після пологів. У важких випадках в ранньому післяпологовому періоді розвивається клініка, подібна до прееклампсії з олігоурією і ексудатом легенів.
Для пролонгування вагітності до терміну розродження життєздатним плодом (на тлі профілактики РДС синдрому) при вираженому багатоводді проводиться амніоредукція, у разі гідротораксу виконується фетальний торакоцентез з установкою плеврально-амніотичного дренажу. Описано проведення селективного фетоциду аномального плода при дискордантній двійні. Вибір способу розродження безальтернативно схиляється на користь операції кесаревого розтину», – повідомив спікер. Він також представив колегам і прокоментував рідкісний випадок спостереження МДС при неіммунній водянці плоду, викликаної аномалією судин пуповини (докладно цей клінічний випадок описано у публікації журналу «Здоров'я жінки» №2 за 2013 р.).
Наприкінці доповіді Миколи Петровича Веропотвеляна, професор С. І. Жук звернулася до присутніх з проханням взяти активну участь у формуванні українського архіву пацієнтів з МДС: «Колеги, велике прохання, надсилайте відомості про таких пацієнтів до Київського перинатального центру, до інших центрів, бо тільки об’єднавшись, ми зможемо надавати їм кваліфіковану медичну допомогу», – наголосила професор.
P.S. За відгуками учасників заходу, можна із стовідсотковою впевненістю стверджувати, що конференція відбулася. Адже, окрім безлічі корисної інформації, представленої спікерами, була жвава, ефективна дискусія, обмін думками, ідеями та досвідом висококласних спеціалістів, небайдужих до своєї професії.
ДетальнішеПРЕЕКЛАМПСІЯ/ ЕКЛАМПСІЯ
Стандартизація надання допомоги з позиції доказової медицини
Гіпертензивні розлади під час вагітності (у тому числі прееклампсія) є однією з найбільш поширених причин материнської захворюваності, тривалої інвалідності та летальних наслідків в усьому світі. Прееклампсія становить собою клінічно маніфестовану форму гестаційної ендотеліопатії та пов’язана з материнськими симптомами гіпертонії та протеїнурії. Епідеміологічні дані свідчать про те, що в останні два десятиріччя у загальній популяції вагітних жінок частота прееклампсії утримується на рівні 10–12%, а еклампсії – 0,05% [1].
Незважаючи на досягнення сучасної медицини, прееклампсія залишається однією з провідних причин материнської смертності, займаючи впродовж останніх десяти років 3–4 місце у структурі причин материнської смертності після кровотеч та сепсису [5, 6].
За даними ВООЗ, у 2003–2007 рр. у 115 країнах, внаслідок ускладнень, пов’язаних із артеріальною гіпертензією, у період вагітності померло 343 000 жінок, що склало 14% від загальної кількості материнських смертей [5].
 Прееклампсія також відіграє значну роль і в структурі перинатальної смертності. Порівняно з перинатальною смертністю в цілому в Україні (14,8–16,5‰), при прееклампсії вона становить, за даними різних авторів, від 10 до 30 ‰ [3]. Крім того, прееклампсія є причиною важкої захворюваності, інвалідизації матерів та їхніх дітей [1, 6]. Водночас, при належному міждисциплінарному менеджменті більшість випадків несприятливих результатів є попереджуваними. Оскільки наслідки важких гіпертензивних розладів знижують якість подальшого життя жінки (висока частота атеросклерозу, цукрового діабету, серцево-судинних захворювань), а частота порушення фізичного, психосоматичного розвитку передчасно народжених дітей є досить високою, так само як і ризик розвитку у них соматичних захворювань у майбутньому, то ця проблема є значущою у соціальному та медичному плані.
Прееклампсія також відіграє значну роль і в структурі перинатальної смертності. Порівняно з перинатальною смертністю в цілому в Україні (14,8–16,5‰), при прееклампсії вона становить, за даними різних авторів, від 10 до 30 ‰ [3]. Крім того, прееклампсія є причиною важкої захворюваності, інвалідизації матерів та їхніх дітей [1, 6]. Водночас, при належному міждисциплінарному менеджменті більшість випадків несприятливих результатів є попереджуваними. Оскільки наслідки важких гіпертензивних розладів знижують якість подальшого життя жінки (висока частота атеросклерозу, цукрового діабету, серцево-судинних захворювань), а частота порушення фізичного, психосоматичного розвитку передчасно народжених дітей є досить високою, так само як і ризик розвитку у них соматичних захворювань у майбутньому, то ця проблема є значущою у соціальному та медичному плані.
У Вінницькій області, згідно даних офіційної статистичної звітності, представлених у довіднику основних показників діяльності установ охорони здоров’я Вінницької області, у 2014 році частота прееклампсії склала 30,8 випадків на 1000 пологів.
Таким чином, прееклампсія є тяжким ускладненням вагітності, а висока частота материнських та перинатальних втрат змушує позиціонувати її як важливу медико-соціальну проблему. Оптимізація надання медичної допомоги з метою профілактики та лікування гіпертензивних порушень у жінок – важливий крок на шляху до досягнення цілей, сформульованих у «Декларації тисячоліття» ООН [8].
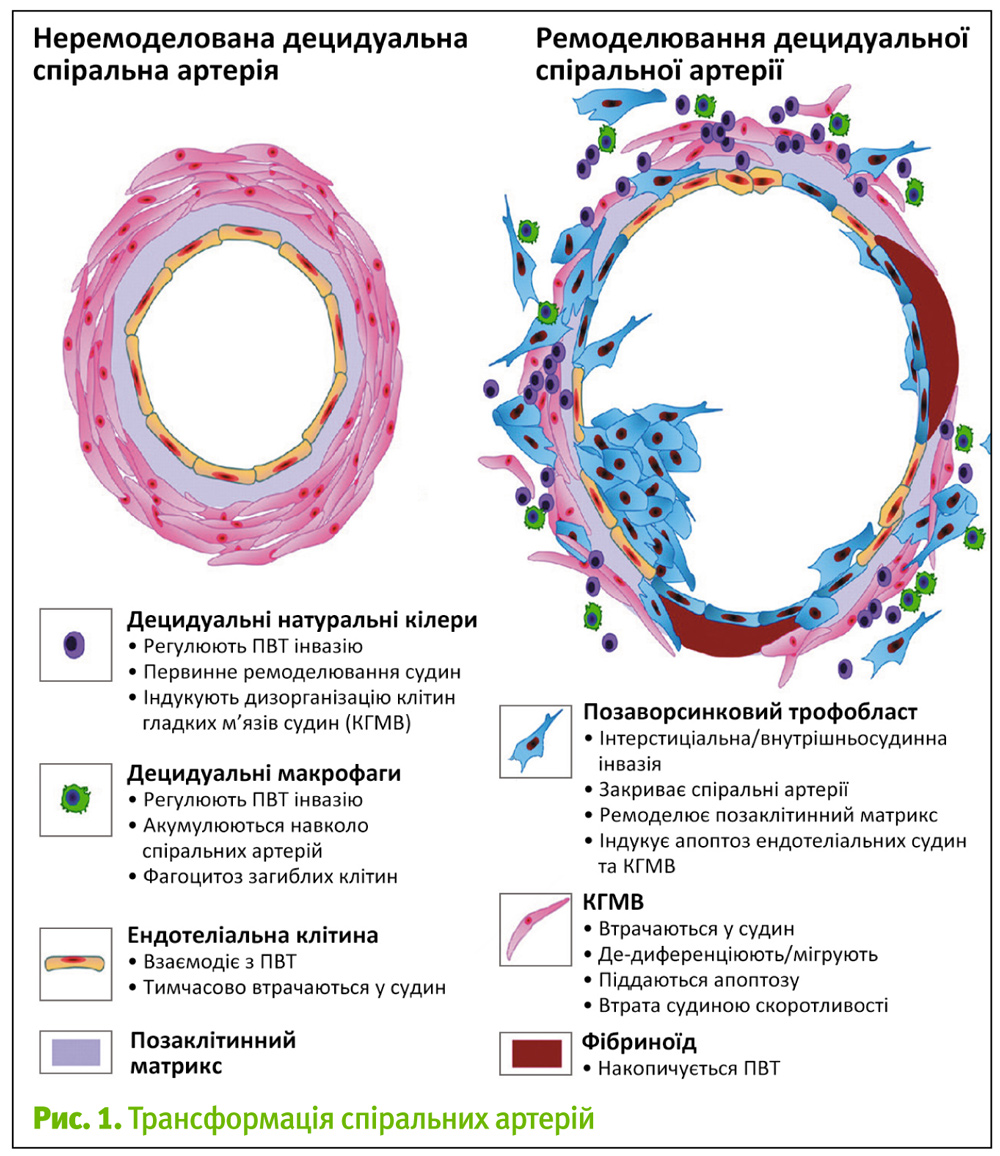
Основи прееклампсії закладаються у момент міграції цитотрофобласта.
Відбувається гальмування міграції трофобласта у спіральні артерії матки, тобто недостатність другої хвилі інвазії цитотрофобласта.
На думку ряду дослідників, факторами, котрі знижують інвазивну здатність трофобласта, є порушення відносин між гуморальним і трансплантаційним імунітетом з одного боку та імунологічною толерантністю – з іншого; мутації генів, відповідальних за синтез сполук, що регулюють тонус судин (ендотеліну-1, NO); блокаду інгібіторів фібринолізу.
При неповноцінній інвазії цитотрофобласта, спіральні артерії не піддаються морфологічним змінам, характерним для вагітності, тобто не відбувається трансформації їх у плацентарні судини.
Зазначені морфологічні особливості спіральних судин матки в міру прогресування вагітності призводять до їх спазму, зниження міжворсинчатого кровоплину та гіпоксії. Неповне закриття просвіту спіральних артерій цитотрофобластичними заторами та передчасний початок матково-плацентарного кровоплину у центральних відділах, що призводить до надмірного надходження материнської крові у міжворсинчатий простір, сприяє механічній дії на хоріон та виникненню оксидативного стресу.
Ішемічно-гіпоксичні зміни, котрі розвиваються у плацентарній тканині, сприяють активізації факторів (молекули клітинної адгезії), що призводять до порушення структури й функції ендотелію або зниження біохімічних сполук (аргінін), які захищають ендотелій від пошкоджень.
Виділяють дві стадії розвитку судинної дисфункції при прееклампсії.
На першому етапі виникає гемодинамічна мальадаптація до вагітності та субоптимальний розвиток плаценти. У результаті порушеної плацентації в цьому органі виробляється ряд біологічно активних речовин.
На другому етапі розвивається пізня судинна дисфункція, що характеризується в основному ендотеліальною дисфункцією. Остання призводить до клінічного синдрому прееклампсії.
Розвитку гестаційної ендотеліопатії сприяють: активація перекисного окислення ліпідів, підвищення активності фосфоліпаз, циркулюючих нейрогормонів (ендотелін, катехоламіни), тромбоксану, зниження активності інгібітора протеаз a2-макроглобуліну, наявність вроджених дефектів гемостазу.
Зміни ендотелію при прееклампсії є специфічними. Розвивається своєрідний ендотеліоз, який виражається у набуханні цитоплазми з відкладенням фібрину навколо базальної мембрани та усередині набряклої ендотеліальної цитоплазми.
Ендотеліоз спочатку має локальний характер в судинах плаценти і матки, потім поширюється на інші органи.
Гестаційна ендотеліопатія призводить до ряду змін, які обумовлюють клінічну картину прееклампсії.
- При ураженні ендотелію блокується синтез вазодилататорів (простациклін, С-натрійуретичний пептид, ендотеліальний релаксуючий чинник – NO), внаслідок чого порушується ендотелійзалежна дилятація.
- При ураженні ендотелію на ранніх термінах вагітності відбувається оголення м’язово-еластичної мембрани судин з розташованими в ній альфа-рецепторами, що призводить до підвищення чутливості судин до вазоактивних речовин.
- Знижуються тромборезистентні властивості судин. Пошкодження ендотелію знижує його антитромботичний потенціал внаслідок порушення синтезу тромбомодуліну, тканинного активатора плазміногену, підвищення агрегації тромбоцитів з подальшим розвитком хронічної форми синдрому дисемінованого внутрішньосудинного згортання крові.
- Активуються фактори запалення, перекисні радикали, цитокіни, котрі, в свою чергу, додатково порушують структуру ендотелію.
- Підвищується проникність судин. Ураження ендотелію поряд із зміною синтезу альдостерону та затримкою, у відповідь на це, натрію та води в клітинах, сприяє патологічній проникності судинної стінки та виходу рідини із судин.
У результаті цього створюються додаткові умови для генералізованого спазму судин, артеріальної гіпертензії, набрякового синдрому.
На тлі прогресування спазму судин, гіперкоагуляції, підвищення агрегації еритроцитів і тромбоцитів і, відповідно, збільшення в’язкості крові формується комплекс мікроциркуляторних порушень, котрі призводять до гіпоперфузії органів (печінки, нирок, плаценти, мозку та ін.).
Поряд із спазмом судин, порушенням реологічних та коагуляційних властивостей крові, у розвитку адекватного гемозабезпечення вагітності важливу роль відіграють зміни макрогемодинаміки, зниження об’ємних показників центральної гемодинаміки: ударного об’єму, хвилинного об’єму серця, об’єму циркулюючої крові (ОЦК), що є значно меншими, ніж при фізіологічному перебігу вагітності.
Низькі значення ОЦК при прееклампсії обумовлені як генералізованою вазоконстрикцією і зниженням обсягу судинного русла, так і підвищеною проникністю судинної стінки та виходом рідкої частини крові в тканини.
Одночасно з цим причиною збільшення кількості інтерстиціальної рідини при прееклампсії виступає дисбаланс колоїдно-осмотичного тиску плазми та тканин, котрі оточують судини, що зумовлене, з одного боку, гіпопротеїнемією, а з іншого – затримкою натрію в тканинах та підвищенням їх гідрофільності.
В результаті у вагітних з прееклампсією формується характерне парадоксальне поєднання: гіповолемія та затримка великої кількості рідини в інтерстиції, що посилює порушення мікрогемодинаміки.
Дистрофічні зміни у тканинах життєво важливих органів багато в чому формуються внаслідок порушення матричної та бар’єрної функцій клітинних мембран. Зміни матричної функції мембран полягають у відхиленні механізму дії різних мембранних білків (транспортних, ферментних, рецепторів гормонів та білків, пов'язаних з імунітетом), що призводить до зміни функцій клітинних структур.
Порушення бар’єрної функції ліпідного шару мембран призводить до зміни функціонування каналів для іонів Ca2+. Масивний перехід іонів Ca2+ в клітину викликає в ній незворотні зміни, енергетичний голод і загибель, з одного боку, а з іншого – м’язову контрактуру та спазм судин. Ймовірно, що еклампсія обумовлена саме порушенням проникності мембран та масивним переміщенням іонів Ca2+ в клітину («кальцієвий парадокс»).
Патологічні зміни, пов’язані з прееклампсією, найбільшою мірою поширюються на канальцевий апарат нирок (гломерулярно-капілярний ендотеліоз), що проявляється дистрофією звивистих канальців з можливою десквамацією та розпадом клітин ниркового епітелію.
Зміни в печінці представлені паренхіматозною та жировою дистрофією гепатоцитів, некрозом та крововиливами. Некрози можуть бути як вогнищевими, так і поширеними. Крововиливи є частіше множинними, різної величини, через них виникає перенапруження капсули печінки, аж до її розриву.
Функціональні та структурні зміни мозку при прееклампсії варіюють в широких межах. Вони зумовлені порушенням мікроциркуляції, утворенням тромбозів в судинах з розвитком дистрофічних змін нервових клітин і периваскулярних некрозів. Характерним (особливо при тяжкій прееклампсії) є набряк головного мозку з підвищенням внутрішньочерепного тиску. Комплекс ішемічних змін, у кінцевому підсумку, може обумовлювати напад еклампсії.
При прееклампсії спостерігаються виражені зміни у плаценті: облітеруючий ендартеріїт, набряк строми ворсин, тромбоз судин і межворсинчатого простору, некроз окремих ворсин, вогнища крововиливу, жирове переродження плацентарної тканини. Зазначені зміни призводять до зниження матково-плацентарного кровоплину, плацентарної дисфункції, затримки розвитку плода.
У рекомендаціях з профілактики та лікування прееклампсії та еклампсії 2011 року підкреслюється, що більшість летальних наслідків, спричинених гіпертензивними порушеннями, можна уникнути за умови, що жінкам, які страждають від подібних ускладнень, буде надана своєчасна й ефективна медична допомога. Розробка та впровадження доказово обґрунтованих протоколів сприятимуть стандартизації та уніфікації діагностики та лікування, застосуванню методики лікування з доведеною ефективністю, що, в свою чергу, дозволить знизити материнську смертність за рахунок зменшення частоти загрожуючих життю ускладнень прееклампсії (інсультів, дихальних порушень та т. п.) [7]. Водночас, на теперішній час в Україні відсутній єдиний підхід до надання невідкладної допомоги при прееклампсії та еклампсії, багато методів лікування не відповідають критеріям, прийнятим в медицині, що заснована на доказах. Адже, як зазначає професор В. І. Медведь, в нашій країні залишається чинним протокол лікування прееклампсії, прийнятий більше 10 років тому, хоча у Європі після 2004 року відбулося три перегляди настанов щодо артеріальної гіпертензії у вагітних [2].
Все викладене вище визначає безсумнівну актуальність розробки та впровадження стандартизованого алгоритму дій надання невідкладної допомоги при тяжкій прееклампсії/еклампсії, оскільки саме вони визначають материнську смертність.
У зв’язку з цим, нами було здійснено спробу стандартизувати дії медичного персоналу у випадках прееклампсії/еклампсії. Процес складання стандарту дій включав наступні етапи:
1) збір сучасних доказів, заснованих на наукових дослідженнях;
2) формулювання рекомендацій на основі аналізу та узагальнення наукових доказів та результатів власних досліджень;
3) планування поширення та впровадження, оцінка результатів впровадження.
При підготовці «Стандарту дій медичного персоналу при наданні медичної допомоги при прееклампсії/еклампсії» нами були вивчені існуючі рекомендації провідних світових організацій: World Health Organization, Society of Obstetricians and Gynaecologists of Canada (SOGC), American Academy of Family Physicians, Royal College of Obstetricians and Gynaecologists (RCOG), International Federation of Obstetrics and Gynecology (FIGO), College National des Gynecologues et Obstetriciens Francais, American College of Obstetricians and Gynecologists (ACOG), а також було проведено пошук найкращих доказів у найбільш авторитетних міжнародних джерелах, зокрема, в Кокранівському спеціалізованому регістрі контрольованих випробувань в розділі «Вагітність та пологи» станом на січень 2015 року. Перевага надавалася тим рекомендаціям, котрі були підтверджені в дослідженнях більш високої якості.
Аналізуючи сучасні протоколи з лікування прееклампсії, необхідно відзначити, що на сьогодні практичні рекомендації засновані на трьох рівнях доказів: 1-й – стандарт, котрий необхідно застосовувати обов’язково; 2-й – рекомендації, які застосовувати бажано; 3-й – опціонна інформація, яка застосовується на розсуд.
Обґрунтуванням заходів, внесених до «Стандарту дій медичного персоналу при наданні медичної допомоги при прееклампсії/еклампсії», стали наступні докази 1-го рівня:
- мета антигіпертензивної терапії – рівень артеріального тиску (АТ) нижче 160/110 мм рт. ст. (І-А) [4];
- при АТ в межах 150–160/100–110 мм рт. ст. (помірна гіпертензія) рішення про призначення антигіпертензивної терапії приймається в індивідуальному порядку (І-А) [4];
- стартова антигіпертензивна терапія в умовах стаціонару повинна бути розпочата з ніфедипіну короткої дії (І-А), альтернативним антигіпертензивним препаратом є метилдопа (I-B) [4];
- преференції при виборі гіпотензивного препарату та способу його введення при тяжкій гіпертензії під час вагітності залежать в першу чергу від досвіду лікаря-консультанта, що призначає даний препарат, вартості препарату і його наявності в даному регіоні; немає переконливих доказів переваг якого-небудь препарату для зниження АТ при тяжкій гіпертензії при вагітності. Вибір препарату повинен бути заснований на досвіді застосування у конкретному закладі (І-A) [8];
- MgSO4 не рекомендується як антигіпертензивний агент (І-Е) [4];
- протисудомна терапія показана при тяжкій прееклампсії (І-А) [4];
- MgSO4 є препаратом першої лінії профілактики та лікування судом (I-A) [4, 8];
- MgSO4 повинен бути використаний у стандартному дозуванні; зазвичай, навантажувальна доза – 4 г, після чого – 1 г/год. (I-A) [4, 8];
- бензодіазепіни не повинні використовуватися для профілактики або лікування судом, крім випадків неефективності MgSO4 або при наявності протипоказань до MgSO4(I-E) [4];
- при проведенні інфузійної терапії до пологів слід обмежити об’єм рідини, що вводиться, до 80 мл/год. при збереженому діурезі (не менше 50 мл/год.) з урахуванням випитої рідини (І-А); перевагу надати збалансованим кристалоїдним розчинам (Рингер, Стерофундин); у жінок з прееклампсією збільшення об’єму плазми не рекомендується (I-E) [4];
- для лікування стійкої олігурії допамін та фуросемід не рекомендуються (I-E) [4];
- при терміні гестації >37 тижнів – розродження впродовж 24–48 годин (І-A) [4].
Із доказів 2-го рівня прийняті рекомендації, котрі стосуються наступних положень:
- ніфедипін і MgSO4 можуть бути використані одночасно (II-2B) [4];
- інгібітори ангіотензинперетворюючого ферменту (АПФ) та блокатори рецепторів ангіотензину не слід використовувати під час вагітності (II-2E) [4];
- внутрішньовенне та пероральне введення рідини повинні бути мінімізовані у жінок з прееклампсією для попередження набряку легенів (II-2B) [4].
Із доказів 3-го рівня рекомендуються наступні:
- інфузійна терапія не повинна проводитися рутинно для лікування олігурії (< 15 мл/год. впродовж 6 год.) (III-D) [4];
- каптоприл per os рекомендується тільки після розродження (III-В) [4];
- антигіпертензивна терапія при годуванні грудьми включає наступні препарати: ніфедипін, каптоприл, еналаприл (III-B) [4].
При тяжкій прееклампсії розвиток ускладнень пов’язаний з відсутністю адекватного моніторингу, котрий показний пацієнткам з АТ≥160/110 мм рт. ст., жінкам, які отримують магнезіальну терапію, та, особливо, при наявності ознак порушення водно-електролітного обміну та/або зниженням діурезу ≤100 мл за 3–4 год. Крім стандартного системного моніторингу жінок, які отримують магнезіальну терапію, важливим є моніторування колінних рефлексів (кожні 30 хв.), неврологічного стану та даних ЕКГ (кожні 24 год.). Обов’язковим є контроль ознак набряку легенів – SрО2, аускультація легень, за показами – рентгенографія легень. Рутинне застосування моніторингу центрального венозного тиску (ЦВТ) не рекомендується (ІІ-2D). Катетеризація центральної вени та моніторинг ЦВТ рекомендується при діурезі ≤100 мл впродовж 3–4 год.
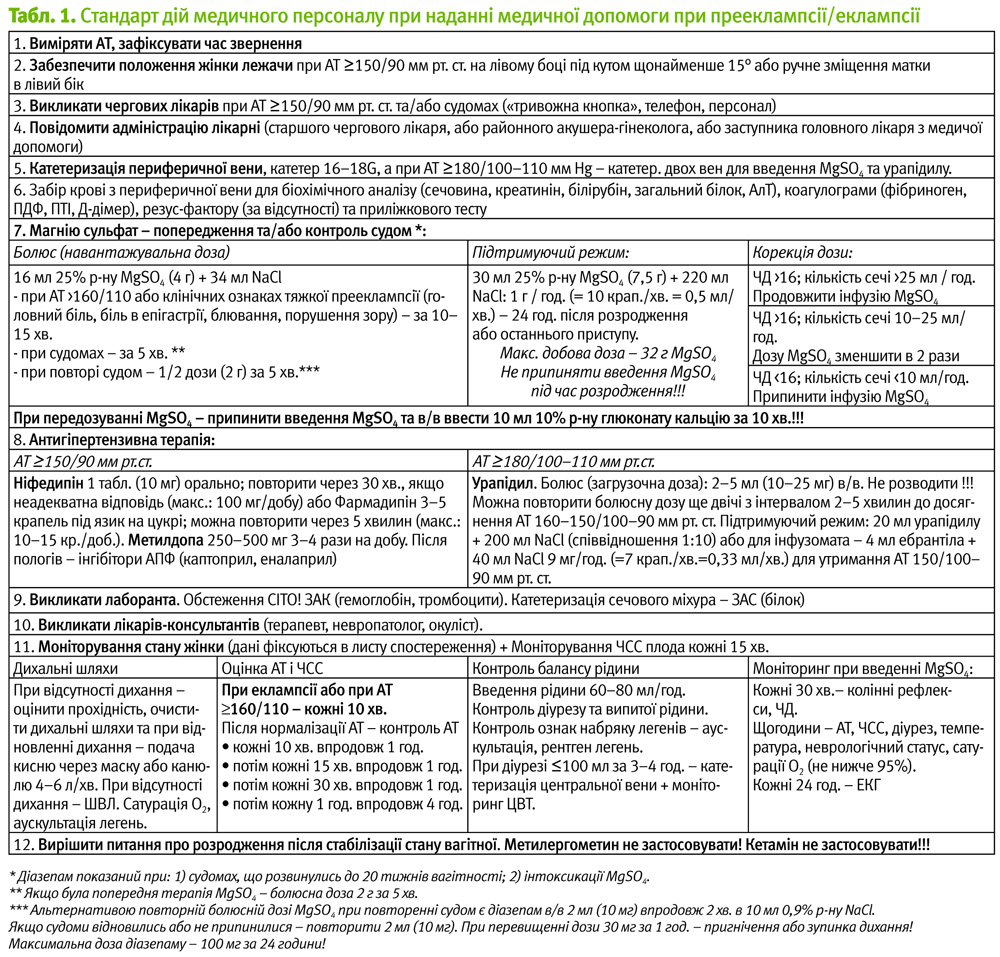
Розроблений нами «Стандарт дій медичного персоналу при наданні медичної допомоги при прееклампсії/еклампсії» містить виключно алгоритм дій лікарів, середнього та молодшого медичного персоналу та організаційні рішення з їхньої реалізації (табл. 1).
У разі появи нових даних, котрі заслуговують на увагу, у «Стандарт дій медичного персоналу при наданні медичної допомоги при прееклампсії/еклампсії» будуть внесені відповідні зміни.
Висновок
Розроблено «Стандарт дій медичного персоналу при наданні медичної допомоги при прееклампсії/еклампсії», котрий дозволить здійснити стандартизацію та уніфікацію моніторину та надання невідкладної допомоги жінкам цієї категорії із застосуванням методик лікування з доведеною ефективністю. Впровадження доказово обгрунтованого стандарту дій вірогідно сприятиме зниженню материнської смертності за рахунок зменшення частоти загрожуючих життю ускладнень прееклампсії. «Стандарт дій медичного персоналу при наданні медичної допомоги при прееклампсії/еклампсії» складається з алгоритму дій середнього медичного персоналу, алгоритму дій лікарів та медикаментозної терапії (магнезіальна терапія, антигіпертензивні препарати), переліку додаткових методів дослідження та алгоритму моніторингу.
Перелік літератури знаходиться у редакції.
Детальніше
ТРАДИЦІЇ ФІТОТЕРАПІЇ
На благо здоров'я жінки
Незважаючи на значний розвиток медицини, невтішною ознакою сучасності залишається неухильне зростання кількості пацієнтів з різними патологіями, зокрема, молочної залози. Більш того, на сьогодні вже мало хто не погодиться з твердженням, що це данина, яку ми вимушені платити цивілізації. Проте, і цей виклик медики змушені прийняти і докласти максимум зусиль для поліпшення ситуації.
Про деякі аспекти даної проблеми ми говоримо сьогодні з лікарем-мамологом Юрієм Ярославовичем Присташем
— Юрій Ярославович, наскільки актуальна проблема захворювань молочної залози? Які тенденції захворюваності?
— Проблема є кричущою! Адже за останні 20 років захворюваність зросла у всьому світі щонайменше у 2,5 рази. За даними ВООЗ та її підрозділу, Міжнародної агенції з дослідження раку, в країнах ЄС щороку на цю недугу хворіє близько 216 тисяч осіб і понад 80 тисяч помирає. Смертність у більшості країн Європи має тенденцію до повільного, але постійного зростання, хоча показники значно відрізняються в різних країнах. Найвищий рівень захворюваності у Нідерландах (91,6 на 100 тис. жіночого населення), Данії (86,2), Франції (83,2), Бельгії (82,2), Швеції (81). Для порівняння: в Іспанії — 47,9, Греції — 47,6, Латвії — 42,2.
В Україні цей показник трохи нижчий – приблизно 60 на 100 тис. жіночого населення. Натомість, пік захворюваності зростає: щороку ми додаємо 2–2,5%. Щодо смертності, то ми, на жаль, випереджаємо всі країни Європи. Достатньо сказати, що в Україні кожна п’ята жінка, яка вперше захворює на рак молочної залози, помирає протягом року з моменту виявлення хвороби, що свідчить про високу кількість занедбаних випадків. Тож очевидно, що для нас патології молочної залози, онкологічні проблеми і, зокрема, рак молочної залози становлять величезну проблему і алгоритм виявлення і вчасного надання медичної допомоги цим пацієнтам потребує вдосконалення. Отже акцент має зміщуватися у бік профілактики.
— Яка структура захворюваності молочної залози в Україні і як ці дані співвідносяться зі світовою статистикою?
— У структурі жіночої смертності рак молочної залози вже довгі роки залишається на першому місці, рак легень – на другому, і вже далі йдуть інші гінекологічні проблеми (рак шийки матки тощо).
— Які основні причини розвитку захворювань молочної залози?
— Причин багато. Це, по-перше, гінекологічні проблеми, зокрема, дисгормональні розлади; пізня вагітність; величезна кількість абортів; неконтрольоване тривале вживання оральних контрацептивів; сексуальні розлади; ендокринні порушення (порушення роботи ендокринних органів, таких як щитоподібна залоза. На цьому аспекті зараз зосереджена величезна увага і ведуться певні дослідження). Ну і, звичайно, стиль, спосіб життя, стресові ситуації, ненормований робочий день, контакт з різними хімічними речовинами тощо. Власне, такий поліморфізм різноманітних провокуючих факторів і сприяє зростанню захворюваності.
— Яка епідеміологія мастопатії?
— Мастопатія виникає у 30–40% жінок, пік захворюваності припадає на 45 років. Потрібно також враховувати дані наукових досліджень, які свідчать: при мастопатії з гіперпластичними процесами ризик розвитку раку зростає в 2,6 рази, при атипових змінах – у 6 разів.
— Розкажіть, будь ласка, про сучасні методи діагностики гормонозалежних захворювань МЗ?
— Діагностика складається з двох етапів: первинна й уточнена. До первинної належить самоогляд пацієнток і огляд лікарями інших спеціальностей. Першим етапом є детальне вивчення анамнезу життя і захворювання, огляд і пальпація залози. При зборі анамнезу необхідно звернути увагу на:
- перенесені та супутні захворювання печінки, щитоподібної залози, статевих та інших органів і систем, які можуть викликати багато гормональних порушень в організмі й обумовити виникнення пухлинного процесу в молочних залозах;
- гінекологічний і репродуктивний анамнез;
- сексуальну функцію;
- соціально-побутову характеристику і професійні фактори;
- спадковість.
Первинна діагностика клінічних форм РМЗ дозволяє у більшості пацієнток із поширеними формами захворювання поставити правильний діагноз. Але при початкових формах хвороби клінічна оцінка характеру патологічного процесу в молочній залозі буває складною. У цьому випадку для уточнення діагнозу ми використовуємо інші методи дослідження – інструментальні та лабораторні.
По-перше, це рентгенологічне дослідження молочних залоз (мамографія) та ультрасонографія. Ці методи можуть доповнювати один одного, але потрібно враховувати відповідний віковий бар’єр: якщо це жінка після 40 років – найчастіше виконується мамографія, для молодих жінок більш показана ультрасонографія. Все це має супроводжуватися морфологічною верифікацією: у залежності від ситуації, ми беремо або тонкоголкову біопсію, або виконуємо гістологічне морфологічне дослідження і тоді вирішуємо, чи вже маємо діагноз, чи пацієнтка потребує ще дообстеження. Зараз ми маємо на озброєнні й більш сучасні методи обстеження – імуноферментні аналізи, які нам показують рецепторний статус пухлини. За потреби, виконують такий високоінформативний метод як магнітно-резонансна томографія.
Отже наразі існує достатньо засобів для того, щоби уточнити діагноз і, відповідно вирішити, які саме підходи до лікування кожної конкретної пацієнтки можна застосувати.
— Чи можна виділити групу ризику жінок, найбільш схильних до мастопатії?
— Таких пацієнток досить багато. В основному, йдеться про молодих жінок. Отже, оскільки мастопатії можна вважати фоновим станом, який може спричинити у подальшому рак молочної залози, фактори ризику майже співпадають з тими, що сприяють і розвитку раку молочної залози: гінекологічний і репродуктивний анамнез; пізні пологи; велика кількість абортів; вживання гормональних препаратів; неконтрольоване або без відповідних показань вживання великої кількості контрацептивів (часто пацієнтки самі їх собі призначають без консультації з гінекологом); побутові проблеми: нерегулярне одноманітне харчування, недосипання; стресові ситуації тощо. Тобто все те, що супроводжує, на жаль, сучасну жінку в її повсякденному житті. Відповідно, рівень захворюваності є високим саме у високорозвинених країнах, адже все, що ми перерахували вище – фактори, які сприяють розвитку мастопатії і всі вони, на жаль, є сучасними реаліями, з якими жінкам у цих країнах доводиться стикатися щодня.
— Яка оптимальна тактика спостереження, лікування та профілактики жінок при виявленні доброякісних новоутворень МЗ?
— Є різні форми мастопатії: дифузна, дифузна фіброзно-кістозна, змішана, вузлова. Але остання – вузлова – форма нас найбільше насторожує. Вузол, що утворився в молочній залозі, потребує відповідного дообстеження на предмет виявлення проліферативних змін (фактично, передракового стану), і до таких пацієнток має бути особливо уважне ставлення, їх потрібно ретельно обстежувати, але, обираючи тактику лікування, не слід забувати, що вузлова мастопатія – це наслідки всіх тих процесів, провокуючих факторів, про які ми вже сьогодні говорили, а не причина. Отже, якщо, наприклад, застосувати хірургічний метод – це буде не більше, ніж ліквідація наслідків, у той час як причина залишиться. Насправді причина є поліорганною, починаючи з дисгормональних змін, закінчуючи способом життя і соціально-побутовими чинниками. Відповідно, ставлення до оперативного лікування цієї патології останнім часом змінилося і стало дуже обережним. Адже за деякий час після хірургічного лікування, пацієнтка знову приходить до лікаря з тими ж самими проблемами, що свідчить про те, що операція не усуває причину захворювання.
Отже потрібен комплексний підхід. У кожної пацієнтки з діагнозом «мастопатія» слід виявити основну причину або фон, на якому розвинулося захворювання (хронічний запальний процес у статевих органах, дисфункція яєчників, захворювання щитоподібної залози, печінки в поєднанні з функціональними розладами нервової системи). Лікування слід починати з впливу на виявлену причину, що у ряді випадків може позитивно позначитися на проявах дифузної мастопатії. Існує велика кількість препаратів, вітамінних комплексів, які застосовуються лікарями у цих випадках. Але у своїй практиці ми користуємось, в основному, фітогормонами – фітоестрогенами природного походження, які найбільш споріднені організму жінки і найбільш плавно регулюють всі проблеми, пов’язані з цією системою, бо якщо говорити про лікування гормональними препаратами, то в цьому випадку вони можуть призвести до погіршення стану. В той час, як фітопрепарати добре переносяться, усувають больовий синдром і, зрештою, виконують головну свою функцію – перешкоджають наростанню мастопатії.
— У даний час на ринку з'являються численні БАДи в тому числі для лікування ФКМ (фіброзно-кістозної мастопатії), чи можна їх розглядати як альтернативний засіб лікування та профілактики захворювань молочних залоз?
– Стосовно БАДів, мушу сказати, що потрібно прагнути користуватися виключно препаратами з доказовою медичною базою. Тобто такими, що пройшли клінічні дослідження, на які позитивно реагують самі пацієнтки, що, власне, ще раз доводить їхню ефективність. БАДи такими чеснотами не володіють. Крім того, у країнах ЄС БАДи мають спеціальне зауваження, що вони не можуть застосовуватись в якості основного засобу лікування або як альтернатива лікарським засобам, тож не знаю, який лікар ризикне призначати їх пацієнтові.
— Яке місце в профілактиці і лікуванні захворювань молочної залози посідають рослинні препарати і чи є серед цієї групи засоби, що володіють доведеною ефективністю?
— Як я вже говорив, ми досить активно і успішно використовуємо препарати цієї групи, в тому числі і тому, що їх ефективність доведена. Наприклад, добре себе зарекомендував і на сьогодні є найбільш перевіреним Мастодинон. Завдяки цьому препарату ми маємо досить хороші результати як при фоновій, так і при основній, а також відновлювальній та профілактичній терапіїї.
Отже, у лікуванні гінекологічних захворювань рослинні лікарські засоби утвердилися давно і міцно. Насамперед, завдяки їхній м’якій дії і відсутності небажаних побічних ефектів. Навіть репродуктологія – сфера, де панують високі медичні технології, які передбачають використання індукторів овуляції, ендоскопічної хірургії, фертилізації in vitro тощо, нині все частіше використовує лікарські рослини, і фітотерапія вважається сьогодні одним з перспективних напрямків у лікуванні безпліддя.
— Який механізм дії цих препаратів забезпечує їх високу ефективність?
– Оскільки ми вже заговорили про Мастодинон, можемо на його прикладі і розібрати це питання. До складу Мастодинону входять спеціальний екстракт Вітексу священного BNO 1095, який стандартизовано за вмістом дітерпенів, обумовлюючих лікарські властивості цієї лікарської рослини, стеблелист василистникоподібний, фіалка альпійська, грудошник гіркий, касатик різнобарвний та лілія тигрова. У зв'язку з тим, що у складі Мастодинону, крім основного компонента (Viteх agnus castus, Вітекс священний, прутняк), містяться ще п'ять гомеопатичних компонентів у розведеннях від D2 до D6, препарат належить до групи комбінованих гомеопатичних препаратів. На сьогоднішній день широко вивчена і показана ефективність Мастодинону в лікуванні доброякісних захворювань молочних залоз, передменструального синдрому (ПМС) і порушень менструального циклу.
Механізм дії Мастодинону полягає у наступному. Препарат знижує підвищені рівні пролактину завдяки допамінергічній дії, усуває дисбаланс між естрогенами і прогестероном шляхом нормалізації недостатності функції жовтого тіла. Гормон гіпофіза пролактин, як відомо, спільно з естрогеном і прогестероном контролює весь процес мамогенезу. У свою чергу, відомо, що патологічне підвищення пролактину може стати причиною мастопатії. Крім цього, її розвитку сприяє порушення менструальної функції (оліго- і аменорея, меноррагії, передменструальний синдром, дисменорея тощо). Нещодавно на заході з’явились публікації стосовно наявності в складі Мастодинону ізофлавону апігеніну, який виявляє антагоністичні властивості стосовно a-естрогенових рецепторів. Таким чином, механізм дії Мастодинону спрямований не тільки на стан молочних залоз, а й опосередковано впливає на гормональну регуляцію стероїдогенезу. Тому цей препарат широко застосовується і добре себе зарекомендував у пацієнток з фіброзно-кістозною хворобою молочних залоз і супутніми порушеннями менструальної функції, ПМС.
Також Мастодинон використовується для «захисту» молочних залоз на фоні замісної гормонотерапії. У нашому нещодавньому дослідженні, ми вивчали можливості використання Мастодинону в якості засобу реабілітації після хірургічних втручань з приводу ФКМ. Як відомо, хірургічне лікування не забезпечує ліквідацію дисгормональних змін, які призвели до виникнення гістологічних змін. Тобто, використовуючи Мастодинон протягом 6 міс. після операції, ми досягли корегування гормонального гомеостазу, ліквідацію мастодинії, покращення УЗД-картини тканин МЗ і, найголовніше, з 30 пролікованих пацієнток, протягом року жодній не проводилася повторна операція. В групі порівняння (30 хворих), повторне хірургічне втручання було у 4 жінок (13,3%).
Отже, резюмуючи, зауважу, що головна перевага цього препарату в тому, що він діє комплексно, впливаючи на причину захворювання: м'яко відновлює порушений природний баланс гормонів, знімає больовий синдром, запобігає розвитку патологічних процесів у молочних залозах і знижує дратівливість, тривожність, притаманні передменструальному синдрому. Іншими словами, є чудовим профілактичним і лікувальним засобом, що повертає жінці психологічний комфорт і нормальне самопочуття.
Загалом, позитивний ефект фітоестрогенів при лікуванні мастопатії пов’язаний з їх слабкою естрогенною активністю, а також здатністю блокувати активність ферменту жирової тканини ароматази, яка бере участь у перетворенні андрогенів в естрогени.
Крім того, Мастодинон, на відміну від численних БАДів, є лікарським препаратом. Він не містить синтетичних гормонів, до його складу входять лише натуральні рослинні екстракти, що обумовлює ще одну його важливу чесноту – добру переносимість пацієнтами.
На сьогодні провідними фахівцями накопичений великий досвід у застосуванні цього препарату, який свідчить про його ефективність, якість і безпеку.
Розмову вела Тетяна Стасенко
Детальніше
