
ЛЮДИ ЧИ БОГИ? (частина 3)
LUDZIE CZY BOGOWIE?
Ми продовжуємо публікувати цитати з 2-го видання польської книжки «LUDZIE CZY BOGOWIE», що містить 27 розмов з найвідомішими польськими лікарями (Dariusz Kortko, Krystyna Bochenek, видавництво AGORA SA, початок матеріалу див. у №9 (66), №1(67).
Переклад Олексія Соловйова.
Є сльози, які можуть вбити
Професор Piotr Morciniec, священнослужитель, біоетик, секретар Товариства Біоетиків Центральної Европи, викладач Опольського університету, душпастир медичних спільнот.
– Як пан розмовляє з лікарями, у яких помер пацієнт?
– Не розмовляю, бо лікарі, на жаль, не приходять до мене з такими проблемами.
– Чому?
– Можливо, тому, що сучасна медицина зосереджена на успіхові, і кожного разу, коли приходить смерть, лікарі трактують її як свою поразку. Це помилка, бо сама смерть належить життю.
– Лікарі того не розуміють? 
– Не знаю. Радше уникають розмов на цю тему… Вважаю, що більшість лікарів є при хворих доти, доки ще «можна щось зробити»… Умираючим більше серця віддають медсестри, які є з ними до кінця…
Коли ми розмовляли з професором Kornelem Gibinskim (див. №9 (66) «З турботою про Жінку». – прим. ред.), він застерігав, що лікарі не дають собі ради зі смертю пацієнтів, бо запрагнули її лікувати, проте смерть не вдасться перемудрити.
…Пацієнти, захлеснуті розвитком медицини, почали трактувати лікарів як нових капеланів, а медицина стала замінником релігії. Трагедія «нової релігії» полягає у тому, що вона не в змозі задовольнити покладені на неї очікування, а «капелани» не мають сили, котрої від них вимагають.
– Пацієнти вірять, що є інакше.
– І звідти розчарування. Люди мають претензії, що лікар не зробив «усього», що мав би. Бо якби зробив, їх близькі б не померли… Оскаржують лікарів за фахові помилки. У високоцивілізованому світі тепер щораз більше лікарів опиняються на лавах підсудних, тільки дев’яносто відсотків тих процесів насправді є справами о нездійсненних очікуваннях, о збуренні віри щодо можливостей медицини.
–Чому так є?
– Живемо у світі, у якому ретельно приховуємо смерть. Маємо бути здорові, гарні та успішні. Старість? Неладна. Навіть в рекламах старі мають вигляд «молодих, здорових і гарних». Гонитва за успіхом не оминає медицини і шкодить їй… Наприклад, не одержить грошей та клініка, що не має наприкінці «успіху»… В епоху боротьби за успіх недостатньо бути добрим лікарем. Потрібно бути примітним, здобути слави…
– Професор Jerzy Holowecki зауважує, що лікар, який дбає про репутацію, не робитиме ризикованої операції…
– На жаль, то правда у непоодиноких випадках. Неймовірно, як швидко в нашій свідомості дійшло до зміни сприйняття лікарської праці. В епоху патерналізму, ще півстоліття тому, пацієнт обдаровував лікаря величезною довірою. Вірив йому майже безмежно. Тепер у медицині з’явився контракт. Пацієнт сплачує послугу й вимагає. Такий зв’язок закреслює дуже важливий елемент, без якого процес лікування стає дуже важким – довіру. Її замінив попит. Ментальність контракту створює з пацієнта клієнта для лікаря, а той клієнт жадає відшкодування у разі невідповідності його очікуванням.
– Бо почувається ошуканим?
– Іноді так. Було б інакше, якби у стосунках лікар – пацієнт було «більше людини». З обох боків.
– Пацієнтки, з якими розмовляв, стверджують, що найліпший лікар – такий, який має для них, передусім, час. Тільки ж добрий лікар все менше має того часу. До нього потрапляють все «складніші випадки», він засипаний звітами і не може присвячувати хворим стільки часу, скільки хотів би.
– То правда. Два роки мешкав у лікарні у Відні й часто чув там такі саме скарги, що з-за монітору та купи паперів не видно пацієнта. То драма.
…
– Чи має право лікар плакати? Багато професорів, з якими ми розмовляли, зізнавалися про сльози.
– Лікар, навіть видатний, є людиною і має право плакати. Але не при пацієнтах. Лікар, який переступає поріг шпиталю, неважливо, чи встав з лівої ноги, чи посварився з дружиною, чи болить у нього зуб, мусить забути про те. Люди однозначно помічають невербальні ознаки. Можна казати пацієнту, що все буде добре, але натомість пацієнт бачить в очах лікаря смуток і не вірить. А якби лікар заплакав при ньому? Такі сльози можуть убити.
– Якщо не може плакати, то як мусить собі зарадити з поразкою?
– Плач по смерті, після втрати – то вже щось інше. Проте лікар, який визнає смерть поразкою, вже зазнав поразки. Твердо мусить подумати і скласти власний стосунок до смерті.
– То не так просто, бо навіть з думками та міцною вірою треба наприкінці стати при помираючому і закрити йому потім очи. Професор Franciszek Kokot стверджує, що неможливо звикнути до смерті. Більше – вигляд помираючої людини вкорочує життя.
– Коли це каже такий заслужений практик, то треба йому вірити. Кожен мусить знайти власний спосіб, немає єдиного рецепту… Лише знаю, що людина, яка не визначила свого ставлення до смерті, буде поганим лікарем. Мусить усвідомлювати, що не є господарем життя та смерті і не має божої сили захисту своїх пацієнтів від смерті. Хто того не розуміє, або тікає, або грає.
– Отець закликає лікарів до роздумів. На які питання повинні собі відповісти?
– Кожен з нас, не лише лікар, мусить поставити собі запитання, в якому з’явиться дрібний додаток: «для мене», наприклад, що означає смерть для мене? Переконання, що смерть напевно прийде, є найліпшими ліками від стресу «бути незамінним». Коли Jan XXIII став папою, записав гасло: «Не будь таким важним». Захворіємо, помремо, а світ не скінчиться. Так вже є, й крапка.
– А якщо смерть видається несправедливою?
– Несправедлива? А що таке справедливість? Віддання кожному того, що йому справедливо належить.
Кожному з нас належить смерть. Належить до людської природи, значить є справедливою. Питання лише, коли вона повинна прийти. Очевидним є, що до більшості людей приходить завчасно.
Можемо також казати о смерті, що невчасна, до якої ми не приготувалися. Проте, ніколи не повинні казати про неї в категоріях, справедлива чи несправедлива.
– Професор Zbigniew Religa не може змиритися, коли помирає молода особа. Він каже, що то несправедливо.
– До отця Jozefa Tishnera написала жінка, яка втратила дочку. Запитала його: «Чому?». «Не знаю», – відписав їй. Немає відповіді на запитання, поставлене так. Тут можна лише сказати, що смерть належить до життя (виділено тлумачем). Недобре, коли лікар каже про несправедливість смерті. Якщо помре трирічна дитина, то буде страшно несправедливим. А коли помирає сорокарічний, то вже більш справедливо? Як окреслити межі справедливої смерти? Чи має п’ятирічна дитина більше прав на життя, ніж дев’яносторічна бабця? Таке ставлення лікаря було б тривожним.
…
– Лікар часто стикається з сакральним. Чи цей фах вимагає поклику?
– Кожна життєва дорога є покликом, але у тому сенсі, про який розмовляємо, знаю принаймні три зайняття, що напевно є покликом: священики, лікарі та батьки. То служба на ціле життя.
…
– Щоразу частіше лікарі, думаючи про спосіб лікування, питають: «Як то зробити?», а повинні питати: «Навіщо це робити?» та «Чи це має сенс?». Відносно нещодавно з’явилася проблема так званого підтримуючого лікування. Покоління старих лікарів таких технічних можливостей не мало. Їх наступники ліпше знають способи лікування, користуються новими способами діагностики та досконалішим обладнанням. Проте, чи ліпше своїх попередників вони знають людину?
Від тлумача:
Піднята тема є злободенною й щодо пренатальної діагностики та медицини плода. По-перше, на мій погляд, у медицині плода найважливішим є обговорення з родиною стосовно можливих внутрішньоутробних діагностико-лікувальних втручань або ятрогенного передчасного розродження чи агресивного неонатального ведення тяжко хворих дітей саме таких питань: «Навіщо це робити?» та «Чи це має сенс?». Остаточне усвідомлене рішення щодо цих питань має прийняти сама родина, але лікар мусить надати батькам неупереджені дані відносно очікуваної мети втручання, можливих ускладнень та вірогідних наслідків. Переконаний, що головним гаслом при обговоренні питань внутрішньоутробних втручань має стати «якомога більше користі плоду при якомога меншій шкоді матері». У неонатальному періоді для тяжко хворих дітей лікарі разом з родиною мають обговорювати не лише питання можливостей сучасної медицини штучно підтримувати в дитині життя, а й право цієї дитини та згоди батьків на «гідну смерть».
По-друге, перед скеруванням вагітних жінок для планових спеціалізованих ультразвукових пренатальних досліджень особистий лікар кожної вагітної мав би приділяти час для чемної, але відвертої розмови з самою жінкою та її чоловіком щодо мети цих пренатальних досліджень. Вкрай важливим є усвідомлення родиною ще до проведення обстежень, що будь-які дослідження не можуть відрізнити усіх хворих дітей від усіх здорових, тому метою пренатальних обстежень є пошук можливих негараздів чи сумнівних даних, а не підтвердження того, що з дитиною «усе добре». В цьому ключі родині заздалегідь бажано пояснити, що переважна кількість знахідок при масових дослідженнях (так званих просівних чи скринінгових) потрібна не для визначення діагнозу та/чи переривання вагітности, а для прийняття вагітною жінкою рішення щодо можливих подальших додаткових обстежень. Підставою для переживань та рішень щодо переривання вагітності має бути винятково встановлений діагноз з поганим прогнозом для життя та/чи здоров’я, а не проміжні дані досліджень.
До того ж, як самим лікарям, так і родинам важливо усвідомлювати різницю між медичною допомогою та соціальними правами на переривання небажаних вагітностей.
* Якщо маєте цікаві й корисні перинатальні тези для оприлюднення у цьому розділі, просимо надсилати їх на адресу Ця електронна адреса захищена від спам-ботів. Вам необхідно увімкнути JavaScript, щоб побачити її.
Детальніше

Магия ультразвука

16 сентября в Киеве прошел мастер-класс Дана Вальского «Допплер в акушерстве и гинекологии». В зале собралось более 150 участников, что явилось красноречивым подтверждением актуальности выбранной темы и большого интереса к заявленному спикеру
Дан Вальский – ведущий специалист отделений медицины плода, УЗД и беременности высокого риска университетской клиники Hadassah в Иерусалиме, одной из крупнейших в Европе клиник, оказывающей услуги пациентам со всего мира.
Надеемся, что каждый участник мастер-класса смог найти для себя что-то новое, интересное. А возможность поближе познакомиться с опытом зарубежных коллег, задать вопросы признанному авторитету в области ультразвуковой диагностики поистине неоценимы.
Такие мастер-классы просто необходимы для поддержания профессионального уровня врачей, для получения новой информации, обмена опытом и клиническими наблюдениями. Участники имели возможность получить знания в краткой, лаконичной, доступной и понятной форме. Это хороший старт для дальнейшего профессионального самосовершенствования в такой загадочной и обширной сфере, как акушерство и гинекология.
Мы хотим представить прошедшую конференцию глазами фоторепортера, пускай говорят фотографии!
Ці та інші фото: https://goo.gl/photos/gyo9CSCWEH9azwmL6



Эмбриональные стволовые клетки и рак
— А что это за звуки, вот там? — спросила Алиса, кивнув на весьма укромные заросли какой-то симпатичной растительности на краю сада.
— А это чудеса, — равнодушно пояснил Чеширский Кот.
— И что же они там делают? — поинтересовалась девочка, неминуемо краснея.
— Как и положено, — Кот зевнул. — Случаются…
Льюис Кэрролл. «Алиса в стране чудес»
Сегодня мы с вами поговорим о стволовых клетках и раке. Тема эта постоянно муссируется в прессе, и многие пациенты этим запуганы. В их понимании «стволовая клетка» – равно «раковая стволовая клетка». Разберемся, так ли это.
В прошлом номере мы привели несколько примеров последствий безграмотного лечения с использованием стволовых клеток. В том числе, и два случая рака. В первом случае (больной телеангиоэктазией) утверждать, что рак вызвали именно стволовые клетки, нельзя. По той причине, что при этом заболевании частота спонтанного возникновения опухолей очень велика даже без введения стволовых клеток. Последние же обладают интересным свойством – «эффектом преследования» раковых клеток.
Суть в том, что стволовые клетки способны встраиваться в опухоль, но при этом сами источником рака не являются. Поэтому обнаружение в опухоли генома донора стволовых клеток не означает, что причиной рака были именно стволовые клетки. У вас дома есть стол? Есть. Значит, я прихожу к выводу, что этот стол был сделан в вашей квартире. Логика примерно такая же…
Совсем другое дело во втором случае, с пациентом, которому неоднократно вводили в спинномозговую жидкость разные виды стволовых клеток, в том числе, эмбриональные стволовые клетки.
Вот мы и подошли к вопросу о классификации стволовых клеток, которые по своим свойствам отличаются так же сильно, как кусок металлической руды от автомашины «Феррари». С этой «руды» и начнем.
Эмбриональные стволовые клетки (ЭСК) оказались в центре внимания мировой общественности в 1998 году, после того как Томсон и Герхарт выделили их из бластоцисты человека и создали бессмертные линии ЭСК. Однако не им принадлежит честь открытия ЭСК.
Еще в конце 50-х годов ХХ века Лерой Стивенс (США), изучая влияние табака на возникновение опухолей у мышей, обнаружил необычно высокую частоту развития тератокарцином (рис. 1) у одной из групп животных.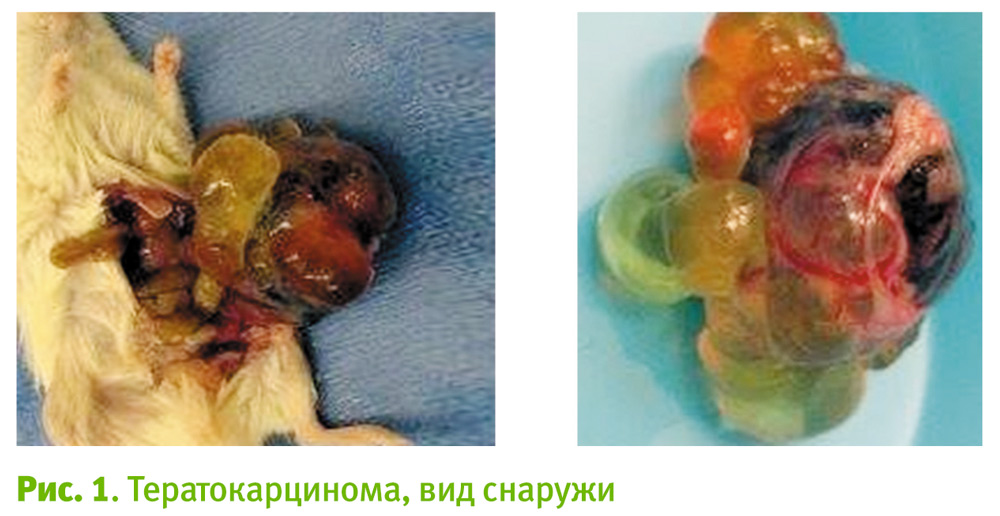
В этих опухолях спонтанно возникали клетки нервной системы, кожи, волос, хряща, фрагменты зубов и костной ткани (рис. 2).
Через несколько лет скрещивания и селекции Стивенс вывел линию мышей с максимальной частотой развития спонтанных тератокарцином. Из этих опухолей Лерой выделил популяцию «раковых» клеток с удивительными свойствами. При введении в брюшную полость эти клетки формировали крупные клеточные агрегаты, в которых происходило образование клеток скелетных мышц, сердца, кожи, волос, нервной ткани, кости, сосудов и т. д. (рис. 3).
Следующий шаг Стивенса был гениален. Он обнаружил сходство клеток тератокарциномы с клетками эмбриобласта предимплантационных зародышей, и первым получил тератокарциномы, вводя суспензию клеток эмбриобласта в ткани взрослых мышей. После введения в брюшную полость животных-реципиентов клетки этих опухолей дифференцировались в нейроны, кардиомиоциты и другие соматические зрелые клетки.
Стивенс понял, что работает со смешанной культурой раковых и эмбриональных прогениторных клеток полового зачатка. Эту примесь эмбриональных нераковых клеток он назвал «эмбриональными плюрипотентыми клетками». Позднее термин Стивенса «эмбриональная стволовая клетка» прижился в научной литературе и замелькал на первых полосах газет и журналов в 1998 году…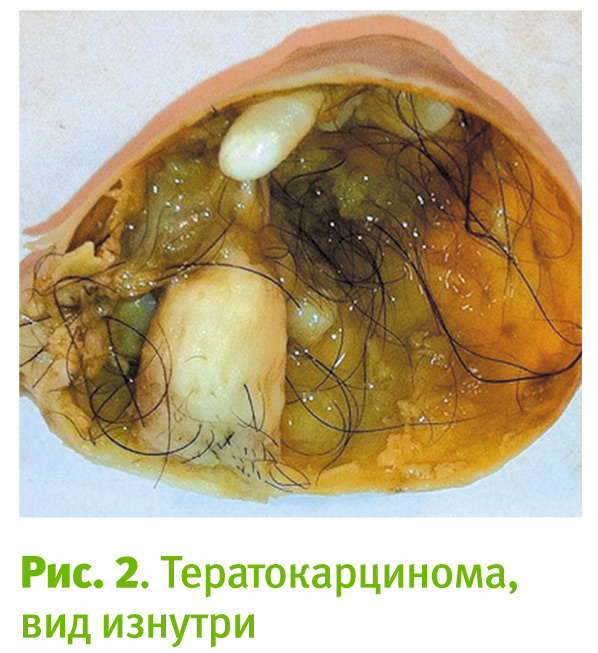
Таким образом, сама история открытия эмбриональных стволовых клеток связана с раковыми опухолями. И ЭСК действительно вызывают рак при введении в мышцы или ткани внутренних органов экспериментальным животным. Но именно поэтому в клинике никто эти клетки для лечения людей не использует!
Однако недобрая слава ЭСК быстро распространилась и на другие виды стволовых клеток, которые на самом деле рака не вызывают! Ситуация еще больше осложнилась и достигла степени канцерофобии, когда были обнаружены так называемые «раковые стволовые клетки».
Сегодня уже доказано, что раковые стволовые клетки присутствуют в любой злокачественной опухоли (рис. 4 – раковые стволовые клетки похожи на репейник; округлые «шарики» – это лимфоциты).
Раковые стволовые клетки не уничтожаются химиотерапией и весьма устойчивы к действию радиации в дормантном (спящем) состоянии. Метастазирование опухоли связано с выходом раковых стволовых клеток в кровоток (гематогенный путь) или лимфоток (лимфогенный путь). Инвазивный рост опухоли обусловлен миграцией раковых стволовых клеток в соседние ткани. На раковых стволовых клетках практически нет молекул главного комплекса гистосовместимости (HLA), что делает их неуязвимыми для Т-лимфоцитов, а от натуральных киллеров (NK-клеток) раковая стволовая клетка успешно прячется, одевая на себя «плащ-невидимку» из тромбоцитов.
Оказалось, что эмбриональная стволовая и раковая стволовая клетки похожи друг на друга даже внешне (рис. 5).
Маркерный белок на их поверхности тоже одинаковый (OCT4), а это значит, что в их геноме активен один и тот же ген (oct4). Но эти клетки не идентичны! Раковая стволовая клетка потеряла способность к дифференцировке, а эмбриональная стволовая клетка дифференцируется во все 240 клеточных типов тканей организма человека…
Если мы не можем использовать ЭСК для лечения болезней, то стоят ли они вообще нашего внимания? Стоят! Биологи и генетики впервые получили в руки прототип той «клетки-праматери», которую в процессе длительного отбора эволюция выбрала для повторения вида в каждом новом поколении. Но это не только чисто научный интерес… Первые результаты успешного перепрограммирования взрослых клеток в ЭСК опубликовал в 2006 году теперь уже Нобелевский лауреат, доктор Шинья Яманака (Shinya Yamanaka) из Университета Киото. Группа ученых под его руководством разработала методику превращения обычных клеток взрослого организма в эмбриональные стволовые клетки путем добавления к соматическим клеткам всего четырех генов: Oct4, Klf4, Sox2 и c-Myc. Полученным таким образом эмбриональные стволовые клетки назвали индуцированными плюрипотентными стволовыми клетками (англ. induced pluripotent stem cells – iPSс). Открытие Яманаки позволяет решить этическую проблему получения ЭСК без необходимости использования эмбрионов и выращивать новые органы и ткани из клеток больного, которые не будут отторгаться его иммунной системой.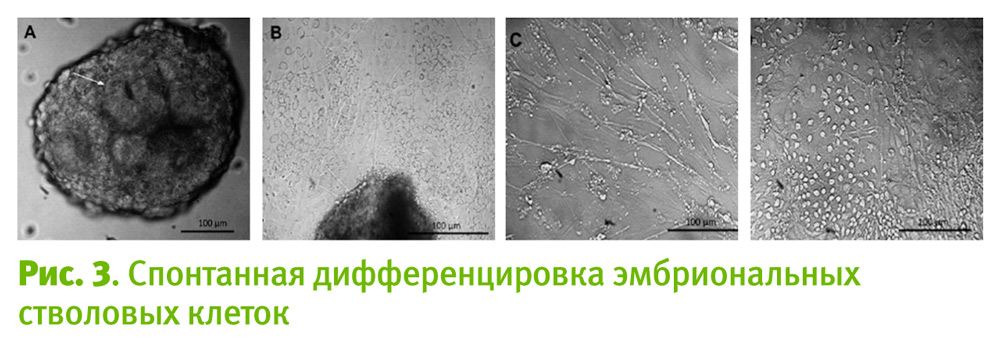
Около трех лет назад группа ученых из Национального Онкологического Исследовательского Центра (Spanish National Cancer Research Center) впервые перепрограммировала взрослые клетки в эмбриональные стволовые клетки непосредственно в организме. Результаты, опубликованные 11 сентября 2013 г. в журнале Nature, могут стать прорывом в регенеративной медицине, позволив манипулировать клетками без необходимости извлечения их из организма.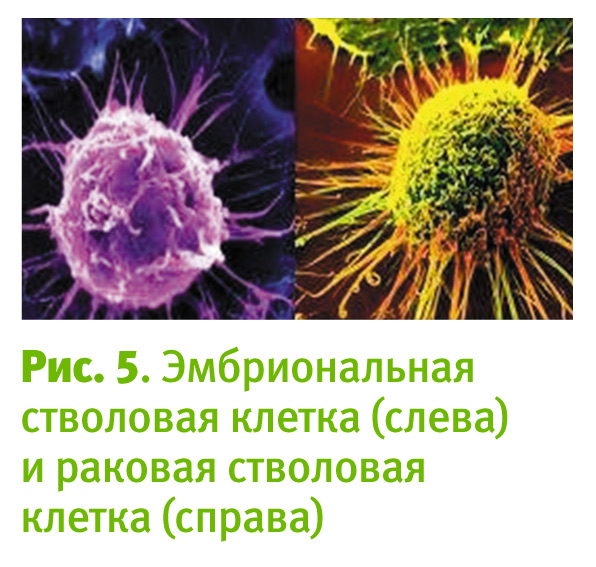
Говоря проще, сделан первый шаг к созданию новых органов для больного человека – без доноров и проблем отторжения трансплантата, так как все ткани этого нового органа будут созданы из обычной клетки самого пациента…
А если дать волю воображению, то и самой трансплантации может не понадобиться, так как возврат обычной соматической клетки к возможностям эмбриональной стволовой клетки способен расширить потенциал регенерации человека до бесконечности…
В заключение я еще раз подчеркну – эмбриональные стволовые клетки, способные дать начало раковой опухоли, для лечения больных никто и нигде не использует. А о других видах стволовых клеток и об эффективности их сегодняшнего применения в практической медицине читайте в следующих выпусках журнала «З турботою про Жiнку».
Детальніше

Врожденные аномалии развития матки или мюллеровы аномалии (Обзор литературы, часть 2)
 Классификация ESHRE/ESGE 2013г.
Классификация ESHRE/ESGE 2013г.
Основой классификации является анатомия. Отклонения в анатомии матки определяются тем же эмбриональным происхожденияем и являются базой для проектирования основных классов. Основные подклассы базируются на клинической актуальности и степени анатомического дефекта. Аномалии шейки и влагалища классифицируются в независимых дополнительных подклассах.
Нормальная матка
Нормальная матка – любая матка, имеющая прямую или изогнутую межостиальную линию, но с внутренним углублением фундальной срединной линии не более 50% от толщины стенки матки.
Морфологически измененная матка
Морфологически измененная матка включает в себя все случаи с нормальным внешним контуром матки, но с аномальной узкой формой полости, исключая перегородку.
Дальнейшее разделение на 3 подгруппы – в соответствии с толщиной боковой стенки и цервикально/фундальным соотношением.
Перегородки матки
Включает все случаи нормального слияния и аномальной абсорбции срединной перегородки. Внутреннее углубление от фундальной срединной линии – более 50% от толщины стенки матки, с нормальным внешним контуром.
Двурогая матка, удвоение тела матки
Включает все случаи дефектов слияния. Матка имеет аномальный внешний контур дна с наличием наружного углубления в срединной фундальной линии, превышающее 50% от толщины стенки матки
Однорогая матка
Включает все случаи односторонних дефектов формирования матки, контрлатеральная часть может быть полностью сформирована либо отсутствовать. «Суботдел» зависит от наличия или отсутствия функциональной рудиментарной полости, сообщающейся или несообщающейся.
Аплазии матки
Включает все случаи аплазии матки. Этот дефект формирования характеризуется либо полным отсутствием матки, либо развитием односторонней латеральной, рудиментарной маточной полости. Обычно ассоциированы с сосуществующими дефектами (вагинальная аплазия/синдром M-R-K-H).
Неклассифицированные случаи
Эта категория предназначена для еще неклассифицированных случаев. Класс был создан для того, чтобы сохранить другие группы «чистыми». Система предназначена для включения всех случаев в результате дефекта формирования, слияния или абсорбции при нормальном эмбриональном развитии.
Для более детального рассмотрения клинического ведения пациенток, имеющих МА, с которыми встречается практикующий доктор при планировании у них беременности, и учитывая, что до недавнего времени самой распространенной и используемой классификацией была и остается классификация Американского общества фертильности 1988 г., ниже приведено описание 5 классов (II–VI). I класс пропущен в виду необходимости проведения реконструктивных хирургических вмешательств, направленных на достижение возможности иметь нормальные сексуальные отношения, и полной невозможности вынашивания беременности, а VII класс – в связи с достаточно редкой встречаемостью, характерной для нашей популяции.
Класс II. Однорогая матка
Однорогая матка возникает в ситуациях, когда один мюллеров канал при формировании полностью или частично изменяется, в то время как второй развивается нормально. Также есть работы, описывающие сосуществование однорогой матки и агенезии ипсилатерального яичника. Некоторые исследователи считают, что формирование однорогой матки может быть следствием агенезии с вовлечением всех структур из одного урогенитального тракта [105, 106, 107]. Распространенность патологии составляет 2,4–13% от всех мюллеровых аномалий и считается самой редкой среди них [8, 9, 45]. Встречаемость однорогой матки в популяции – около 0,06% – по данным ретроспективного обзора, включавшем более 3000 женщин репродуктивного возраста [108].
Этот класс маточных структурных дефектов анатомически разнообразен. Однорогая матка может выявляться изолированно, но чаще ассоциируется с рудиментарным рогом [45, 109, 110]. По классификации AFS в этой группе выделяют 4 категории, на основании наличия или отсутствия рудиментарного рога. Рудиментарный рог может иметь маточную полость с функционирующими эндометрием и в некоторых случаях может быть связь с эндометрием основной полости. Сопутствующие урологические аномалии встречаются достаточно часто – в 44% (особенно если имеет место рудиментарный обструктивный рог) и включают ипсилатеральную почечную агенезию – 67%, подковобразную почку и ипсилатеральную «тазовую» почку – 15% [109].
Несообщающийся рудиментарный рог с наличием эндометрия в полости является наиболее распространенным подтипом однорогой матки и наиболее клинически значимым. Этот подтип ассоциируется с увеличенным процентом заболеваемости: при обструкции функционирующего рудиментарного рога развиваются осложнения (гематометра). Также повышается риск развития эндометриоза, который обычно «разрешается» после удаления рудиментарного рога, при условии проведения ранней диагностики и лечения [39].
Несмотря на возможность нормальной беременности, акушерские исходы неблагоприятны в этой группе. Однорогая матка ассоциируется с наихудшей выживаемостью плодов по сравнению с остальными мюллеровыми аномалиями [14]. Процент кесаревых сечений высок, основные акушерские осложнения включают неправильное предлежание, задержку внутриутробного развития и преждевременное прерывание беременности [97, 111].
Обзор, составленный на основании нескольких работ по маточным аномалиям и исходам беременностей, показал, что однорогие матки имеют наихудшие репродуктивные исходы всех маточных аномалий (и не только врожденных). Это связано с аномальной васкуляризацией и уменьшенной мышечной массой матки. Анализ 393 беременностей при разных категориях однорогой матки выявил: 170 (43,3%) – преждевременные роды, 213 (54,2%) – живорождения, 17 (4,3%) – эктопические беременности, 135 (34,4%) – самопроизвольные выкидыши. Около 2% беременностей наступили в рудиментарном роге [112].
Аналогичный доклад, включивший 20 исследований 290 женщин с подтвержденным хирургически или рентгенологически диагнозом однорогой матки и общим количеством беременностей 468, имели сопоставимые исходы [113]. На основании этих статистических данных есть понимание акушерских исходов для всех групп однорогих маток. Однако в большинстве докладов не разделены однорогие матки по подклассам согласно AFS классификации.
Также в акушерские осложнения может быть вовлечен рудиментарный рог: эктопическая беременность, замершая беременность, разрыв матки (рудиментарного рога) [114]. Поэтому рекомендовано профилактическое удаление рудиментарного рога до планируемой беременности. Беременность в несообщающимся рудиментарном роге редка и предположительно может наступить в результате трансперитонеальной миграции сперматозоидов в маточную трубу рудиментарного рога. Большинство осложнений происходит в первые 20 нед. беременности, к ним относится выкидыши, разрыв матки или материнская смертность (0,5%) [110, 115, 116, 117].
Диагностика однорогой матки
У женщин с несообщающимся, функционирующим рудиментарным рогом могут быть тазовые боли, возникающие обычно вторично, вследствие гематометры или эндометриоза. Проведение гистеросальпингографии очень информативно для диагностики однорогой матки, однако не помогает в диагностике несообщающегося рудиментарного рога. МРТ дает возможность точно идентифицировать различные категории (подклассы) однорогих маток и может быть одним из первых диагностических методов для оценки этой патологии. При однорогих матках МРТ показывает достаточно узкую, латеральноотклоненную бананообразную форму матки. Идентифицируется только одна маточная труба, анатомическая зона расположения соответствует норме, хотя объем матки уменьшен. Рудиментарный рог выявляется как солидное образование (когда отсутствует эндометрий), располагающееся в непосредственной близости к главной полости матки. Также рудиментарный рог может определяться в виде масс мягких тканей.
В случаях, когда присутствует эндометрий, может определяться маленькая полость, сообщающаяся или не сообщающаяся с основной полостью матки [72, 73, 74, 75, 118, 119]. УЗИ с высоким разрешением дает возможность достаточно точно идентифицировать рудиментарный рог и является не менее точным методом в сравнении с лапароскопией [120]. Дополнительно проводится УЗИ почек – для оценки риска наличия врожденной почечной патологии.
Предоперационная подготовка
Однорогая матка – достаточно редкая патология и это отображается на скудных литературных данных в отношении хирургической стратегии, особенно для лечения различных подклассов. Специфика хирургических подходов существенно не изменилась: обычно не показана реконструктивная метропластика [6, 39, 121]. Показанием для оперативного вмешательства является наличие рудиментарного рога с функционирующей полостью. Лапароскопический доступ для проведения гемигистерэктомии является методом выбора [116, 117]. Когда в рудиментарном роге не выявлен эндометрий – хирургическое лечение не показано [112].
Хирургическая тактика удаления рудиментарного рога
Осуществляется путем лапароскопической гемигистерэктомии. Существуют различные анатомические варианты прикрепления рудиментарного рога к однорогой матке, часто два рога соединяет фиброзно-мышечный тяж. Сложности лапароскопической дисекции могут возникать, когда нет наружного разъединения рогов. В таком случае необходима резекция миометрия с помощью биполярной коагуляции на стыке рогов с последующим механическим или лазерным разрезом [116, 117].
В случае наступления беременности в рудиментарном несообщающимся роге, выполняется лапароскопическое удаление беременного рога по тем же принципам, что и вне беременности, с обязательным учитыванием усиленной васкуляризации ножки (тяжа).
Имеются данные о благополучном исходе беременностей в основном роге после предварительного лапароскопического удаления рудиментарного рога [123].
Cutner и соавт. сообщили об опыте наблюдения двух беременностей в несообщающемся рудиментарном роге. Было проведено медикаментозное лечение метотрексатом перед хирургическим удалением рудиментарного рога. Авторы сделали выводы, что такая подготовка позволяет отложить хирургическое вмешательство и сделать его менее инвазивным и безопасным [124].
Вне беременности с целью лечения симптоматической гематометры сообщается о возможности проведения гистероскопической абляции эндометрия. Последующее трехлетнее наблюдение этих пациентов свидетельствует об отсутствии рецидивирующей симптоматики [125].
Также в литературе описано проведение гистероскопической электрокоагуляции для создания связи между рудиментарным и основным рогом с целью дренирования гематометры рудиментарного рога. Спустя 1 месяц после вмешательства выявлялась одиночная полость и отсутствие предшествующей симптоматики [126]. Однако необходимы дальнейшие дополнительные исследования перед широким использованием этих методов лечения.
Послеоперационное ведение
Ассоциированные осложнения включают все осложнения, связанные с проведением лапароскопии в гинекологии.
Послеоперационные акушерские исходы были достаточно благоприятными для этой группы. Donnez&Nisolle сообщили о наблюдении 14-ти женщин с однорогой маткой, перенесших лапароскопическое удаление рудиментарного рога: 8 женщин планировали беременность и у 6 она наступила. У 5 из них – вагинальные роды после 36 недель и у 1 – кесарево сечение по показаниям со стороны плода [116, 117].
Класс III. Удвоение матки
Удвоение матки возникает, когда срединная линия слияния имеет полный или частичный дефект. Эта патология занимает примерно 11% среди врожденных пороков матки [11].
Полная форма удвоения – это наличие двух однорогих маток и двух цервикальных каналов с шейками, имеющих слияние в нижнем сегменте матки. Каждая однорогая матка имеет одну маточную трубу, также может встречаться неправильное расположение яичников [127]. Влагалище может быть одно или иметь место удвоение (дупликация – частый компонент). Удвоение влагалища проявляется в виде продольной (горизонтальной) перегородки, которая проходит либо полностью (полная перегородка) либо частично (неполная перегородка) от шейки до преддверия влагалища. Полная продольная перегородка влагалища встречается в 75% случаев при удвоении матки, хотя перегородка влагалища также может сочетаться и с другими мюллеровыми аномалиями [84, 109, 114].
Пациентки с удвоением матки обычно асимптомны, если нет элемента обструкции. В случаях обструкции может развиваться гематометрокольпос, гематометра, гематосальпинкс.
Агенезия почки ассоциируется с удвоением матки чаще, чем с другими мюллеровыми аномалиями. У этой группы пациенток аномалии почек выявляются в 20% случаев [6].
Односторонняя обструкция влагалища у пациенток с удвоением матки часто ассоциируется с ипсилатеральный почечной и мочеточниковой агенезией – известна как синдром Wunderlich–Herlynwerner (редкая, но хорошо подтвержденная аномалия) [128, 129]. Ряд тематических докладов, касающихся этого синдрома, были опубликованы в период 2000–2004 гг. [130–136] – эти работы также отображают растущее учащение использования МРТ в диагностических целях. Полагают, что почечная агенезия связана с блокированием развития в одном вольфовом протоке, что, в свою очередь, влияет на индукцию нефрогенеза и состояние ипсилатерального мюллерового протока. Смещенный мюллеров проток не способен к правильному слиянию, и как следствие, развивается две однорогие матки. Сообщается о семейных случаях, хотя точно генетическая ассоциация не была идентифицирована [6].
Необычная способность удвоенной матки в том, что во многих случаях возможен coitus в оба влагалища. Кроме того, может наступить естественная беременность в обеих матках одновременно (хотя и редко). Близнецы всегда дизиготные. Некоторые эксперты считают, что каждая беременность отдельно зачата. Эта теория подкрепляется сообщениями, в которых второй близнец рождался после длительного интервала: начиная от трех часов, пяти дней, и до восьми недель после рождения первого близнеца [142–144]. Лактация, как сообщается, появляется после рождения второго близнеца [143].
Подходы к родоразрешению остаются спорными: некоторые эксперты настаивают на безопасности вагинальных родов, в то время как другие выступают за кесарево сечение. Описан один редкий случай, когда один плод из двойни родился путем операции кесарева сечение в сроке 25 нед., а второй родился через естественные родовые пути в сроке 35 нед. Оба ребенка были выписаны домой после выхаживания первого без осложнений [144]. Данные в литературе о беременности двойней при удвоении матки редки и данных о репродуктивных исходах достаточно мало. Эти доклады описывают случаи отслойки плаценты в одной матке и преждевременные роды в одной из маток [144, 145].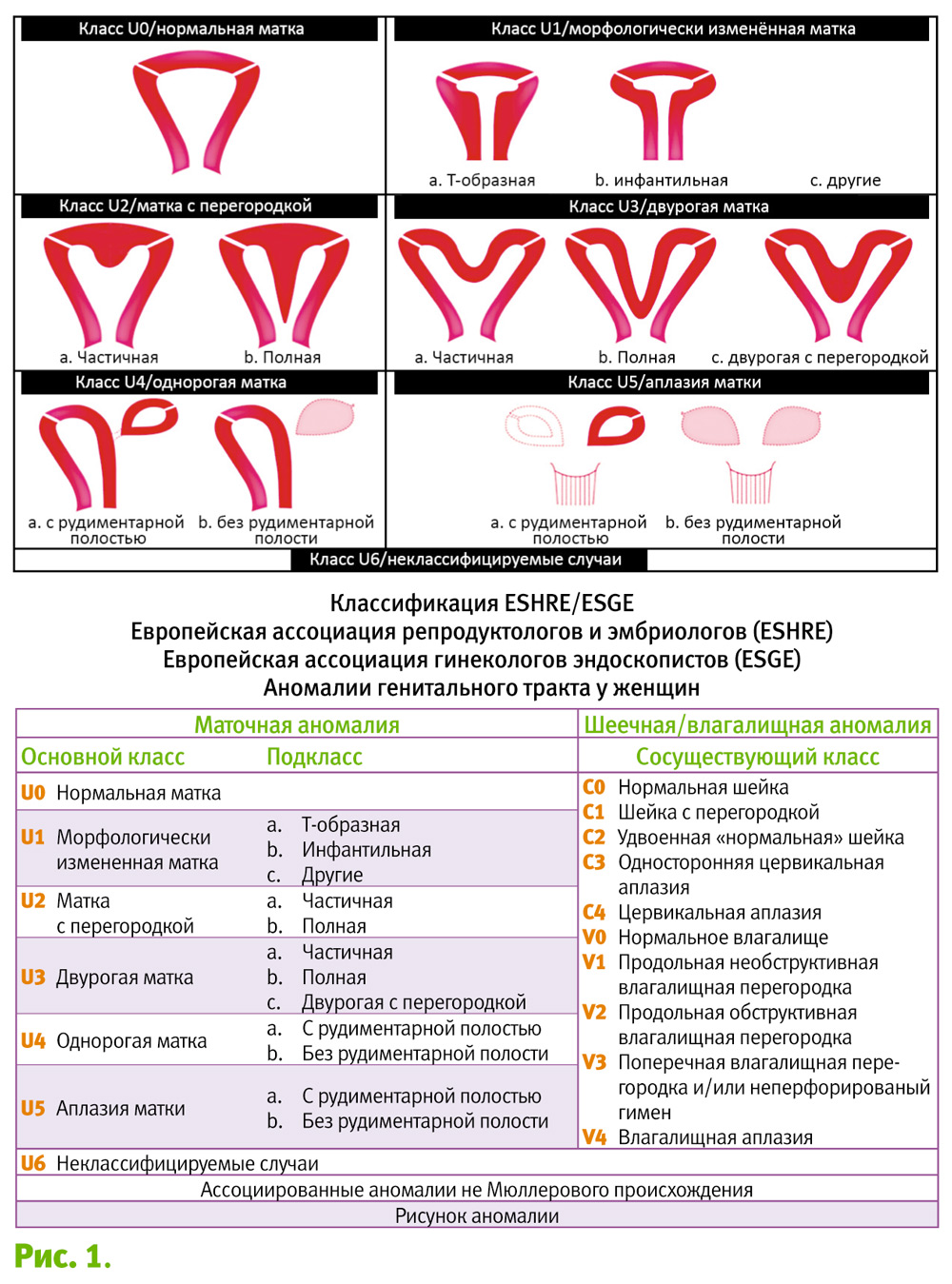
Низкая распространенность случаев удвоения матки отражает скудность данных и в литературе о репродуктивных исходах у таких пациенток. По результатам двух исследований, выявлена следующая статистика для 86 беременностей: 21 (24,4%) – преждевременные роды, 59 (68,6%) – живорождения, 2 (2,3%) – эктопические беременности и 18 (20,9%) – самопроизвольные выкидыши [112]. Неблагоприятные репродуктивные исходы, как считается, возникают как следствие уменьшенного объема каждой матки и сниженной перфузии.
Малигнизация может иметь место и при мюллеровых аномалиях. Рак шейки матки и аденокарциномы эндометрия встречаются редко. Исключительно редкое явление при удвоении матки – развитие односторонних аденокарцином эндометрия [146, 147].
Диагностика при удвоении матки
Удвоение матки без обструкции обычно протекает бессимптомно до менархе. Наиболее частой жалобой является неспособность тампонов удерживать менструальную кровь во влагалище. Диагноз ставится на первичном осмотре органов малого таза при выявлении удвоения шейки матки. Часто в анамнезе выявляется самопроизвольный выкидыш II-го триместра.
При обструктивных формах клинические проявления могут различаться и зависят от степени обструкции (наличия отверстия). Наиболее частые симптомы – это развитие дисменорреи в первые годы после менархе и прогрессирующие тазовые боли. При осмотре обнаруживается одностороннее увеличение органов малого таза (правостороннее увеличение встречается в 2 раза чаще, чем левостороннее). Вторично, на фоне формирования гематокольпоса, могут иметь место ректальные боли, запоры [132].
Методы диагностики аналогичны тем, которые используются при однорогой матке и включают HSG, МРТ, УЗИ с обязательным исследованием мочевыделительной системы для исключения их аномалий. МРТ выявляет два отдельно расположенных рога матки с двумя шейками, зачастую определяется угол между рогами >60° [118, 119]. Обструктивные формы представлены в виде расширенного влагалищного компонента и уменьшения эндометриального расширения [148]. УЗИ является также ценным дополнением [46, 72, 149, 150].
Предоперационная оценка
Односторонняя влагалищная обструкция – это показание для проведения резекции влагалищной перегородки. Хирургическое вмешательство необходимо для сохранения репродуктивной способности и предотвращения нарушений функции матки и труб.
Если обструкция своевременно не ликвидирована после постановки диагноза, ретроградная менструация продолжается и может сформироваться гематометра и гематосальпинкс, а в худшем случае – эндометриоз и спаечный процесс в малом тазу [151]. В случае наступления беременности на фоне имеющейся обструкции влагалища, может быть проведено резецирование перегородки, необходимо по данным УЗИ определить сторону обструкции по отношению к беременной матке (ипси- или контрлатеральная). У некоторых пациентов с длительным анамнезом привычного невынашивания, возможно, имеет смысл проведение метропластики (однако эти данные требуют подтверждения в дальнейших исследованиях), но имеет место высокий риск ИЦН или стеноза шейки матки ввиду технических сложностей при хирургическом объединении шеек [14].
Необходимость удаления необструктивной перегородки у беременных до конца не определена: некоторые исследователи выступают за удаление, в то время как другие не рекомендуют хирургическое вмешательство, если перегородка не препятствует естественному родоразрешению [109].
Хирургическая техника
Удвоение матки с односторонней вагинальной обструкцией: полное удаление и марсупиализация влагалищной перегородки выполняется в один этап вмешательства [152]. Есть единичные сообщения о проведении метропластики как методе, объединяющем полости маток в области тел, не затрагивая их шейки – Strassmann metroplasty [5].
Послеоперационное ведение
Имеется риск вагинального аденоза после удаления перегородки. Рекомендуется серийное взятие мазков и кольпоскопия [128].
Осложнения и результаты
После удаления перегородки, которая вызывала обструкцию, пострадавшие матка и труба обычно нормально восстанавливаются и функционируют. Гематометра и гематосальпинкс могут повториться, если перегородка резецирована не полностью [129, 152]. Сообщается о 10-ти случаях маточной беременности после эпизодов односторонней вагинальной обструкции с последующим хирургическим удалением перегородки, пять из которых завершились срочными родами, четыре – преждевременными и один – самопроизвольный выкидыш малого срока [152].
Продолжение в следующем номере.
Перечень литературы находится в редакции.
Детальніше

Передчасний розрив плодових оболонок – еволюція поглядів
 Спонтанний розрив плодових оболонок є компонентом нормального пологового процесу. Передчасним є розрив плодових оболонок, що відбувся незалежно від гестаційного терміну до початку регулярних перейм (7) [31]. В англомовній літературі існує окрема термінологія для передчасного розриву плодових оболонок (ПРПО) у терміни доношеної вагітності – prelabor membrane rupture та ПРПО при недоношеній вагітності – preterm prelabor membrane rupture [11]. Ця відмінність є доцільною, оскільки відображає 2 різні підходи до подальшого ведення пацієнток. Розрив мембран робить пологи неминучими, а подальше пролонгування вагітності призводить до хоріоамніоніту та інфікування плода
Спонтанний розрив плодових оболонок є компонентом нормального пологового процесу. Передчасним є розрив плодових оболонок, що відбувся незалежно від гестаційного терміну до початку регулярних перейм (7) [31]. В англомовній літературі існує окрема термінологія для передчасного розриву плодових оболонок (ПРПО) у терміни доношеної вагітності – prelabor membrane rupture та ПРПО при недоношеній вагітності – preterm prelabor membrane rupture [11]. Ця відмінність є доцільною, оскільки відображає 2 різні підходи до подальшого ведення пацієнток. Розрив мембран робить пологи неминучими, а подальше пролонгування вагітності призводить до хоріоамніоніту та інфікування плода
ПРПО ускладнює від 8 до 10% всіх доношених вагітностей [9], серед передчасних пологів частота передчасного розриву мембран сягає 30%, серед багатоплодових вагітностей – 40% [26]. За даними Перинатального центру м. Києва, у терміни 22–28 тижнів до 70% всіх передчасних пологів спричинені ПРПО [2].
За даними A. Wolfensberger (2006), саме ПРПО при недоношеній вагітності спричиняє до 20% всіх випадків перинатальної смертності у США. Частота перинатальних ускладнень залежить від терміну, в якому відбувся ПРПО, при недоношеній вагітності терміном до 28 тижнів показник ранньої неонатальної смертності сягає 70%. Розвиток інтраамніотичної інфекції спостерігають у 15–30% випадків ПРПО, у 2–13% таких породіль діагностують післяпологовий ендометрит [6].
Незважаючи на очевидну актуальність проблеми, питання патогенезу та можливого прогнозування ПРПО остаточно не з'ясовані. Формування плодових оболонок відбувається в першому триместрі вагітності, в цьому процесі беруть участь тканини плодового (хоріон) та материнського походження (децидуальна оболонка). Міцність плодових оболонок залежить від стану колагену, їх складу та щільності контакту між шарами [8]. У нормі розрив плодового міхура відбувається на висоті однієї з перейм першого періоду пологів, цьому передує розм'якшення плодових оболонок в області внутрішнього зіву шийки матки, порушення міцності зв'язків між хоріоном та амніоном, що відбувається під впливом численних ферментів – протеаз та фософоліпаз, активованих простагландинами та цитокінами. У випадку ПРПО аналогічні зміни в оболонках відбуваються задовго до пологової діяльності та зумовлені переважно місцевим запальним процесом (Радзінський В. Є., 2011).
Пошук можливих причин ПРПО довгий час цікавив дослідників.
Так, ще 1964 року було продемонстровано роль в цьому процесі нестачі вітаміну С [36].
Останнім часом багато уваги приділяють зв’язку передчасного розриву плодових оболонок із порушенням структури сполучної тканини генетичного походження.
Так, 1997 року Х.Qiun et al. показали зростання паракринної продукції релаксину децидуальною оболонкою, що призводило до активації різного плану колагеназ та зменшення міцності колагену [29].
Серед генетичних причин ПРПО виділяють поліморфізм гену будови колагену 1a2, ендотеліну та інгібітора серин-пептидази.
Дослідженнями M. Ніколаєвої та співав. (2013) показано, що частота різних форм, у тому числі недиференційованих, дисплазії сполучної тканини, при якій порушуються її еластичні властивості, в групах ПРПО сягає 80%. Враховуючи неможливість скринінгового генетичного обстеження вагітних, автори пропонують звертати увагу на такі анамнестичні чинники ризику, як мимовільні викидні, загроза викидня у І триместрі, нейро-циркуляторна дистонія тощо, які в структурі своїх етіологічних чинників також мають порушення нормальної будови сполучної тканини.
Враховуючи походження та будову плодової оболонки, що пошарово складається з амніотичного епітелію, базальної мембрани, сполучнотканинного шару, хоріону та децидуальної оболонки, порушення будови та метаболізму її тканин можна пояснити як плодовими, так і материнськими причинами. Традиційно причиною зниження еластичності амніотичної оболонки вважають активацію процесів апоптозу, зниження вмісту колагенових волокон, підвищення його розчинності, зростання колагенолітичної активності тощо (В. Сидельникова, 2007).
Серед новітніх біохімічних прогностичних чинників ПП особливе місце посідає концентрація фетуїну в навколоплодових водах. Фетуїн становить собою глікопротеїн, на кінцях якого розташовані сіалові кислоти, призначені для зв'язування вільного кальцію. Вперше речовину було виділено із крові тваринних плодів, звідки і походить назва. Крім того, в міжнародній номенклатурі речовина має ще назву a2-HS-глікопротеїну, де HS – скорочення прізвищ Heremas та Shmidt, вчених, що виділили протеїн. Поліморфізм глікопротеїну передбачає існування 2 його споріднених форм – фетуїну А, властивого лише людині, та фетуїну В, спільного для людини і тварин (E. Ducza et al., 2010).
На підставі проведених на тваринах експериментів W. Jahnen-Dechent et al. (2012) показали роль глікопротеїну в пригніченні надмірної кальцифікації тканин, для цього вони створили культуру мишей, позбавлених гену, відповідального за синтез фетуїну. Більшою мірою гомозиготи, меншою – гетерозиготи мали розвиток мікрокальцинатів у м'яких тканинах, серед яких – стінка судини, поверхні суглобів тощо. Проте несподіваним фактом стале звичне невиношування у таких мишей, що відбувалось за типом ПРПО.
2012 року Lydia Shook еt al. опублікували гучне повідомлення про виявлене ними зниження концентрації фетуїну в навколоплодових водах при ПРПО. Такі результати було отримано на підставі вивчення вмісту фетуїну в зразках навколоплодових вод, отриманих з метою амніоцентезу у здорових вагітних, культивування зразків та вивчення утворення скупчень наночастинок кальцію. Автори показали кореляцію між зменшенням концентрацію фетуїну в амніотичній рідині та кількістю зрілих наночастинок у плодових оболонках. Механізм дії недостатнього пригнічення відкладання кальцію полягає у цитотоксичній дії наночастинок на тканину, зменшенні її протизапальної стійкості – надмірній активації протеїназ та колагеназ, зменшенні еластичності плодових оболонок та, як наслідок, – передчасному їх розриві. E. Ducza et al. (2012), вивчивши динаміку концентрації фетуїну в амніотичній рідині мишей протягом вагітності, дійшли висновку, що за нормальної вагітності вміст цього чинника є значно більшим, ніж у невагітних тварин в сироватці, та різко зменшується за 2–3 дні до передбачуваних пологів. Крім того, вивчивши зміни показника при спробі стимуляції ПП простагландинами, автори описали їх як подібні до тих, що мають місце при наближенні фізіологічних пологів. Проте при спробі стимуляції пологів ліпополісахаридом клітинної стінки бактерій, концентрація фетуїну значно зростає.
Таку реактивність протеїну, що виконує роль регулятора кальцієвих каналів, пояснюють його належністю до білків гострої фази запалення та активністю у якості протизапального цитокіну. Так, M. Dimitriou et al. (1996), вивчивши «взаємовідносини» фетуїну та прозапальних цитокінів, показали їх антагоністичну дію. Зокрема, фетуїн in vitro пригнічував антипроліферативну активність фактору некрозу пухлини. Водночас, підвищена концентрація фетуїну також має свої негативні наслідки – виступаючи антагоністом рецепторів інсуліну, фетуїн є одним із чинників ризику розвитку інсулінорезистентності. Остання значно рідше розвивається у вже згаданої вище культури мишей, що позбавлені гену фетуїну, навіть за умови годування їх дієтою, багатою на жири та вуглеводи (Dietzel E. et al., 2013).
Таким чином, патогенез передчасного розриву плодових оболонок не є вивченим настільки досконало, щоб розробляти чутливі діагностичні критерії та профілактичні заходи. Тому більшість лікарів контактує з проблемою ПРПО на етапі невідворотності пологів та необхідності вибору тактики з огляду на незрілість плода, готовність пологових шляхів та ризик інфікування плодового яйця. Протягом останніх 10 років погляди на ведення доношеної та недоношеної вагітності, ускладненої ПРПО, значно змінились.
В першу чергу, це стосується доношеної вагітності. З 1993 року провідною рекомендацією у таких випадках була індукція пологів, вибір препарату для якої залежав від ступеня зрілості шийки матки [33, 34]. Головним аргументом при цьому виступало збільшення з кожними 4 годинами пролонгування вагітності частоти гістологічно виявленого хоріоамніоніту. Haqskoq K.et al. (1994) вказували на зростання ризику неонатального інфікування та дистресу плода з наростаннями тривалості безводного проміжку, та головним аргументом на користь негайної індукції пологів вважали відсутність чітких прогностичних критеріїв перерахованих ускладнень [18].
2007 року Бюлетень Американського коледжу акушерства та гінекології зазначив ефективність очікувальної тактики, зазначаючи, що протягом 12 годин від моменту ПРПО пологи розпочинаються у 50% пацієнток, 24 годин – у 70%, 48 годин – у 85%, 72 годин (без акушерського втручання!) – у 95% пацієнток. За даними A. Coughy et al., (2008), чим меншим є гестаційний термін, тим довшою буде латентна фаза передчасних пологів, спричинених ПРПО. Вкорочення латентної фази першого періоду пологів пропонували прогнозувати за зменшенням товщини міометрію у нижньому сегменті матки (до 12 мм за даними УЗД), втім пізніше цей критерій не знайшов підтвердження [24].
Очікувальна тактика показала зниження частоти абдомінального розродження, переважно за рахунок невдалої індукції пологів та дистресу плода [6]. Протягом наступних 5 років така точка зору домінувала у професійних колах. 2014 року з'являються нові дані про зростання ризику хоріоамніоніту на тлі очікувальної тактики (S. Kilpatrick), що виступають аргументом на користь індукції пологів при ПРПО після 34 тижнів.Тоді як A. Wojcieszek et al. (2014) вказують на відсутність вірогідних відмінностей в частоті хоріоамніоніту та післяпологових септичних ускладнень, перинатальної смертності та неонатального сепсису між очікувальною тактикою та індукцією пологів після 34 тижнів. До слова, в цьому ж дослідженні було проаналізовано ефективність застосування антибактеріальної терапії у разі очікувальної тактики при ПРПО. Таку ефективність було показано лише щодо зниження частоти хоріоамніоніту, щодо неонатального сепису, перинатальної смертності та материнської післяпологової захворюваності відмінностей виявлено не було.
Незважаючи на дискусію, що триває, бюлетень Американського коледжу акушерства та гінекології від 2013 року рекомендує проводити індукцію пологів у терміні після 34 тижнів в разі ПРПО. До очікувальної тактики рекомендовано вдаватись лише за інформованої відмови жінки від індукції в термін після 37 тижнів вагітності, з усвідомленням нею всіх можливих наслідків, та не більше, ніж на 24 години за відсутності ризику розвитку інфекції, викликаної стрептококком групи В. При цьому антибіотик має бути призначений через 18 годин від моменту вилиття вод та вводитися до завершення пологів. Окремою ремаркою в бюлетені зазначено, що латентну фазу пологів у випадку індукції пологів варто продовжити до 12–18 годин, тобто визнавати спробу індукції невдалою лише після цього часу. Ці рекомендації суперечать актуальному наразі Наказу МОЗ України №782 від 29.12.2005 «Про затвердження клінічних протоколів з надання медичної допомоги «Передчасний розрив плодових оболонок». Згідно до нього, перевагу варто віддавати очікувальній тактиці, втім рік видання цих настанов дозволяє очікувати на їх перегляд найближчим часом.
Ще більш складним питанням є тактика ведення ПРПО при недоношеній вагітності. Не викликає сумнівів доцільність певного проміжку очікування для дозрівання легенів плода, для чого з успіхом використовують курс стероїдних гормонів. Проте протягом останнього десятиріччя змінились погляди і на це. 2007 року не викликала сумнівів доцільність проведення стероїдної профілактики в терміни 24–32 тижні, а дані щодо термінів 32–34 тижні були суперечливими саме з позицій ефективності. Пропонувалось рутинна оцінка ступеня зрілості легеневої тканини у ці терміни для визначення необхідності проведення стероїдної профілактики [9]. Американський коледж акушерства та гінекології у своєму бюлетені 2013 року підкреслив зміну поглядів на ведення вагітних з ПРПО в терміни 32–34 тижні, а саме рекомендував проведення курсу дексаметезону/бетаметазону, що має позитивний вплив не лише на частоту розвитку та тяжкість дихальних розладів, але й інших приманних недоношеним ускладнень – некротичного ентероколіту та внутрішньошлуночкових крововиливів [7].
Призначення антибіотиків у разі ПРПО при вагітності менше 34 тижнів є обов’язковим з метою подовження латентної фази. Препаратом вибору на сьогодні є Еритроміцин (10 діб). У разі наявності факторів ризику інфекції, викликаної стрептококком групи В, з початку пологів та до їх завершення призначається антибіотикопрофілактика.
Для лікарів, що безпосередньо надають допомогу вагітним із ПРПО при недоношеній вагітності, з практичної точки зору надзвичайно актуальним є питання видалення цервікального шва з шийки матки та акушерського песарію. Щодо першого, то у дослідженні M. Laskin et al. (2014) було порівняно вплив негайного зняття шва та відкладення його на час проведення курсу профілактики пневмопатії на інфікування матері та плода. Авторами було показано відсутність відмінностей між описаними тактиками за часом пролонгування вагітності, розвитком неонатального сепсису, перинатальною смертністю та материнською післяпологовою захворюваністю. Ефективність акушерського песарію взагалі не є доведеною масштабними дослідженнями [1], тому даних про оптимальний час його видалення при ПРПО не вивчене.
Враховуючи невідворотність пологів внаслідок передчасного розриву плодових оболонок, було здійснено велику кількість спроб попередження подальшого витікання навколоплідних вод. Плодові оболонки надзвичай бідно постачаються кров'ю,тому демонструють в експерименті майже повну відсутність загоєння. Вважається, що закриття дефекту мембран після амніоцентезу відбувається за рахунок їх злипання, а не шляхом проліферації клітин та типового процесу загоєння [17]. Тим не менше, запропоновано численні спроби закриття цього дефекту, що є наслідком спонтанного розриву плодових оболонок. З цією метою використовували механічні пристрої [35], желатинові та колагенові тампони [28], фібринові імпланти [30]. 2011 року J. Deprest et al. запропонували застосовувати з цією метою спеціальний біологічно активний матеріал, що містить стимулятори клітинної проліферації. 2016 року A. Crowley et al. опублікували результати мета-аналізу, присвяченого оцінці ефективності цих методів. Аналіз включив 141 вагітну, в результатах не показано жодних статистично вірогідних змін в показниках перинатальної смертності та материнської захворюваності, як при порівнянні традиційної тактики із кожним із перелічених методів, так і при порівнянні методів між собою. Єдиним позитивним впливом, що його автори виявили саме від застосування біологічно активного матеріалу, є зменшення частоти пологів до 37 тижнів. Втім, це зниження частоти передчасних пологів не супроводжувалось зменшенням показника перинатальної смертності, частота неонатального сепсису навіть мала тенденцію до збільшення. Таким чином, на сучасному етапі розвитку акушерства питання відновлення плодових оболонок не є перспективним.
Більші шанси на широке впровадження має амніоінфузія як спроба відновлення обсягу амніотичної рідини при передчасному розриві плодових оболонок при недоношеній вагітності. Вперше такий спосіб було запропоновано 1983 року F. Miyazaki та N. Taylor з метою запобігання стиснення судин пуповини. Пізніше було показано, що комбінація повторної амніоінфузії фізіологічного розчину та антибактеріальної терапії при ПРПО дозволяє продовжити вагітність при недоношеній вагітності [25]. 2012 року G. Hofmeyr et al. у рамках Кохрейнівського співтовариства опублікували аналіз досліджень, що продемонстрував ефективність амніоінфузії при доношеній вагітності з точки зору зниження частоти кесарського розтину з причини дистресу плода.
2014 року той самий колектив провів огляд досліджень, присвячених застосуванню методики при недоношеній вагітності, порівнюючи очікувальну тактику із трансцервікальною та трансбдомінальною амніоінфузією [21]. Серед результатів трансцервікальної амніоінфузії автори відмітили покращення середнього значення Рh пуповинної крові та зменшення частоти варіабельних децелерацій, що дозволило їм оцінити метод як ефективний з точки зору профілактики дистресу плода. Натомість, лише при трансабдомінальній амніоінфузії на підставі 4 рандомізованих досліджень було показано зниження показників перинатальної смертності та неонатального сепсису, а також післяпологового сепсису.
Тим не менше, на сучасному етапі акушерства відсутня достатня кількість та якість доказів щодо ефективності амніоінфузії для зниження частоти кесарського розтину, народження дітей з низькою оцінкою за Апгар та неонатальної смертності. Отже, проведення її не рекомендується (RCOG, 2010).
Було досліджено також економічну доцільність госпіталізації пацієнток із ПРПО [6]. Ризик дистресу плода, спричиненого здавленням пуповини, її випадінням, передчасного відшарування плаценти не виправдовував перебування таких пацієнток вдома ні з точки зору неонатальних наслідків, ні з економічних позицій.
2014 року G. Senoun et al. опублікували результати мета-аналізу, присвяченого порівнянню материнських та неонатальних наслідків госпіталізації та домашнього перебування пацієнток із ПРПО при недоношеній вагітності. До аналізу було включено лише 2 дослідження, що відповідали вимогам доказових висновків та охоплювали 116 вагітних з гестаційним терміном 34–37 тижнів. Варто зазначити, що незалежно від режиму перебування, всі пацієнтки не отримували токоліз, їм було призначено лише пероральні антибактеріальні препарати, тобто за лікуванням групи в обох дослідженнях було стандартизовано.
На відміну від попередніх даних, автори не отримали вірогідних відмінностей у тривалості пролонгування вагітності, вазі новонароджених, оцінці їх за шкалою Апгар, частоті вродженого інфікування, тривалості реанімаційної підтримки, показникові неонатальної смертності. Що стосується материнських наслідків, то в обох групах з однаковою, незначною частотою було зареєстровано випадки хоріоамніоніту, післяпологового ендометриту. Єдиною статистичною відмінністю між групами стала більш висока частота абдомінального розродження у групі стаціонарного лікування, якій автори не знайшли пояснення. Тим не менше, світовий дослід та досвід Перинатального центру м. Києва, де щороку відбувається не менше 600 ПП, свідчить про доцільність госпіталізації пацієнток із ПРПО при недоношеній вагітності. Це дозволяє ретельно спостерігати за станом плода, контролювати вчасність та режим застосування антибактеріальних препаратів, швидко розпочати надання медичної допомоги у разі передчасного відшарування плаценти.
Важливими ланками надання медичної допомоги вагітним із ПРПО при недоношеній вагітності є профілактика інфікування гемолітичним стрептококом групи В та нейропротекція недоношеного плода, проте ці проблеми заслуговують на окремі огляди, з якими читача буде ознайомлено у майбутніх випусках. На особливу увагу заслуговує також індукція пологів в разі ПРПО як при доношеній, так і при недоношеній вагітності, що також буде висвітлено у майбутніх публікаціях.
Перелік літератури знаходиться у редакції.
Детальніше

Ведення жінок з нудотою і блюванням під час вагітності (частина 2)
 Шановні колеги! До вашої уваги – друга частина клінічних рекомендацій Королівського коледжу акушерів та гінекологів щодо ведення жінок з нудотою та блюванням під час вагітності. Метою даного керівництва є надання заснованої на фактичних даних або найкращому клінічному практичному досвіді інформації у розрізі груп населення, що перебувають в умовах амбулаторного догляду та стаціонару. Дане керівництво було опубліковано у червні 2016 року
Шановні колеги! До вашої уваги – друга частина клінічних рекомендацій Королівського коледжу акушерів та гінекологів щодо ведення жінок з нудотою та блюванням під час вагітності. Метою даного керівництва є надання заснованої на фактичних даних або найкращому клінічному практичному досвіді інформації у розрізі груп населення, що перебувають в умовах амбулаторного догляду та стаціонару. Дане керівництво було опубліковано у червні 2016 року
- Моніторинг стану та побічні ефекти
6.1 Ускладнення або несприятливі ефекти, що можуть статися внаслідок НБВ і ТБВ та стратегії їх профілактики
Детальніше