
Сучасні можливості діагностики порушень стану вагінального біотопа

Вагінальна екосистема бере участь у процесі репродукції, захищає від значної кількості інфекційних патогенів і є однією з важливих регуляторних систем, яка має великий вплив на здоров’я жінки. Більшість захворювань, які порушують мікробний пейзаж у піхві, супроводжуються появою патологічних виділень зі статевих шляхів [7, 11]. Наявність піхвових білей є найбільш частою причиною візиту до гінеколога. При цьому майже 70% випадків становлять вагінальний кандидоз (ВК), бактеріальний вагіноз (БВ) і трихомонадний вагініт. Інші 30% складають аеробний вагініт, десквамативний запальний вагініт, атрофічний вагініт, цитолітичний вагіноз (ЦВ) та інші рідкісні захворювання [15, 17]
Усі ці патологічні стани можна поділити за патогенезом на незапальні та запальні. Серед незапальних найбільш поширеним є БВ. Наявність вираженої клінічної картини у вигляді подразнення, гнійних виділень і наявність поліморфноядерних нейтрофілів у аналізі виділень характерно для запального процесу. Найбільша кількість піхвових білей зустрічається при БВ, аеробному вагініті, ВК і трихомоніазі. Ураження цервікального епітелію хламідійною або гонококковою інфекцією також призводить до значних виділень з піхви [13]. Окрім цього, появою білей супроводжуються неспецифічні вагініти та цервіцити, ектопія циліндричного епітелію. Подібною симптоматикою можуть характеризуватися вульварні дерматози або алергічні реакції [15]. Тому пріоритетом у веденні жінок з патологічними виділеннями є діагностика етіологічного фактора.
Питання етіології БВ до сих пір залишається дискусійним. Нещодавно з’явилася концептуальна модель патогенезу БВ. Первинними етіологічними факторами цього захворювання вважають Gardnerella vaginalis і Prevotella bivia. Вони є традиційними коменсалами вагінального біотопу. Вторинно до них приєднуються Atopobium vaginae і Sneathia spp., що характеризує наявність плідного альянсу в біоплівці [8–10]. Останнє супроводжується пригніченням локальної імунної відповіді на рівні слизової піхви. Тому БВ є незапальною хворобою з дефіцитом лейкоцитарної реакції. Цьому сприяє наявність анаеробних мікроорганізмів. На тлі БВ значно підвищений рівень запальних захворювань малого тазу, інфекцій матері та плода під час вагітності та у пуерперії [1, 2]. БВ призводить до майже повної загибелі лактобацил. Існує точка зору, що БВ є locus minori resistencia у жінок із запальними захворюваннями органів малого тазу. Це сприяє хронізації процесу та обумовлює схильність до рецидивування [3].
На сьогодні відомо більше ніж 200 мікробних штамів, що можуть знаходитися у піхві в нормальних або патологічних умовах. Вагінальний мікробіом залежить від впливу зовнішнього середовища, генетичних і етнічних факторів, поведінкових особливостей. У піхві здорових жінок визначаються лише деякі типи лактобацил. Ці мікроорганізми мають синергічний з гуморальними факторами імунітету, антибактеріальними речовинами, цитокінами та дефензинами вплив на екологічний пейзаж вагіни [7, 13].
Надмірний зріст лактобацил також негативно впливає на стан епітелію піхви завдяки порушенню кислотно-лужного балансу. Це руйнує вагінальний епітелій. Відомо, що значне збільшення вмісту у піхвовій мікробіоті L. crispatus є ключовим фактором розвитку ЦВ [5]. ЦВ характеризується значною колонізацією лактобацил, що призводить до різкого зниження рН, запальними змінами слизової піхви та цитолізом епітелію. При бактеріоскопії існують деякі труднощі у діагностиці цитолізу. Іноді лаборанти помилково вважають цитолітичні клітини «ключовими», що призводить до хибної діагностики БВ [15]. Деякі зовнішні або внутрішні фактори, які впливають на вагінальний мікробіом, можуть призводити до ЦВ. У нещодавних дослідженнях було доведено, що у жінок з ЦВ домінування Lactobacillus spp. серед інших коменсалів вагінального біотопа викликає лізис епітелію [17]. Отже, Lactobacillus crispatus і Lactobacillus sp. є біомаркерами ЦВ. При цьому Lactobacillus sp. у нормальних умовах має регулюючий вплив на інші лактобацилли шляхом стримування їх зайвої колонізації.
ВК на сьогодні має «нове» обличчя, що обумовлено змінами у внутрішньородовому складі та появою інвазивних властивостей Candida. Певну роль у цьому процесі зіграв невдалий досвід тривалого використання антимікотичних препаратів системної дії. ВК може виникати спільно з БВ. Candida albicans традиційно вважається найбільш поширеним коменсалом урогенітальної системи. Поширеність Candida non-albicans зросла з 10% до 45% [6]. Відомо, що клінічна симптоматика при наявності C. glabrata, C. tropicalis, C. krusei, C. parapsilosis і C. guilliermondii є менш вираженою. Також існує тенденція до хронізації процесу з рецидивуванням і залежність від коморбідної патології [5, 15].
Аеробний вагініт був вперше описаний у 2002 році. Він характеризується дисбіозом піхви з переважно аеробною мікрофлорою, кишковими бактеріями, різними рівнями вираженості запалення у слизовій піхви та порушенням дозрівання вагінального епітелію. У анаеробного вагініту є спільні риси з БВ: загибель лактобацил, наявність значних білей з гнилісним запахом і підвищення рН. Проте, при аеробному вагініті піхвова слизова виглядає гіперемованою і набряклою. Іноді навіть відмічаються невеликі ерозії та виразки [4]. При БВ частіше за все зустрічаються сірі рідкі виділення, а на тлі аеробного вагініту – жовто-зелені слизової консистенції. При БВ у піхві виявляються переважно анаеробні коменсали. А при аеробному вагініті найчастіше зустрічаються Streptococcus agalactiae, Staphylocuccus aureus або Escherichia coli [11]. При мікроскопії піхвових виділень у пацієнток з аеробним вагінітом відмічається наявність лейкоцитів і незрілих парабазальних епітеліальних клітин.
Десквамативний запальний вагініт – це рідкісна форма хронічного гнійного запалення піхви. Етіологія і патогенез десквамативного запального вагініту є не досить вивченими. Клінічна симптоматика є досить неспецифічною: гнійні виділення, подразнення піхви та вульви, диспареунія. Тому десквамативний запальний вагініт є діагнозом виключення. При огляді слизової піхви відмічається гіперемія і петехії. Вагінальне рН є підвищеним, а при мікроскопії визначається збільшений вміст незрілих епітеліальних клітин [12]. Найчастіше виникає у жінок перименопаузального віку. Тому необхідно диференціювати з БВ, ВК, аеробним вагінітом і атрофічним вагінітом. Останній є проявом проміжних перименопаузальних розладів і може поєднуватися з іншими симптомами урогенітальної атрофії [11].
Емфізематозний вагініт зустрічається дуже рідко і характеризується присутністю множинних заповнених газом кіст на слизовій оболонці піхви або екзоцервіксі. Етіологія залишається невідомою. Перебіг захворювання, як правило, доброякісний. Хворі скаржаться на свербіж і кров’яні виділення з піхви. При обстеженні можна знайти ознаки гострого або хронічного запалення. Огляд у дзеркалах супроводжується крепітацією [16]. Ця патологія може бути приводом для гіпердіагностики та надмірного лікування.
Безумовно, що обстеження жінок з піхвовими виділеннями має враховувати наявність збудників захворювань, що передаються статевим шляхом: гонореї, хламідіозу і мікоплазмозу. У одному дослідженні було проведено оцінку діагностичної цінності 4 симптомів для виявлення лабораторно підтвердженої гонореї, хламідіозу, трихомоніазу, вірусу папіломи людини та сифілісу серед 1337 статевозрілих жінок з Ірану. Було встановлено, що 37,7% обстежених мали вагінальні виділення, 25,9% повідомили про біль або печію, 3,0% – генітальні виразки, а 1,4% – статеві бородавки. У той же самий час наявність лабораторно підтвердженого сифілісу, гонореї, хламідіозу, трихомоніаза та віруса папіломи людини становила: 0,4%, 1,3%, 6,0%, 11,9% та 41,9%, відповідно. Чутливість наявності вагінальних виділень становила 40,3% для виявлення трикомоніазу, 37,5% при хламідіозі та 37,5% при гонореї. Чутливість болі та печії коливалася від 12,5% при гонореї до 25,2% при трихомоніазі. Чутливість генітальної виразки та статевих бородавок була дуже низькою для усіх статевих інфекцій. Чутливість усіх симптомів у поєднанні також була нижчою 50%. Серед безсимптомних респондентів 41,2% мали позитивний результат на вірус папіломи людини, 11,8% – на трихомоніаз та менше 6,6% на інші інфекції, що розповсюджуються статевим шляхом [14]. Тому діагностика і лікування хворих на інфекції, що передаються статевим шляхом, на підставі клінічних симптомів є неприпустими і можуть призвести до неправильної класифікації значної частини випадків.
Найважливішу роль у менеджменті хворих з патологічними піхвовими виділеннями відіграє лабораторна діагностика. Сучасні діагностичні тести базуються на методах ампліфікації нуклеїнових кислот. Це дозволяє виділити фрагменти збудника навіть при наявності однієї копії у зразку матеріалу. На сьогодні ці методи мають найбільшу діагностичну точність. Чутливість тестів останнього покоління на тлі полімеразної ланцюгової реакції у режимі реального часу є максимальною і наближається до 100% [2, 3].
В Україні великою популярністю користується тест «Флороценоз». «Флороценоз» – це група досліджень на основі високоточної мультиплексної ПЛР-діагностики у режимі реального часу, що дозволяє у якісному і кількісному форматі діагностувати основні форми урогенітальних інфекцій: гонококкову, хламідійну, мікоплазмову і трихомонадну. Також можливо встановлювати наявність клінічно значущих видів кандид: С. albicans, C. glabrata, C. krusei, C. parapsilosis/C. tropicalis. До «Флороценозу» входить 5 тестів: на аероби, Candida spp., БВ, мікоплазми та інфекції, що передаються статевим шляхом (N. gonorrhoeae, C. trachomatis, M. genitatalium, T. vaginalis). Особливість методу діагностики дозволяє провести диференціальне виявлення важко культивованих мікроорганізмів (Atopobium vaginae, Gardnerella vaginalis). Це забезпечує можливість діагностувати безсимптомні форми БВ, ВК, викликаний С. non-albicans, і оцінювати ризик рецидиву захворювання.
Проведення тесту «Флороценоз» дозволяє:
- провести комплексну оцінку маркерів анаеробного дисбіозу в кількісному форматі;
- визначити співвідношення між мікроорганізмами;
- і зробити висновок про стан вагінального біотопу.
Наприклад, при БВ природна лактофлора пригнічується іншою мікрофлорою (Bacteria spp, Gardnerella vaginalis, Atopobium vaginae). При аеробному вагініті відмічається переважання аеробів (Enterobacteriaceae, Streptococcus spp., Staphylococcus spp.) на тлі зниження «корисних» лактобацил. А мікоплазмова інфекція асоційована з умовно-патогенними мікоплазмами і уреаплазмами, які можуть бути присутніми у незначній кількості серед інших резидентних штамів: Ureaplasma parvum, Ureaplasma urealyticum, Mycoplasma hominis [3, 15, 17].
Висновок
Тест «Флороценоз» – надійний діагностичний інструмент акушера-гінеколога. Дизайн тестів створено відповідно до сучасних наукових знань і уявлень про урогенітальні інфекції. Він забезпечує комбінування мікроорганізмів за нозологіями і синдромами. Надає значні можливості застосування для диференціальної діагностики, скринінгу і контролю лікування, а також максимальну швидкість отримання результатів. «Флороценоз» – це універсальність підходу при мінімальної ймовірності лабораторної помилки. Залишається лише використовувати його у повсякденній роботі задля збереження здоров’я жінки.
Перелік літератури
- Allsworth J. E. Bacterial vaginosis–race and sexual transmission: issues of causation // Sex Transm Dis. – 2010. – Vol. 37. – P. 137-139.
- Cartwright C. P., Pherson A. J., Harris A. B., et al. Multicenter study establishing the clinical validity of a nucleic-acid amplification-based assay for the diagnosis of bacterial vaginosis // Diagn Microbiol Infect Dis. – 2018. – Vol. 92, No 3. – P. 173-178.
- Coleman J. S., Gaydos C. A. Molecular Diagnosis of Bacterial Vaginosis: an Update // J Clin Microbiol. – 2018. – Vol. 56, No 9. – pii: e00342-18.
- Donders G.G.G., Bellen G., Grinceviciene S., et al. Aerobic vaginitis: no longer a stranger // Res Microbiol. – 2017. – Vol. 168, No 9-10. – P.845-58.
- Hu Z., Zhou W., Mu L., et al. Identification of cytolytic vaginosis versus vulvovaginal candidiasis // J Low Genit Tract Dis. – 2015. – Vol. 19, No 2. – P. 152-5.
- Makanjuola O., Bongomin F., Fayemiwo S. A. An Update on the Roles of Non-albicans Candida Species in Vulvovaginitis // J Fungi (Basel). – 2018. – Vol. 4, No 4. – pii: E121.
- Mendling W. Vaginal microbiota // Adv Exp Med Biol. – 2016. – Vol. 902. – P. 83-93.
- Muzny C.A., Laniewski P., Schwebke J.R., Herbst-Kralovetz M.M. Host-vaginal microbiota interactions in the pathogenesis of bacterial vaginosis // Curr Opin Infect Dis. – 2020. – Vol. 33, No 1. – P. 59-65.
- Muzny C. A., Schwebke J. R. Pathogenesis of Bacterial Vaginosis: Discussion of Current Hypotheses // J Infect Dis. –2016. – Vol. 214, Suppl. 1. – S.1-5.
- Muzny C.A., Taylor C.M., Swords W.E., et al. An Updated Conceptual Model on the Pathogenesis of Bacterial Vaginosis // J Infect Dis. – 2019. –pii: jiz342.
- Paladine H. L., Desai U. A. Vaginitis: Diagnosis and Treatment // Am Fam Physician. – 2018. – Vol. 97, No 5. – P. 321-329.
- Reichman O., Sobel J. Desquamative inflammatory vaginitis // Best Pract Res Clin Obstet Gynaecol. – 2014. – Vol. 28, No 7. – P. 1042-50.
- Reid G. Has knowledge of the vaginal microbiome altered approaches to health and disease? // F1000Res. – 2018. – Vol. 13, No 7. – P. 460.
- Shahesmaeili A., Karamouzian M., Shokoohi M., et al. Symptom-Based Versus Laboratory-Based Diagnosis of Five Sexually Transmitted Infections in Female Sex Workers in Iran // AIDS Behav. – 2018. – Vol. 22, No Suppl. 1. – P. 19-25.
- Sherrard J., Wilson J., Donders G., et al. 2018 European (IUSTI/WHO) International Union against sexually transmitted infections (IUSTI) World Health Organisation (WHO) guideline on the management of vaginal discharge // Int J STD AIDS.– 2018. – Vol. 29, No 13. – P. 1258-1272.
- Tereso A. F. B., Granadas J. C. C., Baptista M. F. S. What you should know about emphysematous vaginitis? // Clin Case Rep. – 2019. – Vol. 7, No 12. – P. 2590-2591.
- Vaginitis in Nonpregnant Patients: ACOG Practice Bulletin, Number 215 // Obstet Gynecol. – 2020. – Vol. 135, No 1. – e1-e17.

Детальніше

Вже вчетверте 8–9 листопада у Києві відбувся Профі-Лаб «Східноєвропейські зустрічі професіоналів: ультразвук в акушерстві та гінекології»
Вже вчетверте 8–9 листопада у Києві відбувся Профі-Лаб «Східноєвропейські зустрічі професіоналів: ультразвук в акушерстві та гінекології»
У програмі були представлені дуже важливі для кожного практикуючого лікаря теми: специфічні ускладнення вади серця у плода при монохоріальній двійні; скринінг вроджених вад розвитку плода в 11–14 тижнів вагітності; скелетні дисплазії; ехо-маркери аномалій обличчя плода; ехографія рубця матки після кесарського розтину; оцінка глибокого інфільтративного ендометріозу; оваріальні кісти у вагітних та інші.
Всі учасники мали можливість відвідати майстер-класи професора Rabih Chaoui з Німеччини «Дослідження серця плода для досвідчених фахівців» та нейрофізіолога Han Zhen з Канади, яка представила аналіз складних клінічних випадків у І, ІІ та ІІІ триместрах.
З цьогорічних нововведень можна назвати роботу паралельного залу із лайв-стрімом кейсів від лікарів-практиків, де кожен бажаючий міг стати спікером та представити свій клінічний досвід, а також HANDS-ON залу для вдосконалення практичних навичок з майстер-класами знаних спеціалістів.
Найсучасніші знання та атмосфера професійного спілкування неодмінно запам’ятаються учасникам конференції!




Сучасні погляди на доцільність та способи лікування нетримання сечі у жінок
Нетримання сечі (НС) традиційно визначають як мимовільну втрату сечі, або як сечопускання тоді, коли особа цього не бажає, або неможливість попередити сечопускання. Частоту НС в популяції важко точно оцінити, адже не завжди жінки, що мають цю скаргу, готові активно обговорювати її з лікарем. За офіційною статистикою, частота коливається у межах 10–40%, тяжких форм — 3–17%. НС асоційоване з фізичним дискомфортом, сексуальною дисфункцією, розладами психологічного балансу, втратою незалежності та зменшенням соціальної активності
НС поділяють на стресове, ургентне та змішане. Стресове НС (СНС) – мимовільна втрата сечі при фізичній активності, що супроводжується підвищенням тиску в черевній порожнині (кашель, чхання тощо). Міжнародна урогінекологічна асоціація пропонує виділяти окрему форму уродинамічного СНС – мимовільного сечопускання при підвищенні внутрішньочеревного тиску за відсутності скорочення детрузора. Встановлення такого діагнозу вимагає виконання уродинамічного дослідження, тому він не зазнав широкого застосування в практиці. Ургентне НС – відсутність контролю за сечопусканням.
Близько до питання НС перебуває проблема гіперактивного сечового міхура – мимовільного скорочення детрузора, що лежить у площині неврологічних розладів та також вимагає проведення неврологічного дослідження [10].
1 з 3 жінок старших 18 років має проблему СНС, кожна жінка після досягнення цього віку має ймовірність 14% протягом життя зазнати оперативного втручання з приводу СНС [9].
Патогенез або механізм НС достеменно невідомий. Так, T. Enhorung (1961), провівши вимірювання тиску в черевній порожнині та в уретрі, припустив, що хвиля, ініційована кашлем чи іншим напруженням, передається в уретру, супроводжуючись зменшенням обтураційних можливостей уретрального сфінктера, що призводить до СНС. Первинний дефект м’язів уретрального сфінктера було винесено як першопричину НСMcGuire (1990). Ці дві теорії лягли в основу розробки таких оперативних втручань, як кольпосуспензія та везико-уретральна суспензія.
Протилежна теорія носить назву «теорії гамака». Їі автор Lancey (1994) взяв за основу умову, необхідну для утримання сечі під час підвищення внутрішньочеревного тиску. В нормі підвищення тиску в черевній порожнині супроводжується його передачею на шийку сечового міхура, що надає уретрі більш проксимального положення, що призводить до її стискання між лонно-везікальною фасцією та передньою стінкою піхви. Більш сучасні дослідження показали, що роль у цьому стисканні та залежному від нього утриманні сечі відіграють лонно-уретральні зв’язки, що є локалізованими у середній третині уретри. Спричинене віком, гормональними змінами та генетичною схильністю ослаблення цих зв’язок та фасцій має наслідком недостатнє стискання уретри під час підвищення черевного тиску та НС. Ця теорія стала науковим обґрунтуванням іншого виду оперативного втручання – імплантації підтримуючої стрічки (слінгу) у проекцію середньої третини уретри піхви [9].
Попри розробку різних способів корекції НС, проблема залишається актуальною, тому до уваги читача запропоновано огляд сучасних аналізів ефективності лікування.
Зміна способу життя є найдоступнішим та безпечним способом лікування проблеми. 2015 року M. Imamura et al. опублікували в рамках Кохрейнівського співтовариства результати мета-аналізу, присвяченого вивченню ефективності поведінкових реакцій щодо лікування НС. Зокрема, 4 дослідження, які охопили 4701 жінку, вивчали ефективність втрати ваги для усунення симптомів НС. Лише в одному дослідженні, що порівнювало учасниць програм втрати ваги з групою контролю, які зовсім не отримувала лікування, отримано докази низької сили стосовно зменшення або зникнення симптомів через 6 місяців (76% в групі учасниць програми втрати ваги проти 54% в групі контролю), відмінності між групами зберігались протягом 18 місяців від початку спостереження.
У цьому дослідженні відсутні дані стосовно покращення якості життя від застосування запропонованого заходу.
Дуже низьку силу доказів мають результати ще одного дослідження, яке продемонструвало зменшення кількості випадків НС на тиждень при досягненні втрати ваги шляхом модифікації способу життя при порівнянні з фармакологічним зменшенням ваги.
Наступним способом лікування НС з категорії заходів модифікації способу життя є обмеження споживання рідини. До аналізу було включено три дослідження, що охопили загалом 181 жінку та порівнювали обмеження споживання рідини з відсутністю лікування.
Отримано дуже низької сили докази стосовно покращення якості життя на кілька пунктів у жінок, що вдавались до обмеження споживання рідини, натомість більшість із них вказувала на закрепи, головний біль та відчутну спрагу.
Три дослідження, що охопили 160 жінок, порівнювали ефективність обмеження кофеїнвмісних напоїв з відсутністю лікування, ще два (охоплено 42 жінки) – звичайну дієту з дієтою, збагаченою содою. Низька методологічна якість цих досліджень не дозволяє робити висновків стосовно ефективності описаних методів.
Для таких змін способу життя, як обмеження вживання алкоголю, солодкого, відмова від паління, уникнення закрепів, тяжких фізичних навантажень, помірні фізичні тренування, у жодному з включених до мета-аналізу рандомізованих або квазі-рандомізованих досліджень не було продемонстровано ефективності в зменшенні або усуненні проявів НС [11].
Кероване сечопускання – до цієї групи належать всі рекомендації стосовно розкладу відвідування туалету та спорожнення сечового міхура (відвідування туалету по годинах). Лише один мета-аналіз було присвячено вивченню ефективності цього заходу [12] при порівнянні з відсутністю лікування. До нього було включено 9 досліджень, які охоплювали 674 жінки, переважно похилого віку.
Мета-аналіз продемонстрував зменшення кількості епізодів НС протягом першого року спостереження. Натомість зазначено про відсутність доказів ефективності заходу після одного або 5 років його застосування, а також про збереження ефекту після відмови від заходу.
Акупунктура як спосіб нетрадиційного лікування набуває все більшої популярності, особливо в країнах Азії. Y. Wang et al. (2013) об’єднали у мета-аналіз 17 досліджень, що порівнювали ефективність застосування акупунктури для лікування НС з медикаментозною терапією. Аналіз показав відсутність статистично обґрунтованих доказів більш високої ефективності акупунктури, проте чітко було окреслено значно меншу кількість побічних ефектів, ніж при медикаментозному лікуванні.
Одним з найбільш поширених неінвазивних способів лікування НС є тренування м’язів тазового дна. Переважно рекомендують цей захід для лікування СНС, значно рідше – змішаного або УНС. 2018 року Ch. Dumoulin et al. опублікували результати системного аналізу порівняння ефективності цього заходу з відсутністю лікування. До аналізу було включено 31 дослідження, він охопив 1817 жінок з різними формами нетримання сечі.
Всі дослідження тривали не менше 12 місяців, автори порівнювали частоту повного усунення симптомів та клінічне покращення, покрашення якості життя, кількість епізодів нетримання сечі протягом 24 годин та протягом годинного «тесту прокладки».
Було зазначено, що пацієнтки, які протягом 12 місяців адекватно використовували вправи м’язів тазового дна, у вісім разів частіше свідчили про зникнення епізодів СНС (тобто про клінічне одужання), ніж пацієнтки, що не отримували лікування (56% проти 6%), що є свідченням високої якості доказовості.
Щодо всіх видів НС (як стресового, так і ургентного), застосування тренування м’язів тазового дна в шість разів збільшує ймовірність клінічного одужання при порівнянні з відсутністю лікування (35% проти 6%) (середня якість доказовості). Клінічне покращення жінки з СНС відмічали у шість разів частіше у разі дотримання тренування м’язів тазового дна, ніж у разі відсутності лікування (74% проти 11%), а при аналізі групи з всіма формами НС ця відмінність зменшується до двох разів (67% проти 29%) (середня сила доказів).
Якість життя у жінок з СНС, що дотримувались тренувань м’язів тазового дна, вивчали 6 досліджень, всі вони відмітили істотне покращення цього показника при порівнянні з відсутністю лікування (середня сила доказів).
Ще 4 дослідження вивчали аналогічне питання у жінок з УНС, одне – у жінок з змішаним НС, в них також виявлено істотне покращення якості життя при дотриманні тренувань, щоправда, силу цих доказів системним аналізом визнано як слабку.
Дотримання тренувань м’язів тазового дна через 12 місяців призводить до статистично значимого зменшення кількості мимовільних сечопускань протягом доби у жінок з СНС (7 досліджень, середня сила доказів) та у жінок з всіма видами НС (4 дослідження, середня сила доказів).
При аналізі кількості спонтанних сечопускань протягом годинного «тесту прокладки» також було підтверджено значно більшу ефективність від дотримання тренувань м’язів тазового дна, ніж від відсутності лікування, як у разі виключно СНС (4 дослідження, середня сила доказів), так і при всіх видах НС (2 дослідження, середня сила доказів).
Крім того, системний аналіз окреслив переважну задоволеність пацієнток від описаного методу лікування, одночасне покращення сексуальної функції. У метода цілком відсутні небажані побічні ефекти, тому його сміливо можна рекомендувати жінкам зі скаргами на НС будь-якого віку [2].
Одним з прикладів медикаментозної терапії НС є призначення естрогенів місцево або системно. Теоретичне обґрунтування такого призначення лежить в площині високої чутливості тканини малого тазу, у тому числі сечового міхура та м’язів тазового дна, до естрогенів. 2012 року CodyJ et al. надали результати мета-аналізу, до якого ввійшли 42 дослідження ефективності призначення естрогенів для лікування НС. В цілому ці дослідження охопили 19 676 жінок, були гетерогенними за типом препарату, його дозою, тривалістю застосування та способом введення.
У цілому мета-аналіз засвідчив, що застосування препаратів естрогенів лише посилює прояви НС (відносний ризик посилення симптомів – 1,32). Виділення окремо жінок з інтактною маткою та приймом перорально комбінації естрогену та прогестерону також демонструє відносний ризик 1,11. Зниження частоти та тяжкості НС виявлено лише у дослідженнях, які в основі мали застосування локальних форм естрогенів (відносний ризик 0,76), проте у цих жінок зберігались 1–2 епізоди НС протягом доби [14].
Іншою групою препаратів, застосування яких для лікування НС має теоретичне обґрунтування, є антихолінергічні засоби. 2012 було оприлюднено результати мета-аналізу, що порівнював ефективність цього заходу з іншими методами терапії НС. Зокрема, жінки, що отримували антихолінергічний препарат, більш часто реєстрували зменшення частоти та тяжкості НС, ніж жінки, які практикували тренування м’язів тазового дна. Водночас, комбінація тренувань м’язів тазового дна та ентихолінергічного препарату була більш ефективною, ніж кожен із методів окремо. Методологія досліджень не надала можливості порівняти ефективність призначення антихолінергічного препарату та різних методів електричної стимуляції нервів (інтравагінальної, черезшкірної тощо). Крім того, відсутня достатня кількість доказів того, що ефект від лікування зберігається після відміни препарату [15].
Введення ботулотоксину субуретрально або безпосередньо в тканину детрузора розглядали як перспективний метод лікування гіперактивного сечового міхура, що клінічно має подібні риси до НС [16]. При порівнянні з плацебо на підставі результатів 19 досліджень було продемонстровано значно більшу ефективність такого втручання. Позитивні результати було показано вже від низьких доз препарату — 100–150 ОД, проте більш високі дози (300 ОД) мають більш виражений та тривалий ефект. Більш ефективним було введення препарату субуретрально, ніж в детрузор. Переваги методу полягають у значній тривалості ефекту (кілька місяців), відсутності рефракторності при повторних введеннях та побічних ефектів.
Одним з популярних методів оперативного лікування НС є імплантація слінгів. Операція полягає у розміщенні спеціальної стрічки (слінг) навколо середньої третини уретри. Мета полягає у спробі відновити або посилити підтримку уретри під час значного підвищення внутрішньочеревного тиску (чхання, кашель тощо) та попередити мимовільне сечопускання. Ультразвуковими дослідженнями було підтверджено динамічну обструкцію слінгом уретри при підвищенні внутрішньочеревного тиску [3].
Доступом до встановлення слінгу може бути ретропубарний – через невеликий отвір над лобком двома голками смужку проводять у напрямку від піхви до черевної порожнини та у зворотному напрямку, а також трансобтураторний – через невеликий отвір в передній стінці піхви слінг підводять під середній відділ уретри, в горизонтальній площині між двома затульними отворами, не зав’язуючи, вільні краї смужки фіксують під шкірою. При застосуванні ретропубарного доступу існує ризик травми сечового міхура та уретри, тому його виконання слід супроводжувати цистоскопією, трансобтураторний доступ такої особливості не має.
Матеріали, з яких виконують слінги, можуть мати натуральне походження (з тканин людини або тварин) або синтетичні [17].
За даними FDA, протягом 2010 року в США було виконано 250 000 операцій імплантації синтетичних слінгів, операція мала тенденцію стати одним з найбільш популярних неінвазивних втручань. Побічні ефекти від операції включають біль, диспареунію, персистуюче нетримання сечі, ерозію слінга.
За даними великих досліджень в Шотландії [6] та Британії [7], кожна 10-та жінка після операції встановлення синтетичного імпланта зазнає ускладнень – кровотеча, інфікування, виражений больовий синдром, спонтанне або ятрогенне видалення слінга. 5% прооперованих пацієнток протягом найближчих 5 років мають необхідність повторного хірургічного втручання з приводу НС.
Gurol-UngaciI et al. (2018) опублікували результати ретроспективного національного популяційного дослідження у межах Об’єднаного королівства, що охопило 100 000 жінок, які зазнали операції встановлення слінга протягом останніх 9 років. Кінцевою точкою спостереження була необхідність видалення слінга, частота якої протягом 9 років після втручання склала 3,3%. Ризик видалення слінга був вищим при застосуванні ретропубарного доступу (3,6%), ніж трансобтураторного. Ризик необхідності повторної операції з приводу НС склав 1,3% протягом першого року від первинного втручання, 3,5% – протягом 5 років та 4,6% – протягом 9 років спостереження [8].
Ford A. et al. (2017) опублікували великий аналіз порівняння ефективності альтернативних способів імплантації слінгів – ретропубарного та трансобтураторного. На підставі аналізу 55 досліджень, що охопили понад 8600 жінок, було показано, що ці 2 доступи не мають істотних відмінностей за такими показниками як короткотривала (протягом 1 року після операції) відсутність симптомів, середньотривала (від 1 до 5 років) та довготривала (після 5 років від операції).
Загалом про відсутність НС через 5 років після імплантації слінга свідчили від 43 до 92% жінок з трансобтураторним введенням слінга та від 51 до 88% жінок з ретропубарним доступом імплантації.
Частота ускладнень, серед яких було враховано травму сечового міхура та судин, була низькою в обох варіантах, проте статистично вірогідно меншою при застосуванні трансобтураторного доступу.
Меншими у такому випадку були середня тривалість операції та післяопераційного перебування у стаціонарі, об’єм крововтрати. Однаково низькою – не більше 0,2% в обох варіантах – була частота специфічного для імплантації слінга ускладнення – його ерозії та необхідності видалення [9].
У середині другої декади ХХІ сторіччя бурхливу реакцію мало рішення FDA про заборону використання уретральних слінгів в США. Це питання дуже ретельно обговорено у науковій медичній пресі, у тому числі – і на сторінках нашого журналу (див. №3/2019). Попри це у Європі триває як використання слінгів у практиці, так і наукове дослідження ефективності та безпеки їх застосування.
Зокрема, на підставі 34 досліджень було сформовано мета-аналіз L. Saraswat et al. (2020), який порівнював різні типи встановлення слінгів з альтернативними способами лікування. Показано, що оперативне лікування виступає більш ефективним способом, ніж медикаментозне, слінги показані більш ефективними, ніж різні модифікації кольпосуспензії.
Метод не продемонстрував значних побічних ефектів та ускладнень у даному мета-аналізі. Порівняння слінгів з натуральних матеріалів з синтетичними не виявило значних відмінностей в їх ефективності, як в короткому періоді часі від операції (до 1 року), так і в середньому (1–5 років) та віддаленому (понад 5 років) [17].
Кольпосуспензія – найбільш популярний спосіб оперативного лікування. На сучасному етапі є можливість виконання її лапароскопічним або відкритим доступом (операції Burch та Marshall-Marchetti-Krantz). В усіх варіантах принцип втручання полягає у двобічному з’єднанні швами стінки піхви та контрлатеральної частини шийки сечового міхура. Лапароскопічний доступ вирізняє можливість екстраперитонеального виконання.
Freites J.et al. (2019) оприлюднили результат мета-аналізу, що порівнював ефективність альтернативних доступів кольпосуспензії. До аналізу було включено 13 досліджень та попри значну їх гетерогенність, пов’язану з відмінностями застосованих шовних матеріалів та тривалістю спостереження за пацієнтками, певні статистичні закономірності було виявлено. В першу чергу, вони стосувались незначного зростання ефективності щодо ознаки відсутності симптомів протягом 18 місяців від операції – попри незначне цифрове значення (відносний ризик 1,04), вона має високу силу доказів.
Щодо таких ознак, як відсутність симптомів протягом 1 та 5 років від операції, відмінностей між методами не виявлено. Застосування лапароскопічного доступу дозволяє більш швидко повернутись до звичної фізичної активності, супроводжується меншою крововтратою та меншою тривалістю сечового міхура, ніж при відкритій кольпосуспензії. Натомість лапаросопічний доступ асоційований з більшим ризиком травми сечового міхура та появи симптомів гіперактивного сечового міхура протягом перших 18 місяців. Щоправда, при подальшому спостереженні (до 5 років та більше) відмінності між методами за ознакою гіперактивного сечового міхура зникають.
Менш ефективними хірургічними методами лікування НС є передня кольпорафія та імплантація штучного сфінктера.
Таким чином, спектр можливостей надання допомоги жінками різного віку з проблемою НС є досить широким. При виборі потенційного методу лікування слід враховувати його інвазивність, побічні ефекти та потенційну користь для інших аспектів життя жінки.
Перелік літератури
1. Glazener CMA, Cooper K, Mashayekhi A. Anterior vaginal repair for urinary incontinence in women. Cochrane Database of Systematic Reviews 2017, Issue 7. Art. No.: CD001755. DOI: 10.1002/14651858.CD001755.pub2.
- Dumoulin C, Cacciari LP, Hay‐Smith EJC. Pelvic floor muscle training versus no treatment, or inactive control treatments, for urinary incontinence in women. Cochrane Database of Systematic Reviews 2018, Issue 10. Art. No.: CD005654. DOI: 10.1002/14651858.CD005654.pub4.
- Mid-urethral sling operations for stress urinary incontinence in women (Review) 11 Copyright © 2017 The Cochrane Collaboration.
- Coyne KS, Kvasz M, Ireland AM, Milsom I, Kopp ZS, Chapple CR. Urinary incontinence and its relationship to mental health and health-related quality of life in menand women in Sweden, the United Kingdom, and the United States. EurUrol. 2012;61(1):88-95. doi:10.1016/j.eururo.2011.07.049
- US Food&Drug Administration. Considerationsaboutsurgicalmesh for SUI. https://www.fda.gov/MedicalDevices/ProductsandMedicalProcedures/ImplantsandProsthetics/UroGynSurgicalMesh/ucm345219.htm. Accessed September 19, 2018.
- Morling JR, McAllister DA, Agur W, etal. Adverse events after first, single, mesh and non-mesh surgical procedures for stress urinary incontinence and pelvic organ pro lapsein Scotland, 1997-2016: a population-based cohort study. Lancet. 2017;389(10069):629-640. doi:10.1016/S0140-6736(16)32572-7
- Keltie K, Elneil S, Monga A, et al. Complications following vaginal mesh procedures for stress urinary incontinence: an 8 year study of 92,246 women. SciRep. 2017;7(1):12015. doi:10.1038/s41598-017-11821-w
- Gurol-Urganci I, Geary RS, Mamza JB, etal. Long-term Rate of Mesh Sling Removal Following Midurethral Mesh Sling Insertion Among Women With Stress Urinary Incontinence. JAMA. 2018;320(16):1659–1669. doi:10.1001/jama.2018.14997
- Ford AA, Rogerson L, Cody JD, Aluko P, Ogah JA. Mid-urethral sling operations for stress urinary incontinence in women. Cochrane Database of Systematic Reviews 2017, Issue 7. Art. No.: CD006375. DOI: 10.1002/14651858.CD006375.pub4.
- Freites J, Stewart F, Omar MI, Mashayekhi A, Agur WI. Laparoscopic colposuspension for urinary incontinence in women. Cochrane Database of Systematic Reviews 2019, Issue 12. Art. No.: CD002239. DOI: 10.1002/14651858.CD002239.pub4.
- Imamura M, Williams K, Wells M, McGrother C. Lifestyle interventions for the treatment of urinary incontinence in adults. Cochrane Database of Systematic Reviews 2015, Issue 12. Art. No.: CD003505. DOI: 10.1002/14651858.CD003505.pub5.
- Eustice S, Roe B, Paterson J. Prompted voiding for the management of urinary incontinence in adults. Cochrane Database of Systematic Reviews 2000, Issue 2. Art. No.: CD002113. DOI: 10.1002/14651858.CD002113.
- Wang Y, Zhishun L, Peng W, Zhao J, Liu B. Acupuncture for stress urinary incontinence in adults. Cochrane Database of Systematic Reviews 2013, Issue 7. Art. No.: CD009408. DOI: 10.1002/14651858.CD009408.pub2.
- CochraneDatabaseSystRev.2012 Oct 17;10:CD001405. doi: 10.1002/14651858.CD001405.pub3.
Oestrogen therapy for urinary incontinence in post-menopausal women.
Cody JD1, Jacobs ML, Richardson K, Moehrer B, Hextall A.
- CochraneDatabaseSystRev.2012 Dec 12;12:CD003193. doi: 10.1002/14651858.CD003193.pub4.
Anticholinergic drugs versus non-drug active therapies for non-neurogenic overactive bladder syndrome in adults.
Rai BP1, Cody JD, Alhasso A, Stewart L
16 Botulinum toxin injections for adults with over active bladder syndrome.
Duthie JB1, Vincent M, Herbison GP, Wilson DI, Wilson D.
- Saraswat L, Rehman H, Omar M, Cody JD, Aluko P, Glazener CMA. Traditional suburethral sling operations for urinary incontinence in women. Cochrane Database of Systematic Reviews 2020, Issue 1. Art. No.: CD001754. DOI: 10.1002/14651858.CD001754.pub5
Детальніше

ОГЛЯД публікацій за грудень 2019 – січень 2020
Шановні читачі! Пропонуємо вашій увазі нову рубрику, в якій ми знайомимо вас з новинками фахових періодичних видань. У цьому номері представлено огляд публікацій за грудень 2019–січень 2020 р.
Метформін для індукції овуляції (виключаючи гонадотропіни) у жінок із СПКЯ
Cochrane Library
Метою дослідження було оцінити ефективність та безпеку метформіну в поєднанні або порівняно з кломіфеном цитратом (КЦ), летрозолом та лапароскопічним дриллінгом яєчників (ЛДЯ) для поліпшення репродуктивних результатів та зменшення супутніх шлунково-кишкових побічних ефектів у жінок із СПКЯ, яким проводиться індукція овуляції. Порівняно з плацебо, метформін може збільшувати рівень живонароджень.
Автори не впевнені, чи покращує комбінація метформіну та КЦ показники живонароджень у порівнянні з тільки КЦ, однак побічні ефекти з боку шлунково-кишкового тракту, ймовірно, збільшуються при комбінованій терапії. При порівнянні метформіну та КЦ, дані стосовно живонароджень були непереконливі, а результати обмежені, через слабку доказову базу.
doi.org/10.1002/14651858.CD013505
Систематичний огляд Cochrane
Лапароскопічна кольпосуспензія при нетриманні сечі у жінок
Cochrane Library
Метою дослідження було оцінити лапароскопічну кольпосуспензію при нетриманні сечі у жінок та узагальнити основні результати економічної оцінки втручання. Дані свідчать про те, що з точки зору суб’єктивного виліковування нетримання сечі протягом 18 місяців, ймовірно, існує невелика різниця між лапароскопічною кольпосуспензією і відкритою кольпосуспензією та між лапароскопічною кольпосуспензією і встановленням мідуретрального слінгу. Однак, велика частина доказів є низької якості, це означає, що залишається значна ступінь невизначеності щодо лапароскопічної кольпоспензії.
https://doi.org/10.1002/14651858.CD002239.pub4
Проспективне обсерваційне дослідження
Вплив відкладеного перетискання пуповини на показники газів пуповинної крові після вагінальних пологів і кесаревого розтину у доношених новонароджених без внутрішньоутробного дистресу
BJOG: An international Journal of Obstetrics & Gynaecology
Метою дослідження було оцінити зміни показників газів пуповинної крові після відкладеного на 3 хвилини перетискання пуповини після вагінальних пологів і кесаревого розтину (КР) у доношених новонароджених без внутрішньоутробного дистресу. Було проведено порівняння парних артеріально-венозних зразків пуповинної крові, взятих при народженні з неперетисненої пуповини і після відкладеного на 3 хвилини перетискання пуповини, після 97 вагінальних пологів та 124 КР. Кислотно-основний стан після відкладеного на 3 хвилини перетискання пуповини зміщувався у бік змішаного ацидозу після КР та переважно в бік метаболічного ацидозу після вагінальних пологів. При КР спостерігалось більш виражене збільшення лактату порівняно з вагінальними пологами.
doi.org/10.1111/1471-0528.16026
Короткий науковий огляд
Результати вагітності у жінок з розривом матки або неспроможністю рубця на матці в анамнезі
Obstetrics & Gynecology
Протягом періоду дослідження 37 жінок (59 вагітностей) мали анамнез розриву матки, і 50 жінок (75 вагітностей) – неспроможності рубця на матці. Ці 87 жінок (134 вагітності) склали серію випадків. Результати, про які повідомляється в цьому огляді – це важка захворюваність (розрив матки, гістеректомія, переливання крові, цистотомія, пошкодження кишечника, штучна вентиляція легенів, надходження до відділення інтенсивної терапії, тромбоз, повторна операція, материнська смерть і перинатальна смерть). Автори також повідомляють про менш серйозну захворюваність, таку як передлежання плаценти, placenta accretа та виявлення неспроможності рубця під час розродження.
У якості висновку: жінки з анамнезом розриву матки або неспроможності рубця на матці, мабуть, мають низький ризик несприятливих наслідків при наступних вагітностях, якщо вони ведуться стандартизованим способом, включаючи кесарів розтин до початку пологів або на початку передчасних пологів. Автори закликають інші центри повідомляти про результаті вагітностей у таких жінок.
doi.org/10.1097/AOG.0000000000003622
Керівництво RCOG
Колапс під час вагітності та у післяпологовому періоді
BJOG: An international Journal of Obstetrics & Gynaecology
Метою цього керівництва було обговорити ідентифікацію жінок з ризиком розвитку колапсу, описати фізіологічні та анатомічні зміни, які впливають на реанімаційні заходи під час вагітності, оптимальне початкове лікування колапсу, виконання перимортального кесаревого розтину, подальше лікування колапсу, наслідки для матері та дитини та систему забезпечення стандартів клінічної практики.
obgyn.onlinelibrary.wiley.com/doi/pdf/10.1111/1471-0528.15995
Практичний бюлетень ACOG
Вагініт у невагітних пацієнток
Obstetrics & Gynecology
Вагініт – це запалення або інфекція піхви, яка пов’язана із спектром симптомів, включаючи вульвовагінальний свербіж, печіння, подразнення, диспареунію, «рибний» запах та аномальні виділення з піхви. Вагінальні симптоми є однією з найчастіших причин відвідування пацієнтками акушера-гінеколога і можуть мати важливі наслідки, такі як дискомфорт та біль, пропуски школи та роботи, порушення сексуальної функції та самосприйняття. Метою даного документа є надання оновленого науково-обґрунтованого керівництва з діагностики та лікування поширених причин вагініту у невагітних пацієнток. Інформація про лікування вагініту у пацієнток з вірусом імунодефіциту людини (ВІЛ) представлена в інших джерелах.
doi.org/10.1097/AOG.0000000000003604
Думка комітету ACOG
Спадкові ракові синдроми і оцінка ризику
Obstetrics & Gynecology
Спадкові ракові синдроми – це генетична схильність до певних типів раку, які часто маніфестують в ранньому віці і які викликані спадковими патогенними варіантами одного або декількох генів. Найбільш поширені спадкові ракові синдроми у жінок включають синдром спадкового раку молочної залози і яєчників. Оцінка спадкового ризику раку є ключовим фактором для виявлення пацієнтів та сімей, у яких може бути підвищений ризик розвитку певного типу раку. Оцінка повинна регулярно проводитися акушером-гінекологом.
Ця редакція думки комітету включає оновлення, пов’язані зі спадковим раком молочної залози та яєчників, каскадним тестуванням та направленням до фахівців з генетики.
doi.org/10.1097/AOG.0000000000003563
Думка комітету ACOG
Насильницькі дії сексуального характеру
Obstetrics & Gynecology
Акушерсько-гінекологічне обстеження включає взаємодію з пацієнткою під час емоціональної вразливості, чутливі фізичні огляди та необхідне з медичної точи зору розкриття приватної інформації про симптоми та переживання жінки. Відносини між пацієнткою і лікарем порушуються, коли виникає плутанина щодо професійних ролей і поведінки або допускається сексуальна експлуатація і заподіяння шкоди. Насильницькі дії сексуального характеру з боку лікарів – це зловживання професійною владою і порушення довіри пацієнтки. Хоча в клінічній практиці насильницькі дії сексуального характеру зустрічаються не часто, навіть один епізод є неприпустимим. Рутинна присутність компаньйонів під час оглядів, на додаток до інших практик, викладених в цьому документі, допоможе переконати пацієнтів і громадськість в тому, що акушери-гінекологи докладають максимум зусиль для створення безпечного середовища для всіх пацієнток.
doi.org/10.1097/AOG.0000000000003608
Практичний бюлетень ACOG
Макросомія
Obstetrics & Gynecology
Підозра на макросомію часто зустрічається в акушерській практиці. Зі збільшенням ваги при народженні зростає ймовірність аномалій пологової діяльності, дистоції плечиків, та пологових травм. Метою даного документа є кількісна оцінка цих ризиків, огляд точності і обмежень методів оцінки передбачуваної ваги плода і пропозиції клінічного ведення при вагітності з підозрою на макросомію. Цей документ був переглянутий з метою включення в нього нової літератури і оновленої інформації щодо профілактики макросоміі.
doi.org/10.1097/AOG.0000000000003606
Міжнародне рандомізоване подвійне сліпе плацебо-контрольоване дослідження
Анастразол для профілактики раку молочної залози: тривалі результати.
The Lancet
Два великих клінічних дослідження продемонстрували зниження частоти розвитку раку молочної залози у жінок з групи високого ризику в перші 5 років спостереження після застосування інгібіторів ароматази. У цьому аналізі автори повідомляють про віддалені результати подальшого спостереження після дослідження IBIS-II, в якому порівнювали анастразол з плацебо з метою визначення ефективності анастрозолу для запобігання раку молочної залози (як інвазійного, так і потокової карциноми in situ) після закінчення лікування. Жінки в постменопаузі з підвищеним ризиком розвитку раку молочної залози були випадковим чином розподілені (1:1) в групу анастрозолу (1 мг в день, перорально), або плацебо щодня протягом 5 років. Після завершення лікування, щорічно проводився збір даних про захворюваність на рак молочної залози, смертність, інші види раку і небажані явища (серцево-судинні події і переломи). Цей аналіз виявив значуще триваюче зниження рівня раку молочної залози після лікування анастрозолом, без будь-яких ознак нових пізніх побічних ефектів. Потрібні подальші спостереження для оцінки впливу на смертність від раку молочної залози.
doi.org/10.1016/S0140-6736(19)32955-1
Керівництво NICE
Менопауза: діагностика та менеджмент
NICE guideline
Керівництво охоплює жінок як в перименопаузі, так і в постменопаузі, а також особливі потреби жінок з передчасним виснаженням яєчників і жінок з гормоночутливим раком (наприклад, раком молочної залози). Дане керівництво зосереджене на клінічному лікуванні симптомів, пов’язаних з менопаузою, розглядає як фармацевтичні, так і немедикаментозні методи лікування, включає економічний аналіз і розглядає переваги і несприятливі ефекти замісної гормональної терапії.
nice.org.uk/guidance/ng23
Директива Американської Академії Педіатрії
Екстрена контрацепція
Pediatrcis
Незважаючи на значне зниження за останні 20 років, у Сполучених Штатах, як і раніше, відзначається значно вищий рівень народжуваності серед підлітків, ніж в інших країнах з високим рівнем доходу. Використання екстреної контрацепції (ЕК) протягом 120 годин після незахищеного або недостатньо захищеного статевого акту може знизити ризик вагітності. Методи екстреної контрацепції включають пероральні препарати, марковані та призначені для використання в якості екстреної контрацепції Управлінням із санітарного нагляду за якістю харчових продуктів і медикаментів США (уліпрістал та левоноргестрел), використання “off-label” комбінованих оральних контрацептивів і введення внутрішньоматкової спіралі. Мета цієї директиви полягає в тому, щоб:
- Навчити педіатрів та інших лікарів доступним методам екстреної контрацепції.
- Надати поточні дані про безпеку, ефективність та використанні екстреної контрацепції у підлітків;
- Заохотити регулярне консультування і призначення екстреної контрацепції у якості однієї зі стратегій охорони здоров’я щодо зменшення рівня вагітності у підлітків.
doi.org/10.1542/peds.2019-3149
Керівництво Квінсленду
Спостереження за станом плода під час пологів
Queensland Clinical Guidelines
Основна мета спостереження за станом плода під час пологів – запобігання несприятливим перинатальним наслідкам, що виникають у результаті метаболічного ацидозу у плода, пов’язаного з пологами. Оскільки мозок плода регулює частоту серцевих скорочень плода за допомогою взаємодії симпатичної і парасимпатичної нервової системи, моніторинг частоти серцевих скорочень плода можна використовувати як показник оксигенації мозку плода. За відсутності факторів ризику, постійний моніторинг частоти серцевих скорочень плода не має доведених переваг і може збільшувати частоту втручань при нормальних спонтанних пологих, які тривають менше 12 годин в активній фазі. Це керівництво узгоджується з клінічними керівництвом по спостереженню за станом плода, опублікованим Королівським коледжем акушерів-гінекологів Австралії і Нової Зеландії (RANZCOG), і засноване на ньому.
health.qld.gov.au/__data/assets/pdf_file/0012/140043/g-ifs.pdf
Перехресне багатоцентрове дослідження
Жіноча сексуальність та вагінальне здоров’я в менопаузі
Menopause
Первинна мета цього дослідження полягала в тому, щоб оцінити зміни в жіночій сексуальності під час менопаузи, вторинна мета – перевірити зв’язок змін жіночої сексуальності з вагінальної атрофією та її симптомами. Було проведене перехресне багатоцентрове дослідження за участю 518 жінок у віці від 40 до 55 років, які зверталися за амбулаторною гінекологічною допомогою у 30 центрах по всій Італії. Сексуальна дисфункція, яка визначалась за шкалою індексу жіночої сексуальної функції (ІЖСВ) <26,55, відзначалася у 70,6% учасниць, збільшившись з 55% у віці від 40 до 45 років до 82,8% у віці від 52 до 55 років. Вагінальна сухість була єдиною змінною, що незалежно корелювала з кожним доменом ІЖСФ, включаючи бажання, збудження, лубрикацію (зволоження), оргазм, задоволеність статевим життям і диспареунію.
doi.org/10.1097/GME.0000000000001427
Систематичний огляд та мета-аналіз рандомізовних контрольованих досліджень
Використання мізопростолу перед встановленням внутрішньоматкової системи
The European Journal of Contraception & Reproductive Health Care
Мізопростол використовується перед введенням внутрішньоматкової системи для підготовки шийки матки. Однак, оскільки наявні дані є суперечливими, метою дослідження було оцінити частоту невдалого введення внутрішньоматкової системи, больові відчуття, частоту використання розширювачів шийки матки та побічні наслідки після використання мізопростолу. У результаті дослідження було виявлено, що частота невдалого введення внутрішньоматкової системи зменшується у жінок з анамнезом кесаревого розтину та у жінок з анамнезом невдалого введення після використання мізопростолу. Але, хоч премедикація мізопростолом зменшила кількість невдалих спроб введення, вона значно посилила небажані ефекти і мала гетерогенний характер ефективності; таким чином, рутинне використання мізопростолу не підтверджується доказами.
doi.org/10.1080/13625187.2019.1706079
Популяційне поперечне дослідження
Поширеність потенційно непотрібних бімануальних вагінальних оглядів та мазків за Папаніколау серед дівчат-підлітків та молодих жінок у віці 15–20 років у США
JAMA Internal Medicine
Метою було оцінити поширеність потенційно непотрібних бімануальних вагінальних оглядів та мазків за Папаніколау (Пап-тест) серед дівчат-підлітків та молодих жінок у віці до 21 року (далі – молоді жінки) у США та визначити фактори, пов’язані з отриманням цих обстежень. За результатами цього популяційного поперечного дослідження з використанням даних 2011–2017 років, 2,6 мільйонам молодих жінок у Сполучених Штатах було проведено бімануальний вагінальний огляд, 54,4% з них були потенційно непотрібними. 2,2 млн. молодих жінок було проведено Пап-тест і 71,9% з них були потенційно непотрібними. Цей аналіз показав, що більше половини вагінальних оглядів і майже три чверті Пап-тестів, проведених серед молодих жінок в період з 2011 по 2017 роки, були потенційно непотрібними, піддаючи жінок ризику можливої шкоди.
doi.org/10.1001/jamainternmed.2019.5727
Огляд чотирьох національних керівництв
Оперативні вагінальні пологи
Journal of Perinatal Medicine
Метою даного дослідження було розглянути і порівняти рекомендації з опублікованих керівництв з ведення оперативних вагінальних пологів (ОВП). Був проведених огляд керівництв Королівського коледжу акушерів та гінекологів (RCOG), Королівського Австралійського і Новозеландського коледжу акушерів і гінекологів (RANZCOG), Товариства акушерів і гінекологів Канади (SOGC) і Американського коледжу акушерів і гінекологів (ACOG) з інструментальних вагінальних пологів. У всіх керівництвах вказується, що використання будь-якого інструменту має ґрунтуватися на клінічних обставинах і досвіді лікаря. Показання, протипоказання, причини і класифікація ОВП в цілому дуже схожі у розглянутих керівництвах. Не існує єдиної думки про фактичну техніку, яка повинна використовуватися, включаючи тип щипців або вакууму та силу і тривалість тракцій.
doi.org/10.1515/jpm-2019-0433
Думка комітету ASRM
Збереження фертильності у пацієнток, що проходять гонадотоксичну терапію або гонадектомію
Fertility and Sterility
Пацієнтам, які готуються до проведення гонадотоксичної медикаментозної терапії, променевої терапії або гонадектомії, повинна бути надана консультація щодо доступних варіантів збереження фертильності. Збереження фертильності найкраще може бути забезпечено комплексними програмами, які розроблені для вирішення унікальних проблем, що стоять перед цими пацієнтами. Цей документ замінює документ з аналогічною назвою, який був опублікований в 2013 році.
doi.org/10.1016/j.fertnstert.2019.09.013
Ретроспективне когортне дослідження
Зв’язок між лікуванням неплідності та ризиком розвитку раку у дітей
Jama
Метою дослідження було вивчити зв’язок між різними видами лікування неплідності і ризиком розвитку раку у дітей. Після 12,2 мільйонів людино-років спостереження (в середньому 11,3 років) рівень захворюваності на рак у дітей склав 17,5 на 100 000 дітей, народжених від фертильних жінок (n=910 291), і 44,4 на 100 000 дітей, що народилися після трансферу кріоконсервованих-розморожених ембріонів (n=3 356).
У порівнянні з дітьми, народженими від фертильних жінок, трансфер кріоконсервованих-розморожених ембріонів був пов’язаний з підвищеним ризиком розвитку раку у дітей (14 випадків раку; відношення моментного ризику [hazard ratio, HR] 2,43 [ДІ 95%, 1,44–4,11]; різниця в рівні захворюваності 26,9 [95% ДІ 2,8–51,0] на 100 000), переважно через підвищений ризик лейкемії (5 випадків раку; частота захворюваності 14,4 на 100 000; HR 2,87 [ДІ 95%, 1,19–6 , 93]; різниця в рівні захворюваності, 10,1 [95% ДІ -4,0–24,2] на 100 000) та пухлин симпатичної нервової системи (<5 випадків раку; HR 7,82 [95% ДІ 2,47–24,70]).
Серед дітей, що народилися в Данії після трансферу кріоконсервованих-відталих ембріонів було виявлено невелике, але статистично значуще підвищення ризику розвитку раку в дитячому віці; зв’язку з іншими типами лікування неплідності виявлено не було.
doi.org/10.1001/jama.2019.18037
Проспективне когортне дослідження
Діагностичне значення тесту «Chorioquick» для виявлення хоріоамніоніту у жінок з передчасним розривом плодових оболонок
International Journal of Gynecology & Obstetrics
Метою було визначити точність напівкількісного експрес-тесту визначення інтерлейкіну-6 (IL-6) у вагінальному секреті («Chorioquick») для виявлення хоріоамніоніту у жінок з передчасним розривом плодових оболонок (ПРПО). До проспективного когортного дослідження, яке проводилося в 5 госпіталях третинного рівня в Нігерії залучалися жінки з підтвердженим ПРПО з 1 серпня 2017 р. по 31 жовтня 2018 р. Зразки цервіковагінального секрету були протестовані за допомогою тесту Chorioquick. Хоріоамніоніт був гістологічно підтверджений після пологів. Основними критеріями були чутливість, специфічність і точність. Загалом чутливість тесту склала 97.5% (95% довірчий інтервал [ДІ] 85.3–99.9), специфічність 87.9% (70.9–96.0), і точність 93.2% (79.5–99.1). Аналіз підгрупи жінок в гестаційному терміні <37 тижнів вагітності показав чутливість 100,0% (95% ДІ 83,4–100,0), специфічність 91,3% (70,5–98,5) і точність 95,8% (82,5–99,5).
doi.org/10.1002/ijgo.13095
Детальніше

Підготовка шийки матки до пологів
In dubio abstine/
Якщо сумніваєшся – утримайся.
Латинський вираз
Найкраща битва – та, що не відбулася.
Сунь Цзи
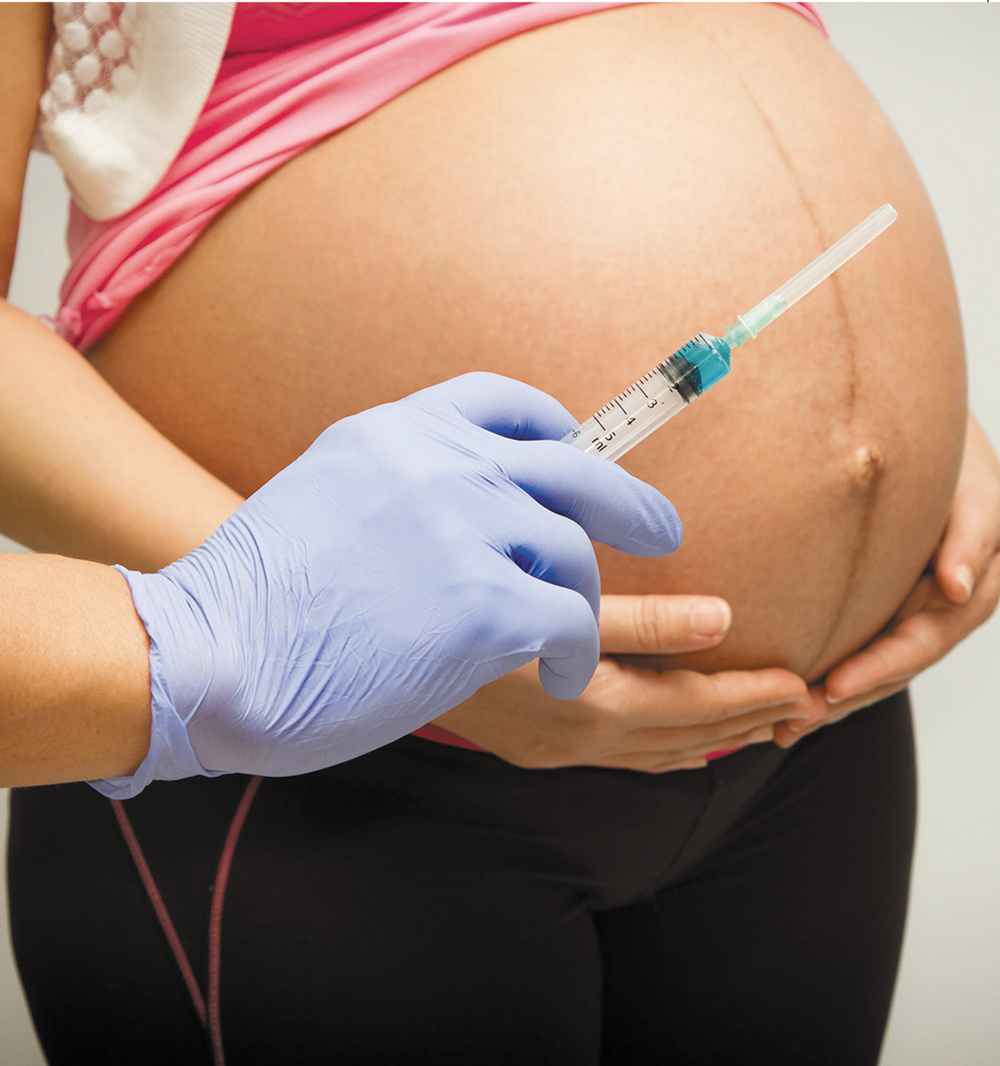
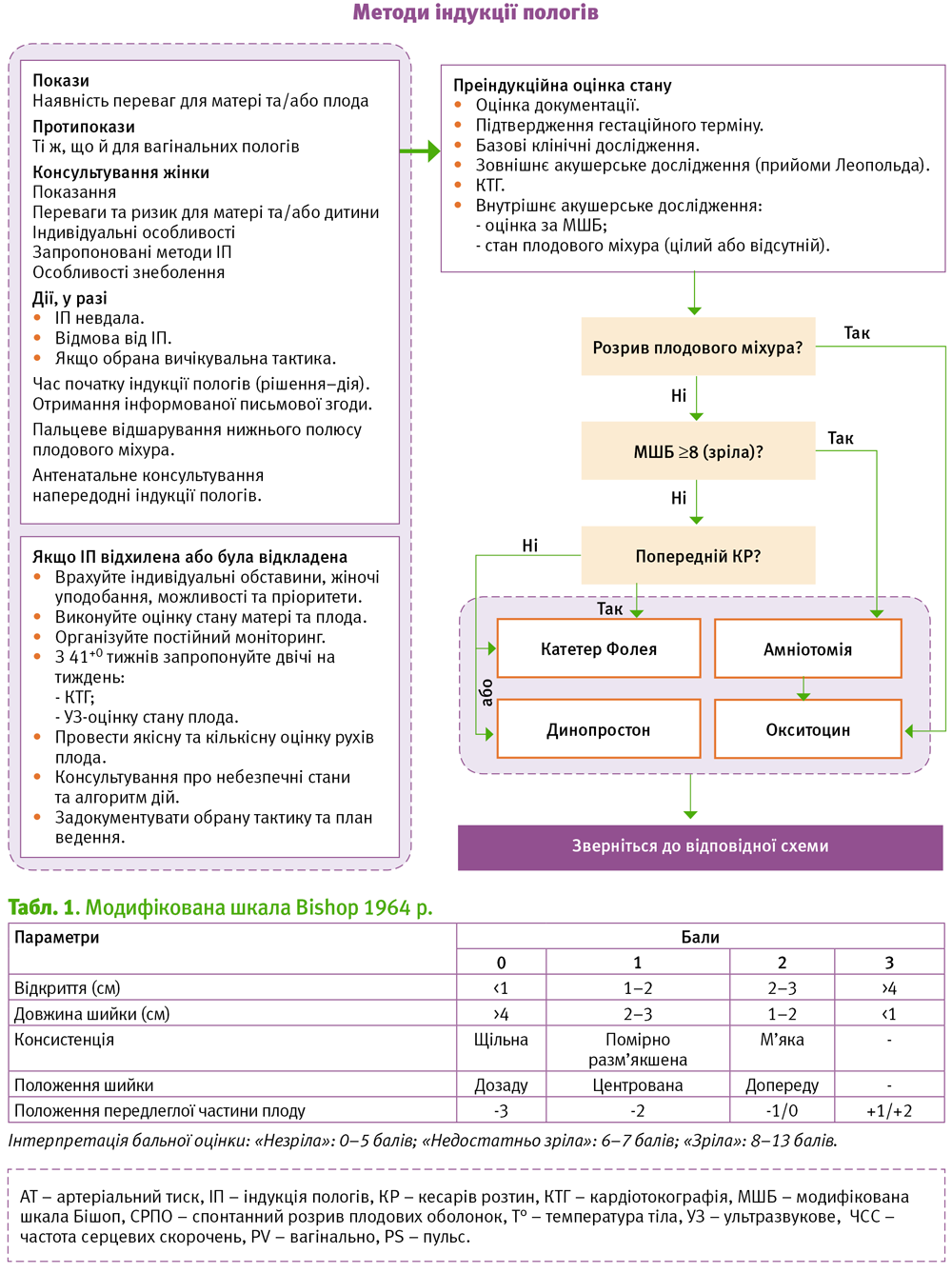
Щорічно у сучасному акушерстві спостерігається тенденція до збільшення частоти індукції пологів. У розвинених країнах більш ніж 25% термінових пологів є індукованими. У країнах, що розвиваються, частка таких пологів, як правило, нижча, проте у деяких випадках може бути так само висока, як і у розвинених регіонах [MacKenzie I. Z., 2006; ВООЗ, 2014].
Безпека і ефективність індукції пологів залежить від правильного вибору показань і протипоказань, часу проведення, послідовності застосування різних методів, які доречні у кожній конкретній клінічній ситуації. Дане положення обумовлює необхідність розробки чітких алгоритмів, що використовуються для «дозрівання» шийки матки і пологозбудження.
Індукцію пологів рекомендовано застосовувати у тих випадках, у яких, на думку лікаря, ризики, пов’язані з очікуванням спонтанного початку пологів, перевищують ризики, що пов’язані зі скороченням тривалості вагітності завдяки індукції. Ці обставини, як правило, включають термін вагітності від 41 повного тижня і більше, передчасний розрив плодових оболонок, гіпертензивні порушення, обтяжений стан матері, антенатальну загибель плода, затримку внутрішньоутробного розвитку, гемолітичну хворобу плода, хоріоамніоніт та інші ускладнення. Незважаючи на те, що наразі не рекомендують такий підхід, індукція пологів все частіше використовується на прохання вагітних жінок для скорочення тривалості вагітності або для вибору часу народження дитини, зручного для матері і/або медичних працівників (ВООЗ, 2014).
Протипоказання до індукції пологів в цілому ідентичні таким при спонтанних пологах через природні пологові шляхи. Вони можуть носити абсолютний характер (передлежання плаценти, поперечне положення плода та ін.) або бути відносними, що проявляються в особливих ситуаціях. Не показане проведення пологозбудження при розташуванні голівки плода над входом у таз, але у цій ситуації можливе проведення преіндукції пологів, у процесі якої можна розраховувати на її фіксацію до площини входу в малий таз. При ознаках хоріоамніоніту не рекомендоване застосування механічніх методів преіндукції пологів, але можливе використання інших (ВООЗ, 2014).
Необхідні умови для успішної індукції пологів
- Оцінка показань і протипоказань для індукції пологів.
- Максимально точний підрахунок гестаційного терміну (УЗД до 12–14 тижнів вагітності – найбільш точний метод, який знижує потребу в індукції пологів з приводу «уявної переношеності»).
- Оцінка стану матері та плода.
- «Зріла» шийка матки (оцінка за шкалою Бішоп ³8 балів).
- Наявність навченого персоналу алгоритмів індукції пологів.
- Наявність можливості проведення оперативного розродження, в тому числі вагінального (вакуум-екстракція, накладення щипців і т. д.).
Дозрівання шийки матки та індукція пологів
Спонтанному початку пологів передують структурні зміни або «дозрівання» шийки матки, що може бути спричинено взаємодією оксиду азоту з численними цитокінами та вільними радикалами. Далі йдуть взаємопов’язані та узгоджені зміни рівнів естрогену, прогестерону, простагландинів, кортикотропного рилізинг гормону, а також кортизолу з їх рецепторами, що викликає початок пологів. Однак немає чіткого розмежування між етапами дозрівання шийки матки і початком пологів, оскільки вони зливаються в одному безперервному процесі. Більшість засобів, що застосовуються для дозрівання шийки матки, призводять до індукції пологів, якщо використовуються у більш високій концентрації, частіше або триваліше. Тому було запропоновано, що дозрівання шийки матки та індукція пологів не повинні розглядатися як окремі процеси (Elmahdy M. et al, 2016).
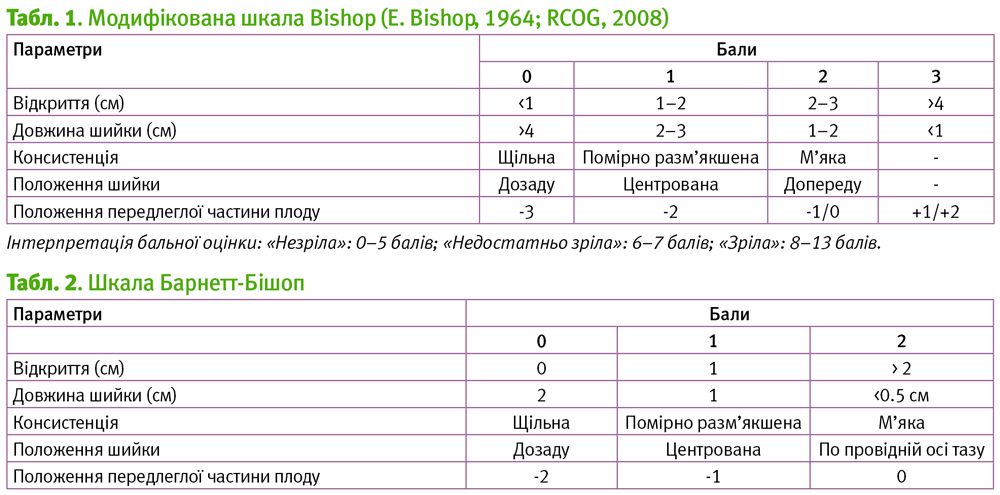
Структурна зрілість шийки матки – найбільш важливий предиктор успішності індукції пологів. З метою стандартизації підходів оцінки «зрілості» пологових шляхів доктором Едвардом Бішопом була розроблена бальна шкала 1964 р., представлена у табл. 1.
Американська школа визначає відношення передлеглої частини плоду до площин малого тазу під час її просування пологовими шляхами, використовуючи поняття «рівень малого тазу», і виділяє такі рівні:
- площина, що проходить через сідничні ості, – рівень 0 (голівка плоду великим сегментом у вході в малий таз);
- розташування передлеглої частини вище рівня 0 позначають відповідно як рівні -1, -2, -3;
- розташування передлеглої частини нижче рівня 0 позначають відповідно як рівні +1, +2, +3.
При цьому рівень +3 відповідає розташуванню головки на тазовому дні.
Більшість досліджень показали, що жінки, які мають відкриття шийки матки 2 см та її згладження на 80%, м’яку консистенцію, центроване положення щодо осі тазу, розташування голівки щодо інтерспінальної лінії +1, отримають найбільш успішний результат індукції пологів.
Разом з тим, у більшості країн світу використовується не оригінальна шкала Бішоп, а її модифікація, так звана шкала Барнетт–Бішоп, у якій кожен показник оцінюється не за трибальною, а за двобальною системою. При використанні цієї шкали шийка матки вважається зрілою при оцінці ³6 балів.
Як альтернативу шкалі Бішоп, Hatfield з співавт. (2007) провели мета-аналіз 20 досліджень, в яких предиктором успішності індукції пологів було визначення довжини шийки матки за допомогою трансвагінального УЗД. В результаті було встановлено, що довжина шийки матки, виміряна трансвагінально, не має прогностичних переваг у порівнянні зі шкалою Бішоп (табл. 2).
Як було сказано раніше, принципово важливим фактором успішності індукції пологів є «зрілість» шийки матки, у зв’язку з чим було запропоновано ряд методик підготовки шийки матки.
Засоби з доведеною ефективністю, але відсутніми даними безпечності або наявними даними про небезпечний вплив
Застосування донаторів оксиду азоту
Дослідження свідчать про те, що оксид азоту бере участь у процесі дозрівання шийки матки на пізніх стадіях вагітності (Thomson et al. 1997, Chanrachakul et al. 2002). Донатори оксиду азоту можуть впливати на дозрівання шийки матки, стимулюючи синтез простагландинів і тромбоксану з шийки матки (Ledingham et al. 1999). Було вивчено місцеве застосування глицерилтринітрату, ізосорбіду мононітрату та ізосорбіду динітрату протягом І і ІІІ триместрів вагітності з метою визначення впливу на структурні зміни шийки матки (Chwalisz et al., 1997). Ці засоби показали свою ефективність у дозріванні шийки матки протягом 24 годин та зменшенні випадків гіперстимуляції, але пов’язані з виникненням небажаних ефектів, а саме головних болей, нудоти та блювота чи запаморочення.
У мета-аналізі 23 досліджень, які включали 4777 жінок, проводилось порівняння донаторів оксиду азоту з плацебо, вагінальними та інтрацервікальними простагландинами Е2, вагінальним застосуванням мізопростолу та катетером Фолея. Стандартна доза ізосорбіду моногідрату становила 40 мг у заднє склепіння піхви. Застосування цієї групи препаратів мало очевидні потенційні переваги у досягненні зрілості шийки матки, але в даний час існує обмежене число доказів покращення результатів для матері або плоду та відсутні дані безпеки. Необхідні подальші дослідження ефективності та безпеки, перед тим, як рекомендувати застосування методики для широкого використання (Cochrane Database of Systematic Reviews, 2016).
Застосування антигестагену «міфепристон»
У 1980 р в лабораторії фірми “Russel Uclaf” був розроблений і ліцензований міфепристон – антиглюкокортикоїд для терапії депресивних станів у хворих з синдромом Кушинга, у якого було виявлено антигестагенний та антиандрогенний ефект. З початку 1990-х рр. він став широко застосовуватися для проведення медикаментозного аборту в I триместрі, переривання вагітності в II у зв’язку з антенатальною загибеллю або вадами розвитку плода, а також при консервативному лікуванні ектопічної вагітності.
Міфепристон володіє високою спорідненістю до рецепторів прогестерону, що обумовлює його ефективність щодо підготовки шийки матки до пологів, в той же час його антиандрогенний та антиглюкокортикоїдний вплив зумовлює непередбачуваний пул негативних наслідків для матері та дитини.
Останній систематичний огляд бази даних Cochrane, присвячений підготовці шийки матки до пологів із застосуванням міфепристону, включає 10 рандомізованих досліджень (1108 жінок).
Результати аналізу показали, що міфепристон значно частіше, ніж плацебо, викликає дозрівання шийки матки, або розвиток пологової діяльності протягом 48 годин (RR – 2,41; 95% CI – 1,70–3,42) і цей ефект зберігається протягом 96 годин. При цьому, при застосуванні міфепристону доведено збільшення материнських ускладнень на 60% (RR – 1,51; 95% CI – 1,06–2,15), частоти інструментальних пологів на 43% (RR – 1,43; 95% CI – 1,04–1,96) та більш високий ризик зміни серцевого ритму плоду на кардіотокограмі на 60% (RR – 1,60; 95% CI – 1,12–2,29).
Наявні світові рекомендації з використання препарату для підготовки шийки матки до пологів досить категорично наполягають на можливості використання препарату тільки у жінки з завмерлою вагітністю, в тому числі з антенатальною загибеллю плода, а використання його допускається тільки після отримання інформованої згоди пацієнтки.
Жодна прогресивна країна світу не має даного препарату в клінічних настановах серед альтернатив щодо індукції пологів на живих плодах!
Протипоказання: живий плід, гіперчутливість до препарату, хронічна надниркова недостатність або тривалий прийом кортикостероїдів, геморагічні порушення або прийом антикоагулянтів.
Спосіб застосування при антенатальній загибелі плоду: загальна доза 200 мг, пероральне застосування такої дози препарату припустиме лише в умовах пологового блоку, під цілодобовим спостереженням медичного персоналу. Якщо зміни в шийці матки неадекватні після першої дози (не досягнули ступеня зрілості 8 балів і більше), прийом препарату може бути повторений лише через 24 години.
Заходи індукції пологів з доведеною ефективністю та безпечністю
Заходи з підготовки шийки матки і індукції пологів повинні здійснюватися в установі не нижче 2 рівня надання акушерсько-гінекологічної допомоги. Залежно від застосованого методу, для підготовки шийки матки протягом перших годин пацієнтка повинна знаходиться під постійним медичним наглядом; при індукції пологів – безперервно.
Головні принципи індукції пологів:
- Наявність чітких медичних показань для індукції пологів (ризики пролонгації вагітності повинні бути вищі ризику індукції).
- Наявність стратегії проведення підготовки шийки матки та індукції пологів (у залежності від стану шийки матки, наявного запасу часу).
- Дотримання етапності підготовки шийки матки і пологозбудження.
- Методологічний підхід, з дотриманням чіткого алгоритму застосування кожного з методів дозрівання шийки матки та індукції маткових скорочень.
Методи, які використовуються для підготовки пологових шляхів, включають в себе різні форми механічної цервікальної дилятації та фармакологічної підготовки.
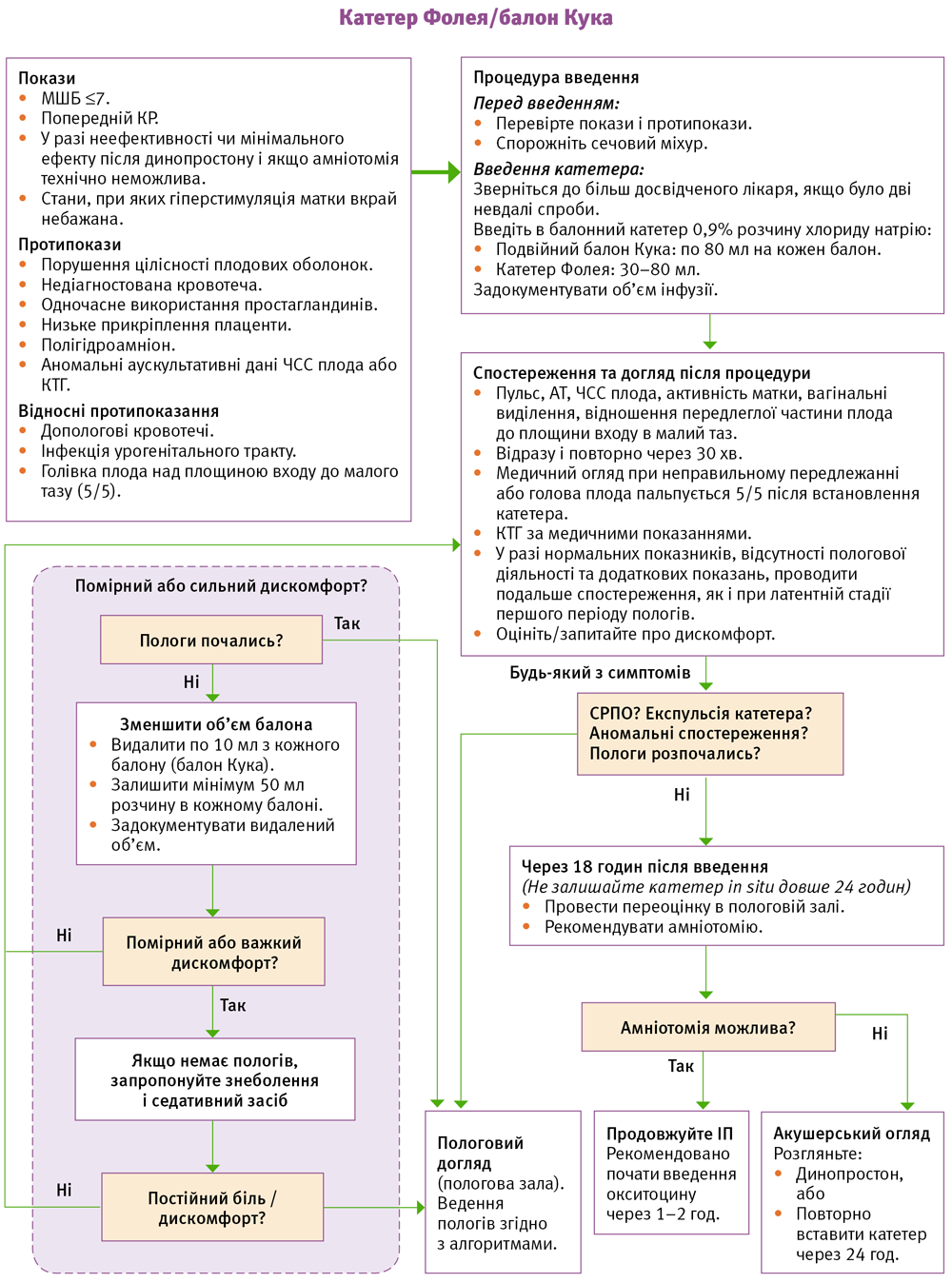
Механічні методи преіндукції пологів.
Механічні методи підготовки до пологів включають: введення в шийку матки балона (катетера Фолея, двобалонного катетера Кука), ламінарій або гігроскопічних дилятаторів. З цих методів ВООЗ рекомендує застосовувати балон (ВООЗ, 2014 р.), оскільки ефективність і безпечність застосування катетера Фолея підтвердили численні дослідження. Для нашої країни вагомою перевагою використання даного методу є його низька вартість.
Рандомізовані дослідження підготовки шийки матки за допомогою катетера Фолея, проведені Chung і співав. (2003), показали належну ефективність застосування балонної преіндукції у порівнянні з 25 мкг мізопростолу, або при поєднанні балонного дозрівання з 25 мкг мізопростолу. А дослідження, перевірені Culver і співавт. у 2004 р., у яких оцінювали інтервал часу, затрачений на преіндукцію-індукцію-пологи із застосуванням катетера Фолея з наступною індукцією окситоцином, у порівнянні з преіндукцією 25 мкг мізопростолу з наступним введенням окситоцину, показали, що інтервал часу преіндукція-індукція-пологи був значно коротший в групі жінок, де була застосована схема катетер + окситоцин і склало 16 годин у порівнянні з 22 годинами у другій групі.
Трансцервікальне введення катетера Фолея створює низхідне напруження на шийку матки, прискорюючи її дозрівання, шляхом дилатації, вкорочення та розм’якшення, створюючи сприятливий фон для подальшого пологозбудження. Для проведення методики використовують катетери Фолея об’ємом 30 мл (14G) або 60 мл (18-22-24 G), при цьому необхідно надати перевагу останньому (мал. 1).
Методика інтрацервікального введення катетера Фолея складається з наступних етапів:
- Оголення шийки матки в дзеркалах і обробка пологових шляхів водним розчином антисептика.
- Введення катетера Фолея за допомогою вікончатого затискача у цервікальний канал за внутрішній зів.
- Наповнення балона катетера стерильним фізіологічним розчином в об’ємі 30–80 мл з наступною фіксацією з натягом, закріплення пластиром дистального кінця катетера до стегна матері.
- Час, на який катетер залишають ретроцервікально, становить не менше 12–24 години, або до самостійної експульсії, або до розвитку спонтанної пологової діяльності.
Докази щодо використання ламінарій характеризуються низькою якістю. В цілому, при порівнянні застосування ламінарій з плацебо, індукцією окситоцином або простагландинами, було продемонстровано, що з точки зору пріоритетних результатів статистично значуща різниця між цими методами була відсутня. Однак, в порівнянні з простагландинами, застосування ламінарій характеризувалося меншим ризиком гіперстимуляції матки зі зміною частоти серцевих скорочень плода (ВООЗ, 2014).
Методика застосування паличок ламінарій наступна: у цервікальний канал вводять від 1 до 5 ламінарій, попередньо змочених у фізіологічному розчині, на 24 години з подальшою оцінкою ступеня зрілості шийки матки. При необхідності процедуру можна повторити.
Якщо у жінки в ІІ чи ІІІ триместрах вагітності була кровотеча, низьке розташування плаценти – 2 см і менше від внутрішнього зіва, передчасний розрив плодових оболонок, або наявні ознаки вагінальної інфекції, хоріонамніоніту – використання механічних методів «дозрівання» пологових шляхів протипоказано.
Фармакологічні методи підготовки шийки матки
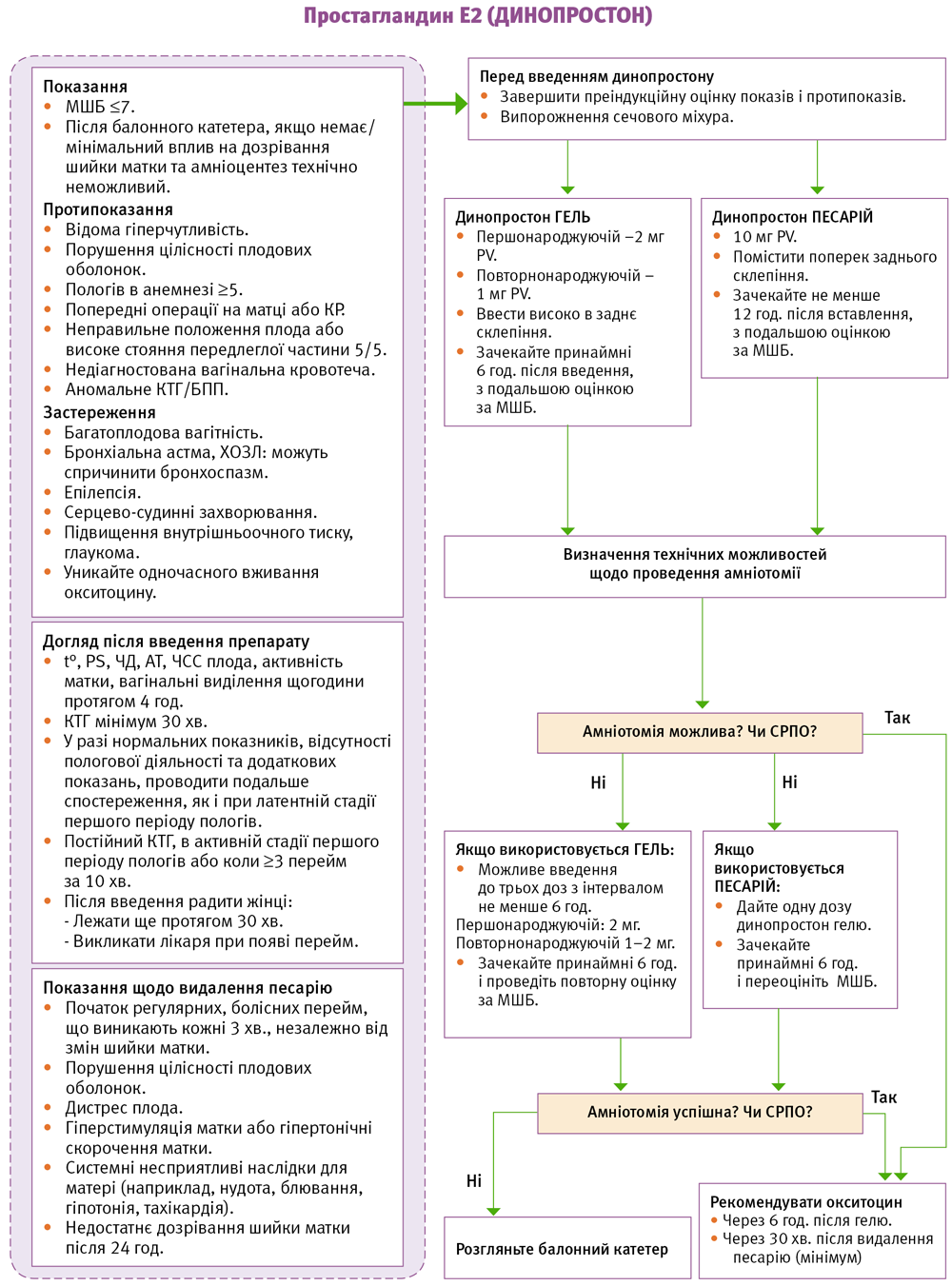
Простагландини групи Е2
Локальне введення простагландину групи Е2 – динопростону є найбільш частим з методів, що застосовують з метою підготовки шийки матки у світі (ACOG, 1999). Owen та співавт. (1991) провели мета-аналіз 18 досліджень, що включають 1811 жінок. Вони встановили, що простагландини групи Е2 покращують оцінку ступеня зрілості шийки матки за шкалою Бішоп і достовірно вкорочують інтервал часу преіндукція-індукція-пологи у порівнянні з тими жінками, у яких для індукції був використаний тільки окситоцин.
Схема використання препаратів, що містять динопростон з метою преіндукції:
А. Інтравагінальне використання:
- початкова доза для першонароджуючих – 1 чи 2 мг та 1 мг для повторнонароджуючих вагінально у заднє склепіння піхви. Оцінка зрілості шийки матки проводиться кожні 6 годин та, при недостатньому ефекті, проводиться повторне введення препарату в дозі 1 чи 2 мг, але не більше трьох доз упродовж доби, з інтервалом не менше 6 годин.
В. Інтрацервікальне введення (на сьогодні практично
не використовується):
- початкова доза складає 0,5 мг кожні 6 годин, загалом не перевищуючи трьох доз, або альтернативна схема: початкова доза 0,5 мг 3 рази на день до двох діб.
При введенні динопростону слід ретельно стежити за тим, щоб препарат не потрапив у порожнину матки, оскільки він може викликати гіпертонус міометрія.
Потрібно пам’ятати! Використання окситоцину з метою пологозбудження неприпустимо раніше 6 годин після останньої дози простагландину
У Європейських країнах та США широке застосування знайшов вагінальний аплікатор «Cervidil», який містить 10 мг динопростону для вагінального застосування у вигляді маленького прямокутного мішечка з подовженим провідником для легкого вилучення його з пологових шляхів.
Аплікатор, введений вагінально, повільно вивільняє динопростон зі швидкістю 0,3 мг/год. протягом 12 годин. «Cervidil» вводиться у заднє склепіння піхви без використання додаткових лубрикантів, тому що вони можуть порушити виділення препарату з аплікатора. Після введення, вагітна повинна залишатися у положенні лежачи протягом не менше двох годин. Аплікатор видаляють через 12 годин або з появою спонтанної пологової діяльності.
Дослідження ефективності та безпеки інтрацервікального гелю у порівнянні з інравагінальним аплікатором, проведені Perry і Leaphart (2004 р.), показали, що використання інтравагінального аплікатора «Cervidil» було асоційоване з більш швидкими пологами – 11.7 у порівнянні з 16,2 години при інрацервікальному використанні динопростону у вигляді гелю.
Простагландини групи Е1
Мізопростол (off-label) – синтетичний простагландин E1, що випускається в дозі 100 або 200 мкг в таблетованій формі для лікування пептичних виразок. Так само цей препарат застосовується для підготовки до пологів шляхом орального або вагінального способу застосування, однак, незважаючи на численні клінічні випробування безпечності та ефективності цього препарату, дана технологія все ще залишається нелегальною у багатьох країнах світу. Разом з тим, FIGO рекомендує використання мізопростолу для підготовки незрілої шийки матки до пологів (FIGO, 2012).
Американська асоціація акушерів-гінекологів провела огляд 19 рандомізованих контрольованих досліджень, що включають понад 1900 вагітних жінок, де була доведена ефективність і безпека мізопростолу в дозі 25 мкг для «дозрівання» шийки матки. Частота побічних ефектів у вигляді тахіситолії матки, меконіальної аспірації, розвитку дистресу плода була порівнянна із застосуванням динопростону (von Gemund і співавт, 2004). У той же час, збільшення дози до 50 мкг мізопростолу було асоційоване зі збільшенням ризику небажаних явищ як для матері, так і для плода (Wing і співавт., 1995).
А. Схема вагінального шляху введення мізопростолу:
- Вагінальне введення у заднє склепіння 25 мкг мізопростолу кожні 6 годин, але не більше 8 доз.
Б. Оральне застосування мізопростолу:
Має відповідну ефективність і безпечність в порівнянні з вагінальним його застосуванням. Методика підготовки та схема використання розчину мізопростолу для перорального застосування:
- Одну таблетку мізопростолу (200 мкг) розчинити у 200 мл питної води, або 100 мкг препарату в 100 мл води, отримавши таким чином концентрацію препарату 1 мкг/1 мл розчину.
- Разова доза становить 25 мл розчину (25 мкг мізопростолу), яку дають вагітній пити кожні 2 години (але не більше 8 разів)
- Прийом препарату припиняють, якщо з’являється пологова діяльність.
- При досягненні «зрілої» шийки матки, починаємо пологозбудження шляхом амнітоміі, з подальшим введенням розчину окситоцину.
Потрібно пам’ятати! Використання окситоцину з метою пологозбудження неприпустимо раніше 6 годин після прийому останньої дози мізопростолу
На сьогодні не рекомендується призначення більше 25 мкг мізопростолу одноразово (незалежно від шляху введення) при вагітності понад 26 тижнів (навіть при наявності мертвого плоду у матці!).
Особливості застосування та протипокази препаратів простагландинового ряду
Препарати простагландинового ряду повинні застосовуватися винятково в акушерському стаціонарі, в умовах, де є можливість стежити за матковою активністю і серцевим ритмом плода (ACOG, 1995). Ця рекомендація зумовлена тим фактом, що використання простагландинів асоціюється з матковою тахисистолією і, як наслідок, дистресом плода. Надмірна маткова активність була описана при вагінальному застосуванні простагландинів Е2 і Е1 в 1–5% вагітних (Brindley і Sokol, 1988; Rayburn, 1989).
Відповідно до положення ACOG (1999), були визначені критерії маткової активності за наступними ступенями:
- Маткова тахісистолія – 6 перейм за 10-хвилинний інтервал протягом не менше 30 хвилин.
- Матковий гіпертонус – маткове скорочення, яке триває більш ніж 2 хвилини.
- Гіперстимуляція матки – маткова тахіситолія, яка призвела до порушення внутрішньоутробного стану плоду.
У разі розвитку тахісістолії матки при застосуванні аплікатора «Cervidil» аплікатор негайно видаляють, що зазвичай призводить до регресу маткової активності. Це є, безсумнівно, одною з переваг в порівнянні з інтрацервікальним гелем, видалення якого з каналу, на жаль, не покращує ситуацію.
Так само, використання простагландинів протипоказано при бронхіальній астмі, глаукомі, гіперчутливості до простагландинів.
При наявності рубця на матці після попереднього кесаревого розтину, застосування мізопростолу або інших простагландинів асоційоване зі збільшенням ризику розриву матки по рубцю, при цьому частота розвитку даного ускладнення становить 5 випадків на 89 вагітних жінок (6%), в той час, як ризик розриву матки без застосування простагландинів становить 1 випадок на 423 вагітних з рубцем на матці (Plaut і співавт., 1999) і тому не рекомендується використання простагландинів у жінок з рубцем на матці!
З обережністю слід застосовувати вагінальну\інтрацервікальну форму простагландину при допологовому відходженні навколоплодових вод, що асоційоване зі збільшенням частоти хоріоамніонітів.
Наприкінці слід зазначити, що індукція пологів є радикальним втручанням у формування пологового процесу, що, найчастіше, визначає той пул ускладнень, які, так чи інакше, пов’язані з цими втручаннями.
Ось чому індукція може використовуватися тільки тоді, коли ризики від пролонгації вагітності (з точки зору матері і плоду) перевищують ризики від самої індукції.
Кожен акушер-гінеколог повинен керуватися чіткими показаннями до використання вищезазначених методик, розуміти короткострокові та довгострокові наслідки застосування обраного методу, при цьому обирати найбільш безпечний метод преіндукції та індукції пологів.
Детальніше
Міжнародний Словник з Допомоги в питаннях Неплідности та Плідности – 2017 (Частина 1)
The International Glossary on Infertility and Fertility Care
Fernando Zegers-Hochschilda, G. David Adamsonb, Silke Dyerc, Catherine Racowskyd,Jacques de Mouzone, Rebecca Sokolf, Laura Rienzig, Arne Sundeh, Lone Schmidti, Ian D. Cookej, Joe Leigh Simpsonk, and Sheryl van der Poell
a University Diego Portales, Program of Ethics and Public Policies in Human Reproduction; Clinica las Condes, Unit of Reproductive Medicine, Santiago, Chile; b ICMART, Palo Alto Medical Foundation Fertility Physicians of Northern California, Palo Alto, CA, USA; c Department of Obstetrics & Gynecology, Groote Schuur Hospital and Faculty of Health Sciences, University of Cape Town, Cape Town, South Africa; d Department of Obstetrics, Gynecology and Reproductive Biology, Brigham and Women’s Hospital, Harvard Medical School, Boston, MA 02115, USA; e INSERM, EIM-ESHRE, ICMART, 15 rue Guilleminot, 75014 Paris, France; f Department of Medicine and Obstetrics and Gynecology, Keck School of Medicine, University of Southern California, Los Angeles, CA 90007, USA; g GENERA Center for Reproductive Medicine, Valle Giulia Clinic, 00197 Rome, Italy; h Department of Obstetrics and Gynecology, St. Olav’s University Hospital, Trondheim, Norway; i Institute of Public Health, University of Copenhagen, Copenhagen, Denmark; j Academic Unit of Reproductive and Developmental Medicine, Department of Oncology and Metabolism, University of Sheffield, Sheffield, UK; k March of Dimes Foundation, White Plains, NY, USA; and l The Population Council, The Rockefeller University, New York, NY 10065, USA
Детальніше