
ПИТАННЯ ДО МАММОЛОГА (частина 1)
 За молочну залозу «відповідає» декілька медичних галузей — мамологія, акушерство та гінекологія, онкологія. Важливо, щоб рекомендації спеціалістів не були суперечливими – від цього залежить успіх лікування. Та чи завжди достатньо спеціальних знань лікарю першої ланки? На запитання читачів відповідає експерт-мамолог Світлана Ласачко
За молочну залозу «відповідає» декілька медичних галузей — мамологія, акушерство та гінекологія, онкологія. Важливо, щоб рекомендації спеціалістів не були суперечливими – від цього залежить успіх лікування. Та чи завжди достатньо спеціальних знань лікарю першої ланки? На запитання читачів відповідає експерт-мамолог Світлана Ласачко
Детальніше
ВСУПЕРЕЧ ДОЛІ
Оптимізація профілактики та корекції системних порушень у жінок з хірургічною менопаузою
Збільшення частоти випадків доброякісних новоутворень матки та яєчників серед жінок репродуктивного та пременопаузального віку у 68–72% випадків є поштовхом до оперативного втручання, що змушує приділяти все більшу увагу проблемі хірургічної менопаузи. Термін «хірургічна менопауза» використовується стосовно жінок, менструальна функція яких була штучно припинена у результаті видалення яєчників, яєчників і матки або тільки матки. Якщо два перші варіанти можна віднести до естрогендефіцитних, то у хірургічній менопаузі при збереженні одного або обох яєчників такої ясності немає. Дані літератури стосовно функції яєчників після гістеректомії вкрай суперечливі, що відбивається на певних ускладненнях при виборі обсягу оперативного втручання та відсутності єдиного підходу до профілактики менопаузальних порушень [1, 2, 4, 7]. Значне зростання захворювань серед жінок у віці, що збігається з настанням менопаузи, є серйозним аргументом, щоб вважати менопаузу та пов’язані з нею зміни в організмі одним з основних чинників, що визначають якість і тривалість життя жінки [3, 8].
Детальніше
АУТОВОСПАЛИТЕЛЬНЫЕ СИНДРОМЫ КАК ПРИЧИНА РЕЦИДИВИРУЮЩЕЙ ЛИХОРАДКИ У ДЕТЕЙ (ЧАСТЬ 2)
(Окончание. Начало – в №1 (46) 2014)
Криопирин-ассоциированные периодические синдромы (Cryopyrin-Associated Periodic Syndromes – CAPS) связаны с мутациями в гене NLRP3 (CIAS1), кодирующем синтез белка криопирина (NALP3/PYPAF1). Ген NLRP3 (CIAS1) локализован на длинном плече 1-й пары хромосом (1q44) и экспрессируется в полиморфноядерных лейкоцитах, моноцитах и хондроцитах. Криопирин – основной компонент NLRP3-инфламмасомы – цитоплазматического белкового комплекса, запускающего воспалительную реакцию при контакте фагоцитов с микроорганизмами (рис. 1).
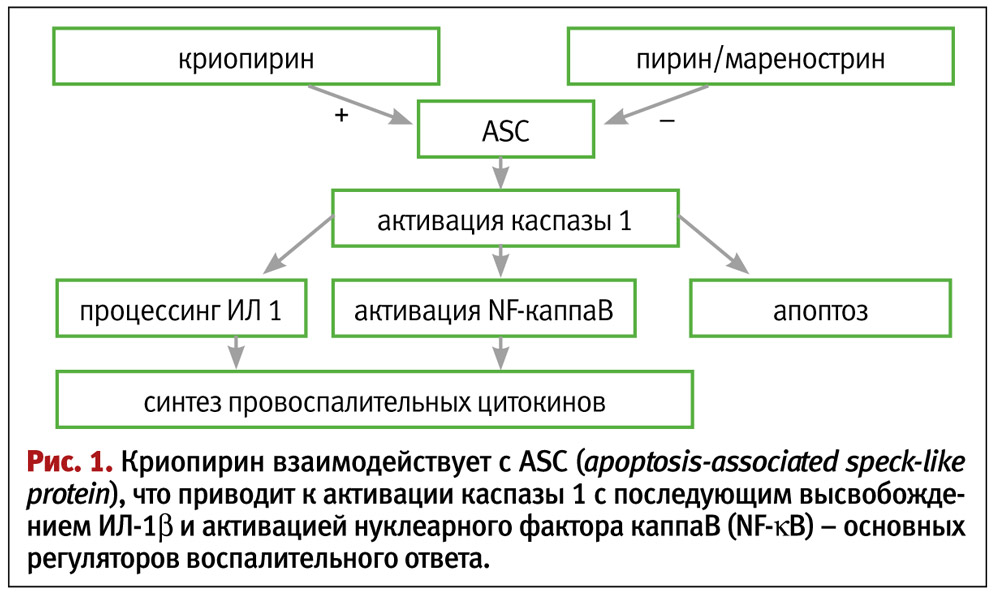
Инфламмасомы – важный компонент системы врожденного иммунитета, которая основана на клеточной системе быстрого распознавания генетически инородных структур и их уничтожения. Распознавание патогенов осуществляется мембранными Тoll-подобными рецепторами и цитозольными NOD-подобными рецепторами. Некоторые NOD-подобные рецепторы распознают не только инфекционные сигналы, но и т. н. немикробные «сигналы опасности». В частности, известными лигандами криопирина являются бактериальная и вирусная РНК, а также кристаллы мочевой кислоты. При связывании лиганда криопирин взаимодействует с протеином ASC, что приводит к активации каспазы 1, и в дальнейшем – к внутриклеточному процессингу и образованию зрелой активной формы интерлейкина 1b.
При криопирин-ассоциированных периодических синдромах (CAPS) мутации в гене NLRP3 (CIAS1) приводят к постоянной избыточной продукции ИЛ-1b, тогда как в норме его синтез увеличивается только в ответ на инфекцию.
 Известны 3 формы CAPS:
Известны 3 формы CAPS:
1) семейный холодовой аутовоспалительный синдром (Familial Cold Autoinflammatory Syndrome – FCAS) – впервые описан в 1940 г.;
2) синдром Макл–Уэлса (Muckle–Wells Syndrome – MWS) – впервые описан в 1962 г.;
3) хронический младенческий нервно-кожно-артикулярный синдром/ младенческое мультисистемное воспалительное заболевание (Chronic Infantile Onset Neurologic Cutneous Articular/Neonatal Onset Multisystem Inflammatory Disease – CINCA/NOMID) – впервые описан в 1981 г.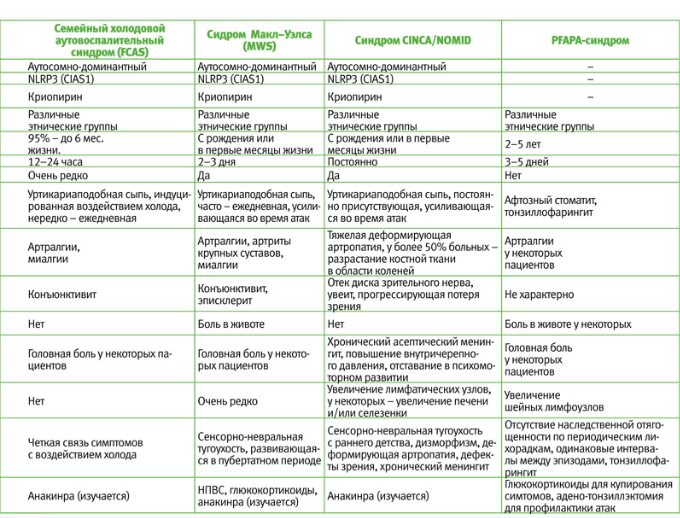
Для всех этих заболеваний характерны:
- раннее начало (на первом году жизни, иногда – позже);
- наличие рецидивирующей или постоянной лихорадки, уртикариаподобной сыпи, поражения суставов различной степени, конъюнктивита и головной боли;
- аутосомно-доминантный тип наследования.
В настоящее время идентифицированы 111 мутаций в гене NLRP3 (CIAS1), приводящих к развитию криопиринопатий. FCAS, MWS и CINCA/NOMID были описаны в разное время и ранее считались самостоятельными нозологическими единицами. Однако, после того, как были выявлены общие патогенетические механизмы и генетическая основа этих заболеваний, их объединили в одну группу – CAPS, и в настоящее время считают различными клиническими вариантами одного заболевания. При этом FCAS – легкая форма с благоприятным прогнозом, MWS протекает тяжелее с возможностью развития необратимых изменений в некоторых органах (тугоухость, амилоидоз), а CINCA/NOMID – наиболее тяжелый вариант криопиринопатий, при котором упорное воспаление быстро приводит к необратимым изменениям в большинстве органов и систем организма.
Сыпь – наиболее ранний и постоянный признак CAPS. У большинства пациентов сыпь появляется уже при рождении или вскоре после него. В некоторых случаях MWS и FCAS сыпь может появиться в более позднем возрасте. Макулопапулярная, напоминающая крапивницу, сыпь покрывает все тело и усиливается в периоды воспалительных атак. Чаще всего сыпь не зудит, но некоторые пациенты жалуются на зуд или даже жжение. При биопсии кожи в области элементов сыпи выявляют увеличение количества нейтрофилов вокруг спиралевидных выводных протоков эккринных потовых желез и кровеносных сосудов. У некоторых пациентов, как правило, с FCAS, сыпь отмечается только во время воспалительных атак, но у большинства больных сыпь имеет место практически каждый день, во время атак значительно усиливаясь.
Семейный холодовой аутовоспалительный синдром (FCAS), известный также как семейная холодовая крапивница (familial cold urticaria – FCU) и холодовая гиперчувствительность, характеризуется появлением сыпи, артралгий, конъюнктивита и лихорадки после воздействия холода. FCAS отличается от других наследственных синдромов периодической лихорадки наличием четкого провоцирующего фактора – холода, ранним началом (обычно до шестимесячного возраста) и небольшой продолжительностью эпизодов – менее 24 часов.
У 95% пациентов приступы начинаются в течение первых 6 месяцев, у 60% – в течение первых нескольких дней жизни. Средний возраст начала симптомов – 47 дней, с диапазоном от 2 часов до 10 лет. Тяжесть течения не зависит от возраста начала симптомов. Сыпь максимально выражена в подростковом возрасте и в юности.
Воспалительные атаки при FCAS всегда связаны с воздействием холода. При этом диапазон температур, способных вызвать симптомы заболевания, и длительность воздействия значительно варьируют. У одних пациентов симптомы появляются после серьезного переохлаждения (например, в холодные ветреные дни), а у других – после совсем незначительных воздействий (употребление холодной пищи или напитков, плавание, пребывание вблизи кондиционера).
Симптомы появляются через 1–2 часа после воздействия холода. Помимо сыпи, обычно отмечается лихорадка с ознобом (93%), полиартралгии (96%) и конъюнктивит (84%). Реже в период приступа у пациентов наблюдается обильное потоотделение (78%), сонливость (67%), головная боль (58%), неукротимая жажда (53%), тошнота (51%) и миалгии. Развитие артритов не характерно для воспалительных атак при FCAS. Средняя длительность приступа – 12 часов (от 30 минут до 72 часов), у 94% пациентов большинство приступов заканчивается менее чем за 24 часа.
Диагностические критерии семейного холодового аутовоспалительного синдрома – FCAS (Hoffman HM et al., 2001)
- Рецидивирующие эпизоды лихорадки и сыпи, возникающие после воздействия холода (естественного и/или экспериментального).
- Аутосомно-доминантный тип наследования.
- Возраст начала заболевания – менее 6 месяцев жизни.
- Продолжительность большинства приступов менее 24 часов.
- Конъюнктивит, связанный с приступами.
- Отсутствие глухоты, периорбитального отёка, увеличения лимфоузлов и серозитов.
FCAS следует отличать, в первую очередь, от приобретенной холодовой крапивницы – наиболее частой формы физической крапивницы, при которой симптомы обусловлены дегрануляцией тучных клеток с высвобождением гистамина. В отличие от FCAS, приобретенная холодовая крапивница обычно возникает у взрослых и спонтанно разрешается. Сыпь при приобретенной холодовой крапивнице возникает непосредственно после прямого воздействия холода (в течение нескольких минут), проходит в течение нескольких часов и может сопровождаться ангионевротическим отеком, бронхиальной обструкцией и гипотензией.
Кроме того, проводится дифференциальная диагностика с другими синдромами периодической лихорадки, криоглобулинемией и крапивницей.
Синдром Макл–Уэлса (MWS) – более тяжелый вариант криопиринопатии, при котором помимо сыпи, лихорадки и конъюнктивита, в период воспалительных атак отмечается артрит и боль в животе. У части пациентов с возрастом развивается сенсорная тугоухость.
Воспалительные атаки при синдроме Макл–Уэлса длятся 24–72 часа и чаще всего провоцируются холодом, сыростью, стрессом, физическими нагрузками и неизвестными факторами. При этом связь приступов с воздействием холода не так очевидна, как при FCAS. Суставной синдром при MWS может варьировать от непродолжительных артралгий до полиартритов с вовлечением, как правило, крупных суставов. Нейросенсорная тугоухость развивается у 50–70% пациентов, обычно в подростковом возрасте.
После нескольких лет заболевания у 20–40% больных MWS развивается системный амилоидоз, тогда как при FCAS описаны лишь единичные случаи этого осложнения.
Дифференцировать синдром Макл–Уэлса нужно не только с другими аутовоспалительными заболеваниями, но и нередко с синдромом Альпорта, при котором, как известно, имеют место тугоухость, поражение глаз и почечная недостаточность.
Синдром CINCA/NOMID – наиболее тяжелая форма CAPS, характеризующаяся персистирующим выраженным воспалением с поражением кожи, костей, суставов и ЦНС.
В отличие от других синдромов периодической лихорадки, при синдроме CINCA/NOMID лихорадка присутствует практически ежедневно, нередко с первых дней жизни, или же могут отмечаться непродолжительные, но очень частые эпизоды лихорадки. Также постоянным симптомом является уртикариаподобная сыпь, которая может менять локализацию, быть более или менее выраженной, но присутствует практически все время от начала заболевания.
Поражение ЦНС у пациентов с синдромом CINCA/NOMID характеризуется развитием хронического асептического менингита, вызванного нейтрофильной инфильтрацией мозговых оболочек, который проявляется, в первую очередь, головными болями и раздражительностью. В дальнейшем присоединяются симптомы повышения внутричерепного давления (отек дисков зрительных нервов, наружная и внутренняя гидроцефалия, атрофия мозга). У большинства детей с синдромом CINCA/NOMID уже в раннем детстве формируется нейросенсорная тугоухость. Нередко дети отстают в умственном развитии и страдают от симптоматической эпилепсии.
Стойкие изменения суставов появляются в течение первых лет жизни в виде полиартрита с симметричным поражением крупных суставов. Характерен усиленный рост метафизов и эпифизов длинных трубчатых костей, надколенника, а также ускорение оссификации ядер окостенения, что приводит к серьезным деформациям и контрактурам в конечностях, нарушению их функции и болевому синдрому.
Поражение глаз при синдроме CINCA/NOMID характеризуется конъюнктивитом, передним (50%) или задним (20%) увеитом, атрофией зрительного нерва (25%). Больные имеют дизморфические особенности: седловидную переносицу, макроцефалию, нависающий лоб, низкий рост с короткими утолщенными конечностями, контрактуры суставов (особенно, коленных). Нередко определяется увеличение лимфатических узлов и селезенки.
Синдром CINCA/NOMID дифференцируют с другими аутовоспалительными синдромами, а также с болезнью Стилла. Отличием поражения суставов при синдроме CINCA/NOMID является формирование суставных контрактур за счет разрастания костной ткани, а не утолщения синовиальных оболочек и периартикулярных тканей, что имеет место при болезни Стилла.
Диагностика криопиринопатий
Диагностика криопиринопатий базируется, в первую очередь, на клинико-анамнестических данных. Наличие характерного симптомокомплекса в сочетании с указанием на аналогичные симптомы у ближайших родственников пациентов в нескольких поколениях имеет место у большинства больных с FCAS и MWS. При синдроме CINCA/NOMID более чем в половине случаев наследственность не отягощена, заболевание вызвано мутацией de novo.
В период воспалительных атак в крови повышаются уровни острофазовых показателей (лейкоциты, СОЭ, СРБ), при синдроме CINCA/NOMID может также отмечаться анемия, повышение уровня эозинофилов в крови и спинномозговой жидкости, гиперглобулинемия. Для верификации патогномоничных для синдрома CINCA/NOMID изменений костей и суставов проводится рентгенография коленей. С целью подтверждения диагноза FCAS может быть проведена холодовая проба: к коже на 5 минут прикладывают кубик льда, после чего фиксируют характерные для FCAS изменения. Кроме того, в западных странах доступно генетическое исследование, подтверждающее наличие мутаций в гене NLRP3 (CIAS1).
До недавнего времени в терапии криопиринопатий с небольшим успехом применяли глюкокортикоиды, колхицин, цитостатики. При этом пациенты с синдромом CINCA/NOMID погибали еще в детском возрасте. Однако в настоящее время возможности лечения криопиринопатий значительно расширились – применение рекомбинантных антагонистов рецепторов ИЛ-1 (рилонацепт, канакинумаб, анакинра) позволяет эффективно контролировать симптомы заболеваний.
Синдром PFAPA (Periodic Fever, Aphthous Stomatitis, Pharyngitis, Adenitis Syndrome) впервые был описан G. S. Marshall в 1987 на основании наблюдения 12 детей с периодической лихорадкой, сопровождавшейся фарингитом, афтозным стоматитом и увеличением шейных лимфоузлов. Первоначально этот синдром был назван «синдромом Маршалла», но позднее более распространенным названием стала аббревиатура, отражающая основные клинические проявления синдрома – «PFAPA».
В отличие от других синдромов периодической лихорадки, синдром PFAPA является спорадическим заболеванием, никаких данных, позволяющих предположить его наследственный характер, пока не получено. Этиология неизвестна. Есть данные, что в период приступов лихорадки в крови отмечается повышение уровней провоспалительных цитокинов: ИЛ1b, ТNFa, ИЛ6 и ИЛ12р70. При этом в межприступный период полной нормализации этих показателей не наблюдается, что указывает на то, что воспалительный процесс персистирует.
Болеют чаще всего дети в возрасте от 2 до 5 лет, с небольшим преобладанием мальчиков. Никаких этнических особенностей нет. Синдром PFAPA – самый распространенный из синдромов периодической лихорадки, он встречается гораздо чаще, чем моногенные аутовоспалительные синдромы.
Эпизоды лихорадки при PFAPA-синдроме длятся от 3 до 5 дней и повторяются каждые 3–5 недель. Температура тела повышается резко, нередко до 40–41°С, лихорадка сопровождается ознобом. Небольшие (менее 1 см в диаметре) афты на слизистой оболочке полости рта или на губах появляются в течение 12–24 часов от начала лихорадки, они умеренно болезненны и в течение недели заживают полностью без образования рубцов. В большинстве случаев также отмечается двустороннее увеличение шейных лимфоузлов и тонзиллофарингит, обычно без формирования налетов на миндалинах. Другие, менее распространенные симптомы – боль в животе, артралгии и головная боль.
В период лихорадки у большинства детей в крови определяется повышение СОЭ, количества лейкоцитов и уровня С-реактивного белка. В посевах мазков с миндалин, взятых во время эпизодов лихорадки, b-гемолитический стрептококк группы А отсутствует. Увеличение концентрации IgD иногда может иметь место, но оно не столь значительно, как при HIDS.
В межприступном периоде дети с синдромом PFAPA хорошо себя чувствуют, никаких отклонений при клиническом и лабораторном обследовании не выявляется, никакого негативного воздействия на рост и развитие детей воспалительные атаки не имеют.
Прогноз при синдроме PFAPA весьма благоприятный. У большинства детей после 5–7-летнего возраста симптомы полностью проходят. Лишь у небольшого числа пациентов старше 7 лет после того, как классический клинический симптомокомплекс перестал появляться, еще в течение нескольких лет могут отмечаться редкие и нерегулярные неклассические эпизоды.
Критерии диагностики синдрома PFAPA (K. T. Thomas et al., 1999)
Наличие всех 3 критериев из следующих:
1) 3 и более документированных эпизода лихорадки, длившихся не более 5 дней, с равномерными интервалами между эпизодами длительностью от 3 до 6 недель;
2) наличие во время эпизодов лихорадки шейной лимфаденопатии, тонзиллофарингита и/или афтозного стоматита;
3) нормальное состояние между эпизодами, отсутствие нарушений роста и развития.
Критерии, исключающие PFAPA:
1) нейтропения во время эпизода лихорадки или непосредственно предшествующая ему;
2) атипичная симптоматика;
3) повышение острофазовых показателей между эпизодами;
4) указания на периодические лихорадки в семейном анамнезе.
Единого мнения относительно лечения детей с синдромом PFAPA нет. Учитывая доброкачественный характер его течения, спонтанное разрешение с возрастом, приходится выбирать лишь те лечебные мероприятия, при которых риск побочных эффектов минимален. Лечебная тактика при синдроме PFAPA преследует 2 цели: 1) купирование симптомов во время эпизодов лихорадки; 2) предупреждение новых атак заболевания.
Нестероидные противовоспалительные препараты и парацетамол при PFAPA-синдроме недостаточно эффективны. Назначение глюкокортикоидов (от 0,5 мг/кг до 1–2 мг/кг в сутки по преднизолону) коротким курсом в начале атаки способствует быстрому купированию симптомов. Однако, применение кортикостероидов при каждом лихорадочном эпизоде способствует сокращению интервала между атаками.
Как показывают проведенные недавно рандомизированные контролируемые исследования, наиболее эффективной мерой профилактики воспалительных атак при синдроме PFAPA является аденотонзиллэктомия.
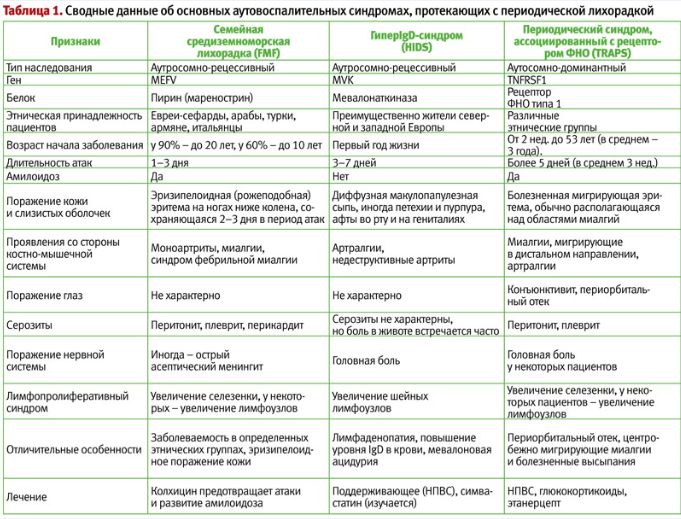
Дифференциальная диагностика синдромов периодической лихорадки основывается, в первую очередь, на клинико-анамнестических данных (табл. 1), т. к. генетическое исследование дорого и доступно лишь в немногих центрах. При этом принципиально важно отличать синдром PFAPA от моногенных синдромов периодической лихорадки (особенно, FMF, HIDS и TRAPS), поскольку последние имеют не такой благоприятный прогноз, как синдром PFAPA, и требуют иных подходов к лечению. С другой стороны, критерии диагностики синдрома PFAPA низкоспецифичны. Как показывают исследования M. Gattorno, под диагностические критерии синдрома PFAPA попадают 83% больных с гипер IgD-синдромом, 57% больных TRAPS и 8% больных семейной средиземноморской лихорадкой. В связи с этим, была предложена т. н. шкала Gaslini, включающая признаки, наличие которых указывает на вероятность моногенного синдрома периодической лихорадки, что, в свою очередь, требует проведения генетических тестов. Эти признаки включают:
- начало заболевания в раннем возрасте;
- наличие периодической лихорадки в семейном анамнезе;
- боль в животе/груди;
- диарею;
- афтозный стоматит.

Заключение
Аутовоспалительные синдромы – недавно сформировавшееся направление в современной ревматологии, но интерес к ним неуклонно растет. По мере ознакомления медицинской общественности с клинико-генетическими особенностями аутовоспалительных синдромов, и в том числе тех, что проявляются периодической лихорадкой, эта патология диагностируется все чаще.
Первые симптомы большинства этих заболеваний появляются в детском возрасте, поэтому именно для педиатров важно уметь заподозрить аутовоспалительный синдром. Еще большее значение своевременной диагностике аутовоспалительных синдромов придает тот факт, что в настоящее время, благодаря использованию генно-инженерных препаратов, способных ингибировать медиаторы системы врожденного иммунитета, в лечении данной патологии наметился прорыв, когда удается полностью контролировать симптомы заболеваний, считавшихся ранее инвалидизирующими или даже смертельными.
Наличие у ребенка 2 или 3 документированных эпизодов лихорадки в сочетании с характерными (описанными выше) клиническими и лабораторными данными должно стать поводом для направления к детскому ревматологу и/или инфекционисту для уточнения диагноза и дальнейшего обследования. Диагностика аутовоспалительных синдромов, протекающих с периодической лихорадкой, требует исключения инфекционной, аутоиммунной, онкологической патологии и врожденных иммунодефицитных заболеваний. Значительным подспорьем в диагностике синдромов периодической лихорадки стали генетические исследования, которые становятся все более доступными для многих стран благодаря международным программам (проект EUROFEVER).
Список литературы находится в редакции.
ДетальнішеТЕРАПЕВТИЧЕСКАЯ ТАКТИКА ПРИ ЛИХОРАДОЧНЫХ СОСТОЯНИЯХ У ДЕТЕЙ
Инфекционные болезни у детей относятся к наиболее частым причинам обращения за медицинской помощью. Лидирующие позиции в данной патологии занимают острые респираторные и острые кишечные инфекции. Одним из первых и важных симптомов, характерных для острых инфекционных заболеваний у детей и заставляющих родителей ребенка обратиться к врачу, является повышение температуры тела.
В настоящее время большинство специалистов острое повышение температуры тела у ребенка в ответ на воздействие патогенных возбудителей при развитии инфекционного процесса считают адаптационной реакцией организма, оказывающей положительное влияние на процессы активации иммунной системы [1].
Выделяют два основных типа повышения температуры тела – «розовая» и «бледная» лихорадки. Ключевым в механизме развития различных типов лихорадочной реакции является соответствие или несоответствие теплопродукции и теплоотдачи, которые могут варьировать у разных пациентов при одинаковом уровне гипертермии. Разные клинические варианты лихорадки требуют от врача дифференцированного подхода к терапевтической тактике.
«Розовая» лихорадка
При развитии «розового» типа лихорадочной реакции отмечается соответствие теплоотдачи и теплопродукции. У таких пациентов даже при фебрильных значениях уровня температуры тела сознание, как правило, не нарушено, при осмотре ребенок активен, кожные покровы умеренно гиперемированы, влажные, горячие на ощупь, конечности теплые. Имеющаяся тахикардия и учащение дыхания соответствуют степени повышения температуры тела – на каждый градус свыше 37°С отмечается учащение ритма сердца на 10–20 уд./мин. и дыхания на 4–5 дыхательных движений в минуту. Данное состояние свидетельствует об адекватном течении лихорадочной реакции и, как правило, не требует применения жаропонижающих лекарственных средств.
«Бледная» лихорадка
Появление озноба, бледности кожных покровов, акроцианоза, бледности и «мраморности» кожных покровов, положительного симптома «белого пятна», холодных на ощупь конечностей при высоком уровне повышения температуры тела, нарушений сознания (бред, галлюцинации, выраженная вялость, сонливость) указывает на развитие «бледной» лихорадки, требующей назначения жаропонижающих препаратов в сочетании с сосудорасширяющими и антигистаминными средствами [3].
Тактика лечения
Терапевтическая тактика у лихорадящих пациентов состоит из двух основных компонентов:
1) проведение собственно этиотропной терапии инфекционного заболевания;
2) симптоматическая терапия лихорадочного состояния, которая может осуществляться физическими и фармакологическими методами.
Общим в тактике ведения лихорадящих больных является обязательное динамическое наблюдение за состоянием пациента, использование жаропонижающих средств строго по показаниям с учетом их фармакокинетики, фармакодинамики и показателей безопасности применения у пациентов разных возрастных групп. Не следует добиваться снижения температуры тела строго до нормальных показателей, у большинства пациентов снижение температуры тела на 1–1,5°С приводит к улучшению самочувствия и оптимизации показателей гемодинамики.
При благоприятном течении лихорадочной реакции у детей, не входящих в группу риска развития осложнений, в качестве стартовой терапии показано назначение физических методов охлаждения, направленных на усиление теплоотдачи.
Показанием для медикаментозной коррекции повышения температуры тела у пациентов с «розовым» типом лихорадки является повышение аксиллярной температуры у ранее здоровых детей в возрасте старше 3 мес. до 39,1°C. Детям с фебрильными судорогами в анамнезе, а также пациентам с «бледным» типом лихорадки показано назначение жаропонижающих препаратов при температуре тела более 38,0°C, детям с тяжелыми заболеваниями сердца и легких – при температуре тела выше 38,5°C, детям первых 3 мес. жизни – при температуре тела выше 38,0°C [2, 5, 6]. При этом, в случае развития у пациента «бледной» лихорадки, прием жаропонижающих лекарственных средств необходимо сочетать с сосудорасширяющими препаратами (папаверин 1 мг/кг, но-шпа 1 мг/кг). Это позволит оптимизировать гемодинамические показатели у таких больных и увеличить теплоотдачу.
Выбор жаропонижающих лекарственных средств в педиатрической практике определяется показателями безопасности и эффективности.
Наиболее оправдано при острых респираторных инфекциях у детей назначение нестероидных противовоспалительных препаратов (НПВП), так как с клинической точки зрения сочетание противовоспалительного, болеутоляющего и жаропонижающего действий данной группы лекарственных препаратов направлено на купирование основных симптомов этой группы инфекционных заболеваний. При этом отличительной особенностью жаропонижающего эффекта НПВП является влияние только на повышенную температуру тела и отсутствие действия при нормальной температуре тела, в отличие от «гипотермических» средств (хлорпромазин и др.).
Общим для НПВП в механизме действия является угнетение синтеза простагландинов из арахидоновой кислоты путем ингибирования фермента циклооксигеназы. Такая неспецифичность противовоспалительного эффекта является преимуществом, позволяющим использовать данную категорию лекарственных средств независимо от этиологических и нозологических особенностей острых респираторных заболеваний [6].
НПВП представлены следующими классами фармакологических веществ: салицилаты (ацетил-салициловая кислота и др.), пиразолидоны (фенилбутазон), производные индолуксусной (индометацин и др.) и фенилуксусной (диклофенак) кислот, оксикамы (пероксикам и др.), производные пропионовой кислоты (ибупрофен и др.), алкалоны (набуметон), производные сульфонамида (нимесулид и др.), производные антраниловой кислоты (мефенаминовая кислота и др.), пиразолоны (метамизол и др.), производные парааминофена (парацетамол и др.), производные гетероарилуксусной кислоты (кеторолак) [7].
Большинство специалистов во всем мире не рекомендуют применение ацетилсалициловой кислоты как жаропонижающего средства у детей до 12 лет ввиду высокого риска развития при вирусных инфекциях у детей синдрома Рея, характеризующегося токсической энцефалопатией и жировой дегенерацией внутренних органов, преимущественно печени и головного мозга [2, 5]. Также исключены из клинической практики амидопирин из-за своей высокой токсичности, а в большинстве стран мира и метамизол из-за риска развития агранулоцитоза [8].
Во всем мире для терапии лихорадочных реакций у детей рекомендованы такие НПВП как ибупрофен и парацетамол. Они являются единственными представителями своей группы, разрешенными для безрецептурного применения при лихорадке и боли у детей.
Ибупрофен
Синтезированный в 1961 г. ибупрофен широко используется в педиатрии с 1969 г. В отличие от парацетамола, данный препарат характеризуется неселективным блокирующим действием на оба изофермента циклооксигеназы. Это обеспечивает не только жаропонижающий эффект, но и более выраженное анальгезирующее и противовоспалительное воздействие. Это делает ибупрофен препаратом выбора у пациентов, лихорадка у которых сопровождается воспалительными процессами, например при ангине, отите, артритах и т. д. [6].
Проведенные клинические исследования показывают, что по эффективности терапии лихорадки у детей ибупрофен имеет преимущества перед парацетамолом и другими НПВП. По данным проведенного мета-анализа, у детей разовые дозы ибупрофена (4–10 мг/кг) и ацетаминофена (7–15 мг/кг) имеют сходный профиль безопасности в качестве анальгетиков или жаропонижающих средств. Однако ибупрофен продемонстрировал большую эффективность жаропонижающего эффекта, чем парацетамол, при оценке уровня повышения температуры через 2, 4 и 6 ч. после начала лечения [11].
Более высокая клиническая эффективность ибупрофена была продемонстрирована в двойном слепом рандомизированном исследовании, в котором осуществлялось наблюдение за пациентами в возрасте от 2 до 11 лет с лихорадкой разного уровня [12]. Сравнивалась эффективность, переносимость и безопасность ибупрофена, ацетаминофена и плацебо. Всего в исследовании приняли участие 127 детей. В группах детей, при терапии повышения температуры тела которых использовались ибупрофен и ацетаминофен, отмечались хорошая переносимость и большая эффективность, чем в группе плацебо. При этом было показано, что ибупрофен более эффективен в снижении высокой температуры тела (>39,2°С), чем парацетамол. В отличие от парацетамола, ибупрофен отличает выраженный анальгезирующий эффект. Так, в опубликованном метаанализе данных 85 сравнительных клинических исследований показано, что ибупрофен более эффективен, чем ацетаминофен, для лечения болевого синдрома, сочетающегося с лихорадкой, как у детей, так и у взрослых, при этом оба препарата показали одинаковый профиль безопасности [13]. В последние годы рядом исследователей было показано наличие иммуномодулирующего действия у ибупрофена, которое сопровождается выработкой эндогенного интерферона, что становится особенно актуальным в терапии острых вирусных инфекций у детей [14].
«Нурофен для детей» – оригинальный препарат ибупрофена, разработанный в Великобритании. В настоящее время широта терапевтического потенциала данного препарата обеспечивается наличием разных лекарственных форм Нурофена как для перорального, так и для ректального применения у детей:
- суспензия для приема внутрь (100 мг/5 мл) с клубничным или апельсиновым вкусом;
- ректальные суппозитории по 60 мг;
- таблетированная форма – Нурофен для детей с 6 лет.
Отличительной особенностью препарата является высокий профиль безопасности применения, в том числе у детей с хроническими заболеваниями, так как суспензия «Нурофен для детей» не содержит сахара, алкоголя и красителей.
Удобными и терапевтически эффективными являются ректальные лекарственные формы, которые во многих случаях могут служить альтернативой не только пероральным, но и инъекционным формам. Они показаны пациентам, для которых прием лекарственного средства через рот затруднен (отказ ребенка, тошнота, рвота, срыгивания). Отличительной особенностью ректальных форм «Нурофен для детей» является быстрое всасывание и высокая биодоступность ибупрофена, а также безболезненность и простота применения, что делает «Нурофен для детей» препаратом выбора.
Таким образом, в тактике ведения лихорадящего больного ибупрофен («Нурофен для детей») является оптимальным лекарственным средством для стартовой терапии, так как обладает благоприятным профилем эффективности и безопасности для детей в разовой дозе 5–10 мг/кг, обеспечивает быстрое снижение высокой температуры тела при лихорадке, обладает длительным жаропонижающим и анальгезирующим эффектами и хорошей переносимостью у детей, начиная с 3 мес. жизни.
По материалам журнала «Рациональная фармакотерапия».
Детальніше
МІЖНАРОДНИЙ ДЕНЬ ЛЮДИНИ З СИНДРОМОМ ДАУНА: здоров'я та добробут для всіх
18 березня у Києві пройшла прес-конференція «Міжнародний День людини з синдромом Дауна: здоров'я та добробут для всіх», приурочена до тематичного дня, який відзначається 21 березня, і цього року відбудеться удев'яте

Дата Міжнародного дня символізує унікальність трисомії 21-ї хромосоми, яка викликає синдром Дауна. У цей день ініціативні групи організовують та беруть участь у заходах по всьому світу. Головна мета активістів – підвищення обізнаності громадськості про права, процес соціалізації і сприяння добробуту людей із синдромом. Тема заходів цього року – «Здоров'я та добробут для всіх».
На заході у Києві провідні експерти у сфері охорони здоров'я, представники міжнародної спільноти, бізнесу та соціального сектору надали інформацію про синдром Дауна, особливості способу життя, стану здоров'я, медичних і соціальних потреб людей з синдромом, а також про соціальні проекти, які проводяться в Україні.
Частота синдрому Дауна серед новонароджених, згідно із загальною статистикою, становить один випадок на 700 дітей. В Україні, станом на 1 січня 2013 року, налічувалося 3 780 дітей із синдромом Дауна.
Анатолій Косаковський, д. мед. н., головний дитячий оториноларинголог МОЗ України, поділився з присутніми інформацією про медичні потреби та асоційовані захворювання, ризик розвитку яких високий серед людей з синдромом: «Синдром Дауна – одна з найпоширеніших форм генетичних аномалій, і пов'язана вона з присутністю додаткової хромосоми у клітинах людини. На даний момент невідомо, чим саме викликана її поява.
До асоційованих захворювань, ризик розвитку яких високий у людей з синдромом Дауна, можна віднести серцеві порушення, аномалії шлунково-кишкового тракту, порушення слуху та зору, функції щитовидної залози. Про подібну специфіку повинні знати не тільки батьки дитини, але також і медичні працівники. Люди з синдромом Дауна можуть мати проблеми зі здоров'ям протягом усього життя, тому вони повинні мати доступ до адекватного медичного обслуговування, нарівні з іншими пацієнтами. А вся інформація про ускладнення, надана лікарями, повинна бути точною, зрозумілою і перевіреною».
Детальніше"ДІТИ СОНЦЯ" МОЖУТЬ БАГАТО СКАЗАТИ, АЛЕ ЇХ ТРЕБА ЦЬОМУ НАВЧИТИ
Міжнародний день людей з синдромом Дауна відзначають 21 березня із 2006 року. День вибраний невипадково: 21 день третього місяця символічно показує, що синдром Дауна пов'язаний із трьома копіями зайвої 21-ї хромосоми. У кожній клітині звичайної людини – їх 46, а у тих, хто має синдром Дауна, – 47.
Синдром Дауна (далі СД) – один з найпоширеніших хромосомних розладів. У медичній та дефектологічній літературі синдром Дауна є основною ознакою психопатологічних порушень і розглядається як диференційована форма розумової відсталості, що поділяється на ступені:
- Глибока ступінь розумової відсталості.
- Важка ступінь розумової відсталості.
- Середня або помірна ступінь розумової відсталості.
- Слабка або легка ступінь розумової відсталості.
Інтелект людей з синдромом Дауна звичайно знижений до рівня помірної розумової відсталості. Коефіцієнт інтелектуального розвитку (IQ) коливається між 20 і 49, хоча в окремих випадках може бути вищим або нижчим від цих меж (було зареєстровано випадки, коли IQ хворих на СД сягав 80%).
У процесі психічного розвитку спостерігаються певні варіації, проте характерні його особливості у дітей з СД можна описати у загальних рисах. У ранньому дитинстві дуже спокійні і тихі. Більшість дітей з СД багато сплять, погано їдять і не вимагають їжі. Вони пізно вчаться сидіти і ходити. Затримка мовлення може тривати роками, а коли ці діти все ж навчаться говорити (вимовляти прості слова і короткі речення), вони не в змозі вести зв’язну бесіду. Уважність і здатність до концентрації уваги дуже низькі; пам’ять, як правило, погана, хоча трапляються і винятки. Здібності до навчання обмежені, але діти часто є спостережливими, допитливими і схильними до наслідування. У цілому діти з СД життєрадісні, полюбляють музику, охоче танцюють і стають улюбленцями через свою добру вдачу, ніжність і чуйність. Трапляються випадки тривожних, агресивних проявів, але вони складають незначний відсоток від усіх хворих. Ступінь розумової відсталості певною мірою коливається, тому важко прогнозувати, яким буде рівень інтелекту в дитини. Психічний розвиток до певної міри обумовлюється впливом навколишнього середовища.
У дітей із синдромом Дауна відзначається збереженість елементарних емоцій. Більшість з них лагідні, доброзичливі. Деякі проявляють позитивні емоції до дорослих, контактують з ними, деякі – переважно до тих людей, з якими вони постійно спілкуються. Позитивні емоції спостерігаються частіше, ніж негативні. Коли в них щось не виходить, вони не засмучуються. Їм властиві страх, радість, сум. Звичайно, емоційні реакції за силою не відповідають причині, що їх викликала. Частіше вони виражені недостатньо яскраво, хоча зустрічаються і занадто сильні переживання з незначної причини.
Труднощі в освоєнні мови у дітей з синдромом Дауна пов'язані з частими інфекційними захворюваннями середнього вуха, зниженням гостроти слуху, зниженим м'язовим тонусом, маленькою порожниною рота, затримкою в інтелектуальному розвитку. Крім того, у дітей з синдромом Дауна маленькі та вузькі вушні канали. Все це негативно впливає на слухове сприйняття і уміння слухати, тобто чути послідовні узгоджені звуки навколишнього середовища, концентрувати на них увагу і впізнавати їх.
За офіційною статистикою, в Україні проживає близько 15 тисяч людей із даним синдромом, з них майже 8 тисяч – діти. Проблема хромосомних захворювань щодня стає дедалі актуальнішою. Численні дослідження свідчать про наступне співвідношення віку матерів та частоти народження дітей з СД: 15–19 років — 1 випадок на 2300 народжень; від 20 до 24 років — 1 на 1600; 25–29 років — 1 на 1200; 30–34 роки — 1 на 870; 35–39 років — 1 на 300; 40–44 роки – 1 на 80; після 45 років цей показник становить 1 випадок на 45 народжень. Ці цифри показують динаміку зростання частоти синдрому Дауна з віком матері. В той же час вік батька не впливає на частоту вказаної патології. За даними Всесвітньої організації охорони здоров’я, з синдромом Дауна народжується одне з 700–1000 немовлят. В Україні щороку народжуються понад 400 дітей із цією генетичною аномалією (у 2012 році — 445 дітей).
У державі поки що не відпрацьована методика, системна модель підтримки та професійної допомоги людям з СД та їх сім’ям, тому від чотирьох з п’яти українських немовлят з СД відмовляються батьки у пологовому будинку, бо найчастіше не знають, або мають хибне уявлення про перспективу подальшого розвитку дитини (важка ступінь розумової відсталості, серйозні труднощі в навчанні і т. д.).
Протягом багатьох років у медичній, педагогічній та психологічній науці існувала думка про безнадійність цього діагнозу для подальшого розвитку особистості. Вважалося, що людина із синдромом Дауна нездатна до навчання, а проби лікування даного «генетичного захворювання» були заздалегідь приречені. На сьогоднішній день відомі випадки психолого-педагогічної реабілітації окремих дітей з синдром Дауна, коли в результаті величезних зусиль вони навчалися у звичайних школах, а найбільш наполегливі змогли отримати вищу освіту. У розвинених країнах люди з СД працюють офіціантами, продавцями, асистентами вихователя. Вони будують особисте життя і створюють сім’ї. Це говорить про те, що робота з такими дітьми – справа небезнадійна, але вимагає спеціальних знань і великих душевних та фізичних витрат.
У Сумському обласному центрі соціальної реабілітації дітей-інвалідів (далі Центр), за рік проходять комплексну реабілітацію близько 700 дітей-інвалідів з різними нозологіями, з них 5–6% — діти з СД.
Комплекс послуг для дітей з СД надається за напрямками: когнітивний розвиток, мовленнєвий, соціально-емоційний, фізичний. Психологічна робота є ефективною тому, що вона поєднується з комплексною роботою всіх спеціалістів Центру — вчителів-реабілітологів, логопеда, музичного керівника, фахівця з фізичної реабілітації та батьків. Основною задачею психокорекційної роботи у Центрі з дітьми із СД є корекція їх інтелектуального розвитку, стимуляція емоційно-вольових процесів.
З 2011 року для дітей з СД за сприянням Всеукраїнської благодійної організації «Даун Синдром», у Центрі використовується програма «Дивись і вчись. Мова та читання» — програма занять, розроблена, щоб допомогти малюкам із синдромом Дауна навчитися говорити та читати, в основу якої покладений тридцятирічний досвід роботи з дітьми даної нозології британської вченої С. Баклі.
Сью Баклі наголошує, що експеримент, котрий проводився у різних куточках світу протягом багатьох років, підтверджується існуванням певних труднощів, котрі проходять діти з синдромом Дауна у процесі розвитку мови, якщо вони сприймають мову лише на слух, а затримка у даній області, у свою чергу, призводить до затримки розвитку пізнавальної діяльності.
Досвід Міжнародного фонду сприяння навчанню дітей з синдромом Дауна запевняє у правомірності гіпотези, що одним із сильних засобів допомоги дітям даної категорії у попередженні мовних та когнітивних труднощів може стати читання.
В експерименті, котрий проводився в кінці 1990-х років у Портсмутському університеті (Англія) і продовжувався 3 роки, приймали участь 18 дітей з СД і 17 типово розвинених дітей у віці від 2 до 4 років, з ними займалися спеціалісти та батьки за програмою Сью Баклі. У перший рік обидві групи розвивалися з однаковою швидкістю. Через 6 місяців середній об’єм словника у дітей з нормою складав 15 слів, у дітей з СД — 17. Різниця в успішності між групами була значною (були діти, котрі не засвоювали жодного слова, а деякі навчилися читати 66 з 70 слів). До третього року навчання, коли середній вік становив 6–7 років і діти з нормою у розвитку навчалися у загальноосвітній школі, показники успішності по читанню і розуміння прочитаного були близькими в обох групах.
Ці дані підтвердили припущення, що здатність до читання – сильна сторона дітей з СД і в багатьох з них рівень розвитку зорової диференціації і зорової пам’яті, необхідний для оволодіння глобальним читанням, відповідає віку.
Експериментальні дані показали, що через три роки від початку експерименту ті діти з СД, котрі навчалися читати за Програмою, у мовному відношенні випередили тих, кого не навчали читати на 8 місяців у розвитку експресивної мови і на 11 місяців у розумінні мови.
Але не всі діти з СД з експериментальної групи до 6–7 років навчилися читати (лише 11 з 18, тобто 61%, а з 17 типово розвинених навчилися читати 16). Чому не навчилися решта? У авторів Програми немає даних і вони не можуть пояснити це явище, оскільки відсутні надійні дані, скільки часу займалися батьки з дітьми (за Програмою рекомендовано займатися по 15–20 хв. щодня).
З висновку експерименту, діти з СД можуть вчитися читати написані тексти друкованими літерами так успішно, як і діти з нормою у рівні розвитку того ж віку. Отримані докази того, що прогрес в читанні позитивно відображається на швидкості розвитку мови, включаючи експресивну мову.
Важливо починати навчання читанню досить рано, до 3 років. Це забезпечує можливість сильно впливати на мовний розвиток, оскільки період від 2 до 7 років є часом максимальної готовності мозку до розвитку мови, а особливо до таких її аспектів як граматика та фонетика.
Апробація програми запевнила її авторів у тому, що вона дозволяє, по-перше, досягти постійних досягнень у розвитку мови дітей з СД, а по-друге, отримати великий об’єм інформація про словниковий запас і граматичний устрій мови таких дітей.
За кордоном два аспекти мовного розвитку розглядаються по-різному. До розвитку мови відносяться запас та активне використання словника (лексичний запас), а також формування граматичного устрою мови. Під розвитком мови розуміють постановку правильної та чіткої звуковимови і розвиток фонематичного слуху; слуху (уміння називати і диференціювати фонеми).
Для всіх дітей розвиток – це процес росту та освоєння нових знань і умінь. З кожним днем, з кожним тижнем зростає їх досвід відносин з оточенням, і вони починають цей досвід усвідомлювати. Найважливіший досвід в житті маленьких дітей – контакт з людьми, яких вони бачать, чують, відчувають, грають з ними. Не дивно, що більшість дитячих реакцій соціальні, тому що вони посміхаються і встановлюють контакт очима при соціальній взаємодії з дорослими. У цих ранніх взаємодіях вони поступово вчаться спілкуватися; вони белькочуть, а потім слухають і навчаються переконувати іншу людину відповісти. Вони також навчаються інтерпретувати почуття інших людей, наприклад, задоволення, гнів, смуток, які супроводжуються відповідними виразами обличчя, жестами і тоном голосу. Це початок соціального навчання. Незважаючи на те, що діти з СД можуть трохи пізніше почати посміхатися, встановлювати контакт очима, їх розвиток у перший рік життя в цілому не відрізняється від звичайного. Вони виявляють інтерес до людей, соціально чуйні і сприйнятливі, і ця тенденція гарного соціального та емоційного розвитку та гарного розвитку невербальних навичок спілкування зазвичай зберігається і у наступні роки.
Програма Сью Баклі «Дивись і вчись» становить собою низку практичних ресурсів для сприяння освіті та розвитку дітей з СД, а також інших осіб із візуальним сприйняттям інформації, та надає чіткі, покрокові вказівки для розвитку конкретних умінь, а також передбачає початок корекційно-розвивальної роботи з дитиною раннього віку. Саме від цього залежить ефективність та результативність реабілітаційного впливу. Програма призначена для закріплення та доповнення розвитку мови, який відбувається засобами повсякденного спілкування дитини через ігрову діяльність.
Програма Сью Баклі «Дивись і вчись: Мова та читання» – це покрокова, структурована програма раннього навчання мові, вона включає 4 книги, кожна з яких охоплює певну сферу розвитку та сприяє формуванню двох ключових мовних сфер:
- розвитку словникового запасу (кількість слів, які знає малюк);
- формуванню граматичних навичок (знання та вміння поєднувати ці слова у речення).
А перш ніж діти з СД навчаться користуватися словами для спілкування, вони повинні навчитися розуміти їх. Для того, щоб почати розуміти значення слів, у дітей є можливість чути ці слова на заняттях у штучно створених ситуаціях, в яких вони можуть зрозуміти їхнє значення або за діями близьких людей. Тому не дивно, що перші 100 слів, які починають вимовляти різні діти, дуже схожі, і це ті слова, які найбільш часто вживаються в контексті сімейного життя, слова, які називають знайомі предмети, дії і людей. Навчання мови – непросте завдання, вирішення якої, зокрема, залежить від наявності хорошого слуху, оскільки більшість дітей навчаються говорити своєю рідною мовою, слухаючи тих, хто в їх середовищі розмовляє нею. Діти з синдромом Дауна навчаються розуміти ті ж самі перші слова, що й інші діти, але це, як правило, відбувається пізніше.
Впровадження програми Сью Баклі «Дивись і вчись: Мова та читання», у Центрі, де розширюються можливості корекційної роботи з дітьми даної нозології, дає можливість продуктивніше співпрацювати спеціалістам Центру з батьками як у межах установи, так і вдома (у містах, області чи віддалених районах сільської місцевості кожен батько сам може виготовити матеріал для заняття).
Слід відзначити позитивні моменти, які від самого початку допомогли працювати з даним дидактичним матеріалом:
- Чітко структурований матеріал та яскраві картинки дозволяють задіяти їхні сильні сторони, стимулюють цікавість, увагу, мовлення.
- Чітко сформульовані інструкції та щоденники спостереження за діяльність дітей дають можливість батькам відслідковувати позитивну динаміку розвитку.
- Методика дає можливість вести записи, що може дитина:
- розуміти слово;
- показати слово жестом;
- вживати слово (імітація);
- використати слово спонтанно;
- вимовити слово достатньо чітко, щоб його зрозуміли.
- Проводиться підготовка до навчання читанню, розвиваючи навички візуального сприйняття через використання певних вправ.
- Програма пропонує діяльність, якою можна займатися регулярно вдома.
- Матеріали програми доступні на сайті ВБО «Даун Синдром» www. downsyndrome.org.ua.
Для заняття можна вибрати будь-який час, який вважається кращим і для того, хто буде проводити заняття, і для дитини (наприклад, коли дитина ще не надто втомлена).
Якщо для дитини цей вид вправ є новим, заняття можуть тривати кілька хвилин. Головне, щоб дитина не втратила зацікавленості. Поступово слід збільшувати тривалість кожного заняття. Проте, завжди завершувати його на позитивній ноті. Обов’язково потрібно стежити за дитиною та звертати увагу на ознаки того, коли вона вже починає втрачати інтерес до заняття. Найкращий принцип для заохочення успіхів, – проводити заняття недовго, але часто. В ідеальному варіанті це має бути щодня.
Адаптуючи закордонну методику реабілітації дітей з синдромом Дауна в умовах Центру, використовуючи її в поєднанні з різними навчальними засобами (іграшковими тваринами, книгами, розрізними картинками, фотоматеріалами і т. д.), забезпечується крок за кроком розвиток дитини.
Коли ж можна починати проводити з дитиною спеціальні навчальні заняття? С. Баклі зазначає, що перший крок методики «Дивись і вчись: малюнки до перших слів» можна розпочати тільки тоді, коли дитина навчилася виконувати прості прохання дорослого у побутових ситуаціях та виявляє цікавість до розглядання фотографій, ілюстрацій у книжці.
Пропонується така послідовність використання вправ:
- роздивляємося малюнки;
- підбираємо парні малюнки;
- вибираємо малюнки;
- називаємо малюнки.
Заняття за даною програмою бажано б проводити у добре освітленому, тихому кабінеті. Щоб у полі зору дитини не було багато предметів, які б її більше приваблювали. Сідати потрібно напроти дитини за столом, чи на підлозі, у залежності від того, що буде кращим для неї, на однаковому рівні, щоб дитина могла добре бачити педагога (батька).
Інколи, а особливо на перших заняттях за програмою, дитині нецікаво грати лише з малюнками. Площинні малюнки не завжди дають змогу зрозуміти дітям призначення зображувальних предметів Зважаючи на те, що основна діяльність дітей з СД – маніпуляція, у Центрі реабілітації зібрано колекцію іграшок до методики «Дивись і вчись. Мова та читання», відповідно до зображень на картках, щоб показувати їх разом з малюнками.
Програма «Дивись і вчись. Мова та читання» не містить матеріалів щодо власного імені дитини, або до слів «мама», «тато»… С. Баклі рекомендує створити власні матеріали для того, щоб навчити дитину читати і вимовляти своє ім’я та інші слова, які використовуються у родині. Такий матеріал зручно зберігати у вигляді особистої книжки, в якій для кращої концентрації уваги на одному розвороті розміщена тільки одна фотокартка. Фотокартки підбираються за темами: «Ранок», «Готуюсь до сну», «Магазин», «Розпорядок дня» (можна оформити як особисту книжку, або як серію магнітиків на холодильнику).
Наведемо приклад особистої книжки з теми «Сім’я», в якій розміщуємо фотокартки близьких людей: мами, тата, дитини, бабусі, дідуся, братиків чи сестричок і спільна. Внизу під кожною фотографією друкованими літерами підписуємо: мама, тато, ім’я дитини, ще нижче «Я» (усвідомлення себе як особистості з’явиться пізніше, дитина зможе про себе сказати «я» не раніше 3-х років). Взявши книжку до рук, починаємо працювати:
— Тобі дати цю книгу, так? (Супроводжуємо «так» жестом: кивком голови. Чекаємо відповіді дитини. Даємо книгу).
— Відкрий книгу (допомагаємо відкрити книгу на першій сторінці).
— Подивись, де мама? (вказуємо своїм пальцем на фото мами).
— Покажи маму (допомагаємо показати маму).
— Мама! Ти показав маму.
А згодом ми запитаємо:
— Це мама, так ? (чекаємо відповіді дитини).
— Це мама? (чекаємо відповіді дитини).
А згодом ми запитаємо:
— Хто це? Якщо дитина засвоїла дане слово, таку ж послідовність дій пропонуємо дитині і з іншою фотокарткою.
Необхідно ретельно продумувати емоційне забарвлення заняття, щоб стимулювати бажання дитини вимовити слово спочатку разом з педагогом, потім віддзеркалено і, нарешті, самостійно.
Питання формулюємо так, щоб з них було зрозуміло, що той, хто запитує, чекає відповіді. Згодом уникаємо питань, які потребують коротких відповідей: «так», «ні». Не забуватимемо змінювати питання, щоб у дитини не склалося враження, що розмова – це відповідь на питання: «Що це?».
Коли діти вже накопичили словничок із 50 слів, вони починають поєднувати два слова разом у словосполучення: «киця спить», «ляля їсть».
У наступній власній книжці дитина «колекціонуватиме» цікаві події – це не тільки розвиватиме її, але й згуртовуватиме родину. І хоча з віком чіткість спогадів втрачатиметься, у пам'яті залишатиметься атмосфера радості й любові, що панувала тоді.
Фахівцями установи успішно застосовується нова цікава, сучасна методика С. Баклі «Дивись і вчись. Мовлення», «Дивись і вчись. Читання». У 2013 році заняття за цією методикою відвідало 22 дитини з СД. У них чітко прослідковується позитивна динаміка розвитку: розширився пасивний словник, навчилися співвідносили назву предмета з видом, розвивалося зв'язне мовлення, діти почали сприймати структуру заняття, виконувати словесні інструкції середнього ступеня складності, у спілкуванні проявляти ініціативу, звертатися до дорослих, засвоювати навички самообслуговування, розвивати другий мовний рівень розвитку (мовлення за допомогою нескладних речень).
Запам’ятайте, для того, щоб дитині було цікаво вчитися, використовуйте якнайбільше різноманітних дидактичних матеріалів. Діти із СД у будь-якому віці легше запам’ятовують те, що вони бачать, а не те, що чують.
Детальніше