 Резюме
Резюме
В Германии в начале 70-х годов были реализованы два проекта, связанные с внедрением компьютерных систем в рамках цитологического скрининга рака шейки матки. Однако вскоре выяснилось, что при автоматизированной системе оценки клеточного материала цитологические препараты должны отвечать определенным критериям: изолированное, в одном оптическом поле (монослое) размещение клеток в препарате, высокая контрастность между ядрами, цитоплазмой и фоном, «четкий и чистый» фон. «Традиционный» Пап-тест не соответствовал этим требованиям.
 Проблема была решена путем внедрения препарата изолированных клеток (монодисперсии), сепарации и очищения клеток. В результате появилась жидкостная цитология (liquid based cytology, LBC). В настоящее время в Германии используются три LBC-системы: ThinPrep®, SurePath® и метод PapSpin®. Основное различие между LBC-препаратами и традиционными Пап-мазками – чистый фон, который обеспечивает LBC, что помогает адекватно идентифицировать и интерпретировать патологически измененные клетки. Имеющийся опыт свидетельствует, что жидкостные цитологические методы обладают рядом преимуществ (табл. 1) по сравнению с традиционными техниками приготовления препарата:
Проблема была решена путем внедрения препарата изолированных клеток (монодисперсии), сепарации и очищения клеток. В результате появилась жидкостная цитология (liquid based cytology, LBC). В настоящее время в Германии используются три LBC-системы: ThinPrep®, SurePath® и метод PapSpin®. Основное различие между LBC-препаратами и традиционными Пап-мазками – чистый фон, который обеспечивает LBC, что помогает адекватно идентифицировать и интерпретировать патологически измененные клетки. Имеющийся опыт свидетельствует, что жидкостные цитологические методы обладают рядом преимуществ (табл. 1) по сравнению с традиционными техниками приготовления препарата:
а) сокращением количества неадекватных образцов,
б) повышением чувствительности,
в) возможностью сокращения времени для интерпретации образца.
В настоящее время в США 98% Пап-тестов основаны на методе жидкостной цитологии. Метод LBC имеет огромную популярность среди цитологов США, что убедительно подтвердил директор отделения цитопатологии университета Вермонта (США), который пожаловался на то, что он «сыт по горло» анализом плохо сохраненных образцов, высушенных на воздухе, с пятнами крови на предметных стеклах. Тем более, что эти проблемы могут быть полностью устранены с помощью LBC.
Введение
В 1943 году Папаниколау (Papanicolaou) и Траут (Traut) опубликовали знаменитую монографию о цитологическом исследовании эпителия влагалища как методе скрининга рака шейки матки. Технология забора клеток эпителия шейки матки, нанесения их на предметное стекло с последующей фиксацией, окрашиванием и микроскопической оценкой с тех пор существенно не изменилась. Способ хорошо себя зарекомендовал и привел в конечном результате к уменьшению количества диагностики карцином шейки матки в Германии. Тем не менее, основной проблемой цитологического скрининга с помощью Пап-теста было получение значительного количества ложноотрицательных результатов. На основании мета-анализов предполагается, что частота ложноотрицательных результатов в мире составляет примерно 50% (Nanda et al., 2000). Такая низкая чувствительность метода может быть компенсирована путем регулярного участия женщин в скрининге. Возможные причины ложноотрицательных результатов цитологии приведены в таблице 2.
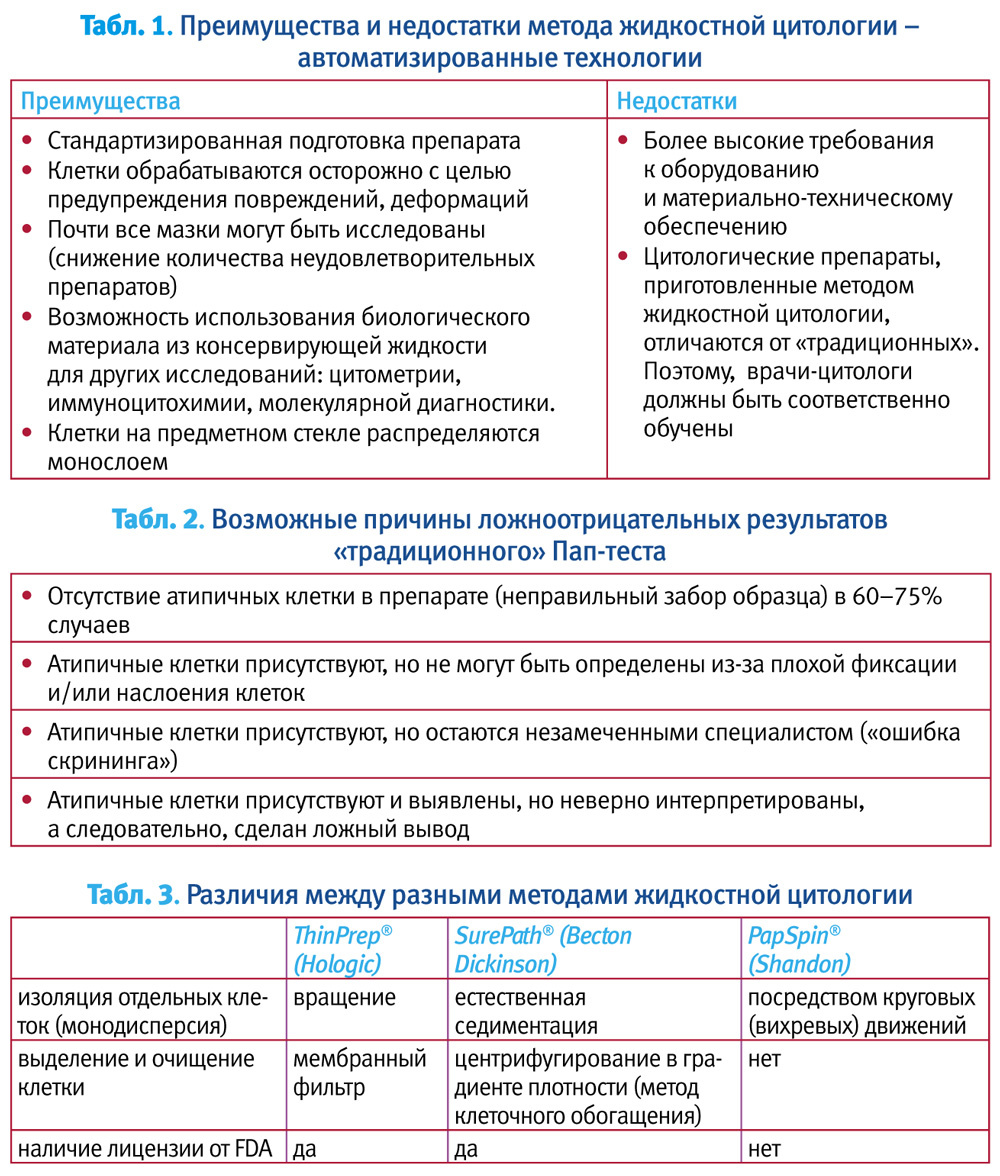
При традиционном Пап-тесте сложно стандартизировать подготовительные этапы, особенно перенос клеток на предметное стекло и их фиксацию. В результате подготовленные препараты показывают различную картинку (рис. 1).
Метод жидкостной цитологии с помощью автоматизированных технологий решает проблему стандартизации переноса клеток на предметное стекло, их фиксацию и окрашивание.
Системы жидкостной цитологии
В настоящее время в Германии доступны три системы жидкостной цитологии: ThinPrep® (Hologic), BD SurePathTM PapTest (Becton Dickinson) и PapSpin® (ThermoShandon). Основные отличия между системами показаны в таблице 3.
Процедура забора образца клеток практически одинакова для всех автоматизированных технологий (ThinPrep®, SurePath®): после забора клеточного материала щеточкой ее рабочая часть отделяется и помещается в контейнер с жидкостью. Состав жидкостей запатентован и является буферной средой с низким содержанием спирта (метанола), что соответствует требованиям как к транспортной, так и фиксирующей среде для клеток.
Цели жидкостной цитологии
- Использование полученного клеточного материала в полном объеме для цитологического исследования.
- Повышение качества препарата, частично из-за устранения элементов распада (например, воспалительных клеток, слизи, фибрина).
- Оптимизация визуального морфологического анализа на основе более качественной подачи материала.
- Соответствие препарата критериям для компьютерного анализа клеточного материала.
- Использование биологического материала для дальнейших морфологических и неморфологических исследований.
Изготовление цитологических препаратов методом жидкостной цитологии
Технология SurePath® (Becton Dickinson)
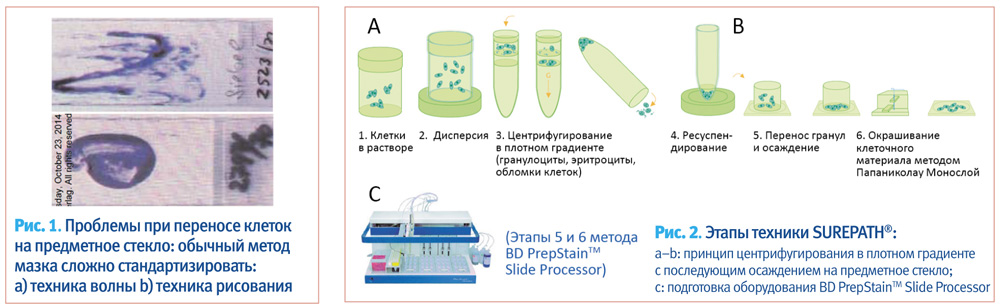
Даная система основана на центрифугировании в плотном градиенте (рис. 2) – методе «клеточного обогащения». Контейнеры с образцами сначала перемешивают с помощью специального шейкера, что приводит к изоляции отдельных клеток. Далее часть пробы помещают в центрифужную пробирку для центрифугирования в градиенте плотности. В данном процессе клетки разделяются в зависимости от их веса. Гранулоциты, эритроциты и обломки клеток, которые имеют более низкий удельный вес, чем эпителиальные клетки, накапливаются выше градиента плотности, а затем удаляются аспиратором. Между тем, осевшие формы содержат популяцию клеток, «идеальную» для диагностики; осадок переносится в камеру для осаждения, которая установлена на предметном стекле. На предметном стекле клетки оседают в тонких слоях, а остаток жидкости удаляют. Окрашивание клеточного материала по Папаниколау является неотъемлемой частью автоматизированного процесса.
За и против: «лицензированные методы» против «нелицензированных»
Методы, которые не регламентированы FDA (PapSpin® среди прочих), не включают в себя основные этапы стандартизированной подготовки, в частности выделение клеток и их очищение, поэтому подготовленный препарат по-прежнему содержит воспалительные клетки, кровь, фибрин и детрит, что усложняет его интерпретацию.
Выделение и очищение клеток методом технологий ThinPrep® Pap-test (Hologic) и SurePath® Pap-test (Becton Dickinson) обеспечивает получение диагностически релевантного препарата. С помощью технологий центрифугирования, при которых предварительное выделение и очищение клеток затруднительно, возможно получение только скопления случайно релевантных клеток.
Жидкостная цитология в качестве платформы для молекулярного Пап-теста – возможность экономии затрат на здравоохранение?
Кроме получения ложноотрицательных цитологических результатов, возможны ложноположительные цитологические находки, что является причиной низкой прогностической ценности (positive predictive value, PPV) положительного цитологического исследования. Согласно данным литературы, PPV атипичных результатов цитологического исследования составляет от 11,4% (Petry et al. 2003; Ronco et al. 2006) до 70,6% (Schneider, 2000) по отношению к гистологическому диагнозу «цервикальная интраэпителиальная неоплазия II стадии».
Одной из главных мер, принятых для повышения PPV, является ВПЧ-сортировка атипичных цитологических находок. При одновременном проведении генотипирования ВПЧ можно достичь PPV, равной 88,2%, для цервикальной дисплазии и карциномы средней и высокой степени (≥ цервикальной интраэпителиальной неоплазии II) (Bollmann и др., 2007). Такой многомодальный риск-адаптированный скрининг рака шейки матки позволяет избежать ненужного хирургического вмешательства и экономит затраты.
Критерии, согласно которым метод жидкостной цитологии (SurePath®BD) был регламентирован FDA:
- утвержден в качестве альтернативы обычному Пап-тесту (1999);
- одобрен как более эффективный метод (+64,4%) для выявления поражений средней и тяжелой степени по сравнению с обычным Пап-тестом (2003);
- фокусная точечная система (Focal Point System) одобрена для первичного скрининга цитологических препаратов (25% препаратов система идентифицирует как «без патологических изменений», таким образом, не требуя «дальнейшего пересмотра»).
В настоящее время для PapSpin® и других тонкопленочных методов лицензирование не проводилось.
Повышение производительности
Английское пилотное исследование показало повышение скрининга на 9% при использовании препаратов методом жидкостной цитологии с использованием автоматизированных технологий. Количество неудовлетворительных препаратов снизилось с 9,1% (обычная цитология) до 1,6% (жидкостная цитология) (Moss и др. 2002). Этот процент еще выше при сочетании с компьютерными методами (Wilbur et al., 1998; Davey et al., 2007).
Список литературы находится в редакции.
* Статья опубликована в журнале Gynakol Geburtsmed Gynakol Endokrinol 2008; 4(2): 164–180. REINHARD BOLLMANN, Институт патологии Бонн-Дуйсдорфа, Бонн, Германия. С полной версией статьи можно ознакомиться по ссылке: http://gyn.akademos.de/pdfdown/akademos-cme-130-0f4cefbe.pdf

коментарів