
ЗАМЕТКИ ПРАКТИКА
 Журнал «З турботою про Жінку» пригласил зав. отделением онкогинекологии Киевского городского клинического онкологического центра, к. мед. н., главного консультанта по онкогинекологии ГОЗ г. Киева, ассистента кафедры онкогинекологиии НМУ им. А. А. Богомольца Елену Петровну Манжуру поговорить о трудностях диагностики, возможностях лечения и необходимости профилактики рака шейки матки
Журнал «З турботою про Жінку» пригласил зав. отделением онкогинекологии Киевского городского клинического онкологического центра, к. мед. н., главного консультанта по онкогинекологии ГОЗ г. Киева, ассистента кафедры онкогинекологиии НМУ им. А. А. Богомольца Елену Петровну Манжуру поговорить о трудностях диагностики, возможностях лечения и необходимости профилактики рака шейки матки
– Елена Петровна, почему, по Вашему мнению, проблема патологии шейки матки сохраняет актуальность сегодня?
Елена Манжура: Эта проблема актуальна, поскольку, во-первых, заболеваемость неуклонно растет. Кроме всего прочего, рак шейки матки очень помолодел (РШМ). Все это заставляет врачей-онкологов, онкогинекологов бить тревогу. Более того, в причинах смерти молодых женщин (от 18 до 29 лет), среди всей онкологической заболеваемости, рак шейки матки стоит на втором месте после лейкемии. Опасность заключается в том, что заболевание не имеет специфических симптомов, а отсутствие культуры ежегодного скрининга приводит к диагностике на поздней стадии.
– Традиционно считается, что ведущим фактором РШМ является вирус папилломы человека. Насколько такое утверждение правомерно сегодня?
Е. М.: Безусловно, ВПЧ – ключевой этиологический фактор РШМ. Хотя, любые инфекции, которыми может быть поражена женщина длительное время, могут вызвать рак шейки матки (по теории Вирхова). Но, если с бактериями мы научились справляться и у нас есть для этого надежные препараты – антибактериальные лекарственные средства, то против ВПЧ специфических средств нет. Коварство вируса еще в том, что он постоянно мутирует. Поэтому мы не можем медикаментозно контролировать вирус, как это происходит в случае бактериальной инфекции. Именно поэтому ВПЧ играет основную роль в возникновении рака шейки матки. Представляют особенную опасность и ускоряют прогрессию процесса антибиотико-вирусные ассоциации.
Какова ситуация в Украине с ВПЧ-ассоциированными заболеваниями? Есть существенные различия по сравнению со статистическими данными других стран (Европы, США прочее)?
– Ситуация с этой группой заболеваний в Украине примерно такая, как и во всем мире. Сюда относится, в том числе, и папилломатоз гортани у новорожденных. Если женщина – носитель ВПЧ, и у нее есть яркие проявления в виде вирусных кандилом, то рожать естественным путем ей нежелательно. Лучше такой женщине выполнить кесарево сечение, для того, чтобы избежать впоследствии инфицирования плода. Папилломавирусная инфекция – это нередкое заболевание, вирусом поражено до 80% населения. Но существует очень много штаммов вируса папилломы человека, среди которых есть высоко- и низкоонкогенные. Например, папиломы на коже могут быть вызваны доброкачественными серотипами ВПЧ.
– Какие современные методы диагностики одобрены и рекомендуются ведущими мировыми медицинскими организациями?
Какие применяете Вы? Какие из них считаете наиболее точными и информативными?
Е. М.: Наиболее точным и информативным методом на сегодня является цитологическое исследование – мазок по Папаниколау, жидкостная цитология и ВПЧ-тестирование. Именно их используют в качестве скрининговых методов. Но, безусловно, мы должны не забывать о специальных методиках – кольпоскопии, прицельной биопсии и цервикальном кюретаже.
– Елена Петровна, как Вы считаете, достачно ли одного скрининга, если мы говорим об отдельно взятой пациентке? Современный вектор на профилактическую медицину предусматривает скрининговое выявление пациентов высокого риска того или иного заболевания. Существует ли сегодня доступный и простой способ скрининга РШМ и предраковых состояний шейки матки?
Е. М.: Скрининг, если он организован правильно, – это современный метод выявления онко- или других заболеваний в популяции. Это по сути, раннее выявление предопухолевой патологии или начального неинвазивного рака. Для того, чтобы охватить все население простым и недорогим методом исследования, достаточно одного цитологического исследования.
Но вот, если в образце выявлена патология эпителия, тогда женщину нужно дообследовать более тщательно. Провести ВПЧ-тестирование. Если тест покажет наличие высокоонкогенного штамма ВПЧ, обязательно необходимо повторить цитологический мазок по Папаниколау, чтобы хорошо рассмотреть, внедрился ли этот вирус в клетки или нет, поскольку тест на вирус нам покажет только факт присутствия вируса в организме, но к каким последствиям он привел, мы не узнаем без более глубокого исследования.
Доступным и простым, неинвазивным исследованием является кольпоскопия. Если говорить о скрининге в нашей стране, то пока что, к сожалению, нет государственных программ, и мы должны рассчитывать на личную ответственность каждой женщины по отношению к своему здоровью.
– Вы говорили об омоложении рака шейки матки, с чем это связано, по Вашему мнению?
Е. М.: Во-первых, это связано с несоблюдением культуры половой жизни. Во-вторых, в популяции большое количество инфицированного населения. Молодые люди забывают об использовании простых барьерных методов – презервативов. А так как в нашем обществе, к сожалению, нет культуры профилактических осмотров, молодые девушки приходят уже с тяжелыми дисплазиями шейки матки и даже с инвазивным раком шейки матки. Речь идет об очень молодом возрасте — 22–23 года!
– Насколько часто сегодня врачи ставят диагноз «эрозия шейки матки»?
Е. М.: Раньше этот диагноз, действительно, был очень распространенным, но процент истинных эрозий очень невысок. На самом деле, имеется ввиду эктопия шейки матки (эктопия цилиндрического эпителия). Сейчас употреблять термин «эрозия» не вполне корректно, поскольку настоящая эрозия – это когда на подслизистом слое нет эпителия. Другими словами, если есть эпителий шейки матки, то это уже не эрозия, а эктопия.
– Что Вы думаете о вакцинации против ВПЧ? Когда и кому она показана? Безопасна ли такая вакцинация?
Е. М.: В рекомендациях по вакцинации говорится о том, что ее необходимо провести до первого контакта с вирусом – возбудителем заболевания. Другими словами, до начала половой жизни. Но даже, если у девушки уже живущей половой жизнью, или у рожавшей женщины, есть, к примеру, рецидивирующая дисплазия, связанная с наличием ВПЧ-инфекции, есть смысл ее вакцинировать для предупреждения рецидива этой дисплазии, но только после проведения курса лечебных мероприятий. Что касается безопасности, как любой лекарственный препарат, вакцина может вызывать побочные реакции, от этого никто не застрахован. Но, в то же время, процент этих осложнений очень низкий, поскольку культуры вируса в вакцине нет. Кроме того, на сегодня нет лекарственных средств от ВПЧ. Я придерживаюсь мнения, которое разделяют и мои коллеги – онкогинекологи и онкологи, что вакцинация как профилактика имеет смысл, ведь мы никак иначе не можем влиять на вирус. Но, если женщина уже заболела, и вирус ВПЧ вызывает в ее организме патологические изменения в эпителии, внедряясь в клетку, справиться с этим уже очень сложно. Только следует помнить, что однократная вакцинация не дает пожизненного иммунитета, для получения напряженного иммунитета необходимы курсы ревакцинации.
– Расскажите, пожалуйста, об особенностях ведения беременности, если у женщины выявлена патология ШМ?
Е. М.: Если у женщины выявлена ВПЧ-ассоциированная патология шейки матки во время беременности, то основная тактика – наблюдение, но если цитологически подтверждена тяжелая дисплазия (или даже начальный рак), такая пациентка наблюдается акушерами-гинекологами совместно с онкогинекологами и именно онкогинекологи дают рекомендации о пролонгировании этой беременности или ее прерывании. Поэтому, женщинам необходимо обследоваться перед планируемой беременностью. Вообще, каждая женщина должна помнить, что раз в год необходимо посещать гинеколога. Тогда проблем подобного рода не будет.
– Какие современные методы лечения ВПЧ-ассоциированных заболеваний Вы используете в своей практике?
Е. М.: Как я уже говорила, нет лекарственных средств, непосредственно влияющих на вирус. Но наша иммунная система, к счастью, может сама с ним справиться. И первое, что я рекомендую, – это укрепление иммунной системы, для того, чтобы вирус покинул организм человека. Здесь хороши все методы: и здоровое питание, и режим труда и отдыха, и культура половой жизни, о которой мы уже говорили. В группе риска оказываются молодые люди, как раз по той причине, что они не соблюдают таких простых рекомендаций. Поэтому очень важно объяснять, что, для того, чтобы иммунная система функционировала нормально, в рационе питания должны быть сухофрукты, орехи, рыба. Тогда Т-лимфоцитам будет из чего черпать ресурсы для борьбы с болезнями, в том числе вызванными вирусами. Но, если вирус папилломы человека уже вызвал необратимые изменения в организме (к примеру, на коже – папилломы, бородавки, на шейке матки – тяжелая дисплазия), то, конечно, речь будет идти и о хирургическом лечении, и неспецифической противовирусной терапии. Одним из самых радикальных методов является электроэксцизия. В любом случае, и папилломы, и очаги дисплазии нужно удалять. Не следует пренебрегать этапом реабилитации после хирургического лечения, т. к. именно этот период – залог успешности противорецидивной профилактики. Мы всегда рекомендуем курс вагинальных средств, ускоряющих регенерацию и эпителизацию. Например, те же свечи Ревитакса – это уникальный состав, т. к. с одной стороны, они безопасны, а с другой – обеспечивают профилактику восходящей инфекции, снимают воспалительную реакцию, стимулируют регенерацию, повышают местный клеточный иммунитет.
– Что делать после того, как женщина прошла курс лечения?
Е. М.: Конечно, это регулярное посещение гинеколога, соблюдение культуры половой жизни (вирус ВПЧ передается только половым путем, поэтому, несколько половых партнеров – в несколько раз более высокий риск заражения), по возможности избегать стрессов, следить за тем, чтобы питание было сбалансированным и качественным. Если после хирургического лечения возник рецидив, то необходимо:
- повтор глубокой диагностики и выявление причин;
- Определяем иммуногистохимические маркеры (онкобелки Е6/Е7; онкобелок р16INK4a, антиген Ki-67). Это нужно для прогнозирования онкологической прогрессии и как инструмент для убеждения пациентки в степени риска развития РШМ («юридическая защита врача»). Кроме того, я считаю, что любой женщине с ВПЧ-ассоциированной патологией шейки матки необходимо обязательное восстановление биоценоза влагалища, усиление иммунитета (иммуномодуляторы), применение методов неспецифической онкопрофилактики (индол-3-карбинол, эпигаллокатехин-3-галлат) в режиме длительного приема – 3–6 месяцев.
Материал подготовила
Александра Загородняя.
Детальніше

Искусство предвидеть
Профи-Лаб «ЗУСТРІЧІ ПРОФЕСІОНАЛІВ: вагітність, пологи, післяпологовий період»
Рекордное количество участников, 400 представителей акушерского сообщества, стали свидетелями ярких, интересных и полезных докладов. Два дня конференции объединяла тема «Предикторы в акушерстве».
Предиктивная медицина все еще находится в начале своего пути. Но уже накоплен достаточный международный опыт, позволяющий строить прогнозы и управлять акушерскими рисками. Отечественные и зарубежные спикеры делились своим опытом и знаниями в этой области.
Активно обсуждались предикторы патологического течения многоплодной беременности, современных подходов к прогнозированию плацентарной дисфункции, группы риска преждевременных родов с позиций доказательной медицины, пуповинные факторы риска гибели плода, предикторы эмболии околоплодными водами, результаты исследования HAPO и многое другое. Большой интерес участников вызвал мастер-класс «Рациональное сопровождение тазового предлежания». Это был действительно праздник единения науки и практики!
Переход от диагностики к прогнозированию акушерских осложнений, а от них к профилактике и строго индивидуальному лечению — вполне обозримые горизонты предиктивного акушерства.


Экстрафетальные стволовые клетки
– Человечество может все. Изумительное развитие науки в течение одного века и еще более изумительные и быстрые успехи ее за последнее двадцатилетие благодаря неслыханным открытиям, преобразовавшим важнейшие наши представления о мире, – это триумфальное шествие человеческого ума открывает человеческой деятельности безграничные просторы.
Р. Роллан
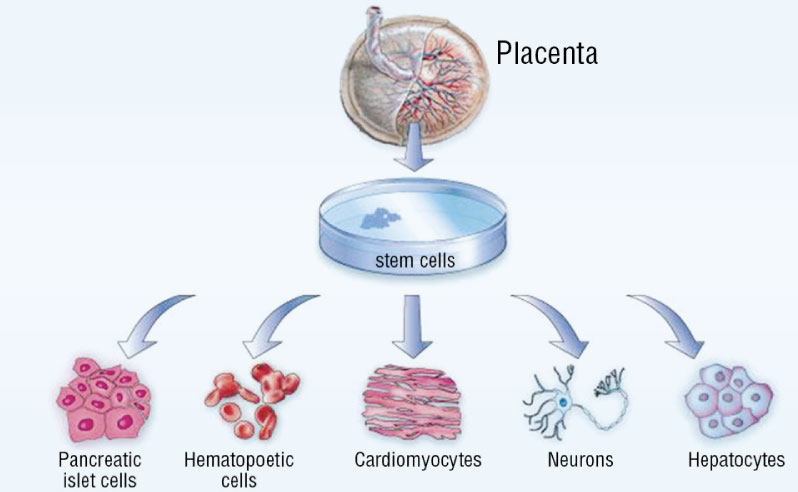
Продолжаем наше знакомство с регенеративной медициной и ее инструментами – стволовыми клетками. В этой статье я намеренно использовал, в общем-то, нестандартное определение для стволовых клеток плаценты, пуповины, амниотической жидкости и плодовых оболочек. Дело в том, что сегодня, особенно в зарубежной научной литературе, эти клетки определяют как фетальные. В принципе неверно! Эти стволовые клетки происходят из экстрафетальных тканей, которые развиваются из трофоэктобласта, а не из внутренней клеточной массы. Трофоэктобласт дает в процессе развития плаценту, пуповину и оболочки плодного яйца, а внутренняя клеточная масса – плод. Это имеет большое значение с этической точки зрения.
Очень важно, что такие стволовые экстрафетальные клетки, как и клетки кордовой (пуповинной) крови, генетически идентичны клеткам плода. И в этом их главное преимущество. Они иммунологически совместимы с их «донором» – новорожденным человечком, которому через много-много лет стволовые клетки, сохраненные его родителями, способны вернуть молодость, или же спасти его от смертельного заболевания…
Мы все давно знаем, что животные после родов поедают свою плаценту, но долгое время не задумывались над простым вопросом – а зачем? После некоторых размышлений пришли к выводу – для усиления лактации. Но только ли для этого?
В 2009 году в журнале ScienceDaily появилась первая статья с робким названием «Placenta: New Source for Harvesting Stem Cells». Не хватало только знака вопроса… К счастью, сегодня научная мысль, благодаря современным технологиям, очень быстро проходит проверку практикой. Оказалось, что плацента содержит не только мезенхимальные стволовые клетки, дающие начало элементам соединительной ткани, но и гемопоэтические клетки… А это значит, что плацента принимает участие в кроветворении плода, несмотря на то, что это – экстрафетальный орган… 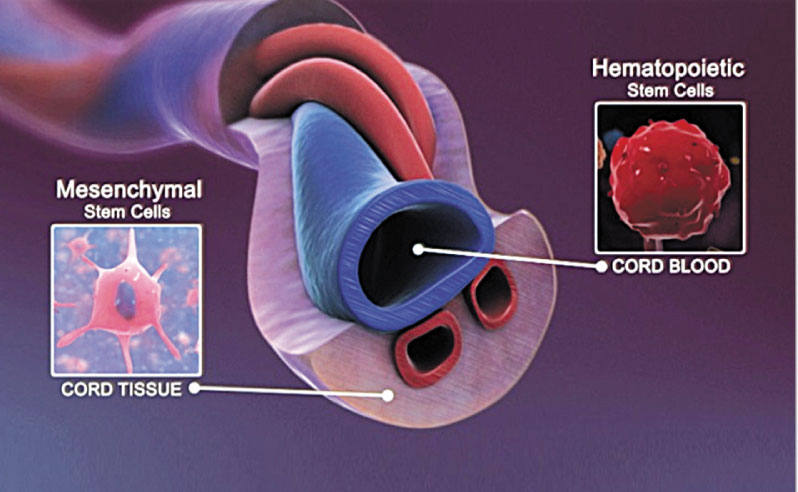
Но оставим пока эту тему для дальнейших научных исследований. Нам важнее понять, что именно из экстрафетального материала, который сегодня просто-напросто утилизируется, важно сохранить для здорового будущего наших детей. Стволовые экстрафетальные клетки способны дифференцироваться в зрелые клетки жизненно важных органов, замещать и восстанавливать функцию поврежденных болезнью тканей.
Всем уже известно о существовании банков кордовой крови. Известно также, что стволовые клетки пуповинной крови были успешно использованы для лечения анемии де Тони–Дебре–Фанкони… Но только ли кордовую кровь следует сохранять?
Оказывается, нет, не только и даже не столько пуповинную кровь, сколько все экстрафетальные ткани. Давайте посмотрим… Плацента – мезенхимальные и гемопоэтические стволовые клетки, амнион и амниотическая жидкость – источники так называемых амниотических эпителиальных клеток, прекрасно заживляющих хронические раны и язвы, хорион – хорионические мезенхимальные стволовые клетки, пуповина (корд) – мезенхимальные стволовые клетки Вартонова геля, кордовая кровь – гемопоэтические стволовые клетки…
Какое богатство человечество веками выбрасывало в мусор! Но на то и существует наука, чтобы мы все больше и глубже познавали сами себя…
Мне могут скептически возразить, что, на сегодня, дескать, клетки этого типа мало кто применяет, и они еще не прошли весь сложный этап доклинического изучения и клинических исследований. Да, это так. Но уже сейчас у нас есть технологии по размножению экстрафетальных стволовых клеток и их эффективному использованию при остеоартритах и анемиях. И это только начало…
Так не лучше ли собрать эти клетки и хранить их для своего ребенка, нежели просто отмахнуться и потерять такую возможность навсегда?
Сразу замечу, я не имею отношения, абсолютно никакого отношения, ни к одному из банков кордовой крови в Украине. Поэтому не стоит рассматривать эту статью как некий рекламный проект…
Это – мое мнение, которое я никому не навязываю…
Детальніше
«ЛАГІДНИЙ» ДІАБЕТ МОЛОДОГО ВІКУ
Гестаційний діабет (ГД) може бути першим проявом цукрового діабету дорослого типу у молодих (діабету типу GCK-MODY 2 – maturity onset diabetes of the young) – моногенного захворювання, спричиненого мутацією гену, відповідального за синтез глюкокінази (GCK)
Це захворювання спричинене мутацією гену глюкокінази, локалізованого на 7 хромосомі. Мутація спричинює дисфункцію бета-острівців підшлункової залози. Вперше описана у 1992 році, вона успадковується домінантно, тому є велика ймовірність успадкування діабету дітьми таких матерів.
На розвиток діабету типу GCK-MODY 2 мало впливають чинники зовнішнього середовища, а особи, в яких підтвердили генетичний дефект, мають 90% ризику захворювання. Це захворювання є найчастішим типом діабету, який діагностують до 35-річного віку. Серед пацієнток із гестаційним діабетом воно трапляється у 2–5% випадків.
Особливістю ГТТ у хворих з діабетом MODY 2 є гіперглікемія натще, водночас рівень глюкози через 2 години після навантаження суттєво нижчий, ніж можна було б сподіватися на основі базального її рівня. Рівень HbA1c буває лише дуже помірно підвищеним, а діабетичний кетоацидоз при цій формі захворювання трапляється вкрай рідко.
Як лікувальні заходи звичайно рекомендують відповідну дієту і стиль життя, а при мутації генів транскрипційних чинників також застосовують препарати сульфонілсечовини.
Незважаючи на легкий перебіг, це захворювання вже через кілька років після свого початку може спричинити тяжкі серцево-судинні ускладнення. Це, зокрема, ішемічна хвороба серця, інфаркт міокарда або інсульт.
Часто, не знаючи результатів генетичних досліджень, до гестаційного діабету ставляться легковажно, а пацієнтка і її дитина не потрапляють своєчасно під опіку діабетолога.
Це неправильно, оскільки своєчасна діагностика розладів вуглеводного метаболізму, які до певного часу характеризуються латентним перебігом, дає змогу запропонувати раціональний алгоритм профілактики та лікування та запобігти серйозним ускладненням цього хронічного захворювання.
У записник клініцисту
Гестаційний діабет може бути першим проявом генетично зумовленого діабету типу GCK-MODY 2 – захворювання, яке незважаючи на легкий перебіг, досить швидко зумовлює серйозні органічні ускладнення. Такого перебігу подій можна сподіватися у 2–5% пацієнток із гестаційним діабетом.
Генетичний характер названого заворювання зобов’язує до ретельного обстеження усіх жінок, які перенесли гестаційний діабет, та їх дітей. Оптимальним є виконання генетичного дослідження, яке дає змогу підтвердити чи заперечити діагноз.
За www.diabetesgenes.org
Детальніше

Холестатический гепатоз беременных: аспекты современной тактики ведения беременности и родов

25–26 сентября в Киеве собрались ведущие специалисты в области акушерства, гинекологии, эндокринной гинекологии, гинекологической хирургии, репродуктологии. Встречи проводились в рамках научно-практической конференции и Пленума общественной организации «Ассоциация акушеров-гинекологов Украины» «Инновационные подходы в акушерстве, гинекологии и репродуктологии», на заседания также были приглашены гости из-за рубежа. Одной из тем, обсуждавшихся в рамках нескольких секционных заседаний, стало применение прогестерона в терапии невынашивания беременности. Во время заседания, посвященного инновациям в акушерстве и гинекологии, шла речь о риске развития холестатического гепатоза на фоне длительного приема некоторых аналогов прогестерона.
 С докладом на тему «Холестатический гепатоз беременных. Аспекты современной тактики» выступил гость из Республики Беларусь, заведующий родовым отделением УЗ «5-я клиническая больница» г. Минска, к. мед. н. Василий Анатольевич Шостак. Начиная доклад, он представил украинской аудитории общую информацию по ведению беременных в соответствии с белорусскими протоколами, среди прочего отметив, что в Белоруссии терапия по сохранению беременности проводится в стационаре с ранних сроков при наличии у женщин каких-либо жалоб. Поводом для проведения клинических исследований, предложенных вниманию украинских коллег, послужил резкий рост частоты холестатического гепатоза у беременных, а также существенных изменений в биохимических анализах крови после протокольной систематизации обследования при диспансерном наблюдении беременных.
С докладом на тему «Холестатический гепатоз беременных. Аспекты современной тактики» выступил гость из Республики Беларусь, заведующий родовым отделением УЗ «5-я клиническая больница» г. Минска, к. мед. н. Василий Анатольевич Шостак. Начиная доклад, он представил украинской аудитории общую информацию по ведению беременных в соответствии с белорусскими протоколами, среди прочего отметив, что в Белоруссии терапия по сохранению беременности проводится в стационаре с ранних сроков при наличии у женщин каких-либо жалоб. Поводом для проведения клинических исследований, предложенных вниманию украинских коллег, послужил резкий рост частоты холестатического гепатоза у беременных, а также существенных изменений в биохимических анализах крови после протокольной систематизации обследования при диспансерном наблюдении беременных.
Докладчик отметил, что традиционно в классическом акушерстве принято относить к группе атипичных гестозов три осложнения беременности: холестатический гепатоз беременных (внутрипеченочный холестаз беременных), острый жировой гепатоз (острая желтая дистрофия печени) и HELLP-синдром. Физиология беременности такова, что при нормальном ее течении увеличиваются уровни холестерина, желчных кислот и щелочной фосфатазы. Причем уровень последней при беременности резко повышается за счет ее выработки плацентой и поэтому изолированно ни в коей мере не может служить маркером развития патологии печени у беременных. Нормальным остается количество в сыворотке крови билирубина и g-глютамилтранспептидазы.
В. А. Шостак отметил, что акушерам-гинекологам необходимо помнить о пяти синдромах повреждения печени (желтуха, холестаз, цитолиз, мезенхимально-воспалительный синдром и синдром печеночной недостаточности) и понимать, какая акушерская патология соответствует каждому из этих синдромов.
Чрезвычайно важным для акушерства является цитолиз (существенное увеличение аланин- и аспартатаминотрансфераз, лактатдегидрогеназы), который свидетельствует о развитии HELLP-синдрома. Синдром печеночной недостаточности соответствует острому жировому гепатозу, холестаз – холестатическому гепатозу беременных (ХГБ). Отсутствие общепринятого толкования последней нозологии предопределило ряд других названий, которые используются в постсоветских странах и по сей день – «желтуха беременных», «поздний гестоз с печеночным синдромом», «гепатопатия беременных», «идиопатическая желтуха беременных», «рецидивирующая семейная желтуха беременных», «генерализированный зуд беременных». При этом ХГБ был впервые описан в 1959 году в Швеции, но наблюдения подобного заболевания у беременных отмечены с конца XIX века. По определению докладчика, ХГБ – это осложнение беременности, характеризующееся нарушением функции печени, желтушной окраской кожи и слизистых оболочек, что обусловлено гипербилирубинемией, и кожным зудом, который обычно предшествует желтухе и обусловлен гиперхолеацидемией. Клинически ХГБ представляет собой зуд с наличием или без желтухи, а лабораторно – холеацидемию и, возможно, гипербилирубинемию.
Говоря об акушерской значимости ХГБ, В. А. Шостак напомнил, что на первом месте среди его осложнений – преждевременные роды и послеродовые маточные кровотечения вследствие нарушения синтеза витамин-К-зависимых факторов свертывания. Важно, что холестаз беременных предрасполагает к развитию желчнокаменной болезни, следовательно, женщинам, имеющим в анамнезе это заболевание, в перспективе противопоказаны пероральные контрацептивы. Частота рецидивов ХГБ при последующих беременностях достигает 50%. Докладчик отметил, что гиперхолестеринемия может быть связана с генетическими факторами, гормональной терапией (до и во время беременности), гипофункцией коры надпочечников; генерализованный зуд, в свою очередь, связан с отложением желчных кислот в подкожной жировой клетчатке; холестаз объясняется изменением соотношения фосфолипидов и белков в мембранах гепатоцитов с нарушением экскреции желчи и липидов. Развитию желтухи способствует функциональная недостаточность печени из-за перенесенных ранее вирусного гепатита и/или других заболеваний печени. Кроме того, предполагается роль генетически повышенной чувствительности к эстрогенам (эстрогены снижают образование и выделение желчи). Установлено, что при холестазе беременных уровень конъюгированных эстрогенов в сыворотке повышен, а экскреция их с желчью и мочой снижена.
Причиной развития холестатического гепатоза также может быть использование гепатотоксичных препаратов до и во время беременности. И если о токсичном влиянии на функцию печени ряда антибиотиков врачи, как правило, хорошо помнят, то о воздействии гормонов акушеры-гинекологи почему-то знают мало. В качестве примера такого влияния докладчик привел информацию о микронизированном прогестероне, который в Республике Беларусь по инструкции к препарату 2011 года (Утрожестан) следовало применять внутрь в дозе 400 мг каждые 6–8 ч. до 36 нед. беременности, то есть до 1600 мг/сут. Однако еще в 1998 г. производитель препарата распространил информационное письмо по всем странам, где использовался данный препарат. В письме, приведенном в докладе, признавая, что имело место развитие холестаза у пациенток, принимавших микронизированный прогестерон перорально в течение ІІ и ІІІ триместров беременности для предотвращения преждевременных родов, производитель предлагал изменения в инструкцию, ограничив суточную дозу 400 мг только интравагинально и срок гестации максимум 12 нед. беременности.
Говоря о клинических критериях холестаза, докладчик напомнил, что это: кожный зуд, значительный и постоянный, вызванный гиперхолеацидемией, а также желтуха, поздняя и незначительная, вызванная гипербилирубинемией. Лабораторно выявляют повышение общего билирубина (не выше 90–100 мкмоль/л), гиперхолеацидемию, повышение g-ГТП, щелочной фосфатазы, но без изменения уровня других ферментов (АлАТ, АсАТ, ЛДГ).
Далее в докладе шла речь о стратегии при ХГБ. Докладчик особо остановился на том, что все беременные с клиникой гастроинтестинального дискомфорта и/или симптомами гестоза/преэклампсии должны быть госпитализированы, обследованы для выявления маркеров НELLP-синдрома, при его верификации – родоразрешены. При верификации холестаза следует пролонгировать беременность до зрелости плода. Акушерская тактика заключается в пролонгировании беременности до 37–38 нед. на фоне лечения холестаза: показаны диетотерапия и применение гепатопротекторов, энтеросорбентов, а также десенсибилизация.
Статья публикуется в сокращении. Полный текст находится в редакции.
По материалам журнала «ЗДОРОВЬЕ ЖЕНЩИНЫ».
Детальніше

ВРОЖДЕННЫЕ АНОМАЛИИ РАЗВИТИЯ МАТКИ ИЛИ МЮЛЛЕРОВЫ АНОМАЛИИ (Обзор литературы, часть 3)
Классификация ESHRE/ESGE 2013г.
Класс IV Двурогая матка
Двурогая матка формируется в результате неполного слияния мюллеровых протоков на уровне дна матки. При этом аномальная нижняя часть матки и шейка имеют полное слияние (объединение) – в результате формируются две отдельные взаимодействующие полости с единым цервикальным каналом и одним влагалищем. Имеется мышечная внутриматочная перегородка с соответствующим наружным углублением (выемкой) в области дна матки. Глубина выемки и длина внутриматочной перегородки у взрослых пациентов полностью коррелируют со степенью неполного слияния мюллеровых протоков у плода [121].
Подклассы двурогих маток зависят от длины перегородки. При полной внутриматочной перегородке имеет место двурогая матка с одной шейкой и двурогая матка с удвоением шейки. Когда перегородка занимает только область дна – неполная (частичная) двурогая матка.
Двурогая матка считается случайным открытием. Не так давно эта врожденная аномалия идентифицирована как нечастый компонент «мягкого» варианта порока уроректальной перегородки [153].
Женщины с двурогой маткой, как правило, имеют определенные репродуктивно-ассоциированные проблемы. Аномалия может не быть идентифицирована вплоть до срока родов.
В большинстве исследований женщин с бесплодием частота встречаемости двурогих маток незначительно отличалась от контрольной группы, соответственно предполагается, что эти пациентки не имеют принципиальных сложностей с зачатием [108]. Примерно 60% пациенток имеют роды жизнеспособным плодом, но также могут иметь место преждевременные роды и самопроизвольный выкидыш позднего срока [154].
Акушерские исходы могут зависеть от длины мышечной перегородки, т. е. является ли «двурогость» полной или частичной. В одной из работ можно видеть следующую статистику среди женщин с неполной двурогой маткой: самопроизвольный аборт – 28%, преждевременные роды – 20%. Эти цифры сильно контрастируют с данными среди женщин с полной двурогой маткой: 66% – уровень самопроизвольных абортов и преждевременных родов [12].
Редки случаи беременности двойней в одном роге двурогой матки (один случай, описывающий такое состояние, закончился досрочным прерыванием беременности в 22 нед. гестации) [155].
Данные литературы, описывающие репродуктивные исходы у женщин с двурогими матками, скудны. В обширном исследовании репродуктивных результатов у пациенток с мюллеровыми аномалиями (Lin et al.) сообщается об анализе 56 беременностей при двурогих матках: 14 (25%) – преждевременные роды, 35 (63%) – живорождений и 14 (25%) – самопроизвольные аборты. Авторы не разделяли двурогие матки на подклассы [112].
Заболеваемость женщин с двурогими матками другими гинекологическими болезнями такая же, как и при отсутствии врожденных отклонений, в т. ч. и раком. Описывается карцинома эндометрия в одном из рогов после лечения тамоксифеном по поводу рака молочной железы [156].
Диагностика
Важным шагом является дифференциальная диагностика двурогой матки и внутриматочной перегородки. Важность точности постановки диагноза обуславливается принципиально разными лечебными подходами. Двурогая матка не требует предварительной хирургической коррекции и ассоциируется с меньшими репродуктивными проблемами. При наличии же внутриматочной перегородки риск репродуктивных отклонений и необходимость хирургического вмешательства выше.
Оценка двурогой матки начинается с проведения УЗИ в лютеиновую фазу, когда М-эхо эндометрия лучше контрастируется. Сонографические работы, основанные на определении угла между рогами, все же не дают возможности точно различить перегородку и двурогую матку. Наружный угол между рогами может достигать >105O. Ткань миометрия, которая разделяет два рога, имеет сигнал такой же интенсивности, что и миометрий [118, 157]. Наружный контур двурогой матки имеет углубление, которое точно контрастируется в сравнении с нормальной маткой или маткой с наличием перегородки, особенно в режиме 3-D исследования [75].
При МРТ-исследовании матки с перегородкой выявляется четкая продольная полная или частичная перегородка, разделяющая полость и имеющая угол между рогами >75O, но <105O. И в этих случаях может быть рассмотрено проведение других диагностических исследований (в т. ч. лапароскопии).
При проведении лапароскопии четко определяется наружный контур матки, по которому и различается двурогая матка и матка с перегородкой, т. к. в основе лежит именно анатомическое строение наружного контура (т. е. матка с внутренней перегородкой имеет наружное строение дна такое же, как нормальная матка).
Проверенным и надежным методом в оценке внутриматочной патологии является HSG. Однако этот метод не дает точности в дифференциальной диагностике двурогой матки и перегородки, т. к. изображение полостей очень схожи – визуализируются две полости в обоих случаях [72, 149, 150]. Диагностическая точность HSG с целью дифференциации составляет 55% [158, 159].
Предоперационная оценка
Двурогие матки редко требуют хирургической реконструкции [71]. Преимущества метропластики ни разу не были изучены в проспективных работах и большинство отчетов являются наблюдательными исследованиями [121]. Считается, что метропластика может быть применена для женщин, имеющих повторные самопроизвольные выкидыши II-го триместра, преждевременные роды, и у которых исключены другие этиологические факторы [121, 122].
Хирургические методы
Описано несколько техник метропластики, но техника Strassmann является хирургией выбора для унификации двурогих и удвоенных маток. Трансцервикальный лизис срединной части, используемый при других аномалиях, в этой ситуации противопоказан, т. к. может иметь место перфорация матки [14]. По технике Strassmann удаляется перегородка путем клиновидной резекции с последующим объединением двух полостей. Также имеют место модификации этого хирургического метода. Проводят предоперационное профилактическое введение антибиотиков и стандартные профилактические технологии с целью минимизации спаечного процесса во время хирургического вмешательства. Если присутствует две шейки – их объединение не рекомендуется. Планирование беременности возможно не ранее, чем через 3 месяца [14]. Большинство женщин с двурогими матками, которым была выполнена метропластика, могут расчитывать на беременность и роды жизнеспособным плодом. Трансабдоминальная метропластика может существенно улучшить репродуктивный прогноз у женщин, которые имели в анамнезе повторные самопроизвольные выкидыши или преждевременные роды до операции [122]. Strassmann сообщает о 263 беременностях у женщин после метропластики: 86% – роды жизнеспособным плодом [5]. Важно, что большинство родов были через естественные родовые пути без сообщений о разрыве матки во время беременности или родов. Несмотря на это, некоторые эксперты все же рекомендуют плановое кесарево сечение. Еще одно исследование 22-х женщин с двурогой маткой, перенесших метропластику по Strassmann: 19 (86%) имели срочные роды жизнеспособным плодом без клинически значимых осложнений и все были родоразрешены путем операции кесарева сечения [160].
Класс V. Матка с перегородкой
Матка с перегородкой является наиболее распространенной структурной патологией среди всех аномалий мюллеровых протоков. Формирование происходит в результате неполной резорбции медиальной перегородки после полного слияния мюллеровых протоков. Обычно перегородка располагается в области дна матки и представляет слабо васкуляризированную фиброзно-мышечную ткань [10]. Существуют многочисленные вариации перегородок. Полная перегородка исходит из дна матки, доходит до внутреннего зева и делит полость пополам. Такой вариант аномалии часто ассоциируется с продольной влагалищной перегородкой [12]. Частичная перегородка не доходит до внутреннего зева. Иногда встречаются сегментарные перегородки, при которых возможна частичная связь между эндометриальной полостью [120].
Вариант аномалии матки с перегородкой, который характеризуется триадой: полная перегородка, удвоение шейки и перегородка влагалища может встречаться чаще, чем ранее описывалось [26, 27, 48, 111, 161–164]. Наиболее распространенные симптомы при этом – диспареуния, дисменорея, привычное невынашивание, первичное или вторичное бесплодие [164].
В случае обнаружения удвоения шейки нужно проводить дифференциальную диагностику с удвоением матки – т. к. будет различаться репродуктивный прогноз и необходимы разные стратегии лечения. Полная перегородка резецируется гистероскопически, а при удвоении матки хирургическое вмешательство не рекомендуется.
При проведении лапароскопии выявляется ровный наружный контур, как и при нормальной матке [164]. Эта аномалия «бросает вызов» общепринятой теории о развитии мюллеровых протоков, т. к. свидетельствует, что слияние протоков может происходить в 2-х направлениях.
Редкий вариант матки с перегородкой – матка Роберта [165]. Эта патология характеризуется наличием полной перегородки с несообщающимися полостями и слепо оканчивающимся рогом, что клинически проявляется односторонней гематометрой, дисменореей. Сообщается о 26 недельной беременности при матке Роберта, которая, к сожалению, закончилась рождением нежизнеспособного плода [166].
При наличии матки с перегородкой констатируются наихудшие репродуктивные исходы (по сравнению со всеми другими мюллеровыми аномалиями). Обзор объединенных данных показывает следующую статистику: 146 (10%) – преждевременные роды (N=1459), 90 (58,1%) – живорождения (N=155), 3 (1,9%) – эктопические беременности (N=155) и 1105 (75,7%) – самопроизвольные выкидыши (N=1459) [112]. Несмотря на такие неутешительные данные, наличие матки с перегородкой не всегда связано с неблагоприятным акушерским исходом и соответственно факт имеющейся патологии сам по себе не может быть обязательным показанием к оперативному вмешательству.
Диагностика
Необходим комплекс диагностических методов для постановки окончательного диагноза. Наиболее часто проводят ГСГ, гистероскопию, лапароскопию. УЗИ и МРТ также полезны. На ГСГ выявляется матка с двумя полостями, оценивается длина, толщина перегородки и проходимость маточных труб. Однако ни ГСГ, ни гистероскопия не позволяют отличить матку с перегородкой от двурогой матки [159, 167]. Лапароскопия, с целью визуализации наружного контура дна матки, является наиболее точным диагностическим методом. Трансвагинальное УЗИ (особенно 3D) является достаточно точным для диагностики: чувствительность – 100%, специфичность – 80% [150]. УЗИ с цветным допплеровским картированием изображения дает 95% чувствительности и 99,3% специфичности [168]. В проспективном исследовании 40 женщин с привычными репродуктивными потерями в анамнезе, точность 3D УЗ-сонограмм была 92% [169]. Но, к сожалению, трехмерное УЗИ не является широко доступным.
МРТ позволяет отлично оценить структуру тканей и надежно дифференцировать перегородки и двурогие матки [170]. На МРТ определяется низкая интенсивность сигнала для перегородки и нормальный наружный контур дна [75].
Предоперационная оценка
Решение о проведении хирургической коррекции основывается на неблагоприятном репродуктивном анамнезе, а не на изолированном наличии перегородки [12]. Кандидаты для оперативного вмешательства – это женщины, имеющие выкидыши во II-м триместре беременности или преждевременные роды [16, 170]. Резекцию перегородки проводят в раннюю фолликулярную фазу, когда толщина эндометрия наименьшая. Некоторые авторы рекомендуют предоперационную медикаментозную терапию (прогестинами, даназолом, аГНРГ) – для уменьшения толщины эндометрия и улучшения визуализации [167, 171].
Аномалии мочевыводящей системы обычно не коррелируют с этой патологией, однако все же рекомендуется проведение УЗИ почек (для исключения возможной патологии).
Хирургические методы
Метод выбора – гистероскопическая метропластика с одновременной лапароскопией [14, 171, 172] для снижения риска перфорации матки во время истечения перегородки. Также польза совместной лапароскопии заключается в возможности точно визуализировать наружный контур матки и достоверно исключить другую патологию органов малого таза. Как альтернатива – трансвагинальный интраоперационный УЗ-контроль во время резекции [174]. Мнения по поводу иссечения шеечной перегородки при ее наличии различны, т. к. высок риск хирургических осложнений и несостоятельности шейки в будущем. В последнее время эксперты не рекомендуют резецирование перегородки шейки матки [48, 175].
Гистероскопическая метропластика может быть проведена мини-ножницами, путем электрохирургии или лазером. Риск кровотечения, как правило, минимален, т. к. перегородка слабо васкуляризирована [48, 171–173, 175–177].
Послеоперационное ведение
Проведение послеоперационной постановки ВМС в течение 1 месяца является спорным [178, 179]. Некоторые авторы считают, что постановка ВМС является профилактическим методом для предотвращения внутриматочной адгезии. Однако большинство экспертов утверждают, что эта процедура не является необходимой и может провоцировать местное воспаление с последующим образованием синехий [14, 180]. Конъюгированные эстрогены по 1,25 мг в сутки на 25 дней с присоединением прогестерона по 10 мг в день с 21 по 25-й дни терапии часто назначаются после хирургического вмешательства с целью улучшения эпителизации. В настоящее время пока не достигнуто единого решения в вопросе необходимости назначения гормональной терапии [121, 181]. Послеоперационное назначение антибиотиков проводится пациентам с воспалительными заболеваниями органов малого таза в анамнезе и нет рекомендаций преимущества рутинного назначения. Через 1 месяц рекомендуется контрольное обследование: диагностическая гистероскопия, ГСГ или УЗИ (лучше во II-ю фазу цикла). Если по результатам контрольного обследования отклонений не выявлено, разрешается планирование беременности.
Осложнения и результаты
Litta и соавт. сообщают об отсутствии серьезных осложнений после гистероскопической метропластики. Все пациенты были выписаны домой через 6 часов после операции [175]. Возможна перфорация и ее риск снижается при проведении одновременной лапароскопии. Во время операции также имеется риск разрыва шейки матки; сообщается о послеоперационном кровотечени (до 3%) [179]. Большинство исследований говорят о минимальном риске кровопотери во время этого вмешательства [183]. Как потенциальное осложнение, может иметь место риск разрыва матки при последующей беременности [184]. Остаточная перегородка, по данным одного исследования, включавшего 68 женщин после гистероскопической метропластики, составила – 44,1%. Авторы пришли к выводу, что остаточная перегородка <1см не дает клинически значимых для репродукции побочных эффектов и повторное иссечение не проводилось [177]. Считается, что репродуктивная функция пациенток после оперативной коррекции улучшается, однако это не подтверждено рандомизированными контролируемыми исследованиями четкой оценки репродуктивных исходов. Данные большинства отчетов – наблюдательные. Сообщается о снижении уровня самопроизвольных выкидышей с 86% до 12% (N=115) [183]. Еще одно исследование дает 86% срочных родов [185]. Более ранние исследования подтверждают эти данные [186].
Класс VI. Аркуатная матка
Аркуатная матка является результатом почти полной резорбции маточновлагалищной перегородки. Она характеризуется небольшим внутриматочным углублением (менее 1 см) с локализацией в области дна. Чаще всего такую аномалию обнаруживают на ГСГ [17, 189].
Классификация этой аномалии изначально вызывала затруднения – по системе Buttram&Gibbons она рассматривалась как легкая форма двурогой матки [45].
По классификации AFS она была отнесена в отдельную группу, созданную именно для этой аномалии и базирующуюся на ее наружном объединении, которое и отличает ее от матки с перегородкой. Обе классификации высказывают предположение, что аркуатная матка – это вариант нормальной формы матки. В сравнении с другими дефектами развития мюллеровых протоков, аркуатная матка имеет клинически благоприятный прогноз, нечастую ассоциацию с неблагоприятной акушерской статистикой: не дает ухудшение репродуктивных исходов [112, 190].
Диагностика и подходы клинического ведения при аркуатной матке
Литературные данные в отношении диагностики, схем ведения и репродуктивных исходов ограничены и противоречивы. На ГСГ визуализируется одна полость с фундальным седловидным углублением. На МРТ можно видеть выпуклый или плоский наружный контур матки, а внутреннее углубление достаточно широкое и однородное с такой же интенсивностью сигнала, как и миометрий. Иногда выявляется аномальное кровоснабжение миометрия в области фундального углубления [17, 148, 189].
Также необходимо исследование почек для исключения сочетанных аномалий (хотя обследование мочевыделительной системы в этом случае не является обязательным). Клинические подходы к ведению пациенток с аркуатной маткой такие же, как и для матки с перегородкой: только определенной группе пациенток с отягощенным репродуктивным анамнезом рекомендована хирургическая коррекция. На основании анализа 283 беременностей [112] получены следующие статистические результаты: 10 (5,1%) из 195 – преждевременные роды, 129 (66,2%) из 195 – живорождения, 7 (6,3%) – эктопические беременности и 57 (20,1%) из 283 – самопроизвольные выкидыши.
Выводы
Аномалии мюллеровых протоков – это морфологически разнообразная группа нарушений, в которую вовлечены внутренние половые органы. Постановка точного диагноза имеет важное значение, т. к. от него зависит клинический прогноз фертильности и стратегия дальнейшего ведения пациента. Подход хирургической коррекции мюллеровых дефектов является узкоспецифичным и может меняться в зависимости от принадлежности к конкретной группе аномалий. Ценность большинства хирургических вмешательств определяется послеоперационной возможностью пациенток иметь здоровые половые отношения и благоприятные репродуктивные исходы.
Несмотря на отсутствие высококачественных доказательных РКИ, хирургическую коррекцию рекомендуется проводить пациентам с ВАМ при перегородках, рудиментарном роге, морфологически измененных матках.
Эти пациенты должны быть направлены на оперативное лечение к профильным специалистам на базе современной эндоскопической хирургии с опытом работы в области маточных аномалий.
Перечень литературы находится в редакции.
Детальніше
