
ДЕФИЦИТ ЖЕЛЕЗА У РЕБЕНКА И ЕГО ИНТЕЛЛЕКТ
 Существует ли взаимосвязь? (часть І)
Существует ли взаимосвязь? (часть І)
Дефицит железа (ДЖ) остается одной из важнейших проблем здравоохранения во всем мире. Железодефицитное состояние (ЖДС) отмечено у 4–5 млрд. людей на планете, из них около 30% страдают собственно железодефицитной анемией (ЖДА). ЖДА являйся наиболее распространенным заболеванием крови, составляя до 90% всех анемий в детском возрасте
Эксперты ВОЗ (2002) это состояние относят к числу факторов, от которых во многом зависит заболеваемость, инвалидность, смертность, продолжительность жизни. Чаще дефицитом железа страдают дети первых трех лет жизни, подростки, беременные и кормящие женщины. По данным ВОЗ, в Европе за последнее десятилетие цифры распространенности ЖДА составляли не ниже 26 % у детей до 5 лет, а в более старшем возрасте достигли 9,3–9,8% среди всей детской популяции. Особо тревожны эти показатели в связи с прямой взаимосвязью между дефицитом железа у ребенка и формированием у него навыков, умений, в первую очередь определяющих его социальную функцию не только на ближайшие годы, но и на десятилетия.
Поэтому у родителей и педагогов возникают вопросы о взаимосвязи дефицита железа у детей с показателями нервно-психического развития, познавательными функциями, уровнем интеллекта. На эти непростые вопросы педиатрам, семейным врачам зачастую сложно ответить.
В связи с приведенными данными, мы поставили перед собой задачу обобщить наиболее частые вопросы, возникающие при анализе данной проблемы, привести наиболее адаптированные для родительского восприятия ответы.
Первое сообщение на эту тему, публикуемое в этом номере журнала «З турботою про Дитину», посвящено особенностям проявления различных по степени тяжести железодефицитных состояний у детей до шестилетнего возраста. Второе сообщение, которое Вы найдете в следующем номере журнала, будет посвящено данной проблеме у детей школьного возраста, а также вопросам профилактики железодефицитных состояний у детей разных возрастных групп.
Итак, разберем наиболее типичные вопросы о взаимосвязи железодефицитных состояний с формированием личности в раннем и дошкольном возрасте ребенка и постараемся ответить на них.
Вопрос первый. Какова роль железа в организме человека?
Железо, в силу важности выполняемых им функций, признано жизненно необходимым. Железо является обязательным и незаменимым компонентом ферментных систем организма, обеспечивающих должный уровень системного и клеточного аэробного метаболизма. С участием этого микроэлемента в организме осуществляются такие биохимические процессы как: транспорт и депонирование кислорода (гемоглобин, миоглобин); транспорт электронов (цитохромы, железосеропротеиды), синтез ДНК, тканевое дыхание. Железо участвует в работе окислительно-восстановительных ферментов (оксидаза, гидроксилаза, супероксиддисмутаза). Депонируется железо при избытке поступления в организм в виде железосодержащих веществ (ферритин и гемосидерин).
Вопрос второй. Какие системы детского организма наиболее уязвимы перед дефицитом железа?
Длительный дефицит железа приводит к задержке физического и нервно-психического развития ребенка, влияет на иммунную систему, ухудшает работу сердечно-сосудистой системы, желудочно-кишечного тракта, работу эндокринных желез, вызывает астеновегетативные проявления, нарушаются процессы тканевого дыхания, что вызывает дистрофические процессы в тканях организма.
Но особенно чувствительным органом к дефициту железа является мозг плода и ребенка. Роль железа в нейрофизиологии весьма существенна.
Согласно современным исследованиям, наибольшее содержание железа, после гемоглобина эритроцитов, наблюдается в клетках головного мозга. Серией экспериментальных работ, проведенных в ведущих научных центрах Северной Америки, было доказано, что дефицит железа может оказывать специфическое воздействие как на центральную нервную систему (нервные клетки, миелин), так и на процесс передачи нервных импульсов. Железо в тканях головного мозга участвует в генерации импульсов в нервных синапсах, в процессах миелинизации нервных волокон, оказывает влияние на функции гипоталамуса. В случае недостатка железа снижается количество и чувствительность допаминовых рецепторов (Д2). Это ведет к нарушению метаболизма допамина в нервных синапсах, в результате чего уменьшается стимулирующий эффект на следующую клетку и сокращается количество проходящих импульсов. В результате этих исследований ученые пришли к выводу, что дефицит железа, сопровождающийся снижением дофаминергической активности, может привести к изменению поведенческих реакций, познавательных функций, негативно повлиять на способность к обучению и на память (A. B. Bruner, et al.,1996).
Кора головного мозга играет основную роль в таких процессах как внимание, память, перцептивное сознание, мышление, язык. У животных с дефицитом железа наблюдаются метаболические и структурные изменения в коре головного мозга, которые отвечают за эквиваленты некоторых из указанных функций (B. Lozoff et al. 2006; K.L. Ward et al. 2007). В этих же исследованиях было продемонстрировано, что при дефиците железа снижается содержание липидов и белков в миелине. Дефекты миелинизации на раннем этапе развития мозга сохраняются во взрослом возрасте, несмотря на последующее восполнение запасов железа.
Гиппокамп – центральная структура памяти, отвечающая за опознание, пространственную память, переход из кратковременной памяти в долговременную. В эксперименте на молодых животных было доказано, что эта структура мозга особенно чувствительна к раннему дефициту железа (В.Lozoff et al. 2006, K.L. Ward et al., 2007).
Вопрос третий. Влияние анемии беременной на плод и дальнейшее развитие ребенка
Многие годы бытовало ошибочное представление о том, что незначительное снижением концентрации гемоглобина у беременной (в пределах до 90 г/л) не оказывает влияния на развитие плода. Бытовал такой тезис – «плод забирает от матери все необходимое для его развития».
Однако, рядом научных исследований (T. D. Wachs et al., 2005; В. Lozoff, 2007; P. V. Tran et al., 2008 и др.) было доказано, что плод недостаточно защищен от влияния дефицита железа у матери; состояние обмена железа у матери отражается на показателях обмена железа у плода. Изменение обмена железа у тандема «беременная–плод» может быть предиктором отклонений в социальном и эмоциональном поведении ребенка. Даже если ребенок родился от матери с умеренным дефицитом железа во время беременности, при нормальных показателях гемоглобина и эритроцитов (латентный дефицит железа), он все равно попадает в группу риска по возникновению патологии, сопровождающейся снижением иммунологического ответа в первые 24 месяца жизни (R. D. Baker, 2010).
В работах ряда исследователей (И. Н. Захарова, Ю. А. Дмитриева, 2011; Т. В. Казюкова, и соавт., 2012; В. А. Кувшинников и соавт. ,2011 и др.) было показано, что у детей, рожденных от матерей, страдавших анемией беременных, была высокая степень риска задержки показателей статико-кинетических функций. Следует помнить, что дефицит железа у плода приводит к необратимым нарушениям роста массы мозга, процесса миелинизации и проведения нервных импульсов через синапсы. Эти изменения не удается полностью корректировать препаратами железа, назначаемыми в первые месяцы жизни. В последующем у ребенка отмечают те или иные уровни задержки психического и моторного развития, нарушение когнитивных функций.
Вопрос четвертый. Железодефицитное состояние (ЖДС) и железодефицитная анемия (ЖДА) – равнозначные понятия?
Нет, эти понятия не равнозначные. В стадии дефицита железа входят: предлатентный дефицит железа, латентный дефицит железа (ЛДЖ) и ЖДА.
Стадия предлатентного дефицита железа характеризуется рядом изменений на тканевом уровне, которые не имеют клинической картины.
А вот для латентного дефицита железа характерна определенная клиника: наличие тканевых проявлений (сухость кожи, ломкость волос, гиперпигментация кожи локтевой и коленных областей); астеновегетативный синдром; снижение уровня железа в депо и сыворотке крови. При этом уровень гемоглобина в периферической крови соответствует возрастной норме, показатели периферической крови изменены мало. То есть, клиническая картина латентного дефицита железа обусловлена преимущественно трофическими нарушениями.
Железодефицитная анемия (ЖДА) – верхушка «айсберга» железодефицитного состояния, которая характеризуется: снижением уровня гемоглобина в крови; микроцитарной анемией; существенными изменениями параметров железа в крови – снижением, вплоть до отсутствия депо железа; снижением насыщения трансферрина железом.
Для ЖДА типичны такие клинические симптомы: эпителиальный, астеноневротический, сердечно-сосудистый, гепатолиенальный (преимущественно в раннем возрасте), мышечный, иммунодефицитный.
Вопрос пятый. Как проявляется взаимосвязь дефицита железа с показателями нервно-психического развития, способности к обучению, развития памяти у детей раннего и дошкольного возраста?
Группой американских исследователей (R. D. Baker, 2010 и др.) было показано, что даже через пять лет после ЖДА, перенесенной в возрасте 12–24 месяцев, у ребенка отмечают задержку умственного и моторного развития, а также трудности в обучении.
Рядом исследователей (D. M. Tucker, Н. Н. Sandstead, J. G. Penland et al., 2006) также было высказано мнение о том, что дефицит железа изменяет эмоциональное состояние грудных детей настолько, что они становятся более углубленными в себя, осторожными и неуверенными. В результате этого дети грудного возраста могут быть менее способными взаимодействовать с окружающим миром и учиться у него, что мешает их интеллектуальному развитию. У детей дошкольного возраста (36–72 месяца) установлена связь между дефицитом железа и низкими результатами в обучении, особенно при выполнении заданий, требующих повышенного внимания и распознавания. Для них характерно обеднение эмоциональной сферы, преобладание плохого настроения, вялости, раздражительности, плаксивости.
Вопрос шестой. Какая же тактика врача в вопросах лечения дефицита железа у детей?
Успех в лечении ЖДА и качество жизни пациентов зависят от правильно построенной тактики лечения этого состояния. Терапия ЖДА и ЖДС у детей различных возрастных групп должна быть комплексной и базироваться на четырех принципах: нормализация режима и питания ребенка; возможная коррекция причины железодефицитного состояния; назначение препаратов железа; поддерживающая терапия.
Важнейшим фактором коррекции железодефицита является сбалансированное питание, и в первую очередь – грудное вскармливание. Грудное молоко не только содержит железо в высокобиодоступной форме, но и повышает абсорбцию железа из других продуктов, употребляемых одновременно. Однако, интенсивные обменные процессы у грудных детей приводят к тому, что к 5–6-му месяцу жизни антенатальные (внутриутробные) запасы железа истощаются даже у детей с благополучным перинатальным анамнезом. Это происходит как у малышей, которые вскармливаются грудным молоком, так и при вскармливании адаптированными молочными смесями, обогащенными железом.
Для малышей очень важно своевременное введение прикорма, введение в рацион мяса, особенно телятины, гречневой и овсяной круп, фруктовых и овощных пюре, кисломолочных продуктов, отваров шиповника и сухофруктов. В более старшем возрасте в рационе у ребенка и подростка, кроме вышеуказанных продуктов, должны быть мясные субпродукты, богатые железом, рыба, твердые сорта сыра, яичный желток, морская капуста, грецкий орех, яблоки, морковь и др. В этом аспекте следует отметить неблагоприятный эффект вегетарианства в детском и подростковом возрасте.
Следует помнить, что аскорбиновая, лимонная, янтарная и яблочная кислоты, фруктоза, сорбит и ряд других компонентов усиливают всасывание железа. Тормозят утилизацию железа чай, молоко, некоторые виды каш. Эти продукты не следует давать ребенку в течении 1–2 часов до или после приема препаратов железа.
Терапия ЖДА препаратами железа является очень важным этапом лечения. Соответственно Приказу МЗУ от 10.01.2005 г. №5 «Протокол лечения железодефицитной анемии у детей» назначение лечебных доз препаратов железа при стойком уровне гемоглобина 100г/л и выше не показано.
Однако в этом правиле есть исключения. Так, у детей, рожденных с малой массой, в первые месяцы, даже годы жизни, всегда есть дефицит железа. Поэтому у таких детей, даже при уровне гемоглобина 100 г/л и выше, имеется необходимость в назначении препаратов железа. В таких случаях очень важна консультация и наблюдение неонатолога, педиатра, детского гематолога.
Если у ребенка выявлена ЖДА, то при уровне гемоглобина ниже 100 г/л обойтись без лечебных доз препаратов железа невозможно.
Вопрос седьмой. Какая терапия железодефицитных анемий является наиболее современной?
Терапия ЖДА препаратами железа является очень важным этапом лечения. Выбору препарата для коррекции анемии придается особое значение, поскольку длительность лечения может составлять от нескольких недель до многих месяцев. При этом важны не только эффективность препарата железа, но и отсутствие побочных эффектов и осложнений, приверженность к проводимой терапии.
Следует помнить, что при проведении терапии ЖДА, используют препараты железа, которые разделены на две группы:
1) ионные железосодержащие препараты (солевые соединения железа);
2) неионные соединения, к которым относятся препараты, представленные гидроксид-полимальтозным комплексом трехвалентного железа.
Действительно, многие годы в лечении ЖДА активно применялись препараты двухвалентного железа, которые обладают хорошей растворимостью и высокой диссоциацией в растворах. Это позволяет двухвалентному железу, которое поступает в организм, быстро соединяться с транспортными белками, после чего происходит его проникновение в клетку. На протяжении этого этапа происходит ряд биохимических процессов, превращение двухвалентного в трехвалентное железо, затем поступление на митохондрии и использование для синтеза гема, цитохромов и других железосодержащих соединений.
Именно эти биохимические свойства солевых препаратов железа (быстрая растворимость и высокая диссоциация) с одной стороны, способствуют видимости быстрого насыщения организма железом. В то же время, эти же особенности ионных форм железа вызывают металлический привкус, потемнение зубов и десен, диспептические явления из-за раздражения слизистой оболочки желудка и кишечника (тошноту, чувство переполнения желудка, рвоту, запоры, диарею), аллергические реакции по типу крапивницы. Эти негативные моменты препятствуют интервально обоснованному курсу лечения. Кроме того, в просвете кишечника соли железа легко взаимодействуют с компонентами пищи (фитинами, оксалатами, танинами) и лекарственными препаратами, что резко снижает абсорбцию железа. Назначение натощак солевых препаратов железа с целью исключения подобного взаимодействия может, напротив, усилить повреждающее действие солей железа на слизистую оболочку кишечника, вплоть до ее некроза. Описанные осложнения и нежелательные последствия применения солевых форм ферропрепаратов резко снижают эффективность терапии препаратами двухвалентного железа.
Вторая группа препаратов железа – несолевые (неионные) трехвалентные не уступают солевым по антианемической эффективности, но являются более безопасными. Это обусловлено их химической структурой, представленной гидроксид-полимальтозным комплексом трехвалентного железа (ГПК-Fe3+). Такая структура комплексов препятствует высвобождению свободных ионов железа в желудочно-кишечном канале. Резорбция железа из ГПК-Fe3+ приближена к абсорбции гемового железа, т. к. структура препарата сходна с естественным соединением железа ферритином. Благодаря такому сходству железо (III) поступает из кишечника в кровь путем активного всасывания и переносится на транспортные формы. Всасываемое железо связывается с ферритином и сохраняется в организме, преимущественно в печени. Позже в костном мозгу оно включается в состав гемоглобина.
Неионная структура ГПК-Fe3+ и активный транспортный механизм всасывания предохраняют организм от избытка свободных ионов металла, которые и вызывают нежелательные эффекты у препаратов двухвалентного железа. При этом сохраняются физиологические процессы саморегуляции, которые предохраняют кишечник от токсических эффектов.
Главными требованиями, предъявляемыми к препаратам железа для приема внутрь, используемым в детской практике, являются: достаточная биодоступность; высокая безопасность; хорошие органолептические характеристики; лекарственные формы, удобные для пациентов всех возрастов. Этим критериям в наибольшей степени соответствуют препараты на основе гидроксид-полимальтозного комплекса трехвалентного железа (ГПК Fe3+). В педиатрической практике хорошо зарекомендовал себя препарат Мальтофер (производитель – компания Вифор, Швейцария). Средняя терапевтическая доза препарата Мальтофер у детей первых трех лет жизни составляет 3–5 мг/кг/сутки. При этом применение препарата Мальтофер не требует постепенного увеличения дозы, его можно смешивать с фруктовыми и овощными соками.
Как мы указывали выше, в следующем номере журнала уважаемые читатели смогут ознакомиться с наиболее частыми вопросами, которые возникают у родителей, педагогов, подростков о взаимосвязи дефицита железа с показателями когнитивных функций, уровнем интеллекта у школьников.
Детальніше

СИНДРОМ ТИРЕОТОКСИКОЗА
 Заболевания щитовидной железы у детей и подростков занимают первое место среди всех эндокринопатий в Украине. Распространенность тиреотоксикоза, по данным МЗ Украины, в 2012 году составила 0,05 на 1000 детей, при этом девочки страдают данной патологией в 10 раз чаще, чем мальчики
Заболевания щитовидной железы у детей и подростков занимают первое место среди всех эндокринопатий в Украине. Распространенность тиреотоксикоза, по данным МЗ Украины, в 2012 году составила 0,05 на 1000 детей, при этом девочки страдают данной патологией в 10 раз чаще, чем мальчики
Несмотря на четко сформулированные клинические признаки синдрома тиреотоксикоза у детей, диагностика его в ряде случаев представляет определенные сложности. Зачастую, наличие у ребенка зоба в сочетании с признаками аутоиммунного поражения щитовидной железы (повышение содержания антител к тиреопероксидазе (АТ-ТПО) в сыворотке крови) ошибочно трактуется врачами как гипертиреоидная стадия аутоиммунного тиреоидита (АИТ) даже при длительной тахикардии, выраженном экзофтальме, глазных симптомах, стойком повышении тиреоидных гормонов и значительном снижении ТТГ (тиреотропный гормон).
В этой связи представляется актуальным описание дифференциально-диагностических критериев тиреотоксикоза у детей.
Синдром тиреотоксикоза – это патологический синдром, который характеризуется определенными клиническими проявлениями в результате повышения содержания тиреоидных гормонов: Т4св. (свободный тироксин, тетрайодтиронин) и Т3св. (свободный трийодтиронин) в крови и тканях. В то же время, под гипертиреозом понимают увеличение содержания тиреоидных гормонов в крови.
Тиреотоксикоз у детей в более чем 90% случаев обусловлен диффузным токсическим зобом. Среди других причин тиреотоксикоза следует иметь в виду гипертиреоидную фазу аутоиммунного тиреоидита, токсическую аденому щитовидной железы, многоузловой токсический зоб, ТТГ-секретирующую аденому гипофиза, йод-индуцированный тиреотоксикоз, транзиторный тиреотоксикоз новорожденных, хронический лимфоцитарный тиреоидит (хашитоксикоз). Необходимо еще раз подчеркнуть, что ДТЗ, так же как и АИТ, является аутоиммунным заболеванием, о чем нередко забывают врачи, устанавливая диагноз.
В случаях предположения о тиреотоксикозе, первоочередным исследованием является определение уровня тиреоидных гормонов. При этом диагностически значимым является повышенный или определяемый на верхней границе нормы уровень Т4св. и Т3св. в крови в сочетании с пониженным уровнем ТТГ.
С целью уточнения причины тиреотоксикоза необходимо проведение УЗ-исследования щитовидной железы, а также определение тиреоглобулина и антитиреоидных антител в крови (АТ-ТПО и антител к рецепторам ТТГ). В случае одновременного повышения тиреоидных гормонов и ТТГ, следует подумать о тиреотоксикозе вторичного (гипофизарного) генеза с последующим проведением визуализации гипофиза.
Антитела к ТПО – антитела к ферменту клеток щитовидной железы, участвующему в синтезе тиреоидных гормонов. Они являются показателем агрессии иммунной системы по отношению к собственному организму. Тиреоидная пероксидаза обеспечивает образование активной формы йода, которая способна включаться в процесс йодификации тиреоглобулина. Антитела к ферменту блокируют его активность, вследствие чего снижается секреция тиреоидных гормонов (T4,T3). Однако АТ-ТПО могут быть только «свидетелями» аутоиммунного процесса. Антитела к тиреопероксидазе – наиболее чувствительный тест для обнаружения аутоиммунного заболевания щитовидной железы. Обычно их появление является первым сдвигом, который наблюдается в ходе развивающегося гипотиреоза вследствие тиреоидита Хашимото. При использовании достаточно чувствительных методов АТ-ТПО обнаруживаются у 95% людей с тиреоидитом Хашимото, и примерно у 85% пациентов с болезнью Грейвса. Обнаружение АТ-ТПО во время беременности говорит о риске развития у матери послеродового тиреоидита и возможном влиянии на развитие ребенка.
Повышение уровня АТ-ТПО выявляется при болезни Грейвса (диффузный токсический зоб), узловом токсическом зобе, подостром тиреоидите (де Кревена), послеродовой дисфункции щитовидной железы, хроническом тиреоидите (Хашимото), идиопатическом гипотиреозе, нетиреоидных аутоиммунных заболеваниях.
Антитела к тиреоглобулину (АТ-ТГ, anti-thyroglobulin autoantibodies) – аутоантитела к белку-предшественнику тиреоидных гормонов. Тиреоглобулин – йодированный белок, из которого образуются тиреоидные гормоны (Т3 и Т4). Он продуцируется в организме только клетками щитовидной железы и накапливается в фолликулах железы в виде коллоида. Небольшие количества тиреоглобулина (пропорциональные общей массе ткани железы и активности стимулирующих влияний ТТГ) поступают в кровь во время секреции тиреоидных гормонов. Низкие концентрации антител к тиреоглобулину обнаруживаются примерно у 10% здоровых индивидуумов.
АТ-ТГ в высоких титрах часто присутствуют у пациентов с аутоиммунными заболеваниями щитовидной железы (30% пациентов с болезнью Грейвса, 85% пациентов с тиреоидитом Хашимото).
Использование АТ-ТГ в целях выявления аутоиммунных заболеваний щитовидной железы целесообразно в йоддефицитных регионах, особенно при обследовании пациентов с узловым зобом.
Определение АТ-ТГ полезно также при мониторинге терапии йодом эндемического зоба, поскольку йодированный тиреоглобулин более иммуногенен.
Высокий уровень АТ-ТГ, как и АТ-ТПО, указывает на риск нарушения функции щитовидной железы, в том числе, тиреоидной дисфункции во время беременности, потенциально опасной для плода, послеродового тиреоидита, возможного поражения щитовидной железы у больных с нетиреоидными аутоиммунными эндокринными заболеваниями и членов семей больных с наследственными органоспецифическими аутоиммунными заболеваниями.
Клинический диагноз при увеличении щитовидной железы формулируется с учетом следующих характеристик:
- Форма увеличения щитовидной железы, наличие либо отсутствие узлов
а) диффузный зоб;
б) узловой зоб.
- Локализация зоба:
а) типично расположенный;
б) частично загрудинный;
в) кольцевой;
г) дистопия.
- Размер зоба:
а) при пальпаторном исследовании;
б) при сонографич. исследовании.
- Функциональное состояние щитовидной железы:
а) эутиреоз;
б) гипотиреоз;
в) тиреотоксикоз.
Диффузный токсический зоб (ДТЗ) (болезнь Грейвса–Базедова) – аутоиммунное заболевание, характеризующееся стойким повышением секреции тиреоидных гормонов, диффузным увеличением щитовидной железы в сочетании с эндокринной офтальмопатией у 50–70% больных.
В 1840 году Базедов подробно описал заболевание и выделил 3 основных симптома: зоб, пучеглазие и тахикардию, не утративших и поныне высокую диагностическую значимость. Впервые ДТЗ у ребенка был описан A. Romberg в 1851 году, который диагностировал у 14-летней девочки зоб, тахикардию и аменорею. В России первое описание тиреотоксикоза у ребенка 5 лет сделано Н. Ф. Филатовым в 1902 году.
Этиология заболевания
- инфекции (после острых детских инфекций, обострения хронического тонзиллита);
- психическая и физическая травма;
- инсоляция;
- врожденная предрасположенность.
Патогенез
Патогенез сложный и до конца не установлен. Общепризнана аутоиммунная теория развития ДТЗ, связанная с появлением в сыворотке крови антител к рецепторам тиреотропина на поверхности клеток щитовидной железы.
Собирательное название всех антител щитовидной железы – тиреостимулирующие иммуноглобулины. Наиболее изученным среди них является длительно действующий тиреостимулятор LATS, предотвращающий связывание антигена с компонентами щитовидной железы (т. н. депрессор функции щитовидной железы). Определенную роль в патогенезе ДТЗ играют гуморальный и клеточный иммунитет.
Важное место также отводится влиянию генетических факторов: ген, обуславливающий изменения в иммунокомпетентной системе, локализован на 6-й хромосоме и тесно сцеплен с антигеном HLA- Dw3. Отмечена также большая частота HLA- B8.
Морфологическая структура щитовидной железы при тиреотоксикозе у детей изучена в меньшей мере, чем у взрослых. Отмечены полиморфизм фолликулов, переход кубического эпителия, выстилающего фолликулы, в цилиндрический, наличие значительных утолщений с одновременным образованием сосочковых выростов в просвете фолликулов.
Клиническая картина
Ранний и постоянный симптом ДТЗ –увеличение щитовидной железы, обычно диффузное (узловой зоб встречается у детей редко). Классификация степеней увеличения щитовидной железы представлена в таблице 1. 
В развитии и течении тиреотоксикоза различают 4 стадии (по Milcu):
I cm., невротическая. Клиника вегетативного невроза с общим повышением возбудимости нервной системы, сердцебиениями при малозаметном увеличении щитовидной железы.
II ст., нейрогормональная. Увеличение щитовидной железы в сочетании с классическими симптомами тиреотоксикоза: трудоспособность, похудание, глазные симптомы.
III ст., висцеропатическая. Поражение внутренних органов с нарушением их функции.
IV cт., кахектическая. Необратимые дистрофия, изменения внутренних органов и систем, выражена общая дистрофия или кахексия, склонность к коматозным состояниям, тиреотоксическим кризам, мерцательной аритмии.
Наиболее распространенные клинические проявления тиреотоксикоза у детей представлены в таблице 2.
Изменения сердечно-сосудистой системы
1) Тахикардия 90–120 уд./мин. (пульсовая волна напоминает таковую при аортальной недостаточности). Сохранение тахикардии во время сна – важный признак при дифференциальной диагностике с тахикардиальным неврозом сердца.
2) Усиление сердечного толчка, тоны сердца часто усилены, четкие, акцент II тона над легочной артерией. При тяжелом тиреотоксикозе тоны сердца резко приглушены!
3) Функциональные сердечные шумы – грубый систолический шум на легочной артерии, на верхушке сердца, в V точке (меняется при перемене положения тела). Иногда – функционально-диастолич. шумы.
4) Размеры сердца чаще смещены влево.
5) АД систолическое повышено (150–170 мм. рт. ст.), диастолическое в норме или понижено.
6) На рентгене талия сердца сглажена, левый желудочек увеличен; для дифференциальной диагностики с митральными пороками используют контрастирование пищевода (отклонение тени контрастированного пищевода отсутствует).
Эндокринная офтальмопатия
- экзофтальм,
- отек орбитальных тканей,
- изменения глазных мышц.
Глазные симптомы при ДТЗ изучены довольно полно. Их известно до 40. Приведем некоторые из наиболее часто встречающихся.
Симптом Дальримпля – широкое раскрытие глазных щелей (придает лицу больного выражение страха, удивления, испуга или ужаса).
Симптом Грефе – запаздывание верхнего века при медленном опускании взора вниз.
Симптом Мебиуса – недостаточность конвергенции.
Симптом Штельвага – редкое и неполное мигание.
Симптом Жоффруа – отсутствие морщин на лбу при взгляде вверх.
Изменения нервной системы и психики
85% детей рано обнаруживают моторное возбуждение и эмоциональную неустойчивость; чрезмерно активны, постоянно находятся в движении, нервные, раздражительные, впечатлительные, неуравновешенные. Быстрая смена настроения со склонностью к агрессии и плаксивости. Снижение памяти, расстройство сна. Головная боль – также один из ведущих симптомов заболевания. Отмечается тремор пальцев вытянутых рук. Возможно наличие хорееформного гиперкинеза (насильственные, типичные, быстрые, толчкообразные движения пальцев рук, головы, сокращения мимических мышц и мускулатуры конечностей). Характерны вазомоторные, секреторные и трофические расстройства: гипергидроз, интенсивный и стойкий дермографизм, кожный зуд, повышение кожной температуры.
Наблюдается общая и мышечная слабость. Поражаются преимущественно проксимальные отделы конечностей, атрофия мышц пояса верхних конечностей. Определяются положительный симптом Мари (тремор пальцев вытянутых рук), тремор всего тела (симптом «телеграфного столба»), гиперрефлексия.
Изменения желудочно-кишечного тракта
- рвота и понос встречаются реже, чем у взрослых;
- повышение аппетита;
- прогрессирующее похудение.
Симптомы надпочечниковой недостаточности
- общая слабость и утомляемость;
- пигментация кожных покровов;
- низкое диастолическое АД.
Отмечается также увеличение лимфоузлов. В крови – лимфоцитоз; нарушение экскреции 17-КС и 17-ОКС.
При ДТЗ снижается антитоксическая и гликогенообразовательная функции печени. Нередко выявляется нарушение углеводного обмена (гипергликемическая сахарная кривая). У части детей наблюдаются изменения скелета (усиленный рост, ускоренное окостенение), в ряде случаев – задержка полового развития.
Диагностика
Диагностика основывается на клинической картине, а также лабораторных методах:
- Rö-логически выявляется опережение костного возраста;
- На ЭКГ определяется высокий вольтаж зубцов, синусовая тахикардия, ускорение AV-проводимости;
- Снижение уровня холестерина;
- Повышение уровня Тз и Т4.
Дифференциальная диагностика
- гиперплазия щитовидной железы в пубертатном периоде, когда она сочетается с функциональными нейровегетативными и вегетососудистыми сдвигами;
- при отсутствии зоба и экзофтальма неверно диагностируют ревматизм или врожденный порок сердца.
Лечение
Наиважнейшей задачей лечения тиреотоксикоза является достижение эутиреоидного состояния, а также купирование симптомов патологии сердечно-сосудистой системы.
Первой линией препаратов в лечении тиреотоксикоза, согласно протоколам по детской эндокринологии (приказ МОЗ Украины №254 от 27.04.2006 г.), являются тиреостатики: тирозол, мерказолил, тиамазол, метизол и др. Начальная доза — 0,3–0,5 мг/кг в сутки в зависимости от тяжести тиреотоксикоза. Доза делится на 2–3 приема. При клиническом улучшении (нормализация пульса, отсутствие клинических проявлений тиреотоксикоза), в среднем через 14–21 день, далее каждые 10–16 дней, дозу снижают на 2,5–5 мг до поддерживающей. Средняя поддерживающая доза — 2,5–7,5 мг/сутки (приблизительно 50% от начальной) – 1 раз в день. Подобную терапию продолжают в течение 1–1,5 лет. Длительность тиреостатической терапии у детей может достигать 2 лет.
Использование настоящей схемы предполагает постоянный контроль за функцией щитовидной железы с соответствующей коррекцией дозы для поддержания эутиреоидного состояния.
На фоне приема препаратов тиамазола могут возникать побочные эффекты: аллергические реакции в виде зудящей кожной сыпи, тошноты, изменений со стороны периферической крови: лейкопении, агранулоцитоза, тромбоцитопении.
Патогенетическую тиреостатическую терапию при тиреотоксикозе сочетают с применением β-адреноблокаторов, которые тормозят активность симпатоадреналовой системы, уменьшая нагрузку на сердце и снижая потребность миокарда в кислороде.
Бета-адреноблокаторы (анаприлин, пропранолол) — первые 4 недели, одновременно с тиреостатиками — 1–2 мг/кг в сутки в 3–4 приема. При нормализации пульса — постепенное снижение дозы до полной отмены препарата (резкое прекращение приема препарата может приводить к «синдрому отмены» с ухудшением состояния).
Совместное использование β-адреноблокаторов с тиреостатиками приводит к более быстрому устранению тахикардии. Кроме этого, применение β-блокаторов способствует уменьшению выраженности потливости, тремора и повышенной возбудимости. Однако необходимо отметить, что β-блокаторы не являются средством этиотропного лечения и должны использоваться только в сочетании с патогенетической (тиреостатической) терапией.
Показания для назначения глюкокортикоидов
- тяжелое течение тиреотоксикоза в сочетании с эндокринной офтальмопатией;
- признаки надпочечниковой недостатночности;
- лейкопения, тромбоцитопения;
- в случае присоединения сопутствующей патологии,
- на фоне стресса – для предупреждения острой надпочечниковой недостаточности.
Назначается преднизолон коротким курсом в средней дозе 0,2–0,3 мг/кг/сутки в 2–3 приема, с постепенным снижением через 7–10 дней на 2,5–5 мг каждые 5–7 дней до полной отмены.
Дополнительные методы лечения: санация очагов хронической инфекции, седативные препараты, витамины, гепатопротекторы.
Длительность терапии, в среднем, 1–2 года; у некоторых больных достигает 3 и более лет. Лечение проводят под контролем анализов крови (при начальной дозе – 1 раз в неделю). При появлении лейкопении назначают стимуляторы лейкопоэза (пентоксил, лейкоген, нуклеинат натрия и др.) в сочетании с преднизолоном. Повторная реакция крови после возобновления лечения требует его прекращения.
Хирургическое лечение показано при тяжелых формах диффузного токсического зоба, не поддающегося консервативной терапии. В предоперационном периоде большое внимание уделяют назначению стероидных препаратов. За 2 недели до оперативного вмешательства назначают преднизолон по 5–10 мг/сутки, по показаниям — за 1–2 дня до операции — гидрокортизон по 25–50 мг в/м, ДОКСА.
Основные принципы субтотальной субфасциальной резекции по О. В. Николаеву
- минимальное травмирование тканей достигается ограничением зоны операции пределами 4-й фасции шеи, которая висцеральным листком покрывает щитовидную железу, а париетальным – прилегающие к ней мышцы;
- минимальная кровопотеря;
- правильное положение больного на операционном столе;
- совершенная анестезия.
Соблюдение этих условий обеспечивает профилактику послеоперационного тиреотоксикоза.
Проводя дифференциальную диагностику тиреотоксикоза, необходимо отметить, что признаки тиреотоксикоза могут появляться также и в начальной стадии аутоиммунного тиреоидита, однако их выраженность и длительность значительно меньше, чем при ДТЗ.
Как правило, продолжительность тиреотоксической стадии АИТ не превышает нескольких недель, редко – до 4–6 месяцев, трансформируясь затем в гипотиреоз. В то же время при ДТЗ симптомы тиреотоксикоза прогрессивно нарастают.
Критерием адекватности терапии тиреотоксикоза у детей является стойкое поддержание нормального уровня Т4св. и ТТГ в течение 1 года после завершения лечения, что расценивается как наступление ремиссии.
В качестве примера поздней диагностики диффузного токсического зоба приводим клинический случай из практики.
Девочка Л. П., 16 лет, поступила в эндокринологическое отделение с жалобами на увеличение щитовидной железы, общую слабость, раздражительность, учащенные сердцебиения, повышение артериального давления.
Болеет в течение 2,5 лет, когда впервые обнаружено увеличение щитовидной железы 1-й степени. При первоначальном определении тиреоидных гормонов выявлено снижение ТТГ до 0,07 МЕ/мл (N 0,23–3,4), повышение Т4св. и Т3св. в 1,5-2 раза, уровень АТ-ТПО составлял 180,1 МЕ/мл (N до 34,0). Эндокринологом по месту жительства был диагностирован аутоиммунный тиреоидит, назначен йодомарин 150 мкг в сутки, который больная получала в течение 6 месяцев. При повторном УЗИ щитовидной железы было выявлено ее увеличение до 2-й степени, снижение уровня ТТГ, повышение Т4св. в 2,5 раза, нарастание в динамике АТ-ТПО. Тогда же впервые мать отметила увеличение глаз у девочки, а также была зарегистрирована артериальная гипертензия в пределах 130–140/60–70 мм. рт. ст., сопровождавшаяся головной болью. Диагноз эндокринолога по месту жительства: аутоиммунный тиреоидит. Рекомендовано продолжить прием йодомарина в той же дозе, дополнительно назначен пумпан. В дальнейшем мать заметила прогрессирующее увеличение глаз у ребенка, наросла раздражительность, плаксивость, появился тремор пальцев рук, сердцебиение. Направлена в клинику для уточнения диагноза и определения тактики лечения.
 При осмотре девочка правильного телосложения, пониженного питания. Рост 169 см, масса тела 46 кг, ИМТ – 16,01 кг/м2. Половое развитие – 5 стадия по Tanner. АД 150/70 мм рт. ст. Кожные покровы розовые, теплые, гипергидроз ладоней, движения суетливые, тремор тела и пальцев рук. Положительные симптомы Мари и «телеграфного столба». Выражен экзофтальм, гиперпигментация и отечность век. Положительные симптомы Жоффруа, Мебиуса, Штельвага, Дельримпля. Область шеи деформирована за счет увеличенной щитовидной железы, консистенция ее при пальпации мягко-эластическая. В легких дыхание везикулярное. Тоны сердца громкие, ритмичные, ЧСС – 120/мин.
При осмотре девочка правильного телосложения, пониженного питания. Рост 169 см, масса тела 46 кг, ИМТ – 16,01 кг/м2. Половое развитие – 5 стадия по Tanner. АД 150/70 мм рт. ст. Кожные покровы розовые, теплые, гипергидроз ладоней, движения суетливые, тремор тела и пальцев рук. Положительные симптомы Мари и «телеграфного столба». Выражен экзофтальм, гиперпигментация и отечность век. Положительные симптомы Жоффруа, Мебиуса, Штельвага, Дельримпля. Область шеи деформирована за счет увеличенной щитовидной железы, консистенция ее при пальпации мягко-эластическая. В легких дыхание везикулярное. Тоны сердца громкие, ритмичные, ЧСС – 120/мин.
Данные лабораторных и инструментальных исследований. Общий анализ крови в пределах нормы. Незначительно повышены уровни трансаминаз и щелочной фосфатазы. Оральный глюкозо-толерантный тест: тощаковая гликемия – 4,6 ммоль/л, через 2 часа – 6,1 ммоль/л. Уровень гормонов: ТТГ – 0,005 МЕ/мл (N 0,27–4,2), Т4св. – 5,13 нг/дл (N 1,1–1,8), Т3св. – 26,59 пг/мл (N 2,3–5,0), АТ-ТПО – 235,7 МЕ/мл (N до 34,0), АТ к рецепторам ТТГ – более 40 МЕ/мл (N до 1,75). ЭКГ: ритм синусовый, 120 в минуту. УЗИ щитовидной железы: диффузные изменения, эхогенность повышена, увеличение объема до 52,3 см3.
На основании анамнестических, клинических, лабораторных и инструментальных данных обследования установлен диагноз: «Диффузный токсический зоб 2 степени, тиреотоксикоз средней тяжести». Назначена терапия тирозолом в стартовой дозе 25 мг в сутки в сочетании с анаприлином 50 мг в сутки, которая проводилась в течение 3-х недель с последующим постепенным снижением дозы обоих препаратов и отменой, в дальнейшем, анаприлина. На фоне проводимой терапии достигнуты признаки клинико-лабораторного эутиреоза. В настоящее время продолжает получать поддерживающую дозу тирозола – 5 мг в сутки. Через 6 месяцев от начала терапии объем ЩЖ уменьшился вдвое, нормализовались уровни тиреоидных гормонов (ТТГ – 0,8 МЕ/мл, Т4св. – 1,6 нг/дл), уменьшился объем щитовидной железы до 16,4 см3.
Таким образом, данный случай демонстрирует пример поздней диагностики диффузного токсического зоба, который ошибочно рассматривался как тиреотоксическая стадия аутоиммунного тиреоидита.
Учитывая ряд сложностей в постановке диагноза тиреотоксикоза, нами предложена схема дифференциальной диагностики диффузного токсического зоба и тиреотоксической стадии АИТ (см. таблицу 3).
Важно отметить, что, клинически значимыми антитиреоидными антителами при тиреотоксикозе являются: АТ-ТПО, однако, их определение целесообразно только в случаях нарушенной функции ЩЖ. При этом повышение их титра позволяет высказать предположение об АИТ – болезни Хашимото. При ДТЗ титры АТ-ТПО, как правило, ниже, чем при АИТ. Определение содержания АТ-ТПО в динамике нецелесообразно, так как они не обладают прогностической ценностью.
Что касается антител к рецепторам ТТГ, то их повышение весьма характерно для ДТЗ, что может явиться одним из ведущих лабораторных критериев для диагностики тиреотоксикоза. Кроме того, определение уровня АТ к рецепторам ТТГ в динамике позволяет оценить прогноз в условиях проведения и после окончания тиреостатической терапии (определение риска рецидива этого заболевания).
Выводы
- Проведение дифференциальной диагностики тиреотоксикоза у детей предполагает оценку, прежде всего, длительности и выраженности клинико-лабораторных симптомов, таких как зоб, экзофтальм, тахикардия, которые типичны для диффузного токсического зоба. При этом признаки тиреотоксикоза, наблюдаемые в начальной стадии аутоиммунного тиреоидита, менее выражены, нежели при диффузном токсическом зобе.
- Повышение уровня антител к тиреоидной пероксидазе характерно не только для аутоиммунного тиреоидита, но и для диффузного токсического зоба, ввиду аутоиммунного генеза последнего.
- Повышенный уровень антител к рецепторам тиреотропного гормона является одним из наиболее важных диагностических критериев диффузного токсического зоба, наряду со снижением тиреотропина и повышением уровней свободного тироксина и свободного трийодтиронина.

КОНТРАЦЕПЦІЯ У ПІДЛІТКІВ
 Підвищення сексуальної активності підлітків порушує таку важливу медичну проблему як ризик вагітності, а також соціальні, економічні та виховні аспекти, що виникають при ранніх статевих відносинах у підлітковому віці, особливо при незапланованій вагітності
Підвищення сексуальної активності підлітків порушує таку важливу медичну проблему як ризик вагітності, а також соціальні, економічні та виховні аспекти, що виникають при ранніх статевих відносинах у підлітковому віці, особливо при незапланованій вагітності
Невтішна статистика
У світі відмічено зростання статевої активності серед підлітків. Незважаючи на те, що випадки небажаної підліткової вагітності спостерігалися й раніше, останнім часом відзначено зростання кількості статевих зв’язків у більш ранньому віці. Зокрема, С. Пилипенко (2010), О. В. Горбенко (2007), В. Кукочка (2009) констатують, що в умовах сьогодення 88% дівчат і 100% юнаків позитивно ставляться до дошлюбних статевих стосунків [1, 2, 3]. Досвід випадкових статевих контактів зареєстровано серед 35–40% учнівської молоді, приблизно 60% вважають своє статеве життя регулярним, понад 50% відмічають часту зміну сексуальних партнерів. При цьому вражає нерозбірливість підлітків у виборі сексуальних партнерів і той факт, що понад 20% підлітків вступають в інтимні стосунки у перші дні знайомства.
Серед дівчат, які живуть статевим життям, лише 55% регулярно використовують запобіжні засоби [4, 5, 6, 7].
Це призводить до вкрай високої кількості абортів у неповнолітніх, поширеності венеричних хвороб і зростання кількості неповнолітніх матерів.
В усьому світі щорічно здійснюється 50 млн. абортів, 10% яких припадає на пацієнток віком від 15 до 19 років [7, 8, 9]. Наслідками аборту є різні інфекційні захворювання, безпліддя і навіть смерть. Отже, сексуальним партнерам дуже важливо володіти знаннями про методи запобігання небажаній вагітності та хворобам, що передаються статевим шляхом. Стан репродуктивного здоров’я людини тісно пов’язаний з різнобічними аспектами планування сім’ї. Тому статева просвіта у поєднанні з підготовкою до створення майбутньої сім’ї та проведення консультативних послуг з планування сім’ї сприятимуть відстроченню початку статевого життя.
Дитячі рішення – дорослі проблеми
Планування сім’ї вважається основним засобом збереження здоров’я жінок та чоловіків, а також відноситься до розряду фундаментальних прав людини. Впровадження концепції охорони репродуктивного здоров’я є пріоритетною у всьому світі, суттєво впливає на демографічну ситуацію у країні, зниження рівня материнської та дитячої смертності, ускладнень вагітності та пологів [8, 10].
За визначенням Всесвітньої організації охорони здоров’я (ВООЗ), під репродуктивним здоров’ям розуміють стан повного фізичного, психічного і соціального комфорту, а не лише відсутність хвороб репродуктивної системи чи порушення її функцій [4, 5, 6]. Поняття «репродуктивне здоров’я» включає в себе і сексуальне здоров’я – стан, що дозволяє людині повністю відчувати статевий потяг та реалізовувати його, отримуючи при цьому задоволення. В основі сексуального здоров’я лежить статеве виховання. Сексуальне здоров’я пов’язане із сексуальністю, що є центральним аспектом людського буття протягом усього життя і включає в себе секс, статеву ідентифікацію та народження дітей [11, 12]. Формування репродуктивного здоров’я – дуже складний і тривалий процес, оскільки значною мірою визначається умовами розвитку жінки, починаючи ще з особливостей перебігу внутрішньоутробного періоду.
Найбільше навантаження на репродуктивне здоров’я припадає на дітей підліткового віку та молодь. Відповідно до українського законодавства, використовується така вікова градація: діти — 0–18 років, діти підліткового віку (підлітки) — 14–18 років, молодь — 18–35 років [8]. У підлітковому віці відбувається бурхливий розвиток індивіда як на соматичному, так і на психічному рівнях формуванням усіх функціональних систем організму і цілісної особистості. Саме в цей період відбувається активний розвиток репродуктивної сфери та формуються основи репродуктивної поведінки [10, 12].
Коли людина вступає у пубертатний період, вона не стає дорослою, але перестає бути дитиною. Розпочинається підлітковий вік, доволі кризовий період життя. У підлітка змінюється ставлення до себе і навколишнього світу, розвивається мислення. Дуже важливими стають стосунки з ровесниками, позиція у їхньому колективі. Часто підлітки сприймають себе як дорослих, але батьки і вчителі вважають їх дітьми. Таке становище сприяє виникненню кризи.
Підлітки намагаються самоствердитися в колективі ровесників, похизуватися, продемонструвати свою дорослість і «крутизну». У цьому прагненні здобути визнання і повагу вони здатні на необдумані вчинки [3, 7, 13].
Сучасний стан здоров’я молоді, який із року в рік погіршується, зумовлений низьким економічним рівнем сімей, фізичними та психоемоційними навантаженнями, наявністю стресових ситуацій та іншими факторами [4, 14]. Провідну роль відіграють і виявлені ознаки кризових явищ в ідеологічній та духовній сферах підлітків і молоді, поширення шкідливих звичок і ризикової поведінки серед цієї категорії. До вагомих факторів, які впливають на стан репродуктивного здоров’я молоді, слід віднести й такі психосоціальні чинники як вільне ставлення до шлюбу; недостатній рівень загальної та репродуктивної культури населення; високий рівень штучного переривання вагітності, що (особливо у ранньому репродуктивному віці) ставить під загрозу репродуктивні можливості жінки у майбутньому; трансформацію репродуктивної поведінки [4, 15].
Суспільство стало більш припустимо ставитись до дошлюбних статевих стосунків. На тлі цього спостерігається масове зниження віку початку статевого життя і відповідно, зростання кількості підліткових вагітностей та абортів [14, 16]. У більшості українських сімей статеве виховання неадекватне, тому молоді люди отримують відповідну інформацію від товаришів, яка часто буває неправильною чи недостатньою.
Особливістю нашого часу стала відсутність системи фахового статевого виховання та великий тиск на молодь сексуально спрямованої та сексуально агресивної реклами і засобів масової інформації (ЗМІ) [12]. Серед джерел інформації для підлітків щодо питань статевих відносин перше місце поділяють ЗМІ та старші за віком підлітки — 70–80% інформації, друге місце посідають друзі — 30–40%, далі йдуть педагоги — 10–20%, представники громадських установ та лікарі — 1–20% інформації [17]. Завершують цей перелік батьки — 1–10% інформації. Отже, основним чином саме ЗМІ та старші за віком підлітки виконують функцію сексуальної просвіти щодо сучасних підлітків.
Підлітки не повністю усвідомлюють зв’язок між сексуальними стосунками і вагітністю, їхня сексуальна активність поєднується з дефіцитом знань щодо попередження незапланованої вагітності, інфекцій, що передаються статевим шляхом та вірусу імунодефіциту людини (ІПСШ\ВІЛ), що призводить до незапланованої вагітності і пологів у ранньому віці чи абортів, запальних захворювань органів малого тазу, і як наслідок, до порушень репродуктивного здоров’я [1, 2, 18, 19]. Тому потрібне об’єднання зусиль медиків, батьків, освіти та соціальної служби. При цьому слід підкреслити, що реальна інформація про методи планування сім'ї та їх вплив на статеву поведінку недостатня та не завжди відповідає потребам дівчат-підлітків.
Планування сім’ї – комплекс медико-соціальних заходів, спрямованих на зниження захворюваності, збереження здоров’я жінок, запобігання незапланованій вагітності, забезпечення оптимальних інтервалів між пологами, кількості дітей у сім’ї, попередження занадто ранніх, пізніх, частих пологів, профілактику інфекцій, що передаються статевим шляхом, ВІЛ (Міжнародна конференція з питань народонаселення і розвитку, Каїр, 1994 р.) [8].
Виважена альтернатива
Однією з складових системи планування сім’ї є контрацепція – методи попередження незапланованої вагітності [8, 10, 20]. Уникнення незапланованої і ризикованої вагітності є основною стратегією зменшення дитячої та материнської смертності. Ефективним заходом удосконалення та покращення послуг з планування сім’ї є вибір методу контрацепції відповідно до періодів життя, післяпологової та післяабортної контрацепції з дотриманням прав пацієнта, його бажання, можливостей, прихильності до застосування того чи іншого контрацептиву.
Попередження ранньої вагітності, а саме відстрочення народження першої дитини до 20-річного віку матері має великі переваги як для самої матері, так і для дитини. Слід зазначити, що перші пологи більш рекомендовані після досягнення жінкою 20-річного віку. У матерів віком до 20 років зростає ризик народження дітей з меншою вагою, підвищується рівень малюкової смертності (Botting et al., 1998), виникають проблеми з грудним вигодовуванням, серед 15–19-річних удвічі збільшується ризик смерті при народженні дитини порівняно з 20–24-річними (ФНООН, 1997) [8].
Найбільш вдалою альтернативою штучного переривання вагітності є контрацепція. Але впровадження даної альтернативи ускладнюється низькою обізнаністю сучасної молоді щодо засобів контрацепції і відсутності у них відповідального ставлення до свого статевого життя.
Згідно з рекомендаціями ВООЗ («Медичні критерії прийнятності використання методів контрацепції», четверте видання, 2009), підлітки можуть використовувати будь-який метод контрацепції і повинні мати велику свободу вибору у цьому плані [8]. Сам собою вік не є достатньою основою для обмеження доступу до того чи іншого методу контрацепції.
Консультативні послуги з питань контрацепції повинні ґрунтуватися на принципах поважання прав людини та передбачати комплексну оцінку життєвих обставин і стану здоров’я пацієнта з урахуванням його потреб [7, 10, 22]. При виборі контрацептивного засобу фахівець і пацієнт виходять з того, що метод повинен бути ефективним і зручним у застосуванні, можливий ризик ускладнень має бути зведений до мінімуму. Протизаплідний ефект має бути тимчасовим, щоб репродуктивна функція могла відновлюватись за бажанням користувача. При цьому не повинні порушуватися фізіологія статевого акту і виникати негативні емоції. Метод може також позитивно впливати на здоров’я користувача (нормалізація гормональних порушень, запобігання ІПСШ тощо). Однією з важливих умов надійної контрацепції та її тривалого використання має бути доступність методу (помірна ціна, наявність у продажу).
Консультування є важливою умовою для початку та продовження використання пацієнтом методу планування сім’ї. Під час консультування підлітків необхідно враховувати відмінність підлітків за духовним та фізичним розвитком від дорослої людини, відсутність шлюбного статусу, емоційну, юридичну та фінансову залежність від батьків, особистий досвід статевого життя, негативне ставлення суспільства до ранніх статевих дошлюбних контактів [23]. Усі ці особливості негативно впливають на широке впровадження медичної допомоги з питань контрацепції у підлітків у повсякденне життя.
Основними принципами консультування підлітків є встановлення довіри між лікарем та пацієнтом-підлітком та забезпечення конфіденційності [24]. Для підлітка на перший план виступає відчуття «людського відношення» з боку лікаря, в основу чого покладена довіра. Підлітки, як правило, бояться осуду своєї поведінки з боку дорослих, або ж своїх однолітків і хочуть бути впевненими в тому, що їх таємниця не буде розголошена. Крім цього, їх обіймає страх, що батьки будуть знати про їхнє інтимне життя. Підлітки хочуть бути впевненими, що лікарі допоможуть їм вирішити проблеми і не стануть втручатися у їхнє особисте життя. Встановлення довірчих відносин з підлітками вимагає співчуття і неупередженого відношення з боку медичних працівників.
Консультування з питань планування сім’ї повинно допомогти підлітку набути знань про відповідальну статеву поведінку та безпечні статеві стосунки, бути зацікавленим у профілактиці порушень здоров’я, вибрати метод контрацепції та правильно його використовувати [10, 23, 24]. Консультант має обговорити з підлітком можливі медичні проблеми, пов’язані з раннім початком статевого життя, такі як ризик виникнення раку шийки матки, а також пряму залежність між кількістю сексуальних партнерів і ризиком виникнення захворювань, що передаються статевим шляхом. Підлітків слід поінформувати про місце звернення у разі виникнення проблем репродуктивної сфери чи використання методу контрацепції.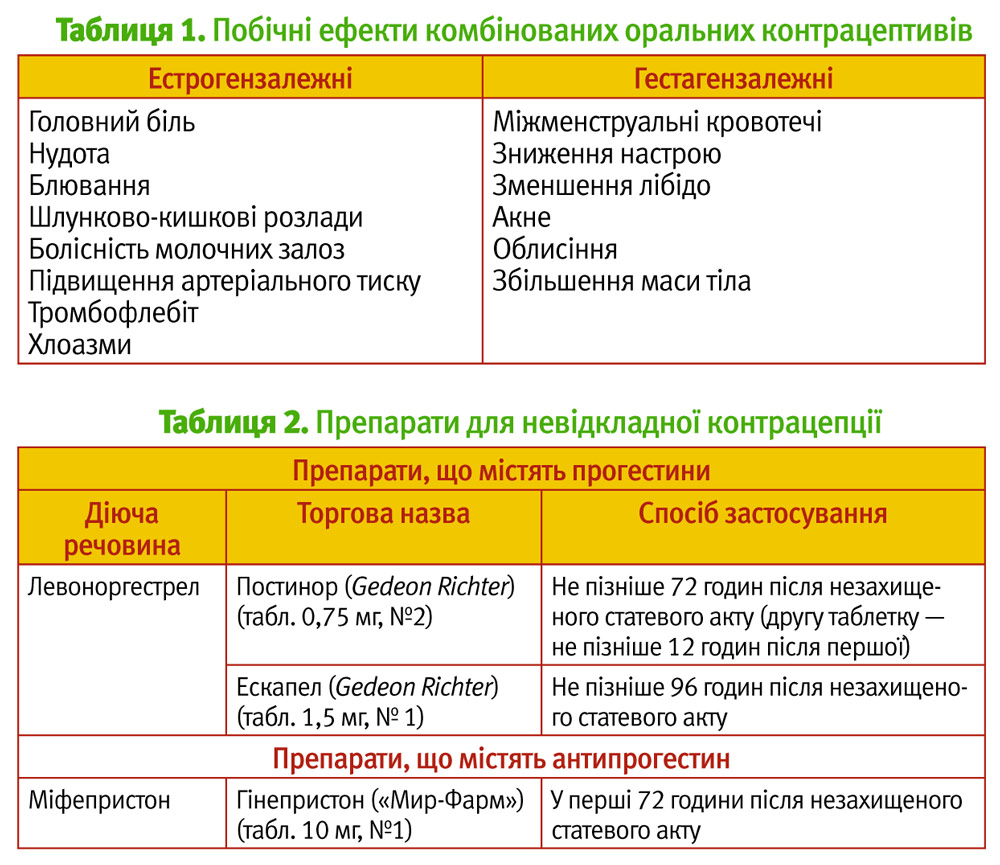
Якісне консультування концентрується на потребах конкретного пацієнта у конкретній ситуації, що є запорукою успіху використання конкретного засобу контрацепції та попередження незапланованої вагітності [8]. Професіоналізм консультанта залежить багато в чому від його готовності вислухати, правильно і своєчасно відповісти на всі запитання та намагатися подолати сумніви пацієнта про вибір методу.
Перед проведенням консультування доцільно визначити рівень поінформованості підлітка щодо методів контрацепції. У подальшому консультування проводиться з урахуванням його рівня знань.
Для підлітків, які мають статеві стосунки, консультація про методи контрацепції починається з бесіди про те, що найнадійнішим способом уникнення вагітності та, безперечно, найкращим засобом контрацепції для молодих людей є відсутність сексуальних контактів [23, 24]. Необхідно пояснити підлітку, що утримання (відсутність статевих стосунків) – найкращий захист від захворювань, які передаються статевим шляхом.
Під час початкового (первинного) консультування описуються методи контрацепції, і пацієнту допомагають обрати той, який найбільше йому підходить. Інформація про метод, який зацікавить пацієнта, повинна включати механізм дії ефективність методу, переваги і недоліки, можливі побічні ефекти, можливість повторного звернення під час виникнення запитань. Слід заохочувати підлітка ставити запитання.
Участь батьків в консультуванні їхніх дітей з проблем сексуальної поведінки вважається дуже делікатною проблемою [23, 24]. Юридична сторона консультування підлітка передбачає необхідність поставити до відома батьків. У тих випадках, коли підліток бажає збереження конфіденційності, лікар повинен надати консультацію чи допомогу без відома батьків. За можливості вибору, рішення приймається за участю батьків.
Визначаємо орієнтири
Із сучасних методів контрацепції підліткам можуть бути рекомендовані бар’єрні, хімічні, гормональні методи, а також методи невідкладної контрацепції [15, 16, 20]. Слід враховувати, що кожен метод, поряд з перевагами, має свої недоліки, що обмежує його застосування.
Презерватив вважається найкращим засобом контрацепції для підлітків [18, 19, 22]. Використання чоловічого презерватива захищає не лише від небажаної вагітності, але й від ІПСШ, у тому числі від ВІЛ. Перевагами є також мала ймовірність побічних ефектів, можливість застосування без призначення лікаря, простота використання та відносна дешевизна. Основними недоліками є дискомфорт, алергічні реакції на латекс, відносно частий розрив презерватива, залежність від партнера. Піхвові діафрагми та шийкові ковпачки внаслідок низької ефективності та досить складної техніки використання мало підходять для цієї вікової категорії. Контрацептивна губка, що поєднує в собі механічний та хімічний методи, також має відносно низьку ефективність.
Сперміцидні методи контрацепції, дія яких проявляється у фрагментації сперматозоїдів, можуть бути рекомендовані підліткам у поєднанні з бар’єрним методом, що знижує ризик вагітності та забезпечує захист від інфекцій, що передаються статевим шляхом [13, 25]. Недоліками сперміцидів є необхідність введення перед кожним статевим контактом, можливі незручності під час введення і вилучення з піхви, а також необхідність спеціального догляду, що обмежує застосування цього методу підлітків. Перевагою бар’єрних та сперміцидних методів є можливість їх використання при нерегулярних та епізодичних статевих відносинах.
До високоефективних методів попередження небажаної вагітності, які можуть бути рекомендовані підліткам, відносять гормональні контрацептиви. Варто зауважити, що гормональна контрацепція допустима для підлітків, які ведуть регулярне статеве життя і мають достатню інформацію про застосування цього методу [7, 10, 13].
У випадку призначення гормональних контрацептивів дівчаткам-підліткам необхідно враховувати сімейний анамнез, характер місячних і частоту статевих стосунків, початок регулярних місячних, екстрагенітальні захворювання [8, 16].
Механізм дії гормональних контрацептивів полягає у пригніченні секреції гонадотропних гормонів та овуляторної функції яєчників, підвищенні в’язкості цервікального слизу, що перешкоджає проникненню сперматозоїдів у порожнину матки, попередженні імплантації яйцеклітини у зв’язку зі змінами ендометрію.
Гормональні препарати з контрацептивною дією представлені монокомпонентними, що містять гестагени, та комбінованими лікарськими засобами, до складу яких входять гестагенний та естрогенний компоненти [18]. Естроген у комбінованих контрацептивних засобах представлений етінілестрадіолом або естрадіолу валератом. Головними небажаними побічними ефектами гестагенного компоненту є збільшення маси тіла, посилення росту небажаного волосся, депресія, зменшення толерантності до глюкози. Тому гестагенний компонент упродовж часу існування комбінованих контрацептивних засобів зазнає постійного вдосконалення.
Вибір гормональної контрацепції має бути особливо ретельним у групі жінок до 18 років, бо в цій групі збереження репродуктивного здоров’я є підґрунтям народження майбутніх поколінь. Особливість репродуктивної системи у період статевого становлення обумовлена функціональною незрілістю. Серед комбінованих оральних контрацептивів (КОК) для підлітків найбільш прийнятними є мікродозовані (містять 0,015–0,020 мг етінілестрадіолу) та високоселективні прогестагени третього покоління. Для цієї вікової категорії ВООЗ рекомендує монофазні та трифазні КОК, які забезпечують найменше втручання у перебіг фізіологічних процесів в організмі підлітків.
Протягом останніх десятиліть пошуки нових гормональних контрацептивів були спрямовані на зниження дози естрогенного компоненту, а також на застосування більш адекватних гестагенів. В останні роки відбуваються позитивні зміни щодо гормональної контрацепції у підлітків як з боку медиків, так і суспільної думки [26].
Перевагами застосування КОК підлітками є зменшення випадків надмірних менструальних кровотеч та альгодисменореї, порушень менструального циклу, частоти фолікулярних кіст яєчника, анемії, ендометріозу, вугрового висипання [23].
Під час застосування КОК можуть виникати побічні ефекти, що поділяються на естроген- та гестагензалежні (табл. 1). Слід пам’ятати, що ці побічні ефекти, особливо у препаратів останнього покоління, зведені до мінімуму [16, 21]. Вони спостерігаються у перші місяці прийому, потім зменшуються або повністю зникають.
Оральні контрацептивні таблетки стають усе більш популярними серед підлітків, тому що вони не впливають на сексуальну активність і забезпечують високий контрацептивний ефект. Кількість невдач у 4 рази вища у тих, хто використовує презервативи, і у 6–7 разів – при використанні сперміцидів. З цієї причини значна частина сексуально активних підлітків обирає КОК [23].
Мікродози гестагенів (міні-пілі) можуть бути застосовані у підлітків, які мають протипоказання до прийому КОК: порушення згортання крові, цукровий діабет, захворювання печінки та ін. Ін’єкційні та підшкірні імпланти для дівчаток застосовувати небажано.
У даний час накопичується досвід використання підлітками альтернативних таблеткам методів гормональної контрацепції (вагінальне кільце, контрацептивний пластир). Ефективність цих засобів контрацепції не поступається КОК, багато жінок надають їм перевагу, особливо молоді жінки, яким складно пам'ятати про щоденний прийом таблеток.
У дослідженнях А. Д. Зернюк (2006) відзначена 100% контрацептивна ефективність пластиря у підлітків, спостерігалося позитивне сприйняття більшістю дівчат даного засобу за рахунок простоти застосування, відсутності неприємних відчуттів під час статевого контакту [26]. Перевагою стала відсутність необхідності щоденного застосування препарату, що знімало психологічну напругу у підлітків, у яких немає навиків прийому гормональних контрацептивів. Відзначено позитивний терапевтичний ефект контрацептивного пластиря у пацієнток з різними формами порушення менструального циклу (дисменорея, передменструальний синдром, гіперполіменорея).
На думку Ю. А. Гуркіна, А. Д. Зернюк (2009), сучасні гормональні контрацептиви високоефективні (100%), легко переносяться і прийнятні юними жінками, незалежно від способу застосування, та складають основу контрацептологічного супроводу сучасних підлітків (у проведених дослідженнях комплаєнтність препаратів становила: КОК – 76,5%, вагінального кільця – 78,6%, контрацептивного пластиря – 63,6%) [27]. Іноваційні гормональні контрацептиви (вагінальне кільце і контрацептивний пластир) можуть бути рекомендовані як засоби першого вибору, за рахунок простоти і зручності у використанні, що обумовлює меншу ступінь психологічного навантаження і гарантує меншу частоту порушення режиму застосування.
Серйозним недоліком гормональних засобів контрацепції є те, що вони не захищають від інфекцій, що передаються статевим шляхом. З урахуванням даної проблеми жінкам цієї вікової групи рекомендовано так званий подвійний голландський метод: одночасне застосування гормонального орального контрацептиву з презервативом, коли висока ефективність орального контрацептиву поєднується з додатковою профілактичною дією презерватива [19, 28].
Диспансерне спостереження необхідне за всіма юними жінками, які використовують гормональні методи контрацепції, оскільки це дозволяє деталізувати підбір контрацептивів, своєчасно попередити розвиток негативних побічних ефектів, і тим самим зменшити відсоток відмови від подальшого використання гормональної контрацепції.
Невідкладна допомога
Актуальним для підлітків є питання невідкладної контрацепції [10, 26]. Застосування засобів невідкладної контрацепції не повинно бути постійним, але інформацію про можливість їх використання необхідно поширювати серед підлітків, оскільки саме ця сексуально активна група перебуває в зоні ризику незапланованої вагітності. Раціональне використання невідкладної контрацепції сприяє зменшенню кількості абортів.
Невідкладна контрацепція — методи, які застосовують після статевого акту, але перед імплантацією, і призначені в якості резервного засобу для епізодичного використання, а не як основний метод. Існує декілька варіантів невідкладної контрацепції: введення ВМС, застосування таблетованих препаратів, які містять естрогени і прогестагеновий компонент — КОК (метод Юзпе), тільки прогестагеновий компоненет – левоноргестрел та антипрогестагеновий препарат міфепристон [28].
До сучасних методів невідкладної контрацепції, що можуть бути рекомендовані дівчатам до 18 років, відносять КОК, які застосовуються за методом Юзпе: дворазове призначення 200 мкг етінілестрадіолу та 1 мг левоноргестрелу протягом 72 годин після статевого акту з перервою у 12 годин. Перевагою цього методу є те, що з цією метою можна використовувати будь-який КОК, що є у продажу, при цьому кількість таблеток залежатиме від їх складу та дозування. Такий метод контрацепції повинен контролюватися лікарем та має побічні ефекти: нудота спостерігається у 64%, блювання — у 16%, частота невдач коливається у межах 0,2–7,4% випадків [28].
Для невідкладної контрацепції можуть бути рекомендовані також спеціальні препарати (табл. 2). За рекомендаціями ВООЗ, препаратом першого вибору є левоноргестрел у дозі 1,5 мг. Це зумовлено тим, що він не чинить тератогенного ефекту. Завдяки цьому, у тих випадках, коли жінка все ж таки завагітніла, можливо зберегти вагітність.
Слід пам’ятати, що застосування методів невідкладної контрацепції для жінок усіх вікових груп можливе лише в екстрених випадках та не повинно бути регулярним.
Не рекомендується!
ВМС підліткам застосовувати недоцільно внаслідок недостатніх розмірів матки, а також у випадку наявності декількох статевих партнерів. Для дівчаток-підлітків існує великий ризик запальних захворювань статевих органів у разі використання внутрішньоматкового засобу [23]. Велика кількість експульсій, больовий синдром та збільшення кількості менструальної крові зумовлюють неприйнятність цього методу контрацепції для підлітків. Враховуючи великий ризик запальних захворювань статевих органів, пов'язаний з незапланованою сексуальною поведінкою, підліткам не варто рекомендувати застосування ВМС.
Природні методи контрацепції для підлітків небажані через низьку ефективність, адже їх застосування потребує від дівчини високого рівня медико-біологічних знань, досвіду, навичок, регулярного фіксування дат менструації. Однак, у будь-якому випадку консультанти повинні знайомити підлітків із змінами в жіночому організмі, пов’язаними з менструальними циклами.
Таким чином, для підлітків, які мають статеві контакти, необхідний доступний метод контрацепції. На сьогодні існує великий вибір. Причому одні засоби та методи найкраще підходять для підлітків (бар'єрний метод у поєднанні зі сперміцидами, гормональні препарати), тоді як інші є малопридатними для них (внутрішньоматкові засоби, природні методи).
Необхідно здійснювати індивідуальний підбір методу контрацепції з урахуванням характеру і ступеня відповідальності підлітка, інтенсивності його статевого життя, наявності або відсутності екстрагенітальних захворювань, постійного статевого партнера і планів щодо термінів майбутньої вагітності. Правильна та сучасна контрацепція дозволяє зберегти репродуктивне здоров'я дівчини-підлітка та майбутньої матері.
Більшість молодих людей мають потребу у підвищенні рівня знань щодо методів контрацепції. На жаль, у молоді простежується тенденція самостійно вирішувати проблеми репродуктивного здоров’я і розвитку, без допомоги досвідчених фахівців, що ускладнює ситуацію щодо охорони їхнього здоров’я. Це потребує вирішення питань статевої освіти та культури підлітків і молоді.
Перелік літератури
знаходиться у редакції.
Детальніше

УСКЛАДНЕННЯ ПІСЛЯ ВАКЦИНАЦІЇ
 Практичні аспекти нагляду за несприятливими подіями після імунізації при застосуванні вакцин, анатоксинів та туберкульозного алергену: роль лікаря першого контакту
Практичні аспекти нагляду за несприятливими подіями після імунізації при застосуванні вакцин, анатоксинів та туберкульозного алергену: роль лікаря першого контакту
Імунізація є одним з найбільш успішних і економічно ефективних засобів у збереженні здоров’я населення. Вона забезпечила глобальну ліквідацію віспи, а також поліомієліту в різних країнах світу. За оцінками ВООЗ, на даний момент імунізація щорічно запобігає від 2 до 3 мільйонів смертей від дифтерії, правця, кашлюку та інших інфекцій у всіх вікових групах. У 2011 році серед дітей віком один рік близько 83% (109 мільйонів немовлят) були вакциновані трьома дозами вакцини проти дифтерії, правця та кашлюку, близько 84% (110 мільйонів) – вакциною проти епідемічного паротиту і близько 88% (114 мільйонів) – вакциною БЦЖ.
Важливим компонентом програми вакцинації є безпека, що стала таким же важливим аспектом успішної програми імунопрофілактики, як і ефективність. Використання вакцин, порівняно з іншими лікарськими препаратами, супроводжується більшим ризиком виникнення кризових ситуацій – наприклад, недовіри, страхів, комунікаційних проблем. Це пов’язано із застосуванням вакцин за інших умов, ніж призначення з терапевтичною метою лікарських препаратів.
Так, вакцини зазвичай вводять особам без видимих ознак порушення здоров’я, в тому числі немовлятам. Умови, за яких вони вводяться, значно відрізняються – від спеціалізованих кабінетів великих медичних закладів до фельдшерсько-акушерських пунктів, сільських амбулаторій, амбулаторій сімейного лікаря. Оцінка, дозвіл на проведення вакцинації, контроль і нагляд за імунобіологічними препаратами – основні проблемні аспекти для національних регуляторних органів (наприклад, МОЗ України, Державної служби з лікарських засобів), обумовлені постійно зростаючою кількістю інноваційних препаратів, комплексними проблемами якості та новими досягненнями у галузі науки і техніки.
Складність виконання програм імунопрофілактики також пов’язана з тим, що переваги імунізації часто непомітні та неочевидні для більшості населення країни. Особливо, якщо частота захворювання, щодо якого проводиться вакцинація у відповідності до календаря щеплень, є низькою. Однак порушення здоров’я у щеплених часто безапеляційно пов’язують з проведеною вакцинацією, особливо, якщо вакцинована особа була здоровою на момент проведення імунізації. Хоча дане порушення здоров’я могло бути обумовлене іншими факторами, ці фактори часто залишаються поза увагою багатьох пересічних громадян країни, громадських активістів, а часто й медичних працівників, вони не враховуються при встановленні причинно-наслідкового зв’язку між проведеною вакцинацією та порушенням здоров’я, виникненням хвороби. Страх виникнення ускладнень, реальних чи уявних, утримує багатьох людей від вакцинації.
Проблеми, пов'язані з реакцією на вакцину, а також небажанням пройти вакцинацію, відомі вже протягом багатьох років у розвинених країнах і часто виникають на тлі успіхів від імунізації. З розширенням програм імунізації у країнах з низьким і середнім прибутком за останні кілька десятиліть подібні проблеми виникли також і в цих країнах.
Зважаючи на важливість та критичність розслідування будь-якого випадку порушення стану здоров’я після вакцинації, будь-які сигнали про те, що вакцини призводять до побічних явищ, необхідно розглядати швидко та ефективно. У зворотному випадку це може підірвати довіру до вакцини, вакцинації, поширюватимуться чутки, що в кінцевому підсумку матиме серйозні наслідки для охоплення щепленнями населення та рівня захворюваності.
Іноді для отримання переконливих доказів того, що вакцинація не є причиною виникнення тих чи інших хвороб, необхідно провести ряд додаткових досліджень. Проведення таких досліджень часто потребує декількох років (наприклад, щодо зв'язку аутизму з вакцинами проти кору, епідемічного паротиту і краснухи, енцефалопатії та кашлюку). Незважаючи на отримані надійні підтвердження, що вакцина є безпечною, довіру до вакцинації повернути тяжко, як і відновити рівні охоплення вакцинацією.
З іншого боку, завжди слід пам'ятати, що вакцини не на 100% безпечні, і що шкода може бути завдана внаслідок помилок, допущених при імунізації. Таким чином, побічні реакції, пов'язані з вакциною, і побічні явища, пов'язані з помилкою при імунізації, можуть виникнути у здорових пацієнтів, і тому повинні бути негайно виявлені для визначення подальших дій: від навчання медичного персоналу, що проводить вакцинацію, до заборони використання тієї чи іншої вакцини. Вжиття належних заходів до мінімізації побічних ефектів, у свою чергу, посприяє збереженню рівнів охоплення та перешкоджатиме поширенню чуток та страхів щодо вакцинації. Проведення розслідування, встановлення причинно-наслідкового зв'язку між вакцинацією та порушенням у стані здоров’я є ключовим компонентом оцінки ризиків НППІ, процесу прийняття рішень та ініціації дій.
Важливим також є розуміння, у першу чергу, медичним працівником, реальності виникнення побічних ефектів на вакцину, правильності трактування інструкцій до вакцин, анатоксинів, а саме розділу інструкції, у якому викладаються «побічні ефекти» на даний препарат.
Традиційно в Україні в інструкціях використовуються термін «Побічні ефекти», що у розумінні багатьох лікарів означає «прямий» зв’язок між вакциною та наведеним у даній інструкції порушенням здоров’я. Таке розуміння помилкове та небезпечне, оскільки призводить до неправильних висновків щодо реальних побічних ефектів на дану вакцину.
В англомовному варіанті це звучить як «Аdverse events/effects», що дослівно та за смислом перекладається як «Несприятлива подія/ефект». Також може бути використаний термін «Undesirable effects», що перекладається як «Небажані ефекти». Термін же «Side effects», що дослівно означає «Побічні ефекти», використовується лише для інцидентів, що мають доведений причинно-наслідковий зв’язок.
Розділ «Побічні ефекти» інструкцій вакцин, зареєстрованих в Україні, частіше відображає не побічні ефекти, що мають доведені причинно-наслідкові зв’язки, а відомості про порушення у стані здоров’я, що були зареєстровані як у доліцензійному, так і в післяліцензійному моніторингу.
Таким чином, правильне розуміння та трактування інформації, що подана в інструкції до вакцини, є важливим для уникнення помилкових тверджень щодо побічних ефектів, якісного консультування пацієнта перед вакцинацією та при проведенні розслідування післявакцинальних подій.
З метою моніторингу за можливими побічними ефектами вакцин, а також порушеннями у стані здоров’я, що можуть бути пов’язані не лише з вакциною як препаратом, а й з помилками техніки вакцинації, в світі використовується термін «Adverse event following immunization (AEFI)», що в адаптації до української мови звучить як «Несприятлива подія після імунізації (НППІ)». Відповідно до визначення ВООЗ, НППІ визначається як будь-яке несприятливе медичне явище, яке виникає після імунізації і не обов'язково має причинний зв'язок із застосуванням вакцини. Несприятливе явище може бути будь-якою несприятливою або небажаною ознакою, порушенням результатів лабораторних аналізів, симптомом або захворюванням. Визначення причинно-наслідкового зв’язку між НППІ та конкретною вакциною – складний процес, що передбачає оцінку багатьох факторів та певних критеріїв. Тут варто зауважити, що розуміється під причинно-наслідковим зв’язком. Причинно-наслідковий зв'язок – взаємозв'язок між двома явищами (причиною і наслідком (ефектом)), де друге явище є наслідком першого. Пряма причина – фактор, за відсутності якого ефект не виникає (необхідна причина). Іноді існує кілька факторів, які можуть спровокувати ефект (явище) або можуть відігравати роль супутніх чинників таким чином, що виникає ефект (явище). Багато факторів приймається до уваги при визначенні того, чи дійсно побічне явище викликане вакциною. Вакцини часто вводять дітям у тому віці, коли можуть проявитися багато патологічних станів, незалежно від того, чи була проведена вакцинація, чи ні. Вакцини, що вводяться дорослим, також можуть збігатися з абсолютно різними факторами ризику появи явища. Той факт, що введення вакцини передує виникненню явища, ще не свідчить автоматично про те, що вакцина викликала або сприяла розвитку цього явища. Адже при масовій вакцинації населення деякі серйозні порушення у стані здоров’я, що трапляються рідко, як на тлі вакцинації, так і без неї, будуть випадково співпадати з періодом після вакцинації серед вакцинованих.
Підтвердження зв'язку між вакциною, потенційною причиною і окремим явищем отримують з епідеміологічних досліджень відповідно до наукового методу, намагаючись уникнути похибок і факторів, що спотворюють результати. Наприклад, пацієнт – курець з раком в грудях у сімейному анамнезі. Чи є паління причиною раку? Чи це лише супутній чинник? Подібним чином, для проведення оцінки причинно-наслідкового зв'язку в окремих випадках після вакцинації, навіть якщо існують докази причинного зв'язку між деякими вакцинами та НППІ (наприклад, між вакциною проти кору і тромбоцитопенією), важливо розглянути всі можливі пояснення даного явища і ступінь ймовірності кожного з них, перед тим, як приписати явище вакцині, дефекту якості вакцини, помилці, допущеній в процесі імунізації, психологічному стресу, пов'язаному з імунізацією, або простому збігу в часі.
В Україні з набуттям чинності наказу №595 МОЗ України від 16.09.2011 р. «Про порядок проведення профілактичних щеплень в Україні та контроль якості й обігу медичних імунобіологічних препаратів» було введено термін «НППІ» – усі захворювання, які зареєстровані у щепленого протягом післявакцинального періоду. До НППІ належать: ускладнений перебіг післявакцинального періоду та післявакцинальні реакції і ускладнення.
Як видно з тексту, при порівнянні з оригінальним визначенням ННПІ від ВООЗ та визначенням НППІ, прийнятим в України, є відмінності. Тим не менше, мета введення до професійної термінології терміну «НППІ» є незмінною – оптимізація системи збору інформації щодо можливих побічних ефектів вакцинації, виявлення нових побічних ефектів, що не були виявлені при доліцензійних дослідженнях або ж в інших дослідженнях вакцин. Неправильне трактування ННПІ, нерозуміння мети використання цього терміну породжує помилкові твердження щодо безпеки вакцинації, неправильні висновки при проведенні розслідування післявакцинальних подій на місцях. На превеликий жаль, багато медичних працівників не володіють навичками інтерпретації результатів досліджень побічних ефектів вакцин. Незважаючи на це, лікарі часто формують свою думку про безпечність вакцин, ґрунтуючись на доступній інформації, нерідко керуючись звітними даними, отриманими за результатами проведення далеких від наукового підходу спостережень або аналітичних досліджень, що не відповідають критеріям проведення наукових досліджень з високим рівнем методологічного опрацювання. Патологічні процеси, що виникли після вакцинації, не варто вважати побічними ефектами до тих пір, поки не буде встановлений їх причинно-наслідковий зв’язок, а не лише часовий.
Зважаючи на цю проблему, в Україні наказом №595 МОЗ України від 16.09.2011 р. «Про порядок проведення профілактичних щеплень в Україні та контроль якості й обігу медичних імунобіологічних препаратів» з метою оптимізації розслідування післявакцинальних подій введено в дію створення груп оперативного реагування на несприятливі події після імунізації при застосуванні вакцин, анатоксинів та алергену туберкульозного у разі госпіталізації або летального випадку. Склад групи формується залежно від клінічних проявів НППІ та складності випадку після застосування вакцин, анатоксинів та алергену туберкульозного.
Центральна група оперативного реагування створюється при МОЗ України та складається з головних спеціалістів МОЗ і профільних спеціалістів, які залучаються у разі потреби. На рівні регіонів групу оперативного реагування очолює голова, який має спеціальність «лікар-педіатр» або «лікар-терапевт». Склад групи у відповідності до наказу МОЗ України затверджується відповідним наказом Управління/Департаменту охорони здоров’я та до неї входять профільні спеціалісти, а саме: судово-медичний експерт, патологоанатом, терапевт, педіатр, невролог/дитячий невролог, інфекціоніст/дитячий інфекціоніст, алерголог/дитячий алерголог, імунолог/дитячий імунолог, анестезіолог/дитячий анестезіолог.
Заключний висновок груп оперативного реагування щодо розслідування НППІ надається до Управління громадського здоров’я та санітарно-епідемічного благополуччя населення МОЗ України та Департаменту імуно-біологічних препаратів та імунопрофілактики ДП «Державний експертний центр МОЗ України» протягом 30 днів з моменту реєстрації несприятливої події після імунізації.
Не менш важливим є питання моніторингу за можливими побічними ефектами вакцинації й у випадку госпіталізації, смерті, – своєчасного початку розслідування. У даному аспекті від лікаря першого контакту залежить подання повідомлення про випадок НППІ. У відповідності до чинного наказу МОЗ України, виявлення НППІ здійснюють на всіх рівнях медичного обслуговування і спостереження: медичні працівники, що проводять щеплення; медичні працівники, що проводять лікування в медичних закладах; батьки або опікуни дитини, інші законні представники, попередньо проінформовані про можливі реакції або ускладнення після застосування певної вакцини, анатоксину, алергену туберкульозного.
Лікарі усіх закладів охорони здоров’я, незалежно від підпорядкування та форм власності, зобов’язані фіксувати інформацію про реакції у картці-повідомленні про побічну реакцію чи відсутність ефективності лікарського засобу при медичному застосуванні за формою № 137/0, затвердженою наказом МОЗ України від 27.12.2006 №898, зареєстрованим у Міністерстві юстиції України 29.01.2007 за №73/13340 (також за іншими формами, передбаченими наказом МОЗ України від 16.09.2011 №595).
Реєстрації підлягають усі випадки реакцій та ускладнень відповідно до Переліку можливих несприятливих подій після імунізації, що потребують подальшого розслідування та подані в наказі МОЗ України №595. Реєстрація проводиться з відповідним записом у формах первинної медичної документації: в Історії розвитку дитини – форма № 112/0, затверджена наказом МОЗ України від 27.12.99 №302, Медичній карті амбулаторного хворого – форма № 025/0, затверджена наказом МОЗ України від 27.12.99 №302, Медичній карті стаціонарного хворого – форма № 003/0, затверджена наказом МОЗ України від 26.07.99 №184, та Карті профілактичних щеплень – форма №063/0, затверджена наказом МОЗ України від 10.01.2006 №1, зареєстрованим у Міністерстві юстиції України 08.06.2006 за № 686/12560.
Як було зазначено вище, сам пацієнт або ж батьки дитини можуть самостійно повідомити про НППІ, заповнивши відповідну форму. З даною формою можна ознайомитися на сайті Державної служби України з лікарських засобів. Форма може бути заповнена в он-лайн режимі – «Карта-повідомлення для надання пацієнтом та/або його представником, організаціями, які представляють інтереси пацієнтів, інформації про побічну реакцію та/або відсутність ефективності лікарського засобу (вакцини) при його медичному застосуванні» (drlz.kiev.ua/). Такий підхід збільшує чутливість системи моніторингу до виявлення можливих побічних ефектів. Хоча й, звісно, зрозуміло, що специфічність щодо виявлення побічних ефектів є низькою.
Створена на сьогодні система моніторингу та розслідування НППІ хоча й потребує подальшого вдосконалення, все ж таки має значення для збору даних та є основою для подальших кроків.
Детальніше
ІХТІОЗ
 Дерматологічний менеджмент з перших днів життя
Дерматологічний менеджмент з перших днів життя
Що робити акушеру-гінекологу у випадку народження дитини з іхтіозом? Якими принципами терапії необхідно керуватись, щоб мінімізувати негативні наслідки для шкіри? За якими основними принципами необхідно провести місцеву терапію? Це основні актуальні питання, що можуть стати точками взаємодії акушерів-гінекологів та дерматологів
Наведемо ряд рекомендацій, що допоможуть розпочати терапію-догляд за шкірою одразу після народження.
Перші описи захворювання були знайдені у древній китайській та індійській літературі ще за декілька віків до нашої ери. Одним з перших у 1808 році зробив науковий опис патологічного стану Європейський вчений Willan.
Іхтіоз може вродженим або розвиватись протягом життя. У одних випадках хвороба вражає винятково шкіру, в інших – також внутрішні органи. Діагностично достовірно описані майже всі форми іхтіозу і виокремлені характерні ознаки тих чи інших. Але встановлення точного діагнозу на сьогоднішній день є основною проблемою.
Іхтіози становлять собою групу гетерогенних захворювань шкіри, що характеризуються генералізованим лущенням шкіри, спричинені аномаліями диференціювання епідермісу. Назва «Іхтіоз» виникла від грецького слова «Ichtys» – риба, і зумовлена зовнішньою схожість ураженої шкіри з лускою риб.
Виділяють два основних принципи класифікації іхтіозів:
- Генетичний, у залежності від типу генетичного успадкування (аномалії):
- Спадково-обумовлений іхтіоз;
- Спадкові синдроми, які включають в себе іхтіоз;
- Іхтіозоформні стани, такі як гіповітаміноз А, злоякісні новоутворення шкіри, хвороби крові.
Наприклад, є так званий звичайний іхтіоз рецесивний, зчеплений з Х-хромосомою. Прояви захворювання відрізняються тим, що лущення на шкірі виражено сильніше, воно захоплює практично всі шкірні покриви хворого. Також буває сухість шкіри. Найбільш явні вогнища ураження розташовані, як правило, в підколінних, ліктьових ямках, в області обличчя, що не є характерним для домінантної форми іхтіозу. Дана обставина в деяких випадках допомагає лікарю у правильній постановці діагнозу. Успадкування захворювання пов'язане з успадкуванням статі. Найчастіше хворими є хлопчики, дівчатка – абсолютно здорові носії патологічного гена, які згодом передають його синам. Ті, будучи хворими, передають цей ген дочкам, які стають носієм, і т. д. Дівчинка може захворіти лише у тому випадку, якщо вона отримає одночасно дві хромосоми з ураженим геном (однаХ-хромосома від матері, інша – від батька). У цьому випадку захворювання протікає дуже важко і навіть може призвести до загибелі дитини.
Всі хлопчики, як відомо, мають лише одну Х-хромосому, тому носіями бути не можуть.
Досить виражене при іхтіозі ураження шкіри голови. Відзначається лущення, випадання волосся, місцями навіть облисіння. Самі лусочки при рецессивному іхтіозі великі, товсті, мають темне забарвлення. Як видно, дана форма захворювання має характерні особливості шкірних проявів, які дозволяють у деяких випадках відрізняти її від домінантної форми захворювання.
Крім того, зміни спостерігаються і з боку багатьох інших органів і систем. Такі діти часто страждають на розумову відсталість, епілепсію, помутніння рогівки ока, порушення розвитку скелета та інших органів.
- За білковою аномалією, що дає розуміння основних патогенетичних ланок гіперкератозу (табл. 1).
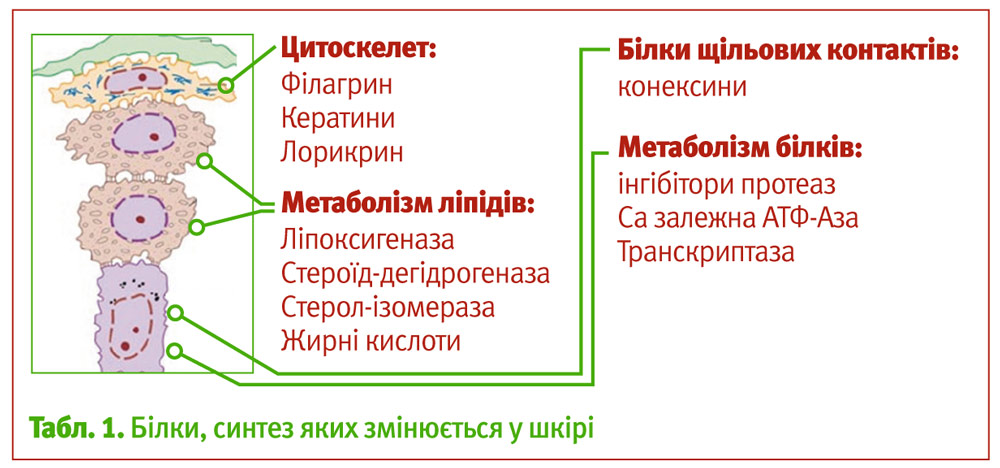
Клінічно, у залежності від характеру лусочок, виділяють такі форми:
- Ксеродермія. Лусочки дуже дрібні, сіруватого кольору, зовні нагадують висівки.
- Простий іхтіоз. Ділянки лущення великих розмірів. Самі лусочки досить великі, за зовнішнім виглядом нагадують пластинки. Виражена сухість шкіри в області патологічних вогнищ
- Блискучий, або перламутровий, іхтіоз. Названий за виглядом лусочок – при розгляді вони здаються блискучими. Вогнища ураження ще більше, ніж у попередньому випадку.
- Змієподібний іхтіоз. Названий за характерним зовнішнім виглядом хворого. Лусочки при цьому дуже товсті, щільні, грубі і нагадують шкіру змії.
- Голчастий іхтіоз. Найбільш важкий різновид захворювання. Лусочки при цьому мають вигляд голок і шпильок, у результаті чого шкіра хворого нагадує шкіру дикобраза з голками.
- Чорний іхтіоз. При цьому лусочки мають темне забарвлення. Найбільш часто даний різновид спостерігається у літніх людей, шкіра яких взагалі схильна до утворення пігментних плям.
В залежності від тяжкості хвороби, розрізняють:
- Важка форма (немовля народжується недоношеним і в перші дні гине);
- Середньої тяжкості (сумісна з життям);
- Пізня форма (характеризується відстроченими першими появами до двох–трьох місяців життя або навіть до п'яти років).
Клінічні ознаки:
- часто слабовиражені;
- сухі, маленькі прямокутні лусочки з'являються на розгинальних поверхнях кінцівок;
- уражені ділянки мають вигляд асфальту чи риб'ячої луски;
- шкірні складки яскраво виражені;
- явища фолікулярний кератозу;
- лущення рідко покриває все тіло.
Рекомендації для акушерів і фельдшерів по догляду за шкірою новонароджених у перші хвилини життя:
Загальні поради
При підозрі на наявність у дитини іхтіозу необхідно запросити або отримати всі належні інструкції по догляду за шкірою у лікаря дерматовенеролога.
Основні принципи терапії:
- постійне зволоження, зменшення трансепідермальної втрати вологи.
- контроль товщини гіперкератотичних нашарувань (зведення його до можливого мінімуму).
Ступінь вираженості шкірних проявів може бути різним, тому місцева терапія завжди підбирається індивідуально. В разі виявлення перинатальних ознак розвитку хвороби необхідно запросити дерматовенеролога для бесіди з батьками, щоб ті, у свою чергу, отримали максимальну інформацію про засоби місцевого догляду за особливою шкірою таких діточок. Величезну роль відіграє інформаційна підтримка батьків і правильне інструктування медичного персоналу. Дерматолог повідомить і навчить основним технікам нанесення місцевих препаратів і доглядових засобів з метою профілактики порушення шкірних покривів та їх інфікування.
З часом близькі люди стануть найкращими експертами у лікуванні своєї дитини і лише вони зможуть прийняти рішення, який доглядовий засіб є найефективнішим у їхньому випадку. Це має бути провідною темою у спілкуванні акушерів з вагітною при виявленні внутрішньоутробних ознак патології і взятті на облік.
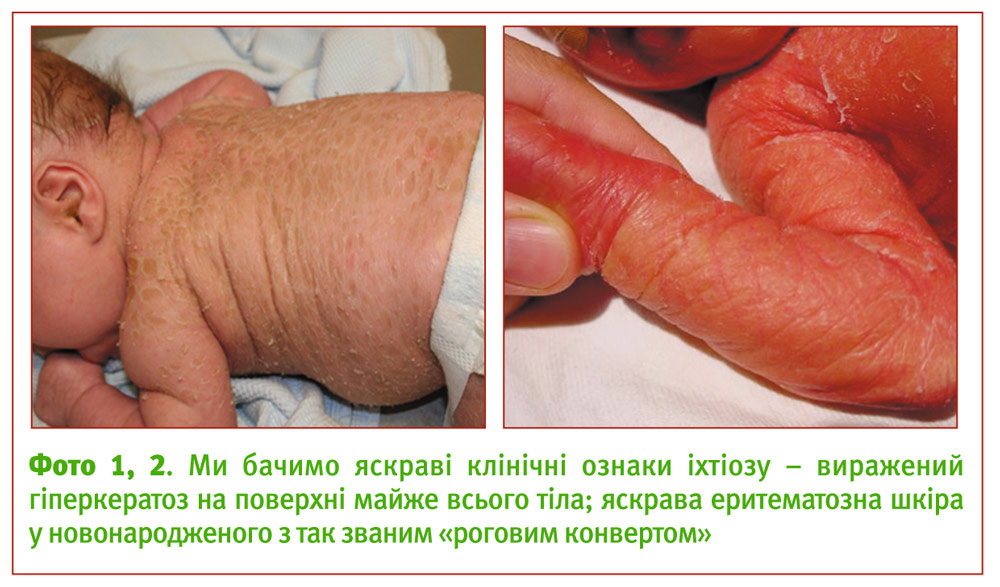
Ванни
Необхідно пам’ятати, що сухій шкірі не вистачає не лише бар’єрного ліпідного шару, але, у першу чергу, води. Тому одразу після народження, не давши шкірі обсохнути, необхідно провести купання немовляти, що зволожить шкіру і не дасть втратити еластичність – це дозволить безболісно і з мінімальним травмуванням, обережно зняти нашарування рушником та перед цим, ще до обтирання, шкіру необхідно змастити зволожуючим засобом (емольєнтом) і тільки потім продовжити процедуру.
Можливий варіант одразу ж обгорнути дитину зволоженою теплою ковдрою, що теж не дасть шкірі пересохнути. Необхідно використовувати м’які миючі олійки, креми і у жодному разі – звичайні лужні мила, що після висихання спричинять загальне відчуття сухості і стягнутості шкірних покривів. Воду для ванн необхідно пом’якшувати, це можуть бути натуральні інгредієнти (відвар рису, льону, вівсяних пластівців) або готові суспензії (повинні містити похідні ліпідів – кераміди, рослинні олії – какао, манго, іланг-іланг).
Якщо на шкірі спостерігаються ознаки інфекції, у воду необхідно додати антисептик (марганець). Якщо спостерігаються масивні гіперкератотичні нашарування на волосистій частині голови, слід змастити поверхню вазеліном, це спростить процедуру очищення шкіри. Необхідно ретельно просушити поверхню шкіри, щоб уникнути мацерації у делікатних місцях (шкірні складки) і одразу ж нанести зволожуючі засоби з вираженим бар’єрним ефектом. Водні процедури слід робити як можна частіше (до 3 разів на добу), якщо спостерігається об’єктивне покращення стану шкіри!
Місцева терапія: креми, лосьйони, мазі
Обробка шкіри дитини повинна виконуватись регулярно (2 рази на добу) у теплій (25ОС), з непересушеним повітрям, кімнаті, це відіграє важливу роль, адже функція терморегуляції шкіри значно порушена. Засоби наносяться на шкіру тонким, але помітним шаром. Малюки краще реагують на підігріті до температури тіла лосьйони, мазі та креми; вони мають більш пластичну структуру у підігрітому вигляді, тому добре проникають у тріщинки чи пори шкіри. Засоби наносяться повільними масажними рухами, щоб добре втерти і розподілити їх на поверхні. Але у жодному разі не прикладайте зусилля, щоб не травмувати шкіру. Після цього необхідно обгорнути шкіру дещо вологою бавовняною тканиною, щоб та добре прилягала до тіла. Зверніть увагу, тканина не повинна містити синтетичних волокон і мати свій натуральний колір.
Звертайте увагу на склад доглядового засобу – може містити альфа-гідрокси кислоти (молочна 2% або гліколева 1,5%), саліцилову кислоту 2%, гліцерин, сечовину 2–8%, пропіленгліколь. Емольєнти, що мають у складі кераміди, фосфоліпіди, тригліцериди, сквален, дуже добре відновлюють захисний ліпідний бар’єр «іхтіозної» шкіри; мають наноситись після кожного купання і за потребою.
Пелюшки і засоби особистої гігієни:
Одноразові підгузки з активними сорбуючими компонентами більшою мірою підходять для шкіри делікатних зон – не пропускають вологу, тому в зоні їх контакту шкіра іноді виглядає краще, ніж на поверхні тіла. Багаторазові підгузки, виготовлені з бавовни, менш ефективні, але поверх можна одягати тканини, що не пропускають вологу, що забезпечує контакт натуральних тканин зі шкірою і не викликає подразнень. Якщо з якихось причин дитині не підходять підгузки, необхідно використовувати вільне пеленання, поверх тканини, не обмежуючи рухливості, слід прикріпити вологоутримуючі тканини (синтетичні). Під них можна нанести тоненьким шаром зволожуючі засоби, та пам’ятайте про контроль стану шкіри, щоб запобігти оклюзивним явищам! Також необхідно виключити механічне тертя або тиск на виступаючі ділянки для цього тканими нетреба туго фіксувати на шкірі. Уникайте постійного контакту зі шкірою синтетичних тканин рано чи пізно вони викличуть подразнення. Пелюшки мають бути дещо вологими і підігрітими до температури тіла.
Профілактика інфекцій шкіри:
Шкірні покриви хворих дітей мають порушену бар’єрну і захисну функції і є більш чутливими до виникнення запальних процесів.
Частіше за все, запалення провокуються бактеріями і дріжджоподібними видами грибків. Всі дефекти на шкірі потребують якнайшвидшої обробки дезінфікуючими засобами на водній основі (розчин марганцю, хлоргексидину біглюконату, декаметоксин). Пам’ятайте, що при цьому загальний стан немовляти погіршується не завжди, тому часто проводьте огляд шкірних покривів. Якщо місцева терапія не допомогла, і впродовж 3 днів не спостерігається клінічне покращення, необхідно призначити системні антибактеріальні препарати у відповідних дозуваннях.
Харчування
Зазвичай прикладання до грудей є дискомфортним для дітей з іхтіозом і їм необхідно забезпечити раціональне штучне вигодовування. Важливо розуміти, що шкіра потребує великої кількості корисних інгредієнтів (вітамінів, мікроелементів і структурних компонентів) для нормального функціонування. Збільшення втрати вологи і змертвілого епідермісу чинять величезне навантаження на організм. Часто діти, що мають ті чи інші глобальні проблеми із шкірою, схильні до повільного росту. Потреби таких дітей у надходженні поживних речовин в багато разів перевищують потреби здорових, що, до того ж, також активно ростуть. Заздалегідь необхідно провести консультацію з педіатром, що зобов’язаний розробити індивідуальний графік годувань, запропонувати калорійне меню, щоб перекрити підвищені потреби малюка. Клінічне мислення у харчуванні повинне бути спрямоване на збільшення кратності годувань з різноманітним меню з метою інтенсифікації харчування; по можливості, слід зберегти грудне вигодовування – найбільш корисне для дитини у ранньому віці; підключити харчові добавки. У більшості випадків їжа повинна бути м’якою і мати легкозасвоювану форму – перетерті пюре, смузі. Важливо пам’ятати, що дитина не повинна відчувати голод!
Температурні умови:
Діти з іхтіозом більш чутливі до високих температур, вологості повітря оточуючого середовища. Прегрівання стає серйозною проблемою, оскільки через потовщену шкіру не відбувається нормальна терморегуляція, потовиділення знижене. При перегріванні дітки можуть бути примхливими, або навпаки, стати пригніченими і апатичними. Якщо спостерігаєте такі ознаки, якнайшвидше заберіть дитину у прохолодне місце, дайте достатню кількість прохолодної рідини, а краще за все, проведіть обтирання водою, знявши увесь одяг! У палаті, де перебуває немовля, температура повинна становити 25ОС, вологість повітря – близько 90%.
Системна терапія:
Похідні вітаміну А здатні значно покращити стан шкірних покривів дітей; вони є доброю альтернативою для контролю хвороби. Перед призначенням лікар має пояснити батькам всі можливі побічні дії препарату і рішення про їх призначення прийняти лише разом з батьками. Похідні віт. А являють альтернативно довготривалою терапією, що є найбільш ефективним методом корекції стану шкіри на сьогодні.
Шановні колеги, хочу дати перелік web-ресурсів, що допоможуть ознайомитись глибше з проблемою і у разі потреби, отримати необхідну інформаційну підтримку світової спільноти:
- Фонд для хворих на іхтіоз і схожі дерматози – http://www.skalyskin.org/; Ця електронна адреса захищена від спам-ботів. Вам необхідно увімкнути JavaScript, щоб побачити її..
- Генетичні тести
http://www.genetests.org. - «Менделівська
спадщина людства»
http://www.ncbi.nlm.nih.gov. - Національний реєстр іхтіозів
і схожих дерматозів
http://www.skinregestry.org.
В Україні Ви також можете знайти підтримку, звернувшись до МГО «Дерматологи – Дітям», президентом якої є Людмила Андріївна Дерев’янко, а також до кабінету Бульозного епідермолізу, куруючим лікарем якого є Інна Гедеон (м. Київ, вул. Чорновола 28/1, Охматдит (11 корпус, 5- й поверх)).
Детальніше
ІЄРАРХІЯ СТАТІ
Порушення статевого диференціювання (частина 2)
Клініка основних форм гермафродитизму
(початок у №4 (49) 2014)
- Несправжній жіночий гермафродитизм
Для розвитку цього синдрому потрібний внутрішньоутробний надлишок андрогенів за наявності у плоду каріотипу 46, ХХ. Надлишок андрогенів може створюватися як самим плодом, так і виникати в материнському організмі.
Перша ситуація розвивається при вірильних формах гіперплазії кори наднирників у плоду (див. вище). Друга виникає внаслідок секреторної дії материнських пухлин – андростером різної локалізації, а також за наявності у матері вродженої дисфункції кори наднирників.
Доволі рідко причиною несправжнього жіночого гермафродитизму може бути ятрогенна вірилізація – наслідок вживання матір’ю препаратів з андрогенними властивостями, гестагенів.
Єдиною ознакою захворювання є інтерсексуальна будова зовнішніх статевих органів. Каріотип у хворих завжди жіночий, гонади і внутрішні геніталії сформовані за жіночим типом, зовнішні – вірилізовані.
Ступінь вірилізації зовнішніх геніталій при цій формі несправжнього жіночого гермафродитизму (НЖГ) менша, ніж при вродженій дисфункції кори наднирників.
Гіпертрофія та вірилізація клітора спостерігається у всіх хворих з несправжнім жіночим гермафродитизмом. Крім того, інколи буває зрощення великих статевих губ, урогенітальний синус за типом гіпоспадії. Фізичний і статевий розвиток, як правило, нормальний. Вторинні статеві ознаки у хворих завжди жіночого типу і з’являються у відповідні строки.
Несправжній жіночий гермафродитизм оваріального генезу
За останні роки з’являються повідомлення про порушення функції яєчників у хворих на НЖГ. При цьому у хворих на НЖГ буває виражена вірилізація зовнішніх геніталій (гіпертрофія клітора, зрощення великих статевих губ, урогенітальний синус). Матері дівчат були здоровими і під час вагітності не приймали жодних гормональних препаратів. Припускають, що у результаті генетичної патології порушується стероїдогенез у яєчниках плода, що є причиною підвищеного синтезу андрогенів у період гестації і гермафродитної будови зовнішніх геніталій. Останнє стає причиною андрогенізації на фоні пубертатного періоду і полікістозних змін в яєчниках. У деяких хворих клініка НЖГ поєднується з гіпогонадизмом.
Таким чином, для даного варіанту гермафродитизму характерна вірилізація зовнішніх геніталій і патологія пубертатного періоду. При цьому у одних хворих на фоні пубертатного періоду прогресує вірилізація, у інших – гіпогонадизм.
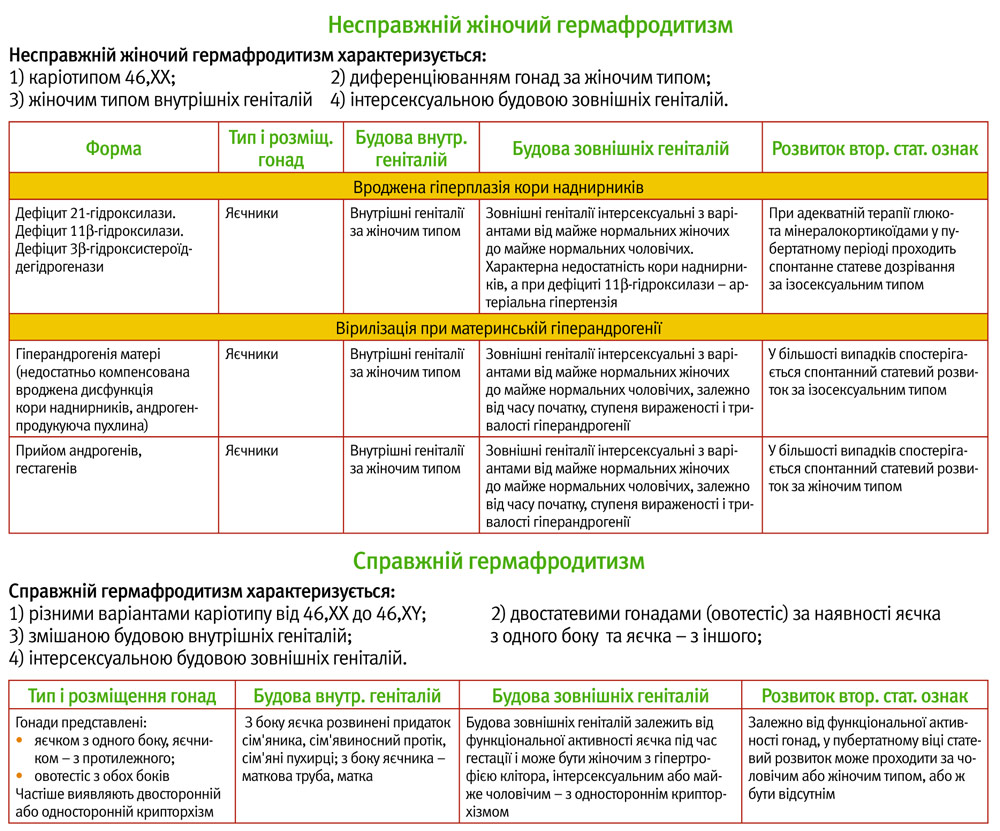
- Справжній гермафродитизм
Для цього виду порушення статевої диференціації характерна наявність у одного індивідууму двох статевих залоз різної статі, або гонади змішаного типу (овотестіс).
Справжній гермафродитизм характеризується:
- різними варіантами каріотипу від 46,ХХ до 46,ХY. У більшості хворих каріотип – 46,ХХ/46,ХХY;
- двостатевими гонадами, які представлені яєчком з одного боку, яєчником або овотестіс з протилежного боку; овотестіс з обох боків; часто діагностують односторонній чи двосторонній крипторхізм;
- змішаною будовою внутрішніх геніталій;
- інтерсексуальною будовою зовнішніх геніталій.
Будова внутрішніх геніталій
На боці яєчка знаходиться придаток сім’яника, сім’явиносячий проток, на боці яєчника – матка і маточна труба.
Будова зовнішніх геніталій
Залежить від функціональної активності яєчка у період ембріогенезу і може бути жіночою з гіпертрофією клітора, інтерсексуальною або майже чоловічою з одностороннім крипторхізмом.
Розвиток вторинних статевих ознак
Залежно від функціональної активності гонад, статевий розвиток у пубертатному періоді може проходити за чоловічим, жіночим типом або бути відсутнім.
Наявність матки, вагіни, овотестіс і оваріальної тканини дозволяє пацієнтам добре адаптуватися в жіночій статі.
У тих випадках, коли маскулінізація зовнішніх геніталій задовільна, можливий вибір чоловічої статі виховання, однак видалення гонад, як овотестіс, так і тестикул – обов’язкове, оскільки при справжньому гермафродитизмі буває високий ризик малігнізації тестикулярної тканини. З пубертатного віку проводиться замісна терапія чоловічими статевими гормонами.
Таким чином, справжній гермафродитизм характеризується змішаною будовою гонад, зовнішніх і внутрішніх геніталій, вторинних статевих ознак.
Для клініки різних форм порушень статевого диференціювання без гермафродитизму характерна: правильна за жіночим або чоловічим типом будова зовнішніх геніталій і поява симптомів гіпогонадизму в пубертатному віці.
У більшості хворих спостерігається порушення росту, стигми дизембріогенезу, вроджені вади розвитку, які допомагають запідозрити цю патологію у ранньому дитинстві.
У переважної більшості хворих поставити діагноз гермафродитизму легко. Значно складніше встановити варіант гермафродитизму. У зв’язку з цим, всі методи обстеження хворих спрямовані на встановлення статі гонад, уточнення їх функціональної активності – варіанту гермафродитизму.
Діагностика порушень статевого диференціювання
Діагностика включає такі етапи:
- оцінка будови, ступеня вірилізації зовнішніх статевих органів, вираженості вторинних і третинних статевих ознак;
- оцінка розмірів, положення, форми і консистенції гонад;
- антропометрія, визначення типу тілобудови, наявність вроджених мікроаномалій та інших вад розвитку;
- визначення статевого хроматину, каріотипу, за необхідності – молекулярно-цитогенетичне дослідження;
- візуалізацію внутрішніх геніталій: ультрасонографію, генітографію, за необхідності – лапароскопію (лапаротомію) з біопсією гонад;
- дослідження базальних рівнів гормонів гіпофізу, наднирників і статевих залоз;
- проведення функціональних проб з хоріонічним гонадотропіном і/або депотестостероном;
- пробне лікування андрогенами;
- консультація гінеколога, уролога, ендокринолога.
Принципи вибору статі
Диференціальна діагностика гермафродитизму заснована на даних клініки, каріотипування, результатах візуалізації внутрішніх геніталій, результатах гормональних досліджень. При цьому потрібно враховувати стан гонад, будову внутрішніх і зовнішніх геніталій, можливість їх корекції відповідно до обраної статі, а також особливості перебігу пубертату (фемінізація, андрогенізація або гіпогонадизм), що визначає необхідність і характер гормональної терапії.
Відсутність гонад при пальпації дозволяє думати, що у новонародженого – НЖГ; у той же час, наявність гонад свідчить на користь НЧГ.
Потрібно провести дослідження статевого хроматину і каріотипу, які дозволять виділити всі випадки НЖГ (каріотип 46,ХХ), причиною якого найчастіше є вроджена дисфункція кори наднирників.
Значно рідше причиною бісексуальної будови зовнішніх геніталій при каріотипі 46,ХХ є справжній гермафродитизм, дефіцит ароматази або екзогенна андрогенізація.
При НЖГ паспортна стать завжди жіноча.
У тих випадках, коли гонади пальпуються у розщепленій калитці чи пахових каналах і визначається негативний статевий хроматин, каріотип 46,ХY, передбачається наявність змішаної тестикулярної дизгенезії яєчок або інші варіанти НЧГ.
Наступним ступенем діагностики є УЗД внутрішніх статевих органів. Наявність матки, фалопієвих труб, верхньої третини вагіни дозволяє діагностувати синдром змішаної дизгенезії тестикул. Відсутність матки, придатків, наявність вагінального відростка, який сліпо закінчується, є характерним для всіх варіантів НЧГ.
Дефіцит 5a-редуктази як причина НЧГ, зустрічається відносно часто. Рання діагностика дефіциту 5a-редуктази важлива, оскільки ці хворі добре адаптуються без гормональної корекції в чоловічій статі. Діагноз ставлять за підвищенням коефіцієнту Т/ДГТ (>35) у відповідь на стимуляцію ХГ.
Синдром андрогенової нечутливості (тестикулярна фемінізація) – найчастіша причина НЧГ. Захворювання може вражати членів однієї сім’ї, тому сімейний анамнез принципово важливий для діагностики цієї форми захворювання. Повна форма ТФ, як правило, діагностується лише у період пубертації. Основою діагностики служить визначення каріотипу 46,ХY у пацієнток з первинною аменореєю і відсутністю статевого оволосіння.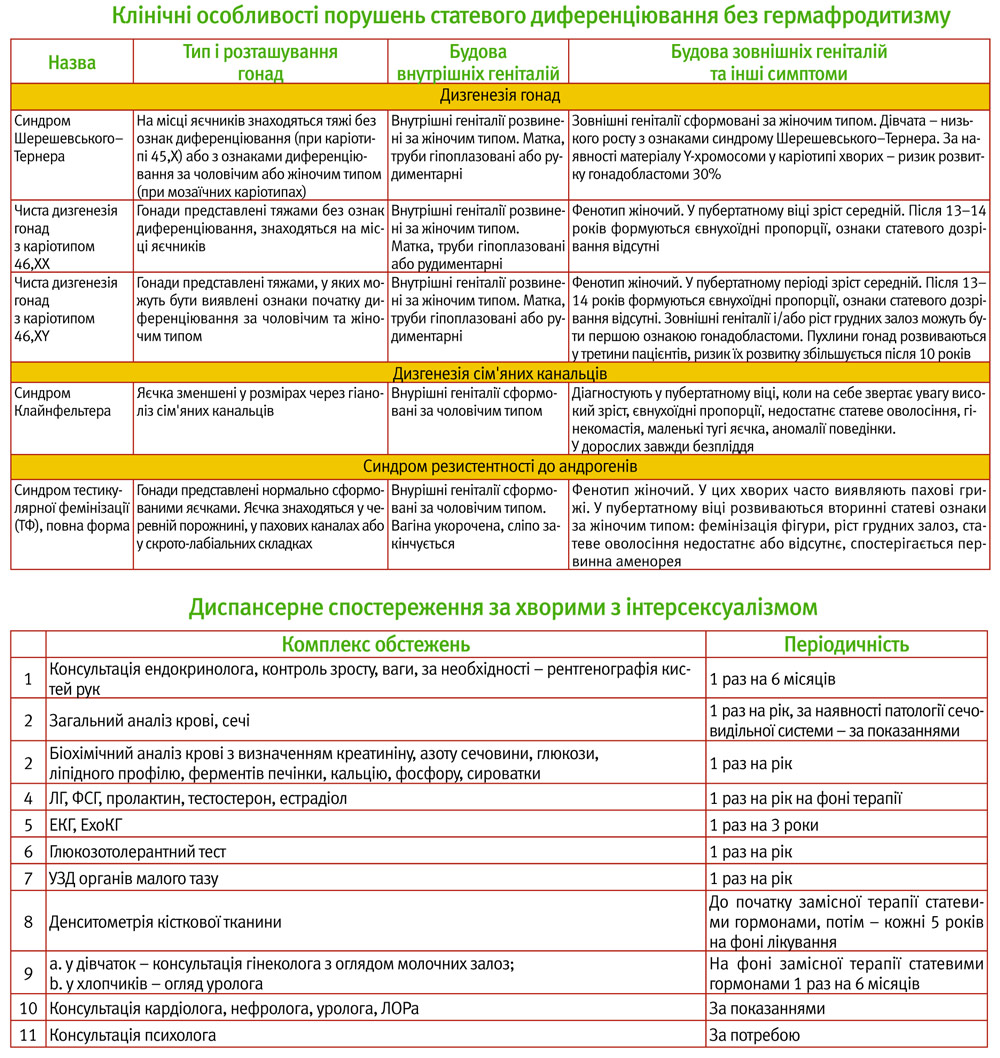
Неповну форму ТФ дуже складно диференціювати від інших форм НЧГ.
Практичне значення для діагностики має визначення чутливості до андрогенів з введенням пролонгованих препаратів тестостерону. При задовільній чутливості до андрогенів у період лікування значно збільшується у розмірах статевий член, з’являються ерекції. Позитивна реакція на введення тестостерону характерна для дефіциту 5a-редуктази (синдрома Рейфенштейна). У цих випадках можливо чекати задовільної адаптації пацієнта у чоловічій статі.
Значно складніше вирішується питання з вибору статі у хворих зі змішаною дизгенезією тестикулів. При змішаній дизгенезії тестикулів у хворого виявляється один функціонально активний тестикул і задовільна маскулінізація зовнішніх геніталій, що дозволяє вибрати чоловічу стать виховання. У допубертатному віці проводиться хірургічне видалення стрека, мюлерових похідних і маскулінізуюча пластика зовнішніх геніталій.
Диференційний діагноз різних форм НЧГ дуже складний, тому вибір статі, як правило, вирішується на користь жіночої. Це виправдано, тому що більшість випадків НЧГ обумовлені нечутливістю до андрогенів і незадовільною адаптацією в чоловічій статі.
При достатньому розвитку кавернозних тіл статевого члена при НЧГ дитина виховується у чоловічій статі.
Вибір жіночої статі потребує фемінізуючої корекції зовнішніх геніталій і гонадектомії. При повній формі ТФ корекція зовнішніх геніталій не потрібна, гонадектомія – обов’язкова. З пубертатного віку проводиться замісна терапія жіночими статевими гормонами. Всім хворим з НЧГ, адаптованим в жіночій статі, показаний кольпопоез. Його потрібно проводити після початку естрогенотерапії.
Хворих із справжнім гермафродитизмом, особливо з каріотипом 46,ХХ, потрібно адаптувати у жіночій статі. Гонадектомія (видалення ovotestis і тканини яєчка) – обов’язкова. Наявність матки, вагіни дозволяє пацієнтам добре адаптуватися у жіночій статі. При задовільній маскулінізації зовнішніх геніталій можливий вибір чоловічої статі виховання. Гонадектомія – обов’язкова, оскільки існує високий ризик малігнізації тестикулярної тканини. З пубертатного віку проводиться замісна терапія чоловічими статевими гормонами.
Синдром Шерешевського–Тернера потрібно відрізняти від змішаної дизгенезії гонад, чистої дизгенезії гонад 46ХХ або 46ХУ і синдрому Нунан:
- при змішаній дизгенезії гонад з одного боку виявляється яєчко, з іншого – тяжевидна гонада;
- при чистій дизгенезії гонад з двох боків виявляються тяжевидні гонади, але каріотип – 46ХХ або 46ХY;
- синдром Нунан за клінічною картиною близький до синдрому Шерешевського–Тернера. Але ця патологія зустрічається у осіб і чоловічої, і жіночої статі. При цитогенетичному дослідженні аномалії каріотипу не виявляються. У дівчат з синдромом Нунан функція яєчників, як правило, не порушена, інколи – дещо знижені рівні гонадотропінів.
Комплексна терапія при інтерсексуалізмі направлена на максимальну адаптацію хворих у суспільстві. Практика показує, що така адаптація найкраща, якщо у хворих рано встановлена стать, коли архітектоніка скелету, характер вторинних статевих ознак протягом всього життя відповідають паспортній статі, сам хворий і оточуючі його люди не мають сумніву в правильності вибраної статі.
Терапія гермафродитизму зводиться до вибору паспортної статі, формування фенотипу відповідно до обраної статі й створення умов для правильного статевого виховання у цій статі. Паспортною статтю визначається характер коригуючої і гормональної терапії, а також можливість адаптуватися хворому у статевому і соціально-психологічному плані.
Наскільки вдало вибрана стать новонародженому з гермафродитними геніталіями, залежить життя хворого, його доля. З перших днів життя, як тільки оприлюднена стать новонародженої дитини, починається її статеве виховання. Статтю дитини визначається вибір імені, іграшок, одягу, відношення до нього оточуючих. Статева самосвідомість формується у віці 1,5–3 роки. У шкільні роки поділ за статтю стає особливо чітким.
Тому кращим строком для вирішення питання про стать дитини є період новонародженості або перші два років життя. Зміна паспортної статі у дітей, старших за 3–4 роки, небажана. За наявності абсолютних показань за анатомічною будовою статевих органів можливо змінювати стать у пубертатному періоді. У цьому віці хворі вже здатні аналізувати свій стан. Поява вторинних статевих ознак, протилежних паспортній статі, викликає сумніви у правильності обраної статі.
Питання вибору статі не ідентичне встановленню гонадної статі. Паспортна стать при гермафродитизмі не завжди відповідає біологічній, оскільки питання статі мусить вирішуватись, виходячи з принципу доцільності, кращої адаптації в суспільстві. Для правильного вирішення питання про стать хворого потрібно точно визначити варіант гермафродитизму.
Таким чином, терапія гермафродитизму починається з вибору статі. У подальшому весь комплекс терапевтичних заходів мусить бути підкорений обраній статі й спрямований на виправлення фенотипу відповідно до обраної статі.
При проведенні оперативної корекції зовнішніх геніталій необхідно робити все задля створення умов для статевого життя у майбутньому.
Інколи визначити стать дитини буває неможливо.
Тепер розглянемо порушення статевої ідентифікації (тобто, порушення на психічному, соціальному та громадському рівні).
Розлади статевої ідентифікації у дітей
МКХ-10: F64.2
Ці розлади виникають у дитячому віці задовго до початку пубертатного періоду і характеризуються постійною незадоволеністю своєю статтю, з наполегливим бажанням і заявами про приналежність до іншої статі. Розлад частіше починається у дошкільному віці та спостерігається, як правило, серед хлопчиків. Поведінка характеризується потягом до вбрання, гри та звичок, притаманних протилежній статі, з ігноруванням своєї. Розлад супроводжується глибокою зміною відчуття статевої належності, що можливо розглядати як рудиментарні деперсоналізаційні розлади. Діагностика розладів статевої ідентифікації передбачає відсутність ознак розладу статевого дозрівання.
Цей дитячий патерн, як правило, зникає в підлітковому віці або ранній зрілості. Отже транссексуальні дорослі у дитинстві могли мати порушення гендерної ідентифікації, однак більшість дітей з порушенням гендерної ідентифікації НЕ перетворюються на дорослих транссексуалів. Деякі дорослі, які страждають на транссексуалізм, не проявляють жодних симптомів до настання середнього віку.
Діагностика
Клінічні діагностичні критерії, згідно з МКХ-10
А. Дитина демонструє стан дистресу і наполегливо висловлює бажання бути хлопчиком (дівчинкою) чи стверджує, що вона є хлопчиком (дівчинкою).
Такі висловлювання у дівчаток не пов’язані з уявою про переваги чоловічої статі.
Б. (1) У дівчаток спостерігається одна з таких ознак:
- Дівчинка не сприймає жіноче вбрання і прагне носити чоловіче.
- Дівчинка постійно заперечує жіночі анатомічні структури, про що свідчить одна з таких ознак:
- a) твердження про існування члена або заяви про те, що він «виросте» у майбутньому;
- b) відмова від сечовипускання у сидячому положенні;
- c) негативне ставлення до перспективи появи у майбутньому грудних залоз чи менструацій.
(2) У хлопчиків спостерігається одна з таких ознак:
- Переодягання у жіноче вбрання, імітування жіночої поведінки, участь у дівочих типах гри та відмовляння від хлопчачого типу поведінки.
- Хлопчик постійно заперечує чоловічі анатомічні структури, про що свідчить один з висловів:
- a) коли він стане дорослим, то буде жінкою (а не гратиме роль жінки);
- b) його статеві органи жахливі і у майбутньому зникнуть;
- c) краще не мати статевих органів.
В. Дитина ще не досягла пубертатного віку.
Г. Розлад спостерігається протягом не менше шести місяців.
Порушення статевої ідентифікації (транссексуалізм)
За різними даними, серед чоловіків транссексуалами є від 1 до 3 на 100 тис. населення. Співвідношення між чоловіками-транссексуалами та жінками-транссексуалками становить від 2:1 до 8:1. У чоловіків транссексуалізм найпомітніший у 23–24, у жінок – у 25 років.
Транссексуалізм (лат. trans – зміна і sexus – стать) — стійка невідповідність статевої ідентифікації суб'єкта його біологічній статі, переконаність у «неправильності» своєї статі, бажання належати до протилежної, попри правильне формування гонад, урогенітального тракту і вторинних статевих ознак.
Причинами транссексуалізму є порушення у процесі внутрішньоутробного розвитку відповідальних за статевий потяг і статеву поведінку мозкових структур (найбільше – у гіпоталамусі). Це призводить до викривлення самоідентифікації, попри правильне виховання статі. На порушення ідентичності впливають ендогенні (підвищення ембріонального андрогену або відсутність естрогену) й екзогенні (інтоксикація, використання фармакологічних препаратів під час вагітності) фактори.
Вчені з Нідерландів провели аутопсію мозку шести людей, що змінили свою стать з чоловічої на жіночу. Вони виявили, що група клітин у гіпоталамусі, так зване опорне ядро термінального тяжа (BST) (bed nucleus of stria terminalis), у цих людей за величиною була у два рази меншою, ніж у нормальних чоловіків. Оскільки у жінки ця група клітин набагато менша, ніж у чоловіка, то фактично у людей, схильних до транссексуалізму, ця група клітин була такого ж розміру, як і в осіб протилежної статі. Вчені не знають напевно, яку саме функцію виконує ця група клітин у людей, але відомо, що вона допомагає контролювати сексуальну поведінку у щурів-самців. Хоча можна інтерпретувати ці дані й інакше. Може виявитися і так, що чоловіки з транссексуалізмом володіють якимись істотними біологічними відмінностями, і саме тому їх стать заподіює їм такі незручності.
Відчуття належності до іншої статі виникає вже в дитинстві. Дитина просить називати її іменем протилежної статі, стверджує, що вона – не хлопчик, а дівчинка (навпаки), носить нейтральний за статевими ознаками одяг. У такий спосіб діти борються з батьками і оточенням за власне Я.
Статево-рольові ігри («доньки-матері», «козаки-розбійники» та ін.) можуть слугувати індикатором сформованості статевої самосвідомості.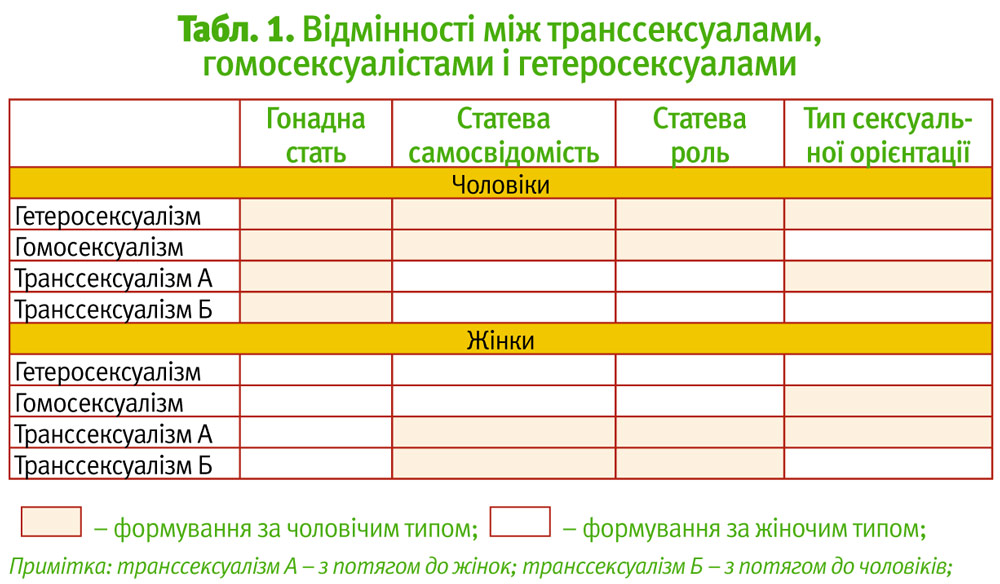
Із початком активного функціонування статевих залоз відчуття належності до протилежної статі швидко посилюється. Розвиток статевих органів і вторинних статевих ознак підлітки-транссексуали сприймають дуже гостро, адже це свідчить про їх належність не до тієї статі. Дівчат хвилює збільшення молочних залоз, тому вони їх бинтують, заморожують. Юнаки тяжко переживають ріст статевих органів, ерекцію. Щоб сховати статевий член, вони прив'язують його або в інший спосіб фіксують до промежини. У 18% випадків юнаки наважуються на ампутацію статевого члена або повну кастрацію.
Прояви транссексуалізму не можна ототожнювати з гомосексуалізмом і трансвестизмом. Транссексуали, які страждають від невідповідповідності власної статевої ідентичності біологічній статі, прагнуть змінити свою зовнішність, носити адекватний їх самовідчуттю одяг. Пасивний гомосексуаліст чи активна лесбіянка застосовують одяг іншої статі, щоб заявити про характер своєї сексуальності, привернути увагу потенційних партнерів. Для трансвестита мотивом використання одягу чужої статі обов'язково є сексуальна насолода (яку він часто не може отримати в інший спосіб), що не виключає розглядання себе в дзеркалі (нарцисизм) і мастурбування. Більшість трансвеститів є гетеросексуалами. Відмінності між транссексуалами, гомосексуалістами і гетеросексуалами наведено у таблиці 1.
Співвідношення гонадної статі, статевої самосвідомості, статевої ролі і типу сексуальної орієнтації за гетеросексуалізму, гомосексуалізму, транссексуалізму у чоловіків та жінок
Формування статевого потягу транссексуалів здебільшого відповідає статевій самосвідомості. І хоча статевий потяг у них за зовнішніми ознаками подібний до гомосексуального, їхнє лібідо спрямоване на протилежну стать. Наприклад, чоловік-транссексуал обирає партнером гетеросексуального чоловіка, оскільки сприймає себе жінкою і зв'язок з іншою жінкою вважає гомосексуальним (те саме, тільки навпаки, стосується жінок-транссексуалок).
За статистикою, 53% чоловіків і 61% жінок вступають у статеві контакти з представниками своєї паспортної статі, а з представниками протилежної мають статевий контакт 20% чоловіків і 8% жінок. Неприємності, сексуальні проблеми, які виникають за такого характеру потягу, для транссексуала менш серйозні, ніж основна проблема – забезпечення відповідності свого зовнішнього вигляду статевій самосвідомості, визнання належності до іншої статі.
Залежно від сили прояву розрізняють такі форми транссексуалізму:
- легка (спостерігається в більшості випадків). Спричинюють її менш грубі (порівняно з другою формою) порушення статевої диференціації структур мозку в пренатальному періоді, тому у таких випадках суттєво допомогти може правильне та вчасне статеве виховання. Осіб з легкою формою транссексуалізму вважають соціально адаптованими. Більшість таких чоловіків і жінок адаптується, знаходячи компенсацію у виборі фаху, характерного для протилежної статі. Жінки обирають чоловічі професії (пілот, капітан, хірург та ін.), самоутверджуються, на рівних взаємодіють у чоловічому середовищі (манера триматися, стиль одягу тощо). Чоловікам соціально адаптуватися буває важче, оскільки ще в дитинстві з них кепкують, насміхаються. Пізніше вони обирають жіночі професії, які серед чоловіків викликають подив. Попри те, жіночі колективи, у яких вони працюють, зазвичай ставляться до них доброзичливо. Особам, які мають легку форму транссексуалізму, зміна статі не рекомендується, та вони потребують раціональної психотерапії, спрямованої на соціальну і сексуальну адаптацію;
- виражена. Статева самосвідомість осіб з такою формою транссексуалізму не залежить від впливу мікросоціального середовища, статеве виховання виявляється абсолютно неефективним: прагнення до зміни статі у них настільки сильне, що людина готова на все, навіть на хірургічну операцію зі зміни статі. Суїцидальні думки виникають у 60% таких чоловіків і 23% жінок, а спроба їх здійснення – у 20% чоловіків і 8% жінок. Враховуючи високий ризик суїциду, лікування вираженого транссексуалізму можливе лише як зміна статі – хірургічно-косметологічна терапія та гормонотерапія. Зміна чоловічої статі на жіночу оперативним шляхом вважається менш складною, ніж навпаки, та відбувається у кілька етапів. Однак у будь-якому разі операція можлива лише: а) по завершенню психосексуального розвитку (хоча після 20–21 року зміна статі пов'язана з певними труднощами: зміна спеціальності, місця проживання, перебудова взаємин із рідними та знайомими); б) після всебічного фізіологічного і психологічного обстеження; в) після здійснення психосоціальної адаптації до нової статевої ролі; г) після курсу гормонального лікування, спрямованого на формування ознак обраної статі; ґ) при гарантії піклування з боку рідних чи друзів у післяопераційний період.
Оскільки соціальна стать не обов'язково збігається з біологічною статтю індивіда, з його/її статтю виховання або з його/її паспортною статтю, у наукових дослідженнях використовується розуміння ґендера у широкому сенсі.
У психології та сексології під поняттям «ґендер» розуміється сукупність стандартів і сценаріїв поведінки, котрі суспільство визначає як «жіночі» і «чоловічі», котрі виражаються у двох головних категоріях — маскулінність і фемінність. Вони, у свою чергу, оприявнюються у стилі одягу, способах ходіння та говоріння, у манерах, захопленнях та інших способах поводження.
Всесвітня організація охорони здоров'я (ВООЗ) використовує термін «ґендер» для визначення «соціально обумовлених ролей, моделей поведінки, діяльності, а також атрибутів, які дане товариство вважає необхідними для чоловіків і жінок».
Зазвичай в суспільстві можна розрізнити два гендера – чоловічий і жіночий, проте набір гендерів буває набагато ширше, зокрема, в Таїланді розрізняють п'ять гендерів, включаючи катой і два гендера лесбіянок, що відрізняються маскулінністю та фемінністю. У чукчів до кінця XX століття розрізнялися чоловіки – гетеросексуали, чоловіки – гетеросексуали, що носили жіночий одяг, чоловіки – гомосексуалісти, що носили жіночий одяг, жінки – гетеросексуали і жінки, що носили чоловічий одяг. При цьому носіння одягу могло означати і виконання відповідних соціальних функцій.
У випадках інтерсексуальності визначити справжню біологічну стать дитини буває тяжко, а часом і зовсім неможливо.
З 1 листопада 2013 року у Німеччині почали діяти нові правила. Набув чинності закон, за яким більше не буде потрібно вносити у свідоцтво про народження стать дитини. Відповідна графа може залишитися незаповненою. З правової точки зору це означає, що людина, у якої наявні ознаки обох статей, може бути не тільки чоловіком чи жінкою. Ставши дорослою, вона сама зможе обрати собі стать або зовсім не робити такого вибору.
Так, в Австралії стать інтерсексуалів визначається як «інша». Її вносять у документи замість колишньої вказівки на чоловічу чи жіночу стать.
Такі мусульманські країни, як Афганістан, Непал або Пакистан, теж вже офіційно визнали існування двостатевих людей.
Висновки
Таким чином, стає зрозумілим, що порушення статевої диференціації та ідентифікації – поліетіологічна та поліпатогенетична патологія. Вона може включати чи не включати попередні рівні. Та тільки розуміння всіх рівнів порушення, комплексний та неупереджений підхід до діагностики цієї патології може застерегти нас від лікарських помилок та зламаних людських доль.
Детальніше
