Резюме:
Розповсюдженість, а також можливі репродуктивні, метаболічні та онкологічні наслідки синдрому полікістозних яєчників визначають необхідність ранньої діагностики даної патології. Враховуючи, що синдром полікістозних яєчників є діагнозом виключення, лабораторна діагностика має першочергове значення в постановці діагнозу та диференційній діагностиці гіперандрогенних станів.
Ключові слова:
Гіперандрогенія, синдром полікістозних яєчників, лабораторна діагностика, тестостерон, 17-ОНП.
DOI
https://doi.org/10.37529/ztz.2020.3/3-20-14
Синдром полікістозних яєчників (СПКЯ) – поліендокринний синдром, можливо, генетично детермінований, який супроводжується порушенням функції яєчників (відсутністю або нерегулярністю овуляції, підвищеною секрецією андрогенів та естрогенів), підшлункової залози (гіперсекреція інсуліну), кори наднирників (гіперсекреція наднирникових андрогенів), гіпоталамуса та гіпофіза [1]. СПКЯ найбільш розповсюджена ендокринопатія у жінок репродуктивного віку, частота якої складає 6–19% у залежності від популяції та критеріїв діагностики [2-4].
Проблема діагностики та вибору подальшого лікування пацієнток з СПКЯ важлива не тільки для гінекологів, репродуктологів, ендокринологів, а й для лікарів інших спеціальностей – дерматологів, кардіологів, онкологів. Враховуючи можливі наслідки даної патології, усіх жінок із СПКЯ рекомендовано оцінювати як групу ризику серцево-судинних захворювань – артеріальної гіпертензії, тромбозів, тромбоемболій і т. д. [5]. Крім того, враховуючи той факт, що дана патологія є складовою метаболічного синдрому, пацієнтки з СПКЯ входять до групи високого ризику з розвитку гіперплазії ендометрія, раку ендометрію та молочних залоз, цукрового діабету 2-го типу.
Клінічна картина СПКЯ може включати наступні симптоми: гіперандрогенію, мультифолікулярну структуру яєчників, ановуляцію. Комбінація вказаних ознак визначає фенотип захворювання.
Гіперандрогенію розрізняють клінічну та біохімічну. Клінічна гіперандрогенія проявляється гірсутизмом, акне, себореєю, алопецією, які обумовлені стимуляцією андрогенових рецепторів, та порушенням менструального циклу (ПМЦ), безпліддям.
Гірсутизм оцінюється за модифікованою шкалою Феррімана–Галлвея, яка відображає розповсюдженість термінального волосся в 9 андрогензалежних зонах за 5-бальною шкалою (від 0 до 4 балів) [6]. Загальний показник гірсутизму може коливатися від 0 до 36 балів. Критерії оцінки ступеня тяжкості гірсутизму: 8–15 балів – легкий, 16–25 балів – помірний, більше 25 балів – тяжкий [6]. На загальний показник гірсутизму впливає етнічна належність жінки, тому іноді ступінь гірсутизму може бути завищений. Для виключення вищевказаної ситуації враховувати необхідно лише посилений ріст термінального волосся, що має довжину більше 5 мм, змінене за формою і структурою та, зазвичай, є пігментованим. Ступінь порідіння волосся в ділянці центрального та бокового проділу оцінюється за шкалою Людвіга [5]. Визначення ступеня тяжкості перебігу акне здійснюється згідно з адаптованою таблицею, рекомендованою у 2016 р. (табл. 1) [6].
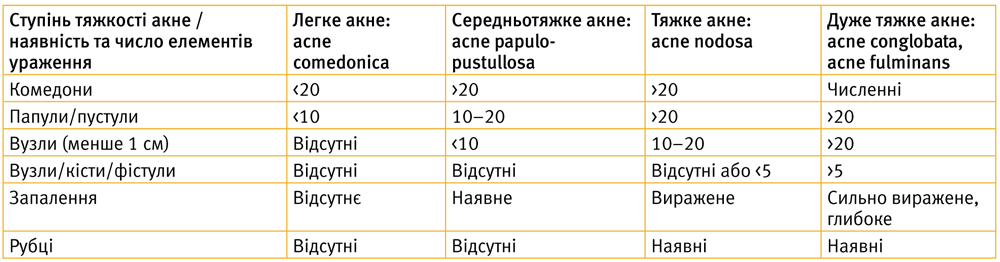
Табл. 1
Вираженість клінічних симптомів не завжди корелює з високим рівнем андрогенів. Ознаки біохімічної гіперандрогенії є менш суб’єктивними, але залежать від чіткості роботи та «безпомилковості» лабораторії. При прийомі комбінованих оральних контрацептивів (КОК) для отримання достовірних лабораторних результатів необхідно відмінити дані препарати на 3 міс. або більше і лише потім проводити лабораторне обстеження [5]. Основний тест, з якого починається лабораторна діагностика гіперандрогенії, – загальний тестостерон. Коливання рівня тестостерону протягом менструального циклу досить незначні, а тому аналіз крові для визначення тестостерону може бути зданий в будь-яку фазу циклу. Важливо враховувати, що для достовірності оцінки рівня активного тестостерону у жінок необхідно визначати концентрацію глобуліну, що зв'язує статеві стероїди (ГЗСС) та обчислювати індекс вільного тестостерону (ІВТ), що розраховується за формулою:

ГЗСС – білок, який синтезується в печінці та змінюється під впливом цілого ряду факторів, на які теж потрібно зважати. Причинами зниження ГЗСС можуть бути гіпотиреоз, гіперінсулінемія, ожиріння, гіпоестрогенія, патологія печінки, нефротичний синдром. Вищевказана патологія призводить до збільшення концентрації біологічно активного тестостерону та клінічних проявів гіперандрогенії. Андростендіон і дегідроепіандростерона сульфат (ДГЕА-С) дозволяють отримати додаткову інформацію щодо наявності гіперандрогенії при СПКЯ [6]. Антимюллерів гормон (АМГ) не рекомендовано використовувати для діагностики СПКЯ як єдиний предиктор; хоча можливість використання АМГ залежить від стандартизації дослідження, вікових та етнічних порогових значень [5]. Однією з морфологічних ознак СПКЯ є збільшення кількості примордіальних, зріючих і кістозно атрезуючих фолікулів. Враховуючи, що АМГ корелює з кількістю антральних фолікулів, цей показник можна вважати додатковим маркером гіперандрогенії та олігоовуляції у жінок із СПКЯ [7]. Доведено, що рівень АМГ у пацієнток з полікістозними яєчниками у 2-4 рази вищий, ніж у здорових жінок [8, 9].
При підвищених рівнях загального тестостерону, ІВТ важливо виключити андрогенпродукуючі пухлини яєчників та наднирників, для яких характерне раптове та швидко прогресуюче наростання симптомів гіперандрогенії, що буде підтверджено значно підвищеними рівнями андрогенів. А саме при підозрі пухлини яєчників: загальний тестостерон >3,5–7 нмоль/л та ДГЕА-С <600 мкг/дл, при підозрі пухлини наднирників: загальний тестостерон >3,5–7 нмоль/л та ДГЕА-С >600 мкг/дл (за умови: 17-ОНП <2 нг/дл) [10]. Підтвердження діагнозу андрогенпродукуючих пухлин яєчників або наднирників відбувається за результатами інструментальної діагностики (магнітно-резонансної та комп’ютерної томографії) [11].
При підвищеному рівні 17-ОНП >2 нг/дл сироватці крові необхідно виключити некласичну вроджену дисфункцію кори наднирників (нВДКН).
Критерій «мультифолікулярна структура яєчників» за результатами ультразвукового дослідження (УЗД) органів малого тазу (ОМТ) має на увазі наявність 20 та більше фолікулів з об'ємом хоча б одного яєчника більше 10 куб. см при відсутності домінантного фолікула, кісти жовтого тіла [5]. Даний критерій може бути правомірним у жінок, гінекологічний вік яких більше 8 років, оскільки мультифолікулярна будова яєчників є ознакою статевого дозрівання. Якщо проводиться трансбдомінальне УЗД ОМТ, то в якості критерія використовується об'єм яєчника більше 10 куб. см [5]. Але все ж таки перевага надається трансвагінальному дослідженню. УЗД необхідно проводити на 3–5 день менструального циклу при регулярних менструаціях або на 3–5 день прогестаген-індукованої кровотечі при опсоменореї або аменореї. Розрахунок оваріального об’єму проводиться з використанням формули: V=a×b×c×0,5, де V – об’єм яєчника (куб. см), a – довжина яєчника (см), b – ширина яєчника (см), c – товщина яєчника (см). Підрахунок фолікулів проводять в поздовжньому, поперечному, передньо-задньому перерізах [12].
Третім критерієм СПКЯ є овуляторна дисфункція, наслідком якої є неплідність, а опосередкованою ознакою – аменорея або олігоменорея (до 8 менструальних циклів за рік). FIGO (International Federation of Gynecology and Obstetrics) в 2018 р. встановила параметри нормального менструального циклу: частота (інтервал між менструаціями): ≥24 – ≤38 днів, тривалість кровотечі: ≤ 8 днів, варіабельність МЦ ≤7–9 днів: (у віці 18–25 років – ≤9 днів, у віці 26–41 рік – ≤7 днів, у віці 42–45 років – ≤9 днів), обсяг щомісячної менструальної крововтрати – нормальний (оцінюється пацієнткою), відсутні міжменструальні кровотечі, двофазність (наявність овуляції), відсутність больових проявів. Вірогідність діагнозу СПКЯ залежить від виявлених ПМЦ, які визначені в рекомендаціях з менеджменту пацієнток з СПКЯ (табл. 2) [5].

Табл. 2
Овуляторна дисфункція може виникати при регулярних циклах та може бути підтверджена показниками рівня прогестерону в сироватці крові [5]. При зниженні рівня прогестерону нижче 3-4 нг/мл цикл вважається ановуляторним. Свідченням хронічної ановуляторної дисфункції є виявлення 2-х ановуляторних циклів з 3-х [13].
У залежності від поєднання критеріїв розрізняють 4 фенотипи СПКЯ [6]:
А – повний або класичний (полікістозна морфологія яєчників + гіперандрогенія +
хронічна ановуляція).
В – неповний класичний (гіперандрогенія + хронічна ановуляція).
С – овуляторна форма (полікістозна морфологія яєчників + гіперандрогенія).
D – нормоандрогенна форма (полікістозна морфологія яєчників + хронічна ановуляція).
Незважаючи на чіткі критерії діагностики СПКЯ, цей діагноз потребує виключення інших захворювань, що мають схожу клінічну картину, а тому можуть «імітувати» СПКЯ [14]. Такими ендокринними порушеннями є: гіперпролактинемія, акромегалія, захворювання щитоподібної залози, гіперкортицизм та некласична вроджена дисфункція кори наднирників (дефіцит 21-гідроксилази).
Виявлення гіперпролактинемії можливе у 7–52% жінок із СПКЯ [14,15]. Патогенез гіперандрогенії при гіперпролактинемії можливо пов'язаний зі стимуляцією секреції андрогенів наднирниками [16].
Гіперпролактинемія визначається високим рівнем пролактину (ПРЛ) в сироватці крові. Незалежно від референтних значень, які надає лабораторія, підвищеним вважається рівень ПРЛ більше 25 нг/мл [17]. Зазвичай рівень ПРЛ у пацієнтів з гіперпролактинемією співвідноситься з етіологією патологічного процесу (табл. 3) [18].
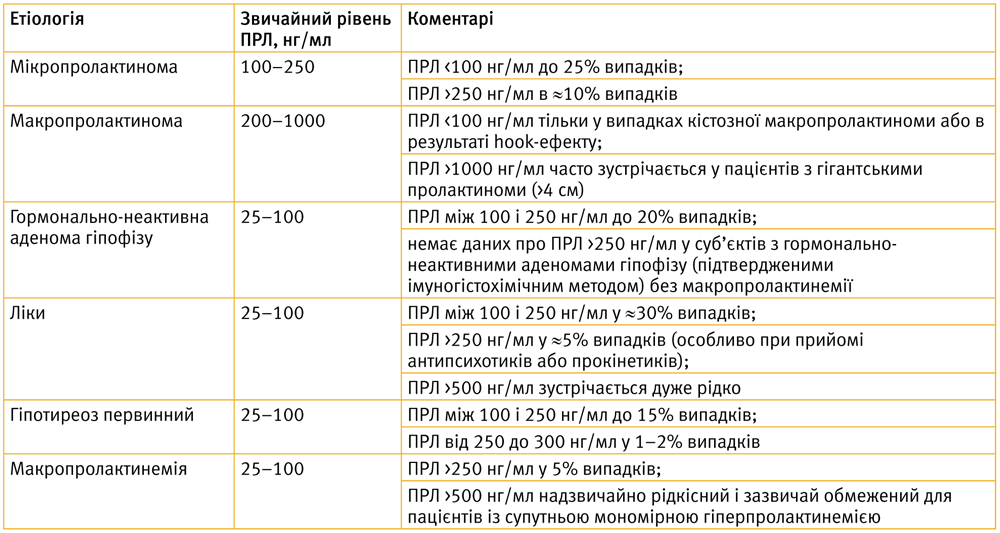
Табл. 3
Якщо виявлено підвищений рівень ПРЛ за відсутності відповідної клінічної картини, слід запідозрити наявність макропролактинемії. Макропролактин (молекулярна маса від 150 до 170 кДа) – це переважно комплекси ПРЛ-IgG, ПРЛ-IgA або полімерних агрегатів високоглікозильованих мономерів ПРЛ [19]. Серед випадків гіперпролактинемії поширеність макропролактинемії може складати від 4% до 40% [20]. У більшості людей ПРЛ у сироватці крові переважно (≈85%) є мономірним, але в деяких випадках можлива діагностика макропролактину [21, 22]. Слід пам’ятати, що макропролактинемія може співіснувати з дійсно підвищеним рівнем пролактину.
Гіперпролактинемія може бути не тільки патологічною, що необхідно враховувати при обстеженні пацієнтки (табл. 4) [23].

Табл. 4
Необхідним є дотримання всіх умов преаналітичного етапу, що дозволить звести до мінімуму фактори, які впливають на результати ПРЛ. Якщо дотримано всіх правил підготовки пацієнта, наступний крок при виявленні високого рівня ПРЛ – виключення вагітності, первинного гіпотиреозу, гіперпролактинемії, індукованої лікарськими засобами, та інших причин. При виключенні вищезазначених станів проводиться макропролактин-скринінг та МРТ гіпофізу, що дозволить здійснити диференційну діагностику між ідіопатичною гіперпролактинемією, макропролактинемією та пролактинсекретуючою аденомою гіпофізу [18].
«Імітувати» клінічну картину СПКЯ може акромегалія. Традиційно це захворювання вважається орфанним, враховуючи розповсюдженість — 70–130 випадків на 1 млн. населення [24]. У жінок з гіперсоматотропінемією ПМЦ зустрічаються у 32–87%, галакторея у 5–48% випадків [25]. Крім того, може спостерігатися потовщення шкіри, гірсутизм, гіпергідроз. При цьому інших клінічних симптомів (головний біль, акромегалоїдні риси обличчя, артропатія, порушення вуглеводного обміну та ін.) може ще не бути або вони будуть малопомітні. Тому для правильного вибору тактики ведення пацієнтки з гіперандрогенією важливо проведення скринінгу для виключення гіперсоматотропінемії. З цією метою використовують визначення інсуліноподібного фактору росту-1 (ІФР-1, Соматомедин С) у сироватці крові [26].
ІФР-1 – це поліпептид, який синтезується під впливом соматотропного гормону в печінці, у кардіоміоцитах, гладком’язових клітинах судин, фібробластах, адипоцитах [26]. Рівень ІФР-1 в крові відображає добовий соматотропіновий секреторний статус і є базовим показником для діагностики акромегалії [27]. Підвищення ІФР-1 (використовують вікові референтні межі) визначає необхідність подальшого обстеження пацієнтки – проведення глюкозо-толерантного тесту з визначенням рівня соматотропного гормону та проведення МРТ гіпофізу. Оральні (не трансдермальні) естрогени знижують показники ІФР-1, тому у жінок, які приймають КОК, інтерпретація результатів ІФР-1 повинна бути обережна [24].
При диференційній діагностиці СПКЯ необхідне виключення гіперкортицизму. ПМЦ при гіперкортицизмі зустрічається у 38–69% жінок, гірсутизм – у 34%, облисіння – у 8–30% [28]. У якості досліджень першої лінії для виключення гіперпродукції кортизолу можливе використання одного з тестів:
- визначення кортизолу в слині о 23:00;
- визначення рівня вільного кортизолу в добовій сечі;
- 1-мг дексаметазоновий супресивний тест.
При виборі діагностичного тесту важливо враховувати: діагностичну інформативність, можливість проведення в амбулаторних умовах та простоту виконання. Найбільшу чутливість та специфічність для скринінгу гіперкортицизму має нічне визначення кортизолу в слині, яке дозволяє оцінити концентрацію біологічно активного гормону та враховує циркадні ритми кортизолу. Це дослідження, на відміну від визначення кортизолу в добовій сечі або сироватці, може бути використане у вагітних та у жінок, які приймають КОК. В теперішній час для підтвердження або виключення гіперкортицизму рекомендується поєднання двох лабораторних тестів або використання одного тесту не менше чим двічі у різні дні. Комбінація досліджень дозволяє підвищити чутливість методик до 100%, а специфічність – до 97,4% [29].
Важливими є умови підготовки пацієнтки та дотримання правил здачі аналізів. При визначенні кортизолу в добовій сечі обов’язково використовується консервант (порошок борної кислоти). Сечу потрібно збирати протягом доби, дотримуючись звичайного питного режиму. Отримання хибнопозитивних результатів можливе при надлишковому вживанні рідини (більше 5 л/добу), хибнонегативних – при порушенні правил збору сечі (більше 24 годин), надлишковому вживанні солі, стресі. Враховуючи вплив деяких лікарських препаратів (глюкокортикоїди, КОК, естрогени, спіронолактон, фуросемід, барбітурати, інсулін, аспірин, атропін, індометацин, кетоконазол, леводопа, морфін, ніфедипін та ін.) на рівень кортизолу, перед збором сечі необхідно ретельно збирати анамнез на предмет прийому медикаментів та визначити тест, якому надати перевагу та використати в якості скринінгу гіперкортицизму.
Нічний супресивний 1-мг дексаметазоновий тест базується на принципі пригнічення секреції АКТГ з наступним зниженням продукції кортизолу. Методика проведення тесту наступна: пацієнтка приймає о 23:00 1 мг дексаметазону, а потім о 8–9 годині наступного ранку натще проводиться забір крові для визначення рівня кортизолу. Діагноз гіперкортицизму можливо запідозрити при рівні кортизолу крові >1,8 мкг/дл (50 нмоль/л) [29]. Проведення даного дослідження можливе в амбулаторних умовах та не потребує попередньої підготовки пацієнтки. Важлива своєчасність прийому пацієнткою дексаметазону.
Преаналітичний етап визначення кортизолу в слині має ряд переваг: безболісність і неінвазивність методики, відсутність фармакологічного втручання та необхідності госпіталізації пацієнтки, а також виключається участь медичного персоналу. Правила збору матеріалу наступні: протягом 30 хв. до збору слини не вживати їжу та напої, не палити, не чистити зуби; протягом доби виключити вживання спиртних напоїв; уникати зразків, контамінованих кров’ю (навіть злегка червоних), виключити попадання частинок губної помади.
Запідозрити нВДКН можна по гінекологічному (ПМЦ, гірсутизм, недостатність лютеїнової фази) та репродуктивному анамнезу (неплідність, невиношування вагітності). 90–95% всіх ферментних дефектів при ВДКН виникають внаслідок дефіциту ферменту 21-гідроксилази. Ступінь недостатності цього ферменту залежить від «об’єму» мутації: збереження активності 21-гідроксилази більше 5% призведе до нВДКН, зниження активності до 0-2% – до класичної ВДКН [30].
Маркер нВДКН (дефіцит 21-гідроксилази) – підвищений рівень 17-ОНП в сироватці крові. Для отримання достовірного лабораторного результату важливо визначати 17-ОНП рано вранці близько 8:00, в ранню фолікулярну фазу (3–5 день менструального циклу) [31]. Результат базального 17-ОНП <2 нг/мл дозволяє виключити діагноз нВДКН [31, 32]. При цьому залишається можливість гетерозиготного носійства даного захворювання. Отримання результату базального 17-ОНП ˃10 нг/мл, підтверджує діагноз нВДКН, оскільки існує приблизний зв'язок між базальним та стимульованим рівнями 17-ОНП у осіб без патології, у пацієнтів, гетерозиготних за дефіцитом 21-гідроксилази та при наявності легкого (некласичного) чи тяжкого дефіциту 21-гідроксилази [32]. Рівень 17-ОНП від 2 до 10 нг/дл потребує подальшого дообстеження у вигляді проведення проби з козинтропіном. Рівень стимульованого 17-ОНП ≤10 нг/мл виключає нВДКН, ˃10 нг/мл підтверджує діагноз нВДКН.
Тест з козинтропіном повинен проводитися для підтвердження діагнозу до початку лікування глюкокортикоїдами, оскільки результати проби можуть бути сумнівні. Якщо пацієнтка вживає глюкокортикоїди, або неможливо провести даний тест в зв’язку з відсутністю даного препарату (препарат не зареєстрований в Україні), у якості другого етапу обстеження з метою виключення нВДКН, виконується молекулярно-генетичний аналіз. Враховуючи ситуацію з відсутністю реєстрації козинтропіну в Україні, проведення проби малоймовірне. Тому в якості 2-го етапу діагностики нВДКН на «перший» план виходить молекулярно-генетичне обстеження. Спочатку здійснюється пошук частих мутацій в гені CYP21 – V281L, P30L, Р453S, P105L, R339H, V304M, G375S. У хворих з нВДКН в 70% хромосом виявляється мутація V281L в 7 екзоні. Виявлення двох мутацій дозволяє поставити діагноз (табл. 5). При виявленні однієї мутації проводиться повне секвенування гену CYP21 [30, 32, 34].
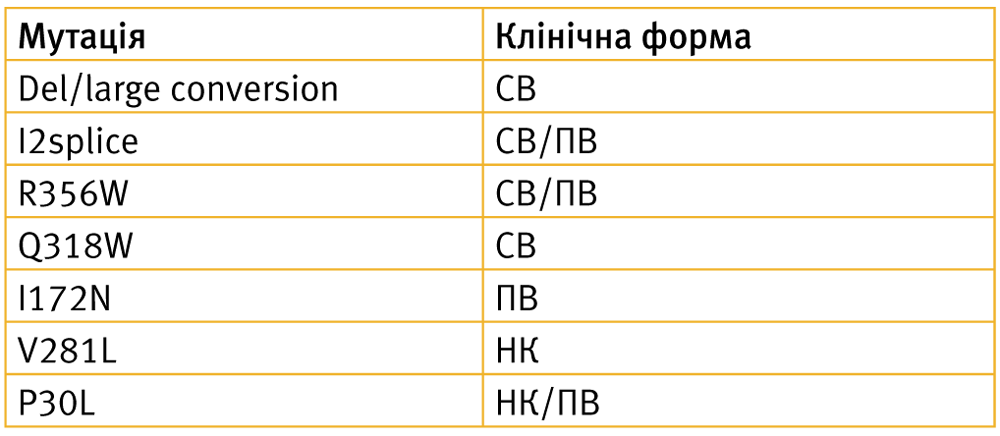
Табл. 5
СВ – сільвтрачаюча форма, ПВ – проста вірильна форма, НК – некласична форма
Крім констатації факту гіперандрогенії та виключення причин, які можуть призвести до СПКЯ, важливо розібратися з можливими патогенетичними механізмами з метою подальшого впливу на них. Як один з ланцюгів патогенезу СПКЯ, розглядається інсулінорезистентність, яка в подальшому призводить до компенсаторного збільшення секреції інсуліну бета-клітинами підшлункової залози. Крім того, інсулін чинить пряму стимулюючу дію на секрецію андрогенів тека-клітинами яєчників та підсилює ЛГ-залежний синтез андростендіону стромальними та тека-клітинами яєчників [35]. Крім інсулінорезистентності, у пацієнток з СПКЯ виявляються порушення толерантності до глюкози в 30–40% та цукровий діабет 2-го типу в 7,5% випадків [36, 37]. Діагностика порушень вуглеводного обміну полягає в визначенні глікемії (натще і постпрандіальної) та глікованого гемоглобіну, а при необхідності – проведення глюкозо-толерантного тесту (75 г глюкози). Для виявлення нечутливості до інсуліну останнім часом найчастіше використовується індекс НОМА, показники якого високо корелюють з результатами еуглікемічного гіперінсулінемічного клемп-методу – «золотого стандарту» оцінки інсулінорезистентності [38].
Таким чином, для встановлення діагнозу СПКЯ та вибору подальшої тактики лікування пацієнток необхідно використати ряд лабораторних тестів, які дозволять встановити наявність біохімічної гіперандрогенії, провести диференційну діагностику, виключивши патологію, яка може «імітувати» дане захворювання, та виявити патогенетичні механізми.
Література:
- Sosnova, E.A., «Polycystic ovary syndrome.» Аrkhiv Akusherstva i Ginekologii im. V.F. Snegireva (V.F. Snegirev Archives of Obstetrics and Gynecology, Russian journal). 2016; 3(3): 116-129. (In Russ.). doi.org/10.18821/2313-8726-2016-3-3-116-129.
- Fauser, B.C., Tarlatzis, B.C., Rebar, R.W., et al., «Consensus on women's health aspects of polycystic ovary syndrome (PCOS): the Amsterdam ESHRE/ASRM-Sponsored 3rd PCOS Consensus Workshop Group.» Fertil Steril. 2012 Jan;97(1):28-38.e25. doi: 10.1016/j.fertnstert.2011.09.024.
- Teede, H., Deeks, A., Moran, L., «Polycystic ovary syndrome: a complex condition with psychological, reproductive and metabolic manifestations that impacts on health across the lifespan.» BMC Med. 2010 Jun 30;8:41. doi: 10.1186/1741-7015-8-41.
- Azziz, R., Carmina, E., Chen, Z., et al., «Polycystic ovary syndrome.» Nat Rev Dis Primers. 2016 Aug 11;2:16057. doi: 10.1038/nrdp.
- Teede, H.J., Misso, M.L., Costello, M.F., et al., International PCOS Network, «Recommendations from the international evidence-based guideline for the assessment and management of polycystic ovary syndrome.» Fertil Steril. 2018 Aug;110(3):364-379. doi: 10.1016/j.fertnstert.2018.05.004.
- Kaminskyi, V.V., Tatarchuk, T.F., Dubossarskaya Y., et al., «National consensus on Management of Patients with Hyperandrogenia.» Reproductive Endocrinology. 4.30(2016):8–18. doi: dx.doi.org/10.18370/2309-4117.
- Conway, G., Dewailly, D., Diamanti-Kandarakis, E., et al., «Special Interest Group.The polycystic ovary syndrome: a position statement from the European Society of Endocrinology.» Eur J Endocrinol. 2014 Oct;171(4):P1-29. doi: 10.1530/EJE-14-0253
- Mulders, A.G., Laven, J.S., Eijkemans, M.J., de Jong, F.H., Themmen, A.P., Fauser, B.C., «Changes in anti-Müllerian hormone serum concentrations over time suggest delayed ovarian ageing in normogonadotrophic anovulatory infertility.» Hum Reprod. 2004 Sep;19(9):2036-42. doi.org/10.1093/humrep/deh373.
- Piltonen, T., Morin-Papunen, L., Koivunen, R., Perheentupa, A., Ruokonen, A., Tapanainen, J.S., «Serum anti-Müllerian hormone levels remain high until late reproductive age and decrease during metformin therapy in women with polycystic ovary syndrome.» Hum Reprod. 2005 Jul;20(7):1820-6. doi.org/10.1093/humrep/deh850.
- Pugeat, M., Plotton, I., de la Perrière, A.B., Raverot, G., Déchaud, H., Raverot, V., «Мanagement of endocrine disease Hyperandrogenic states in women: pitfalls in laboratory diagnosis.» Eur J Endocrinol. 2018 Apr;178(4):R141-R154. doi: 10.1530/EJE-17-0776.
- Комиссаренко И. В. Классификация злокачественных опухолей надпочечников / И. В. Комиссаренко, С. И. Рыбаков, А. Н. Кваченюк // Клініч. хірургія. - 2004. - № 9. - С. 25-27.
- Попова С.С. Наследственная и врождённая патология в структуре эндокринопатий, сопровождающихся поликистозом яичников // Ультразвуковая перинатальная диагностика. - 2005. - № 20. – С. 55-58.
- Azziz, R., Carmina, E., Dewailly, D., et al., «Positions statement: criteria for defining polycystic ovary syndrome as a predominantly hyperandrogenic syndrome: an Androgen Excess Society guideline.» J Clin Endocrinol Metab. 2006 Nov;91(11):4237-45.
- Kyritsi, E.M., Dimitriadis, G.K., Angelousi, A., et al., «The value of prolactin in predicting prolactinoma in hyperprolactinaemic polycystic ovarian syndrome.» Eur J Clin Invest. 2018 Jul;48(7):e12961. doi: 10.1111/eci.12961.
- Kyritsi, E.M., Dimitriadis, G.K., Kyrou, I., Kaltsas, G., Randeva, H.S., «PCOS remains a diagnosis of exclusion: A concise review of key endocrinopathies to exclude.» Clin Endocrinol (Oxf). 2017 Jan;86(1):1-6. doi: 10.1111/cen.13245.
- Moria, Y., Kortbawi, R., El-Asmar, N., Arafah, B.M., «Increased androgen secretion in patients with prolactinomas: The impact of altered HPA function.» Pituitary 2019 Apr;22(2): 170-178. doi: 10.1007/s11102-019-00948-w.
- Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group, «Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome.» Fertil Steril. 2004 Jan;81(1):19-25.
- Vilar, L., Vilar, CF., Lyra, R., Freitas, M.C., «Pitfalls in the Diagnostic Evaluation of Hyperprolactinemia.» Neuroendocrinology 109 (2019): 7–19. doi:10.1159/000499694.
- Lippi, G., Plebani, M. «Macroprolactin: Searching for a needle in a haystack?» Clin. Chem. Lab. Med. 54 (2016): 519–522. doi: 10.1515/cclm-2015-1283.
- Samson, S.L., Hamrahian, A.H., Ezzat, S.; AACE Neuroendocrine and Pituitary Scientific Committee; American College of Endocrinology (ACE), «American Association of Clinical Endocrinologists, American College of Endocrinology disease state clinical review: clinical relevance of macroprolactin in the absence or presence of true hyperprolactinemia.» Endocr Pract. 2015 Dec;21(12):1427-35. doi: 10.4158/EP15938.
- Melmed, S., Casanueva, F.F., Homan, A.R., et al., «Diagnosis and treatment of hyperprolactinemia: an Endocrine Society clinical practice guideline.» J Clin Endocrinol Metab. 2011 Feb;96(2):273-88. doi: 10.1210/jc.2010-1692.
- Vilar, L., Fleseriu, M., Bronstein, M.D., «Challenges and pitfalls in the diagnosis of hyperprolactinemia.» Arq Bras Endocrinol Metabol. 2014 Feb;58(1):9-22. dx.doi.org/10.1590/0004-2730000003002.
- Demssie, Y., Davis, J., «Hyperprolactinaemia.» Clinical medicine (London, England) 8(2):216-9 · May 2008. DOI: 10.7861/clinmedicine.8-2-216.
- Pronin, V.S., Pronin, E.V., «International consensus recommendation on the diagnosis and treatment of acromegaly.» Endokrinologiya: novosti, mneniya, obuchenie [Endocrinology: News, Opinions, Training]. 2019; 8 (1): 49–62. doi: 10.24411/2304-9529-2019-11006.
- Melmed, S., Casanueva, F.F., Klibanski, A., et al., «A consensus on the diagnosis and treatment of acromegaly complications.» Pituitary. 2013 Sep;16(3):294-302. doi: 10.1007/s11102-012-0420-x.
- Melmed, S., Bronstein, M.D., Chanson, P., et al., «A Consensus Statement on acromegaly therapeutic outcomes.» Nat Rev Endocrinol. 2018 Sep;14(9):552-561. doi: 10.1038/s41574-018-0058-5.
- Weber, M.M., Auernhammer, C.J., Lee, P.D., Engelhardt, D., Zachoval, R., «Insulin-like growth factors and insulin-like growth factor binding proteins in adult patients with severe liver disease before and after orthotopic liver transplantation.» Horm Res. 2002;57(3-4):105-12.
- Melnichenko G.A., Dedov I.I., Belaya Z.E., et al. «Cushing’s disease: the clinical features, diagnostics, differential diagnostics, and methods of treatment.» Problems of Endocrinology. - 2015. - Т. 61. - №2. - C. 55-77. doi: 10.14341/probl201561255-77.
- Nieman L., «Cushing’s syndrome: update on signs, symptoms and biochemical screening.» Eur J Endocrinol. 2015 Oct;173(4):M33-8. doi: 10.1530/EJE-15-0464.
- Melnichenko, G.A., Troshina, E.A., Molashenko, N.V., Sazonova, A.I., Uzhegova, Zh.A., «Russian Association of Endocrinologists clinical practice guidelines for diagnosis, treatment and preventive measures in congenital adrenal hyperplasia due to 21-hydroxylase deficiency patients in adulthood.» Consilium Medicum. 2016; 18 (4): 8–19.
- Speiser, P.W., Arlt, W., Auchus,, R.J., et al., «White PCCongenital Adrenal Hyperplasia Due to Steroid 21-Hydroxylase Deficiency: An Endocrine Society Clinical Practice Guideline» J Clin Endocrinol Metab. 2018 Nov 1;103(11):4043-4088. doi: 10.1210/jc.2018-01865.
- Speiser, P.W., Azziz, R., Baskin, L.S., et al., «Congenital Adrenal Hyperplasia Due to Steroid 21-hydroxylase Deficiency: An Endocrine Society Clinical Practice Guideline» // J Clin Endocrinol Metab. 2010 Sep;95(9):4133-60. doi: 10.1210/jc.2009-2631.
- New, M.I., Lorenzen, F., Lerner, A.J., et al., «Genotyping steroid 21-hydroxylase deficiency: hormonal reference data.» J Clin Endocrinol Metab. 1983 Aug;57(2):320-6.
- Адреногенітальний синдром у дітей: неонатальний скринінг, діагностика і лікування: Методичні рекомендації. – Харків, 2013. – 44 с.
- Baillargeon, J.P., Carpentier, A., «Role of insulin in the hyperandrogenemia of lean women with polycystic ovary syndrome and normal insulin sensitivity.» Fertil Steril. 2007 Oct;88(4):886-93.
- Legro, R.S., Kunselman, A.R., Dodson, W.C., Dunaif, A., «Prevalence and predictors of risk for type 2 diabetes mellitus and impaired glucose tolerance in polycystic ovary syndrome: a prospective, controlled study in 254 aff ected women.» J Clin Endocrinol Metab. 1999 Jan;84(1):165-9.
- Ehrmann, D.A., Barnes, R.B., Rosenfield, R.L., Cavaghan, M.K., Imperial, J., «Prevalence of impaired glucose tolerance and diabetes in women with polycystic ovary syndrome.» Diabetes Care. 1999 Jan;22(1):141-6.
- Matthews, D.R., Hosker, J.P., Rudenski, A.S., Naylor, B.A., Treacher, D.F., Turner, R.C., «Homeostasis model assessment: insulin resistance and beta-cell function from fasting plasma glucose and insulin concentration in man.» Diabetologia. 1985 Jul;28(7):412-9.


коментарів