
Нові настанови стандартизують розрахунки очікуваних пологів за датами
New Guidelines Standardize Pregnancy Due Date Estimates
Medscape Medical News
Оприлюднено 25 вересня 2014 р. Джерело: www.medscape.com/viewarticle/832357?src=wnl_int_edit_tp10&uac=171030SR
Автор: Troy Brown; Переклад українською: Олексій Соловйов; до перекладу первинного огляду Troy’а Brown’а від вересня 2014 р. додано вільно відібрані тлумачем цитати з переглянутої у травні 2017 р. настанови; такі цитати й нові твердження від правок 2017 року виділено у нижченаведеному тексті жирним шрифтом.
Повний текст переглянутого у травні 2017 року спільного документу (Committee Opinion, No 700, May 2017, "Methods for Estimating the Due Date") цих поважних організацій – ACOG (American College of Obstetricians and Gynecologists, Американського Товариства акушерів і гінекологів), AIUM (American Institute of Ultrasoundin Medicine, Американського інституту ультразвуку в медицині) та SMFM (Society for Maternal-Fetal Medicine, Спільноти материнсько-плодової медицини) – можна безоплатно завантажити тут: http://www.acog.org/Resources-And-Publications/Committee-Opinions/Committee-on-Obstetric-Practice/Methods-for-Estimating-the-Due-Date.
Нові настанови розрахунків очікуваної дати пологів (estimated due date, EDD) були розроблені ACOG, AIUM та SMFM і будуть оприлюднені в Obstetrics&Gynecology та Journal of Ultrasound in Medicine.
Ключові медичні групи кажуть, що нові настанови щодо розрахунків вагітности за датами допоможуть виправити поточні розбіжності розрахунків віку вагітности і полегшать узгодженість догляду вагітних жінок та їх дітей.
«Правильно визначена EDD належить до найважливіших результатів оцінки перебігу вагітности з початку спостереження від раннього віку», – пишуть автори. «Ця інформація має життєво важливе значення для узгодження потрібної акушерської допомоги, планування та оцінки деяких допологових досліджень, визначення відповідності росту плода, а також розробки заходів для запобігання передчасних або пізніх пологів та пов’язаних з ними захворювань… Послідовний і вимогливий підхід до точного датування також є імперативом публічного здоров’я та наукових досліджень внаслідок його впливу на створення дизайнів наукових праць та демографічну статистику», – кажуть вони.
Настанови підкреслюють важливість високоякісного ультразвукового дослідження у І триместрі вагітності. Автори зауважують, що традиційна оцінка віку вагітности, що ґрунтується на першому дні останніх місячних, використана сама по собі, може бути хибною, оскільки лише близько половини жінок можуть точно назвати дати своїх останніх місячних. До того ж, місячний цикл може виявитися нерівномірним у своїй тривалості, а час овуляції може змінюватись.

Вимірювання куприко-тім’яного розміру (КТР) є тим точнішими, чим меншим є вік вагітности у І триместрі під час ультразвукового дослідження. Як розмір, слід використовувати середнє значення з трьох окремих вимірювань поздовжнього зрізу в дійсно серединній плоскості, зі статевим горбиком та спинномозковим каналом на зрізі, по прямій лінії вимірюючи довжину між найвіддаленішими точками тім’я та куприка. Середній розмір плодового міхура для оцінки EDD використовувати не радимо.
Настанова також стосується розрахунків EDD у ІІ й ІІІ триместрах вагітности. «Уніфікований підхід до визначення EDD буде корисним лікарям при усіх типах вагітностей, особливо для жінок, які раніше вже мали медичні проблеми впродовж вагітності», – сказав James D. Goldberg, MD, заступник голови ACOG's Committee on Obstetric Practice, що розробляв загальну думку комітету.
«Для деяких жінок, особливо з попередніми передчасними пологами чи іншими ускладненнями, наприклад, вертикальним розрізом при цісарському розтині, точніші EDD є важливими для безпечнішого планування догляду їх поточної вагітности та для визначення вчасних пологів», – зазначив Joshua A. Copel, MD, залучений з AIUM член.
Наприклад, одне дослідження знайшло зменшення потреб збудження пологів у групі жінок, випадковісно розподілених для здійснення звичайного УЗД 1-го триместру, порівняно до тих, кому робили УЗД лише у ІІ триместрі. Огляд Cochrane дійшов висновку, що ультразвук може зменшувати кількість індукцій пологів та є провідним способом раннього визначення багатоплодових вагітностей.
Для встановлення EDD при вагітностях внаслідок запліднення in vitro слід використати вік зародка та дату його переносу. Наприклад, для 5-денного зародка EDD буде 261 день після дня його переносу до порожнини матки. Подібно, EDD для триденного зародка має бути на 263 день з дня його переносу.
ACOG, AIUM та SMFM надають наступні поради щодо способу визначення віку вагітности й очікуваних пологів:
- Найточнішим способом визначення або підтвердження віку вагітности є ультразвукове вимірювання зародка чи плода у І триместрі вагітности (до і включно з 13 тижнів 6/7 днів вагітности).
- Як вагітність одержана внаслідок допоміжних репродуктивних технологій, для визначення EDD слід користуватись віком вагітности, що походить зі штучного запліднення. Наприклад, для встановлення EDD при вагітностях внаслідок запліднення in vitro слід використати вік зародка та дату його переносу.
- Як лише одержано дані щодо останніх місячних та дані першого точного УЗД чи обидва разом, слід розрахувати та обговорити з пацієнткою, а також чітко записати у картці пацієнтки вік її вагітности та очікувану дату пологів. Пізніші зміни EDD можуть бути зроблені тільки в рідкісних випадках, мають бути обговореними з пацієнткою та чітко записані у медичній карті пацієнтки.
- Коли визначено способами, описаними в цьому документі, очікуваний вік вагітности й дату пологів, ліпшу положничу оцінку з метою клінічного догляду слід записати у свідоцтві про народження (від тлумача: так і написано – «on the birth certificate»; ймовірно, що йдеться про медичне свідоцтво, а не про «Свідоцтво про народження» як документ РАГС, прийнятий у нас). З метою наукових досліджень чи опитувань слід використовувати найліпші розрахунки для визначення віку вагітности, а не розрахунки на підставі лише даних про останні місячні.
- Вагітність без ультразвукового дослідження, що підтвердило би чи переглянуло попередні EDD до 22 тижнів 0/7 днів віку вагітности слід вважати недостатньо точно (suboptimally) оціненою.
«Це добре для наших пацієнток. Маємо значні розбіжності у способах різних лікарів розраховувати EDD своїх пацієнток; стандартизація дозволить поліпшити догляд вагітних. Цей новий стандарт може поліпшити наслідки станів високого ризику, що потребують планування пологів при доношених та переношених вагітностях», – сказав Sean C. Blackwell, MD, залучений з SMFM член ACOG.
Від упорядника розділу й тлумача Олексія Соловйова:
Якщо хтось із шановних читачів вважатиме цей матеріал зайвим чи непотрібним або не актуальним для українських лікарів, то раджу, по-перше, замислитись, а чому ж тоді стільки уваги питанню точнішого визначення віку вагітности та очікуваної дати пологів приділяють аж три найповажніші лікарські громадські організації у США, ще й переглянули та доповнили зміст свого спільного документа лишень через три роки від його прийняття. Невже у США лікарі менш досвідчені та освічені, ніж українські? J
По-друге, подивіться на чинні в Україні зразки так званих «обмінних карт» чи «книжок диспансеризації» вагітних, де досі містяться графи для заповнення не лише щодо останніх місячних, а й щодо рухів дитини…
По-третє, досі особисто й у своєму власному робочому кабінеті час від часу бачу пацієнток, яким в наш час, у першому триместрі вагітности, на підставі ультразвукового дослідження, лікарями виставляються терміни вагітности, що на два тижні відрізняються від загальноприйнятих! Тобто, деякі з нас досі користуються старими радянськими друкованими табличками, де умовний термін вагітности розраховується не від умовного 1-го дня останніх місячних, а від умовного дня запліднення…
Ну, і на останок – для тих, хто має сумнів в актуальності піднятої теми: досі, кожного дня, навіть «у столиці нашої Батьківщини», самими лікарями, в протоколах УЗД 1-го триместру, масово зустрічаються записи на кшталт: «КТР дорівнює…, що відповідає умовному терміну вагітности… тиж… днів», але в висновках протоколу УЗД все одно буде написано, що вагітність терміном «11–12» чи «13–14» тижнів…
Таким чином, навіть запровадивши в Україні згадану настанову, але залишивши існуючий стан речей з подібними висновками + «дані про дату перших рухів дитини», ми зведемо на ніц сам сенс настанови.
Тому й зустрічаємо на кожному кроці не лише пацієнток, а й самих лікарів, які просять наприкінці 3-го триместру вагітности «зробити якісне УЗІ» для… «уточнення терміну гестації».
Детальніше

Black Sea Pearl
ІV-й міжнародний конгрес з гемостазіології, анестезіології та інтенсивної терапії
Одесса... Аркадія… ці слова підіймають настрій! І не дивно, Аркадія є найпопулярнішим курортним районом Одеси. Район розташований на березі Чорного моря в Приморському районі міста, неподалік від 5–7 станції Великого Фонтану. Саме цей відомий пляж «Аркадія» був обраний засновниками міста в якості головного, та названий на честь однієї гірської області в Греції.

Для анестезіологів України Одесса та Аркадія асоціюється не тільки з теплим морем та гарним пляжем. Тут за традицією пройшов ІV-й міжнародний конгрес з гемостазіології, анестезіології та інтенсивної терапії «Black Sea Pearl». Організатором конгресу був д. мед. н., проф. О. О. Тарабрін. Йому, разом зі своєю потужною командою, вдалось перетворити 23–25 травня на справжнє свято науки.
У роботі конгресу брали участь провідні фахівці з України, Ізраїлю, Росії, Молдови, Німеччини,Франції, Італії. Гарна організація, професійне товариство, можливість спілкування на актуальні теми, цікаві дискусії – ось завдяки чому конгрес справді пройшов вдало.
Під час конгресу було прочитано понад п’ятдесят лекцій та доповідей, проводились цікаві майстер-класи. Кожен з учасників міг обрати особисто йому цікаву тему, прослухати її та взяти участь в обговоренні. Конгрес проходив в санаторії «Аркадія» з розвиненою інфраструктурою та сучасними лекційними залами.
Розпочався конгрес з привітання акад. НАМН України, д. мед. н., проф. В. М. Запорожана. До речі, акушерська секція на конгресі була дуже добре представлена, їй виділили цілий день в основній залі. І це не дивно, оскільки до Одеси приїхали всесвітньо відомі метри акушерської анестезіології. Дозвольте коротко зупинитись безпосередньо на цій медичній дисципліні.
Надзвичайно цікаві доповіді були прочитані метром акушерської анестезіології, проф. Є. М. Шифманом з Москви. Перша лекція була присвячена масивним акушерським кровотечам. Єфим Мунійович наголосив, що 75–90% всіх масивних акушерських кровотеч пов’язано з матковою атонією. При наданні допомоги потрібно обов’язково приділяти увагу температурі інфузійних розчинів, оскільки холодні інфузійні розчини у великому об’ємі посилюють або спричиняють коагулопатію. Також в післяопераційному періоді необхідно уникати гіперволемії. Велику зацікавленість серед слухачів викликала тема застосування утеротоніків. Професором Шифманом було підкреслено, що для забезпечення скорочення матки потрібні менші дози окситоцину. Введення 3 Од окситоцину протягом 15 с під час планових операцій має явні переваги в утеротонічних властивостях та щодо гемодинамічних порушень перед постійною інфузією більших доз. Було чітко наголошено, що введення 10 Од окситоцину болюсно може призвести до летальних наслідків від кардіоваскулярних ускладнень! Доповідач навів схему, опубліковану у поважному журналі International Journal of Obstetric Anesthesia «Oxytocin protocols during cesarean delivery: time to acknowledge the risk/benefit ratio?» L. Tsen & M. Balki:
1) 3 ОД. ударна доза
2) 3 хв. оцінка ситуації
3) 3 ОД доза спасіння
4) 3 загальні дози (1 ударна, 2 спасіння)
5) 3 ОД/л – робоча суміш, інфузоматом 100 мл/год. – доза підтримки.
Також було наголошено, що метилергометрин повинен вводитися суворо за показами, з обов'язковим інформуванням анестезіолога.
Доповідь була надзвичайно цікавою, було багато коментарів та питань, і якби не ліміт часу, дискусія тривала би до вечора.
Не менш цікавою темою, піднятою професором Шифманом, була «Тромботична мікроангіопатія в акушерській практиці». Це клінічний синдром, для якого характерні: тромбоцитопенія, мікроангіопатична гемолітична анемія (неімунна гемолітична анемія) та мікроваскулярний тромбоз кінцевих артеріол і капілярів з множинною дисфункцією органів. Тромбоцитопенія – другий за частотою «гематологічний прояв» вагітності після анемії. У III триместрі частота тромбоцитопенії складає 6,6–11,6%. HELLP-синдром, прееклампсія та атиповий гемолітико-уремічний синдром відносяться до різновидностей тромботичної мікроангіопатії. Гемоліз, який ми можемо побачити макроскопічно лише в 10% випадках, діагностично мало про що нам говорить, просто констатує факт – що він є!

А от наявність фрагментів еритроцитів (шизоцити) в мазку крові свідчить не просто про розвиток гемолізу, а саме про розвиток мікроангіопатичного гемолізу! Це підтверджує приналежність прееклампсії до групи тромботичних мікроангіопатій. При імунному гемолізі шизоцитів немає.
Автором було приділено багато уваги диференціальній діагностиці між прееклампсією з HELLP-синдромом та атиповим гемолітико-уремічним синдромом. Відмічено, що після розродження при прееклампсії настає покращення стану породіллі, а при атиповому гемолітико-уремічному синдромі відбувається персистування тромботичної мікроангіопатії, наростання креатиніну, синдрому поліорганної недостатності.
Надзвичайно цікавою темою, про яку говорилось низкою авторів, була тема TRALI-синдрому (гострого посттрансфузійного ураження легень). І недаремно, оскільки FDA офіційно визнало TRALI-синдром провідною причиною смерті (до 38% у структурі всіх транфузіонних ускладнень). Частота синдрому TRALI сягає 0,3% на одну одиницю перелитої плазми крові. Критерії діагностики:
- Гостра дихальна недостатність протягом 6 год. після трансфузії.
- Різко виникла двостороння інфільтрація легень (Rg).
- Для підтвердження імунного генезу:
- АТ до HLA або до аллоантигенів нейтрофілів людини (в донорській крові).
- Виявлення антилейкоцитарних АГ (у реципієнта).
Короткий та дієвий рецепт, як позбутись TRALI-синдрому в акушерстві: не використовувати плазму від жінок-донорів! Саме на цьому наголошували наші ізраїльські колеги, коли ми обговорювали дану тему.
Також цікаву та змістовну доповідь щодо сучасних принципів у післяопераційному знеболенні зробив професор Ю. Ю. Кобиляцький (Дніпропетровськ, Україна).
Він наголосив, що чим вища інтенсивність болю в післяопераційному періоді, тим більша вірогідність її хронізації. Доповідач підкреслив важливість впровадження в практику принципів мультимодального підходу до знеболення.
Автор цього репортажу також мав можливість поділитись сучасним підходом до знеболення в акушерстві, який активно впроваджується в пологовому будинку «Лелека» у м. Києві.

Надзвичайно важливим є використання регіонарних методик знеболення, оскільки завдяки їм можна повністю відмовитись від наркотичних анальгетиків у післяопераційному періоді. Рання активація пацієнток (харчування та рух в межах палати), контрольоване використання утеротоніків (без потреби не призначаємо) та регіонарні методи знеболення роблять післяопераційний період в акушерстві приємним та безболісним.
Великим блоком доповідей була представлені проблемні питання гемостазу. Одним з провідних фахівців в Україні з питань гемостазу є проф. О. О. Тарабрін, який разом з проф. І. І. Тютріном (Томськ, Росія) поділились своїм досвідом роботи з тромбоеластографом. Завдяки сучасним приладам у нас є можливість on line діагностувати проблеми гемостазу, що однозначно пришвидшить надання допомоги та безперечно покращить її якість.
На майстер-класі був продемонстрований гемовіскозіметр, досвід використання якого є найбільшим саме у одеситів. Використання низькочастотної вібраційної п'єзоелектричної гемовіскозіметрії дозволяє оперативно і достовірно оцінити кінетику тромбоутворення від початкової в'язкості аж до утворення згустка і його фібринолізу, а отже, виявити гемокоагуляційні розлади до-, під час та після операції, що дозволяє своєчасно проводити їхню профілактику і комплексну корекцію, а також контролювати дію про- і антикоагулянтів.
Також змістовні доповіді проф. Р. О. Ткаченка, проф. Я. М. Підгірного та президента асоціації анестезіологів України проф. С. О. Дуброва були присвячені сепсису та антибіотикотерапії. Всі автори дійшли спільної думки, що анатомо-функціональні особливості вагітної/породіллі необхідно враховувати при проведенні волемічної ресусцитації та антибактеріальної терапії.
Актуальну тему для обговорення підняв колега з Ізраїлю – проф. Олександр Злотник (Soroka University Medical Center). Мова йшла про анестезію у вагітних з надлишковою масою тіла. Для запобігання розвитку некерованої артеріальної гіпотензії при спінальній анестезії під час кесаревого розтину використовують різні методи розрахунку доз місцевого анестетика. Деякі з них засновані на застосуванні фіксованих доз препаратів, інші — на розрахунку дози місцевого анестетика за морфометричними характеристиками пацієнта. Цей варіант більш обґрунтований, оскільки встановлено, що довжина і маса тіла значно впливають на остаточний рівень блока. Час розвитку сенсорного блока зростає із збільшенням довжини тіла і зменшується зі збільшенням маси.
Разом з анестезіологами в залі були присутні акушери-гінекологи, які зробили секцію живою та особливо цікавою, оскільки багато питань у сучасній медицині виникають на стику двох, а іноді трьох спеціальностей. Займатись лікуванням хворих, що знаходяться у критичному стані, без гармонії у поглядах різних фахівців неможливо. Важливо, щоб така гармонія досягалась не на вибуху емоцій, які супроводжують критичні стани, а заздалегідь – у ході планових дискусій, навчань і тренінгів.
Ну і звичайно – дружня вечеря, що проходила у ресторані неподалік від моря. Зібрались майже всі учасники конгресу. У неформальній обстановці можна було обговорити всі насущні питання, поділитись досвідом, перейняти щось нове. Вечеря проходила під гарну музику, зі смачними стравами та різноманітними напоями. З часом вечеря перейшла у веселу вечірку з танцями, але це вже зовсім інша історія. Було дуже весело, у справжньому одеському дусі.
Детальніше
Власними руками
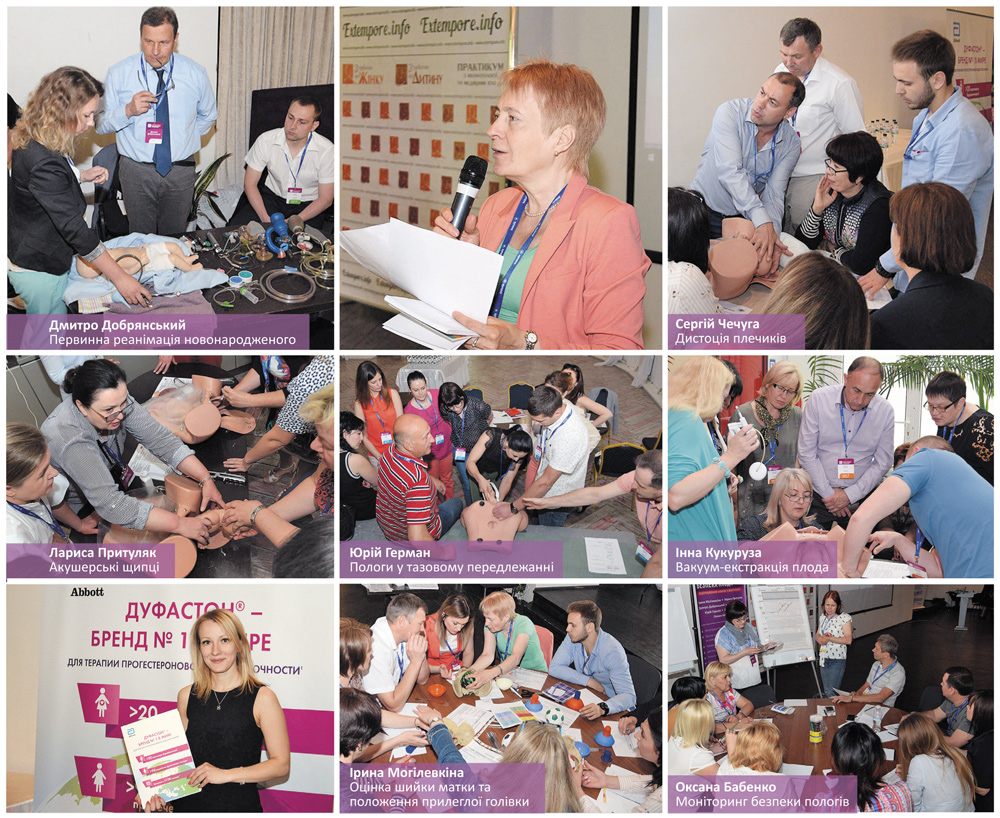
Міні-MBA з акушерства. Модуль 5. Вагінальні пологи: безпека плода.
Відпрацювання практичних навичок у мінігрупах
2 червня в Києві з великим успіхом відбувся інтенсивний, суто практичний майстер-клас з акушерства «Вагінальні пологи: безпека плода».
Чому його варто було відвідати?
Тому, що краще один раз зробити, ніж сто раз почути. Тому, що обрані теми: оцінка шийки матки та положення передлеглої голівки, дистоція плечиків, вакуум-екстракція плода, монiторинг безпеки пологiв, акушерські щипці, пологи у тазовому передлежанні, надзвичайно актуальні та стосуються ситуацій, котрі без належної допомоги несуть загрозу здоров'ю малюка. І головне, що майстер-класс проводила команда досвідчених тренерів за сучасною методикою. Ірина Могілевкіна, Оксана Бабенко, Сергій Чечуга, Дмитро Добрянський, Юрій Герман, Інна Кукуруза, Лариса Притуляк – це справжні фахівці, під контролем якіх учасники могли оновити чи отримати відповідні навички.
Скачати усі фотографії: goo.gl/photos/QQJvN23QGrQeUtSJ6
Детальніше

Рак молочної залози: про що варто пам’ятати акушеру-гінекологу?
Рівень захворюваності та смертність від раку в Україні постійно підвищується у зв'язку з несприятливою екологічною ситуацією та збільшенням кількості людей старше 60 років, у яких ризик появи раку значно підвищений [1]. Серед онкопатології на сьогодні у жінок найчастіше діагностують рак молочної залози (РМЗ), товстого кишечника, шлунку, легень та шийки матки [2].
РМЗ – найбільш поширений тип раку і найчастіша причина смертності від раку серед жінок у всьому світі [3, 4]. Рівень захворюваності на РМЗ в Україні у 2014 р. становив 60,6 випадків на 100 тис. жіночого населення. За даними Національного канцер-реєстру України, щорічний приріст цієї онкопатології перевищує 2%. Так, у 2014 р. в Україні зареєстровано 13 744 нових випадків захворювання, а загальна кількість померлих жінок від РМЗ склала 5926 осіб [3].
Незважаючи на успіхи в лікуванні, у 20–30% випадків у пацієнтів з ранніми стадіями РМЗ буде розвиватися рецидив з віддаленим метастазуванням [5]. У менш розвинених країнах спостерігають гірші результати лікування раку і підвищення смертності внаслідок діагностики на більш розповсюдженій стадії.
Поряд зі зростанням захворюваності на РМЗ останніми десятиліттями все частіше це захворювання діагностується у жінок молодого віку. Встановлено, що 37% хворих на РМЗ – особи репродуктивного віку [6, 7].
Ризик появи РМЗ визначається морфологічними особливостями гіперплазій молочної залози і значною мірою генетично детермінований [8]. На думку більшості науковців, РМЗ – це ендокринна патологія, яка пов’язана з репродуктивним анамнезом жінки.
До групи високого ризику РМЗ відносять осіб з поєднанням певних генетичних, фенотипічних факторів та особливостей стилю життя [9]. Основними факторами, що підвищують ризик захворювання на РМЗ, є: вік старше 40 років; спадкова і сімейна схильність; пізня менопауза; ранній початок менструацій (до 12 років); народження першої дитини у віці старше 30 років; переривання вагітності; відсутність пологів в анамнезі; наявність фіброзно-кістозної мастопатії та інших проліферативних захворювань молочних залоз; ожиріння; цукровий діабет; гіпертонічна хвороба; систематичне паління та вживання алкоголю. Несприятливими факторами є малорухливий спосіб життя, тривала інсоляція, дія на організм різних канцерогенів та стресу.
Основними факторами ризику РМЗ є обтяжений сімейний анамнез і вік. Спостерігають два піки захворюваності на РМЗ – у 45–47 та 70–75 років. В основі синдрому спадкового РМЗ лежить мутація генів BRCA1 і BRCA2 [10]. У нормі протеїни, які кодуються цими генами, захищають клітину від малігнізації, оскільки беруть участь у репарації дволанцюгової структури ДНК. Мутація будь-якого з цих генів призводить до безупинного росту клітин та зумовлює переродження у рак. Приблизно 7 % випадків РМЗ пов’язані з вродженою мутацією BRCA1 або BRCA2. У носіїв пошкоджених генів з’являється схильність до розвитку злоякісного захворювання.
Морфофункціональна мінливість тканин молочних залоз протягом репродуктивного періоду життя визначає схильність залози до виникнення різних патологічних процесів, клінічними проявами яких є больовий синдром та ущільнення тканин [8]. Частота виявлення доброякісних дисплазій молочних залоз у жінок репродуктивного віку складає понад 40% [6, 11]. При цьому основною причиною їх виникнення вважається порушення балансу між рівнями естрогенів і прогестерону з формуванням відносної гіперестрогенії.
Враховуючи патогенетичні механізми розвитку доброякісних гіперплазій молочних залоз та високу частоту дисгормональних порушень при цьому, корекція клінічних проявів мастодинії та масталгії є першочерговим завданням гінеколога [11, 12].
У веденні пацієнток з доброякісними гіперплазіями молочних залоз важливою є узгоджена взаємодія різних спеціалістів. Саме гінеколог разом з онкологом визначають патогенез захворювання уданої пацієнтки і розробляють тактику спостереження та лікування. Згідно сучасних принципів ведення пацієнток з доброякісними гіперплазіями молочних залоз, недостатнім є тільки спостереження з періодичним проведенням УЗД та мамографії. Обов’язковим є призначення курсів комплексної патогенетичної терапії для стабілізації гормонального та імунного гомеостазу, нормалізації функції шлунково-кишкового тракту, стану центральної і вегетативної нервової системи [6, 10, 13].
Профілактичними заходами щодо появи доброякісних гіперплазій молочних залоз є достатній рівень фізичної активності, переважання у раціоні продуктів з вмістом поліненасичених жирних кислот, морепродуктів, відмова від алкоголю і паління. Рекомендовано обмеження кофеїну, шоколаду, вживання вітамінів А і Е [6, 8, 9].
Діагностика РМЗ складається з двох етапів: первинна і уточнена [14]. До первинної відноситься самоогляд пацієнток і огляд лікарями інших спеціальностей. Першим етапом є детальний збір анамнезу життя і захворювання, огляд і пальпація молочних залоз. При зборі анамнезу необхідно звернути увагу на: перенесені і супутні захворювання печінки, щитоподібної залози, статевих та інших органів і систем, які можуть викликати ряд гормональних порушень в організмі і обумовити виникнення пухлинного процесу в молочних залозах; гінекологічний і репродуктивний анамнез; сексуальну функцію; соціально-побутову характеристику і професійні фактори; спадковість [4, 6, 8, 9].
Для ранньої діагностики захворювань молочних залоз важливими є самообстеження, клінічне обстеження, УЗД і/або мамографія. Проводити самообстеження слід щомісяця на 7–9-й день менструального циклу.
Важливо навчити пацієнток правильній методиці самообстеження. Огляд молочних залоз проводять під час прийому лікаря 1 раз на рік. Саме спеціаліст (гінеколог, мамолог, онколог), зазвичай, виявляє утворення в молочній залозі розміром від 1–2 см.

Доступність молочних залоз для обстеження та проста методика огляду іноді призводить до неправильної інтерпретації результатів клінічного дослідження, особливо, коли здійснюється недостатньо підготовленими спеціалістами. Все це зумовлює як гіпо-, так і гіпердіагностику. Тому мануальне обстеження слід доповнювати інструментальними дослідженнями [15].
Одними з провідних методів діагностики різних форм РМЗ є променевий метод. Мамографія своєчасно розпізнає патологічні зміни в молочних залозах у 95–97% випадків.
Ефективність УЗД у діагностиці пухлин діаметром <1 см складає біля 58%. Недоліками методує низька інформативність під час оцінки дифузних змін [16, 17].
Мамографія – це рентгенографія молочної залози без застосування контрастних речовин. Згідно рекомендацій Американського онкологічного товариства (2015), жінки з середнім ризиком появи РМЗ повинні проходити щорічно мамографію, починаючи з 45 років. Жінки віком 55 років і старше проходять скринінг 1 раз на 2 роки, або, за можливості, продовжують щорічні обстеження [18].
Рентгенівська картина молочних залоз у кожної жінки індивідуальна. Під час опису мамограмм розрізняють первинні і вторинні ознаки злоякісності.
Первинною та основною рентгенологічною ознакою РМЗ є наявність пухлинної тіні та мікрокальцинатів. Вторинними рентгенологічними ознаками онкопатології є симптоми, пов’язані зі станом шкіри, соска, оточуючих тканин, тощо [16, 17, 19].
Незважаючи на ефективність рентгенологічного методу, у деяких пацієнток діагностичні можливості мамографії різко знижуються – у випадку виражених дифузних форм мастопатії, у молодих пацієнток з щільними молочними залозами, за наявності імплантів, при виражених запальних змінах, набряку залози і фонових захворюваннях типу фіброаденоматозу. У таких випадках доцільним є застосування УЗД молочних залоз [14, 15].
Ультразвукове сканування виконується лінійним датчиком з частотою 7,5–10 МГц.
Перевагами ультразвукових досліджень молочних залоз є: безпека відносно дозового навантаження, що дає змогу обстежувати вагітних та годуючих жінок; висока роздільна здатність, що важливо під час обстеження щільних молочних залоз у молодих жінок; диференційна діагностика солідного і кістозного утворення; оцінка стану імплантів молочних залоз; обстеження молочних залоз в гострий період травмиабо запалення; візуалізація регіонарних лімфатичних вузлів; проведення прицільних пункційних біопсій під візуальним контролем утворень у молочній залозі; динамічне дослідження протягом лікування [17, 20].
Ехографічними критеріями РМЗ є неправильна форма, нечіткі контури, гіпоехогенна неоднорідна структура утворення, гіперехогенні включення різного розміру, акустичні тіні. Соноеластографія дозволяє проводити якісну оцінку жорсткості у вигляді колірного картування і кількісну оцінку деформацій тканин, що залежить від стану тканин. Для уточнення діагнозу використовують допплерівське сканування, мамосцинтиграфію, комп’ютерну томографію (КТ), магнітно-резонансну томографію (МРТ), позитронно-емісійну томографію [4, 6, 14].
З метою стандартизації результатів обстеження молочних залоз променевими методами візуалізації (мамографія, УЗД, КТ, МРТ) застосовується шкала BI-RADS (Breast Imaging Reporting and Data System) [20]. Використання цієї шкали покращило інтерпретацію виявленої патології за ступенем ризику наявності злоякісного утворення і стандартизувало лікувально-діагностичні алгоритми.
Основною метою дослідження є не так визначення морфологічного діагнозу (фіброаденома, кіста, рак тощо), як розробка тактики ведення, або менеджменту окремої пацієнтки. Тактика може бути різною – щорічне динамічне спостереження чи проведення біопсії для морфологічної верифікації патологічного процесу, що має більш важливе значення як для лікаря, так і для пацієнтки.
Для верифікації діагнозу застосовують пункційну біопсію новоутворення, найчастіше під контролем УЗД, з наступним цитологічним дослідженням пунктату [4, 9, 19].
Сучасним методом в онкології є імуногістохімічна діагностика, яка дозволяє прогнозувати перебіг захворювання, обґрунтувати доцільність застосування гормонотерапії, хіміотерапії і додаткового протипухлинного лікування [14]. При РМЗ практичне значення має визначення естрогенових рецепторів (ER), прогестеронових рецепторів (PgR), HER-2/new (c-erbB-2) (аналог рецепторів до факторів росту, продукт онкогену), мутації генів-супресорів p53, BRCA-1, BRCA-2 (Brest Cancer genes).
Однією з причин незадовільних результатів лікування раку в Україні є відсутність практичних втілень рекомендацій і засобів профілактики, а також низька ефективність програм раннього виявлення раку (рання діагностика у симптомних і скринінг у безсимптомних пацієнтів). У результаті кількість хворих з ранніми клінічними стадіями раку, які підлягають радикальному лікуванню, в Україні не перевищує 60%, а майже всі людські і фінансові ресурси системи охорони здоров’я спрямовуються на лікування хворих з пізніми стадіями захворювань без надії на повне вилікування [1, 2, 7].
Якщо рак виявлено на ранній стадії, то у 90% випадків він піддається успішному лікуванню. Саме тому потрібна якісна та професійна робота з населенням як лікарів загальної практики, так і вузьких спеціалістів-онкологів, а також пацієнтських організацій. Широке впровадження профілактики дозволяє в багатьох випадках уникнути недуги та знизити захворюваність і смертність від раку [2, 4, 18, 21, 22]. Особливістю РМЗ є досить ранній початок метастазування. Проведення мамографічного скринінгу в розвинених країнах давно стало нормою. Загальними правилами є проходження мамографії в жінок, старших 45–50 років, кожні 2–3 роки, у проміжках – регулярне самообстеження та клінічне обстеження молочних залоз лікарями.
Важливою проблемою ранньої діагностики патології молочних залоз є відношення самих жінок до проходження мамографічного скринінгу. Тому актуальним є інформування жіночого населення про значення профілактики та методи діагностики захворювання. Жінки іноді бояться можливості виявлення злоякісної пухлини, байдуже відносяться до свого здоров'я чи невпевнені у необхідності проведення обстеження. У даній ситуації залучення жінок до обстеження здійснюється лікарями первинної ланки та акушераими-гінекологами, які найбільше контактують з даним контингентом пацієнток у щоденній клінічній практиці.
Вибір методу лікування РМЗ визначається стадією захворювання, клінічною формою пухлини, віком та загальним станом, а також додатковими даними, що характеризують окремі властивості пухлини та організму жінки [5, 6, 9]. Перед призначенням лікування обов’язкова морфологічна верифікація діагнозу і максимально точне визначення стадії захворювання.
Лікування пацієнток, хворих на РМЗ, здійснюється у спеціалізованих онкологічних установах. Тактика та стратегія лікування визначається після огляду спеціалістів – хірурга-онколога, лікаря з променевої терапії в онкологічному закладі. У лікуванні РМЗ, залежно від стадії захворювання, наявності супутньої патології, віку та тяжкості стану пацієнтки застосовують усі відомі в онкології методи: хірургічний, променевий, системний та різні їх комбінації у поєднанні з гормональною, хіміотерапією та іншими лікувальними засобами [23, 24].
У більшості випадків РМЗ залишається гормонозалежною та гормоночутливою пухлиною [24, 25]. Ендокринна терапія пухлин – пріоритетний та перспективний напрямок лікування та профілактики в онкології, в основі якого лежить таргетно-молекулярний вплив на ракові клітини. Саме у випадках гормонозалежних пухлин гормонотерапія є частиною ад’ювантного лікування. Ендокринну терапію також можна проводити як паліативну при метастатичних формах РМЗ, а також у неоад’ювантному режимі для зменшення розмірів первинної пухлини.
Вибір гормонотерапії залежить від рецепторного статусу пухлини, віку жінки та її менструальної функції, а також від групи ризику рецидиву хвороби. Гормональна терапія РМЗ може включати пригнічення функції яєчників, застосування селективних модуляторів естрогенових рецепторів (selective estrogen receptor modulators — SERMs), селективних інгібіторів естрогенових рецепторів (selective estrogen receptor down-regulators — SERDs) та інгібіторів ароматази або комбінації цих лікарських засобів. При цьому SERMs блокують естрогенові рецептори, а інгібітори ароматази — біосинтез естрогенів [24].
Модулятори естрогенових рецепторів (ЕР) тривалий час широко застосовують у лікуванні хворих на РМЗ. Найчастіше призначають тамоксифен (ТАМ) як препарат вибору при естрогенпозитивному статусі пухлини (ЕР+). До антиестрогенів нових генерацій належать препарати ралоксифен, тореміфен та фулвестрант. Побічною дією ТАМ є його проестрогенний вплив на інші тканини, що зумовлює низку небажаних наслідків – гіперплазію ендометрію та розвиток карциноми, тромбоемболічні ускладнення та гепатотоксичні ефекти.
Найменш токсичними препаратами вважаються ралоксифен та тораміфен. Істинним антиестрогеном на сьогодні є лише фулвестрант, який здатний руйнувати ЕР-пухлини, знижувати їх експресію та позбавлений естрогенної активності.
Застосування інгібіторів ароматази (ІА) призводить до блокування активності ферменту ароматази, що відповідає за синтез естрогенів з андрогенів у жінок у постменопаузальний період. Першим препаратом цієї групи був аміноглютетимід, але через виражену токсичність (блокада синтезу не лише естрогенів, але й кортикостероїдів) він не знайшов широкого використання у клінічній практиці. Згодом з’явилися нові сучасні препарати третього покоління – летрозол, анастрозол, екземестан.
Основною причиною неефективності гормонотерапії при РМЗ вважають гормональну резистентність – стійкість пухлини до впливу гормональних цитостатичних препаратів [25].
Незважаючи на широкий спектр методів лікування хворих на РМЗ, вирішальним залишається хірургічне втручання [14, 23]. При початкових стадіях процесу хірургічний метод залишається основним і найбільш ефективним. При застосуванні комплексної терапії операція також залишається найважливішою ланкою лікування. У залежності від порядку використання відносно операції, консервативні методи застосовують або в ад’ювантному режимі (направленому проти невеликої кількості клітин мікрометастазів), або в неоад’ювантному, що проводиться до початку лікування з метою девіталізації та запобігання розповсюдженню пухлинних клітин. В Україні питання неоад’ювантних методів лікування є особливо актуальним, тому що серед вперше виявлених випадків захворювання місцево-поширені форми РМЗ діагностуються більш ніж у 50% хворих.
Розвиток онкології протягом останніх 30 років призвів до появи нових технологій у діагностиці, медикаментозній та радіотерапії, що значно покращило результати лікування хворих на РМЗ. Постало питання про формування спеціалізованих відділень – мамологічних центрів, де у повному обсязі були б забезпечені всі етапи діагностики, лікування та реабілітації пацієнток з РМЗ. Завдання таких центрів – надати максимально якісний і повний спектр допомоги, реабілітації та супроводу пацієнтки на будь-якому з етапів лікування, включно із симптоматичною терапією при термінальних формах хвороби [23].
Сучасним напрямком є естетичність хірургічних втручань у хворих на РМЗ, враховуючи психологічні та соціальні аспекти, пов’язані з РМЗ, зокрема, страх пацієнток втратити після лікування самовідчуття повноцінності, привабливості та соціальний статус [23, 26]. Онкопластична хірургія молочної залози – це стратегія, що використовує принципи пластичної хірургії для часткової чи повної реконструкції дефектів молочної залози чи грудної стінки, що утворюються при видаленні пухлини. Багаторічні спостереження показали онкологічну безпеку даного підходу зі значним збільшенням задоволення пацієнтів результатами хірургічного лікування. Поступово ця стратегія стає золотим стандартом у світі і все більше поширюється в Україні.
Застосування променевої терапії (ПТ) у лікуванні РМЗ дозволяє розширити показання для органозберігаючих операцій, які поступово витіснили розширені та надрадикальні [14]. Опромінення після органозберігаючих операцій знижує частоту реґіонарних рецидивів у молочній залозі та на грудній стінці. ПТ доцільно застосовувати після виконання органозберігаючих операцій у молодих хворих. Як самостійний спосіб лікування РМЗ, у теперішній час ПТ застосовується тільки при відмові хворої від операції, або наявності абсолютних протипоказань до неї. У якості альтернативних методів передопераційного протипухлинного впливу поступово стали ширше використовувати хіміотерапію та гормонотерапію.
На сьогодні нараховується більше 30 різних схем хіміотерапії (ХТ), які ґрунтуються на органотропності препаратів та на індивідуальній чутливості пухлин до лікування [14, 27]. Особливого поширення при лікуванні РМЗ набула неоад'ювантна поліхіміотерапія. Перевагами методу є зменшення біологічної активності пухлинних клітин як в пухлинному осередку, так і у віддалених мікрометастазах, створення сприятливих умов для проведення операції, зниження вірогідності генералізації РМЗ, можливість визначення чутливості пухлини.
Теорія «мінімальної післяопераційної залишкової хвороби» говорить про збереження в організмі хворих злоякісних клітин (після видалення основної пухлини), які не визначаються клінічними та інструментальними методами і можуть бути причиною подальшого утворення метастазів [27].
Застосування протипухлинного післяопераційного лікування приводить до відтермінування (іноді багаторічного) прогресування захворювання.
Висновки
Таким чином, РМЗ є актуальною медичною та соціально-економічною проблемою сучасного суспільства. Діагностика та лікування РМЗ потребує комплексного мультидисциплінарного підходу. Практичному лікарю слід знати, що постійне динамічне спостереження і патогенетична терапія мастопатії (корекція гормонального статусу і супутньої патології) є важливою ланкою профілактики РМЗ.
Сучасні алгоритми хірургічного лікування дозволяють оптимально визначити об’єм операції у хворих РМЗз урахуванням індивідуальних анатомічних особливостей і стадії процесу. Лікування повинно бути спрямоване не тільки на продовження життя, але й на забезпечення відповідної якості життя пацієнток з РМЗ.
Повний перелік літератури знаходиться у редакції.
ДетальнішеКістозно змінена плацента
ЕХОГРАФІЧНА ДІАГНОСТИКА ПЛАЦЕНТАРНОЇ МЕЗЕНХІМАЛЬНОЇ ДИСПЛАЗІЇ
Плацентарна мезенхімальна дисплазія (ПМД) належить до рідкісних плацентарних судинних аномалій, ехографічно характеризується плацентомегалією та численними гроноподібними кістозними порожнинами, що нагадують міхурцевий занесок. Представляємо випадок ПМД, діагностований у ІІ триместрі вагітності зі сприятливим перинатальним результатом
Тридцятитрирічна вагітна була скерована на консультативне ультразвукове дослідження (УЗД) у 19 тижнів вагітності внаслідок підозри на велику хоріангіому плаценти. Теперішня вагітність друга, перша закінчилася народженням здорової дитини. Клінічний перебіг цієї вагітності без особливостей. При УЗД розміри і анатомія плода відповідали очікуваному терміну вагітності.
Детальніше
Європа – варта вас!
До вашої уваги – інтервью з провідним чеським фахівцем з медицини плода, професором Павлом Цалдою. Ми зустрілися під час його візиту до Києва, куди він прилетів для участі в Східноєвропейських зустрічах професіоналів, присвячених материнсько-плодовій медицині. Професор пробув в Києві два дні, відвідав Лавру, високо оцінив організацію конференції, побажав нам успіхів і пообіцяв повернутися. Сказав, що в Україні можна було би проводити форуми ще більшого масштабу – якби не війна.
В одному зі своїх інтерв'ю Павел Цалда досить точно сказав про професію, якій присвятив життя: «Акушерство – надзвичайно етично забарвлена дисципліна, магія якої має особливий заряд і романтику, це пристрасть, від якої важко відмовитись»

Prof. Pavel Calda, MD, PhD
Професор Карлового Університету,
Прага, Чеська Республіка
- Керівник підрозділу ультразвукової діагностики та Центру Фетальної медицини у Празі
- Консультант з ультразвукової пренатальної діагностики та фетальної медицини.
- Дійсний член багатьох міжнародних профільних асоціацій.
- Володар премій у сфері акушерства та гінекології, іммунології.
- Автор трьох монографій та п'яти розділів у книгах
з акушерства та гінекології, автор 57 наукових статей.
ЗТЖ: Як Ви прийшли до медицини?
Павел Цалда: Я народився у родині лікарів, але коли мені було 16 чи 17 років, я захоплювався фотографією, і це в мене виходило непогано. Тож у медицину я йти зовсім не збирався. Втім, у якійсь момент я відчув, що навчання в Університеті принесе в мою творчість щось нове, отже, це було радше прагнення кінематографічності. Чому медицина? А чому б і ні? Принаймні такою була моя відповідь. І я, до речі, був непоганим студентом, але насправді мені хотілося більшого, ніж просто ходити на пари, а саме наповну користуватись можливостями, які мені надавало студентство.
Тому зараз, коли наставництво вже багато років – мій обов'язок, я завжди згадую себе в ті роки і розумію, що в голові у майбутніх лікарів не завжди все складено по поличках. Тож намагаюся не вбити творчий початок і м’яко скерувати його шляхом медичного пізнання, уміння надихатися і надихати їм дуже знадобиться. Ми постійно обговорюємо зі студентами їхні життєві успіхи, а не тільки виконання програми навчання, лікар має залишатися в першу чергу людиною, щасливою людиною. Лікарська освіта часто вбиває в нас тих, хто вперше став на поріг факультету.
ЗТЖ: Що найбільше вразило Вас на етапі навчання?
Павел Цалда: О, це був великий час. Усе в нашій сфері тільки починалося. Тільки подумайте, я бачив перші ультразвукові прилади, що працюють в режимі реального часу і доклав руки до їхнього тестування. Тоді це здавалося дивом. А у 1979 році я вперше потрапив до Америки. Уявіть простого хлопця з соціалістичного табору, який потрапляє на іншу планету. Це був шок, але й величезне відкриття – світ може бути глобальним, а надбання спільними. Сьогодні це вже нікого не дивує.
ЗТЖ: Вам було не складно працювати на першій посаді?
Павел Цалда: Першу посаду я отримав після року служби в армії, куди потрапив після університету, тож налякати мене вже ніщо не могло. Я не мав достатньо досвіду в акушерстві і гінекології, але під час навчання вивчав лапароскопію в США і вмів виконувати базові інвазивні процедури: амніоцентез та кордоцентез. У ті часи фетальна медицина та ендоскопія були новинками, отже мені вдалося швидко завоювати авторитет.
ЗТЖ: Якими були ваші перші кроки у медицині плода?
Павел Цалда: Кінець 70-х був дуже хвилюючим часом встановлення міжнародних зв'язків, люди з Чехії почали подорожувати світом. А далі – варто було лише вийти з дому. Кожна подорож приносила нові знайомства. Так у Детройті ми потоваришували з Ромеро, у Лондоні – з Ніколаїдесом.
Після 1989 р. з'явилось багато нових можливостей для змін і розвитку. Я став асоційованим професором і це додало мені можливостей.
Так склалося, що часто змінював місця роботи – шпиталі, клініки, колективи. Спочатку було важко, але згодом розумієш – всі зміни відбуваються на краще, тому що дають змогу змінюватися самому. На краще чи на гірше – залежить тільки від тебе. Так врешті я став президентом Чеського товариства ультразвуку в акушерстві та гінекології. Видав книгу з ультразвукових досліджень в акушерстві та гінекології, яка вже пережила 2 видання, з тисячами зображень на 500 сторінках. Це був вагомий внесок у розвиток чеської медицини. Тому зараз можу дозволити собі розслабитися (сміється).
ЗТЖ: Добре, давайте поговоримо про медицину в Чехії. У Чеській республіці багато жінок народжує після 35 років?
Павел Цалда: Дуже багато. Так само, як і в сусідній Німеччині, всі користуються контрацептивними засобами, як скажені, аж до сивини. Це фактично стає стилем життя. Я не дуже добре ставлюся до цього.
ЗТЖ: А яка ситуація щодо переривань вагітності у Чехії?
Павел Цалда: Ми маємо закон про аборти. Переривання дозволене до 6 тижнів, на більшому терміні страхові компанії оплачують аборти за умови, що вони виконуються за медичними показаннями. У нас дуже добре працює програма планування сім'ї, тому рівень абортів у Чехії є дуже низьким. Він не залежить від віку, це можуть бути і юні дівчата, і жінки старшого віку. У цілому, штучним перериванням вагітності в Чехії не зловживають.
ЗТЖ: Як щодо переривання вагітності після 22 тижнів за медичними показаннями?
Павел Цалда: Ми можемо перервати вагітність у будь-який термін.
ЗТЖ: За згодою спеціальної комісії?
Павел Цалда: Так. Ми можемо переривати вагітність навіть після 30 тижнів у випадку тяжких вад розвитку плода, і не вказано, що мається на увазі, просто «тяжкі вади розвитку».
ЗТЖ: Гаразд, spina bifida – тяжка вада чи ні?
Павел Цалда: Залежить від конкретного випадку. Ми намагаємося створити прогноз для рухової активності кінцівок, роботи тазових органів, визначаємо каріотип дитини, прислухаємося до думки батьків.
ЗТЖ: Чи часто жінки в Чехії переривають вагітність при анеуплоїдії?
Павел Цалда: Так, більшість.
ЗТЖ: Для переривання вагітності потрібна згода комітету з етики університету або шпиталю?
Павел Цалда: Так, кожний шпиталь має свій комітет.
ЗТЖ: Хто входить до цього комітету?
Павел Цалда: Акушери, неонатолог, старша акушерка, секретар або іноді юрист. Для переривання вагітності потрібен операційний блок, за його відсутності операції не виконують.
ЗТЖ: Якщо пацієнтці в пізньому терміні відмовлено, вона може звернутися до іншого закладу, іншого комітету?
Павел Цалда: Вона має право звернутись до суду і почати юридичний процес, проте таких випадків практично не буває. Справа в тому, що ми нічого не тримаємо в секреті, ми максимально відкриті, як реаліті-шоу на вечірньому телебаченні, тому вся інформація подається пацієнтам і колегам без жодного викривлення. От і немає чого судитися, про що сперечатися.
ЗТЖ: Чи виконуєте ви фетальні втручання і які саме?
Павел Цалда: Так, ми застосовуємо фетоскопію для лазерної коагуляції анастомозів при ФФТС, проте таких випадків не дуже багато.
ЗТЖ: Як щодо внутрішньоутробних переливань?
Павел Цалда: Обов’язково. Я виконав перше внутрішньоутробне переливання в Чеській республіці у 1991 р., проте, знов таки, ми робимо їх не так часто, оскільки давно застосовуємо анти-D профілактику.
ЗТЖ: Чи виконуєте ви трахеальні оклюзії при діафрагмальній грижі?
Павел Цалда: Це можливо технічно, проте ми цього не робимо, не маємо достатньо досвіду. У Чехії історично склалося так, що лікування діафрагмальної грижі досить успішно виконується після пологів із застосуванням ЕКМО.
ЗТЖ: Як щодо плодових операцій при spina bifida?
Павел Цалда: Ми оперуємо їх уже після народження, зазвичай радимо жінкам продовжувати вагітність, визнаючи всі ризики.
ЗТЖ: Чи будуть ваші діти займатися медициною?
Павел Цалда: У 18–19 років дуже сподівався помітити їхнє зацікавлення, але його не виникло. Медицина – це вибір на все життя, тому ні до чого їх не примушував, вони самостійно обрали свої професії. І, незважаючи на те, що мої батьки і батьки моїх батьків були лікарями – я останній лікар в сім'ї.
ЗТЖ: Ви сказали, що у Чехії середній вік матерів зростає?
Павел Цалда: На жаль, так. Вік народження першої дитини зростає, загалом більше 50% дітей жінки народжують після 25 років. І я не здивуюся, що скоро доведеться посунути межі репродуктивного віку до 50 років. Це призводить не тільки до зростання анеуплоїдій, але й складнощів з виношуванням дитини. Багато жінок наважуються завести дитину наприкінці репродуктивного віку, бо добре себе почувають, але, як відомо, у цьому віці кількість та якість яйцеклітин катастрофічно падає. Часто доводиться використовувати заморожені яйцеклітини.
ЗТЖ: Тобто відкривається шлях для застосування ДРТ?
Павел Цалда: Правильно. Я вважаю, що цими технологіями дещо зловживають. Потрібно пропагувати більшості жінок, щоб вони вагітніли у свої молоді літа (20–25 років). Зменшиться кількість проблемних вагітностей. Це буде дешевше, легше, без застосування ДРТ і матиме позитивний ефект для суспільства, омолоджуючи його, і вигідно для економіки країни також.
Отже, я за пропаганду вагітностей у ранньому репродуктивному віці, а молоді пропагують – заморозьте яйцеклітини та робіть кар’єру або розважайтесь. Це порочний шлях, як на мене. Ми і наші батьки прекрасно встигали усе вчасно.
ЗТЖ: В Чехії є й приватні, і державні центри ДРТ?
Павел Цалда: Ми маємо переважно приватні і два державні центри.
ЗТЖ: Скільки коштують послуги в середньому?
Павел Цалда: Вони змінюються в залежності від багатьох речей. Більшості жінок послуги ДРТ покриває система страхування. Проте є обмеження, народження першої дитини в 48 років страховка ніколи не покриє.
ЗТЖ: Як щодо наукової роботи? Чи фінансує держава дослідження, проекти?
Павел Цалда: Я кілька разів отримував гранти на дослідження від державних структур. Є багато агенцій, які фінансують наукові дослідження.
ЗТЖ: Чи існує можливість молодим фахівцям з України проходити стажування в Чехії? Наші лікарі часто стажуються в Німеччині, працюють там у різних клініках. Чи не планується започаткувати щось подібне в Чехії?
Павел Цалда: Так, у нас на навчанні теж були лікарі з Києва. Це було цікаво.
ЗТЖ: Лікарі з України можуть приїхати, наприклад, на двотижневе навчання?
Павел Цалда: Так, зазвичай це можливо, адміністрація лікарень це дозволяє.
ЗТЖ: Чеські лікарі публікують свої роботи у міжнародних наукових журналах?
Павел Цалда: Обов'язково, вони повинні це робити. Якщо ви працюєте в університеті, для вас дуже важливо мати публікації.
ЗТЖ: А якщо лікар працює не в університетській лікарні?
Павел Цалда: Якщо він працює у шпиталі загального профілю, публікуватись не обов'язково, проте це завжди бажано. Державна програма, за наявності науковців, може виділити фінансування для такого шпиталю. Кошти розподіляються на інвестиційні витрати, на подорожі, на реактиви.
ЗТЖ: Чи часто молоді чеські лікарі переїздять до Німеччини на роботу?
Павел Цалда: Загалом люди не дуже схильні покидати Чехію. Вони їдуть і потім повертаються назад. Переїзди до іншої країни не є масовими. Але ми підтримуємо людей, які виїжджають за кордон, щоб набратися досвіду.
ЗТЖ: Чи стикаєтесь ви з корупцією в Чеській республіці?
Павел Цалда: Корупція існує в усіх країнах. Відіграє роль рівень корупції. Головне, що може її стримати це наявність покарання. Коли корупція карається – вона не зникає, але виходить на такі рівні, де прості люди її не відчувають.
ЗТЖ: Отже, корупцію неможливо перемогти?
Павел Цалда: Важливо створити умови, щоб люди не могли вільно користуватися великими сумами готівки. Бо, якщо вони можуть піти в банк і зняти готівку – вони можуть заплатити всім, повз усі контролюючі органи. Потрібна прозорість у русі коштів і незалежність прийняття рішень від керівника чи адміністратора. Насправді, на базовому рівні все просто, слід тільки прийняти німецькі закони і ніколи не робити заборонених речей (сміється). І творити здорове середовище самостійно, не чекаючи на добрих царів. Саме середовище формує рішення, процеси, вирішує, що добре, що зле. Можливо, наразі Україна більше схильна до цих проблем, порівняно з моєю країною. Але тільки люди можуть визначити функціональну систему, яка встановлює, що є хорошим, а що – поганим.
ЗТЖ: Ви б хотіли ще повернутися в Україну?
Павел Цалда: Так, звичайно! Мені дуже подобається українська культура, мистецтво, кухня. Мрію, щоб побільше людей побачили Київ, це фантастичне місто. Мені було б цікавіше провести уїк-енд в Києві, ніж в Парижі. Слід розвивати туристичну сферу, але дуже важливо орієнтуватись на середній клас європейців, не робити все занадто дешевим, бо сюди їздитимуть непутящі люди і це ні до чого доброго не приведе.
ЗТЖ: Щоб ви хотіли сказати нашим читачам на останок?
Павел Цалда: Україна є неповторною країною, зі своєю історією і традиціями, зовсім відмінними від Росії. І тільки зараз більшість людей бачать цю відмінність, тому що починають спілкуватися з освіченими верствами. Європейці повинні змінитися, щоб перестати бачити в українцях лише працівників на будівництві. Але нам потрібна і ваша допомога: чим більше ваших інтелектуалів з’являтиметься на європейській сцені – тим швидше станете своїми, бо ви того варті. А Європа – варта вас.
Бесіду вів Віктор Ошовський
Детальніше