Стволовые клетки и экзосомы
Если на клетке слона прочтёшь надпись «буйвол», не верь глазам своим
Козьма Прутков
Для регенеративной медицины очень важен вопрос о том, как регулируется восстановление клеточной массы в случае естественной смерти клеток и замены их новыми клетками (физиологическая регенерация) или при гибели части клеток вследствие патологического процесса (репаративная регенерация).
Известно, что региональные стволовые клетки находятся в дормантном (спящем) состоянии и не делятся. Классическим примером пробуждения региональных стволовых клеток является регенерация печени после удаления ее части. Даже после экспериментальной резекции половины печени, оставшаяся ее часть может восстанавливаться до стандартных размеров. Недавнее исследование, опубликованное в журнале Liver Transplantation, показало, что печень достигает своего первоначального размера всего через три недели после трансплантации. Когда часть печени пересаживают от донора реципиенту, она в течение одного месяца достигает нормальных размеров, как у донора, так и у реципиента. В то же время, в случае инфаркта миокарда восстановления сердечной мышцы не происходит, а погибшие в результате ишемии кардиомиоциты замещаются соединительной тканью. Почему? Ответ на этот вопрос следуют искать в тех наночастицах, которые до недавнего времени считались… клеточными мусорщиками. Речь идет об экзосомах.
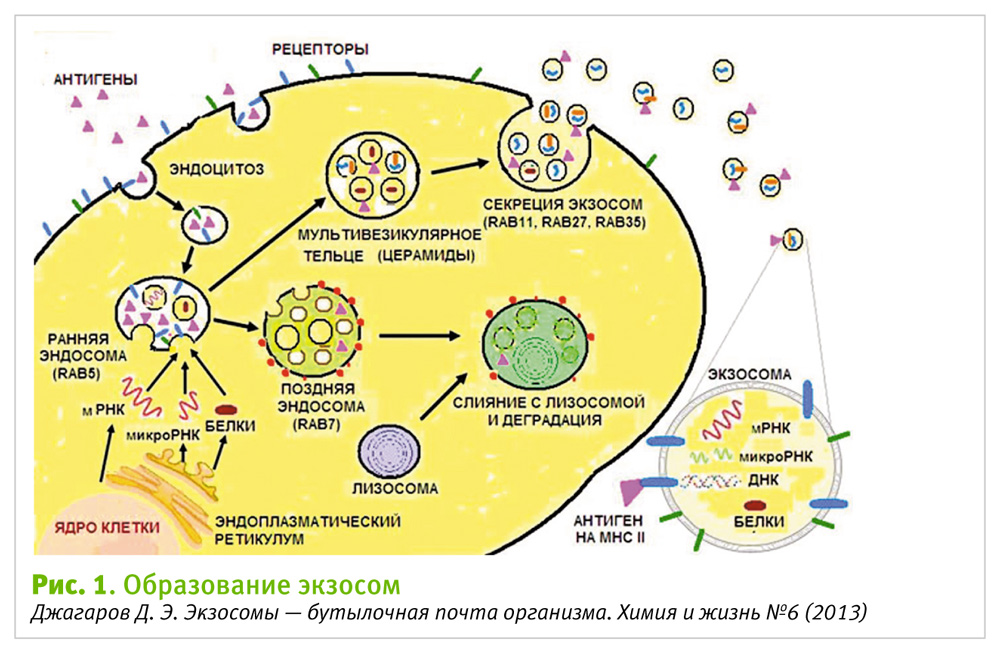
Впервые термин «экзосомы» был предложен в 1981 году для обозначения мембранных везикул (мельчайших пузырьков), которые продуцировали раковые клетки [Trams E. G., Lauter C. J., Salem N. Jr, Heine U. (1981) “Exfoliation of membrane ectoenzymes in the form of micro-vesicles ”Biochim Biophys Acta 645(1):63–70]. Основной функцией экзосом тогда считалось быстрое удаление из клеток некоторых белков, то есть, экзосомам отводилась роль клеточного мусорщика (см. эпиграф). Через 32 года (2013 г.) за открытие везикулярного транспорта была присуждена Нобелевская премия по физиологии и медицине. Такой вот «мусорщик» (рис. 1)…
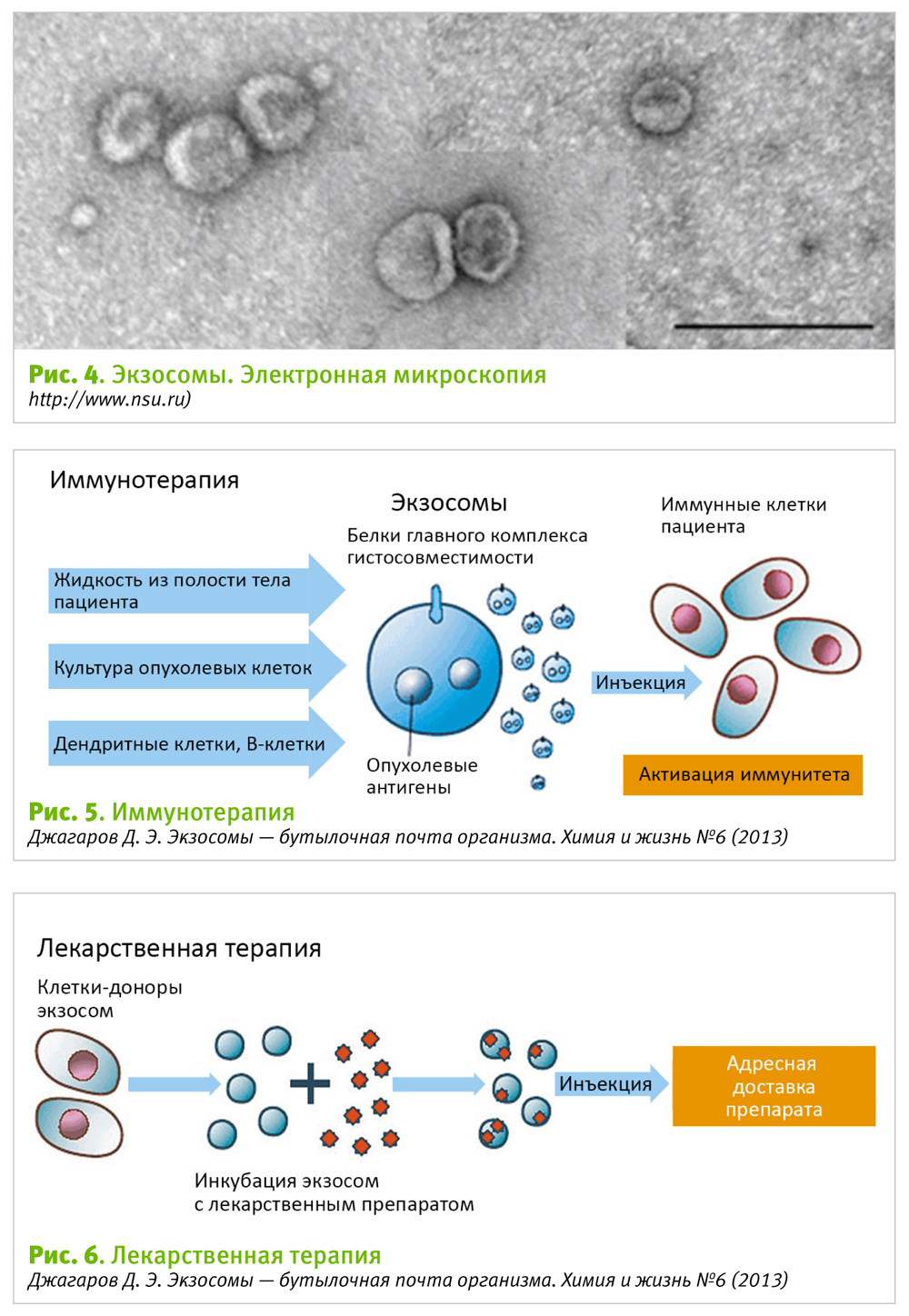
Что же такое экзосомы на самом деле? Экзосомы обладают уникальной структурой, во многом напоминающей миниатюрную копию клетки. Их плазматическая мембрана надежно изолирует содержимое экзосом от внешней среды и повреждения. Состав экзосом включает практически все классы биомолекул клеток: белки, ДНК, РНК, липиды, низкомолекулярные соединения. Кроме того, экзосомы содержат факторы роста и цитокины. Добавим сюда тот факт, что экзосомы могут свободно перемещаться между клетками, проникать в любые биологические жидкости (кровь, лимфа, спинномозговая жидкость, грудное молоко, слюна, сперма, моча) и достигать всех тканей организма. Добавим и поймем, что 30 лет мы смотрели, но не видели важнейший механизм клеточного общения в многоклеточном организме – горизонтальную передачу информации от клетки к клетке.
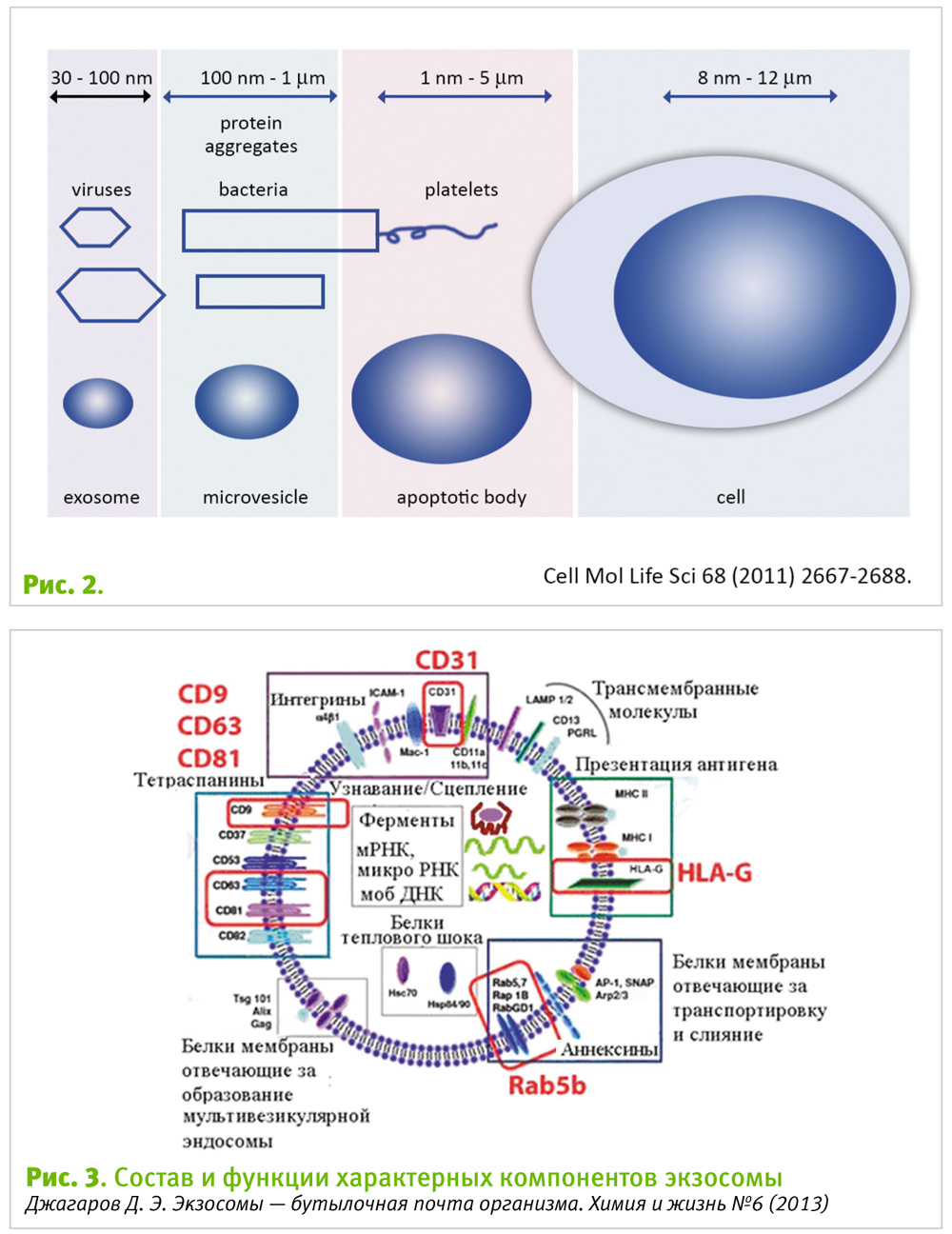
Сегодня принято различать микровезикулы и экзосомы. Микровезикулы представляют собой пузырьки от 100 до 1000 нм в диаметре, образующиеся путем выпячивания плазматической мембраны из клетки наружу с последующим отделением образовавшегося пузырька от мембраны клетки.
Экзосомы – это небольшие мембранные везикулы от 50 до 100 нм в диаметре, образующиеся из эндосомальных мультивезикулярных телец, и секретируемые путем экзоцитоза большинством клеток организма (рис. 2).
Исследования показали, что экзосомы транспортируют в клетки-реципиенты различные биомолекулы – белки, РНК, ДНК, вирусные частицы, вызывая целый каскад изменений на геномном (за счет ДНК) и эпигеномном (микроРНК) уровнях [Ogorevc E., Kralj-Iglic V., Veranic P. (2013) “The role of extracellular vesicles in phenotypic cancer transformation” Radiol Oncol (3):197–205].
Это открытие, которое многое изменит в медицине. Понимание того, что межклеточная коммуникация осуществляется по механизму везикулярного транспорта, в корне меняет наши представления о развитии болезней и их лечении…
Сегодня уже доказано, что состав экзосом не является случайным и не соответствует составу белков плазматических мембран клеток-продуцентов, а представляет собой «микрокарты», программирующие клетку-реципиента к определенным действиям. В частности, взаимодействие изолированных экзосом В-лифоцитов с фолликулярными дендритными клетками, CD8+ и CD4+ T-лимфоцитами приводит к усилению иммунного ответа.
Экзосомы, полученные из инфицированных клеток, содержат патогенные антигены, модулирующие иммунный ответ.
Экзосомы макрофагов, инфицированных вирусом иммунодефицита человека 1-го типа, специфически связываются с T-клетками, что обеспечивает распространение инфекции и супрессию иммунного ответа.
Экзосомы, секретируемые клетками эпителия кишечника, участвуют в регуляции противовоспалительных процессов.
Экзосомы эпителиальных клеток бронхов, содержащие повышенное количество цитокинов, в случае бронхиальной астмы обеспечивают распространение противовоспалительного эффекта по всем тканям дыхательной системы.
Нейроны, олигодендроциты и микроглия секретируют везикулы, которые мигрируют к определенным клеткам-мишеням. Показано участие экзосом в формировании миелина, играющего ключевую роль в функционировании и выживании нервных волокон. Ряд патогенных белков, вызывающих грубую и смертельную патологию центральной нервной системы, например, прионы, обнаруживаются в составе экзосом и могут переноситься от клетки к клетке, то есть, экзосомы способствуют распространению патологического процесса в головном мозге.
Опухолевые клетки продуцируют экзосомы в значительно большем количестве, чем нормальные клетки. «Раковые» экзосомы обнаружены во всех биологических жидкостях организма, включая сыворотку крови, мочу, сперму, асцитную и плевральную жидкости. Посредством переноса информационных молекул, экзосомы провоцируют формирование первичных опухолей и опухолевую прогрессию: изменяют микроокружение стромальных клеток; повышают инвазивную способность клеток; активируют ангиогенез; активируют онкогены; элиминируют проапоптотические факторы; транспортируют индукторы апоптоза в клетки противоопухолевого иммунитета, что вызывает их гибель.
Экзосомы раковой стволовой клетки подавляют противоопухолевый иммунитет: угнетают Т-лимфоциты и натуральные киллеры (NK-клетки); блокируют созревание антиген-презентирующих клеток; увеличивают количество и усиливают активность иммуносупрессорных клеток; способствуют активному переносу различного рода вирусов, включая вирусы, ассоциированные с канцерогенезом.
Кроме того, опухолевые клетки посредством секреции экзосом избавляются от химиопрепаратов (в частности, доксорубицина), и именно этот процесс лежит в основе приобретения раковыми клетками устойчивости к противоопухолевой терапии. Экзосомы раковой стволовой клетки воздействуют на опухолевые клетки с помощью эпигенетических механизмов регуляции транскрипции генов посредством переноса информационных и малых РНК, что лежит в основе феномена генетической нестабильности малигнизированных клеток.
На сегодняшний день установлены следующие функции экзосом:
- регуляция иммунного ответа;
- представление антигена;
- передача РНК и белков;
- передача инфекционных частиц (например, вирусов и прионов);
- передача сигналов от клеток к клеткам;
- участие в модулировании иммунного ответа;
- участие в онкогенезе, метастазировании опухолевых клеток;
- участие в механизмах развития нейродегенеративных заболеваний.
Впечатляет количество экзосом: в 1 мл плазме крови их насчитывается до 900 000 000000 – девятисот миллиардов!
Но не стоит думать, что экзосомы играют в организме человека исключительно негативную роль. Это нормальный физиологический механизм регуляции многоклеточного организма. Экзосомы, секретируемые эмбриональными стволовыми клетками в процессе внутриутробного развития, эпигенетически перепрограммируют различные клетки-мишени зародыша, а экзосомы, продуцируемые мезенхимальными стволовыми клетками (МСК), участвуют в устранении повреждений и регенерации тканей. Известно, что молодые МСК способны продлить жизнь старым животным. Японскими исследователями был идентифицирован фактор, стимулирующий регенерацию тканей. Этот фактор (Gdf6 – growth differentiation factor 6) секретируют молодые МСК. С возрастом продукция этого фактора снижается, что связано со ослаблением синтеза микроРНК-17. Гиперэкспрессия Gdf6 in vivo существенно уменьшала степень связанных со старением угнетения лимфопоэза, недостаточной репарации мышц и предотвращала снижение количества нервных клеток-предшественников в головном мозге.
Биологическая и терапевтическая активность МСК, а также способность к продукции экзосом мезенхимальными стволовыми клетками, обратно коррелируют с возрастом их донора. Предложена гипотеза о том, что, некоторые из переносимых экзосомами микроРНК могут способствовать старению, запуская сигнальные пути, ведущие к одряхлению организма, но другие, наоборот, защищают его от этих процессов. Экзосомы состарившихся клеток с помощью своей микроРНК так изменяют микроокружение, что оно начинает благоприятствовать возрастным заболеваниям, понижению иммунитета, воспалению и нарушению функций различных органов. Экзосомы из молодых клеток, наоборот, способствуют процессам регенерации различных органов и уже используются в регенеративной медицине.
Далеко не полный список возможного применения экзосом в медицине уже включает диагностику болезней, иммунотерапию, изготовление вакцин, модуляцию ангиогенеза, целевую доставку в ткани-мишени различных лекарственных препаратов (в том числе ферментов, препаратов на основе РНК: микроРНК, матричных РНК, малых интерферирующих РНК). Кроме того, экзосомы – безусловный кандидат на поставку в клетки организма «омолаживающих» микроРНК, способных инактивировать процессы старения. Не исключено, что удаляя из кровотока старого организма экзосомы и заменяя их на экзосомы молодого растущего организма, можно будет перепрограммировать клетки так, что они станут моложе…
В нашей лаборатории мы изучаем возможности терапевтического использования экзосомплазмы пуповинной крови, стволовых клеток плаценты, мезенхимальных стволовых клеток костного мозга, пуповины, Вартонова геля, а также фетальных стволовых клеток.
Вполне возможно, что для лечения многих болезней стволовые клетки уже и не понадобятся, достаточно будет использовать их экзосомы, которые отличаются стабильностью, а значит, могут быть доступны в любом медицинском учреждении. Или в аптеке…
Детальніше
Мониторинг сердечной деятельности плода
Современное состояние и перспективы
С момента появления электронного мониторинга частоты сердечных сокращений (ЧСС) плода прошло около полувека. Такой солидный временной интервал позволяет оценивать результаты повсеместного внедрения этой технологии в акушерство и строить определенные прогнозы на будущее. Наиболее распространенной методикой оценки ЧСС в антенатальном периоде и в процессе родов является кардиотокография (КТГ) (Nelson K. B. 2016; Pinas A., Chandraharan E. 2016; Redman C. 2015; Sholapurkar S. L. 2017). КТГ основана на регистрации ультразвуковой волны, отраженной от клапанного аппарата сердца. В этой технологии используется механический кардиоинтервал. Математический аппарат метода включает в себя аутокорреляцию, что подразумевает наличие временнного усреднения ЧСС. Поэтому КТГ не позволяет точно определить ЧСС плода в указанное время, но дает возможность изучать изменчивость или вариабельность сердечного ритма (ВСР) (Hoyer D. et al. 2017). То есть данный метод способен оценивать как кратковременные (осцилляции), так и длительные (акцелерации и децелерации) изменения сердечного ритма плода.
Поскольку ВСР связана с автономной (вегетативной) функцией, то количественная оценка общей мощности спектра ВСР, высокочастотной (вагальной) и низкочастотной (симпатической) составляющих позволяет оценивать влияние регуляторных механизмов на гемодинамику плода (Arias-Ortega R. et al. 2015; David M. et al. 2007). С другой стороны, развитие и созревание автономной нервной регуляции плода является известным критерием оценки его состояния. Безусловно, нарушения нейровегетативной регуляции являются маркером неблагополучия. Поэтому оценка ВСР является удобным подходом к изучению регуляторных механизмов, лежащих в основе поведенческих реакций плода. Это очень важно, так как в соответствии с концепцией «внутриутробного программирования» многие из заболеваний человека являются следствием нарушенной автономной нервной регуляции в антенатальном периоде. Поэтому мониторинг ВСР плода имеет отношение не только к диагностике острого или хронического страдания плода, но и к прогнозированию болезней сердечно-сосудистой системы, метаболических, когнитивных и поведенческих нарушений в будущем (Hoyer D. et al. 2014).
Автономная нервная регуляция распространяет свое влияние на функционирование всех органов и систем. Поэтому оценка параметров ВСР является «окном» в мир регуляторных механизмов плода. Установленная взаимосвязь между увеличением размеров желудочков сердца и возрастающим сердечным выбросом свидетельствует о том, что способность к регуляции гемодинамики появляется по мере развития автономной нервной регуляции в периоде созревания плода (De Vore G. R. 2005). Поэтому кардиоритм является одним из немногих доступных сигналов в пренатальном периоде, на основе которых возможно оценивать функциональное состояние и развитие плода.
В практической работе акушер-гинеколог сталкивается с проблемой диагностики состояния плода. Первыми, кто использовал для этого КТГ, были E. Hon и R. Caldeyro-Barcia. Уже в то время было известно, что брадикардия и (или) длительные децелерации являются признаками страдания плода. Они предложили выделять ранние (доброкачественные или физиологические), поздние и вариабельные децелерации по отношению к началу схватки.
Безусловно, диагностика терминального состояния не представляет сложностей. Проблемой до сих пор остается низкая специфичность в отношении прогнозирования угрожаемых состояний плода (Redman C. 2015).
Тем не менее, в середине 80-х годов прошлого века в Великобритании было показано, что использование КТГ в родах снижает частоту интранатальной гибели плода, а нестрессовый тест (НСТ) позволяет прогнозировать дистресс плода (Sholapurkar S. L. 2015). Еще ранее в США установили целесообразность применения стрессового (окситоцинового) теста (Ugwumadu A. 2014).
Однако, в дальнейшем доказательства диагностической точности КТГ в отношении дистресса плода стали вызывать значительные сомнения. Основным результатом электронного мониторинга плода стало многократное возрастание частоты абдоминального родоразрешения при отсутствии снижения уровня перинатальных повреждений нервной системы и детского церебрального паралича (Nelson K. B. et al. 2016). Высокая частота ложно-положительных результатов КТГ имеет достаточное теоретическое обоснование. В антенатальном периоде существует несколько стационарных состояний плода: спокойного и активного сна, бодрствования (двигательной активности). Основой НСТ является учащение частоты сердечных сокращений плода в ответ на его шевеления. Это опосредовано симпатическими влияниями. Во время сна закономерно регистрируется ареактивный НСТ, что необходимо принимать во внимание (Sholapurkar S. L. 2017). Поэтому биофизическая активность плода не позволяет обозначить «серую» зону между удовлетворительным состоянием и дистрессом плода. Основой диагностики дистресса плода в родах по данным КТГ является появление децелераций. Ранние децелерации, связанные с физиологической реакцией плода на схватку, не представляют опасности (Ayres-de-Campos D. et al. 2015). Децелерации также могут возникать ввиду сдавления предлежащей части, активации барорецепторов в ответ на компрессию пуповины или рефлекса Безольд–Яриша, связанного со сниженным венозным возвратом от плаценты (Sholapurkar S. L. 2013, 2015, 2017). Наиболее исследованным механизмом развития децелераций является периферический хеморефлекс, приводящий к развитию гипотензии у плода. При этом у здорового плода хорошие адаптационные способности препятствуют появлению гипотензии и ишемических повреждений в ответ на схватку (Ayres-de-Campos D. et al. 2015). В общем, децелерации могут быть поделены на две группы. К первой относятся доброкачественные (негипоксические) парасимпатические рефлекторные децелерации. А во второй группе – гипоксические (связанные с хеморефлексом) децелерации, сопровождающиеся кардиодепрессивным влиянием (Sholapurkar S. L. 2017). Поэтому далеко не все вариабельные децелерации свидетельствуют о дистрессе плода.
В 2008 годув National Institute of Child Health and Human Development были приняты рекомендации по стандартизации системы классификации параметров КТГ. Среди них: базальная частота и ее вариабельность, акцелерации, децелерации и изменения, связанные с сократительной деятельностью матки. Также впервые было указано, что умеренная ВСР плода или наличие акцелераций являются подтверждением отсутствия ацидемии у плода в момент исследования, а сниженная ВСР плода или отсутствие акцелераций не могут быть предикторами ацидемии (Ugwumadu A. 2014). National Institute for Health and Care Excellence в 2014 году рекомендовал разделять вариабельные децелерации на типичные и атипичные (Sholapurkar S. L. 2017).
Сложность интерпретации и сомнения в обоснованности визуальной оценки записи привела к появлению автоматизированного анализа параметров КТГ еще 36 лет назад (Fanelli A. et al. 2013). Использование критериев Dawes-Redman способствует некоторому снижению частоты ложноположительных результатов диагностики дистресса плода (Redman C. 2015). При этом STV (кратковременные вариации) признаны стандартным показателем оценки состояния плода у беременных группы высокого риска (мекониальные воды или преэклампсия).
Основной задачей применения КТГ в родах является снижение уровня перинатальной патологии. При этом прогностическая ценность положительного результата – не более 30% (Ayres-de-Campos D. et al. 2015). В настоящий момент существуют рекомендации ACOG об использовании КТГ в родах только у пациенток группы высокого риска. А вот у женщин с неосложненным течением беременности результаты разочаровывают. Было установлено, что чуствительность применения КТГ в родах для прогнозирования гибели плода была 57%, а специфичность – 69% (Nelson K. B. et al. 2016).
Обзор Кохрейна в 2013 году не подтвердил, что КТГ мониторинг в родах снижает частоту интранатальной гибели плода по сравнению с аускультацией сердца плода. В этом обзоре было показано увеличение частоты кесаревых сечений и оперативных пособий в родах через естественные родовые пути. При этом относительный риск ацидемии и детского церебрального паралича были одинаковыми. Поэтому, по-прежнему, низкая специфичность метода требует дополнения в виде рН-метрии крови из предлежащей части плода (Redman C. 2015). Развиваются и альтернативные методы мониторинга плода в родах: пульсоксиметрия и анализ ЭКГ, полученной с предлежащей части плода (Per Olofsson et al. 2014). Однако, ACOG и RCOG не рекомендовали использование пульсоксиметрии в родах (Ayres-de-Campos D. et al. 2015). Последние данные из Кохрейновского обзора не продемонстрировали преимуществ дополнительного анализа сегмента ST по сравнению с изолированным использованием КТГ в родах (Belfort M. A. et al. 2015 ; Pinas A. 2016).
Несмотря на указанные недостатки, КТГ остается наиболее широко используемым методом мониторинга плода. Акушеры-гинекологи во всем мире отводят ему роль юридической защиты в случае рождения ребенка в нарушенном состоянии (Ayres-de-Campos D. et al. 2015). Наличие записи с удовлетворительными параметрами может служить подтверждением отсутствия дистресса плода в момент регистрации.
Существуют определенные перспективы использования КТГ для прогнозирования развития синдрома задержки роста плода. При этом STV и LTV (долговременные вариации) являются наиболее информативными показателями (Fanelli A. et al. 2013). Полученнные результаты могут быть основанием для проведения скрининга на синдром задержки роста плода, особенно в странах с низким уровнем жизни (Hoyer D. et al. 2017). В условиях сельской местности проведение мониторинга ВСР плода у женщин с преэклампсией, недостаточным питанием, экстрагенитальными заболеваниями можно считать экономически обоснованным. В отношении протокола исследования следует заметить, что достаточно получасовой записи. Максимальный уровень показателя LTV отмечается во время периодов бодрствования плода, а STV имеет наибольшее значение во время спокойного сна (Ortiz M. R. et al. 2013; Redman C. 2015). Учитывая, что оптимальное соотношение возможной активности и сна плода отмечается именно за полчаса, то этот временной интервал является наиболее приемлемым для записи КТГ.
Электрофизиологические методы (магнитокардиография и неинвазивная ЭКГ плода) позволяют изучать морфологические параметры комплекса PQRST, достоверно определять показатели ВСР плода на основе регистрации первичных биоэлектрических процессов в сердце для дальнейшего автоматизированного анализа (Bolin E. H. et al. 2016; BeharJ. et al. 2016). Взаимосвязь между STV (показатель вагусной активности по данным КТГ) и SDNN (линейный показатель мощности автономного тона по данным магнитокардиографии или неинвазивной ЭКГ плода) дает надежду на клиническое использование этих методов в перинатологии. Группа немецких ученых разработала комплексный показатель fABAS, который значительно превосходит STV по возможности оценивать созревание автономной нервной регуляции в процессе гестации. Также существуют предварительные данные, свидетельствующие о том, что fABAS позволяет оценивать функциональное состояние плода независимо от стационарного состояния (Hoyer D. et al. 2014, 2017).
Магнитокардиграфия обеспечивает наилучшее качество записи, но не имеет практической перспективы ввиду чрезвычайной дороговизны аппаратуры. В настоящий момент всего лишь несколько исследовательских центров мира имеют в наличии подобное оборудование. Неинвазивная ЭКГ плода, регистрируемая с передней брюшной стенки матери, является перспективным направлением развития мониторинга плода (Fuchs T. et al. 2016). В данный момент эта технология находится на самой начальной стадии внедрения в перинатологию. Основной проблемой является низкое соотношение сигнал/шум, что требует наличия сложных алгоритмов обработки сигналов в программном обеспечении.
Тем не менее, уже появляются данные о возможности применения интервала QT и соотношения T/QRS в диагностике дистресса плода (Behar J. et al. 2016; Lakhno I. 2015, 2016). Также есть результаты, позволяющие использовать неинвазивную ЭКГ плода для диагностики аритмий (Lakhno I. et al. 2017). Этот метод имеет значительные преимущества перед КТГ. Параллельная регистрация кардиоритма матери и плода при проведении неинвазивной ЭКГ позволила установить взаимосвязь между ВСР матери и плода и сформулировать теорию «вагусных отражений» (May L. E. et al. 2014; Lakhno I. 2017).
В апреле прошлого года в университете г. Ланкастер (Великобритания) состоялась конференция ESGCO 2016, в рамках которой была проведена специальная секция, посвященная росту и созреванию плода (Hoyer D. et al. 2017). Было проведено обобщение опыта использования КТГ, магнитокардиографии и неинвазивной ЭКГ плода для мониторинга созревания плода. В настоящий момент проводится подготовка к Jena cooperation study под руководством проф. D. Hoyer. В ходе исследования планируется оценить возможности применения fABAS путем обработки сигналов, регистрируемых с помощью КТГ, магнитокардиографии и неинвазивной ЭКГ плода.
Перинатология – отрасль медицины, направленная на охрану здоровья плода. Она обладает значительным арсеналом методов изучения его поведенческих реакций. Однако, многие проблемы далеки от своего решения. Возможно, необходимо использование новой методологической базы на основе углубленного изучения регуляторных механизмов гемодинамики плода. Это позволит надеяться на лучшее.
Перечень литературы находится в редакции.
Детальніше
Ген коротких хвостів
До вашої уваги – ще один матеріал від авторів науково-популярного порталу «Моя наука» у нашій новій рубриці «Дивовижний світ науки». Портал створений для того, щоб з'являлося більше зрозумілих та якісних текстів українською мовою про наукові досягнення та відкриття, про українських дослідників. Тому й автори цієї рубрики – українські науковці у галузі біології та медицини.
Олексій Болдирєв, науковий редактор порталу «Моя наука» my.science.ua
Всім життям будь-якого організму керують гени. Причому починають своє керування вони дуже рано, коли організм складається з однієї або декількох клітин. Побудова більшості наших органів вимагає злагодженої роботи сотень, а то й тисяч генів. Проте є настільки важливі гени, що їхнє вимкнення призводить до зупинки всього розвитку ембріону. Про деякі з таких генів ми й поговоримо.
Якщо дивитися на місце людини в еволюції всього живого, то нам належить лише менше мільйонної частини всього біорізноманіття. Коли ж взятися перелічувати всіх наших найближчих родичів, то нас з ними все одно не так багато. Людина з погляду систематики – примат, представник одного з рядів ссавців. А ссавці – клас підтипу хребетних тварин. Зоологи протиставляють декілька десятків тисяч хребетних (риб, амфібій, рептилій, птахів та ссавців) більше ніж мільйону всіх інших тварин – безхребетних. Ключова відмінність чується вже в самій назві: наявність чи відсутність хребта, ланцюжка спинних кісток. Звідки ж взялася ця унікальна структура, якої нема в більшості тварин?
На ранніх етапах ембріонального розвитку всіх хребетних хребта теж немає. Зате є штука, яку важко розгледіти в дорослому організмі – хорда. Якщо хребет складається з багатьох окремих кістково-хрящових хребців, то хорда є відносно одноманітною товстою струною сполучної тканини, що тягнеться зі спинного боку тіла зародка. Цей орган споріднює всіх хребетних тварин з двома невеликими групами мешканців моря: головохордовими та покривниками. Покривники – це примітивні тварини, які здебільшого ведуть нерухомий спосіб життя та схожі на невеликі діжечки з отворами, що фільтрують воду, відшукуючи в ній поживні речовини та їстівну планктонну дрібноту. При всій своїй несхожості, за даними молекулярно-генетичного аналізу покривники є найближчими родичами хребетних. Спільну хордову долю виказує їхня рухома личинка, яка володіє хордою, нервовою трубкою, органи чуття.

А ось представника головохордових багато з читачів, напевне, пам'ятають ще зі школи. Це ланцетник, морська тварина, схожа на маленьку рибку. Два десятки видів цих хордових зустрічаються у теплих і помірних регіонах Світового океану. Один з видів можна побачити й у нашому Чорному морі. Вчені давно обрали ланцетника за модельний організм для досліджень походження всіх хребетних. Адже він найбільше схожий на нашого викопного предка, що жив більше 500 мільйонів років тому.Організм ланцетника побудований дуже просто, хоча в нього є більшість систем органів, подібних до наших. Замкнена кровоносна система з потовщеною судиною замість серця на черевному боці, дихальні зябра, які омиваються кров'ю для газообміну, подібні до нирок видільні органи метанефридії, нервова трубка на спині, а під нею осьовий скелет – хорда. Хорда ланцетника є суцільним осьовим скелетом, у якому можна побачити окремі епітеліально-м'язові пластинки. При скороченні м'язів хорда стає більш пружною. Уже можна побачити спільну долю хорди й нервової трубки: вони разом оточені сполучноклітинною оболонкою.
Коли видатний французький зоолог Жорж Кюв'є вперше виділив тип хребетних на початку XIX століття, то ланцетника він туди не включив, а залишив серед типу молюсків, до яких його ще раніше відніс німецький натураліст Петер Паллас. Біологи ще півстоліття сперечались про долю нещасної тваринки, поки професор Київського й Одеського університетів Олександр Ковалевський не дослідив детально анатомію ланцетника та не довів його надзвичайну подібність та еволюційну спорідненість з хребетними.
З молюсків до хордових перетягнув він і покривників, акуратно вивчивши їх ембріологію та будову личинки. Ковалевському також належить низка відкриттів у галузі ембріології; зокрема він виявив, що всі без винятку багатоклітинні тварини проходять стадію гаструли в своєму ембріогенезі.
З досліджень Ковалевського та інших учених стало ясно, що безчерепні й головохордові мають з хребетними спільний план будови. Окрім хорди й зябрових щілин, які теж наявні у хребетних в ембріогенезі, спільним є розташування осьових систем органів. Якщо перерізати видовжене тіло ланцетника, риби, ящірки або людини десь посередині впоперек, то на зрізі ми побачимо таку картину. Найвищою, тобто найближчою до спинної поверхні буде спинний мозок або нервова трубка. Далі лежить хребет або хорда, нижче неї розташований шлунково-кишковий тракт. І нижче травного каналу ми побачимо велику судину або серце з аортою.
Саме в такому вертикальному порядку утворюються ці важливі системи органів під час ембріонального розвитку хребетних.
Цікаво, що якщо перерізати точно таким же чином тіло жука, слимака чи дощового черв'яка, то картина буде зворотна: нервова система у вигляді черевного нервового ланцюжка, як видно з назви, лежить унизу, біля черевної поверхні тіла. Вище знаходиться кишка, а біля самої спини знаходиться велика судина – серце безхребетного. А що як хребетні – то ті самі безхребетні, які стали повзати черевом догори? Смішна думка, на перший погляд.
Проте саме таку ідею висловив старший товариш та одвічний суперник Жоржа Кюв'є – французький натураліст Етьєн Жоффруа Сент-Ілер на початку того ж XIX сторіччя.
Тоді Кюв'є розділив усіх тварин на 4 типи: хребетні, молюски, членистоногі та черви.

Мало того, він ще й постулював, що кожний тип має свій особливий план будови, а тому тварини різних типів не споріднені між собою, чим фактично заперечив їх еволюцію та походження від спільних предків. Водночас ідея еволюції дуже імпонувала Жоффруа, тому він якраз шукав механізмів, як від одного плану будови перейти до іншого. Якщо для червів, членистоногих та молюсків спільні риси вдавалося знайти, то хребетні відрізнялися занадто сильно. Але Жоффруа-таки звернув увагу на розташування нервової та кровоносної системи й вирішив побудувати на цьому хиткому грунті перехід між типами. Кюв'є майстерно висміяв свого колегу під час серії дебатів у Французькій Академії наук, пирскали від цієї «гіпотези інверсії» зоологи, ембріологи та еволюційні біологи наступні півтора століття: це ж треба таке вигадати, ніби еволюція йде такими простими шляхами, взяв – і став повзати на спині!
Однак успіхи молекулярної біології за останні 40 років почали змінювати баланс на користь Жоффруа. Як ми казали на початку, розвиток того чи іншого органу залежить від ансамблів генів, серед яких завжди є найважливіші. Так для появи нервового ланцюжка у дрозофіли потрібна активація роботи генів vnd, indіMsh, які починають працювати в клітинах черевної зони ембріона цієї улюбленої мухи генетиків. Тоді як у зародку миші їхні гомологи Nk2, Gsh1,2 і Msx1,3 роблять те ж саме, але в клітинах, які лежать ближче до спини. Ген netrin майже однаковий у комах і ссавців, і однаково визначає середину осі нервової системи, лише працює на черевній стороні у перших і на спинній у других. Та ж історія з генами, які запускають формування серця. Ген tinman/csk у дрозофіли починає працювати під дорзальною поверхнею ембріона, де невдовзі почне розвиватися серце, а активація його гомологу Nkx2-5 у миші передує початку формування серця на черевному боці1.
Отже молекулярна біологія підтримує старого Жоффруа та цілком припускає можливість еволюційної інверсії. Хоча противники цієї гіпотези теж не здаються: щоб було, що перевертати, останній спільний предок хордових та комах повинен був мати й серце, і осьову нервову систему. Але за нашими сьогоденними уявленнями, це була значно більш примітивна тварина, без таких прогресивних органів. Чи могла вона мати гени, що потрібні для роботи серця або мозку, якщо самі органи в неї не формувалися?
Виявляється, така ситуація не виключена, сьогодні відомо багато прикладів таких преадаптацій, «еволюційних передбачень». Ген з'являється, виконує певну функцію, але в певних умовах змінює свою «професію» та стає вкрай важливим для чогось іншого. Саме так працював таємничий ген Т, ще відомий під назвою Brachyury, диригент формування хорди в ембріогенезі хребетних.
Невідомо, як довго б ми мучились загадкою ембріонального формування хорди, якби не одна жінка. Киянка Надія Добровольська, яку буремна доля закинула аж у Париж, відкрила ген Т у кінці 1920-х років, коли ніхто в світі ще достеменно не уявляв, що таке гени.
Слід сказати, що навряд чи пані Надія, навчаючись у Фундуклеївській гімназії біля сучасної станції метро «Театральна», думала про досліди з ембріонами мишей, генетику й радіобіологію. У 1899 році вона поїхала до Петербургу за іншим: вона бажала стати лікаркою. Справа в тому, що жінки в Російській імперії не могли навчатися в університетах. Але в кінці XIX століття з'явився перший щасливий виняток, Жіночий медичний інститут. У ньому й вивчилася на хірурга Надія Добровольська. Вона стала першокласною спеціалісткою: оперувала, викладала хірургію, проводила наукові дослідження і навіть описала (незалежно від німецьких медиків) хірургічний симптом, названий на її честь2. Вже під час Першої світової війни Добровольська стала першою жінкою, яка очолила кафедру хірургії.
А далі – падіння Російської імперії, громадянська війна. Надія Добровольська за сумним збігом опинилася в лавах Добровольчої же «білої» армії. Разом з розгромленими військами вона евакуювалася з Криму до Єгипту, де деякий час оперувала у таборі біженців прямо посеред пустелі. В якийсь момент доля посміхнулась їй, вдалося дістатися Франції, оселитися в Парижі разом з чоловіком, письменником Завадським. Але у Франції діяв суворий закон: іноземні лікарі не мали права вести медичну практику, поки не отримають місцевий диплом. Надії Добровольській-Завадській було вже 43, вчитися 5 років в університеті не було ані часу, ані грошей. На щастя, вона довідалась, що Інститут Радію славетного подружжя Кюрі відкриває лабораторію з вивчення дії радіаційного випромінення на живі організми. Туди вона й пішла лаборанткою, круто змінивши тематику своєї наукової роботи3.
Професор Клод Рего, який очолював лабораторію радіобіології, поставив Надії Олексіївні ризиковану на той час задачу: опроміненням викликати мутації у мишей та описати функцію порушених генів. Сьогодні ми знаємо, що радіація викликає мутації в генах, але на початку 1920-х років учені не мали однозначних доказів цього. Крім того, генетики переважно працювали з дрозофілами – комахами, які живуть недовго та швидко розмножуються, що потрібно для статистичного аналізу. Втім, Добровольська-Завадська рішуче взялася за справу. Вона опромінювала яєчка самців мишей та отримувала від них нащадків. Методом схрещувань вона отримала близько 3000 мишей, у яких шукала проявлення мутацій.
Одну з таких мутацій вдалося зловити. Її носії мали дуже короткі хвости. Через це Добровольська-Завадська назвала її Brachyury, з грецької «короткий хвіст», а також T – від англійського «tail», «хвіст». Вона спробувала вивести чисту лінію мишей, яка б несла цю домінантну мутацію в обох хромосомах, але не виходило. При схрещуванні двох гетерозигот (тобто носіїв одного мутантного й одного звичайного гену) замість співвідношення 3:1 між короткохвостими й нормальними нащадками, як слідувало б з другого закону Менделя, Добровольська спостерігала співвідношення 2:1. Значить, подумала вона, щось стається з чвертю мишат і вони не народжуються. Дослідивши ембріональний розвиток мишей з мутацією, вона виявила, що деякі зародки дійсно припиняють розвиток на ранній стадії, перетворюються на купку клітин та гинуть.
Надія Добровольська зрозуміла, що наштовхнулася на щось дуже важливе. Вона продовжила вивчати подібні мутації у лабораторних та диких мишей. Їй вдалося знайти ще декілька мутацій, які впливали на форму і довжину хвоста. Деякі з них виявляли свій ефект лише при наявності в тварини паралельної мутації в гені Brachyury.
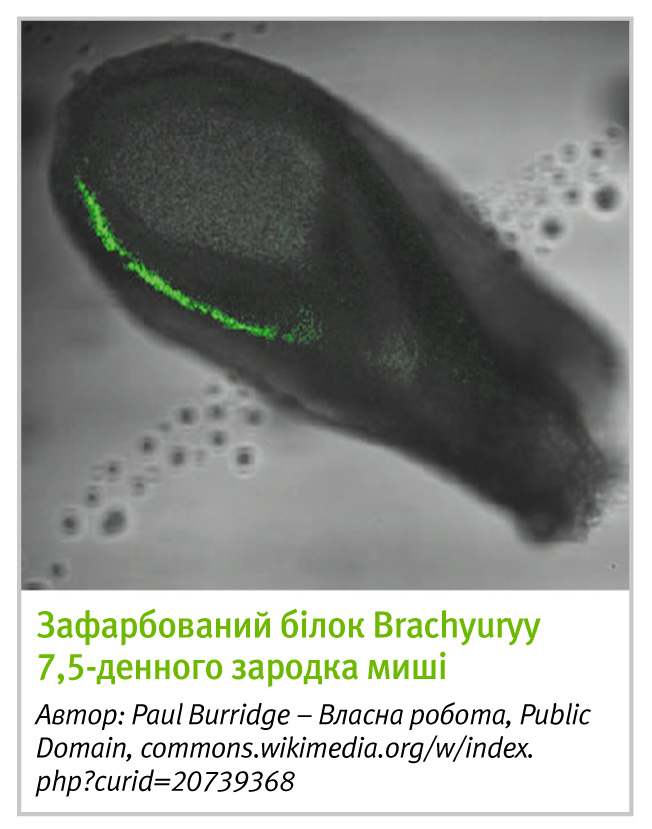
Не маючи технічної можливості проникнути до серцевини клітини, щоб зрозуміти сутність процесів, що відбуваються при мутаціях, Добровольська все ж зробила геніальну здогадку. Разом зі своїм співробітником, також емігрантом, біохіміком Миколою Кобозєвим, вона припустила, що Brachyury є головним регулятором формування хребта й хвоста, а інші гени відповідають за форму та розмір органу. На той момент генетика й ембріологія розвивались окремо, тому така гіпотеза лишилася непоміченою. Але саме так сучасна біологія розвитку й уявляє формування органів в ембріогенезі.
У 1933 році Добровольська-Завадська передала своїх короткохвостих мишей американським дослідникам Чеслі й Данну для подальшого вивчення, а сама зайнялася роллю генів у ракових пухлинах. Саме дослідження американських ембріологів показали, що при порушенні роботи обох генів Brachyury в зародка не відбувається появи хорди, а гетерозиготи з одним поламаним геном мають дефекти в її формуванні. У 1990 році було прочитано послідовність цього гену, а надалі точно вивчено його активацію в ембріогенезі. Отже, T-ген – це транскрипційний фактор, білок, який сідає на ДНК та активує зчитування багатьох генів. А вже ці гени починають працювати для утворення хорди.
Навіщо ж хребетним потрібна ця хорда? Ми ж не ланцетники, в дорослому стані її не маємо. Хорда потрібна в ембріогенезі для формування передньо-задньої осі тіла. Хорда впливає на утворення нервової трубки та на диференціацію навколишньої мезодерми. Вона є важливим організатором розвитку ембріона. Ген Brachyury у ссавців задіяний лише на стадії гаструляції та формування хорди, обмежений майже виключно клітинами хорди та ранньої мезодерми. У риб і амфібій цей ген експресується у хорді та навколо первинного рота (бластопору) при гаструляції. У покривників він також наявний лише в хорді. Подальші дослідження виявили цей білок у формуванні задньої кишки дрозофіли, у голкошкірих він знаходиться у клітинах навколо бластопору4.
Довгий час вважалося, що ген Brachyury наявний лише у тварин, як мають третій зародковий листок, мезодерму. Проте на початку 2010-х його знайшли в кишковопорожнинних, а потім у деякий амеб і грибів. Більше того, вимкнувши Brachyury у зародка жаби, дослідникам вдалося відновити нормальний розвиток вставленням до ембріону гена з амеби! Це свідчить про високу консервативність білка, хоча функція його в одноклітинних організмів залишається неясною. Втім, я певен, що вже невдовзі й цю таємницю науковий загін людства неодмінно розкриє.
- J. Gerhart. Inversion of the chordate body axis: Are there alternatives? Proc Natl Acad Sci U S A. 2000 Apr 25; 97(9): 4445–4448.
- Симптом Добровольської-Ніколадоні полягає у зменшенні пульсу при стисканні артеріовенозної аневризми.
- Про це все ми дізналися завдяки українському професору Інституту клітинної та молекулярної біології (Сингапур) Володимиру Коржу, який дослідив біографію Надії Добровольської-Завадської. V. Korzh, D. Grunwald (2001). Nadine Dobrovolskaya-Zavadskaya and the dawn of developmental genetics. BioEssays 23 (4), 365–371doi:10.1002/bies.1052.
- Satoh, Nori; Tagawa, Kuni; Takahashi, Hiroki (2012). How was the notochord born?. Evolution&Development 14 (1), 56–75. doi:10.1111/j.1525-142X.2011.00522.x

Расстояния – не помеха!
 Более 300 человек приняли участие в Профи-Лабах «ПІВДЕННОукраїнські зустрічі професіоналів» и «Західноукраїнські зустрічі професіоналів», прошедших в Одессе и Львове в июне этого года. Для нас это был первый опыт проведения региональных конференций, и он оправдал все ожидания.
Более 300 человек приняли участие в Профи-Лабах «ПІВДЕННОукраїнські зустрічі професіоналів» и «Західноукраїнські зустрічі професіоналів», прошедших в Одессе и Львове в июне этого года. Для нас это был первый опыт проведения региональных конференций, и он оправдал все ожидания.
Преимущества подобного рода мероприятий очевидны: оперативность проведения, индивидуальный подход при формировании программы, учитывающий специфику региона, низкая стоимость и отсутствие необходимости надолго отрываться от работы. Все эти аргументы убедили нас, что подобная форма образовательных мероприятий должна оказаться эффективной и востребованной. И мы не ошиблись – конференции прошли с большим успехом. Лекции специальных гостей, интереснейшие доклады, мастер-классы, посвященные актуальным проблемам акушерства и гинекологии буквально с первых минут захватили слушателей.
Конечно, во многом успех стал возможен благодаря нашим партнерам: кафедре акушерства и гинекологии факультета последипломного образования Львовского национального медицинского университета им. Данила Галицкого и кафедре акушерства и гинекологии №2 Одесского национального медицинского университета.
Мы надеемся, что конференции подобного рода станут регулярными и традиционными площадками для обмена опытом, демонстрацией новейших разработок и основой для выработки практических рекомендаций при решении проблем.

Детальніше

Дефицит молока
Пути решения проблемы
Первичная гипогалактия, по данным ВОЗ, встречается только у 5% женщин в популяции [2]. Однако первичный дефицит молока не является поводом для перевода ребенка на искусственное вскармливание. Ребенок должен получать грудное молоко, сколько бы его у матери не было, так как даже небольшое его количество будет иметь значение для здоровья, роста и развития.
Если у матери есть проблемы со здоровьем, которые мешают ее организму производить молока в необходимом для ребенка количестве, мы можем постараться минимизировать долю докорма, насколько это будет возможно.
При всем при этом, следует признать, что наиболее частой причиной, по которой матери вводят ребенку докорм смесью и рано прерывают грудное вскармливание, является не истинная гипогалактия, а кажущийся дефицит молока у матери (a perception of insufficient milk production) [1]. Очень часто матери кажется, что у нее мало молока, хотя на самом деле это не так. Частые прикладывания ребенка к груди, продолжительные сосания, неудовлетворенность после кормления, беспокойство во время сосания груди могут натолкнуть мать на мысль, что ее ребенку молока не хватает. Она пробует сцедить молоко, добывает 10–20 мл молока голубоватого цвета, и это только укрепляет ее в мысли, что, скорее всего, с лактацией есть проблемы. После этого она берет бутылочку со смесью и докармливает ребенка в произвольном объеме, как правило, столько, сколько ребенок съест.
И вот тут происходит самое важное: после докорма ребенок наконец-то засыпает и спит беспробудно как минимум на 3 часа, чего еще никогда не было! Итак, дефицит молока – подтвержденный факт!
Дальше все очень тривиально: объем докорма будет постепенно увеличиваться, чего не скажешь об объеме молока. И к 3-м месяцам ребенок будет уже на искусственном вскармливании, если раньше не предпочтет бутылочку маминой груди. Попутно мама, конечно, будет стараться увеличить лактацию разными чаями для лактации и орехами. Но все тщетно. «Ну что ж, я сделала все, что могла, видно я не молочная, но и на смесях растут дети….». К счастью, если женщине повезет, финал у этой истории может быть другим.
Лактация работает по принципу «спрос-предложение». Поэтому для того, чтобы повысить продукцию молока, нам необходимо увеличить частоту и эффективность опорожнения груди.
Исследования подтверждают тот факт, что производство молока обычно соответствует потребностям детей. Объем вырабатываемого молока зависит не столько от концентрации пролактина в крови матери, сколько от степени наполненности груди. К примеру, если ребенок плохо опорожняет одну грудь, но продолжает эффективно сосать вторую, то количество молока, вырабатываемого первой грудью, постепенно уменьшается, тогда как во второй секреция молока будет хорошей. Выработка молока может полностью прекратиться, если молоко из груди не удаляется долго. При этом и окситоцин, и пролактин поступают в обе груди в одинаковых количествах.
Кроме того, в грудном молоке имеется вещество, которое замедляет его выработку, своеобразная «встроенная защита» от переполнения груди. Это вещество назвали «фактор-ингибитор лактации» или просто «ингибитор». Он защищает молочную железу от отрицательных последствий переполнения. При опустошении груди путем сосания или сцеживания молока удаляется и ингибитор. Благодаря этому синтез молока идет быстрее и за единицу времени молочная железа вырабатывает больше молока. Чем более опорожнена грудь, тем быстрее вырабатывается в ней новое молоко.

Рекомендации по налаживанию лактации
Шаг первый и самый важный: оцените организацию грудного вскармливания и исправьте ошибки, если они есть.
Помогите матери подобрать комфортную позицию при кормлении и исправьте прикладывание ребенка к груди таким образом, чтобы он мог получить все молоко, какое уже есть в груди у матери. Не исключено, что только коррекция захвата груди станет единственным необходимым вмешательством, которое наладит лактацию.
Напомним, при неправильной технике захвата груди ребенок не может эффективно опорожнять грудь. Это значит, что количество молока у матери будет постепенно уменьшаться. К сожалению, правильный захват не происходит автоматически – ему нужно обучаться и ребенку, и матери.
Постарайтесь устранить причины, мешающие ребенку правильно захватить и эффективно сосать грудь. Например, если у ребенка имеется короткая уздечка языка, рекомендуйте ее подрезание. Если есть трещины соска, назначьте необходимое лечение. Если есть в уходе пустышка, накладки для сосков и бутылка с соской – убираем. Вода, чай между кормлениями также должны быть исключены.
Если ребенок не нуждается в докорме, его нужно убрать. Если же потребность в докорме есть, обучаем мать альтернативным методам кормления (ложка, шприц без иглы, чашечка, SNS-система и т. д.) в зависимости от объема докорма, возраста ребенка и комфорта матери. В этом случае нужно постараться убедить женщину не докармливать ребенка из бутылки, так как бутылочное кормление может отрицательно сказаться на желании сосать грудь. По мере увеличения выработки молока в ответ на стимуляцию, объем докорма можно будет постепенно сокращать до минимума, а в идеале, убрать его совсем.
Шаг второй: увеличьте частоту кормлений
При нормальной продукции молока частота прикладываний к груди за сутки может быть очень вариабельна. Женщины с большой емкостью груди могут прикладывать ребенка 6 раз в сутки и производить достаточно молока для своих детей, в то время как женщины с маленькой емкостью груди прикладывают детей часто и избегают больших интервалов между кормлениями.
Однако такие режимные моменты, как кормление по часам (например, 1 раз в 3 часа), ограничение продолжительности сосания (например, кормление грудью не более 10–15 минут), исключение ночных кормлений и т. д., могут нанести серьезный ущерб женщине с любой емкостью груди.
Поэтому с целью увеличения выработки молока необходимо увеличить частоту прикладываний к груди. Желательно, чтобы женщина прикладывала ребенка к груди как минимум 10–12 раз в сутки, предлагая обе груди на каждое кормление. Оптимальный интервал между кормлениями днем 1,5–2 часа, ночью — максимум 4 часа. Можно кормить и чаще, при желании ребенка, но не реже. Причем, прикладывать ребенка можно – по кругу, т. е. возвращать к той груди, которую он сосал в начале кормления, после того, как хорошо опорожнил вторую грудь.
При этом важно объяснить матери, что прикладывать ребенка к груди необходимо при возникновении ранних признаков готовности ребенка к кормлению, а не тогда, когда он уже заплакал или закричал. Так его легче будет правильно приложить к груди, он будет более терпелив, будет дольше и активнее сосать.
Если сигналом к прикладыванию к груди является крик ребенка, кормление не будет эффективным: расплакавшемуся ребенку нелегко сразу правильно захватить грудь, он может быстро утомиться и заснуть раньше, чем насытится и хорошо опорожнит грудь.
К ранним признакам готовности к кормлению относят быстрые движения глаз, ерзание, беспокойство, поисковые движения головой, засовывание пальцев в рот, сосательные движения, тихие звуки, похожие на вздохи.
Особое внимание нужно уделить сонливым детям, а также маловесным и недоношенным. В этих случаях матери очень важно будить и прикладывать ребенка по собственной инициативе. Если сонный ребенок вяло сосет, мама может попробовать чаще менять грудь во время одного кормления: как только ребенок начинает медленно сосать или редко глотать, она может менять грудь.
Шаг третий: используйте методику сжатия груди, чтобы стимулировать интерес ребенка к сосанию в процессе кормления
Поскольку поток молока из груди в течение одного кормления не постоянный, при его уменьшении ребенок может капризничать, нервничать, требуя потока. Некоторые дети, особенно те, которых кормили из бутылки, могут вообще отказываться сосать грудь, при ослаблении рефлекса выброса молока. Таким образом, они не высасывают даже то молоко, которое есть у матери. Чтобы увеличить поток молока из груди, можно рекомендовать матери в процессе кормления сжимать грудь.
Эту методику предложил канадский педиатр Джек Ньюмен, который уже более 30 лет оказывает матерям поддержку в грудном вскармливании. Суть метода заключается в том, что в тот момент, когда ребенок просто посасывает грудь, не делая больших активных глотков, мама плавно сжимает грудь подальше от соска и ареолы, разместив большой палец руки с одной стороны, а остальные пальцы – напротив него с другой стороны, и удерживает ее. При этом ей не должно быть больно, а форма груди возле рта ребенка остается неизменной. Как правило, после сжатия ребенок начинает сосать и глотать молоко в ритме «широко открытый рот–пауза–закрытый рот». Удерживать грудь сжатой мама продолжает до тех пор, пока ребенок не перестанет глотать молоко.
После прекращения сжатия ребенок перестает сосать, но после небольшой паузы и возобновления сжатия, он снова начинает активно добывать молоко из груди. Продолжать сжатие нужно до тех пор, пока ребенок не перестанет глотать из нее молоко даже со сжатием. После этого не стоит спешить отнимать ребенка от груди. Если дать ребенку возможность еще побыть у груди, через некоторое время может еще раз сработать рефлекс выброса молока и его поток из груди увеличится сам по себе. Это даст возможность ребенку получить дополнительную порцию молока. После того, как он сам отпустит грудь, его можно переложить ко второй груди и повторить процесс.
Шаг четвертый: дополнительные сцеживания
Поскольку производство молока зависит от спроса, мы можем увеличить спрос за счет дополнительных сессий сцеживаний. Для этого после кормления мама в течение 10–15 минут дополнительно сцеживает вручную или с помощью молокоотсоса (можно в комбинации) обе груди даже если ей кажется, что грудь пустая. Сцеженным молоком мать может докормить ребенка вместо смеси. Эффективность сцеживаний будет выше, если мама будет дополнительно предпринимать меры по стимуляции окситоцинового рефлекса. Исследования показывают, что сцеживание в сочетании с массажем груди или теплым душем позволяют увеличить объем сцеженного молока.
Шаг пятый: стимуляция окситоцинового рефлекса
Для того, чтобы грудь лучше отдавала молоко, как во время сосания, так и во время сцеживания, мы можем посоветовать матери приемы, направленные на стимуляцию окситоцинового рефлекса. При этом важно помнить, что боль, стресс, неуверенность, эмоциональные переживания, физическая усталость – самые главные барьеры на пути активного выброса молока из груди. Мы не сможем добыть из груди молоко, если не заставим хорошо работать окситоциновый рефлекс. Это аксиома! Никакие «разминания», «расцеживания», «пробивания молочных протоков» и прочие танцы с бубнами у груди женщины не помогут молоку выделяться, если ей при этом больно или страшно! Поэтому первое условие для стимуляции работы гормона окситоцина – спокойствие, комфорт, расслабление, отсутствие факторов, повышающих выброс адреналина – антагониста окситоцина.
Присутствие ребенка, физический контакт с ним, особенно кожа к коже, мысли о ребенке, его запах, звуки и т. п., стимулируют работу окситоцина. Из этого следует второе правило: сцеживаться лучше в присутствии ребенка, в идеале – в контакте кожа к коже с ним, а если это по какой-то причине невозможно, то женщине нужно хотя бы думать о ребенке, смотреть на фотографию, видео и т. п.
Окситоцин любит тепло. Поэтому молоко будет лучше из груди выделяться, если перед кормлением или сцеживанием женщина выпьет теплый напиток, сделает теплый душ на молочную железу или теплый сухой компресс.
Также может помочь расслабляющий массаж спины и шеи. Особенно полезен массаж спины вдоль позвоночника на расстоянии 1,5 см справа и слева от него. Непосредственно перед сцеживанием женщине рекомендуется сделать легкий массаж груди в направлении от периферии к соскам, а также нежно похлопать по молочной железе кончиками пальцев.
Шаг шестой: организация быта женщины
Для того, чтобы воплотить все вышеперечисленное, нужно заручиться поддержкой любящих маму близких людей и постараться максимально оградить ее от домашних дел. В ее окружении обязательно найдется тот, кто может приготовить для нее завтрак, заварить чай или наполнить ванну. Маме важно позволить себе больше отдыхать, спать при каждой возможности, хорошо питаться и не забывать пить.
Питание и питьевой режим должны быть полноценными, но не чрезмерными. Для лучшей выработки молока можно рекомендовать женщине пить жидкости столько, чтобы она не испытывала жажды.
Вот, собственно, и все меры по увеличению выработки молока. А как же чаи, травяные сборы и специальные продукты питания, стимулирующие лактацию? Их, на самом деле, не существует. Во всяком случае, тех, эффективность которых научно доказана.
К наиболее популярным лактогонным травам относятся фенугрек (пажитник), волчец кудрявый и галега (козлятник лекарственный), также можно встретить лист малины, галегу, пивные дрожжи, люцерну и крапиву. Но ни в материалах Всемирной организации здравоохранения, ни в рекомендациях Американской Академии Медицины Грудного Вскармливания мы не найдем указаний по использованию тех или иных травили продуктов для стимуляции лактации.
В 2012 году в Journal of Human Lactation был опубликован «Systematic Review of the Efficacy of Herbal Galactogogues» «Системный обзор эффективности растительных лактогонных средств» [6], составленный отделом Эпидемиологии и Биостатистики университета штата Иллинойс, США. В нем исследователи проанализировали все экспериментальные работы, посвященные растительным лактогонам.
В результате, в число растительных средств, эффективнее плацебо, попало всего 5: шатавари, торбанган, пажитник, расторопша и японский травяной чай. Но, к сожалению, по правилам проведения системного обзора, ни одно из исследований не было признано достаточно достоверным. Вывод исследователей был однозначным: «Учитывая недостаточность доказательств этих испытаний, лактогонные травы не рекомендуются для использования».
В этой связи интересным кажется высказывание доктора Джека Ньюмена на этот счет. «Почти у каждого народа есть какая-то трава, растение или средство для увеличения количества молока. Одни могут работать за счет эффекта плацебо — и это хорошо, другие — не работать вообще, третьи действительно могут содержать один или несколько активных компонентов. А в состав некоторых трав могут входить активные компоненты, которые не влияют на лактацию, зато влияют на что-то другое, и эти эффекты не всегда желательны. Учтите, что побочные эффекты, иногда серьезные, могут быть даже у трав. Лекарства натурального происхождения — по-прежнему лекарства, а 100% безопасных лекарств не бывает».
Из медикаментов, чаще всего упоминаемых в качестве стимуляторов лактации, можно отметить домперидон и метоклопрамид, препараты, повышающие моторику желудочно-кишечного тракта, а также обладающие противорвотным действием [4, 8]. У обоих был отмечен побочный эффект – стимуляция выработки пролактина посредством блокировки работы дофамина, деятельность которого заключается в снижении секреции пролактина гипофизом.
Предпочтение отдается домперидону из-за меньшего количества побочных эффектов, таких как головная боль, сухость во рту, спазматическая боль в животе. В большинстве руководств рекомендуется принимать домперидон от 10 до 30 мг 3 раза в день. После начала приема домперидона может пройти 3–4 дня до того, как мама заметит какой-либо эффект, хотя некоторые отмечают повышение количества молока в первые 24 часа. Чтобы достичь максимального эффекта, необходим прием в течение 2–3 недель, но некоторые матери замечают улучшение только после 4 или более недель приема.
В 2012 году Journal of Human Lactation было опубликовано исследование The Effect of Two Different Domperidone Doses on Maternal Milk Production [12], в котором описаны два способа применения домперидона. В течение 4 недель одна группа испытуемых (преимущественно матери недоношенных младенцев) получала по 10 мг домперидона трижды в день, а другая – 20 мг домперидона трижды в день. На пятой неделе эта же доза предлагалась дважды в день, а на шестой – всего 1 раз в день.
В результате выяснилось, что в обеих группах достигался существенный прогресс в выработке молока, но матери, получавшие большую дозу домперидона, вырабатывали существенно больше молока. Хотя на 4–5-й неделях приема препарата различий между группами уже не отмечалось.
По мнению доктора Ньюмена, домперидон лучше работает в следующих случаях для усиления лактации:
- если мама, сцеживающая молоко для больного или недоношенного ребенка, на 4–5-й неделе после родов замечает, что лактация снизилась;
- когда у мамы уменьшается количество молока, в связи с приемом гормональных контрацептивов, в частности, эстрогенсодержащих;
- когда ребенку 3–4 месяца и у мамы без видимых причин уменьшается количество молока;
При релактации, индуцированной лактации (для кормления усыновленного ребенка) домперидон также может быть использован.
Однако, важно помнить, что домперидон – это только вспомогательное средство и назначать его стоит только тогда, когда уже все другие подходы для коррекции дефицита молока задействованы. Ведь реальный стимулятор лактации находится на руках у мамы – это ребенок. И если женщина не исправит ошибки в организации грудного вскармливания и не предпримет других мер по налаживанию лактации, о которых говорилось в этой статье, молока у нее не прибавится, несмотря на прием домперидона.
Если все условия по стимуляции лактации не принесли желаемого результата и не удалось перейти на кормление ребенка исключительно грудью, нужно помочь матери организовать смешанное вскармливание. По исполнению ребенку 6 месяцев смесь постепенно заменяется блюдами прикорма, а грудное вскармливание продолжается без проблем. Только 5% женщин не могут кормить ребенка исключительно грудью до 6 месяцев, но кормить ребенка грудью до 2-х лет и более могут все!
Перечень литературы находится в редакции.
Детальніше
Унікальна ініціатива українських медиків
У чому вона полягає, якими є очікування від її втілення і що спонукало лікарів діяти у дещо незвичному для них напрямку, самі ініціатори розповіли на брифінгу, який відбувся в ІА «УНІАН» 22 червня 2017 року. Приводом для брифінгу стало наступне. Вперше в Україні в сфері акушерства та неонатології лікарі самотужки впроваджують реальний механізм фінансового забезпечення сучасних медичних протоколів допомоги недоношеним дітям через залучення механізму добровільного медичного страхування.
Зокрема, в брифінгу взяли участь лікар-генетик, д. мед. н., генеральний директор пологового будинку «Лелека» та клініки репродуктивної медицини «Надія», лауреат Державної премії України, віце-президент УАРМ (Українська Асоціація репродуктивної медицини) Валерій Зукін; д. мед. н., проф., заступник головного лікаря з неонатології пологового будинку «Лелека» Юрій Батман; член-кор. НАМН України, д. мед. н., проф., заслужений діяч науки і техніки України, завідувач кафедри неонатології НМАПО ім. П. Л. Шупика, головний спеціаліст МОЗ України зі спеціальності «неонатологія» Єлизавета Шунько, а також Тетяна Дерягіна – представник страхової компанії «УПСК».

За даними ВООЗ, 15 мільйонів дітей щорічно народжуються передчасно, і це число дедалі зростає.
Ускладнення у результаті передчасних пологів є основною причиною смерті дітей у віці до п'яти років. Так, у 2015 році вони призвели до майже одного мільйона випадків смерті.
Три чверті таких дітей, за оцінками спеціалістів ВООЗ, можна було б урятувати за допомогою наявних ефективних за вартістю заходів втручання (шляхом надання основних видів допомоги під час пологів і в післяпологовий період кожній матері і кожній дитині).
До основних причин передчасних пологів відносять багатоплодову вагітність, інфекції, а також такі хронічні стани, як діабет і високий кров'яний тиск; проте часто причина залишається не виявленою.
Отже, передчасні пологи – глобальна загальносвітова проблема, але у різних країнах показники передчасних пологів варіюються від 5% до 18% від числа народжених дітей.
В Україні, за даними медичної статистики 2015 року, цей відсоток складав 5,67% (в абсолютних числах – 22631 передчасних пологів за рік).
«Життя передчасно народженої дитини багато в чому залежить від так званої «золотої години», – зауважила Єлизавета Шунько. – «І не тільки саме життя, а й рівень здоров’я дитини у подальшому. Сьогодні розроблено ефективні медичні технології, здатні рятувати життя і здоров’я матері та новонародженої дитини і ними добре оволоділи наші лікарі, але проблема, через що, у тому числі, було організовано сьогоднішній брифінг, полягає у тому, що ці технології є високовартістними, особливо, у частині фармакотерапії і тут вже від медиків мало що залежить. Держава теж не може покривати ці видатки повною мірою, і, до речі, цього собі не можуть дозволити навіть заможні країни. Отже, частина витрат лягає на сім’ї пацієнтів, які не завжди готові до цього, тож потрібно шукати вихід, і дуже добре, що з’явилася можливість застрахуватися на випадок передчасних пологів, забезпечивши у такий спосіб здорове майбутнє своєї дитини. Зрештою, здорова дитина – це щастя не тільки однієї окремо взятої сім’ї, це ще й суттєвий внесок у суспільство, у його розвиток».
Валерій Зукін також додав трохи статистичних даних: «В Україні щороку народжується приблизно 8 000 дітей вагою менше 2000 г, у Києві – близько 1000! Безперечно, медики вже вміють виходжувати таких крихіток, але самим тільки вмінням і знаннями життя не врятуєш, на жаль… Окрім обладнання, для лікування «надмаленьких українців» потрібно багато ліків, витратних матеріалів, парентеральне харчування, тощо», – зауважив В. Д. Зукін.
Він також відзначив, що в цій царині останніми роками відбулися деякі позитивні зрушення, які трохи покращили ситуацію: відділення інтенсивної терапії новонароджених в Україні отримували нове обладнання, було створено нові перинатальні центри. Але кількість таких центрів не може задовольнити таку велику країну, як наша.
Юрій Батман додав до вищенаведеного ще кілька важливих тез. «З 1 січня 2007 року в нашій країні була введена реєстрація недоношених дітей з терміном гестації 22 тижні і масою тіла 500 г. За цей час неонатологи України, що працюють у пологових стаціонарах, відділеннях інтенсивної терапії новонароджених тощо, придбали великий досвід виходжування передчасно народжених дітей, дітей з низькою і навіть екстремально низькою вагою тіла. Але процес виходжування таких діток – це ціла система, яка включає в себе солідну діагностичну, лікувально-контрольну апаратуру, яка, до того ж, нічого не означає без висококваліфікованих фахівців. Апарат, сам по собі, як відомо, не лікує. Отже, важливо все в комплексі, в системі. Причому, це має бути замкнена система: від моменту народження і надання кваліфікованої своєчасної медичної допомоги на сучасному рівні в перші години і навіть хвилини після народження, до моменту виписки зі стаціонару і подальшого спостереження за дитиною. У цю систему входить і обладнання, і витратні матеріали, лікарські засоби тощо. Особливо хочу зауважити, що у цій системі дуже важлива роль відводиться медичній сестрі, адже на ній лежить величезна відповідальність, оскільки більшість маніпуляцій виконує саме медична сестра. Якщо вона десь, не дай, Боже, помилиться, все наше обладнання, знання і досвід, не матимуть значення. Це ще раз підкреслює, що в цій системі важлива кожна ланка і на кожному фахівцеві лежить велика відповідальність. Не випадково у всьому світі вважається, що виходжування новонароджених з низькою вагою тіла є інтегральним показником пологового стаціонару. Не кількість пологів, а саме виживання новонароджених, особливо тих, що народилися передчасно і з низькою масою тіла», – підкреслює неонатолог.
Передчасні пологи – ургентна ситуація і у більшості випадків відбуваються спонтанно, тож результат дуже залежить від того, наскільки медичний заклад, куди буде доставлена породілля, готовий надати необхідну допомогу жінці і новонародженій дитині.
Випадки, коли у відділенні немає необхідних ліків (скажімо, дороговартістного сурфактанту) – на жаль, не така вже й рідкість, тож пацієнтам доводиться купляти ліки самим. При тому, як вже наголошувалося, в екстреному порядку. Добре, якщо фінансовий бік питання – не проблема, а якщо необхідну суму сім’ї знайти складно?. Отже, на думку ініціаторів Програми, іншого механізму, аніж добровільне медичне страхування, поки ніхто не запропонував.
Як наголошувалося під час брифінгу, цей механізм забезпечує повну медичну допомогу недоношеним новонародженим незалежно від ваги при народженні.
Про саму страхову програму присутнім детально розповіла Тетяна Дерягіна, особливо наголосивши, передусім, на двох обставинах: цією програмою може скористатися будь-яка вагітна жінка, незалежно від того, де вона спостерігає свою вагітність (від державної жіночої консультації – до закладу приватної форми власності), і не менш важливо, що програма є цілком доступною, адже її вартість не перевищує навіть розміру мінімальної заробітної платні, встановленої на сьогодні в Україні.
Отже, остаточна оцінка щодо впливу такого кроку на реальну ситуацію – попереду. Але вже зараз зрозуміло, що це реальний шанс для багатьох українських сімей без остраху дивитися у майбутнє, бути впевненими, що, у разі необхідності, медична допомога буде надана вчасно і у повному обсязі.
Детальніше