Герпесвірусні інфекції. Особливості клінічної картини, діагностика, лікування
У своїй практичній діяльності лікарі багатьох спеціальностей зустрічаються із захворюваннями, які викликані вірусами родини Herpesviridae. Герпесвіруси (ГВ) широко поширені у людській популяції, вони характеризуються пантропізмом та здатні вражати практично всі органи та системи організму людини, викликаючи латентну, гостру та хронічну форми інфекції.
Захворювання, обумовлені герпесвірусами, називаються герпесвірусними інфекціями (ГВІ). Вони характеризуються ураженням шкіри, слизових оболонок, нервової системи, очей, внутрішніх органів, сечостатевої системи. Після проникнення віруси герпесу зберігаються (персистують) в організмі людини пожиттєво у вигляді латентної інфекції та можуть під впливом послаблюючих факторів (грип, інші віруси, лікування імунодепресантами, СНІД та ін.) реактивуватися, викликаючи клінічно виражені форми із формуванням вторинної імунної дисфункції та вторинної імунної недостатності (ВІД).
ГВІ є одними з найрозповсюдженіших у світі. У розвинених країнах Європи на них хворіє третина населення. За даними ВООЗ, вони займають друге місце після грипу та ГРВІ у структурі захворюваності та смертності при вірусних інфекціях.
Сприйнятливість людини до ГВ висока. Близько 90% всього населення планети інфіковано одним або декількома серотипами родини ГВ. Від 12 до 25% із них мають рецидивуючі форми захворювань, у 30% інфекція виявляється у субклінічній та латентній формах. Аналіз В. А. Ісаковим щорічної захворюваності ГВІ у Російській Федерації показав, що у 15% дорослого населення має місце герпетичне ураження шкіри та слизових оболонок, генітальний герпес (ГГ) зустрічається у 6–10% дорослого населення, у 60–65% ГВ є причиною патології рогівки ока (90% – ВПГ, 10% – ЦМВ), захворювання нервової системи обумовлені ГВ у 1–1,5%, при цьому в 14–30% випадків тривало зберігаються залишкові явища, летальність при ураженні нервової системи складає від 5 до 70% у залежності від клінічної форми. В Україні відсутня обов’язкова реєстрація захворюваності всіма ГВІ і тому істинна кількість хворих невідома.
Для родини герпесвірусів характерний пантропізм до органів та тканин, пожиттєва персистенція в організмі людини і здатність викликати різноманітні маніфестні форми захворювання. На сьогодні виділено та класифіковано понад 100 представників цієї родини, які викликають захворювання у людини, диких і домашніх тварин, земноводних та плазунів. Із них 8 антигенних серотипів вірусів герпесу виділені від людини: вірус простого герпесу 1-го та 2-го типів (ВПГ-1, ВПГ-2), вірус вітряної віспи – оперізуючого герпесу, або вірус герпесу людини 3-го типу (ВГЛ-3), вірус Епштейна–Барр або вірус герпесу людини 4-го типу (ВГЛ-4), цитомегаловірус, або вірус людини 5-го типу (ВГЛ-5), вірус герпесу людини 6-го типу (ВГЛ-6), вірус герпесу людини 7-го типу (ВГЛ-7), вірус герпесу людини 8-го типу (ВГЛ-8), асоційований із саркомою Капоші (табл. 1).
Усі герпесвіруси є ДНК-вмісткими, схожі за морфологією, способом репродукції в інфікованих клітинах, розміром вібріона, а також здатністю індукувати латентну, гостру та хронічну інфекції у людини. Відповідно до рішення Комітету експертів з таксономії, прийнята та розроблена сучасна класифікація герпесвірусів, де родину герпесвірусів розділяють на три підродини – α, β, γ (табл. 1).
Αльфа (α)-герпесвіруси (Alphaherpesvirinae) характеризуються коротким циклом репродукції з цитопатичним ефектом в клітинах інфікованих культур, патогенні для більшості господарів. У більшості випадків вони персистують у центральній нервовій системі (ЦНС) – у сенсорних гангліях, підтримуючи латентну інфекцію, яка нерідко проявляється, як захворювання, яке періодично загострюється. До підродини Alphaherpesvirinae належить рід Simplexvirus (HSV), до якого включені патогенні для людини віруси HSV-1 (вірус простого герпесу 1-го типу) та HSV-2 (вірус простого герпесу 2-го типу), а також рід Varicellovirus і вірус герпесу 3-го типу – вірус вітряної віспи – оперізуючого герпесу (varicella-zoster herpes), який до нього відноситься. Таким чином, типовими представниками підродини альфа-герпесвірусів є ВПГ-1, ВПГ-2, ВВВ-ОГ (табл. 1).
Бета (β)-герпесвіруси (Betaherpesvirinae) відрізняються чітко вираженою патогенністю для більш вузького кола господарів, менш вираженою цитопатичністю клітин, тривалим циклом реплікації, викликають виникнення маніфестної і латентної інфекції у слинних залозах, нирках та інших органах, можуть бути причиною генералізованого ураження у новонароджених дітей і дорослих при імунодефіцитних станах. До підродини Betaherpesvirinae відносяться патогенний для людини рід Cytomegalovirus, а також рід Roseolovirus, в який включені ВГЛ-6А, ВГЛ-6В, ВГЛ-7 (табл. 1). Їх асоціюють із раптовою екзантемою у дітей та дорослих і синдромом хронічної втоми (СХВ) (табл. 2).
Гамма (γ)-герпесвіруси (Gammaherpesvirinae) характеризуються тропізмом до В- та Т-лімфоцитів, але репродукуються в основному в В-клітинах, у яких вони здатні тривало персистувати. Ці віруси нерідко є причинами тяжких смертельних лімфом, лейкемій, розвитку яких сприяють додаткові фактори – екзогенні, генетичні та інші (табл. 2). Патогенні для людини віруси віднесені до роду Lymhocryptovirus. Це вірус Епштейна–Барр (ЕBV, type 4) – збудник інфекційного мононуклеозу (ІМ), а також ВГЛ-8, який асоційований із саркомою Капоші і відноситься до роду Rhadinovirus (табл. 2).
За останніми даними, вірус ВПГ-2, поряд із вірусами папіломи людини, ЦМВ, хламідіями та мікоплазмами, відіграє значну роль у розвитку непластичних процесів у людини, а саме раку шийки матки, раку передміхурової залози (табл. 2). Він виступає у якості кофактору канцерогенезу, ініціюючи розвиток дисплазії та підтримуючи її у стані стабілізації. ГВ індукують процеси атеросклерозу, де ВПГ виступає в асоціації із ЦМВ. Збільшилась частота виявлення ГВ серед причин урологічної патології у дітей. Так, причиною урологічної патології за даними різних авторів у 40% випадків є ЕБВ, рідше ВПГ-2 та ЦМВ. Показаний несприятливий, інколи фатальний вплив ГВ на перебіг вагітності і пологів, патологію плода і новонароджених. При вагітності у зв’язку із пригніченням клітинного імунітету можливе виникнення дисемінації вірусу із ураженням посліду і інфікуванням плода як висхідним, так і гематогенним шляхом. Встановлено, що ГВ можуть активувати геном вірусу імунодефіциту людини (ВІЛ), який знаходиться стадії провірусу, та є кофактором прогресування ВІЛ-інфекції та СНІДу. Тому ГВІ є однією із СНІД-індикаторних інфекцій.
ГВ вражають еритроцити, тромбоцити, лейкоцити та макрофаги, здатні тривало персистувати в організмі, формуючи нестерильний імунітет. При ГВІ, як при інших хронічних захворюваннях із персистенцією вірусу, виникає імунний дисбаланс із порушенням різних ланок імунної системи і її нездатністю елімінувати віруси із організму. Віруснейтралізуючі антитіла, які зберігаються впродовж всього життя, навіть у високих титрах не попереджують виникнення рецидивів захворювання.
Співіснування вірусу та імунокомпетентного господаря потребує встановлення балансу між швидкістю реплікації вірусу та його елімінацією із організму за допомогою імунної системи, що забезпечує виживання обох видів. В арсеналі імунної системи знаходиться велика кількість різноманітних стратегічних підходів до розпізнавання та елімінації вірусів, у відповідь на які у вірусів відбулося вироблення різноманітних способів уникнення виявлення імунною системою. В процесі тривалої еволюції і у зв’язку із вимушеним співіснуванням вірусів в організмі людини ГВ виробили різноманітні молекулярні механізми для захисту від розпізнавання та елімінацією імунною системою. Так, віруси кодують гомологи цитокінів, хемокінів та їх рецепторів–молекул, які відіграють важливу роль в контролі імунної відповіді. Деякі дослідники вважають, що за рахунок виявлення у людини гомологів вірусних білків можна буде зрозуміти, які гени людини відіграють особливу роль в імунітеті.
Механізми ухиляння вірусів від імунної атаки в цілому можуть бути розділені на три групи:
ухиляння від розпізнавання компонентами гуморального імунітету, наприклад за рахунок зміни імунодомінантних епітопів;
перешкоджання клітинному імунітету, наприклад за рахунок пригнічення презентації вірусних пептидів, а також пригнічення активності НК-клітин (натуральних кілерів);
пригнічення реалізації ефекторних функцій, наприклад експресії цитокінів, а також апоптозу інфікованих клітин.
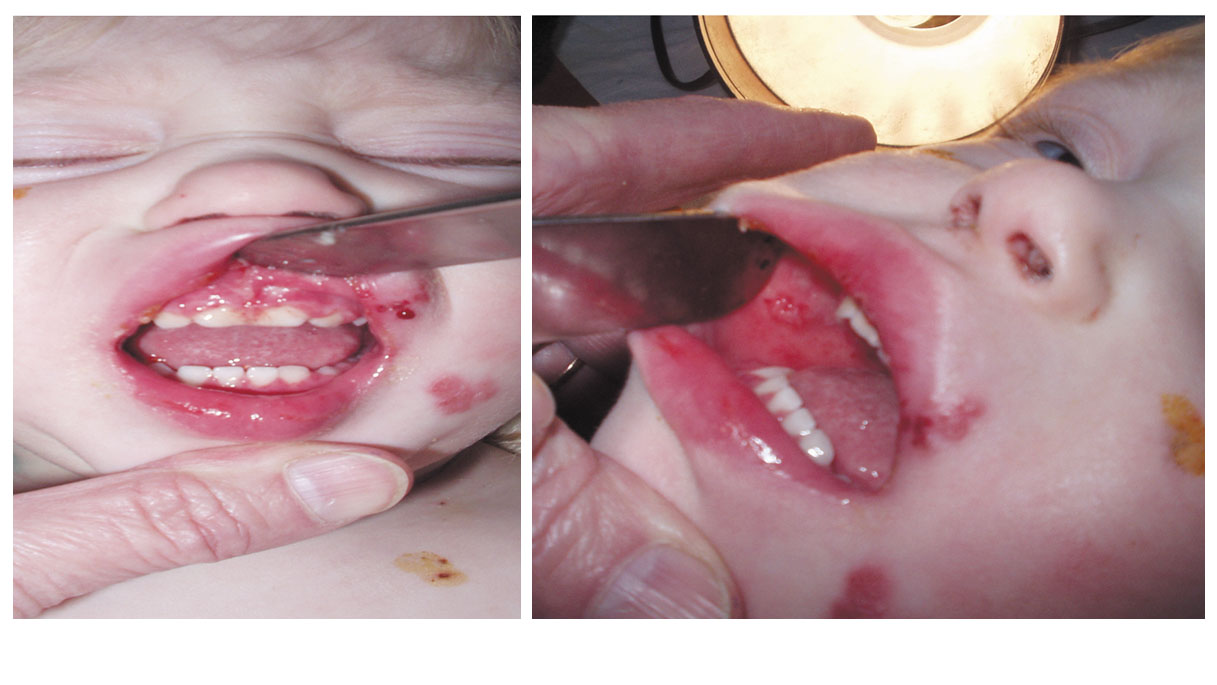
Захворювання, яке викликається герпесвірусами 1-го та 2-го типів (ВПГ-1 (HSV-1), ВПГ-2 (HSV-2)) носить назву герпетична інфекція (ГІ) та характеризується появою пухирцевих висипань на шкірі та слизових оболонках, а також можливістю генералізації процесу, ураженням ЦНС та внутрішньоутробним ураженням плода (рис. 1).
Рисунок 1 – герпетична інфекція: А – herpes labialis і herpes nasalis; В – генералізована форма із ураженням шкіри та герпетичним енцефалітом; С – герметичний енцефаліт, дані МРТ-дослідження.
Інфікованість населення Земної кулі HSV-1 складає 90–97%, HSV-2 – біля 40%. Інфікування проходить у перші 5 років життя дитини. Найбільша сприйнятливість до ГІ відмічається у дітей віком від 5 місяців до 3 років. HSV-1 передається повітряно-крапельним і контактним шляхом і уражує шкіру, слизові оболонки, ЦНС. HSV-2, який спричиняє геніальний герпес, передається статевим, вертикальним шляхом під час пологів (контакт з родовими шляхами матері), трансплацентарно або висхідним шляхом через цервікальний канал в порожнину матки, можливий також трансфузійний або парентеральний шлях передачі.
Незалежно від шляху попадання HSV до організму, первинне розмноження вірусу відбувається у місці вхідних воріт. Вірус розмножується у клітинах екто- та ендодермального походження, зумовлює руйнування епітеліальних клітин. Найбільш характерною є поява пухирців внаслідок так званої балонної дегенерації епітелію. Відбувається дегенерація клітинного ядра, ураження цитоплазматичної мембрани з формуванням багатоядерних гігантських клітин. Висловлюється також гіпотеза, що вірус проникає в дендрити нейронів, що іннервують шкіру, після незначної реплікації у місці інокуляції. Потім вірус потрапляє в сенсорні ганглії, де й відбувається його основна реплікація. Видимі ураження розвиваються, коли вірус повертається до місця інокуляції по сенсорному нерву з наступною реплікацією в шкірі і руйнуванням епітеліальних клітин.
Коли організм господаря не може обмежити реплікацію вірусу, відбувається поширення інфекції нейрогенним, гематогенним та лімфогенним шляхом. Дисемінована інфекція найбільш часто виникає у новонароджених та осіб з порушеннями імунної системи. При генералізованих формах ГІ у внутрішніх органах утворюються вогнища коагуляційного некрозу (рис. 1). HSV проникають у реґіонарні нервові ганглії, де зберігаються протягом тривалого часу, можливо, довічно. HSV-1 частіше персистує в тригемінальних гангліях, HSV-2 – у вузлах крижового нерва.
У латентний період HSV-геном перебуває в неактивному стані. Вірусоносійство (латентна форма) – специфічна особливість ГІ. Активація вірусів пов’язана з недостатньою активністю макрофагів, Т-лімфоцитів-хелперів, цитотоксичних лімфоцитів, а також зменшенням вироблення медіаторів імунітету, в тому числі інтерферонів, інтерлейкінів. Зниження напруженості імунітету, яке може бути спровоковано різними факторами (стресом, гормональними порушеннями, інтеркурентними інфекціями, впливом ультрафіолетового опромінювання, проведенням імуносупресивної терапії), призводить до реактивації вірусів та виникнення рецидиву хвороби. Тяжкий перебіг ГІ часто спостерігається у дітей з дефіцитом клітинної ланки імунітету. ГІ відноситься до індикаторних хвороб СНІДу (внаслідок імунодефіцитного стану).
Герпетичний енцефаліт, спричинений HSV-1, виникає як при первинному інфікуванні (30%), так і при реактивації латентної інфекції (70%). Шляхи проникнення вірусів у мозок: гематогенний та невральний (ретроаксональний). Поширення вірусів у нервовій системі пов’язане з його проникненням у спинномозкову рідину. Первинна реплікація вірусів відбувається у мезенхімальних клітинах мозкових оболонок з подальшим ураженням нейронів і глії. HSV-1 уражає нейрони, астроцити, олігодендроглію, епітелій судин. Патологічні зміни призводять до некрозу клітин і запальної інфільтрації. Ці зміни переважно відбуваються в скроневих звивинах, медіально-базальних відділах лобної та тім’яних часток головного мозку. Таким чином, герпетичний енцефаліт – це некротичний енцефаліт (рис.1).
При енцефаліті, що спричинений HSV-2, зараження дитини відбувається частіше під час її проходження через пологові шляхи матері або трансплацентарним шляхом. Після проникнення вірусів у шкіру та слизові оболонки вони швидко потрапляють у кров та через гематоенцефалічний бар’єр у мозок. У головному мозку розвивається некротичний і запальний процес. Некрози локалізуються у сірій і білій речовині, часто мають дифузний характер і поширюються в глибокі шари мозку (рис. 1).
Класифікація герпетичної інфекції (Лебедев В. В. та ін., 2000)
За механізмом зараження:
1. Набута:
первинна
вторинна (рецидивуюча)
2. Вроджена (внутрішньоутробна інфекція).
За формою перебігу інфекційного процесу:
Латентна – безсимптомне вірусоносійство.
Локалізована.
Поширена.
Генералізована (вісцеральна, дисемінована).
За локалізацією ураження:
Шкіра: простий герпес, герпетиформна екзема, виразково-некротичний герпес, зостероформний герпес.
Слизові оболонки порожнини рота та рото глотки: стоматит, гінгівіт, фарингіт, тонзиліт.
Верхні дихальні шляхи: гостре респіраторне захворювання.
Очі: кератит, кератокон’юнктивіт, ірит, іридоцикліт.
Урогенітальні органи: уретрит, цистит, вульвовагініт, цервіцит.
Нервова система: менінгіт, енцефаліт, менінгоенцефаліт.
Внутрішні органи: езофагіт, пневмонія, гепатит, гломерулонефрит.
За тяжкістю перебігу захворювання:
Легка.
Середньотяжка.
Тяжка.
До первинних форм ГІ відносяться: ГІ новонароджених, енцефаліт, гінгівостоматит, герпетиформна екзема Капоші, первинний герпес шкіри, ока, герпетичний панарицій, кератит.
До вторинних (рецидивуючих форм) ГІ належать герпес шкіри та слизових оболонок, офтальмогерпес, герпес статевих органів.
Первинна ГІ виникає внаслідок першого контакту людини з HSV-1. Як правило, це відбувається у ранньому дитячому віці (до 5 років). У дорослих у віці 16–25 років первинна ГІ може бути обумовлена HSV-2. У 80–90% первинно інфікованих дітей перебіг захворювання латентний і тільки в 10–20% випадків спостерігаються його клінічні прояви.
Після інкубаційного періоду (2–14 днів) з’являється загальноінфекційний синдром з гарячкою та іншими симптомами інтоксикації. Найбільш частими проявами первинної ГІ, викликаної HSV-1, є гінгівостоматит з катаральними явищами у верхніх дихальних шляхах (рис. 4). Іншими проявами так званого орофаціального герпесу можуть бути ураження шкіри, кон’юнктиви та рогівки. HSV-2 частіше викликає генітальний герпес та герпес у новонароджених.
Вторинна (рецидивуюча) ГІ зустрічається у будь-якому віці і зумовлена реактивацією HSV. Рецидиви ГІ спостерігаються приблизно у третини хворих після перенесеної первинної інфекції, частота рецидивів може бути різною. Найбільш частими формами рецидивуючої ГІ є лабіальна та назальна. Рідше виникають рецидиви герпетичного панарицію. Рецидивуючий перебіг захворювання спостерігається у 30–40% хворих на офтальмогерпес та у 50–75% хворих на генітальний герпес.
Крім локалізованих форм ГІ, виділяють генералізовані форми: вісцеральні (гепатит, пневмонія, нефрит) та ураження ЦНС (енцефаліт, менінгіт, мієліт, полірадикулоневрит).
Ураження шкіри частіше спостерігається навколо рота (herpes labialis), носа (herpes nasalis) та вушних раковин (herpes oticum) (рис. 2).
Спочатку в цих місцях виникає помірне свербіння шкіри, печіння та біль. Через 1–2 дні з’являються дрібні з прозорим вмістом пухирці (везикули) на гіперемійованій основі, які розташовані групами. На 3–4-й день пухирці підсихають, на їхньому місці утворюються кірочки, які на 5–7-й день відпадають. Рубців звичайно не утворюється, але помітна незначна пігментація шкіри. Іноді пухирці зливаються, а потім лущаться з утворенням поверхневої ерозії, яка поступово загоюється без змін на шкірі. Можливий повторний висип на тому ж самому місці. В такому випадку термін загоювання подовжується до 2–4 тижнів.
Рисунок 2 – герпетичне зостероформне ураження шкіри у однієї дитини з локалізацією на кисті (А), лобі (В), нозі (С)
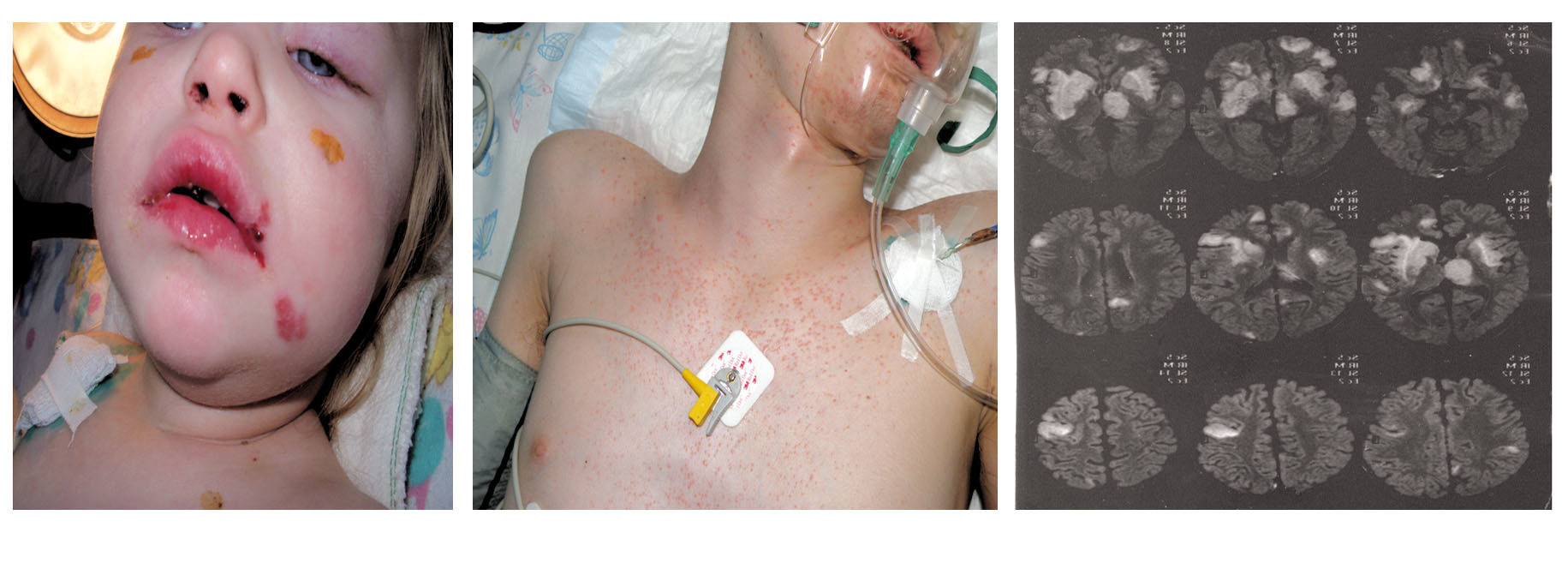 У дітей з дерматозами (екземою, нейродермітом тощо), з наявністю ерозивних уражень шкіри HSV може спричинити розвиток герпетичної екземи (вакциноформний пустульоз, герпетиформна екзема Капоші, варіоліформний пустульоз) (рис. 3). Частіше ця форма спостерігається у дітей раннього віку. Характерний гострий початок з підвищенням температури до 39–40оС та швидко прогресуючими симптомами токсикозу: млявість, блювання, судоми, короткочасна втрата свідомості. Рясний везикульозний висип з’являється вже у перший день хвороби на місцях, які уражені екземою, нейродермітом тощо. Спочатку пухирці заповнені прозорою рідиною, але через 2–3 дні їхній вміст стає каламутним, з’вляється пупкоподібне вдавлення в центрі. Далі пухирці можуть зливатися, лущитися, вкриватися суцільною кіркою. Після відпадіння корок залишається рожева пляма або рубцеві зміни. Відмічається регіонарний лімфаденіт. Перебіг хвороби тривалий, висип зникає через 2–3 тижні, але можливі повторні висипання. Ймовірне нашарування вторинної бактеріальної інфекції, що робить перебіг захворювання більш тяжким. В ослаблених дітей герпетична екзема характеризується особливо тяжким перебігом. В патологічний процес, крім шкіри, залучається також нервова система та вісцеральні органи, у зв’язку з чим може наступити летальний наслідок.
У дітей з дерматозами (екземою, нейродермітом тощо), з наявністю ерозивних уражень шкіри HSV може спричинити розвиток герпетичної екземи (вакциноформний пустульоз, герпетиформна екзема Капоші, варіоліформний пустульоз) (рис. 3). Частіше ця форма спостерігається у дітей раннього віку. Характерний гострий початок з підвищенням температури до 39–40оС та швидко прогресуючими симптомами токсикозу: млявість, блювання, судоми, короткочасна втрата свідомості. Рясний везикульозний висип з’являється вже у перший день хвороби на місцях, які уражені екземою, нейродермітом тощо. Спочатку пухирці заповнені прозорою рідиною, але через 2–3 дні їхній вміст стає каламутним, з’вляється пупкоподібне вдавлення в центрі. Далі пухирці можуть зливатися, лущитися, вкриватися суцільною кіркою. Після відпадіння корок залишається рожева пляма або рубцеві зміни. Відмічається регіонарний лімфаденіт. Перебіг хвороби тривалий, висип зникає через 2–3 тижні, але можливі повторні висипання. Ймовірне нашарування вторинної бактеріальної інфекції, що робить перебіг захворювання більш тяжким. В ослаблених дітей герпетична екзема характеризується особливо тяжким перебігом. В патологічний процес, крім шкіри, залучається також нервова система та вісцеральні органи, у зв’язку з чим може наступити летальний наслідок.
Рисунок 3 – герпетична екзема: герпетиформна екзема Капоші
Ураження шкіри при ГІ в деяких випадках може носити зостероформний, геморагічний, геморагічно-некротичний або виразково-некротичний характер (рис. 2).
Зостероформний герпес характеризується розташуванням висипу вздовж стовбурів нервів, частіше у ділянці обличчя, сідниць та нижніх кінцівок. Від Herpes zoster ця форма звичайного герпесу відрізняється відсутністю вираженого больового синдрому вздовж нервів (рис. 1).
При геморагічній формі пухирці мають кров’янистий вміст. Геморагічно-некротична форма характеризується появою некрозів на місці висипу.
Виразково-некротична форма, як правило, розвивається на фоні тяжкого імунодефіциту будь-якого генезу. У хворих на фоні типового висипу з’являються виразки, які досягають 2–5 см у діаметрі. Пізніше вони зливаються між собою у великі виразкові поверхні з нерівними краями. Такі ураження зберігаються протягом декількох місяців, їх зворотний розвиток відбувається повільно. Якщо виразково-некротичні прояви ГІ зберігаються більше трьох місяців, то їх відносять до СНІД-індикаторних захворювань.
Еритематозна, папульозна та набрякова є атиповими формами ГІ. При них везикули не утворюються, а з’являються гіперемія, дрібні папули, виникає набряк тканин. Часті рецидиви такої форми в одному й тому ж місці можуть бути причиною елефантіазу (елефантіазоподібний герпес).
Виділяють також абортивну форму ГІ, яка також відноситься до атипових форм. При цьому вхідними воротами часто є шкіра пальців рук та долоней. Типові везикули відсутні. Захворювання супроводжується свербінням шкіри, її набряком та гіперемією. В такому випадку іноді встановлюють діагноз «панарицій».
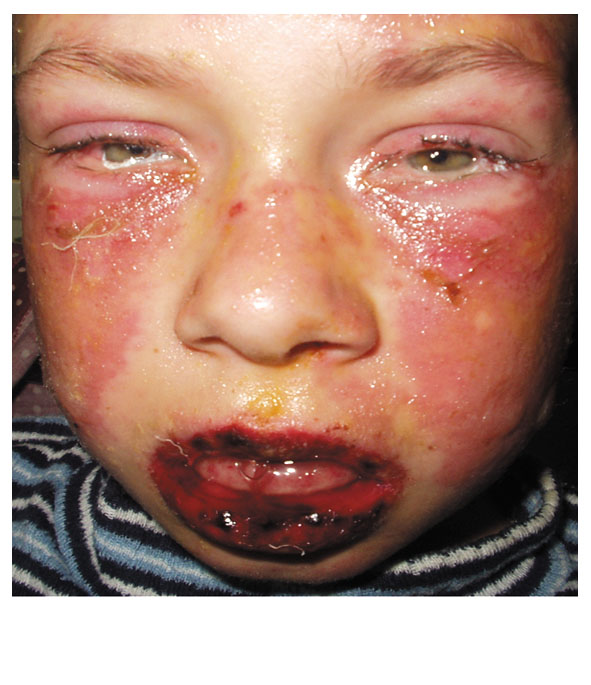
Ураження слизових оболонок ротової порожнини – найбільш часта форма первинного герпесу у дітей, що виникає у віці 6 міс. – 3 роки. Захворювання починається гостро з підвищення температури тіла до 39–40оС. Діти відмовляються від їжі, дуже неспокійні. На слизовій оболонці губ, щік, язика, ясен на фоні гіперемії та набряку з’являються дрібні пухирці, які швидко лопаються, утворюючи ерозії – афти (рис. 4).
Рисунок 4 – орофаціальний герпес: герпетичний гінгівостоматит, herpes labialis та herpes nasalis
Відмічається підвищене слиновиділення. Збільшуються та стають болючими при пальпації регіонарні підщелепні лімфатичні вузли. У 40% хворих в подальшому розвивається хронічний рецидивуючий герпетичний стоматит.
При ураженні HSV слизових оболонок верхніх дихальних шляхів виникає гостре респіраторне захворювання (ГРЗ), яке клінічно не відрізняється від такого іншої етіології. Така форма ГІ складає 5–7% всіх ГРЗ.
Ураження очей (офтальмогерпес) може бути первинним та вторинним (рецидивуючим). Більше 90% випадків припадає на рецидивуючий офтальмогерпес. Ураження очей при ГІ можуть бути поверхневими та глибокими. Поверхневі ураження переднього відділу ока характеризуються розвитком кон’юнктивіту (катарального, фолікулярного, везикульозно-виразкового), поєднаного ураження кон’юнктиви та повік – блефарокон’юнктивіту, каналікуліту, різноманітних кератитів (крапковий, везикульозний, деревоподібний, географічний). Можливий розвиток рецидивуючої ерозії рогівки, а також ізольованого ураження склери у вигляді дифузного епісклериту. При герпетичному кон’юнктивіті слизова оболонка повік, очного яблука гіперемійовані. Характерні помірна світлобоязнь та сльозотеча. Перебіг поверхневих герпетичних уражень очей, як правило, доброякісний.
Глибокі ураження переднього відділу ока характеризуються розповсюдженням інфільтрації в строму рогівки і перебігають у вигляді стромального кератиту, з утворенням виразки або без неї. В більшості випадків вони поєднуються із запаленням переднього відділу судинного тракту з розвитком кератоіридоцикліту, периваскуліту, флеботромбозу сітківки. Наслідками кератоіридоцикліту можуть бути помутніння рогівки та зниження гостроти зору. Іноді розвивається неврит зорового нерву. У новонароджених можуть розвинутися катаракта, хоріоретиніт або увеїт (рис. 5).
Рисунок 5 – герпетичне ураження ока – глибоке ураження переднього відділу ока HSV у вигляді двохбічного ретиніту
Генітальний герпес може бути зумовлений HSV-1 і HSV-2, його частіше діагностують у підлітків та дорослих при зараженні статевим шляхом. У дітей молодших вікових груп ураження статевих органів виникає вторинно після появи інших проявів ГІ. При цьому зараження відбувається через інфіковані руки, рушники, білизну. Клінічно генітальний герпес проявляється гіперемією та набряком статевих органів, везикульозним висипом на слизових оболонках статевих органів, на пігментованих ділянках геніталій, у перианальній ділянці, а також на шкірі сідниць, стегон. Пухирці швидко лускаються, утворюючи ерозивні або ерозивно-виразкові поверхні. Хвороба супроводжується свербінням, відмічається біль в уражених місцях, як правило, підвищується температура тіла. Появі висипань можуть передувати продромальні симптоми – біль, печія, свербіж. У дітей можуть спостерігатися виділення з піхви, уретри, іноді виникають уретрити. У імунокомпетентних осіб первинний геніальний герпес триває протягом 2-3 тижнів. У 50-75% хворих генітальний герпес має рецидивуючий перебіг, в більшості пацієнтів повторне захворювання виникає впродовж року, а характер клінічних проявів визначається станом імунної системи. В імунокомпетентних хворих можуть спостерігатися абортивні рецидиви, які проявляються свербінням, незначною гіперемією та набряком шкіри та слизових оболонок статевих органів без висипу та порушення загального стану. У дітей з вираженим імунодефіцитом рецидиви генітального герпесу супроводжуються тяжкими місцевими змінами ерозивно-виразкового характеру, поширенням процесу на промежину, піхву, шийку матки, уретру, сечовий міхур. У патологічний процес можуть бути втягнуті лімфатичні судини. При цьому вірогідний розвиток лімфостазу, який може призвести до слоновості статевих органів.
Герпетичний енцефаліт можуть викликати як HSV-1 так і HSV-2. Ураження мозку частіше ізольоване без ураження шкіри і слизових оболонок або може бути одним із синдромів генералізованої ГІ, яка спостерігається переважно у новонароджених і дітей раннього віку. Вважають, що у новонароджених етіологічним фактором є в основному HSV-2, а у дітей старшого віку та дорослих - HSV-1. Пік захворюванності на герпетичний енцефаліт, зумовлений HSV-1, приходиться на два вікові періоди - від 6 міс. до 5 років і старше 40 років, а HSV-2 – на 3-14 й день після народження (рис. 6).
Рисунок 6 – герпетичний енцефаліт. А- у дитини К., 5 років; В – у дитини С. 14 років.
При найбільш типовому перебігу герпетичного енцефаліту виділяють 5 періодів:
Загальноінфекційний (1-21 день) - підвищення температури тіла, катар верхніх дихальних шляхів, можливий пухирцевий висип на шкірі та слизових оболонках.
Енцефалічний (1-10 днів) – головний біль, блювання, психічне збудження, марення, галюцинації, афазія, апраксія, агнозія, пірамидні розлади.
Енцефалітичний (коматозний) (1-50 днів) – розлади свідомості, судоми, ознаки коми.
Ранньої реконвалесценції (1-12 місяців) – ретроградна і фіксаційна амнезія, апраксія, втрата набутих навичок, агнозія, регрес у фізичному розвитку.
Залишкових явищ (місяці-роки) – психічні розлади, гіперкінези, парези кінцівок.
Гострий енцефаліт виникає в результаті первинного інфікування, реінфікування чи на фоні активації хронічної герпетичної інфекції. Початок енцефаліту часто співпадає з рецидивом герпесу шкіри та слизових оболонок або після контакту дитини з дорослими із загостренням герпесу шкіри, слизових оболонок.
Загальноінфекційний період енцефаліту супроводжується катаром верхніх дихальних шляхів, підвищенням температури тіла до 380-400С, інтенсивним головним болем, блюванням. Протягом 2-21 днів загальноінфекційний період переходить у енцефалічний. В цей час у дітей наростає головний біль, посилюється блювання, виникає психомоторне збудження. У частини дітей захворювання перебігає за типом інфекційного психозу з мареннями, галюцинаціями. У 3/4 дітей відмічаються коркові порушення, які проявляються як сенсорна афазія Верніке, апраксія (втрата набутих навичок), агнозія (не впізнає оточуюче середовище, батьків), пірамидні розлади, гіперкінези (тремор, стереотипні рухи), підвищення тонусу м’язів. Одними з перших симптомів герпетичного енцефаліту можуть бути генералізовані судоми чи міоритмії (ритмічні скорочення дрібних м’язів навколо рота чи ока).
Наявність у 70%-75% хворих на герпетичний енцефаліт характерних коркових розладів дає можливість його запідозрити до розвитку коми і максимально рано розпочати етіотропну терапію.
Протягом наступних 2-10 днів з’являються легкі розлади свідомості від психічного збудження до легкого сопора, генералізовані клоніко-тонічні судоми, менінгеальні симптоми. У частини хворих енцефалічний період може бути відсутній, захворювання починається одразу з появи загальномозкових та вогнищевих симптомів.
Тривалість енцефалітичного періоду може бути різною: від декількох днів до двох місяців. Основними проявами цього періоду є розлади свідомості різного ступеня, судоми. Також з’являються вогнищеві симптоми: парези, переважно спастичного характеру, ураження черепних нервів, переважно VII пари, розлади дихання, бульбарні порушення.
Після виходу з енцефалітичного періоду у дітей відмічають адинамію, яка чергується з періодами збуждення, а також ретроградну і фіксаційну амнезію, апраксію, агнозію. Відновлення проходить протягом 1-12 міс.
Можливий так званий псевдотуморозний варіант герпетичного енцефаліту, коли при нормальній чи субфебрильній температурі тіла поступово протягом декількох тижнів наростають симптоми ураження ЦНС, ознаки внутришньочерепної гіпертензії, з’являються зміни на очному дні.
Поряд з описаними формами герпетичних енцефалітів виділяють інсультоподібний, стовбуровий, енцефаломієлітичний та деякі інші варіанти.
При герпетичному енцефаліті не завжди виникають запальні зміни в спинномозковій рідині, але можливе поєднане ураження мозку і мозкових оболонок. Тоді в клінічній картині захворювання відмічається виражений менінгеальний синдром, а в лікворі визначають запальні зміни.
Летальність при герпетичному енцефаліті без противірусного лікування становить 60-70%, з лікуванням – 15-20%. Залишкові явища у вигляді грубого органічного дефекту (апалічний синдром, деменція, епілептичні напади, парези, гіпертензивно-гідроцефальний синдром та інше) розвиваються відповідно у 90% та 10-15% випадків. Існує пряма залежність наслідків захворювання від строків початку лікування: при ранньому призначенні препаратів ацикловіру наслідки значно покращуються.
Герпетичний менінгіт перебігає як серозний, асептичний і часто поєднується з первинним генітальним герпесом. В загальній структурі серозних менінгітів питома вага герпетичного складає 10%. Менінгеальний синдром при ньому зберігається досить довго. Плеоцитоз змішаний або лімфоцитарний з домішками еритроцитів. Герпетичний менінгіт має затяжний перебіг, при ньому існує загроза виникнення таких ускладнень як енурез, полірадикулонейропатія, мієліт.
Герпетичний мієліт рідко зустрічається як самостійна форма, частіше як синдром поєднаного ураження центральної та периферичної нервової системи. Домінують сегментарні або провідникові симптоми. Герпетичний енцефаломієліт може починатися з оніміння та пекучості в кінцівках, болей у попереково-крижовому відділі, гіперестезії, слабкості ніг, порушення ходи, функції органів таза. Потім приєднуються пірамідні знаки, парези верхніх кінцівок, спастичні парези ніг переходять у змішані або в’ялі, уражується стовбур мозку у вигляді парезів ІІІ-ІV, VІІ-VІІІ і ХІ-ХІІ пар черепних нервів. Кінцева стадія характеризується розладами дихання внаслідок ураження ядер мозкового стовбура або спинного мозку. Розлади свідомості незначні.
Вісцеральні форми ГІ проявляються гострим паренхіматозним гепатитом, пневмонією, нефритом. Частіше вони спостерігаються у новонароджених, але можуть бути і у дітей старшого віку.
Герпетичний гепатит частіше буває проявом первинної ГІ у новонароджених та дітей перших місяців життя. Він супроводжується високою лихоманкою, вираженими симптомами інтоксикації, блюванням, збільшенням печінки, селезінки, жовтяницею, геморагічним синдромом. Часто має тяжкий перебіг з вираженим холестазом та розвитком гострої печінкової енцефалопатії, печінкової недостатності, можливий летальний наслідок.
Герпетична пневмонія та вогнищевий нефрит клінічно не відрізняються від ураження легень та нирок іншої етіології.
Перебіг ГІ лише у 15-20% хворих буває гострим, а у більшості спостерігаються рецидиви захворювання. Рецидиви виникають під впливом різних стресових факторів: переохолодження, перегрівання, вірусних та бактеріальних інфекцій тощо. Клінічні прояви при рецидивах такі ж самі, як і при гострих форм.
У дітей старшого віку із скомпроментованою імунною системою виділяють хронічну генералізовану форму ГІ, яка характеризується підгострим перебігом, повільним наростанням головного болю, субфебрильною лихоманкою, загальною слабкістю, сниженням пам’яті.
Герпес у ВІЛ-інфікованих розвивається частіше в результаті активації латентної герпетичної інфекції. При цьому захворювання набуває генералізованого характеру. Ознаками генералізації є поширення вірусу по слизових оболонках із порожнини рота на слизові оболонки стравоходу, трахеї, бронхів з наступним виникненням герпетичної пневмонії, а також розвиток хоріоретиніту, менінгоенцефаліту. Герпетичний висип не зникає, а на його місці формуються виразки на шкірі. ГІ у ВІЛ-інфікованих не має тенденції до самовільного виліковування.
HSV може передаватися від матері до дитини у внутрішньоутробному періоді, під час пологів або постнатально. При антенатальній передачі вірусу можливий широкий спектр клінічної картини від локальних ушкоджень очей чи шкіри до поліорганних уражень чи природжених аномалій. Найвищий ризик трансмісії вірусу виникає під час вагінальних пологів, цей шлях інфікування відмічають у 85%-95% випадках зараження HSV. Дитина, проходячи через пологовий канал, контактує з інфікованим секретом пологових шляхів. Вірус проникає через слизові оболонки ротогорла, очей, через пошкоджену шкіру при використанні інвазивного моніторингу чи інших інструментальних втручаннях. На внутрішньоутробне інфікування (трансплацентарне, висхідне проникнення вірусу з цервікального каналу) припадає не більше 5-8% від усіх заражені HSV. Постнатальне зараження настає у 8-10%, джерелом інфекції є вірусоносії – члени родини чи медичний персонал.
Інфекція у новонароджених виникає внаслідок прямого інфікування, яке відбувається найбільш часто в перинатальний період від герпетичного геніального захворювання матері. Вірус може викликати локалізовані ураження шкіри, очей, рота з поширенням від клітини до клітини контактним шляхом, або демсимінуватися за рахунок віремії. Після абсорбції і пенетрацї до клітин господаря наступає реплікація вірусу, яка призводить до набряку клітини, геморагічного некрозу, появі внутрішньоклітинних включень, цитолізу та набряку клітин.
До чинників ризику зараження HSV відносять:
Генітальний герпес у матері під час 3-го триместру вагітності,
Реактивація латентної HSV 2-го типу у пологах,
Інвазивні акушерські процедури,
HSV серологічні відмінності у батьків (HSV серонегативна мати і HSV серопозитовний батько),
Тривалий безводний період,
Вагінальні пологи (порівняно з Кесаревим розтином).
При внутрішньоутробному інфікуванні HSV у новонароджених спостерігається тріада симптомів – везикули на шкірі або рубці на місці везикул, ураження очей (хоріоретиніт, кератоконюктивіт), мікроцефалія чи аненцефалія.
Неонатальна HSV інфекція виникає до 4 тижня життя дитини. Захворювання новонародженого може виявлятися, як: інфекція, локалізована на будь-яких ділянках шкіри, очей, рота (до 40% всіх випадків); ураження ЦНС – герпетичний енцефаліт (до 35%), десимінована інфекція з втягненням у патологічний процес низки органів і систем (приблизно у 25%). Клінічні прояви HSV інфекції у новонародженого залежать від вхідних воріт та від інтенсивності. Дискутується питання щодо безсимптомного перебігу інфекції у немовлят, яка не має віддалених наслідків. У багатьох немовлят, які мають десиміновану форму захворювання чи ураження ЦНС може не бути висипань на шкірі або везикулярний висип з’являється пізніше, від інших симптомів недуги, що викликає певні діагностичні труднощі. Неонатальну HSV інфекцію слід завжди запідозрювати у дітей, які захворіли до 3-х тижневого віку.У численних літературних джерелах наголошується, що протягом останніх 20 років (1987-2007), незважаючи на значні прогрес у діагностичному процесі, не відмічено зменшення інтервалу між першими симптомами захворювання і початком противірусної терапії (який становив і становить в середньому 6 днів), хоча багатьма дослідженнями доказано, що раннє і своєчасне призначення ацикловіру сприяє значно кращим наслідкам захворювання.Інфекційне ураження шкіри, очей, рота виникає приблизно у 40% інфікованих немовлят.
Типовою ознакою є поява міхурців протягом 6 – 9 дня життя дитини, які з’являються на шкірі чи слизових оболонках у місці попадання вірусу. Якщо у дитини були невеликі травми шкіри в пологах то елементи висипу першочергово з’являються в цих місцях. Через декілька днів висипання поширюються й на інші частини тіла. Захворювання супроводжується порушенням загального стану дитини, маніфестацією клінічних симптомів проте прогнозом є більш сприятливим, ніж при інших формах герметичної інфекції. Висип характеризується численними згрупованими, кластерними (багатокамерними) везикулами, хоча зустрічаються і везикули, розташовані окремо. Везикули виникають на місці гіперемії шкіри і звичайно їх діаметр становить 1-2 мм. Іноді вони можуть зливатися у великі булли, розміром більшим від 1 см. Практично у всіх пацієнтів, незважаючи на лікування противірусними препаратами, висипання мають схильність до рецидивів, які повторюються аж до 6 місячного віку (а інколи і довше). Локалізована інфекція орофарингіальної порожнини трапляється у 10% дітей з герпетичною інфекцією. Ураження очей може бути єдиним проявом HSV інфекції. Герпетичне ураження очей протікає як кератоконюктивіт, який, особливо при рецидивах, може прогресувати до хоріоретиніту, катаракти, відшарування сітківки, цей процес часто не залежить від проведеного дитині лікування. Крім кератоконюктивіту при офтальмологічному дослідженні у деяких пацієнтів можна виявити мікроофтальмію і дисплазію ретини. Незважаючи на виключно локальні ураження загальний стан немовлят може бути порушеним, в подальшу в 10%-30% дітей можна спостерігати різноманітну неврологічну симптоматику, затримку психомоторного розвитку. Частота неврологічних ускладнень може бути значно вищою у дітей з рецидивами висипань на шкірі, слизових протягом перших трьох місяців життя, а також у немовлят з позитивними результатами визначення HSV ДНК у лікворі в останні дні противірусної терапії. До віддалених неврологічних проявів при локальних формах інфекції відносять спастичну тетраплегію, мікроцефалію, сліпоту.
Патогенетичні механізми розвитку цих ускладнень невідомі. Незважаючи на відсутність неврологічних симптомів у розпал герпетичного пораження шкіри чи очей погіршення настає у період між 6 - 12 місячним віком. Перебіг захворювання нагадує перинатально набуті сифіліс чи токсоплазмоз. Найважче діагностувати HSV енцефаліт, оскільки багато немовлят не мають типових висипань на час маніфестації симптомів ураження ЦНС. Герпетичну інфекцію слід запідозрювати у новонароджених, у яких виражену картину органічного пошкодження мозку з судомами при відсутності внутрішньошлуночкових крововиливів або важких метаболічних порушень. Зростання плеоцитозу і рівня протеїну в лікворі при негативних результатах бактеріологічного обстеження передусім свідчить про герпетичне ураження ЦНС. У випадках генералізованої HSV інфекції дитина переважно народжується передчасно. Клінічні симптоми захворювання розвиваються у 20% немовлят з неонатальною HSV інфекцією і виникають протягом перших 7-10 днів життя. До основних синдромів відносять гіпертермічний синдром, підвищену збудливість, судоми, респіраторний дистрес, жовтяницю, геморагічний синдром і везикулярну екзантему, яку розцінюють як патогномонічний симптом захворювання. Вторинна віремія призводить до численних уражень внутрішніх органів: легень, наднирників. Можуть виникати ураження гортані, трахеї, стравоходу, шлунку, нижніх відділів ШКТ, селезінки, нирок, підшлункової залози, серця, у більшості хворих (60-75%) виявляють енцефаліт. Діагностичні труднощі часто виникають при відсутності типового висипу на шкірі чи слизових оболонках, оскільки за клінічним перебігом і симптомами неонатальний герпес нагадує сепсис. Загрозливими для життя є ураження печінки, наднирників, HSV пневмоніти, ДВЗ синдром. При неадекватній терапії смертність сягає до 80%.
Дані лабораторних досліджень часто дозволяють встановити ураження певних органів чи систем – печінки (ріні білірубіну, АсАТ, АлАТ), ЦНС (дослідження ліквору, ЕЕГ, методи візуалізації), легень (рентгенографія), крові (за показниками кількості лейкоцитів, факторами згортання крові). Рентгенологічні зміни при HSV ураженні легень характеризуються дифузним ураженням інтерстиціальної тканини з подальшою трансформацією у геморагічний пневмоніт.
Для діагностики локальних уражень ЦНС важливими анамнестичні дані про повторні епізоди герпесу у матері, оскільки антитіла, які передаються траснплацентарно попереджують процесу десимінації вірусу але не запобігають інтраневральній реплікації вірусу з його поширенням по нервових стовбурах до мозку (т.з. ретроградний аксональний шлях поширення). Клінічні симптоми розвиваються пізніше, ніж при десимінованому перебігу захворювання (між 10 – 28 днем життя дитини, іноді неврологічні симптоми можуть вперше виявити і після 6-ти тижневого віку). Неврологічні прояви досить різноманітні, спостерігається млявість, сонливість, зниження апетиту, нестабільна температура тіла, гіпотонія м’язів, проте основними симптомами є судоми. Характерними змінами ліквору є лімфоцитоз, підвищений вміст білка і часто знижений рівень цукру. При цьому варіанті хвороби реєструють високу летальність, яка при ефективному лікуванні сягає 15%, а в третини дітей, які вижили описано розвиток відділених ускладнень – гідроцефалії, мікроцефалії, сліпоти, хоріоретиніту, поренцефалічних кист, спастичних парезів, паралічів, різні ступені затримки психомоторного розвитку.
Мозок новонароджених більш сприйнятливий до виникнення прогресуючих уражень, до вірусних емболізацій, порівняно з мозком дорослих, при HSV енцефалітах більш часто ушкоджуються темпоральні і паріетальні відділи мозку. Як при бактерійних або грибкових менінгітах результат захворювання часто залежить від своєчасної діагностики і своєчасно розпочатого лікування. Інфекційне ураження мозку може виникати як компонент мультиорганного пораження при генералізованій інфекції чи як енцефаліт з (або без) герпетичними ураженнями шкіри, очей, слизової ротової порожнини. Приблизно 1/3 дітей з неонатальною HSV мають лише симптоми енцефаліту. Маніфестація енцефалітів включає судоми (фокальні, генералізовані), летаргію, подразливість, тремор, температурну лабільність, вибухання тім’ячка, симптоми ураження пірамідного тракту. HSV вдається виділити з ліквору хворих дітей у 25-40%. Характерними змінами ліквору є плеоцитоз і протеїнозом. Високоінформативними є дослідження ліквору в динаміці декілька разів, оскільки для герпетичних енцефалітів характерним є прогресивне зростання рівня білка в лікворі. Електроенцефалографія, КТ, МРТ є достатньо інформативними дослідженнями при герпетичних енцефалітах. При герпетичних енцефалітах на ЕЕГ зміни (періодичні латеризаційні епілептоподібні спалахи) виявляються в темпоральних ділянках мозку. В цих же відділах мозку при МРТ можна встановити набряк, геморагічний некроз з втягненням білої речовини мозку.
Смерть дитини, яка найбільш часто зумовлена ураженням стовбуру мозку, настає приблизно в 50% дітей з вірусними енцефалітами, які не отримували належного лікування
Віддалений прогноз герпетичної інфекції при ураженнях ЦНС і при генералізованому перебігу як правило несприятливий. До 75% дітей з цими ураженнями мозку мають затримку психомоторного розвитку, яка пов’язана з мікроцефалією, гідроцефалією, поренцефалічними кистами, спастичними парезами, сліпотою. До кінця не зрозумілим є патогенез цих змін, які пояснюють і безпосереднім впливом вірусу на нейрони мозку і як наслідок імунологічних реакцій організму, які скеровані на вивільнення макроорганізму від вірусів.
Лабораторна діагностика ГІ
Найбільш специфічним методом є ідентифікація HSV на клітинах курячих ембріонів і лабораторних тваринах при їх зараженні інфікованим матеріалом хворого (вміст везикул, змиви з носоглотки, спинномозкова рідина тощо). Але цей метод не отримав широкого застосування через трудомісткість, тривалість культивування та високу вартість. Для швидкої діагностики проводять імуноферментний аналіз (ІФА), який виявляє специфічні антитіла IgM та IgG в крові хворого. Виявлення антитіл класу М свідчить про гостре захворювання, реінфекцію або загострення латентної інфекції. Проте, цей імуноглобулін з’являється в сироватці крові лише на 10-14-й день хвороби, що зменшує його діагностичне значення. Наявність антитіл класу IgG в крові свідчить про хронічну інфекцію, персистенцію вірусу в організмі, а чотириразове зростання титру IgG в динаміці вказує на активацію ГІ. Геном HSV в крові, лікворі, слині чи інших середовищах організму виявляють за допомогою полімеразної ланцюгової реакції (ПЛР). За чутливістю та специфічністю ПЛР не поступається методу вірусологічного дослідження, але значно випереджає його за швидкістю.
Лікування ГІ
За даними Gershburg Е., Pagano J.S. (2005) всі сучасні противірусні препарати для лікування ГІ можуть бути розділені на дві групи:
I. Сполуки, що пригнічують активність РНК-, ДНК-полімерази герпесвірусів:
ациклічні аналоги нуклеозидів (АНА) - ацикловір, ганцикловір, пенцикловір, валацикловір, валганцикловір, фамцикловір, валганцикловір;
ациклічні аналоги нуклеотидів - цидофовір, адефовір;
аналоги пірофосфатів - фоскарнет (фоскавір), фосфоноацетилова кислота;
4 оксо-дигідрохіноліни.
ІІ. Різні сполуки, що не інгібують вірусну РНК-, ДНК-полімеразу (механізм їхньої дії вивчається): марибавір, бета-L-5 урацил йододіоксолан, індолокарбазол.
Ісаков В.А. (2013) пропонує наступну класифікацію противірусних препаратів для лікування та профілактики герпесвірусних інфекцій:
Застосування противірусної терапії ГІ розпочалося у 70-ті роки ХХ ст. з використання першого специфічного протигерпетичного препарату відарабіну. Але цей препарат виявляв значну нейро-, гепато- та гемотоксичність. З 1982 р. почалося впровадження в клінічну практику ацикловіру, що суттєво підвищило ефективність лікування ГІ. Ацикловір пригнічує синтез вірусної ДНК. В інфікованих клітинах він активується під дією вірусної тимідинкінази з утворенням ацикловіртрифосфату, який має більш високий ступінь споріднення з вірусною ДНК-полімеразою, ніж з клітинною, і тому конкурентно блокує вірусну ДНК-полімеразу. Неінфіковані клітини продовжують своє нормальне функціонування.
Встановлено, що при рецидивуючому герпесі шкіри та слизових оболонок ацикловір ефективний тільки під час загострення запального процесу, але препарат не запобігає виникненню рецидивів хвороби. Це пов’язане з тим, що ацикловір блокує тільки активну реплікацию вірусу, яка після його відміни може відновлюватися.
Для лікування герпетичних уражень шкіри та слизових оболонок використовують ацикловір у таблетках, мазі або гелю.
Ацикловір добре проникає через гематоенцефалічний бар’єр, тому високоефективний при герпетичних енцефалітах. Його призначають хворим в дозі 10-15 мг/кг маси тіла кожні 8 годин внутрішньовенно протягом 10-14 днів, у подальшому - перорально по 200 мг 5 разів на добу дітям старше 2 років протягом 2-3 тижнів. Дострокове припинення терапії ацикловіром може сприяти рецидиву герпетичного енцефаліту. Раннє використання ацикловіру при герпетичних енцефалітах знижує летальність при них до 20% проти 60-70% без його застосування, та зменшує кількість залишкових явищ з 50% до 10-15%. Ефективне внутрішньовенне використання ацикловіру при лікуванні генералізованих форм ГІ у новонароджених, що наполовину зменшує кількість несприятливих наслідків.
При офтальмогерпесі ацикловір мало ефективний. Тому доцільно використовувати інші протигерпетичні засоби, такі, як ідоксуридин, трифлуридин.
При лікуванні генітального герпесу рекомендується застосування ацикловіру, валацикловіру, фамцикловіру, ідоксуридину. Достатня ефективність противірусних препаратів при цьому відмічена тільки при призначенні їх не пізніше третього дня від початку захворювання.
В комплексній терапії хворих з ГІ крім противірусних засобів слід застосовувати імунобіологічні препарати, які сприяють нормалізації клітинної та гуморальної ланок імунітету, активують неспецифічні фактори захисту.
Ефективність лікування новонароджених з герпетичною інфекцією залежить від часу призначення противірусної терапії. Лікування повинно проводитися дітям при всіх формах неонатального герпесу. Для новонароджених, у яких є типові везикулярні елементи слід призначити противірусну терапію не очікуючи лабораторного підтвердження HSV інфекції. Дітям з локальними формами – захворюваннями шкіри, очей, рота призначається ацикловір в дозах 10-15 мг/кг кожні 8 годин, протягом 10-14 днів, при герпетичних ураженнях ЦНС і при десимінованих формах захворювання – курс лікування ацикловіром триває 21 день у тих самих дозах.
Профілактика
При гострій формі ГІ дітей треба ізолювати до окремих палат. Дітей з дерматитами, екземою, імунодефіцитними станами, СНІДом, а також тих, хто отримує імуносупресивну терапію, необхідно ізолювати від хворих з ГІ. Обмежити цілування дітей першого року життя, також контакт дітей з хворими на рецидивуючий герпес шкіри та слизових оболонок. Персонал пологових будинків, жіночих консультацій, онкогематологічних відділень та відділень імунодефіцитів та СНІДу на час рецидиву в них герпесу шкіри чи слизових оболонок не допускається до роботи.
При першому або повторному епізоді герпетичної інфекції у вагітної рекомендовано проводити пологи шляхом кесаревого розтину (після спонтанного розриву оболонок Кесарів розтин проводять до 4 год безводного періоду).
Якщо мама страждає на герпетичну інфекцію статевих органів, при активації інфекції під час пологів чи без активації її слід ретельно спостерігати за появою симптомів інфекції у новонароджених – везикулярні висипання, респіраторний дистрес, судоми, симптоми, які нагадують сепсис. При підозрі на інфекцію чи позитивних результатах дослідження на HSV призначають ацикловір.
Список літератури:
- Исаков В.А., Архипова Е.И., Исаков Д.В. Герпесвирусные инфекции человека: руководство для врачей /под редакцией В.А. Исакова.-СПб.: СпецЛит, 2013.-2-е изд., перераб. и доп.-670 с.:ил.
- Principles and practice of pediatric infectious diseases / Ed. by S.S. Long, L.K. Pickering, C.G. Prober // Churchill Livingstone Inc. 1997. - P. 1821
- Crawford D.H. // Philos Trans R Soc Lond B Biol sci. 2001. Vol. 356, № 1408. p. 461-473.
- Иммунология вирусных инфекций у детей. Учебное пособие /под ред. Н.В. Скрипченко.- СПб., 2011.-40 с
- Kopf S., Tonshoff B. // Pediatr. Nephrol. — 2004. — V. 19, N 4. — P. 365—368.
- Зуев В.А. Медленные вирусные инфекции, 1988 г.
- Straus S.E. // J. Infect. Dis. – 1988. – V. 157, N 3. – P. 405—412.
- Kimura H., Morishima T., Kanegane H. et al. // J. Infect. Dis. — 2003. — V. 187. — P. 527—533.
- Інфекційні хвороби в дітей. За ред. професора С.О. Крамарьова і професора О.Б. Надраги / К.:ВСР «Медицина».- 2010. – 392 с.

Сепсис новорожденных. Частина 1. Актуальність проблеми, визначення поняття, класифікація, фактори ризику
Системні бактеріальні інфекції на теперішній час є вагомою причиною захворюваності і смертності новонароджених, а септицемія з доведеною бактеріємією посідає перше місце у загальній структурі нозокоміальних інфекцій новонароджених усіх вагових груп [1, 2]. Кожен рік до 1,6 млн. новонароджених помирають від сепсису [3]. Частота сепсису та інших бактеріальних інфекцій становить від 2 до 10 випадків на 1000 живонароджених. Частота випадків лабораторно підтвердженого раннього неонатального сепсису становить близько 1 на 1000 народжених живими у розвинутих країнах і близько 3 на 1000 народжених живими у лікарнях країн, що розвиваються [2, 4, 5].
ДетальнішеЩо потрібно знати лікарю про вакцинацію
Частина 1. Основні нормативно-правові документи, що регламентують проведення імунопрофілактики в Україні.
Вакцинація в Україні проводиться у відповідності до чинних законів України та Наказів Міністерства Охорони здоров’я України. Знання та виконання статей цих законів та наказів забезпечує як право громадян, так і юридичний захист медичних працівників при виконанні своїх обов’язків. Усім добре знайома теза про те, що незнання законів (читай – в тому числі і наказів профільного міністерства) не звільняє від відповідальності. На превеликий жаль, медичні працівники, як правило, не ознайомлені з рядом законів та наказів, що так чи інакше стосуються імунопрофілактики.
Детальніше
Неонатальна енцефалопатія та неврологічні наслідки. Видання друге
У першій редакції цього звіту Цільова група з вивчення неонатальної енцефалопатії та ДЦП виклала критерії, які вважаються необхідними для встановлення причинного зв'язку між подіями гіпоксії у пологах і церебральним паралічем. На даний час відомі кілька причин, які призводять до виникнення церебрального паралічу в доношених дітей (див. рис. 1). Ознаки і симптоми неонатальної енцефалопатії можуть варіюватися від легких до тяжких, залежно від характеру та термінів виникнення ураження мозку.
Детальніше
Расстройство с дефицитом внимания и гиперактивностью у детей в практике врача первого контакта
Синдром дефицита внимания и гиперактивности является хроническим психическим расстройством, которое проявляется гиперактивностью и импульсивностью в сочетании с невнимательностью, приводящими к стойкой социальной или школьной дезадаптации. Это расстройство имеет целый ряд социально значимых негативных последствий, таких как формирование оппозиционно-вызывающего или асоциального поведения, развитие зависимости от психоактивных веществ, тревожно-депрессивных расстройств, а также увеличение детского травматизма.
Детальніше
Заради простоти. Оптимізація анатомо-морфологічного обстеження серця плода при скринінговому УЗ-дослідженні у ІІ триместрі вагітності
Аномалії серця та магістральних судин зустрічаються з частотою від 7 до 17 на 1000 новонароджених. Ця патологія привертає увагу дослідників у всьому світі не лише у зв’язку із високою частотою, але й тому, що вона є причиною перинатальних втрат і посідає перше місце у структурі смертності від вад розвитку у ранньому неонатальному періоді.
Детальніше