По материалам научно-практической конференции с международным участием (Актуальные вопросы акушерства, гинекологии и перинатологии, Судак 2013)
 В рамках состоявшегося мероприятия заведующая кафедрой акушерства и гинекологии лечебного факультета №2 РНИМУ им. Н. И. Пирогова, доктор медицинских наук, профессор Юлия Эдуардовна Доброхотова рассказала о возможностях сохранения репродуктивной функции у женщин с миомой матки и поделилась собственным опытом применения эмболизации маточных артерий в лечении этой патологии у 1495 пациенток.
В рамках состоявшегося мероприятия заведующая кафедрой акушерства и гинекологии лечебного факультета №2 РНИМУ им. Н. И. Пирогова, доктор медицинских наук, профессор Юлия Эдуардовна Доброхотова рассказала о возможностях сохранения репродуктивной функции у женщин с миомой матки и поделилась собственным опытом применения эмболизации маточных артерий в лечении этой патологии у 1495 пациенток.
— Миома матки – наиболее распространенное заболевание у женщин, и, к сожалению, оно выявляется все чаще. Существуют различные варианты лечения миомы матки, в т. ч. хирургические, медикаментозные. В последние десять лет достаточно широко применяется такой метод как эмболизация маточных артерий (ЭМА). Каждый из вышеперечисленных методов лечения обладает как преимуществами, так и недостатками.
Так, гистерэктомия относится к типу вмешательств «нет органа – нет проблем». Этот метод неприемлем для женщин, желающих сохранить матку и выполнить репродуктивную функцию, а также сопровождается развитием постгистерэктомического синдрома.
При миомэктомии репродуктивная функция сохраняется, однако риск рецидива составляет 30–35%. Кроме того, одним из осложнений миомэктомии является развитие спаечного синдрома. Для медикаментозного лечения применяются агонисты гонадотропин–рилизинг–гормона короткими курсами либо в качестве предоперационной подготовки. Антипрогестины, к которым относится мифепристон, часто вызывают «прорывные» кровотечения.
В случае ЭМА сохраняется и иногда восстанавливается функция репродуктивной системы, наблюдается значительный регресс узлов, при этом риск развития рецидивов крайне низок (<1%).
Первый опыт ЭМА при послеродовых и послеоперационных кровотечениях принадлежит Oliver и соавт. (1979). В 1991–1994 гг. J. Ravina и соавт. опубликовали результаты применения метода в качестве предоперационной подготовки. В России данный метод используется с 1998 г., и в 2006 г. приказом МЗСР РФ эмболизация маточных артерий была включена в список высокотехнологичных вмешательств. Показаниями к применению ЭМА являются клинические ситуации, требующие оперативного лечения, а также сочетание миомы с невынашиванием или бесплодием независимо от размеров узлов. Противопоказания к проведению эмболизации включают воспалительные заболевания, беременность, подозрение на саркому матки, непереносимость контрастного вещества. Кроме того, процедура не проводится при определенных особенностях кровоснабжения яичников и изолированно как один метод лечения при субмукозных, субсерозных узлах на ножке.
Эффективность ЭМА обусловлена особенностями кровоснабжения узлов, а именно наличием перифиброидного сплетения, в котором сосуды узла оканчиваются слепо. После процедуры развивается постэмболизационный синдром, что обусловливает невозможность ее осуществления амбулаторно – требуется госпитализация на 2–3 дня. Постэмболизационный синдром проявляется, прежде всего, выраженными болевыми ощущениями, повышением уровня лейкоцитов в крови, лихорадкой. Согласно нашим наблюдениям, через несколько часов или дней после ЭМА в кровяных выделениях обнаруживаются частички эмболизирующего вещества, что свидетельствует о постепенном восстановлении кровотока в миометрии и эндометрии.
Относительно клинических результатов эмболизации наблюдалось устранение или значительное уменьшение клинических проявлений заболевания в течение 6 месяцев, в том числе меноррагии – в 96,5% случаев, учащенного мочеиспускания, чувства тяжести и диспареунии – в 100% случаев, при этом ни в одном случае новые узлы не появлялись.
Эффект ЭМА при миоме матки развивается за счет уменьшения размеров матки, миграции и размягчения узлов. В первые полгода после вмешательства в среднем на 50% уменьшается объем лидирующего миоматозного узла и матки в целом. Субсерозные узлы 2 типа переходят в узел первого типа и затем – нулевого типа, что облегчает последующее хирургическое вмешательство и делает его менее травматичным. Аналогичный эффект наблюдается и при субмукозных узлах. Кроме того, за счет выраженного размягчения узлов становится возможным удаление узлов размером 10–12 см при обычном расширении цервикального канала. В некоторых случаях наблюдается самостоятельная экспульсия уменьшенных узлов.
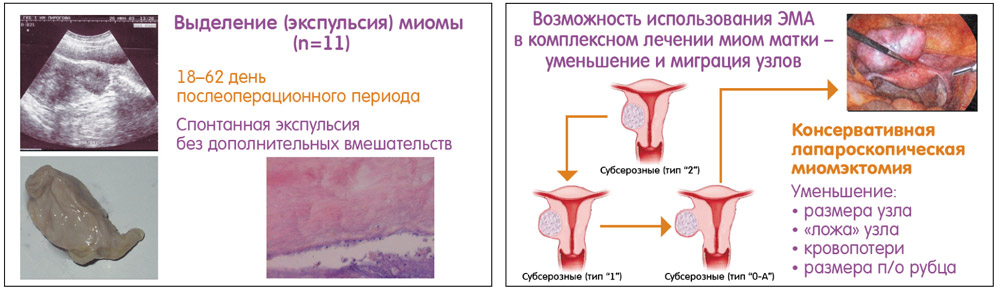
ЭМА возможна при сочетанных гинекологических заболеваниях, в частности, при наличии объемных образований в области яичников, гиперпластических процессов, а также при субсерозных и субмукозных миоматозных узлах, которые раньше относились к абсолютным противопоказаниям к проведению ЭМА. В нашем исследовании сочетание миомы матки с опухолевидными образованиями яичников наблюдалось в 18% случаев. Пациенткам проводили лапароскопию, резекцию яичников с последующим гистологическим исследованием. При доброкачественном процессе в дальнейшем осуществляли лечение миомы.
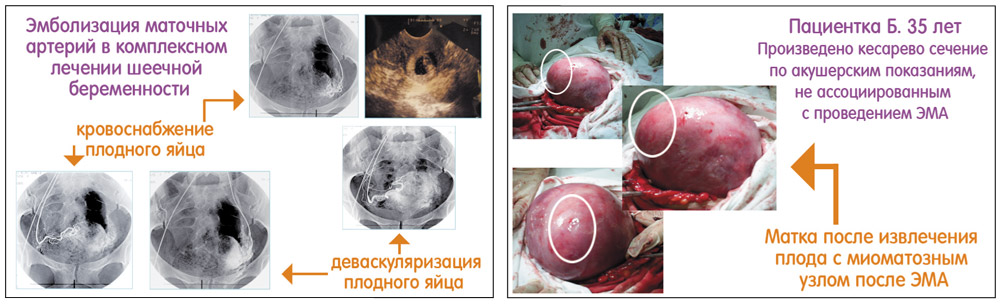
Также ЭМА применялась в комплексном лечении шеечной беременности в сочетании с химиотерапией (внутриартериальное введение метотрексата) и кюретажем (вакуум-экскохлеацией). В данной ситуации проведение ЭМА позволяло достичь немедленной остановки кровотечения, минимальной интраоперационной кровопотери, снизить дозу метотрексата и сократить количество койко-дней в среднем на 50%.
При изучении состояния органов репродуктивной системы нами не отмечено существенного влияния эмболизации на яичники, эндометрий и миометрий через 6 месяцев после ЭМА.
Таким образом, преимуществами ЭМА при лечении миомы матки являются сохранение репродуктивной функции, применение местной анестезии, короткий период госпитализации и реконвалесценции, минимальный риск рецидива заболевания и высокий психологический комфорт пациенток.
По данным большинства авторов, функция яичников после ЭМА не изменяется, однако некоторые исследователи указывают на возможность преходящей (5%) или постоянной (единичные случаи) аменореи вследствие технических ошибок.
В отношении влияния ЭМА на репродуктивную функцию нами получены следующие данные. Беременность планировали 247 пациенток, и 37% из них забеременели, при этом у большинства роды произошли через естественные родовые пути (кесарево сечение во всех случаях проводилось только по акушерским показаниям). На наш взгляд, условиями наступления беременности являются отсутствие кровотока в узле, уменьшение узлов примерно в 2 раза, отсутствие деформации полости матки и срок >1 года после эмболизации.
Всем беременным, перенесшим ЭМА по поводу миомы матки, проводилась гестагенная поддержка беременности (препарат Утрожестан) до 16–20 недель с индивидуальным подбором дозы от 200 до 400 мг. При развитии клиники угрозы прерывания беременности в дальнейшем с токолитической целью в группах риска (истмико-цервикальная недостаточность, преждевременные роды в анамнезе) назначали Утрожестан, в других случаях – препараты магния в сочетании с нифедипином 40 мг/сутки на фоне спазмолитиков.
Микронизированный прогестерон (Утрожестан) оказывает выраженное иммуномодулирующее действие через систему цитокинов – повышает продукцию лимфоцитами прогестерониндуцируемого блокирующего фактора (PIBF). Токолитический эффект Утрожестана достигается за счет блокады PGF2a и α-адренергической стимуляции, усиления β-адренергической стимуляции, снижения концентрации рецепторов окситоцина, уменьшения синтеза простагландина F2a.
Кроме того, на сегодня доказано, что 5α-прегнанолон и прогестерон обладают анксиолитическим эффектом, который опосредуется через рецепторы гамма-аминомасляной кислоты типа А.
У большинства беременных, перенесших ЭМА (96,4%), роды произошли в срок, при этом частота различных методов родоразрешения не отличалась от таковой у здоровых женщин.
В целом, особенностями беременности после ЭМА были продолжительность родов 6,5 часов, отсутствие гипотонии матки в третьем периоде родов, отсутствие случаев кровотечений в раннем и позднем послеродовом периоде, относительно небольшой вес детей. Интересно, что в двух случаях на 12-е и 20-е сутки после родов произошло рождение миоматозных узлов диаметром до 2 см, при этом гистологическое исследование показало изменения, характерные для узлов после ЭМА. Необходимо отметить, что в позднем послеродовом периоде в 18,4% случаев по акушерским показаниям (паритет родов, многоводие, субинволюция матки в анамнезе) мы назначали различную утеротоническую терапию, не опасаясь столкнуться с клиникой нарушения питания в миоматозном узле, что достаточно часто встречается при наличии миомы матки без применения ЭМА.
В заключение следует отметить, что ЭМА является высокоэффективным методом восстановления репродуктивной функции. Безусловно, беременные после ЭМА входят в группу риска и требуют высококвалифицированного наблюдения, однако сама по себе ЭМА не является показанием к оперативному родоразрешению или противопоказанием к беременности и родам в целом. И наконец, ЭМА ни в коем случае не является показанием или поводом к прерыванию беременности.
По материалам газеты «Здоровье Украины».


коментариев