Проблематика
Використання таких дезінфікуючих засобів як глутаральдегід і Ортофтальальдегід (2,4–3,2% глутаральдегід (Cidex®, Metricide®), ортофталевий альдегід 0,55% (Cidex OPA®), має незначний вплив на вірус папіломи людини (ВПЛ), тому є високий потенціал передачі цього вірусу при трансвагінальному ультразвуковому дослідженні, якщо застосовують лише ці методи знезараження.
Вирішення
Дезінфекція трансвагінального датчика ультразвуковою системою з перекисом водню і використання презервативу під час дослідження суттєво знижує потенціал зараження ВПЛ.
Серед медичних обстежень ультразвукове дослідження (УЗД) є універсальним і широкодоступним методом діагностики. Воно відносно просте для виконання, за вигідною ціною, неіонізуюче та неінвазивне або малоінвазивне. Проте незважаючи на нешкідливість УЗД, слід визнати, що ультрасонографічна апаратура є клінічним інструментом, який зазнає фізичного контакту з тілом пацієнта. Таким чином, за аналогією до рук медичного працівника або стетоскопа, ультразвуковий датчик є важливим вектором передачі інфекцї від одного пацієнта до іншого або від лікаря до пацієнта.
Для зниження ризику передачі такої інфекції настанови Американського інституту ультразвуку в медицині (American Institute of Ultrasound in Medicine) рекомендують дотримуватися таких трьох кроків:
1) трансвагінальний датчик слід ретельно очищувати після кожного обстеження;
2) після очищення датчик слід піддавати дезінфекції високого ступеня із застосуванням одного з дезінфектантів;
3) датчик слід покривати одноразовим чохлом при кожному застосуванні.
Нещодавні дослідження засвідчують, що у другого і третього кроків є суттєві недоліки. Зокрема, такі засоби як глутаральдегід і ортофтальальдегід, які використовують для дезінфекції високого ступеня, практично не впливають на ВПЛ 16 і 18 типів. Крім того, комерційні чохли для датчиків характеризуються високим ступенем протікання (8–81%). Ці два недоліки можуть зумовити високий ризик передачі ВПЛ.
Вірус папіломи людини (ВПЛ) – це найпоширеніша інфекція, що передається статевим шляхом у США, яка охоплює більш ніж 8 мільйонів жінок репродуктивного віку. Вірус папіломи людини типів 16 і 18 виявляють приблизно в 70% випадків раку шийки матки.
Вірусний капсид зберігає свою заразність протягом декількох днів і навіть тижнів в навколишньому середовищі, зокрема, на поверхні медичного обладнання. Він дуже стійкий до дії засобів низького рівня дезінфекції. Нещодавні дослідження засвідчують, що ВПЛ стійкий також і до глютаральдегіду і ортофтальальдегіду, які є дезінфектантами високого рівня.
У цьому огляді автори хочуть попередити лікарів УЗД про потенційні недоліки загальноприйнятої дезінфекції і запропонувати безпечніші альтернативні методи. Хоча переконливих випадків ятрогенної передачі ВПЛ через ендовагінальний датчик не зареєстрували, неможливо довести й відсутність такої можливості.
Водночас, безпека пацієнтів вимагає від нас найбезпечніших засобів для того, щоб унеможливити передачу інфекції. Ми не можемо дозволити собі чекати на підтвердження випадків такого зараження через застосування недосконалої дезінфекції.
Крок 1 – очищення
Згідно визначення Центру контролю і профілактики захворювань (CDC), очищення – це видалення видимого забруднення (наприклад, органічних і неорганічних матеріалів) з об'єктів і поверхонь, яке звичайно здійснюється руками або механічним способом з використанням води і детергентів або ферментних засобів. Ретельне очищення важливе перед дезінфекцією високого рівня та стерилізацією, оскільки неорганічні та органічні матеріали, що залишаються на поверхнях, впливають на ефективність такої дезінфекції. Американський інститут ультразвуку в медицині рекомендує очищення четвертинним амонієм у спреї або нанесеним на серветки, проточною водою, рідким милом та/або щіткою для очищення щілин і кутів. Вважають, що таке очищення дає змогу усунути 99% мікробів з поверхні датчика, однак для авторів статті ця думка здається надто оптимістичною.
Фоміти (англ. fomite) – будь-які предмети або субстанції, що містять патогенні мікроорганізми, такі як паразити чи мікроби, при зіткненні з якими виникає ризик зараження. Одним із видів фомітів є гель, який накопичується на поверхні датчика і стає потенційним середовищем для розмноження і поширення інфекційних агентів.
Згідно даних M’Zali et al (2014), після очищення низького рівня (протирання серветками з дезінфектантом) ДНК ВПЛ виявляли на датчиках у 13% випадків. ДНК C. Trachomatis виявляли на 20% датчиків, а мікоплазми – на 8%. Сапрофітні бактерії та типова для середовища флора була на 86% датчиків, а Staphylococcus aureus висівали у 4% випадків.
Крок 2 – дезінфекція високого рівня
Американський інститут ультразвуку у медицині і CDC описують кілька рівнів дезінфекції та стерилізації:
Дезінфекція – це процес, що усуває багато або всі патогенні мікроорганізми, за винятком бактеріальних спор.
Дезінфекція низького рівня – це знищення більшості бактерій, деяких вірусів і деяких грибків. Низький рівень дезінфекціі не обов'язково інактивує мікобактерії туберкульозу і бактеріальні спори.
Дезінфекція середнього рівня – це інактивація мікобактерій туберкульозу, бактерій, більшості вірусів, більшості грибків, а також деяких бактеріальних спор.
Дезінфекція високого рівня – це руйнування/видалення всіх мікроорганізмів, за винятком бактеріальних спор.
Стерилізація – це процес, що руйнує або усуває всі форми мікробного життя і який здійснюється в медичних установах фізичними або хімічними методами.
Виділяють також рівень очищення та/або знезараження для різних типів медичних інструментів:
- Критичні інструменти – призначені для проникнення через шкіру або слизові оболонки (наприклад, хірургічні інструменти) – вимагають стерилізації.
- Субкритичні інструменти, які вступають в контакт зі слизовими оболонками (наприклад, вагінальний ультразвуковий датчик), вимагають високого рівня дезінфекції.
- Некритичні інструменти, які контактують з неушкодженою шкірою і не торкаються слизових оболонок (наприклад, зовнішній ультразвуковий датчик) вимагають лише очищення.
Хоча Адміністрація ліків та харчових продуктів США (FDA) пропонує великий перелік продуктів для дезінфекції високого рівня, для обробки ультразвукових датчиків застосовують лише продукти, які містять глютаральдегід, ортофталальдегід та перекис водню.
У двох недавніх дослідженнях вивчали ефективність різних дезінфектантів високого рівня проти вірусу папіломи людини 16 і 18 типів. У одному дослідженні (Meyers et al., 2014) вірус папіломи людини 16 типу піддавали експозиції з різними дезінфектантами протягом 45 хвилин. При цьому глютаральдегід і ортофталальдегід виявилися неефективними в різних концентраціях, так само як і етанол, ізопропанолол та фенол. Слід зауважити, що 45 хвилин інкубації – це набагато довше, ніж рекомендований час (12 хвилин) для обробки датчика.
У іншому дослідженні (Ryndock et al., 2015) розчин із ВПЛ 16 і 18 типів наносили на пластик (такий, який застосовують для виготовлення датчиків) і після висушування на повітрі обробляли гіпохлоритом, ортофталальдегідом або випарами перекису водню за допомогою ультразвукової системи для стерилізації. При цьому гіпохлорит і перекис водню засвідчили потужну противірусну дію, натомість ортофталальдегід виявився неефективним.
Отже, незважаючи на те, що загальноприйняті способи стерилізації ультразвукових датчиків ефективно знищують більшість мікроорганізмів, ефективність їх щодо ВПЛ залишаєтся сумнівною.
Поки що єдиним способом стерилізації високого рівня для таких датчиків, ефективність якого довели, є обробка випарами перекису водню за допомогою спеціальної ультразвукової системи. Важливим моментом дезінфекції є обробка ручки датчика, оскільки вона не покривається чохлом і може дотикатися до вульви пацієнтки під час трансвагінального обстеження.
Поки що єдина комерційна система Trophon EPR®, у якій датчик поміщають всередину і дезінфікують парою перекису водню, гарантує дезінфекцію високого рівня, є швидким і практичним методом, безпечним для виконавця. Недоліком системи є її значна вартість. Пристрій коштує кілька тисяч доларів плюс витратні матеріали по кілька доларів за одне використання.
Тим не менше, ці витрати можна компенсувати за рахунок економії в інших ділянках.
Тривалість циклу дезінфекції менша, ніж при використанні глутаральдегіду або ортофтальальдегіду, що дає можливість прискорити потік пацієнтів. Крім того, систему ультразвукової обробки з Н2О2 можна використовувати у нічний час. Для персоналу ця система набагато безпечніша з міркувань токсичності та не потребує додаткових засобів захисту. Зрештою, з токи зору безпеки для пацієнтів така система якнайбільш виправдана.
Крок 3 – механічні бар'єри
Згідно настанов Американського інституту ультразвуку в медицині, всі порожнинні датчики повинні бути покриті одноразовим чохлом.
Ці настанови наголошують на неприпустимо високому рівні протікання комерційних чохлів для датчиків (8–81%) та рекомендують замість них застосовувати презервативи або хірургічні рукавички, рівень протікання яких набагато нижчий (0,9–2%).
Як заражаються жінки?
У недавньому огляді Leroy et al (2013) повідомляють, що при застосуванні вагінального датчика поширеність трансмісії інфекцій, які локалізуються у статевих шляхах (ВПЛ, вірус простого герпесу, цитомегаловірус), становить в середньому 1% (з коливаннями у межах 0–10%). І все ж таки сама лише наявність віруса не свідчить про причинний зв’язок. Отже, ми не знаємо, як часто трапляється зараження ВПЛ, і чи таке зрештою трапляється.
Задокументованих випадків зараження в результаті застосування порожнинних датчиків є всього декілька, і всі вони зумовлені субоптимальним виконанням протоколів дезінфекції, головним чином застосування дезінфекції низького рівня у тих випадках, коли треба було застосовувати дезінфекцію високого рівня.
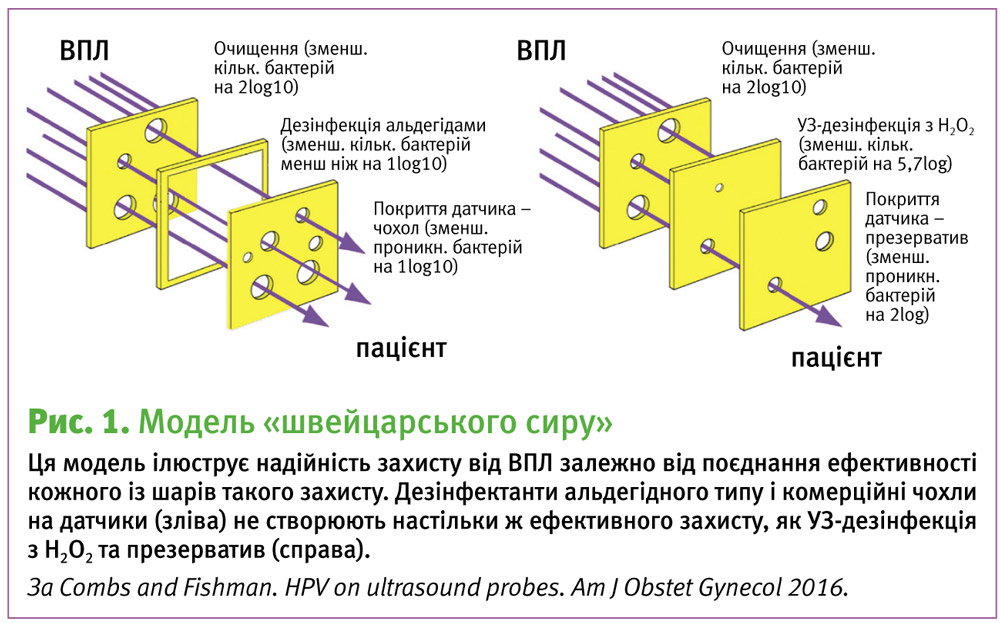
Модель «швейцарського сиру»
Концепцію безпеки пацієнта добре ілюструє модель «швейцарського сиру». У цій моделі намагаються створити шари захисту між потенційною небезпекою (ВПЛ) і пацієнтом. Ні один із шарів сам собою не є досконалим, кожен з них має свої слабкі місця, що відображається на рисунку «дірками у скибках швейцарського сиру» (рис. 1). Якщо дірка проникає через усі шари, захист не спрацьовує.
У цій схемі ми намагаємося оптимізувати безпеку пацієнта шляхом створення додаткових шарів або зменшити «кількість дірок» в окремих шарах. Отже, можемо обрати найліпший захист (ультразвуковий прилад для дезінфекції з Н2О2), а не глютаральдегід або ортофтальлальдегід) та застосовувати презервативи замість комерційних чохлів на датчики.
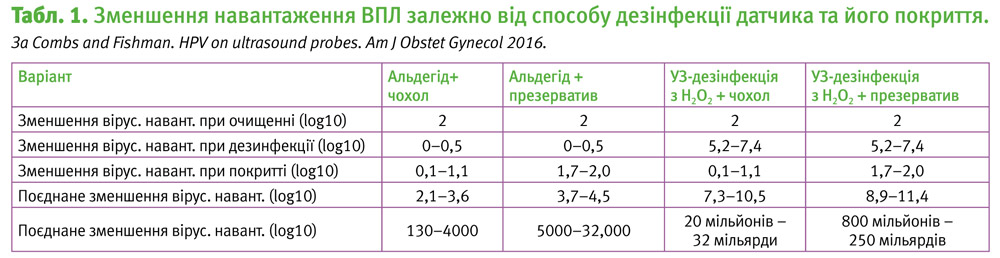
Згідно настанов Американського інституту ультрасонографії в медицині, «очищення, дезінфекція, стерилізація представляють собою статистичне зменшення кількості мікробів на поверхні, а не їх повну ліквідацію». У табл. 1 відображено можливості зменшення вірусного навантаження при кожному з цих кроків. Отже, при очищенні усувається 99% мікробів (2log10), при дезінфекції глютаральдегідом чи ортофтальдегідом 0–0,5 log10, при ультразвуковій дезінфекції з Н2О2 5,2–7,4 log10. Комерційні чохли на датчики характеризуються протіканням у 8–81%, що запобігає проникненню 0,1–1,1 log10 мікробів, натомість для презервативів протікання становить 0,9–2%, що відповідає запобіганню проникненню 0,7–2,0 log10.
Загальне зменшення вірусного навантаження при застосуванні усіх 3 кроків визначають як суму логарифмів, що еквівалентне перемножуванню цих цифр. Отже, поєднання застосування Уз-дезінфекції з Н2О2 та презервативу забезпечує зменшення навантаження ВПЛ у 800 млн.–250 млрд. разів, що принаймні у 200 тис. разів ефективніше, ніж застосування глутаральдегіду та комерційного чохла на датчик.
Рекомендації для безпечної практики
Отже, на основі доступної інформації можна сформулювати такі три рекомендації:
- Для покриття трансвагінального датчика слід застосовувати презерватив, а не комерційний чохол. Якщо у пацієнта є алергія на латекс, слід застосовувати з цієї метою безлатексні хірургічні рукавички.
- Обробку датчика та його ручки за допомогою УЗ-системи з Н2О2 треба виконувати після кожного трансвагінального ультразвукового дослідження.
- Крім того, слід дотримуватись усіх рекомендацій щодо очищення, дезінфекції, покриття та тримання датчиків для порожнинних досліджень.
Зрештою, компетентні установи повинні розробити додаткові рекомендації щодо нейтралізації ВПЛ за допомогою дезінфекції високого рівня. Вірус папіломи людини є одним з найпоширеніших і спричинює ураження шийки матки, анальної зони і ротоглотки, тобто тих ділянок, які найчастіше обстежують за допомогою порожнинних УЗ-датчиків.
Заклик до дії
Незважаючи на доступність інформації в літературі та досліджень, дивно спостерігати, що в рутинній практиці в Україні лише поодинокі лікарі виконують звичайну дезінфекцію датчиків між обстеженнями. Крім того, мало хто використовує рукавички під час усіх обстежень, мало хто і до і після процедури зазвичай миють руки. У згаданому вже огляді зазначають, що навіть після звичайних процедур дезінфекції (низького і середнього рівнів) на поверхні датчика виявляли 12,9% патогенних бактерій і 1% вірусів. Крім того, цей же автор зазначає, що поширеність інфікованих пацієнтів після трансректального УЗД і біопсії з УЗД було 3,1%.
Розумним буде зробити висновок про те, що очищення/дезінфекція датчиків повинні бути систематичними і регулярними. Лікарям УЗД слід чітко розуміти принципи інфекційного контролю, враховувати співвідношення витрат і вигод, зважати на те, що приносить користь не тільки їм і пацієнтам, але і суспільству в цілому.
Цей своєрідний «заклик до дії» спрямований на більш безпечну і якісну практику. Немає потреби чекати на випадок, щоб почати запобігати йому.

коментарів