Опыт клинического применения препаратов интерферона (часть 2)
В настоящее время известно более 20 различных возбудителей инфекционно-воспалительных заболеваний мочеполового тракта, среди которых у больных практически с одинаковой частотой встречаются как облигатные патогены (T. pallidum, N. gonorhoeae, вирус герпеса, вирус папилломы человека), так и представители условно-патогенной микрофлоры (C. albicans, U. urealyticum, M. hominis и др.), а также их ассоцианты (10)
Окончание. Начало статьи читайте в предыдущем номере журнала.
Интерферонотерапия дисбиотических заболеваний влагалища
Другой не менее важной и трудоемкой задачей практикующего гинеколога является лечение дисбиотических заболеваний влагалища – бактериального вагиноза и вульвовагинального кандидоза. В связи с широким и зачастую бессистемным назначением противомикробных и антимикотических препаратов, а также высокой частотой самолечения, возбудители данных заболеваний в настоящее время характеризуются резистентностью в отношении большого числа лекарственных средств. Кроме того, неудачи в лечении кандидоза и бактериального вагиноза обуславливаются имеющимися дисфункциональными изменениями врожденного и адаптивного иммунитета.
Являясь синантропом, С. albicans может избегать иммунологического надзора со стороны хозяина, что позволяет данному микроорганизму персистировать на поверхности слизистых. Важнейшим фактором вирулентности кандид является их способность к обратимому «переключению» с одноклеточных дрожжевых форм в различные нитевидные формы, которые могут быть найдены в любых тканях организма. Исследования последних лет свидетельствуют о том, что дрожжевая форма – это своеобразная стадия покоя кандид, и вопрос о вирулентности данной формы все еще остается открытым (45).
Многолетний опыт исследований патогенеза кандидной инфекции позволяет сделать вывод о способности данного микроорганизма вызывать разнообразные нарушения в функционировании иммунной системы. Известно, что развитие любого инфекционного процесса, ассоциированного с C. albicans, коррелирует с переключением адаптивного иммунного ответа на Th2-путь. Это обусловливает не только повышенную аллергическую настроенность макроорганизма, но и неэффективность осуществляемого фагоцитоза, активность которого напрямую зависит от уровня Th1-цитокинов и подавляется Th2-цитокинами. Концепция о реципрокной регуляции между фагоцитарной системой и Т-клеточным компартментом может служить объяснением неполноценности системного иммунного ответа при грибковом поражении слизистых (45). Бесспорно одно – эффективную защиту в отношении кандидо-ассоциированных инфекций может обеспечить только полноценная интеграция между врожденным и приобретенным иммунитетом.
Эффекты топической интерферонотерапии у пациенток с рецидивирующим вульвовагинальным кандидозом (РВВК) изучены в исследовании Боровикова О. В. и соавт., проведенном на базе кафедры клинической иммунологии, аллергологии и лабораторной диагностики Кубанского ГМУ в 2007 году. Всего в исследовании приняло участие 70 женщин: 40 пациенток с установленным диагнозом РВВК и 30 здоровых женщин (группа иммунологического контроля). Больные были рандомизированы в 2 равнозначные группы: 20 пациенток получали стандартную системную терапию (итраконазол 200 мг 1 раз в течение 3 дней), у других 20 пациенток в дополнение к стандартной терапии использовались суппозитории Генферон ректально в дозе 1000000 МЕ 2 раза в сутки в сочетании с ежедневным однократным вагинальным применением Генферона в дозе 500000 МЕ. Курс иммунотерапии составлял 5 дней.
В результате данного исследования установлено, что применение препарата Генферон способствует активации системного и, в большей степени, местного иммунитета, что выражается в повышении фагоцитарной активности лейкоцитов, нормализации НСТ-стимулированного теста, увеличением CD4+, CD16+, CD56+, CD25+, HLA-DR и соотношения CD4+/CD8+ лимфоцитов, снижении концентрации IgE, повышении IL-1b, IL-8, IL-10 как в периферической крови, так и в цервикально-вагинальной слизи (таблица 2).
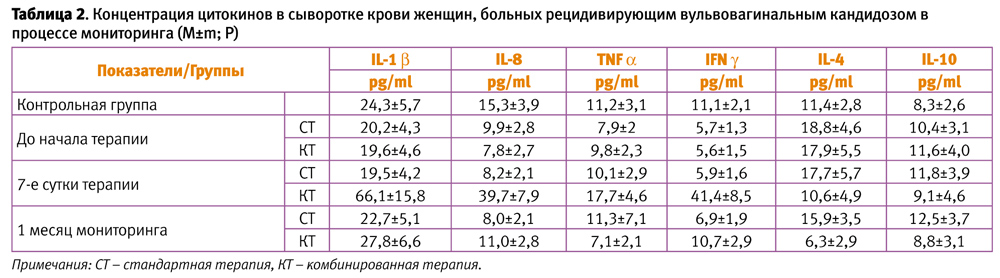
Исследуемая схема иммунокоррекции позволила снизить число рецидивов в основной группе в 6,32 раза (при месячном наблюдении) и в 7,96 раза (при наблюдении в течении полугода). Немаловажно и то, что применение Генферона достоверно снизило интенсивность клинических проявлений РВВК: в 2,1 раза на 7 сутки, в 2,4 раза через 1 месяц, в 2,9 раза через 6 месяцев (16).
Не менее интересными представляются иммунологические изменения, возникающие при бактериальном вагинозе. Известно, что развитие данного заболевания ассоциировано со снижением количества молочнокислых бактерий во влагалище и усиленным ростом разнообразных условно-патогенных облигатных анаэробов (Gardnerella vaginalis, Bacteroides, Prevotella, Mobillincus и др.).
Установлено, что в процессе жизнедеятельности G. vaginalis синтезирует специфический токсин – цитолизин, играющий важную роль в вагинальной экосистеме. Цитолизин может оказывать негативные эффекты в отношении различных иммунокомпетентных клеток. Так, например, в опытах in vitro доказано, что данный токсин в высоких дозах повреждает эндотелиальные клетки пупочной вены и лейкоциты человека. Предполагается, что именно цитолизин токсически воздействует на эпителиоциты влагалища, вызывая их десквамацию и превращение в ключевые клетки. Кроме того, данное вещество ингибирует процессы хемотаксиса полиморфно-ядерных лейкоцитов и угнетает воспалительный ответ в сочетании с другими ингибиторами лейкоцитарных функций, такими как сукцинат, продуцируемый в процессе жизнедеятельности иных облигатных анаэробов.
Важную роль в обеспечении эффективного иммунного ответа в отношении возбудителей бактериального вагиноза играет достаточный уровень sIgA цервикальной слизи. Действие этого иммуноглобулина в случае бактериального вагиноза направлено как на противодействие эффектам цитолизина, так и на сам токсин. Однако эффективность подобной гуморальной защиты при бактериальном вагинозе зачастую оказывается неэффективной ввиду того, что анаэробы способны к выработке специфических IgA-активных протеаз (19). Все это вкупе со склонностью к хроническому рецидивирующему течению бактериального вагиноза создает необходимость включения иммунотропной терапии в стандартные алгоритмы противомикробной терапии.
В 2006 году на базе кафедры акушерства и гинекологии Московского факультета РГМУ с курсом ФУВ было проведено исследование клинической эффективности препарата Генферон в сочетании с комбинированным препаратом Нео-Пенотран у пациенток, страдающих бактериальным вагинозом (БВ).
Всего было включено 120 женщин в возрасте 18–45 лет: I группу составили 40 здоровых женщин (группа иммунологического контроля), II группу – 80 пациенток с установленным диагнозом БВ. Больные II группы были рандомизированы в две равнозначные подгруппы: основную, пациентки которой получали Нео-Пенотран по стандартной схеме в сочетании с препаратом Генферон, который применялся вагинально в дозе 500000 МЕ дважды в сутки в течение 10 дней, и группу сравнения, у пациенток которой применялся только Нео-Пенотран. После завершения лечения микробиологическая картина влагалищного мазка нормализовалась у пациенток обеих групп, концентрация лактобактерий восстановилась до нормы, стабилизировались уровни IL-1b и IL-8. Через 1 месяц после лечения лабораторно подтвержденные рецидивы БВ зарегистрированы у 1 пациентки основной группы и 3 пациенток группы сравнения, через 6 месяцев – в 3 и 9 случаях соответственно. Столь существенные различия в частоте рецидивирования, прежде всего, обусловлены нормализацией иммунологического гомеостаза (1, 12).
Применение интерферона у беременных
Отдельную проблему в акушерско-гинекологической практике составляет эффективное и безопасное лечение УГИ у беременных. Известно, что инфекционные процессы во время беременности обусловливают большинство случаев неблагоприятных исходов: самопроизвольное прерывание, внутриутробное инфицирование плода, гипотрофию, некоторые врожденные пороки развития, реализацию инфекционного процесса в раннем постнатальном периоде и т. п. Главной проблемой терапии УГИ у беременных является невозможность использования широкого ряда препаратов в связи с их токсическим действием на плод. В то же время общепризнанным является и тот факт, что беременность сама по себе характеризуется своеобразной иммуносупрессией (как врожденного, так и приобретенного звена), а в сочетании с хроническим течением той или иной инфекции создает дополнительные трудности для эффективного этиологически и патогенетически обоснованного лечения, в равной степени безопасного как для матери, так и для плода.
Имеющиеся у врачей опасения по поводу проведения иммунотропной терапии у беременных нельзя считать беспочвенными. Действительно, некоторые иммуноактивные препараты способны оказывать эмбриотоксические и тератогенные эффекты, что ограничивает их применение у данной категории больных.
Обращаясь к зарубежному опыту применения препаратов интерферона у беременных, можно сделать вывод об их относительной безопасности: так, в большинстве описанных в литературе случаев интерферон применялся у беременных с целью терапии онкогематологических заболеваний или хронических вирусных болезней печени. При этом интерферон вводился ежедневно в виде подкожных инъекций в дозе от 1 до 8 млн МЕ, продолжительность лечения варьировала от 1 месяца до всего срока беременности. Ни в одном из описанных случаев использование интерферона не вызывало патологии в течении беременности, внутриутробного страдания плода или рождения детей с пороками развития (18, 20–24, 26–29, 31, 32, 35–44, 46, 48, 49, 51–55). До настоящего времени зарубежными исследователями не изучались эффекты малых доз интерферона в терапии инфекционных заболеваний у беременных, что и дало возможность российским ученым стать пионерами в этой области.
Безопасность и эффективность применения препарата Генферон в терапии урогенитальных инфекций у беременных во II и III триместре была изучена в рамках клинического исследования, проведенного на базе Московского областного НИИ акушерства и гинекологии в 2007 г.
В исследовании участвовали 92 беременных, страдающих УГИ. Было сформировано 3 сопоставимые группы:
- 32 пациентки, получавшие Вильпрафен 500 мг дважды в сутки 10 дней в комбинации с препаратом Генферон, вводившимся вагинально в дозе 250000 МЕ дважды в сутки в течение 10 дней;
- 30 пациенток, у которых использовался Вильпрафен 500 мг дважды в сутки 10 дней, свечи Тержинан вагинально 10 дней, затем – Генферон, вводившийся вагинально в дозе 250000 МЕ дважды в сутки в течение 10 дней;
III. 30 беременных, получавших Вильпрафен и Тержинан по указанной схеме. При первичном обследовании УГИ, вызванная одним инфекционным агентом, была выявлена у 31,5% пациенток, в остальных случаях у включенных больных диагностировалась микст-инфекция.
При этом у большинства беременных наблюдались патологические изменения шейки матки (нормальная кольпоскопическая картина зарегистрирована лишь у 21,7% больных). До начала лечения клинические симптомы воспалительного процесса были диагностированы у всех 100% пациенток.
Через 7 дней после начала лечения жалобы отсутствовали у 84,3% пациенток I группы, 93,3% во II группе и 90,0% больных III группы. Повторное исследование методом ПЦР выявило сохранение возбудителя у 3,3% пациенток I группы и 6,2% пациенток, не получавших иммунотропного лечения.
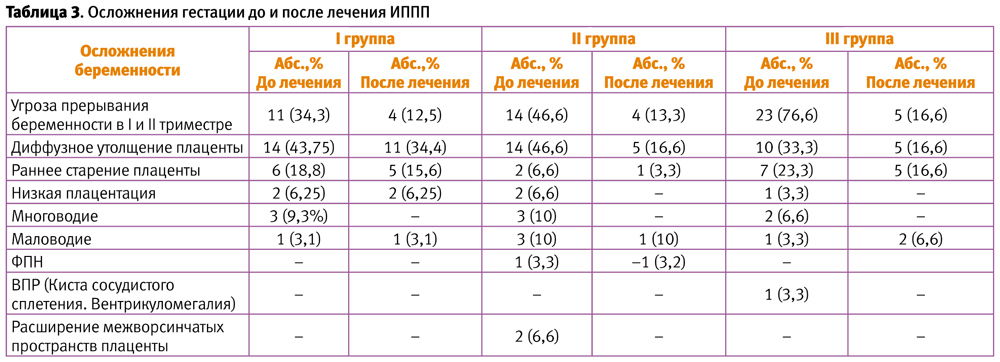
Установлено, что все исследуемые схемы терапии оказывали благотворное влияние на течение беременности и сокращали частоту гестационных осложнений (таблица 3).
По окончании курса терапии выявлены следующие важные закономерности: у пациенток I и II группы отмечено повышение уровня sIgA, уменьшение уровня IgG, в то время как у женщин, не получавших иммунотропной терапии, подобных изменений не выявлено.
За все время исследования ни у одной больной не было диагностировано нарушений в течении беременности, не регистрировалось случаев внутриутробного страдания плода или рождения детей с врожденной патологией. Все исследуемые схемы переносились пациентками хорошо и не вызывали развития побочных явлений (6).
Заключение
Эффективное лечение хронических инфекционно-воспалительных заболеваний мочеполового тракта у женщин до сих пор является актуальным вопросом современной гинекологии. Трудности терапии данной группы заболеваний обусловлены существованием своеобразного порочного круга, который поддерживается, с одной стороны, способностью возбудителей УГИ к своеобразному избеганию иммунологического надзора со стороны макроорганизма, а с другой – вызываемым ими же иммунологическим дефицитом.
Проблема возрастающей резистентности микроорганизмов к препаратам стандартной противомикробной терапии создает острую потребность в поиске новых эффективных лекарственных средств, позволяющих амплифицировать эффекты проводимых лечебных мероприятий.
В настоящее время препараты интерферона заняли важную нишу в лечении УГИ различной этиологии. И если раньше их применение было ограничено в связи с низкой переносимостью и неудобством лекарственной формы, то разработки последних лет позволяют использовать их у широкого круга больных, в том числе и у беременных женщин, начиная с 13 недели беременности. Высокая концентрация действующих веществ непосредственно в очаге поражения, активность в отношении основных возбудителей вирусных и бактериальных инфекций, потребность в проведении иммунокоррекции, достоверная безопасность и простота использования обусловливают целесообразность включения суппозиториев с интерфероном в состав большинства существующих схем терапии УГИ.
Список литературы находится в редакции.
По материалам журнала «Эффективная фармакотерапия в дерматовенерологии и дерматокосметологии, № 3/2010».
Применение препаратов ИФН a в терапии хронических урогенитальных инфекций является патогенетически оправданным еще и потому, что ряд возбудителей данных заболеваний обладает супрессирующим действием как на иммунную систему в целом, так и на выработку интерферона в частности. В случае лечения инфекционно-воспалительных заболеваний мочеполового тракта у женщин предпочтительным является местное лекарственное воздействие, чего удается добиться при использовании интерферонсодержащих суппозиториев для ректального или вагинального применения.
__________________________________
На территории Украины препарат Генферон® зарегистрирован под торговой маркой Генферон®ІБ. Препарат Генферон® в дозе 250 000 МЕ зарегистрирован под торговым названием Генферон®Лайт ІБ».
Препарат Генферон ІБ. Сертификат о государственной регистрации медицинского иммунобиологического препарата Генферон ИБ №857/11-300200000 от 05.10.2011 (дата окончания действия: 05.10.2016). Препарат Генферон ІБ используется в составе комплексной терапии инфекционно-воспалительных заболеваний урогенитального тракта у взрослых. Фармакотерапевтическая группа. Иммуностимуляторы. Интерферон альфа-2b. Код АТС L03A В05. Побочные реакции. Аллергические реакции: возможны аллергические реакции, включая кожные высыпания, зуд. Эти симптомы исчезают через 72 часа после прекращения введения препарата или уменьшения дозы. Иногда могут наблюдаться озноб, повышение температуры тела, утомляемость, потеря аппетита, мышечная и головная боль, боль в суставах, изменения в месте введения, потливость, а также лейко- и тромбоцитопения. Категория отпуска. По рецепту.
Препарат Генферон Лайт ІБ. Сертификат о государственной регистрации медицинского иммунобиологического препарата Генферон Лайт ИБ № 895/12-300200000 от 26.11.2012 (дата окончания действия: 26.11.2017). Препарат Генферон Лайт ІБ используется, как компонент комплексной терапии ОРВИ и других инфекционных заболеваний бактериальной и вирусной этиологии у детей; как компонент комплексной терапии – для лечения острых кишечных инфекций вирусной и смешанной вирусно-бактериальной этиологии у детей; при инфекционно-воспалительных заболеваниях урогенитального тракта у детей и женщин, в том числе беременных. Фармакотерапевтическая группа. Иммуностимуляторы. Интерферон альфа-2b. Код АТС L03A В05. Побочные реакции. До настоящего времени не наблюдалось тяжелых или опасных для жизни побочных явлений. Могут наблюдаться явления, которые возникают при применении всех видов интерферона альфа-2b, такие как озноб, повышение температуры, утомляемость, потеря аппетита, мышечные и головные боли, боли в суставах, потливость, а также лейко- и тромбоцитопения, но чаще они встречаются при превышении суточной дозы свыше 10 000 000 МЕ. Категория отпуска. По рецепту. Данная информация предназначена исключительно для профессиональной деятельности фармацевтических и медицинских работников.

коментарів