Синдром Дауна (СД) — самая известная и наиболее распространенная хромосомная аномалия, приводящая к выраженной умственной отсталости, имеющая характерные фенотипические проявления с нарушением соматического и психофизического развития. ОМIM-190685; МКБ-Х — Q.90. Синоним: трисомия 21, ранее употреблялся термин «монголизм».
Историческая справка
В 1846 году Сегуин (Seguin) описал детей с умственной отсталостью, которые имели монголоидные черты лица. Но он расценил эту патологию как разновидность кретинизма, вызванную снижением функции щитовидной железы. В 1866 году лондонский врач Джон Лэнгдон Хэйдон Даун (John Langdon Haydon Down) опубликовал небольшую статью, в которой настолько детально описал клиническую картину болезни, что она до сих пор считается эталоном. Он также организовал для этих больных специальный приют, которым руководил длительное время, имел большой опыт в их лечении и приобщении к полезной жизни в семье и обществе. Его идеи и нововведения были практичными и новаторскими и изменили отношение к тяжело больным детям. Доктор Даун первым стал различать умственно отсталых детей от детей с кретинизмом (вследствие гипотиреоза) и так называемых монголоидов (детей с СД). Термин «монголоиды» просуществовал в научной медицинской литературе почти 100 лет. В 70-х годах ХХ века специальная комиссия США по медицинской терминологии приняла решение о присвоении этой патологии официального названия — «синдром Дауна», в честь человека, впервые диагностировавшего и описавшего его. Примечательно, что у самого Д. Дауна родился внук с этим синдромом.
Этиология
 Спустя почти 100 лет после описания СД, в 1959 году два независимых исследования Жерома Лежена (Lejeune) и Патриции Джейкобс (Jacobs) установили, что причиной нарушения является трисомия 21 хромосомы, хотя еще в 1932 году Ваарденбург (Waardendurg) и Блеер (Bleyer) выдвинули гипотезу о хромосомном происхождении этого синдрома. В 1987 году идентифицированы гены (Olig 1 и Olig 2), индуцирующие его развитие, расположенные на длинном плече 21 хромосомы дистальнее критической области бэнда q22.1, между сегментами 21q22.1–21q22.3 (максимальный размер этого фрагмента 2000–3000 кб, содержит последовательность генов, определяющих активность ферментов SOD1, ETS2, CBS, нарушение продукции которых отмечается при синдроме Дауна), трипликация которого определяет фенотип СД.
Спустя почти 100 лет после описания СД, в 1959 году два независимых исследования Жерома Лежена (Lejeune) и Патриции Джейкобс (Jacobs) установили, что причиной нарушения является трисомия 21 хромосомы, хотя еще в 1932 году Ваарденбург (Waardendurg) и Блеер (Bleyer) выдвинули гипотезу о хромосомном происхождении этого синдрома. В 1987 году идентифицированы гены (Olig 1 и Olig 2), индуцирующие его развитие, расположенные на длинном плече 21 хромосомы дистальнее критической области бэнда q22.1, между сегментами 21q22.1–21q22.3 (максимальный размер этого фрагмента 2000–3000 кб, содержит последовательность генов, определяющих активность ферментов SOD1, ETS2, CBS, нарушение продукции которых отмечается при синдроме Дауна), трипликация которого определяет фенотип СД.
94% случаев СД представляют собой регулярные трисомии 21 хромосомы, обусловленные нерасхождением хромосом, чаще в I (76%) или реже во II (24%) мейотическом делении гамет, преимущественно материнского происхождения (80%). В пользу существования генного контроля свидетельствуют случаи повторного рождения в некоторых семьях детей с регулярной формой трисомии 21, что может объясняться генетически обусловленной тенденцией к нерасхождению хромосом либо как невыявленный мозаицизм (возможно, с вовлечением гонад), а также более высокой частотой кровнородственных браков между родителями таких детей.
4% СД представляют собой варианты робертсоновских транслокаций, обусловленных почти в половине случаев сегрегацией семейных сбалансированных хромосомных аберраций у родителей, преимущественно материнского происхождения — 39%, отцовского — 3%, имеющего в свою очередь более высокий рекуррентный риск (9–10%) СД для потомства, чем при реципрокных транслокациях отцовского происхождения — 2%. Чаще всего встречаются транслокационные варианты 14/21 хромосом (58–70%), реже 15/21 (22%) и 13/21 (5–10%) хромосом и летальные варианты 21/21. В большинстве случаев транслокационные варианты СД встречаются у молодых родителей в отличие от регулярной формы трисомии, которые чаще наблюдаются у женщин старше 30 лет. Половина наблюдений транслокационного СД возникает de novo вследствие мутаций. Мозаичная форма СД составляет 2% от всех наблюдений и обладает значительным клиническим полиморфизмом фенотипических проявлений.
Распространенность
Средняя популяционная частота СД составляет 1:700–800 новорожденных. Высокая распространенность СД обусловлена довольно низким уровнем внутриутробной гибели плодов и относительно высокой жизнеспособностью больных по сравнению с другими хромосомными синдромами, что объясняется аномалией самой маленькой аутосомы в кариотипе человека. Частота среди новорожденных составляет 0,15%, среди абортусов 3%, среди умерших в перинатальном периоде 1%.
Прогноз
Развитие около 30% плодов с СД спонтанно прерывается в первую половину беременности, преимущественно в ранние сроки. Дети в основном погибают от пороков сердца и врожденного иммунодефицита (около 31% детей с трисомией 21 хромосомы умирают до конца 1-го года жизни, 40% — в конце 3-го года жизни), взрослые — из-за неврологических и злокачественных заболеваний, преждевременного старения организма. Максимальная продолжительность их жизни 50–60 лет. Ежегодно во всем мире рождается свыше 150 тысяч детей с синдромом Дауна: в США — около 5 тысяч, в Украине около 500; в России — более 2500, в бывшем СССР — около 8 тысяч больных с СД. Благодаря упорству, совместным усилиям родителей, психологов, педагогов, медиков, социальных работников удается достичь определенных успехов в социальной реабилитации больных с СД.
Факторы риска
Материнский возраст
Первым обратил внимание на взаимосвязь возраста матери и частотой рождения детей с СД Шатлворт (Shuttleworth) в 1909 году. В 1938 году Блеер (Bleyer), сравнив возраст матерей 2822 детей с СД и 2000000 здоровых новорожденных, определил, что средний возраст первых составил 41 год, а вторых — 24 года соответственно. Многочисленные дальнейшие исследования подтвердили это. Установлено, что с увеличением возраста матери с 20 до 45 лет резко возрастает частота рождения ребенка с СД (с 0,5 до 4,3 на 1000) (табл. 1) и некоторыми другими хромосомными анеуплоидиями. В это же время еще в 1954 году Пенроуз (Penrose) доказал, что возраст отца не влияет на частоту СД.
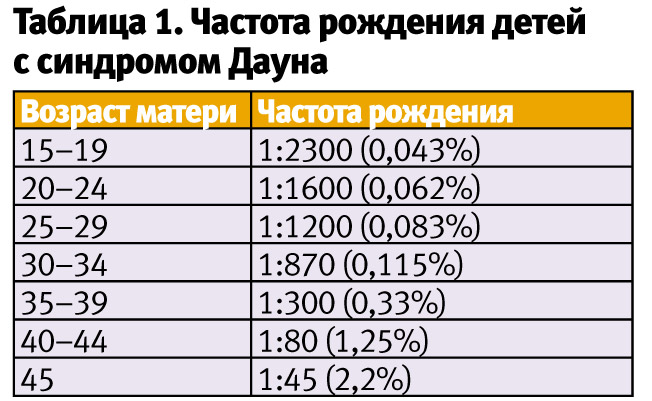
Факторами, повышающими риск нерасхождения хромосом, является наличие мозаицизма или сбалансированных транслокаций у родителей, рождение детей с трисомией. В последние годы отмечено увеличение частоты рождения детей с СД у молодых матерей. Причины, способствующие возникновению трисомии 21, разнообразны. Кроме возраста матери и в значительно меньшей степени возраста отца (перезревание сперматозоидов при нерегулярной, редкой половой жизни в пожилом возрасте) нерасхождению хромосом в мейозе способствует эндокринная незрелость молодых беременных, гормональные контрацептивы, транзиторные периоды периовуляторного перезревания яйцеклетки, гипериндукция овуляции, длительность интергенетического интервала, частота половых сношений, сезонная динамика зачатий в инфекционный и постинфекционный период, а также вредные профессиональные и экологические факторы. Отмечена взаимосвязь увеличения частоты СД от числа предшествующих спонтанных абортов и даже от возраста бабушки по материнской линии.
Фенотипический портрет синдрома Дауна
Синдром Дауна является одной из форм олигофрений, при которой умственная отсталость и задержка развития сочетается со своеобразным соматическим синдромом и специфическим обликом больного. Благодаря самой высокой распространенности среди всех форм умственной отсталости и легкости распознавания, обусловленной характерным фенотипом, дети и взрослые с СД хорошо знакомы не только специалистам. Фенотипически эти больные настолько похожи, что их часто называют «дети одной матери». Однажды увидев такого ребенка или взрослого, его можно с уверенностью выделить из окружающих. Поэтому говорят не о диагностике, а об «узнавании» СД. Действительно, вид больного имеет характерные проявления, которые запоминаются без труда. При этом большая часть симптомов обнаруживается у ребенка сразу же при рождении (табл. 2). И довольно часто присутствует внутриутробно у плода, что дает возможность визуализации некоторых из них при пренатальном ультразвуковом исследовании.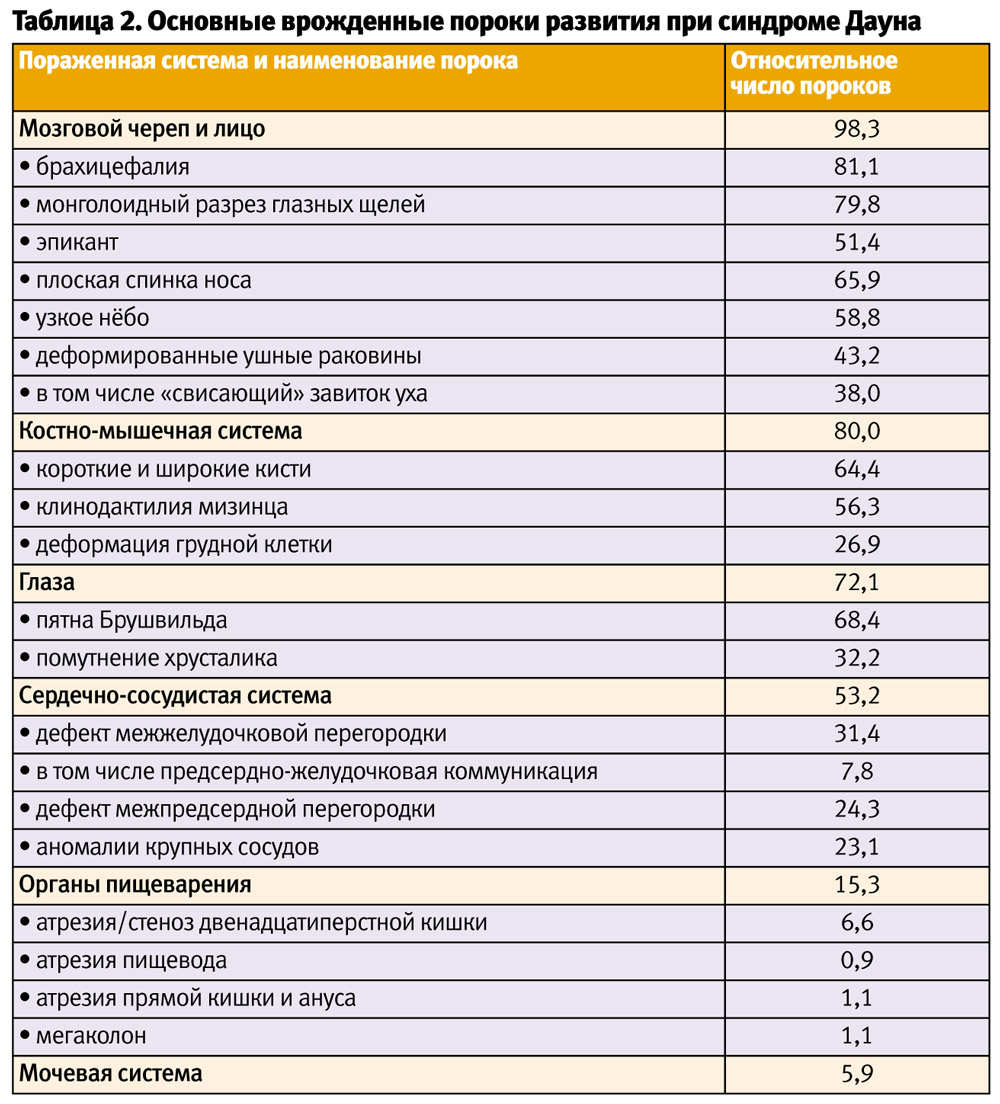
Пренатальная диагностика
До настоящего времени СД — самый сложный и загадочный объект для пренатальной диагностики (ПД), если не сопровождается грубыми ВПР или обнаружением характерных эхографических и биохимических маркеров.
Согласно современной концепции пренатальной профилактики пороков развития и распространенных хромосомных анеуплоидий, важнейшим является формирование групп высокого риска с учетом возраста, анамнеза и результатов ультразвукового и биохимического скрининга, на основе чего беременным избирательно проводятся инвазивные методы пренатальной диагностики (биопсия ворсин хориона [11–14 недель], плацентоцентез [с 15 недель], амниоцентез [17–22 недели], кордоцентез [20–26 недель]) с последующим цитогенетическим исследованием соответственно полученному образцу трофобласта, культуры клеток амниотической жидкости и лимфоцитов крови плода.
Эффективность пренатальной диагностики СД является маркером качества проведения пренатального скрининга в целом.
Скрининг является лишь начальным, предварительным этапом обследования популяции, а лица с положительными результатами скрининга нуждаются в последующем диагностическом обследовании для установления или исключения факта наличия патологического процесса. Говорить об эффективном скрининге можно, если он является массовым, то есть охватывает больше 80% обследуемой части населения. В противном случае скрининг является выборочным (селективным) и не выполняет все возложенные на него задачи.
В 1970-х годах основной метод скрининга хромосомных анеуплоидий (ХА) основывался на возрасте матери, а в 1980-х годах – на биохимии крови матери и детальном ультразвуковом исследовании во II триместре. В 1990-х годах акцент переместился на I триместр, когда стало ясно, что большинство плодов с основными ХА можно идентифицировать путем комбинированного сочетания возраста матери, толщины воротникового пространства (ТВП) у плода, БХ-маркеров крови беременной в I триместре. В последние 10 лет было описано несколько дополнительных ультразвуковых маркеров I триместра, оцениваемых при безвыборочном пренатальном скрининге, которые улучшают частоту выявления анеуплоидий и уменьшают уровень ложноположительных результатов.
Скрининг по возрасту матери
В начале 1970-х годов из числа всех беременных около 5% женщин были в возрасте 35 лет или старше, и в этой группе рождалось около 30% плодов от общего количества с трисомией 21. Таким образом, скрининг на основе возраста матери, с границей по возрасту 35 лет для определения группы высокого риска, был связан с 5% уровнем скрининг-позитивных значений (также называемые ложноположительными, так как большинство плодов в этой группе нормальные) и 30% вероятностью обнаружения трисомии 21 хромосомы. В последующие годы в развитых странах появилась тенденция среди женщин беременеть в более позднем возрасте, так что сейчас в общей популяции беременных около 20% женщин в возрасте 35 лет или старше, и эта группа содержит около 50% от общего числа плодов с трисомией 21.
Биохимический скрининг хромосомных аномалий
II триместр беременности
Первые попытки включения материнских сывороточных маркеров в скрининг ХА были сосредоточены на II триместре беременности и продемонстрировали существенное улучшение уровня определения трисомии 21 по сравнению со скринингом по возрасту матери. При уровне ложноположительных результатов в 5% выявляемость плодов с трисомией 21 возросла с 30 до 60–65% при объединении материнского возраста, сывороточного АФП и fß-ХГЧ (двойной тест), до 65–70% — с дополнительным значением uЕ3 (тройной тест), и от 70 до 75% со значением ингибина А (четверной тест). Если используется интактный ХГЧ, а не fß-ХГЧ, то вероятность обнаружения снижается примерно на 5%.
I триместр беременности
В последние 10 лет биохимические исследования стали проводиться в I триместре, потому что в сочетании с ультразвуковым маркером ТВП плода информативность такого скрининга превосходит скрининг II триместра. Ранний комбинированный скрининг традиционно включает расчет базового риска рождения ребенка с трисомией 21 по возрасту матери с последующей корректировкой показателя риска в зависимости от уровня fß-ХГЧ и РАРР-А (ассоциированном с беременностью плазменного протеина А) в крови матери и величины TВП. При беременностях с трисомией 21 у плода концентрация fß-ХГЧ в сыворотке крови матери примерно в 2 раза выше, а РАРР-А снижен в половину в сравнении с эуплоидными беременностями.
На измеренную концентрацию этих плацентарных продуктов в сыворотке крови влияют такие характеристики матери, как расовое происхождение, вес, курение, способ зачатия, болезни матери и прием гормональных препаратов, а также приборы (биохимические анализаторы), технологические лабораторные методы и реагенты (лабораторные диагностические наборы), используемые для анализа. Следовательно, при расчете рисков анеуплоидий с использованием этих продуктов необходимо принимать во внимание факторы этих материнских переменных при определении МоМ перед сравнением аномальных и нормальных беременностей.
В скрининге на трисомию 21 по материнскому возрасту и сывороточным маркерам (fß-ХГЧ, РАРР-А) частота обнаружения составляет 65% при числе ложноположительных результатов 5%. Проводить анализ лучше с 9 по 10 неделю беременности, так как разница в РАРР-А при наличии трисомии у плода и эуплоидным плодом заметнее на более ранних сроках беременности.
Относительно новым биохимическим маркером анеуплоидий является ADAM 12 (A Disintegrin And Metalloproteinase — дизинтегрин и металлопротеиназа). При беременностях с трисомией его уровень в сыворотке крови матери в I триместре ниже, чем в эуплоидных беременностях. Уровень ADAM 12 при трисомии 21 — 0,96 МоМ (достоверно не отличается от эуплоидных плодов — 1,01 МоМ). Вместе с тем маловероятно, что использование этого маркера улучшит скрининг, так как понижение незначительное и существует значимая связь между ADAM 12 и традиционными биохимическими маркерами fß-ХГЧ и РАРР-А. Повышение уровня ADAM 12 связано с риском возникновения преэклампсии и HELLP-синдрома у беременной.
Еще одним относительно новым биохимическим маркером ХА в сроке беременности 11–13+6 является PIGF (плацентарный фактор роста, ПФР), в первую очередь являющийся общепризнанным ранним высокочувствительным предиктором преэклампсии, гипертензивных состояний и плацентарной дисфункции. Хотя первые исследования ПФР в скрининге синдрома Дауна, выполненные 10 лет назад, показали противоречивые результаты, публикации последних лет свидетельствует о достоверном снижении экскреции ПФР в сыворотке крови матери в 11–13 недель гестации в случае ХА у плода: при трисомии 21 — 0,707 МоМ. В то же время оценка ПФР в сочетании с возрастом матери, РАРР-А, fβ-ХГЧ и измерением ТВП повышает чувствительность скрининга всего на 0,5% при ложноположительном результате — 5%. В настоящее время признано целесообразным дополнительно включить в программу первого биохимического скрининга также определение АФП (в сочетании с РАРР-А, fβ-ХГЧ), снижение которого (0,707 МоМ), как и во II триместре беременности, характерно для трисомии 21.
В то же время определение нескольких маркеров является дорогостоящим и в последнее время критически оценивается рентабельность этих программ и их эффективность. В связи с этим, кроме представленных подходов, актуальным является поиск дополнительных путей пренатальной идентификации хромосомных анеуплоидий, и в этом определенную роль может сыграть эхография в качестве основного способа отбора беременных для пренатального кариотипирования плода на основе выявления при массовом УЗ-скрининге характерных аномалий и наиболее типичных ключевых УЗ-маркеров распространенных хромосомных синдромов, и в первую очередь СД. Организованный массовый УЗ-скрининг реально может охватить более 95% беременных, знание характерных, легко доступных обнаружению эхо-признаков и возможность проведения последующего пренатального кариотипирования плода может внести существенный вклад в диагностику ХА, особенно у молодых матерей.
Пренатальная эхография СД
Внутриутробная предварительная ультразвуковая ПД трисомии 21 основывается на обнаружении визуализированных при эхографии аномалий развития, характерных для СД, и различных УЗ-маркеров:
- Патогномоничных признаков, микроаномалий, являющихся одинаково ценными как при УЗИ, так и при оценке фенотипа (брахицефалия, плоский профиль, макроглоссия, утолщение шейной складки и прочее).
- Специфических эхо-признаков, имеющих диагностическую ценность преимущественно при УЗИ, а при оценке фенотипа, в том числе на аутопсии, или вовсе не учитывающихся, так как они не определяются вне эхографии (гиперэхогенный кишечник), или же имеющих второстепенное значение (кисты сосудистых сплетений, пограничная вентрикулодилатация, умеренная пиелоэктазия, гиперэхогенный фокус).
- Неспецифические фоновые эхо-признаки со стороны провизорных органов беременности, косвенно свидетельствующих о возможной патологии плода (многоводие, аплазия одной артерии пуповины).
С другой стороны, УЗ-маркеры СД могут быть разделены на описательные и биометрические, имеющие количественные критерии — абсолютные и относительные (индексы).
УЗ-маркеры СД, детектируемые в ранние сроки беременности, более универсальны и могут наблюдаться при разных синдромах ХА, в то время как большинство ключевых эхо-маркеров, выявляемых во II триместре беременности, более специфичны для трисомии 21 и других распространенных анеуплоидий.
I триместр беременности
Наиболее известным УЗ-маркером СД, выявляемым при проведении 1-го скринингового УЗИ, является расширение толщины воротникового пространства.
Этот маркер впервые был описан J. Szabo в 1990 году, а термин «воротниковое пространство» (дословно «воротниковая прозрачность» — nuchal translucency) был предложен K. Nickolaides в 1992 году.
Многочисленные исследования в последние 20 лет установили, что измерение ТВП плода обеспечивает ранний и эффективный скрининг трисомии 21 и других распространенных ХА. Кроме того, увеличение ТВП, в том числе у плодов с нормальным кариотипом, связано с врожденными пороками сердца и целым рядом других пороков развития плода и генетическими синдромами, а также неблагоприятными исходами беременности. Оптимальным гестационным сроком для оценки ТВП плода является интервал с 11 до 13/6 недель. Минимальный КТР плода должен быть 45 мм, а максимальный — 84 мм. Нижний предел выбран для того, чтобы обеспечить ультразвуковую диагностику многих основных аномалий плода, которые в противном случае были бы упущены (за исключением структур сердца), а верхний предел для того, чтобы предоставить женщинам с аномальными плодами возможность раннего и безопасного метода прерывания беременности. После 13 недель ТВП начинает уменьшаться, поэтому наиболее оптимальным сроком для оценки ТВП является период — 11/3–12/3 недель беременности.
В дополнение к ТВП, к другим высокочувствительным и специфическим ультразвуковым маркерам трисомии 21 относятся: отсутствие изображения носовой кости, фронтомаксиллярный угол более 88O и гемодинамические (доплерометрические) критерии — реверсные значения кровотока в венозном протоке и трикуспидальная регургитация. Отсутствие изображения носовой кости, увеличение фронтомаксиллярного угла, реверсный кровоток в венозном протоке (a-волна) и недостаточность (регургитация) трехстворчатого клапана наблюдаются примерно у 60; 69; 66 и 55% плодов с трисомией 21 и в 2,5; 5; 3,0 и 1,0% случаев соответственно у плодов с нормальным кариотипом.
В последние два года появились новые эхографические маркеры ХА: интракраниальное пространство (ИП), ретроназальный треугольник (РТ), мандибулярная щель (МЩ), оцениваемые также в 11–13 недель беременности. ИП (расположенное между стволом мозга и хориоидальным сплетением и отражающее IV желудочек) легко визуализируется при стандартном сагиттальном сечении, используемом для оценки ТВП. Его оценка характеризуется высокой воспроизводимостью и не требует дополнительного времени. Размеры ИП не зависят от возраста матери и коррелируют со сроком беременности. Дилатация ИП более 2,5 мм при КТР 45–84 мм, по данным ретроспективного исследования, коррелирует с ХА, в то время как уменьшение ИП является проявлением открытых дефектов спинного мозга. Оценка РТ проводится с помощью объемной эхографии, но возможна и при двумерной оценке лицевых структур плода в коронарной плоскости сканирования. При оценке РТ возможна ранняя диагностика симметричной и асимметричной аплазии носовых костей, расщелины твердого неба и визуализация МЩ, расширение которой наблюдается при гипоплазии нижней челюсти, что характерно для трисомии 18 и ряда моногенных синдромов.
Недавно описанным доплеровским ультразвуковым маркером трисомии 21 в I триместре является увеличение пиковой систолической скорости в печеночной артерии плода. О наличии возможной ХА у плода свидетельствует показатель — более 14 см/с (>95 процентиль) в 11–13 недель беременности и снижение пульсационного индекса менее 2,0.
II триместр беременности
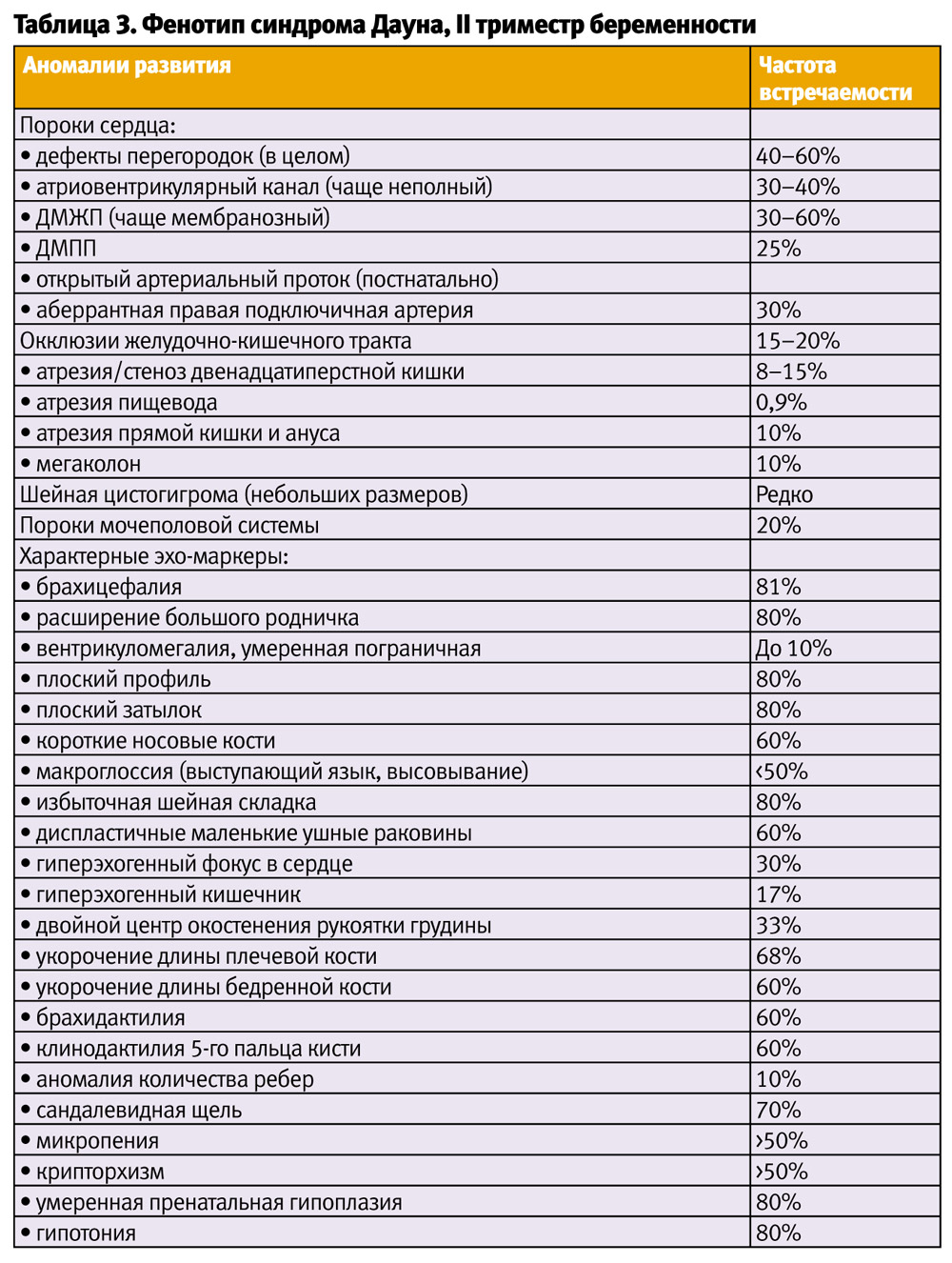
При ультразвуковом сканировании во втором триместре каждый хромосомный синдром имеет свою собственную фенотипическую особенность — характерный симптомокомплекс «эхопортрет» обнаруженных аномалий (табл. 3). Например, при трисомии 21 наблюдаются пороки сердца (предсердно-желудочковый канал, ДМЖП, правая аберрантная подключичная артерия), атрезия двенадцатиперстной кишки, гипоплазия носовых костей, плоский профиль, макроглоссия (высовывание языка), увеличение толщины шейной складки (отек воротниковой зоны) и кожи в области переносицы, увеличение префронтального пространства, гиперэхогенные включения (фокусы) в сердце, эхогенный кишечник, мегаколон, умеренная брахицефалия, пограничная вентрикулодилатация (вентрикуломегалия) боковых желудочков мозга, умеренный гидронефроз/пиелоэктазия, укорочение бедра и ещё большее укорочение плечевой кости, сандалевидная щель на стопе и гипоплазия средней фаланги V пальца (клинодактилия), расширение большого родничка, возможно отсутствие XII пары ребер, широкие крылья подвздошных костей. Каждый из которых имеет определенные четкие эхографические критерии (в том числе с расчетом и оценкой различных индексов), чувствительность, специфичность и прогностическую значимость, на основе чего коррелируется индивидуальный риск СД (базовый по фактору возраста, комбинированный по результатам I триместра или интегрированный по результатам скрининга в I и ІІ триместре беременности).
Было определено, что УЗ-сканирование во ІІ триместре беременности может на 6% повысить вероятность обнаружения трисомии 21, полученную в триместре после проведения комбинированного скрининга, при дополнительном относительном числе ложнопозитивных результатов на 1,2%.
В следующем номере мы расскажем о расчете риска СД по УЗ-маркерам во ІІ триместре беременности, а также о современных моделях и стратегии пренатального скрининга XA.


коментариев