 Последние достижения в области в области неинвазивной пренатальной диагностики (NIPT/NIPD) и новые стратегии пренатального скрининга хромосомных аномалий
Последние достижения в области в области неинвазивной пренатальной диагностики (NIPT/NIPD) и новые стратегии пренатального скрининга хромосомных аномалий
К написанию этой статьи нас подтолкнул бум в области неинвазивной пренатальной диагностики (non-invasive prenatal testing, NIPT), наблюдаемый в мире в последние 2–3 года, и ее агрессивная экспансия в программы пренатального скрининга хромосомных аномалий
Генеральными спонсорами XIII Всемирного конгресса по медицине плода (Ницца, 2014) выступили фирмы-разработчики и производители тест-систем для неинвазивных пренатальных исследований (Ariosa diagnostics, Illumina, Panorama, Sequenom, Berry Genomics), активно предлагающих свою продукцию участникам конгресса.
И хотя отечественная медицина еще не применяет такой вид диагностики в широких масштабах, как это уже практикуется в западных странах, предложение их у нас в стране осуществляется с помощью коммерческих медицинских структур, выполняющих роль посредников между пациентами и такими лабораториями в других странах.
Поэтому, на наш взгляд, целесообразно познакомить отечественных акушеров-гинекологов, врачей УЗД, генетиков и других специалистов с появлением новых возможностей и стратегий в этом направлении.
Введение
Неинвазивная пренатальная диагностика с использованием внеклеточной фетальной ДНК (cell-free fetal DNA, cffDNA) в крови матери уже зарекомендовала себя как наиболее эффективный метод скрининга трисомии 21.
Однако, в отношении других анеуплоидий, микроделеционных/микродупликационных синдромов, многоплодных беременностей, мозаичного кариотипа, моногенных заболеваний, практические результаты пока намного скромнее.
В связи с бурным развитием этого направления назревают вопросы о создании новой общедоступной эффективной модели пренатального скрининга хромосомных анеуплоидий с использованием NIPT. Параллельно с усовершенствованием методик диагностики ведутся подсчеты относительно экономической и социальной целесообразности, а также выгоды использования данного метода с учетом всех возможностей и ограничений.
Концепция NIPTс использованием cfDNA применяется с 1997 года, с момента открытия внеклеточной ДНК (Chiu Lo Y., Galbezta N. et al., 1997 [1]; Rossa W. K., Chiu Lo. Y., 2011 [2]) плодного происхождения в крови матери и первое ее клиническое применение относилось к детекции SRY и RHD генов плода. Однако, главной целью развития этого направления стало замещение пренатального комбинированного скрининга и инвазивных методов пренатальной диагностики (ПД).
Несмотря на стремительное развитие этой области медицинской генетической диагностики, спустя 17 лет возможности и стоимость NIPT пока не позволяют заменить общепринятую модель пренатального скрининга, а тем более, инвазивную ПД.
Поэтому для более широкого понимания вопроса необходимо остановиться, прежде всего, на вопросах внедрения NIPT в схему пренатального скрининга анеуплоидий, а также осветить первые практические проблемы использования NIPT.
Краткое описание методологических подходов диагностики с использованием внеклеточной фетальной ДНК
На сегодняшний день для анализа внеклеточной фетальной ДНК используют три метода: массовый параллельный сиквенс (massively parallel shotgun sequencing (MPSS)), селективное секвенирование хромосом (chromosome selective sequence analysis (CSS)) и анализ однонуклеотидных полиморфизмов (single nucleotide polymorphism (SNP)) (Gratacos E., Nicolaides K., 2014 [3]; Zimmermann B. et al., 2012 [4]; Nicolaides K. et al., 2013 [5]; Nicolaides K. et al., 2014 [6]).
MPSS
При применении этого метода миллионы фрагментов ДНК всех хромосом материнского и фетального происхождения секвенируются одновременно (параллельно). Это осуществляется с помощью различных платформ полногеномного сиквенса нового поколения (NGS, next-generation sequencing), отличительной особенностью которых является возможность анализа коротких (в районе 146 п. н.) фрагментов ДНК.
Такая методика дает возможность улавливать незначительную разницу в количестве хромосомного материала по каждой из хромосом (т. е. определять как избыток, так и недостаток материала). Например, на 21 хромосоме локализовано всего 1,5% фрагментов, подлежащих анализу, а с учетом низкого содержания фетальной фракции ДНК, необходимо уловить повышение их количества в случае трисомии.
Необходимый минимум содержания фетальной фракции для проведения исследований оценивают в 3–4%, но достоверно стабильный результат получают при 10–15% (Gratacos E., Nicolaides K., 2014 [3]; Elles M. J., 2013 [7]).
CSS
Поскольку наиболее частыми являются только несколько хромосомных анеуплоидий (трисомии 21, 13, 18 и моносомия Х) для уменьшения стоимости исследований было предложено проводить целевой (селективный) сиквенс участков хромосом 21, 13, 18, Х, Y. В последние пару лет этот список расширился до 8 хромосом (21, 18, 13, X, Y, 9, 16, 22).
Также стал возможен анализ частых микроделеционных синдромов (Ди-Джорджи, синдром делеции хромосомы 1p36, синдром Прадера–Вилли/Ангельмана, Cridu Chat , Walf–Hirschhorn).
Риск не получения результата при использовании этого метода составляет 2%. Минимальное необходимое содержание cfDNA оценивается в 3–4% (Gratacos E., Nicolaides K., 2014 [3]; Elles M. J., 2013 [7]).
SNP-тестирование
При использовании данного метода производится анализ 20 000 полиморфных локусов на хромосомах 21, 18, 13, X, Y. Такая диагностика основана на индивидуальных однонуклеотидных отличиях матери и плода. В связи с широким захватом диагностируемых точек анализ можно произвести только с помощью сложных математических подсчетов распределения количества материнских и фетальных локусов. Преимуществом данного метода является то, что он позволяет произвести диагностику триплоидий, что пока недостижимо для других методов. Минимальное необходимое содержание cfDNA оценивается в 3–4%. Главным недостатком такого метода является высокий риск неполучения адекватного результата, достигающий 3–5% (Gratacos E., Nicolaides K., 2014 [3]; Nicolaides K. et al., 2013 [5]; Nicolaides K. et al., 2014 [6])).
Практические возможности и проблемы использования NIPT (преаналитический этап)
Анализ проведенных на сегодняшний день исследований показал, что множество вопросов и проблем возникает уже на преаналитическом этапе проведения NIP-тестов.
К главным проблемам относят: выбор оптимальных гестационных сроков, контроль содержания фетальной фракции, условия транспортировки, контроль выделения фетальной ДНК, а также вес матери.
Выбор оптимальных гестационных сроков. Как уже известно, фетальную ДНК в материнской плазме возможно выявить уже на 32 день гестации, но необходимая для исследования концентрация накапливается только к 7-й неделе (необходимый минимум содержания фетальной ДНК составляет 3–4%) (Soo Hyun Kim et al., 2010 [8]). Так, чувствительность до семи недель оценивается в 50–77% (Bustamante-Aragones A. et al., 2012 [9]).
Однако, последний проведенный мета-анализ показал, что оптимальный срок проведения тестирования составляет 10 недель и позже (Gratacos E., Nicolaides K., 2014 [3]).
Транспортировка. На данный момент проблемы обеспечения правильной транспортировки и разработки ее правил нет, поскольку NIP-тестирование проводят несколько частных лабораторий США, Китая, Европы.
Однако, при прогнозируемой тенденции популяризации данного вида исследований это может стать большой проблемой, поскольку, как сообщалось ранее, для проведения анализа необходимо быстрое очищение cffDNA из материнской плазмы, так как время полураспада ее составляет 16–30 минут, и неопределяемой она становится уже через 1–2 часа (Bustamante-Aragones A. et al., 2012 [9]).
Содержание фетальной фракции и контроль ее выделения. На сегодняшний день тяжело практически в каждом конкретном случае определить долю фетальной ДНК (и ее качественную характеристику), а также отсеивать заведомо неподходящие образцы – с этим связывают 1–5% неудач при проведении исследований (Gratacos E., Nicolaides K., 2014 [3]), а также возможность выдачи ложноотрицательных результатов.
Поэтому часто для обогащения образца cfDNA используют следующие методики: экстракция с использованием формальдегида; сепарация по размеру фрагментов; эпигенетические отличия (метилчувствительная рестрикция, иммунопреципитация (MeDIP)) (Peter A. Benn, 2012 [10]).
Вес матери. В исследовании Ashoor G. c соавт. (2012) было показано, что уровень cffDNA в крови беременной взаимосвязан с двумя основными факторами: вес матери и размеры плаценты [11].
Последние проведенные исследования фирмой «Ariosa» (2014) показали четкую зависимость возможности получения результата NIP-теста от веса матери (таблица 1) [12].
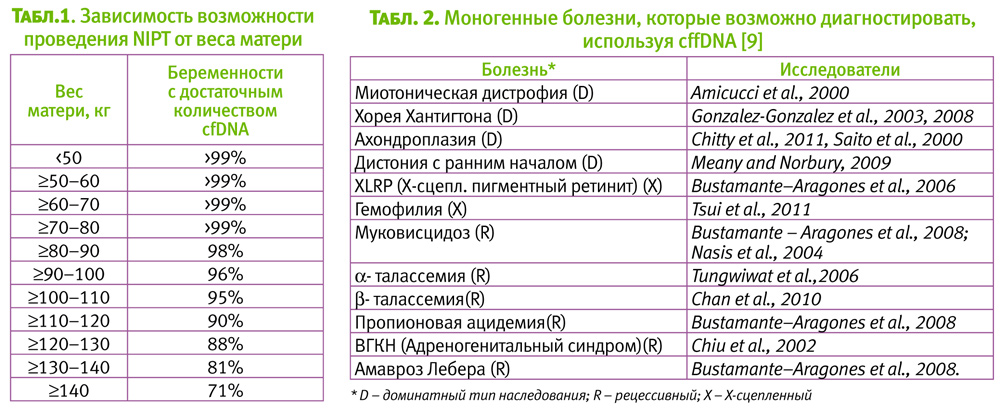
Новейшие практические возможности и проблемы аналитического и постаналитического этапов использования NIPT
Проведенный мета-анализ (Gill M. M. et al., 2014 [13]) практических исследований показал сегодняшние возможности NIP-тестов в отоношении различных видов патологии.
Трисомия 21. Анализ 18 исследований (в общем 809 трисомий 21 и 12 272 одноплодных беременностей без Т21) показал среднюю чувствительность тестов 99% (от 94,4% до 100%), при этом уровень ложноположительных результатов (ЛПР) составил 0,08% (0–2,05%). Уровень чувствительности не отличался для всех трех используемых методов (MPSS, CSS, SNP) ,а вот ложноположительные результаты наблюдались только при использовании метода массового параллельного сиквенса (Gill M. M. et al., 2014 [13]).
Трисомия 18. Изучение 15 работ (301 случай Т18 и 11646 случаев без Т18) показало среднюю чувствительность тестов 96,8% (91,9–100%) и частоту ЛПР равную 0,15% (0–1,98%). И в этом случае большинство ложноположительных проб оказалось при использовании MPSS-метода (Gill M. M. et al., 2014 [13]).
Трисомия 13. Проанализировано 11 работ (85 случаев Т13 и 8339 беременностей без Т13). Чувствительность определения данной трисомии составила 92,1% (78,6–100%) с ЛПР, равным 0,2% (0–1,14%). И в этой группе ложноположительные результаты были выданы только в исследованиях с использованием MPSS-метода (Gill M. M. et al., 2014 [13]).
Моносомия X. В этой группе было изучено 12 работ (139 случаев моносомии Х и 4855 случаев без моносомии Х). Чувствительность определения оказалась на уровне 88,6% при ЛПР 0,12% (все ЛПР получены при использовании MPSS-метода) (Gill M. M. et al., 2014 [13]).
Триплоидии. Как уже описывалось ранее, единственным методом диагностики триплоидий является SNP-тестирование. Однако, здесь также существуют ограничения, поскольку триплоидии представлены двумя фенотипами: диандрией и дигенией, и корректного определения пока добились только для триплодиидий диандрической природы. Такая диагностика позволяет пока только заподозрить наличие дигенической триплоидии на основании низкого содержания фетальной фракции (Nicolaides K. et al., 2014 [6]; Gill M. M. et al., 2014 [13]).
Многоплодие (двойни). Для проведения NIPT двуплодной беременности имеет высокое значение зиготность двойни. На данном этапе является затруднительным анализ монозиготной двойни, поскольку генетически они идентичны. Кроме того, доля фетальной фракции пораженного плода практически всегда меньше, что также затрудняет проведение диагностики. Поэтому авторы методик рекомендуют производить анализ монозиготной двойни по аналогии с одноплодной беременностью (но при этом невозможно определить, какой из плодов имеет генетический дефект), а подход для дизиготной двойни должен основываться на поиске минимальных генетических различий в сравнении с материнским генотипом (Graid. A. Struble at al., 2014 [14]); Maria del Mar Gil et al., 2014 [15]).
По последним данным, проведено только три исследования по проведению NIPT для многоплодных беременностей (18 случаев с Т21 и 209 эуплоидных беременностей). Чувствительность теста составила 94,4% с ЛПР 0%. Также было правильно определено 2 случая трисомии 13 (Gill M. M. et al., 2014 [13]).
Субхромосомные нарушения (микроделеционные синдромы, микродупликации, транслокации). Некоторые компании заявили о возможности проведения субхромосомной диагностики – анализ микроделеций/микродупликаций. Это стало возможным с применением метода «глубокого секвенирования» и анализа до 100 миллионов фрагментов в одном образце. Пока сообщают о возможности диагностики 5 микроделеционных синдромов: синдрома Ди-Джорджи, синдрома делеции хромосомы 1p36, синдрома Прадера–Вилли/Ангельмана, Cridu Chat (синдром кошачьего крика), Walf–Hirschhorn с размером делеций от 2 до 10 Мb (FMF’s 13th World Congress in Fetal Medicine, 2014 [12]).
Также имеются сообщения о первых попытках диагностики микродупликаций 7, 15, 22 хромосом и транслокации 45, XX-15 der (21) t (15;21) (q15; p11.2) (Anupama Srinivasan et al., 2013 [16]).
Это существенно расширает диагностические возможности, поскольку визуально при кариотипировании возможно определить делецию ³7–10 Mb, при применении FISH метода – от 0,8 Mb, а при использовании array CGH — 5–100 kb.
Мозаичный кариотип. Широкомасштабных исследований в этом направлении пока не проводилось, однако первые попытки определения мозаичного кариотипа проводятся.
Согласно первым результатам, пока отмечают высокую частоту ложноотрицательных тестов и нечувствительность к низкому уровню мозаицизма (M. Yao et al., 2014 [17]).
Моногенные заболевания. NIPD применяется для диагностики заболеваний, унаследованных от отца, реже – заболеваний возникших de novo (Rossa W. K., Chiu Lo. Y., 2011 [2]; Saito H. et al., 2000 [18].
В основном, проводят диагностику следующих аутосомно-доминатных заболеваний: ахондроплазии, миотонической дистрофии, с-ма Хантингтона.
Диагностика аутосомно-рецессивных заболеваний проводится только в случае, если супруги являются носителями разных мутаций в определяемом гене. Такой подход применяется для муковисцидоза, талассемии, метаболических заболеваний, гемоглобинопатий и ретинопатий.
При наличии у родителей одинаковых мутаций применяют подход подсчета относительной дозы мутации RMD (relative mutation dosage) (Lun FMF et al. [19]). Этот подход является очень проблематичным в практическом исполнении.
Однако, это не отменяет последующие инвазивные вмешательства, только сокращает группу обследуемых.
Для определения заболеваний de novo диагностическим критерием для отбора пациентов группы риска по-прежнему являются УЗ-маркеры.
Резус-статус и пол плода. Несмотря на то, что диагностика пола и резус-статуса плода положила начало неинвазивной диагностике, до сегодняшнего дня эти методы все еще имеют существенные погрешности.
С 2001 года резус-типирование с использованием cffDNA применяется при ведении женщин с повышенным риском гемолитической болезни новорожденных до развития угрозы для плода или повышения титра (SAC Opinion, 2009 [20]; Daniels G. et al., 2006 [21]). Принцип метода заключается в поиске последовательности ДНК, характерной для гена RhD. Недостатками данного метода являются: невозможность подтверждения выделения плодной ДНК; ложноотрицательный результат как следствие низкой концентрации cfDNA; только для одноплодных беременностей; возможность расхождения генотипа и фенотипа (1% для Европеоидной расы). По подсчетам, риск ложноотрицательного результата составляет около 0,2% (SAC Opinion, 2009 [20]; Daniels G. et al., 2006 [21]).
Определение пола плода проводятся с применением в качестве диагностического маркера генов DYS14 или SRY, расположенных на Y-хромосоме (SAC Opinion, 2009 [20]). Чаще всего такие исследования проводят для исключения X-сцепленных заболеваний (часто врожденной гиперплазии коры надпочечников, гемофилии, миопатий) [22]. Недостатки сходны с методикой определения RHD-гена и кроме того, возможно определение только генетического пола; не исключает наличие генной/хромосомной патологии (н-р, синдромы де ла Шапеля, Нунан, Сваера, тестикулярной феминизации и т. д.).
Ошибка при тестировании после 7 недель беременности составляет 2,2%, а на более ранних сроках — еще больше (SAC Opinion, 2009 [20]).
Первые казусные случаи
Первые зафиксированные казусные случаи пока отодвигают присвоение статуса диагностической процедуры NIP-тестам.
Одной из таких проблем оказалась проблема гипердиагностики. Так, согласно данным Mathias Ehrich [12], из проанализированных 4500 образцов обнаружено 33 случая микроделеций/микродупликаций, 9 случаев (27,3%) микроделеций клинически интерпретировать не удалось, поскольку они ранее были неизвестны. Таким образом, частота патологических беременностей повысилась до 1:200 (что соответствует критерию «каждая женщина >37,5 лет»).
Также появилось сообщение о ошибочном тестировании. Так, в одной из последних публикаций [23] описывался следующий случай: с помощью NIPT в сроке 12 недель был диагностирован высокий риск Т13, плод мужского пола. При этом, проведенное кариотипирование ворсин трофобласта дало следующий результат – 47, XY+18.
В связи с наличием определенных имеющихся недостатков, данная методика меняла свое название, соответственно менялись и критерии ее оценки – от диагностической процедуры (NIPD) к тесту (NIPT) и до NIPS (неивазивный пренатальный скрининг). И ее обратный переход от скрининговой к диагностической процедуре ожидается по предварительным оценкам, не ранее 2017 года [12].
Место NIPT в современной модели пренатального скрининга хромосомных аномалий
Как известно, исторически первой моделью скрининга хромосомных анеуплоидий (большей частью, синдрома Дауна) был скрининг, основывающийся на возрасте матери, который начал применяться с конца 1960-х годов и на протяжении почти 20 лет оставался единственным инструментом отбора на инвазивную ПД. Чувствительность такого подхода оценивалась в пределах 30% с ЛПР около 15% (табл. 3).
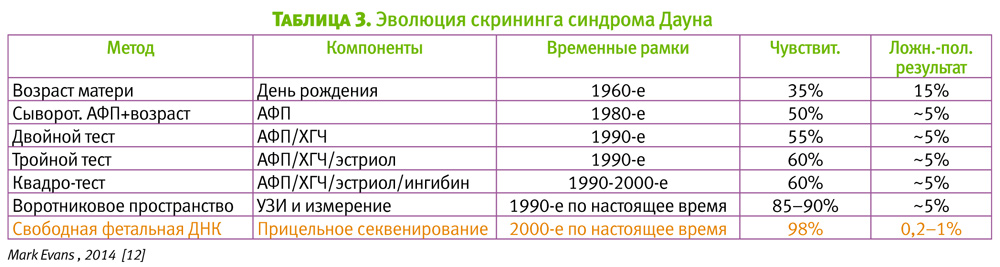 В 1980-90-х годах скрининг основывался на биохимических маркерах ІІ триместра и детальном ультразвуковом исследовании, при этом его чувствительность составляла 55–65% при ЛПР около 5%.
В 1980-90-х годах скрининг основывался на биохимических маркерах ІІ триместра и детальном ультразвуковом исследовании, при этом его чувствительность составляла 55–65% при ЛПР около 5%.
В 1990-х годах акцент сместился на I триместр и за последние 15 лет чувствительность комбинированного скрининга (в 11–14 нед.) в детекции трисомии 21 достигла 85–90% с ЛПР 5%.
Практически до последних лет критерием отбора для проведения инвазивной ПД было пороговое значение риска, приравнивающееся к материнскому возрасту 35 лет (1:250). При таком пороговом значении выявляемость трисомии 21 составляла 0,4% и, с учетом риска СА 0,5–1%, происходило 1–2 прерывания с эуплоидными плодами (после инвазивной ПД).
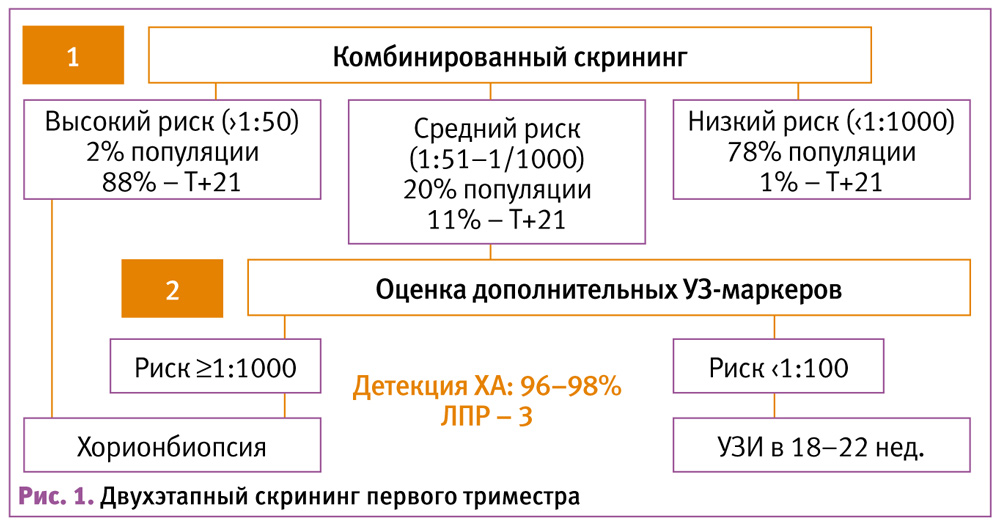
Относительно недавно было предложено применение двухэтапного ранжированного скрининга (рис. 2), когда на первой его стадии оценка риска осуществляется по результатам стандартного комбинированного скрининга (возраст матери, ТВП плода и сывороточные маркеры PAPP-A, b-ХГЧ). У пациенток с риском 1:50 и более анализ считался положительным, а с риском менее 1:1000 – отрицательным. Пациентки с промежуточным риском от 1:51 до 1:1000 проходят вторую стадию скрининга (с прицельной оценкой носовой кости, кровотока в венозном протоке и через трикуспидальный клапан или печеночную артерию), которая модифицирует риск, подсчитанный на первом этапе. Если скорректированный риск составляет 1:100 и более, результат скрининга считается положительным, т. е. предполагает последующее проведение инвазивной процедуры.
На X Всемирном конгрессе Медицины плода (Мальта, 2011 г.) [24] было рекомендовано пороговое значение 1:150. Чувствительность обнаружения ХА в этой модели скрининга составляет 96% при ЛПР 3% (рис. 1) [25].
Логичным было бы предположить, что дальнейшее развитие в этой области должно отвечать следующим задачам: максимальное повышение чувствительности и снижение доли ложноположительных результатов и соответственно, сокращения инвазивных процедур.
 Такая возможность появилась с внедрением NIP-тестов. Однако, несколько лет велись дискуссии о месте NIPT в структуре пренатального скрининга ХА.
Такая возможность появилась с внедрением NIP-тестов. Однако, несколько лет велись дискуссии о месте NIPT в структуре пренатального скрининга ХА.
За это время уже полностью был закрыт вопрос о замещении инвазивной ПД на NIPT, поскольку уровень данного тестирования не соответствует пока критериям диагностической процедуры (рис. 1) (Yiu Man Chan et al., 2014 [26]).
В 2014 году на XIII Всемирном конгрессе по медицине плода (FMF) состоялась отдельная секция, посвященная NIPT, в которой участвовало большое количество экспертов со всего мира. В рамках обсуждения были предложены новые стратегии применения NIPT (рис. 2).
Самая эффективная модель по подсчетам экономической и социальной целесообразности была представлена в виде так называемого «контингентного скрининга» (K. H. Nicolaides, M. M. Gill) (это понятие заменило предыдущее, когда биохимический тест во втором триместре производится только у пациенток из средней группы риска после комбинированного скрининга I триместра и по результатам второго БХ теста решается, необходимо ли пренатальное кариотипирование).
Новая модель контингентного скрининга основана на последовательном применении комбинированного скрининга (с пересмотренной градацией риска по группам) (рис. 3) и NIPT, по результатам которого определяется необходимость проведения инвазивной ПД.
По подсчетам K. H. Nicolaides, применение «рутинного скрининга» (NIPT вместо комбинированного скрининга) позволило бы повысить чувствительность теста до 99% для Т21, Т18 и 96% для Т13 с необходимостью применения инвазивной ПД в 1% популяции.
Модель же контингентного скрининга при почти аналогичной чувствительности к указанным трисомиям позволяет снизить уровень инвазивных вмешательств до 0,8%, что существенно в масштабах популяции [12].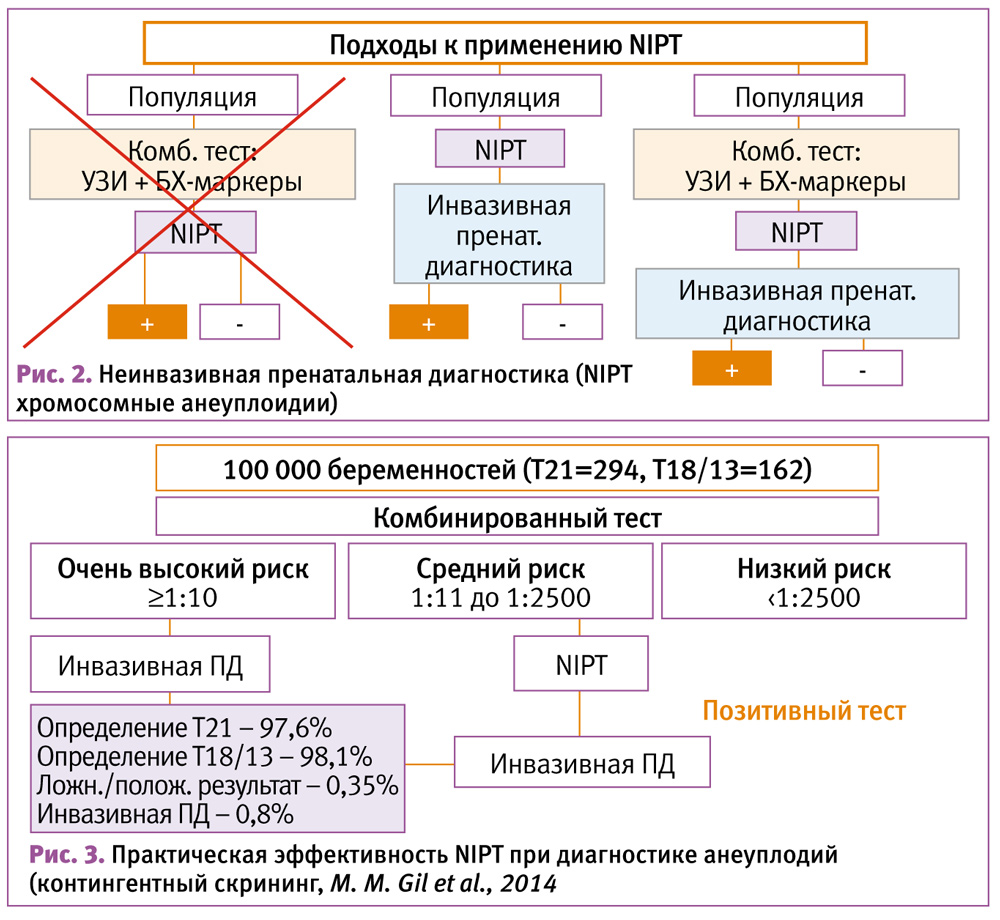
Стоимость исследований
Для тестирования на хромосомные анеуплоидии широкое внедрение NIPT пока остается под вопросом, учитывая высокую стоимость исследований (в Европе стоимость проведения одного теста на анеуплоидии оценивается в 500–2500 EUR.
Стоимость выявления каждого дополнительного случая с-ма Дауна при использовании рутинного скрининга (NIPT) составляет 4 млн. USD.
Если применить к комбинированному скринингу воротниковое пространство (ВП), PAPP-A, b-CGH (стоимостью 200 USD) + 2 дополнительных БХ-маркера PIGF, AFP (+50 USD) + NIPT = контингентный скрининг, то затраты на одного плода с с-м Дауна составят 2,2 млн. USD. При этом, примечательно, что пожизненное содержание человека с синдромом Дауна – 1 млн. USD [30].
Что касается ближайших перспектив дальнейшей интеграции указанных моделей пренатального скрининга в широкую клиническую практику, то по мнению экспертов и многих участников, принимавших активное участие в работе FMF’s 13th World Congress (2014), широкое использование NIPT станет возможным тогда, когда стоимость одного исследования составит около 50 USD/EUR и будет оплачиваться национальными программами и страховыми компаниями.
Первые сообщение о практическом применении рутинного скрининга с использованием NIPT
Модель рутинного скрининга была апробирована на базе South Shore hospital in Massachusets (США) в 2012–1013 гг. [29]. В исследовании приняли участие 1228 женщин. Все пациентки в I триместре прошли ультразвуковое обследование с измерением воротникового пространства (ВП) и обнаружением других структурных аномалий. 96,4% обследованных имели нормальные результаты, расширение ВП, шейная цистогигрома и другие структурные аномалии обнаружены в 3,6% случаев. Из 1184 женщин с нормальными результатами по УЗИ 1153 пациентки прошли NIP-тест. Результат NIPT не удалось получить в 1,2% случаев (14 пациентов). При этом, в дальнейшем в двух случаях были диагностированы осложнения беременности, а в одном – триплоидия.
Таким образом, согласно проведенному протоколу обследования, удалось выявить 15 из 16 аномалий и снизить количество инвазивных процедур по ложноположительным результатам из 30 (за аналогичный период прошлого года) до 4.
Выбор пациента
Yiu Man Chan et al. (2014) провели исследование по оценке мнения женщин относительно применения неинвазивной/инвазивной диагностики. Из 358 приглашенных женщин в исследовании приняли участие только 106 (29,6%), 19,6% выбрали инвазивную пренатальную диагностику и 10% выбрали NIPT. Из необследованных женщин по опросу 50% склонялось к применению NIPT [26].
Это исследование, в принципе, основывалось на общественном мнении по поводу пренатальной диагностики. Так, отмечается, что существуют разные группы пациентов: одни желают получить максимум информации, провести все необходимые процедуры и исследования, чтобы получить «совершенного ребенка» (как правило, это пары старшей возрастной группы); другие хотят иметь ребенка в принципе, не имея о нем заранее никакой информации (как правило, это пары младшей возрастной группы) [12].
Обсуждение
Неоспоримым остается тот факт, что NIPT стремительно захватывает область пренатального скрининга ХА и ее бурное развитие в различных направлениях в скором будущем откроет новые ранее не достижимые возможности диагностики различной генетической патологии.
Поэтому не удивительным является факт наличия как ярых приверженцев, так и скептически настроенных и настороженных специалистов к данному виду диагностики. Такая тенденция наблюдается практически для всех значимых внедрений, претендующих на массовое использование.
В свое время подобная картина наблюдалась в отношении внедрения массового пренатального биохимического скрининга. Так, на одном из первых конгрессов по медицине плода в 90-е годы ХХ века, прозвучавшей репликой «Stop biochemistry!» было высказано негативное отношение к пренатальному биохимическому скринингу в связи с его экспансией и в то время низкой чувствительностью при относительно частых ложноположительных результатах. Однако, после объединения двух подходов (до этого применяющихся независимо один от другого), увенчавшегося созданием модели комбинированного скрининга I триместра [27] с математическим расчетом индивидуального риска ХА, эта стратегия стала эффективной, рекомендована FMF и принята во многих странах мира. Индивидуальный риск, полученный после второго биохимического (ди-, трипло-, квадро-) теста также может быть дополнительно пересчитан с учетом каждого из обнаруженных УЗ-маркеров с помощью доступных электронных калькуляторов [http://www.perinatology.com/calculators/Down%20Syndromee%20Revised%20Risk.htm]. Однако, внимание экспертов и исследователей, занимающихся разработкой и оптимизацией стратегий пренатального скрининга ХА, по-прежнему остается сфокусированным преимущественно на I триметре беременности. Что касается сегодняшних реалий применения NIPT, самым значимым фактором, останавливающим массовое применение, остается его стоимость.
Также немаловажны временные рамки выполнения (от 10 дней до 3–4 недель), т. е. получается, что пока проведение биопсии хориона и кариотипирование даст более быстрый и более точный (надежный) результат.
Таким образом, остающиеся сегодня недостатки NIPT пока не дают возможности говорить о ближайшей перспективе полного замещения пренатального биохимического скрининга (что предполагает сворачивание целой индустрии), а тем более, инвазивной пренатальной диагностики. Однако, применение таких тестов открывает дополнительные диагностические возможности, что соответственно, дает толчок для дальнейшего развития и совершенствования таких технологий.
Мы осмелимся сделать предположение, что со временем, когда цены на NIPT станут значительно доступнее, а MPSS-технология будет давать стабильные высокодостоверные результаты (в сроке 7–9 нед.) по выявлению широкого спектра ХА, – неизвазивные тесты также смогут предлагаться женщинам с привычным невынашиванием беременности перед назначением сохраняющей терапии.
Кроме этого, следует отметить, что помимо наблюдаемого широкого применения внеклеточной ДНК для пренатального исследования, отдельным направлением является неинвазивная пренатальная диагностика с использованием внеклеточной фетальной РНК (уже используется для диагностики анэуплоидий и прогнозирования преэклампсии и преждевременных родов) и клеток плода в материнской крови [29], описание достижения которых требует отдельной публикации.
Полный список литературы
находится в редакции.


коментариев