Среди патологии репродуктивной системы мастопатия занимает лидирующую позицию. Доброкачественные заболевания молочных желез выявляются у 25% женщин в возрасте до 30 лет и у 60% пациенток старше 40 лет. Наиболее часто наблюдается диффузная форма доброкачественной дисгормональной дисплазии молочных желез (№60 по МКБ-10), составляющая 60–80% в популяции. На современном этапе следует рассматривать мастопатию как фоновое заболевание для развития рака молочных желез. Только ранняя диагностика патологии молочных желез на стадии диффузного гиперпластического процесса и проведение патогенетического лечения, а также наблюдение за этими пациентками реализуют профилактику рака молочной железы. Пока же мы наблюдаем страшную реальность – рак молочных желез в настоящий момент занимает 1-е место в онкологической заболеваемости и смертности женщин России [1–3].
 Практическая медицина как никакая другая деятельность, нуждается в разработке методов и критериев, обеспечивающих объективные обоснования принимаемых при обследовании пациентов решений. Доказательная медицина (evidence based medicine) становится технологией и философией современной медицины [4].
Практическая медицина как никакая другая деятельность, нуждается в разработке методов и критериев, обеспечивающих объективные обоснования принимаемых при обследовании пациентов решений. Доказательная медицина (evidence based medicine) становится технологией и философией современной медицины [4].
С 2009 г. выявление и лечение доброкачественной патологии молочных желез входит в обязанности специалиста акушера-гинеколога (приказ Минздрава РФ от 24.09.2008 №623 «О мерах по усовершенствованию акушерско-гинекологической помощи населению РФ», приказ Минздрава РФ от 02.10.2009 №808н «Об утверждении оказания акушерско-гинекологической помощи»). Однако практическая реализация должного встречает определенные затруднения.
Основой для выявления патологии молочных желез является применение ультразвукового исследования (УЗИ) и методов лучевой диагностики – маммографии, магнитно-резонансной томографии. Именно гинеколог должен стать для женщины первым специалистом для выбора дифференцированной тактики: ежегодное наблюдение, лечение диффузных форм мастопатии у гинеколога или направление к онкологу при выявлении узловых форм заболевания и рака молочных желез [5, 6]. Для этих целей наиболее удобным и доступным диагностическим методом является УЗИ. Однако на современном этапе мы имеем трудности, касающиеся интерпретации сонографических характеристик клинических форм диффузной мастопатии разными авторами, что затрудняет работу практикующего специалиста и не позволяет решить глобальную задачу, а именно выполнить раннюю профилактику развития рака молочных желез [7–9].
Цель исследования
Создание современной математической модели ультразвуковой диагностики дисгормональной патологии молочных желез. При помощи разработанной математической модели оценить эффективность препарата Мастодинон в терапии доброкачественной дисплазии молочных желез.
Материалы и методы
В рамках целевой межведомственной научно-практической программы «Здоровье женщины», совместного проекта ГБОУ ВПО «Сибирский государственный медицинский университет» (г. Томск), ФГБУ «Научно-исследовательский институт фармакологии Сибирского отделения РАМН» (г. Томск), ФГБУ «НИИ психического здоровья Сибирского отделения РАМН» (г. Томск) обследовано 266 женщин репродуктивного возраста (руководитель программы – проф. Л. С. Сотникова). Средний возраст пациенток в исследовании был 30,4±0,3 года. Из них 223 пациентки имели в соответствии с клинико-рентгенологической классификацией Н. И. Рожковой (1993 г.) диагноз ДДДМЖ. Наличие дисгормональной патологии молочных желез верифицировалось с помощью УЗИ с использованием линейного датчика 14 МГц с применением цветового и энергетического допплеровского картирования в I фазу менструального цикла (5–10-й день), пациенткам старше 35 лет дополнительно выполняли рентгенологическую маммографию.
Полученные эхографические показатели позволили разделить пациенток с ДДДМЖ на 4 клинические группы: 1-я группа (n=93) – с преобладанием железистого компонента; 2-я группа (n=69) – с преобладанием кистозного компонента; 3-я группа (n=33) – с преобладанием фиброзного компонента; 4-я группа (n=28) – смешанной формы.
Для оценки индивидуальных особенностей пациентки был реализован алгоритм неоднородной последовательной процедуры распознавания в модификации А. А. Генкина, основной целью которого явилась разработка принципов врачебной технологии, позволяющая делать доказательные выводы о состоянии здоровья каждой обследуемой женщины [10].
Из статистических методов обработки результатов обследования проводился анализ вариационных рядов методами описательной статистики с вычислением медианы (Ме) и верхнего и нижнего квартилей. Качественные признаки оценивались путем вычисления абсолютных и относительных частот. Анализ различий по количественным признакам выполнялся методами множественного сравнения независимых групп (ANO-VA – критерий Краскела–Уоллиса) и методами сравнения 2 независимых групп (U-тест Манна–Уитни). Для изучения связей между признаками применялся корреляционный анализ Кенделла. Разницу значений принимали статистически значимой при p<0,05. Статистический анализ данных осуществлялся при помощи пакета программ Statistica 6,0 (StatSoft, USA).
Результаты и обсуждение
Для решения поставленных задач были сформированы 2 группы обследованных женщин: обучающая (n=135) и тестовая (n=88). Из всех эхо-признаков (толщина пре- и ретромаммарной клетчатки, наличие кист, изменение скорости кровотока и эхогенности железистой ткани, наличие перидуктального фиброза и др.), определенных в процессе работы, была построена последовательность, в которой признаки располагались в порядке убывания информативности.
Для обучающей группы в ходе исследования были получены соответствующие диагностические коэффициенты каждого из признаков для двух возможных состояний – «болен», «здоров». Для каждой формы ДДДМЖ по диагностическим коэффициентам с учетом информативности признаков были созданы соответствующие диагностические таблицы.
Качество распознавания с использованием диагностических таблиц затем было проверено при участии тестовой группы женщин. Диагнозы для женщин тестовой группы, полученные с помощью предложенной методики – неоднородной последовательной процедуры распознавания, сопоставлялись с ранее полученными клиническими данными, затем определялось количество правильно и неправильно принятых решений. Анализ полученных результатов показал, что риск ошибки составляет 0,3–0,7 при 95% ДИ, а построенные диагностические таблицы позволяют получить дополнительную информацию для повышения качества диагностики и прогнозирования заболевания. Полученные диагностические таблицы обеспечивали следующее качество распознавания: для ДДДМЖ с преобладанием железистого компонента – 94%, с преобладанием кистозного компонента – 87%, с преобладанием фиброзного компонента – 84%. При смешанном варианте отношение риска составило 0,6 при ДИ 95%.
Практическая значимость разработанной нами математической модели не только позволяет просто и объективно диагностировать форму ДДДМЖ в любом возрасте с применением метода УЗД, но и оценить эффективность проводимых лечебных мероприятий с позиции доказательной медицины (патент РФ от 10.06.2012 №2452389 «Способ дифференциальной диагностики форм фиброзно-кистозной болезни у женщин с сохраненной репродуктивной функцией»).
С применением разработанной нами математической модели в рамках целевой межведомственной научно-практической программы «Здоровье женщины» (СибГМУ, НИИ фармакологии СО РАМН, НИИ психического здоровья СО РАМН) проведена оценка эффективности терапии ДДДМЖ лекарственным препаратом Мастодинон (Бионорика CE, Германия). Клиническое исследование (IV фаза) являлось проспективным (параллельные группы) рандомизированным моноцентровым сравнительным.
В программу исследования вошли 160 пациенток репродуктивного возраста от 24 до 43 лет (средний возраст 34,2±2,2 года) с наличием ДДДМЖ. Препаратом для лечения у 83 пациенток (основная группа) являлся Мастодинон (капли для приема внутрь) в суточной дозе 60 капель курсом 12 нед. и дальнейшим сроком наблюдения до 24 нед. (3 мес). Группа сравнения была сформирована из 37 пациенток, не получавших консервативное лечение. В течение исследования пациентки этих групп посещали врача 3 раза – до начала исследования (визит 0), в начале лечения (визит 1) и через 3 мес. после начала лечения (визит 2). Контрольную группу составили 40 практически здоровых женщин, сопоставимых с основной группой по возрасту, без соматической и гинекологической патологии. У всех женщин было получено добровольное информированное согласие на участие в исследовании.
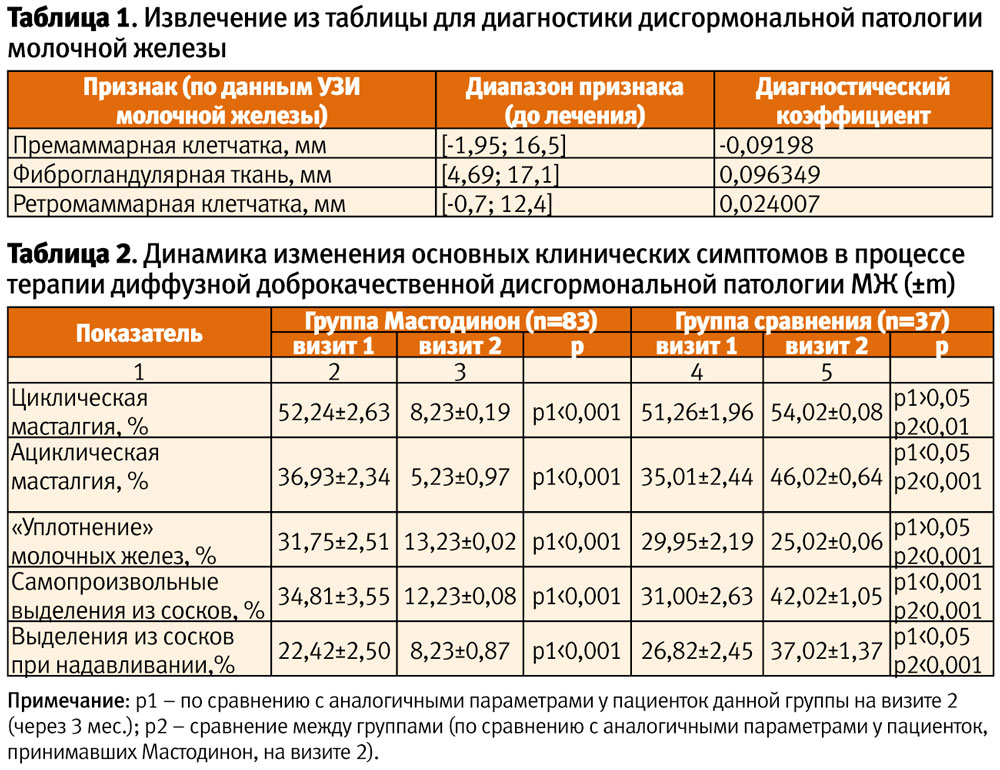
Полученные при объективном осмотре данные были автоматически обработаны с помощью предлагаемого нами диагностического алгоритма. В табл. 1 представлена часть перечня признаков (ключевые эхо-показатели): диапазон, в который попадает признак, и диагностический коэффициент, соответствующий данному диапазону.
При математической обработке полученных результатов сумма всех диагностических коэффициентов была равна 3,836121, что больше, чем пороговое значение, равное 0,97, т. е. основная когорта обследуемых пациенток (n=52) имела ДДДМЖ с преобладанием железистого компонента.
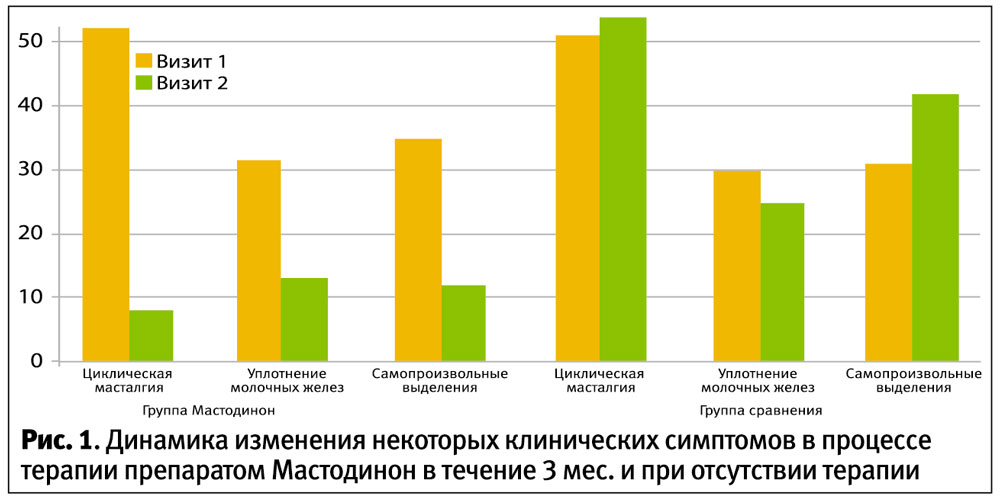
При систематизации многообразных клинических проявлений доброкачественной дисплазии молочных желез у обследованных пациенток выявлено, что основной жалобой являлась умеренно выраженная масталгия, носящая циклический характер. Помимо этого, женщины предъявляли жалобы на ациклическую масталгию, «уплотнение» молочных желез, выделения из сосков – как самопроизвольные, так и при надавливании. На визите 1 основная группа и группа сравнения были сопоставимы по частоте предъявляемых жалоб (p>0,05). Динамика клинических проявлений у пациенток 2 групп представлена в табл. 2 и на рисунке.
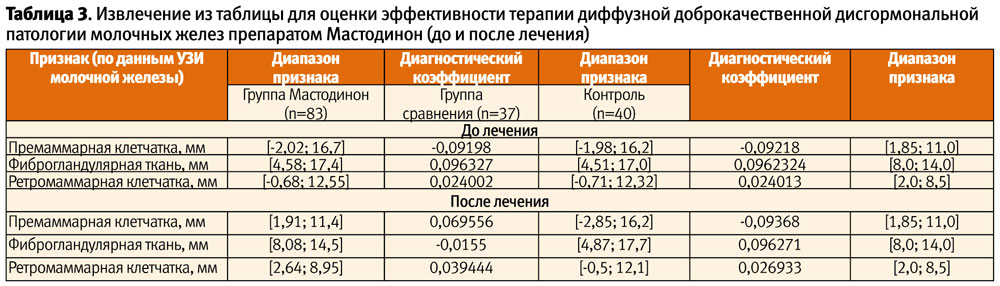
Таким образом, на фоне проводимого лечения препаратом Мастодинон статистически значимо уменьшилась доля пациенток, предъявлявших жалобы; в то же время женщины, не получавшие терапию, стали предъявлять жалобы чаще.
Через 3 мес. (12 нед.) терапии при контрольном обследовании собранные клинико-анамнестические, лабораторные данные и результаты УЗ-сканирования молочных желез пациенток были в виде абсолютных значений признаков внесены в предлагаемый алгоритм с последующим пересчетом диагностических коэффициентов. После математической обработки полученных результатов было выявлено, что основными значимыми объективными критериями оценки эффективности проводимой терапии являлись эхографические показатели (измерение толщины премаммарной клетчатки, толщины фиброгландулярного слоя и толщины ретромаммарной клетчатки). В табл. 3 представлены величины основных эхографических показателей у пациенток всех 3 групп в начале и в конце периода наблюдения.
На визите 3 сумма всех диагностических коэффициентов в группе Мастодинона составила -3,02376, что меньше, чем пороговое значение (-1,255272505). Следовательно, мы сделали вывод, что эхографические показатели состояния молочных желез через 3 мес. терапии препаратом Мастодинон (Бионорика CE, Германия) вошли в диапазон значений, соответствующих показателям здоровых женщин контрольной группы.
Обсуждение результатов и выводы
Сформулированный ведущий диагностический алгоритм и выработанные диагностические коэффициенты для каждой конкретной формы заболевания обеспечивают качество распознавания 87–94% случаев, что позволяет существенно ускорить и облегчить работу специалиста в качественной диагностике дисгормональной патологии молочных желез. На примере применения разработанной нами математической модели возможно максимально объективно проводить диагностику и оценку эффективности проводимой терапии дисгормональной патологии молочных желез (патент РФ от 10.06.2012 №2452389 «Способ дифдиагностики форм фиброзно-кистозной болезни у женщин с сохраненной репродуктивной функцией»).
Лекарственный препарат Мастодинон (Бионорика CE, Германия) действительно имеет доказанную высокую эффективность при терапии ДДДМЖ. Результаты исследования убедительно продемонстрировали как выраженное улучшение клинической картины с практически полным исчезновением жалоб у пациенток (субъективная оценка), так и значимое улучшение эхографических показателей (объективная оценка).
При этом было подтверждено, что отсутствие терапии у пациенток с дисгормональной патологией молочных желез приводит к неблагоприятному прогрессированию основных признаков клинической картины и данных эхографических характеристик заболевания.
Таким образом, в настоящее время мы имеем удобную для широкого применения в практическом здравоохранении математическую модель для ультразвуковой диагностики и объективной оценки эффективности терапии доброкачественной дисплазии молочных желез, что позволяет осуществляемую гинекологами раннюю профилактику рака молочных желез вывести на качественно новый уровень.
Список литературы находится
в редакции.

коментарів