 Когда невозможное становится возможным
Когда невозможное становится возможным
Проблема сохранения репродуктивной функции онкологических пациентов давно привлекала внимание медицинской общественности, и это один из вопросов, актуальность которых формировалась не только по запросу врачей, но и по инициативе самих пациентов. С 2006 года проблема начала обсуждаться в среде мировых онкологов, на конференциях и симпозиумах
Насколько важно сохранять репродуктивную функцию пациентов с онкологическими заболеваниями? Об этом спросили непосредственную целевую аудиторию – десять тысяч респондентов, пациентов с злокачественными новооразованиями. Почти все из них ответили, что это важно не только с точки зрения сохранения репродуктивной функции, но и с точки зрения сохранения качества жизни.
Практически 100% опрошенных пациентов отметили, что если лечащий врач задавал вопрос: «Хотите ли в будущем иметь детей?», то вера в выздоровление и положительный результат лечения значительно усиливались.
Исходя из сказанного, можно уверенно опровергнуть мнение о том, что пациентам с раком не до планирования беременности; мол, они или умрут, или будут рады, что выжили.
И сейчас, когда достижения современной медицины позволяют бороться с онкологическими заболеваниями, сохраняя не только жизнь женщины, но и ее репродуктивную функцию, мы обязаны давать пациентам шанс не только на жизнь, но и на возможность иметь в будущем детей. Вспоминаются слова известной актирисы, певицы Селин Дион: «Нет желания сильнее, чем желание иметь своих детей». Как известно, ее муж Рене перед проведением лечения по поводу рака прошел процедуру криоконсервации спермы, и после его выздоровления паре удалось стать родителями.
Теме сохранения репродуктивной функции пациенток с раком был посвящен доклад ассистента кафедры онкологии НМУ им. А. А. Богомольца, к. мед. н. Ю. А. Тимовской. Не только теория и мировая статистика, но также свой собственный опыт, и впечатляющие достигнутые результаты – благодаря всему этому выступление Ю. А. стало одним из самых ярких событий конференции «Онкопатология и репродуктология – возможности и перспективы», которая состоялась 29 октября в Киеве.
Мы решили опубликовать главные тезисы ее доклада «Сохранение репродуктивной функции у онкологических пациенток». Уверены, что удобный для восприятия формат «из первых уст» поможет каждому врачу акушеру-гинекологу, читающему журнал, пополнить свой багаж практических знаний.
После рака
Актуальность проблемы сохранения фертильности обусловлена повышением уровня онкологической заболеваемости среди лиц молодого возраста в целом, а также тем, что достижения современной медицины позволили значительно увеличить популяцию long term survivors, т. е. людей, прошедших успешное лечение от рака, имеющих устойчивую ремиссию и хороший прогноз.
Сохранение репродуктивной функции у больных со злокачественными образованиями еще недавно было у нас под большим запретом, сегодня мы только начинаем обсуждать эти вопросы, в то время как во многих странах уже приняты стандарты ведения таких пациенток.
Во всем мире сентябрь традиционно посвящен людям, перенесшим онкологическое заболевание в детстве. Согласно статистике, около 30 лет назад в мире было всего лишь 3–4 миллиона людей до 40 лет, болевших раком в детском возрасте и излечившихся, а сегодня их почти 12 миллионов. Один человек из каждых 600 перенес онкологическое заболевание, при этом 83% из них имеет благоприятный прогноз! (Jeruss J. S., Woodruff T. K., 2009).
Вернемся к причинам, обусловившим такую динамику: это диагностика злокачественных процессов на ранних, зачастую доклинических стадиях, популяризация скрининговых программ обследований, успехи молекулярной биологии и онкологии (открытие рецепторов на мембранах опухолевых клеток, изучение сигнальных путей внутри клетки, а также путей активации апоптоза), позволившие внедрить таргетные методы лечения. Усовершенствование лучевой терапии (прежде всего, изобретение и широкое внедрение в клиническую практику киберножа и линейных ускорителей), а также разработка и использование новых цитостатических препаратов улучшило как непосредственные, так и отдаленные результаты лечения онкологических пациентов. Повторюсь, что все это в совокупности обеспечило большой прирост популяции пациентов, которые получали специальное лечение по поводу злокачественных новообразований, и среди которых можно прогнозировать не только хорошие отдаленные результаты лечения, но и сохранение репродуктивной функции.
Чего хотят пациенты?
Общеизвестно, что лечение онкологического заболевания имеет свои последствия. Большинство пациентов больше всего беспокоятся об изменениях внешности, таких как выпадение волос, прибавка массы тела, а также о появлении у них тошноты и рвоты на фоне проведения цитостатической терапии. Есть те, которые задают вопросы о печеночной токсичности противоопухолевой терапии и о ее воздействии на сердце. Однако есть и такие, которых интересует вопрос сохранения их женского здоровья, нормальное функционирование яичников после проведения курсов полихимиотерапии.
Известно, что лучевая и химиотерапия имеют высокую тропность к тканям с высоким митотическим потенциалом, таким как волосяные фолликулы, кишечный эпителий, лейкоциты и ткань яичника. Например, дети, которые получали специальное лечение по поводу злокачественного новообразования до наступления пубертатного возраста, нередко нуждаются в заместительной гормонотерапии для наступления полового созревания.
Противоопухолевое лечение также ассоциируется с ятрогенной недостаточностью яичников, которая может проявляться наступлением ранней менопаузы, а также снижением гормонпродуцирующей функции яичников до уровня ниже необходимого для наступления овуляции.
Риск преждевременного истощения яичникового резерва зависит от уровня овариальной токсичности цитостатика, его комбинации с другими цитостатическими агентами, схем ПХТ, доз и режимов введения. Ранняя менопауза также может развиваться у пациенток, которые получали лучевую терапию на область малого таза и головного мозга. Также имеет значение возраст пациентки: чем ближе к 40 годам, тем выше вероятность истощения яичникового резерва. По нашим данным, аменорея возникает у 70–80% женщин, получавших химиотерапию по поводу рака молочной железы в возрасте до 40 лет.
У женщин также может сохраняться МЦ, однако, отмечается снижение уровня эстрогенов, продуцируемых яичниками ниже уровней необходимых для овуляции и наступления беременности.
Правильный выбор
Не все цитостатики одинаково гонадотоксичны. Наибольшее влияние на половую систему оказывают циклофосфамид, бевацизумаб, доксорубицин и карбоплатин. Эти препараты применяются у больных раком молочной железы, лимфопролиферативными заболеваниями, злокачественными опухолями кишечника и половых органов. К группе с выраженной гонадотоксичностью относятся также дакарбазим (применяется при меланоме, лимфомах).
И наоборот метотрексат, который также широко применяется у онкологических пациенток, имеет низкую степень гонадотоксичности (Donnez et al., 2006) (табл. 1).
 Сохранять или не сохранять?
Сохранять или не сохранять?
Чем выше эффективность проводимой противоопухолевой химиотерапии, тем ниже шанс сохранения нормальной овариальной функции. Однако многие пациентки хотят не только выжить, но и иметь детей в будущем. Впервые этот вопрос был поднят в 2006 году, когда ASCO разработала руководство по сохранению репродуктивной функции у онкологических больных (www.asco.org/guindlines/AmericanSocietyofClinicalOncology).
Официально опубликованные рекомендации Американской ассоциации клинических онкологов (к сожалению, пока нет отечественных рекомендаций) предусматривают обсуждение вопроса сохранения репродуктивной функции с каждым онкологическим пациентом репродуктивного возраста до начала терапии. Это решение должны принимать совместно пациент, онколог и репродуктолог. На практике, онколог может говорить «нет», не вникая в детали, или же репродуктог говорит «да», не владея полной информацией о течении и прогнозе основного заболевания. Важно, что решение должно быть принято до начала противоопухолевой терапии. Иногда к нам обращаются женщины, которые прошли два или три курса химиотерапевтического лечения, и только после этого начинали задумываться: можно ли сохранить овариальную функцию? К сожалению, если этот вопрос не обсуждался и не учитывался изначально, наши возможности очень ограничены...
Поэтому во всех случаях необходим консилиум с учетом мнения пациента.

Методы сохранения фертильности
(www.asco.org/guindlines/AmericanSocietyofClinicalOncology)
Все они делятся на две группы: первая – методы, направленные на снижение риска повреждения яичниковой ткани лучевой- и химиотерапией, вторая группа методов – сохранение биологического материала. К первой группе относятся овариопексия и овариальная супрессия.
Овариопексия, или выведение яичника из зоны лучевого воздействия – самый старый, сегодня не очень популярный, но по-прежнему используемый метод. Он ненадежен (яичник может самопроизвольно опускаться в зону облучения, нет четкой границы зоны облучения, а также существуют индивидуальные дозы радиочувствительности яичниковой ткани, после получения которых в яичнике прекращаются овуляции).
Второй метод данной группы – овариальная супрессия. Гипотетически метод позволяет снизить чувствительность яичниковой ткани к цитостатической терапии за счет выключения овариальной функции. Вопрос эффективности этого метода сохранения фертильности очень активно дискутируется. Метод не считается высокоэффективным, хотя, судя по результатам, полученным во многим клинических исследованиях, он увеличивает шанс на сохранение овариальной функции.
Согласно последним данным, у пациенток, даже с гормон-независиммыми злокачественными опухолями, которым применяли эти препараты с целью протекции ткани яичника от воздействия цитостатиков, улучшаются отдаленные результаты лечения. Необходимо предупредить пациентку, что метод не 100% надежен.
С начала 2000-х годов были внедрены более прогрессивные методы – сохранение биологического материала пациентов перед запланированной противоопухолевой терапией: криоконсервация эмбрионов, ооцитов и яичниковой ткани.
Вклад в будущее
Криоконсервация эмбрионов – самый надежный и эффективный метод сохранения фертильности. Рутинно используется в клинической практике с конца ХХ века с высокой результативностью и обеспечивает 70% вероятности успеха. Метод подходит для женщин, которые имеют партнера и сохраненную яичниковую функцию. К недостаткам относят необходимость стимуляции яичников, а также время, необходимое на осуществление всей процедуры – до нескольких недель. В случае диагностированного онкологического заболевания бывает невозможно отложить начало лечения на такой срок (4–6 недель).
Криоконсервация ооцитов подходит тем женщинам, у которых нет партнера. Дети, родившиеся после применения этого метода, есть во всем мире, а первый такой ребенок родился в далеком 1986 году. Криоконсервация ооцитов допустима для тех пациенток, которым криоконсервация эмбрионов не подходит по религиозным или этическим соображениям. Вероятность успеха ниже, чем при консервации эмбрионов, и доходит до 40%. Однако и времени на осуществление протокола требуется меньше.
Главным недостатком использования криоконсервации эмбрионов и ооцитов есть повышения риска развития рецидива у больных гормонозависимыми опухолями, такими как рак молочной железы, эндометрия и яичника.
Так как оба метода используют контролируемую гиперстимуляцию яичников (во время которой уровень эстрогенов повышается значительно, хоть и кратковременно, но все же это является пусковым фактором, повышающим митотическую активность гормонзависимых опухолей).
Однако наука не стоит на месте, и, если с целью стимуляции назначаются антиэстрогены (тамоксифен) или ингибиторы ароматазы вместе с гонадотропин-релизинг гормонами, у нас есть возможность добиться суперовуляции без повышения уровня эстрогенов в крови.
Поэтому сейчас – это контролируемая стимуляция и юридически не нужно запрещать пациенткам использовать КГЯ как метод сохранения биологического материала.
В 2004 году родились первые дети, появившиеся на свет при помощи инновационного метода криоконсервирования яичниковой ткани. Метод подходит детям, которые получают специальное противоопухолевое лечение до начала пубертатного периода (с согласия родителей), а также молодым пациенткам, которым не рекомедовано откладывать начало специального лечения (рис. 1).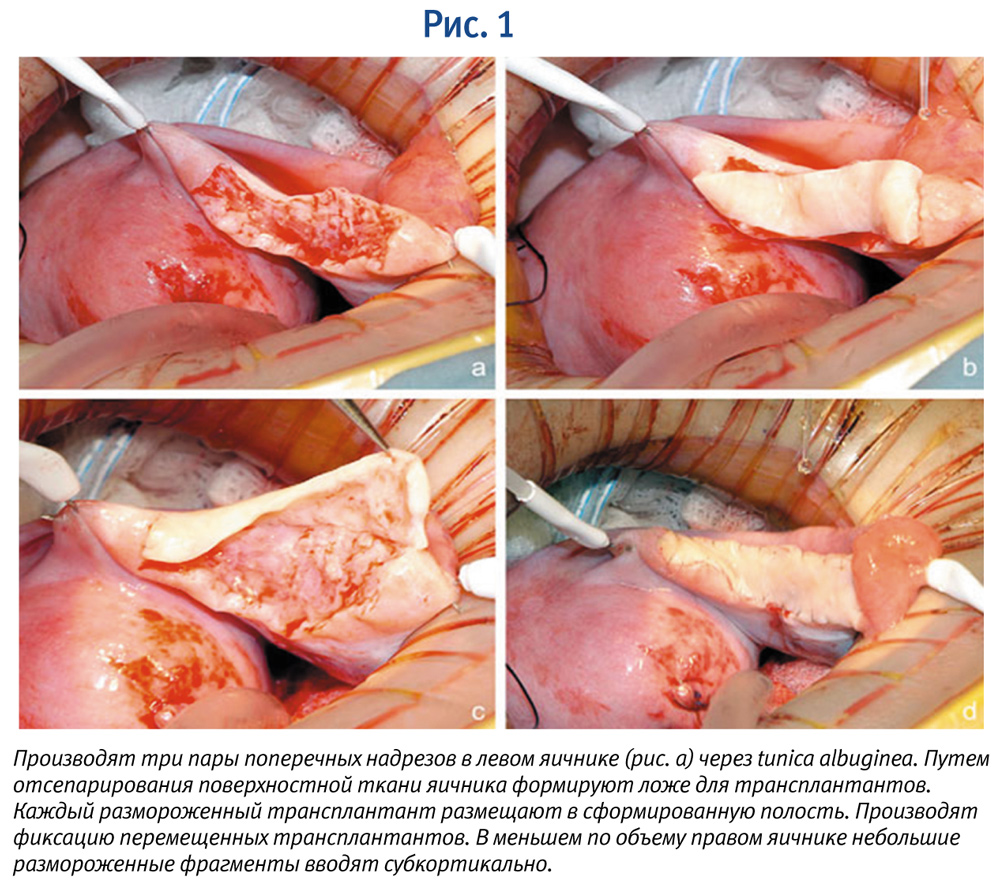
Показания к криоконсервации яичниковой ткани: возраст младше 35 лет, шанс на пятилетнюю выживаемость, отсутствие своих детей, отсутствие инфицированности вирусом гепатита С и носительство ВИЧ. Лапароскопически производится забор аваскулярных фрагментов коры яичника с последующей витрификацией, что позволяет сохранить до 80% фолликулов (Wang et al. 2008).
После достижения ремиссии онкологического заболевания осуществляется ортотопическая аутотрансплантация яичников, т. е. возвращение их на то же место. Гетеротопическая аутотрансплантация также возможна в случае проведенной овариоэктомии, в таком случае ткань яичника пересаживают на стенку малого таза или брюшину, реже – подкожно на предплечье (рис. 2).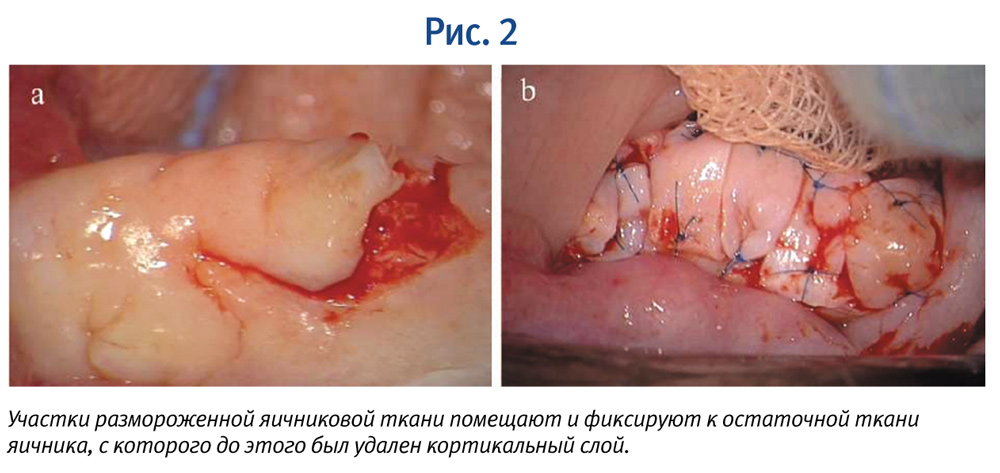
Метод имеет свои недостатки:
1) ишемизация полосок яичниковой ткани, склероз ткани и ее отторжение;
2) пациентки с «бедным ответом»: сохранена менструальная функция, предотвращен ранний климакс, но нет фолликулов и яйцеклеток;
3) лимитированное время жизни криотрансплантанта (от 2 до 10 лет);
4) кроме того, существует риск вовлечения яичника в онкологический процесс – этим вызвана необходимость гистологического исследования материала перед криоконсервацией, что, конечно, создает дополнительную травматизацию биологического материала. Высокий риск контаминации раковыми клетками ткани яичника существует при всех типах гемобластозов, раке желудка и неходжкинских лимфомах, средний риск дает рак молочной железы, колоректальный рак, меланома. При саркоме Юинга, нефробластоме, ходжскинской лимфоме этот риск низкий.
В качестве иллюстрации действенности перечисленных методов можно сказать о пациентке Стинни Бергхольдт, которая после диагностированной саркомы Юинга бедренной кости и произведенной по ее настоянию криоконсервации яичниковой ткани родила двоих здоровых детей.
Последние данные
В 2013 году впервые появились публикации, в которых были описаны клинические случаи наступления беременности у суррогатных матерей, с использованием яйцеклеток пациенток, перенесших овариэктомию по поводу рака яичника, гетеротопическую трансплантацию ткани яичника на стенку таза и контролируемую стимуляцию трансплантанта.
Необходимо помнить о том, что все такие пациентки безусловно должны понимать то, что идут на высокий риск пролонгации заболевания или осложнений от использования таких методов лечения.
Как влияет контролируемая гиперстимуляции на ткани молочной железы?
Не вызывает сомнений воздействие контролируемой гиперстимуляции, необходимой во всех случаях сохранения биологического материала, на дуктальный эпителий молочной железы.
В клетках эпителия возрастает количество митозов, что увеличивает риск развития злокачественного процесса. Для защаты молочной железы у обсуждаемой группы пациенток мы успешно используем препарат Прожестожель.
Для нас как онкологов, ценно то, что действующее вещество не проникает в плазму, а только накапливается в ткани молочных желез. Снижение пролиферативной активности ткани молочной железы позволяет снизить риск возникновения атипичных клеток и злокачественного перерождения.
Препарат также позволяет быстро и эффективно купировать масталгию, которая возникает на фоне проведения, уменьшить отек молочных желез и сецернацию.
Таким образом, большинство методов, позволяющих сохранить репродуктивную функцию женщин с онкологическим диагнозом, связаны с клиниками репродуктивной медицины.
Я консультирую в клинике ВРТ в качестве врача-маммолога и вижу, что в схемах назначения в качестве гестагенной поддержки используется вагинальная форма прогестерона (Утрожестан 200 мг 3 раза в день), который также выбирают репродуктологи во всем мире (согласно опросу 405 клиник в 82 странах мира на 5 континентах) (Luteal-phase support in assisted reproduction treatment: real-life practices reported worldwide by anupdated website-based survey Reprod Biomed Online. 2014 Mar; 28(3): 330-5).
Мы также знаем, что препараты, назначаемые репродуктологами, имеют максимально высокий профиль безопасности и эффективности, так как у всех женщин с бесплодием каждая попытка забеременеть может быть первой и последней, а особенно у пациенток с перенесенной в анамнезе онкологической патологией.
Перенесенная онкопатология не является противопоказанием для назначения Утрожестана и может применяться для гестагенной поддержки у таких женщин. Соответственно, данный препарат, с моей точки зрения, является препаратом выбора и у остальных пациенток, так как ему доверяют специалисты в области сохранения беременности во всем мире.
Помня о том, что желание иметь собственных детей остановить нельзя, несмотря ни на какие диагнозы и жизненные удары, мы находим в себе силы и мотивацию работать дальше, и, во многих случаях, побеждать!


коментарів