В останні роки збільшилася кількість пацієнток, які звертаються у різні лікувальні установи з приводу незлоякісних захворювань молочної залози (МЗ). Найпоширенішим доброякісним захворюванням МЗ є мастопатія, що зустрічається у 20–60% жінок, частіше у віці 20–40 років
Мастопатію як захворювання класично описав J. Velpean у 1838 році. У жінок у репродуктивний період життя циклічно відбувається зміна проліферативних і регресивних змін в епітеліальних і сполучних тканинах МЗ. Нейрогуморальне порушення регуляції цих процесів часто призводить до дифузних змін у МЗ, які зустрічаються у 39% обстежуваних жінок. Вони можуть проявлятися як дифузні та дифузно-вузлові зміни (Н. І. Рожкова, 1993).
Вузлова мастопатія (локалізований аденоматоз) – вогнищева мастопатія на тлі фіброзно-кістозного захворювання МЗ. Онкологія і мамологія розглядають цей вид мастопатії як передпухлинні процеси, на фоні яких підвищується ризик розвитку РМЗ. Вузлові ущільнення можуть мати одинарний або множинний характер, виявлятися в одній або обох МЗ. Морфологічні зміни при вузловій мастопатії представлені великими кістозними порожнинами, сосочковими розростаннями, вираженою проліферацією епітелію (багатошаровістю, поліморфністю, укрупненням ядер, збільшенням кількості мітозів тощо). За ступенем вираженості проліферативних процесів епітелію форма вузлової мастопатії може бути простою або проліферуючою. Проліферуюча форма розглядається як передрак, оскільки найчастіше піддається малігнізації.
Причини розвитку вузлової мастопатії
Пік захворюваності на вузлову мастопатію припадає на 20–40 років, що можна пояснити з точки зору особливості жіночої фізіології. Щомісячні циклічні зміни в організмі жінки репродуктивного періоду відбуваються під впливом основних гормонів – прогестерону, естрогену, пролактину, які забезпечують двофазний характер менструального циклу і викликають певні процеси в тканинах МЗ. Тканини МЗ піддаються такому гормональному впливу [1, 3]:
- естрогени стимулюють проліферацію протоків і сполучної тканини МЗ;
- прогестерон сприяє залозистій трансформації альвеол;
- пролактин сприяє розвитку лактоцитів, секреції молока, є основним гормоном, який забезпечує лактацію;
- гормони щитовидної залози відіграють важливу роль у морфогенезі і функціональній диференціації епітеліальних клітин МЗ;
- кортизон сприяє утворенню рецепторів пролактину в МЗ і стимулює ріст епітеліальних клітин у синергізмі з пролактином.
У нормі в першій фазі менструального циклу естрогени стимулюють проліферативні зміни в залозах; у другій — під впливом гормону-антагоніста прогестерону процеси проліферації гальмуються. На фоні дисбалансу цих гормонів (надлишку естрогенів і зниження рівня прогестерону) відбувається надмірна неконтрольована проліферація тканин МЗ, що призводить до розвитку спочатку дифузної, а потім і вузлової мастопатії. Крім того, в основі розвитку вузлової мастопатії має значення надлишкове вироблення гормону гіпофіза – пролактину. Функціональна гіперпролактинемія, обумовлена підвищенням рівня стресового напруження, – найчастіше порушення гомеостазу цього гормону. Вона сприяє розвитку проліферативних змін в тканинах МЗ і багатьох симптомів передменструального синдрому та, окрім цього, здатна порушувати естроген-прогестероновий баланс за рахунок пригнічення другої фази менструального циклу, а також підвищення рівня експресії естрогенових рецепторів у тканинах органів-мішеней.
Гормональний дисбаланс, який призводить до розвитку вузлової мастопатії, провокується частими штучними абортами, тривалим стресом, неврозами, обмінними порушеннями (цукровий діабет, гіпотиреоз, ожиріння, хронічний гепатит), гінекологічними захворюваннями (аднексити, ендометрити) та іншими причинами. Вузлову мастопатію викликає і безконтрольна гормональна контрацепція (на жаль, масово поширена в наш час), шкідливі звички, короткий або тривалий період лактації.
Симптоми вузлової мастопатії
Прояви вузлової мастопатії характеризуються пухлиноподібними ущільненнями в тканинах МЗ, мають чіткі межі, не спаяні з соском і шкірою. Такі ущільнення можуть виявлятися жінкою під час самообстеження. У передменструальний період ущільнення, і вся МЗ, стають болючими, напруженими, збільшуються в розмірах через набряк. Біль може іррадіювати в плече або лопатку. Після спадання передменструального набряку вузли стають безболісними. Іноді при вузловій мастопатії не виникає жодних хворобливих відчуттів, тоді вузол у залозі стає випадковою знахідкою. Для вузлової мастопатії характерний негативний симптом Кеніга – неможливість пропальпувати вузли МЗ в положенні лежачи. Регіонарні лімфатичні вузли при вузловій мастопатії не збільшені. При вузловій формі мастопатії може спостерігатися виділення із соска окремих крапель при натисканні або достатньо рясного прозорого, жовтувато-коричневого чи молозивоподібного вмісту.
Діагностика
Схожість проявів вузлової мастопатії і раку МЗ диктує необхідність проведення ретельного обстеження у мамолога з використанням клінічних, рентгенологічних, ехографічних, цитологічних та морфологічних методів.
При вузловій мастопатії пальпаторно в МЗ визначається одне або кілька вогнищ ущільнення з чіткими межами. При оглядовій мамографії на рентгенограмах можуть виявлятися ділянки інтенсивного однорідного затемнення, овальні тіні кіст, кальцинати, фіброзні тяжі. Поєднання різних форм вузлової мастопатії дає строкату рентгенологічну картину («місячний рельєф»), що характеризується перебудовою структури залози, множинними ділянками затемнень і просвітлення різної величини і форми, наявністю тяжів сполучної тканини, окремих тіней фіброаденом і кіст. При виявленні кісти МЗ проводиться її пункція з цитологічним дослідженням вмісту. УЗД МЗ з допплерографією дає змогу судити про локалізацію, розміри, васкуляризацію вузлів. Проведення пункційної біопсії МЗ з цитологічним дослідженням клітинного матеріалу необхідне для виключення онкопатології та вибору тактики лікування вузлової мастопатії.
Обов’язково при вузловій мастопатії показане дослідження рівня прогестерону та естрогенів, гормонів щитоподібної залози, печінкових ферментів, проведення УЗД малого тазу і консультації гінеколога.
Лікування
Основним методом лікування вузлової мастопатії є хірургічне втручання, характер і обсяг якого залежить від форми захворювання [2]. Необхідно пам’ятати, що операція – це усунення наслідків, а не причин захворювання. За таких втручань усувається лише частина зміненої тканини. Причини – дисгормональні зміни, ендокринні захворювання – залишаються. Тому після операції необхідно проводити консервативне лікування, спрямоване на усунення причин виникнення дисгормональних розладів і нормалізацію гормонального балансу в організмі, а головне – запобігти рецидиву захворювання.
Основними гормонами, які контролюють функціональну активність МЗ, є естрадіол, прогестерон і пролактин. У результаті багатьох наукових досліджень доведено, що ця патологія пов’язана з порушенням гормонального балансу – зниженням рівня прогестерону на тлі підвищення рівня естрадіолу і пролактину [3].
Хірургічне втручання в цій клінічній ситуації усуває наслідки, а не безпосередню причину захворювання. На сьогодні є багатий клінічний досвід використання в консервативній терапії дисгормональних захворювань МЗ рослинного препарату Мастодинон (головна активна субстанція – спеціальний екстракт Vitexs agnus castus – Bno 1095). У багатьох рандомізованих плацебо-контрольованих дослідженнях, які проведені у Німеччині і країнах Центральної Європи, було продемонстровано здатність цього лікарського засобу нормалізовувати підвищений рівень пролактину (за умови відсутності органічної патології гіпофіза) і ліквідувати мастодинію та, залежно від ступеня, патологічні зміни тканини МЗ. Крім того, нормалізація рівня пролактину зумовлювала відновлення нормального ритму секреції гонадотропінів та нормалізацію естроген-прогестеронового балансу (усунення явищ відносного естрогенового домінування).
Наразі Мастодинон входить до протоколів консервативної терапії дисгормональних захворювань МЗ. Незважаючи на те, що у нашій практиці Мастодинон багато років використовується після оперативного втручання з приводу вузлової фіброзно-кістозної мастопатії з метою негормональної реабілітації жіночої статевої системи, систематизованого наукового аналізу результатів лікування немає. Вивчення потенціалу фітотерапії дало б змогу визначити оптимальний метод лікування цієї патології та зменшити частоту повторних оперативних втручань.
Матеріали та методи дослідження
За період 2012–2013 рр. під спостереженням було 60 пацієнток віком від 18 до 45 років (середній вік 26±2,4 року), які перенесли оперативне втручання з приводу вузлової фіброзно-кістозної мастопатії. Критерії включення в дослідження були такими: стан після оперативного лікування зазначеної патології, відсутність післяопераційного прийому гормональних препаратів або синтетичних інгібіторів секреції пролактину, відсутність онкологічної патології чи пролактиноми гіпофіза. Збір та оцінка індивідуальних даних (скарги, суб’єктивні відчуття, психоемоційний стан пацієнток на період лікування і після нього) проводилися згідно зі спеціально розробленою візуально-аналоговою шкалою. Гістологічний аналіз матеріалу проводився за загальноприйнятою методикою. Гормонограма (рівень пролактину, естрадіолу, прогестерону) проводилася в стандартизованій лабораторії, на 7–14–21-й день менструального циклу на наступний місяць після операції, а також відбувався повтор на третьому і шостому місяцях лікування після операції. Діагноз вузлової мастопатії встановлювався згідно з критеріями, викладеними в ряді публікацій [1–3].
Залежно від схеми післяопераційної реабілітації, методом випадкового розподілу всі пацієнтки були розподілені на дві рівнозначні групи. Основну групу склали 30 пацієнток, які отримували у післяопераційному періоді Мастодинон по 30 крапель або по 1 таблетці двічі на добу протягом шести місяців, а також упродовж 6 тижнів – полівітаміни з мікроелементами, що містять малі дози йоду, вітамінів А, Е, С. Контрольну групу склали 30 пацієнток, які впродовж 6 тижнів отримували загальнозміцнюючу терапію – полівітаміни з мікроелементами, які містять малі дози йоду, вітамінів А, Е, С.
Лікування обох груп було розпочато на наступний місяць після оперативного втручання (за цей час жінки пройшли реабілітаційний період). На етапі післяопераційного лікування через 1, 3 та 6 місяців після втручання проводилась оцінка таких параметрів: дослідження рівнів естрадіолу і пролактину в фолікулярну фазу менструального циклу, прогестерону – в другу фазу циклу. Наприкінці 3 та 6 місяців після початку лікування оцінювався стан МЗ за даними УЗД та визначався ступінь мастодинії за даними візуально-аналогової шкали. Крім того, в щоденниках спостереження пацієнтки фіксували тривалість мастодинії, характер менструального циклу та побічні явища лікарського засобу.
Статистичну обробку результатів дослідження проводили на персональному комп’ютері за допомогою пакета Microsoft Excel 2003.
Результати дослідження та їх обговорення
Аналіз гормонограми, яку проводили перед початком лікування, показав, як ми й передбачали, помірно підвищений рівень пролактину та естрадіолу. Рівень прогестерону був знижений приблизно на 18,5±3% в обох групах (таблиця 1). Таким чином, стан гормонального гомеостазу у жінок характеризувався функціональною гіперпролактинемією, відносною гіперестрогенією та абсолютною гіпопрогестеронемією у другу фазу менструального циклу. 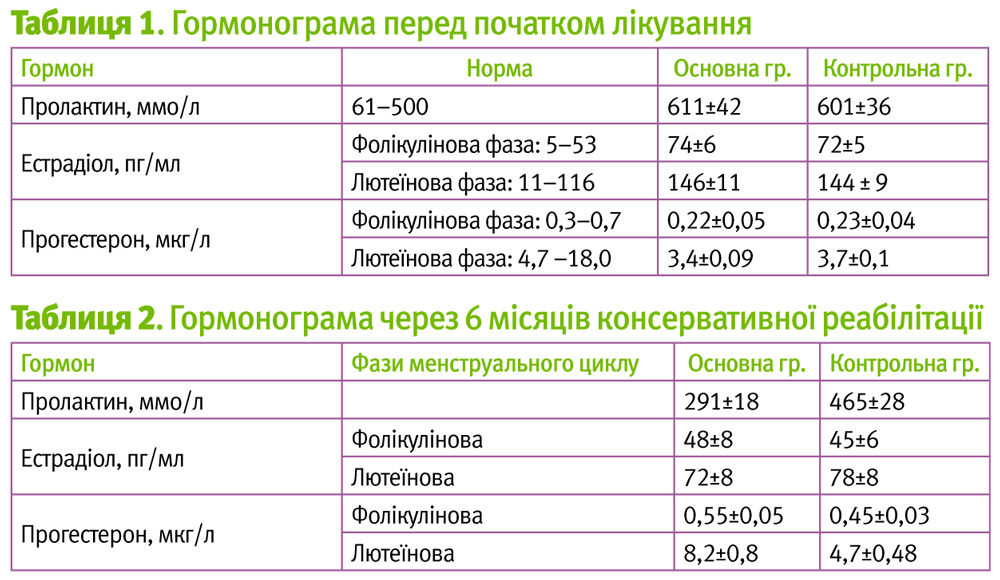
Динамічне спостереження за пацієнтками на фоні терапії показало, що післяопераційна реабілітація достатньо ефективна. Під час лікування зменшилася кількість днів, у які жінки відчували біль. А інтенсивність больового синдрому, яка реєструвалась за візуально-аналоговою шкалою, також зменшилася.
В основній групі зниження больових відчуттів відбувалося більш інтенсивно і стійко – на 32 мм, тоді як у групі контролю – на 20,5 мм. При проведенні ультрасонографії МЗ через 3 місяці в основній групі констатоване значне поліпшення клінічної картини – зменшення набряку залозистого компоненту, фіброзного компоненту, кількості і розміру кіст у 23 хворих (77% пацієнток). У групі контролю також спостерігалася позитивна динаміка у 18 пацієнток (61%).
Після тримісячного прийому Мастодинону рівень пролактину та естрадіолу наблизився до норми (500 мМО/л і 290 пг/мл відповідно), тоді як у групі контролю ці показники не зазнали значних змін. Наведені зміни стали більш виразними після комплексного обстеження через 6 місяців консервативної реабілітації (таблиця 2).
Як бачимо, більш значний терапевтичний ефект проявився через 6 місяців. Аналогічна картина спостерігалася при ультрасонографії МЗ. Так, у групі контролю у 8 пацієнток (26,6%) залишався виражений фіброзний компонент, з набряком строми, розширеними протоками і великою кількістю кіст різного діаметра. Відповідно ця категорія жінок продовжувала скаржитися на дискомфорт, зокрема і в післяопераційній ділянці, масталгію і виражений передменструальний синдром. Тоді як в основній групі зазначені скарги були лише у 2 жінок (6,6%). Протягом подальших 12 місяців у 4 жінок (13,3% пацієнток) групи контролю проведено повторне втручання з приводу вузлоутворення. Більше того, їхній стан здоров’я після повторного втручання суттєво не поліпшився. В основній групі повторних втручань не було.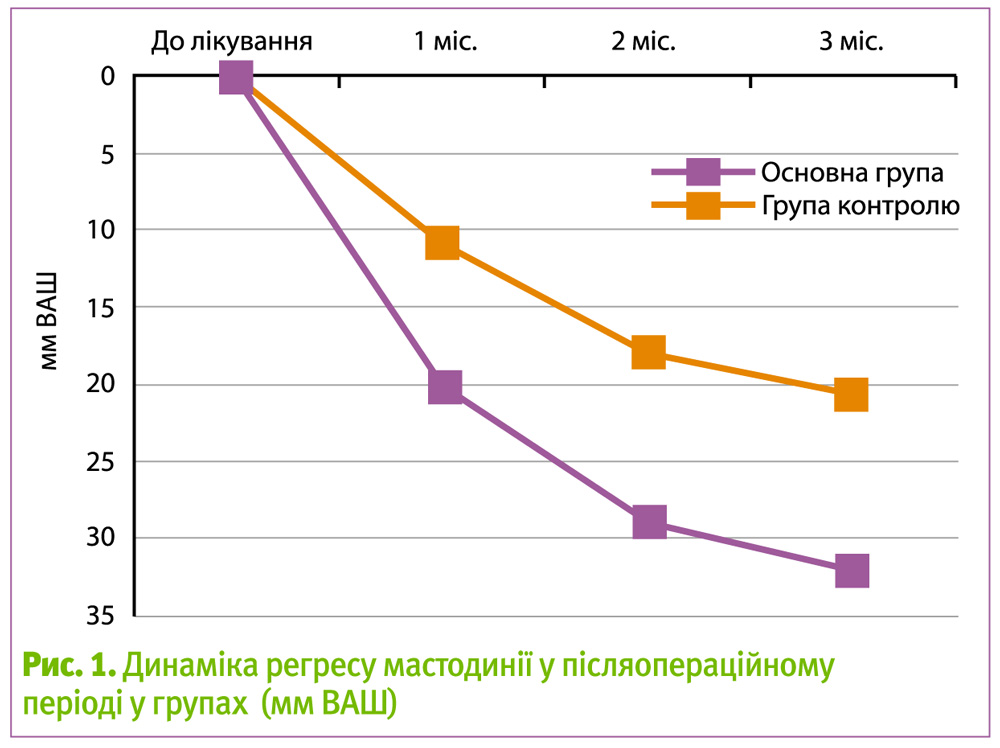
Висновки
Оперативне лікування вузлових форм мастопатії не ліквідує головної причини захворювання – гормональних порушень (гіперпролактинемію, відносну гіперестрогенемію). Крім того, оперативне втручання і пов’язаний з ним стрес може ще глибше посилити ступінь гормональних порушень, а втручання в анатомічну цілісність тканин МЗ сприяє повторним вузлоутворенням.
Патогенетична дія Мастодинону, його властивість м’яко регулювати гормональний гомеостаз через вплив на вісь гіпоталамус–гіпофіз–яєчники, сприяє поліпшенню стану тканини МЗ і профілактиці вузлоутворення у пацієнток з фіброзно-кістозною мастопатією. Цікавим є факт, що суттєве поліпшення гормонального обміну і суб’єктивного стану жінок відбувалося після 5–6 місяців терапії. Це свідчить про необхідність призначати консервативну реабілітацію за допомогою Мастодинону на більш тривалий період.
Post Scriptum
Будучи хірургом до кінчика леза, живучи разом з онконастороженістю в пошуках і в ранньому виявленні неоплазії, схиляю голову перед природою! Лікування травами – найдавніша віха медицини. А в еру «хімізації» сучасні технології фітонірінгу виступають не тільки конкурентом синтетичним сполукам, а й вибором №1 для пацієнтів у зв’язку з максимальною фізіологічною спорідненістю, відсутністю побічних дій і ускладнень, наявним хорошим, переконливим терапевтичним ефектом.
За матеріалами журналу «Ендокринна гінекологія» №6 (14) 2013.
Перелік літератури знаходиться у редакції.


коментарів