
По классификации ВОЗ, среди причин, приводящих к патологической гиперпролактинемии, на первом месте находятся органические поражения гипофиза, морфологическим субстратом которых являются пролактинсинтезирующие опухоли гипофиза (макро- и микропролактиномы), по частоте занимающие третье место среди новообразований центральной нервной системы и составляющие, по данным разных авторов, от 4 до 17% всех опухолей головного мозга.
Наиболее часто встречающейся эндокринно активной опухолью гипофиза является пролактинома — опухоль, исходящая из клеток аденогипофиза (лактотрофов), секретирующих пролактин; она составляет примерно 40–50% гормонально активных аденом и около 30% всех аденом [Osborn A., 2004]. Аденомы гипофиза классифицируются по размеру: менее 10 мм в диаметре считаются микроаденомами, более 10 мм — макроаденомами.
Клинические проявления аденом гипофиза зависят от размеров опухоли, наличия или отсутствия гормональной активности, типа продуцируемого гормона и степени экстраселлярного распространения [Kovacs K., 2005].
Общепризнанно, что манифестирующим признаком пролактиномы гипофиза является повышение уровня гормона пролактина, приводящего к целому симтомокомплексу в виде нарушений овариально-менструального цикла с тенденцией к олигоопсоменорее вплоть до стойкой аменореи, бесплодия, галактореи, болезненности и нагрубания молочных желез, головных болей, нарушений зрения, обилия вегетативных жалоб и др.
Именно вышеуказанные жалобы приводят пациентку на прием к гинекологу, от которого зависит своевременность диагностики, адекватность и пролонгированность терапии, контроль эффективности проведенного лечения.
Однако в своей практической деятельности врач зачастую сталкивается с диссонансом между уровнем пролактина в сыворотке крови и выраженностью клинических проявлений данной патологии. Так, например, при диагностированных микро- и макроаденомах гипофиза, когда по всем литературным данным ожидаемый результат повышения уровня пролактина должен превысить 2000 мМЕ/л [Татарчук Т. Ф., Венцковская И. Б., Ефименко О. А. «Гиперпролактинемия в практике врача-гинеколога», 2007], наблюдаются невыраженные, «стертые» формы клинических проявлений гиперпролактинемий. При этом уровень пролактина колеблется от 800 до 1 600 мМЕ/л. И, наоборот, при высоких цифрах сывороточного пролактина свыше 3000–5000 мМЕ/л клиническая симптоматика может быть невыраженной: не диагностируется органическая патология гипофиза в виде пролактинсекретирующей опухоли, сохраняется менструальный цикл, отсутствуют явления галактореи и т.д.
Возможно, что общий высокий уровень пролактина сыворотки крови как биохимический маркер сбоя в системе «гипоталамус-гипофиз-яичники» не всегда свидетельствует в пользу органической патологии гипофиза. Именно поэтому «нормальный и субнормальный» уровень пролактина при наличии симптоматики гиперпролактинемии не должен быть причиной снижения бдительности врача, поскольку за этим может быть завуалирована серьезная патология, требующая тщательного обследования и лечения больной.
Клиническая активность пролактина определяется общим его количеством, состоянием рецепторов в органах-мишенях, и что особенно важно — соотношением фракций в общем пуле пролактина.
По данным H. L. Fideleff и соавторов (2000), различают 4 фракции пролактина в зависимости от молекулярной массы (ММ):
- малый (little) ПРЛ обладает высокой биологической активностью (ММ 22000);
- большой (big) ПРЛ с ММ 50 000;
- большой-большой (big-big) ПРЛ с ММ 100000;
- гликозилированный ПРЛ с ММ 25 000.
В практической деятельности врача большое значение имеет определение в общем пуле «биологически агрессивного» низкомолекулярного пролактина (н-ПРЛ), вызывающего реализацию патологических проявлений даже при незначительном повышении его общего уровня. С другой стороны, длительно существующая гиперплазия и гиперактивность лактотрофов гипофиза являются провоцирующим фоном возникновения и роста опухоли гипофиза.
Обусловленная опухолью гипофиза хроническая гиперпролактинемия вызывает снижение чувствительности гипоталамуса к эстрогенам с подавлением синтеза гонадотропин-рилизинг-гормонов, вследствие этого нарушается цикличность выделения гипофизом ЛГ и ФСГ, уменьшаются частота и амплитуда пиков секреции ЛГ. Пролактин, конкурентно связываясь с рецепторами гонадотропинов в яичниках, тормозит влияние гонадотропинов на стероидогенез и снижает чувствительность яичников к экзогенным и эндогенным ГТ, что приводит к формированию синдрома гипогонадизма с нарушением менструальной и детородной функций женщины более чем в 25–30% случаев [Гилязутдинов И.А., 2006].
Гиперпролактинемия непосредственно снижает секрецию прогестерона желтым телом и индуцирует ранний лютеолиз [Niswander G.D., 2002]. По существу, результатом нарушений фолликулогенеза является недостаточность лютеиновой фазы (НЛФ) менструального цикла, проявляющаяся в гипофункции желтого тела вследствие недостаточности синтеза прогестерона, что вызывает нарушение секреторной трансформации эндометрия, в последующем приводящее к бесплодию и прерыванию беременности в раннем сроке.
Нами был проведен ретроспективный анализ эффективности консервативного лечения пролактином гипофиза у 40 нерожавших женщин репродуктивного возраста с учетом молекулярного полиморфизма пролактина и коррекцией НЛФ по принципу «трех L»:
- little fraction;
- little dosis;
- long time.
Принцип трех L означает:
- Первое L (little fraction) — при превалировании н-ПРЛ, составляющего по отношению к общему пулу пролактина 99–100%, наблюдается максимальная реализация и манифестация клинической симптоматики даже при невысоких и субнормальных показателях общего пролактина.
- Второе L (little dosis) — наиболее выраженный положительный клинический эффект лечения гиперпролактинемии органического генеза наблюдается при применении микродоз достинекса 0,125 мг 1–2 раза в неделю.
- Третье L (long time) — патогенетически обоснованная пролонгированная терапия пролактином гипофиза проводится до снижения «биологической агрессии» пролактина, а именно: до нормализации процентных показателей little-фракции пролактина, что подтверждается контролируемыми в динамике клиническими результатами в виде уменьшения в размерах или полного исчезновения пролактином гипофиза в ходе лечения. В среднем длительность терапии микродозами каберголина составила 2,5–3,5 года.
Это обусловило цель исследования — определение качественного и количественного состава пролактина, в первую очередь уровня little-фракции ПРЛ у пациенток с диагностированными пролактиномами гипофиза, установление взаимосвязи клинических проявлений и полученных данных гормонального обследования, обоснование дифференцированного подхода в лечении данных пациенток.
Материалы и методы
Для решения поставленной цели проведено комплексное обследование 40 нерожавших женщин в возрасте 18–32 лет с диагностированными у них пролактиномами гипофиза.
При этом 20 пациенткам (1 группа) проводилось лечение по общепринятой методике — терапия агонистами дофамина до нормализации уровня пролактина сыворотки крови и исчезновения клинической симптоматики гиперпролактинемии и 20 — по разработанной нами методике (2 группа) до нормализации уровня little-фракции ПРЛ с одновременной коррекцией НЛФ по принципу трех L.
Контрольную группу составили 20 нерожавших женщин аналогичной возрастной группы без соматической и эндокринной патологии.
Комплексное обследование пациенток включало: общеклиническое и гинекологическое обследования, гормональные исследования, ультразвуковые методы исследования (УЗИ) органов малого таза, щитовидной железы и молочных желез, исследование функции зрительного анализатора с проведением компьютерной периметрии c определением периферических полей зрения, для подтверждения органической патологии гипофиза проводилась компьютерная томография (КТ) головного мозга с внутривенным усилением или магниторезонансная терапия (МРТ).
Определение гормонального профиля пациенток включало:
- определение уровней гормонов ПРЛ, ТТГ, ФСГ, ЛГ, Т3, Т4, АТ к ТПО, эстрадиола, прогестерона, тестостерона, кортизола;
- фракционирование пролактина методом хемилюминесценции.
Предложенный нами комплекс лечебно-профилактических мероприятий был представлен лечением препаратами достинекс микродозами длительно (18–36 месяцев) в комбинации с утрожестаном.
Результаты и их обсуждение
Анализ особенностей клинической характеристики двух групп пациенток показал, что при распределении на группы был полностью соблюден принцип рандомизации.
Подробный сбор общего анамнеза предшествовал началу обследования с целью исключения факторов фармакологической гиперпролактинемии.
Структурный анализ основных проявлений данной патологии показал, что в 60% случаев имело место позднее наступление менархе (в среднем в 15 лет), что нехарактерно для девушек южного региона. В 40% случаев у данного контингента больных отмечалось своевременное наступление менархе, однако через 2–5 лет в этой группе больных возникали сначала периодические 1 раз в 3–6 месяцев «выпадения» менструальных циклов с последующим нарастанием степени тяжести процесса вплоть до стойкой вторичной аменореи.
Жалобы пациенток при обращении к врачу условно можно разделить на следующие подгруппы:
1) НОМЦ: превалирование симптомов нарушения овариально-менструального цикла по типу гипоменструального синдрома и аменореи-2 различной продолжительности и периодичности.
2) Патология молочных желез (МЖ) была представлена следующими изменениями: болезненностью и нагрубанием МЖ за 7–10–15 дней до начала менструации, явлениями галактореи, по частоте встречаемости не превысившей 10%. При аменорее-2 свыше 6 месяцев болезненность МЖ постепенно угасала.
3) Бесплодие первичное и невынашивание беременности были ведущей мотивацией обращения к врачу.
4) Головная боль, нарушения зрения, обилие вегетативных жалоб и др.
При проведении первичного гормонального обследования у 40 женщин с пролактиномами гипофиза выявлены следующие данные:
1) Колебания общего уровня ПРЛ составили 750–3800 мМЕ/л (норма – 300–500 мМЕ/л); в 70% случаев уровень ПРЛ колебался в интервале 750–1250 мМЕ/л.
2) Процентный состав н-ПРЛ по отношению к общему пулу ПРЛ был превалирующим, составив 95–100% (табл. 1).

3) При сохраненном менструальном цикле уровень прогестерона находился в интервале 5–18 нг/мл, определяемый в конце 2-й фазы менструального цикла, при аменорее-2 и гипоменструальном синдроме отмечается значительное снижение уровня прогестерона вплоть до нуля (0–8 нг/мл) у данного контингента больных.
4) Значительное снижение уровня сывороточного эстрадиола наблюдалось при длительной аменорее-2 более 6 месяцев, при сохраненном менструальном цикле показатели гормона эстрадиола имели широкий диапазон от 25 до 240 нг/мл в зависимости от фазы менструального цикла.
5) ТТГ, а также гормоны щитовидной железы — в пределах нормы.
Стоит отметить, что патология МЖ, подтвержденная методом УЗИ, отмечалась у 50% пациенток и была представлена следующими изменениями: умеренная и выраженная дуктэктазия в околососковой зоне или во всех квадрантах; наличие единичных или множественных кистозных образований в молочных железах с размерами 0,5–1,3 см.
Несмотря на многогранность патологии, в зависимости от жалоб обратившихся пациенток, результатов их гормонального обследования, а также результатов УЗИ органов малого таза и МЖ, были сформированы три клинические подгруппы.
В 45% (1-я подгруппа — 18 пациенток) наблюдается позднее менархе с последующим регулярным менструальным циклом в течение 1–3 лет, однако спустя это время происходила смена регулярного менструального цикла на эпизоды гипоменструального синдрома с постепенным нарастанием клиники вплоть до стойкой аменореи-2 продолжительностью 6–8 месяцев. На фоне НОМЦ отмечаются выраженные изменения в яичниках, диагностированные на УЗИ: значительное увеличение яичников в размерах с выраженной кистозной дегенерацией яичников и кистами последних. Следует отметить в данной подгруппе большой процент пациенток, которые в прошлом были прооперированы по поводу кист яичников (20%). На этапе сохраненного менструального цикла пациентки отмечают умеренную болезненность и нагрубание молочных желез за 5–7–10 дней до начала менструации. Однако по мере прогрессирования заболевания болезненность и нагрубание в МЖ постепенно исчезали, но симптом галактореи оставался.
Таким образом, в этой клинической подгруппе отмечается синергизм патологии яичников и молочных желез с преобладанием в симптоматике НОМЦ по типу гипоменструального синдрома или аменореи, а также имеют место незначительные вегето-неврологические изменения.
В 30% случаев (2-я подгруппа — 12 пациенток) доминирующим моносимптомокомплексом представлена проблема патологии МЖ.
У этих пациенток отмечается своевременное наступление менархе с последующим сбережением сохраненного менструального цикла или периодичностью смен регулярного менструального цикла на аменорею-2, однако с жалобами на выраженный болевой синдром, нагрубание и дискомфорт в МЖ за 7–14 дней до начала менструации, явления галактореи. При обследовании у больных выявлены дисгормональные заболевания молочных желез (ДЗМЖ):
- Диффузные с преобладанием:
- железистого компонента (аденоз) — в 25% случаев (10 пациенток);
- фиброзного компонента — у 4-х пациенток;
- кистозного компонента— у 6-ти пациенток.
- Смешанные формы ДЗМЖ — в 35% случаев.
- Узловые формы ДЗМЖ (у 2-х пациенток — 5%).
Две пациентки из этой группы были прооперированы: у пациентки Д. операция секторальной резекции левой МЖ с окончательным гистологическим заключением «фиброзно-кистозная мастопатия с очаговой интрадуктальной и дольковой пролиферацией», второй пациентке проведена секторальная резекция по поводу узловой формы мастопатии с гистологическим заключением «фиброаденома МЖ».
Исходя из полученных клинических примеров, стоит отметить тот факт, что при пролонгировании заболевания без эффективного лечения субъективные симптомы масталгии и мастодинии постепенно угасают, особенно при развитии стойкой аменореи-2. Однако патология молочных желез затем имеет тенденцию к усугублению, проявляясь различными формами мастопатии, требующих в последующем консервативного и оперативного лечения.
В 25% (3-я подгруппа — 10 пациенток) позднее менархе сразу перешло в последующий гипоменструальный синдром со стойкой аменореей-2; в этой группе больных отмечается высокий процент гипоплазий гениталий и различной степени тяжести генитального инфантилизма.
Вегето-неврологические изменения равномерно представлены во всех подгруппах обилием вегетативных жалоб по совокупности формирующих астеновегетативный синдром, при этом у каждой второй больной отмечаются жалобы на головную боль, слабость, головокружения и т.д.
Общеизвестно, что макропролактиномы гипофиза с супраселлярным ростом приводят к вовлечению в патологический процесс оптико-хиазмальной области, и при этом классическим офтальмологическим признаком является битемпоральная верхнеквадрантная гемианопсия, реже — полная битемпоральная гемианопсия.
Наиболее серьезные изменения периферических полей зрения в виде битемпоральной гемианопсии превалировали в группе больных с преобладанием низкомолекулярных фракций ПРЛ по отношению к общему его уровню. В 20% случаев у больных с диагностированными микроаденомами гипофиза и превалированием высокомолекулярных фракций ПРЛ не наблюдались серьезные офтальмологические проблемы в виде нарушений полей зрения.
При обследовании функции зрительного анализатора методом компьютерной периметрии у данного контингента больных выявлены следующие изменения: синдром «сухого глаза» — в 40%, начальные застойные диски зрительных нервов — в 20%, расширение слепого пятна — в 35%, битемпоральная гемианопсия — в 60%, прогрессирующая осложненная миопия высокой степени в сочетании с начальными застойными дисками зрительных нервов обоих глаз — в 15%, субатрофия зрительных нервов — в 10% случаев. Полученные данные офтальмологического исследования согласуются с тем, что вследствие интракраниального расположения зрительных нервов центральное зрение обеспечивается центрально расположенными аксонами или папилломакулярным пучком зрительного нерва. Поэтому при патологии гипофиза центральное зрение страдает на поздних этапах развития заболевания. В первую очередь страдает периферическое зрение, чаще всего это зона перекреста медиальных волокон зрительных нервов. До сих пор традиционно мнение о том, что при аденомах значительных размеров, то есть при макроаденомах, возникает классический офтальмологический симптом битемпоральной гемианопсии вследствие сдавления хиазмы растущей экстраселлярной опухолью гипофиза. Однако полученные данные — выявление в 60% биназального снижения пороговой чувствительности сетчатки, то есть битемпоральной гемианопсии при проведении компьютерной статической периметрии Humphrey при микроаденомах гипофиза, где в силу небольших размеров опухоли гипофиза исключается механизм сдавления хиазмы. Именно это, возможно, позволит достигнуть ранней диагностики органической патологи гипофиза.
При обследовании пациенток методами КТ или МРТ с внутривенным усилением получены следующие данные:
- интраселлярно определялись изоденсивные образования с ровными контурами, округлой формы, диаметром в диапазоне 5–14 мм, умеренно накапливающие контрастное вещество;
- срединные структуры симметричны, не смещены; ширина передних рогов боковых желудочков, а также третьего желудочка в пределах нормы;
- костно-деструктивных изменений турецкого седла не наблюдалось;
- конвекситальные субарахноидальные ликворные пространства не расширены.
Для проведения диагностики пролактином на ранних этапах, а также с целью снижения частоты необоснованных методов исследований, таких как краниография, КТ или МРТ гипофиза, несущих значительную лучевую нагрузку, нами была предложена шкала оценки риска формирования пролактином как метода прогнозирования гиперпролактинемии органического генеза.
Шкала состоит из четырех разделов:
- Анамнез, включающий следующие подпункты:
- материнский анамнез;
- анамнез становления менструальной функции с акцентом на возраст менархе;
- ОГА (отягощенный гинекологический анамнез).
- Клинические данные.
- Данные лабораторных методов исследования.
- Инструментальные методы исследования.
Каждый из разделов оценивается по шкале в баллах по каждому пункту и суммарно. Окончательный подсчет баллов по всем четырем разделам определяет степень риска отнесения больной к группе пациентов с органическими изменениями гипофиза (табл. 2).
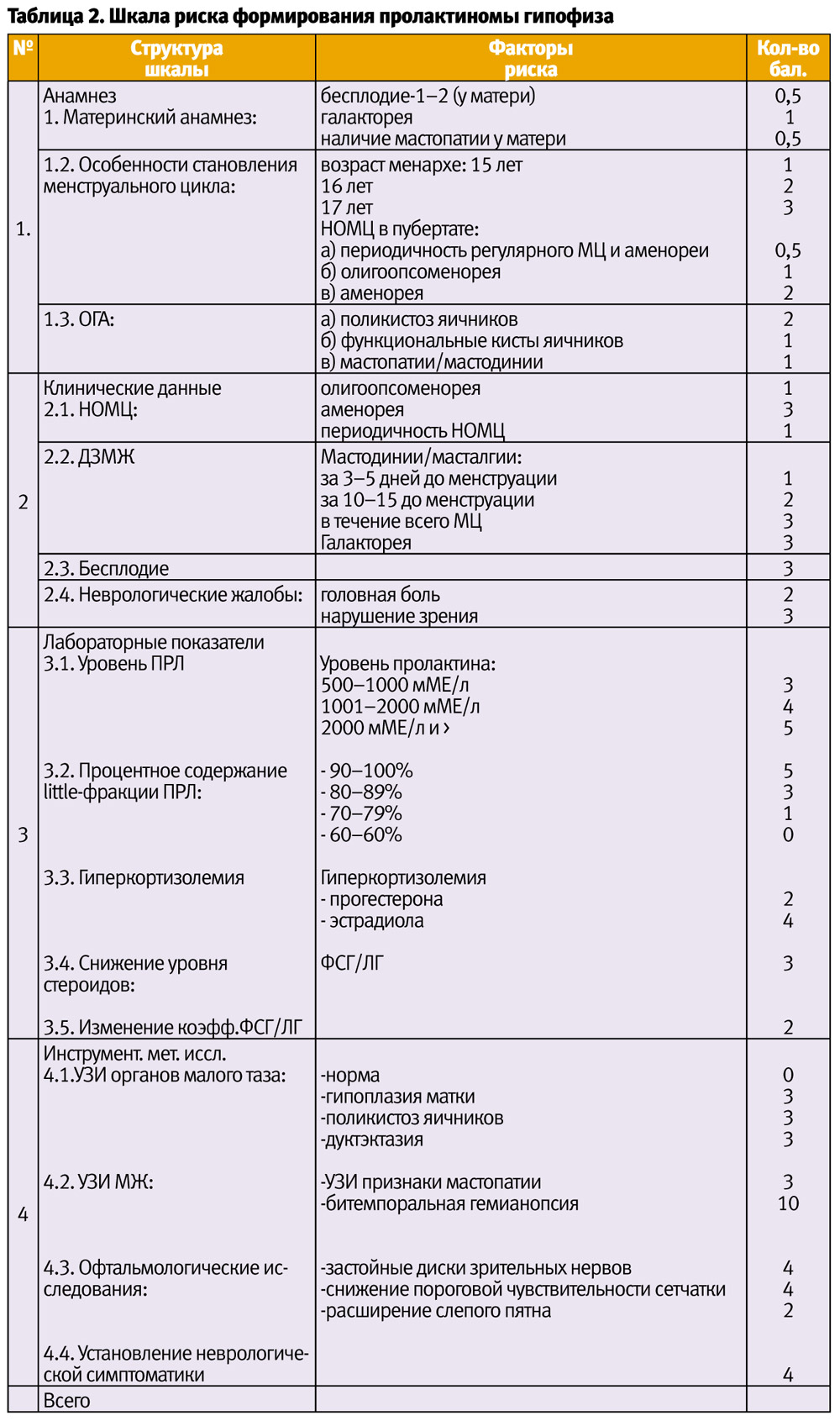
Нами предложено различать 3 степени риска по совокупности баллов:
- низкая — < 30 баллов;
- средняя — 31–60 баллов;
- высокая степень риска — 61–100 баллов.
При установлении высокой степени риска образования пролактиномы гипофиза для уточнения диагноза пациентка нуждается в проведении КТ с внутривенным усилением или МРТ головного мозга. Проведение КТ с внутривенным усилением или МРТ является золотым стандартом диагностики пролактином гипофиза. Однако скрининговая оценка по шкале прогноза позволит избегнуть излишней лучевой нагрузки.
Клинические аспекты современного алгоритма диагностики микропролактином гипофиза у женщин репродуктивного возраста
Учитывая высокую частоту встречаемости (от 17 до 47%) гиперпролактинемических состояний, необходима современная научно обоснованная система отбора пациенток группы риска по формированию пролактином гипофиза у женщин репродуктивного возраста на основе алгоритма диагностических мероприятий.
Началу обследования пациенток должен предшествовать сбор общего анамнеза с акцентом на факторах, способных вызвать:
- Фармакологическую гиперпролактинемию (прием нейролептиков, антидепрессантов, противорвотных средств, опиатов и других). Учитывая возраст пациенток(14–18 лет), у которых половой дебют в 60% случаев приходится на 15,8 лет, для которых прием гормональных контрацептивов, в частности КОК, возможно, создает фон к развитию медикаментозной гиперпролактинемии.
- Психогенную гиперпролактинемию в ответ на стрессовые ситуации, тем более что возрастной ценз пациенток определяет незавершенность формирования психоэмоциональной сферы.
- Вторичную гиперпролактинемию в ответ на соматическую экстрагенитальную патологию: гипотиреоз, почечная, печеночная недостаточность и др.
- Материнский анамнез с его наследственной генетически обусловленной предрасположенностью к гормональным нарушениям был подробно описан выше.
Особое внимание следует уделять вопросам нарушения становления менструальной функции в период полового созревания, особенно фактору позднего наступления менархе как фактору риска уже произошедшего сбоя в системе «гипоталамус-гипофиз-яичники» на этапе формирования репродуктивной системы.
Традиционное определение уровня пролактина не должно ограничиваться абсолютными цифрами данного гормона, поскольку его биологическая активность определяется не только уровнем гормона в крови, сколько преобладанием его низкомолекулярной фракции по отношению к общему пулу пролактина как маркера «истинной гиперпролактинемии». Полный спектр гормональных исследований должен включать определение гормонов тиреоидной панели, стероидных гомонов, надпочечников, ФСГ, ЛГ и других. Для правильной постановки диагноза необходимо проведение полного клинического обследования, включая УЗИ органов малого таза, УЗИ МЖ и щитовидной железы.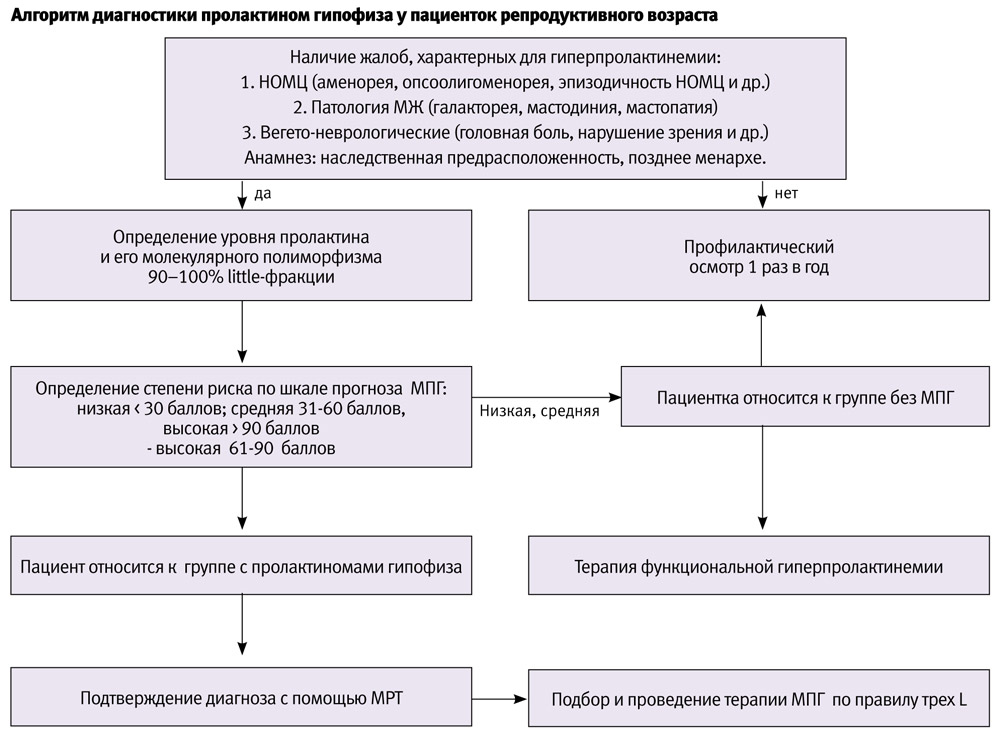
Выводы
- Между выраженностью клинических проявлений и общим уровнем ПРЛ не отмечается пропорциональной зависимости, однако отмечается прямая коррелятивная зависимость между тяжестью нарушений менструального цикла и процентным превосходством низкомолекулярного ПРЛ по отношению к высокомолекулярным фракциям.
- Исследование функции зрительного анализатора в сочетании с определением качественного и количественного состояния ПРЛ должно стать базовым маркером неблагополучия в гипоталамо-гипофизарной области, прогнозом риска роста пролактиномы гипофиза, а также критерием эффективности проведенного лечения.
- Использование шкалы для оценки риска формирования пролактиномы гипофиза поможет практическому врачу избежать ошибок в гипо- и гипердиагностике сложной и многогранной патологии гипофиза.
- Применение алгоритма диагностики пролактином гипофиза позволит избежать излишней лучевой нагрузки при проведении дифференциальной диагностики генеза гиперпролактинемий.



коментарів