Опыт клинического применения препаратов интерферона
В настоящее время известно более 20 различных возбудителей инфекционно-воспалительных заболеваний мочеполового тракта, среди которых у больных практически с одинаковой частотой встречаются как облигатные патогены (T. pallidum, N. gonorhoeae, вирус герпеса, вирус папилломы человека), так и представители условно-патогенной микрофлоры (C. albicans, U. urealyticum, M. hominis и др.), а также их ассоцианты (10)
По данным ВОЗ, ежегодно в мире регистрируется более 150 млн. новых случаев урогенитальных инфекций (УГИ), что придает сложившейся ситуации характер эпидемии (6, 9, 10, 11). Столь высокая заболеваемость УГИ обусловлена рядом факторов, среди которых наиболее важную роль играет, с одной стороны, частое стертое или бессимптомное течение, а с другой – неэффективность проводимого лечения. Неудачи в терапии УГИ могут быть связаны с резистентностью возбудителей к стандартным противомикробным препаратам, несоблюдением врачебных рекомендаций (низкой комплаентностью), особенностями жизненного цикла патогена, повторным реинфицированием от полового партнера и т. д. В части случаев несостоятельными оказываются иммунологические механизмы защиты организма от действия патогена, что может быть обусловлено транзиторным иммунодефицитом или свойствами микроорганизма (способность к внутриклеточному существованию, латентному персистированию, размножению в иммуноцитах и т. п.). Эти факторы служат причиной частой хронизации УГИ, что влечет за собой повышение числа бесплодных браков, патологическое течение беременности, внутриутробную гипотрофию и инфицирование плода и, в конечном итоге, реализацию инфекционного процесса в раннем постнатальном периоде и росту неонатальной смертности (6, 10). Согласно современным данным, смертность новорожденных вследствие внутриутробной инфекции занимает второе место по частоте после родовой травмы.
Таким образом, УГИ являются острой медицинской и социально-экономической проблемой, требующей от практической медицины активного поиска новых эффективных терапевтических схем.
Любой инфекционный процесс (вирусной, бактериальной, грибковой или протозойной этиологии) является своего рода соревнованием между патогеном и защитными механизмами макроорганизма, предопределяющим исход инфекционного процесса (8). В условиях хронического течения заболевания, сопровождающегося общими нарушениями иммунного гомеостаза, истощением иммунокомпетентных клеток, снижением выработки гуморальных факторов, борьба с инфекцией зачастую оказывается неэффективной даже в случае использования современных этиотропных агентов (9).
Именно поэтому с целью повышения эффективности стандартной противомикробной терапии УГИ в современных условиях принято использовать различные иммунотропные препараты: интерферон и его индукторы, интерлейкины, различные иммуностимулирующие препараты, полученные путем химического синтеза или представляющие собой компоненты бактериальной стенки и др. Наиболее широкое распространение в гинекологии получили препараты экзогенного интерферона, его индукторы, а также иммуностимуляторы (3, 4, 10, 15, 17, 25, 30). При назначении лекарственных средств указанных групп необходимо учитывать различия в механизмах действия и скорости наступления иммуномодулирующего/иммуностимулирующего эффекта.
Так, в процессе иммунокоррекции в настоящее время часто используют как препараты, стимулирующие выработку эндогенного интерферона, так и сами цитокины. Индукторы стимулируют в организме синтез цитокинов, но этот синтез, естественно, выше в здоровых и малоповрежденных клетках. В случаях непосредственного инфицирования клеток иммунной системы, при глубоком угнетении функциональной активности иммуноцитов у больных (что характерно для любой хронической инфекции) применение индукторов ведет к дополнительной стимуляции пораженных клеток и не позволяет добиться достаточного иммуностимулирующего и корригирующего эффекта. Кроме того, многие индукторы быстрее разрушаются в организме, чем цитокины.
Отметим, что на практике в реализации индукционного механизма обнаруживаются свои «подводные камни». Во-первых, выработка эндогенного интерферона происходит достаточно медленно, и зачастую инфекционный агент размножается опережающими темпами. Во-вторых, потенциал клеток к выработке интерферона быстро иссякает (это особенно касается пораженных клеток), что существенно ограничивает защитные возможности организма. В-третьих, не существует однозначных данных о таргетном воздействии индукторов на одну лишь систему интерферона, в связи с чем нельзя с полной уверенностью утверждать о безопасности приема средств, относящихся к индукторам интерферона (3–5, 9, 14, 17, 57).
При использовании иммуностимуляторов, представляющих собой фрагменты бактерий, необходимо учитывать их относительно ограниченное воздействие на иммунную систему, направленное, в основном, на элиминацию внеклеточных микроорганизмов. Иммуностимулирующие препараты химического или животного происхождения обладают плеотропными эффектами, направленными, прежде всего, на повышение киллерного потенциала и создающие тем самым риск аутоагрессии в отношении собственных тканей.
Именно поэтому большинство лекарственных препаратов иммуностимулирующего ряда не назначаются в период беременности и грудного вскармливания.
Интерферон и его терапевтические эффекты
Одними из наиболее изученных и широко применяемых экзогенных цитокинов являются препараты интерферона-a.
Интерферон альфа (ИФНa) обладает противовирусным, опосредованным антибактериальным, противоопухолевым и иммуномодулирующим действием.
Противовирусное действие интерферона обусловлено его действием на различные стадии жизненного цикла вируса. Данный цитокин активирует ряд генов, ответственных за прямой противовирусный эффект. Данный эффект реализуется путем вовлечения ds-РНК-зависимой протеинкиназы Р (PKR), которая блокирует трансляцию вирусной мРНК и запускает апоптоз вирусинфицированной клетки через Bcl-2 и каспаза-зависимые механизмы (8). Другим механизмом противовирусного действия ИФНa является активация латентной РНК-эндонуклеазы, разрушающей вирусную РНК, а также семейства Мх-белков, которые препятствуют сборке вирусов. 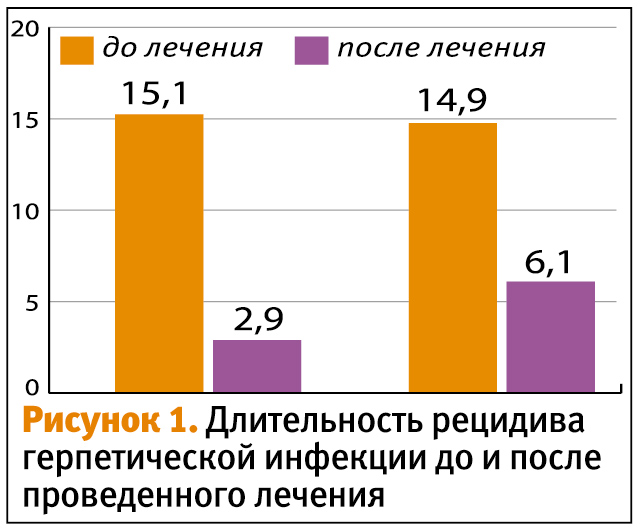
Иммуномодулирующее действие ИФНa выражается в индукции экспрессии молекул МНС I класса, модуляции и повышении продукции антител, усилении клеточной цитотоксичности Т-лимфоцитов и NK-клеток, ингибировании пролиферативной активности Т-лимфоцитов (8, 14). ИФНa способствует преимущественной дифференцировке Т-хелперов в Th1-лимфоциты, что снижает предрасположенность организма к аллергическим реакциям немедленного типа. Помимо этого, ИФНa препятствует апоптозу Т-лимфоцитов и Т-клеток памяти и повышает активность NK-клеток и антигенпрезентирующих клеток. Особенности иммуномодулирующего действия ИФНa позволяют считать его важнейшим связующим звеном между компонентами врожденного и адаптивного иммунитета (5).
За счет стимуляции процессов фагоцитоза и повышения активности макрофагов и NK-клеток ИФНa оказывает опосредованное антибактериальное действие в отношении как внутри-, так и внеклеточных возбудителей и способствует амплификации эффектов антибиотикотерапии. В российских исследованиях установлено, что ИФНa в зависимости от дозы способен оказывать бактериостатические и бактерицидные эффекты (9). ИФНa ограничивает рост опухоли, препятствуя синтезу опухолевых белков и ингибируя активность онкогенов, а также останавливая рост новых сосудов. Благодаря иммуномодулирующему действию (активация цитотоксических Т-лимфоцитов, NK-клеток и др.) ИФНa повышает эффективность противоопухолевого надзора (3, 5, 8, 14).
Применение препаратов ИФНa в терапии хронических УГИ является патогенетически оправданным еще и потому, что ряд возбудителей данных заболеваний обладает супрессирующим действием как на иммунную систему в целом, так и на выработку интерферона в частности. В случае лечения инфекционно-воспалительных заболеваний мочеполового тракта у женщин предпочтительным является местное лекарственное воздействие, чего удается добиться при использовании интерферонсодержащих суппозиториев для ректального или вагинального применения. В настоящее время в России с этой целью используются следующие лекарственные средства: Кипферон, Виферон, Гиаферон и Генферон. За рубежом также применяются топические препараты интерферона (в виде кремов, гелей), однако их использование несколько ограничено ввиду недостаточной стабильности лекарственной формы (56). Наиболее современным российским препаратом ИФНa в лекарственной форме суппозитории для ректального и вагинального введения является комплексный препарат Генферон, производимый отечественной биотехнологической компанией «Биокад». Помимо интерферона, Генферон содержит аминокислоту таурин, оказывающую выраженное антиоксидантное, репаративное и метаболическое действие, а также местный анестетик бензокаин, эффективно купирующий болевой синдром, весьма характерный для пациенток, страдающих хроническими УГИ.
Интерферонотерапия папилломавирусной и герпесвирусной инфекций
Как уже упоминалось выше, большинство хронических инфекционных процессов поддерживаются способностью возбудителей тем или иным образом избегать иммунологического контроля, а также вызывать нарушения иммунного гомеостаза.
Интересным с этой точки зрения представляются заболевания, ассоциированные с вирусом папилломы человека. Известно, что в зависимости от серотипа, которых для ВПЧ выделено уже более 100, инфекция может протекать в виде различных клинических вариантов (вульгарные бородавки, аногенитальные кондиломы, дисплазия шейки матки, папилломатоз наружных гениталий и т. д.). Сложность в осуществлении полноценного и эффективного иммунологического ответа на ВПЧ-инфекцию связана с особенностями жизненного цикла вируса.
ВПЧ строго эпителиотропен и поражает клетки эпителия эктодермального происхождения. ВПЧ не обладает цитопатическим действием в отношении кератиноцитов, в которых происходит его размножение, и не инфицирует эпидермальные антигенпрезентирующие клетки. Поскольку в течении ВПЧ-инфекции отсутствует фаза виремии, т. е. выхода вирусных частиц в кровоток, невозможным становится развитие полноценного системного иммунного ответа (2, 3, 13, 17, 30, 33, 56).
ВПЧ синтезирует специфические белки, которые помимо прямого онкогенного действия (стимуляция пролиферации и опухолевой трансформации клеток) способны оказывать супрессирующее влияние на определенные звенья иммунной системы. Так, вирусный белок Е7 блокирует большинство генов, индуцируемых ИФНa, и таким образом нейтрализует его противовирусную и противоопухолевую активность. Этот же белок инактивирует фактор активности ИФНaIRF, ингибирует экспрессию генов главного комплекса гистосовместимости, тормозит созревание антигенпрезентирующих клеток. Белок Е5 закисляет рН в эндосомах и препятствует процессингу и презентированию антигена дендритными клетками. Белок Е6 ингибирует действие лимфокина IL-18, играющего важную роль в формировании Т-киллерного иммунного ответа. Немаловажной способностью ВПЧ является его угнетающее влияние на уровень эндогенного интерферона.
В комплексной терапии ВПЧ препараты интерферона используются уже не одно десятилетие и зарекомендовали себя как лекарственные средства, существенно повышающие эффективность стандартного лечения. В исследовании Howard D. и соавт. (30) исследовались терапевтические эффекты применения ИФНa у больных с папилломатозом гениталий после проведения деструктивного лечения. Пациентам основной группы интерферон вводился внутрь поражений в дозе 1000000 МЕ 1 раз в 3 дня в течение 3 недель, в то время как больным из группы сравнения было проведено только деструктивное лечение и назначено плацебо (изотонический раствор). В результате проведенных лечебных мероприятий проявления папилломатоза исчезли у 48,5% больных, получавших интерферон, и только у 14,3% пациентов группы сравнения. Эффективность включения ИФНa в стандартное лечение рефрактерных поражений аногенитальной области, вызванных ВПЧ, подтверждена и в исследовании Paavonen J., в котором интерферон вводился подкожно в дозе 3000000 МЕ 3 раза в неделю в течение 3 недель (33).
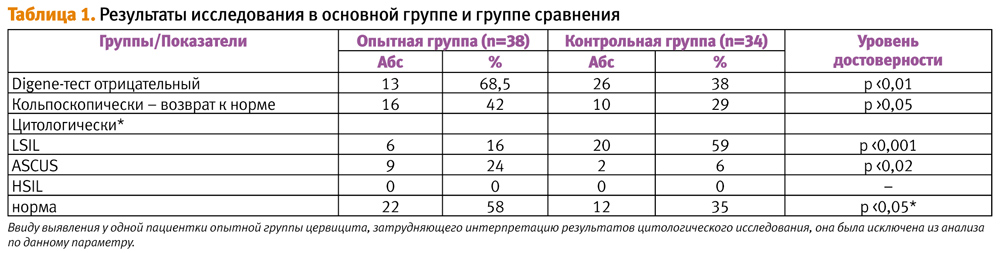
В 2006–2007 гг. на базе ФГУ «Научный центр акушерства, гинекологии и перинатологии Росмедтехнологий» было проведено сравнительное рандомизированное двойное слепое плацебо-контролируемое клиническое исследование эффективности препарата Генферон для лечения плоскоклеточных интраэпителиальных поражений шейки матки низкой степени тяжести, ассоциированных с ВПЧ высокоонкогенного риска. 40 женщин репродуктивного возраста с подтвержденным диагнозом интраэпителиального поражения шейки матки низкой степени (LSIL) и наличием ВПЧ высокоонкогенного риска были рандомизированы в две группы: I из 23 человек получала Генферон, II из 17 человек – плацебо. Введение препарата в дозировке 500000 МЕ или плацебо осуществлялось вагинально 2 раза в сутки в течение 10 дней с последующим назначением 1 раз в сутки через день в течение 3 месяцев.
По окончании лечения Pap-тест выявил регресс ВПЧ-ассоциированных изменений шейки матки в 90,5% случаев в группе, получавшей Генферон (группа плацебо – 40%). Отрицательный результат Digene-теста был достигнут в 71,4% случаев (группа плацебо – 26,6%), при этом снижение количества ВПЧ у пациенток, принимавших Генферон, выявлялось в 100% случаев (13). Результаты исследования представлены в таблице 1.
Немаловажным фактором неудач в лечении УГИ является частое выявление микст-инфекций, в частности ВПЧ и вируса простого герпеса. Так же, как и в случае ВПЧ, вирус герпеса вызывает разнообразные нарушения в функционировании иммунной системы. Иммунопатологические механизмы при герпетической инфекции включают и недостаточно напряженный ответ в отношении персистирующего возбудителя, и неэффективную регуляцию специфического иммунитета. Вирус герпеса не только персистирует в иммунокомпетентных клетках, но и репродуцируется в них, что вызывает снижение их функциональной активности и, в конечном итоге, гибель. Кроме этого, вирус герпеса способен продуцировать ложные рецепторы интерферона, что обусловливает его недостаточную активность в условиях сохранения физиологической концентрации. Вирус герпеса угнетает процессы презентации антигена путем экспрессии молекул псевдо-МНС I класса, ответственных за развитие цитотоксического иммунного ответа (4, 9, 34).
Иммунологический статус больных герпетической инфекцией имеет свои специфические черты: характерно снижение общего количества лейкоцитов, уровня ИФН и CD4+, тенденция к снижению CD8+, CD16+, CD56+, накоплению ЦИК. Все указанные изменения делают элиминацию вируса невозможной и создают благоприятные условия для распространения и рецидивирования инфекции (4).
Результаты сравнительного двойного слепого рандомизированного исследования Eron L. J. и соавт. свидетельствуют об эффективности препаратов интерферона в лечении рецидивирующего генитального герпеса. Было включено 37 больных в периоде ремиссии, не получавших на момент включения противовирусной и иммуносупрессивной терапии, частота рецидивов генитального герпеса у которых составляла 8 и более в год. Пациенты были разделены на 2 группы: основную, в терапии которой использовался ИФНa (подкожно) в дозе 3000000 МЕ или плацебо трижды в неделю в течение 3 месяцев. Время до развития рецидива в основной группе составило 35 дней (плацебо – 28), при этом 16,6% пациентов основной группы были свободны от рецидива в течение всего периода наблюдения, в то время как в группе сравнения подобных явлений не наблюдалось (25).
С целью изучения эффективности и безопасности препарата Генферон в 2004 г. на кафедре дерматовенерологии Государственного института усовершенствования врачей Министерства обороны РФ (ГИУВ МО РФ) было проведено клиническое исследование, в которое было включено 60 женщин с диагнозом рецидивирующего генитального герпеса и сопутствующей микст-инфекцией урогенитального тракта.
При клинико-лабораторном обследовании было обнаружено частое сочетание генитального герпеса с папилломавирусной инфекцией (22%) и урогенитальным кандидозом (16%), что согласуется с данными литературы (Губанова Е. И., 2000; Зудин А. Б., 2000; Гладько О. В., 2003; Катханова О. А., 2003).
Методом случайной выборки были сформированы 2 группы из 30 женщин, равнозначные по возрасту, тяжести проявлений и частоте рецидивов генитального герпеса. I группа (30 женщин) с целью лечения острой герпетической инфекции получала ацикловир по 0,2 г 5 раз в день в течение 5 дней в сочетании с Генфероном по 500000 МЕ 2 раза в день вагинально в течение 10 дней. В последующем пациентки получали Генферон вагинально по 500000 МЕ 2 раза в день через 1 день в течение 5 месяцев с целью профилактики рецидивов. II группа (30 женщин) с целью лечения острой герпетической инфекции получала ацикловир по 0,2 г 5 раз в день в течение 5 дней. В последующем пациентки получали ацикловир 400 мг 2 раза в день ежедневно в течение 5 месяцев.
Основным показателем тяжести течения генитального герпеса является количество возникающих рецидивов. Данные о количестве рецидивов в процессе лечения (5 месяцев) и после лечения (7 меcяцев) пересчитывались на 1 год. До лечения у пациенток I группы (ацикловир + Генферон) количество рецидивов снизилось в 4,8 раза (p < 0,05), тогда как у пациенток II группы (ацикловир) снизилось в 2,4 раза (p < 0,05).
Длительность рецидива на фоне проводимой профилактической терапии статистически достоверно уменьшилась в обеих группах, в I группе с 15,1±1,09 дня до 2,9±0,14 дня, то есть в 5,1 раза (p <0,05), во II группе – с 14,9±1,04 дня до 6,1±0,77, то есть в 2,4 раза (p <0,05) (см. рисунок).
Снижение числа рецидивов и уменьшение их продолжительности было достоверно более выражено в группе больных, получавших препарат Генферон (p < 0,05).
Данные, полученные в ходе проведенного исследования, согласуются как с отечественными, так и зарубежными литературными источниками и свидетельствуют об ощутимом положительном влиянии топической интерферонотерапии в сочетании со стандартным противовирусным лечением на течение различных по тяжести форм генитального герпеса (15, 50).
Окончание читайте в следующем номере.
Список литературы находится в редакции.
По материалам журнала «Эффективная фармакотерапия в дерматовенерологии и дерматокосметологии, № 3/2010».
На территории Украины препарат Генферон® зарегистрирован под торговой маркой Генферон®ІБ.
Препарат Генферон ІБ. Сертификат о государственной регистрации медицинского иммунобиологического препарата Генферон ИБ №857/11-300200000 от 05.10.2011 (дата окончания действия: 05.10.2016). Препарат Генферон ІБ используется в составе комплексной терапии инфекционно-воспалительных заболеваний урогенитального тракта у взрослых. Фармакотерапевтическая группа. Иммуностимуляторы. Интерферон альфа-2b. Код АТС L03A В05. Побочные реакции. Аллергические реакции: возможны аллергические реакции, включая кожные высыпания, зуд. Эти симптомы исчезают через 72 часа после прекращения введения препарата или уменьшения дозы. Иногда могут наблюдаться озноб, повышение температуры тела, утомляемость, потеря аппетита, мышечная и головная боль, боль в суставах, изменения в месте введения, потливость, а также лейко- и тромбоцитопения. Категория отпуска. По рецепту.
Препарат Генферон Лайт ІБ. Сертификат о государственной регистрации медицинского иммунобиологического препарата Генферон Лайт ИБ № 895/12-300200000 от 26.11.2012 (дата окончания действия: 26.11.2017). Препарат Генферон Лайт ІБ используется, как компонент комплексной терапии ОРВИ и других инфекционных заболеваний бактериальной и вирусной этиологии у детей; как компонент комплексной терапии – для лечения острых кишечных инфекций вирусной и смешанной вирусно-бактериальной этиологии у детей; при инфекционно-воспалительных заболеваниях урогенитального тракта у детей и женщин, в том числе беременных. Фармакотерапевтическая группа. Иммуностимуляторы. Интерферон альфа-2b. Код АТС L03A В05. Побочные реакции. До настоящего времени не наблюдалось тяжелых или опасных для жизни побочных явлений. Могут наблюдаться явления, которые возникают при применении всех видов интерферона альфа-2b, такие как озноб, повышение температуры, утомляемость, потеря аппетита, мышечные и головные боли, боли в суставах, потливость, а также лейко- и тромбоцитопения, но чаще они встречаются при превышении суточной дозы свыше 10 000 000 МЕ. Категория отпуска. По рецепту. Данная информация предназначена исключительно для профессиональной деятельности фармацевтических и медицинских работников.

коментариев