Атопический дерматит (АД) – хроническое воспалительное заболевание кожи, сопровождающееся зудом. Распространенность его довольно высока и составляет около 10% (от 2% в Иране и Китае до 20% в Скандинавии, Англии и Австралии). Чаще всего, пациенты с АД – это дети раннего возраста. Заболевание в 65% случаев манифестирует до 1 года жизни, и у 85% пациентов – до 5 лет. Понятно, что при такой распространенности основное бремя ведения пациентов с АД ложится на плечи врачей первичного звена. Безусловно, дерматологи и аллергологи могут обеспечить более квалифицированный подход к лечению пациентов с АД, но этих специалистов просто не хватает. Тем более что в обычных случаях АД вполне успешно можно лечить и на первичном уровне.
За последние годы был опубликован целый ряд руководств по диагностике и лечению АД, в том числе, адресованных врачам общей практики (последнее руководство – в 2014 г.). Кроме того, благодаря новым данным о патогенезе АД изменился подход к его лечению – акцент сместился на наружную терапию. В данной статье мы попытались обобщить современные сведения об АД, в большей мере необходимые именно врачам первичного звена.
Этиопатогенез
Этиопатогенез АД сложен и обусловлен взаимодействием многих факторов, таких как дисфункция кожного барьера, генетическая предрасположенность, иммунная дисфункция, внешние неблагоприятные воздействия. Еще недавно основным патогенетическим механизмом развития воспалительных изменений в коже при АД считалась дисрегуляция T-хелперов, повышенная продукция IgE и клеточно-опосредованная гиперреактивность. Однако, недавние исследования показали, что ключевую роль в патогенезе АД играет нарушение барьерной функции кожи.
Основная функция кожного барьера – ограничение потерь жидкости и предотвращение проникновения через кожу болезнетворных микроорганизмов, аллергенов и ирритантов. Целостность кожного барьера обеспечивает поверхностный слой кожи или роговой слой (stratum corneum). В терминальной дифференцировке эпидермиса и формировании кожного барьера, в том числе и рогового слоя, важное значение имеет белок филаггрин. У 50% пациентов со среднетяжелым и тяжелым АД выявлены мутации в гене FLG (кодирующем филаггрин), которые приводят к нарушению синтеза и структуры этого белка (всего описано более 40 мутаций). Наличие мутаций FLG увеличивает риск развития АД в 2–3 раза.
NB! Пищевая аллергия НЕ является причиной атопического дерматита, пищевые аллергены - это триггеры его обострений
Предложено несколько теорий, объясняющих, каким образом дефекты филаггрина способствуют развитию АД. Неадекватный синтез филаггрина приводит к снижению способности кератиноцитов препятствовать трансэпидермальным потерям воды и таким образом поддерживать гидратацию кожи. Это приводит к сухости кожи, которая, в свою очередь, сопровождается зудом, а впоследствии и другими симптомами АД. Нарушение целостности кожного барьера также может способствовать проникновению аэроаллергенов с последующим развитием в коже воспалительного ответа. Согласно другой теории, нарушение барьерных свойств кожи приводит к изменению pH на ее поверхности. Это способствует размножению и росту бактерий, таких как Staphylococcus aureus, что, в свою очередь, стимулирует неспецифические иммунные реакции, воспаление и повреждение кожи.
Аллергия и АД
 Взаимосвязь между пищевой аллергией и АД существует, но, по всей видимости, часто переоценивается. Более 90% родителей ошибочно полагают, что пищевая аллергия – единственная или главная причина заболевания кожи ребенка. Концентрация усилий не на соответствующем местном лечении проявлений АД, а на исключении всех возможных пищевых аллергенов приводит к назначению строгих ограничительных диет, которые, в свою очередь, могут способствовать развитию дефицита различных пищевых нутриентов (белка, микроэлементов) и существенному снижению качества жизни пациентов и их родителей. Кроме того, из-за отсутствия видимого эффекта от одних лишь элиминационных мероприятий нередко назначается избыточная системная медикаментозная терапия, тогда как эффективное местное лечение обычно уменьшает беспокойство родителей относительно пищевой аллергии.
Взаимосвязь между пищевой аллергией и АД существует, но, по всей видимости, часто переоценивается. Более 90% родителей ошибочно полагают, что пищевая аллергия – единственная или главная причина заболевания кожи ребенка. Концентрация усилий не на соответствующем местном лечении проявлений АД, а на исключении всех возможных пищевых аллергенов приводит к назначению строгих ограничительных диет, которые, в свою очередь, могут способствовать развитию дефицита различных пищевых нутриентов (белка, микроэлементов) и существенному снижению качества жизни пациентов и их родителей. Кроме того, из-за отсутствия видимого эффекта от одних лишь элиминационных мероприятий нередко назначается избыточная системная медикаментозная терапия, тогда как эффективное местное лечение обычно уменьшает беспокойство родителей относительно пищевой аллергии.
Истинный индуцированный пищевыми аллергенами АД встречается редко. Чаще всего пищевая аллергия проявляется такими IgE-опосредованными кожными реакциями как острая крапивница и отек Квинке. Обострение или усиление симптомов АД, вызванное воздействием пищевых аллергенов, как правило, является не IgE-опосредованной реакцией, а проявлением гиперчувствительности замедленного типа и обычно развивается спустя 2–6 часов после действия аллергена.
Преувеличение роли пищевой аллергии в генезе АД связано с наблюдением, что у пациентов с АД она часто имеет место. Действительно, если в общей популяции распространенность пищевой аллергии среди детей первых 5 лет жизни составляет около 5%, то у детей с АД — 30–40%, и до 80% этих детей имеют повышенные концентрации специфических IgE к пищевым аллергенам, даже в отсутствие клинических проявлений пищевой аллергии. Кроме того, при наличии пищевой аллергии АД характеризуется более ранним началом и более тяжелыми проявлениями. Чем раньше у ребенка появились признаки АД, тем выше риск наличия пищевой аллергии.
Таким образом, наличие пищевой аллергии – фактор риска более тяжелого течения АД и худшего прогноза. Поэтому исключение из рациона ребенка с АД всех потенциально аллергенных продуктов малоэффективно, особенно если сенсибилизация (IgE- или не-IgE-опосредованная) к ним подтверждена только лабораторными данными (без клинической верификации). Единственное исключение – яйца. Было показано, что у детей с АД, имеющих повышенный уровень специфических IgE к белку яиц, исключение их из диеты в половине случаев сопровождается существенным клиническим улучшением.
Выявление сенсибилизации к пищевым продуктам (в первую очередь, к молоку, яйцам, арахису, пшенице и сое) в настоящее время рекомендуется детям младше 5 лет при:
1) среднетяжелом и тяжелом АД, плохо поддающемся адекватной местной терапии и/или
2) наличии четкой связи между употреблением в пищу определенных продуктов и появлением кожных высыпаний.
После 3 лет сенсибилизация к пищевым аллергенам уменьшается, и основное значение приобретает воздействие аэроаллергенов. Наиболее распространенными аэроаллергенами, которые могут вызвать обострение АД, являются клещи домашней пыли, плесень, пыльца, перхоть животных.
Как известно, в концепции «атопического марша» АД является первым «шагом» в прогрессии целого ряда аллергических заболеваний. Принимая во внимание, что нарушения функции кожного барьера, обусловленные мутациями FLG, способствуют проникновению в кожу аэроаллергенов с последующей эпикутанной сенсибилизацией, становится понятным, почему раннее оптимальное и эффективное лечение АД, как показывают исследования, снижает риск развития в дальнейшем аллергического ринита и бронхиальной астмы.
Аллергический контактный дерматит – реакция гиперчувствительности замедленного типа на кожные аллергены, роль которой в персистировании симптомов АД недооценивается. Среди детей с трудно поддающимся лечению АД до 50% имеют, по крайней мере, 1 положительный результат патч-теста на кутанные аллергены. Возможность контактной аллергии следует учитывать во всех случаях необычного или трудно контролируемого течения АД.
Таким образом, атопический дерматит развивается у генетически предрасположенных лиц в результате воздействия различных внешнесредовых факторов (триггеров).
В настоящее время главными факторами риска развития АД считают:
1) мутации в гене FLG, снижающие функцию филаггрина;
2) отягощенный по атопии семейный анамнез.
Триггерами АД могут быть:
1) контактные раздражители – мыло, растворители, шерсть, одежда, механические раздражители, синтетические моющие средства, консерванты, отдушки;
2) аэроаллергены;
3) микроорганизмы – S. aureus, Pityrosporum, Candida, Trichophyton, Malassezia furfur;
4) пот;
5) стресс;
6) воздействие высоких или низких температур.
Диагностика
Диагностика АД базируется, в основном, на клинических данных, поскольку нет надежных лабораторных или иных маркеров заболевания. Наиболее ранними и до сих пор широко используемыми являются критерии Hanifin and Rajka, предложенные в 1980 году (табл. 1). Диагноз АД устанавливается при наличии у пациента 3 обязательных (больших) и 3 дополнительных (малых) критериев. В то же время, для клинической практики эти критерии не совсем удобны. С одной стороны, они громоздки, с другой – некоторые из малых критериев неспецифичны, например – белый лишай, а другие хоть и являются весьма характерными для АД, но очень редко встречаются (экзема сосков или хейлит). В связи с этим многими исследовательскими группами предлагались различные модификации критериев Hanifin and Rajka, и в 2003 году на согласительной конференции, организованной Американской ассоциацией дерматологии, были утверждены модифицированные критерии диагностики АД, более гибкие и удобные для практики, а также применимые для всех возрастных групп.
Согласно этим критериям диагностики АД (Eichenfield et al., 2003) основными клиническими признаками заболевания являются: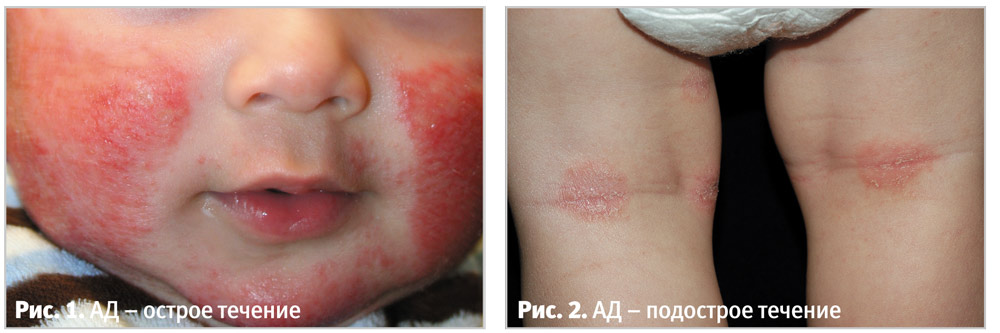
1) зуд;
2) экзематозные высыпания на коже (острые, подострые или хронические), имеющие:
а) типичные морфологические и возрастные особенности;
б) хроническое или рецидивирующие течение.
Острые проявления АД характеризуются наличием пузырьков и пузырей с интенсивным покраснением кожи, мокнутием и выраженным зудом (рис. 1). При подостром течении зуд умеренный, может отмечаться боль, жжение, кожа гиперемирована, с шелушением, расчесами, трещинами, имеет вид обожженной или ошпаренной (рис. 2).
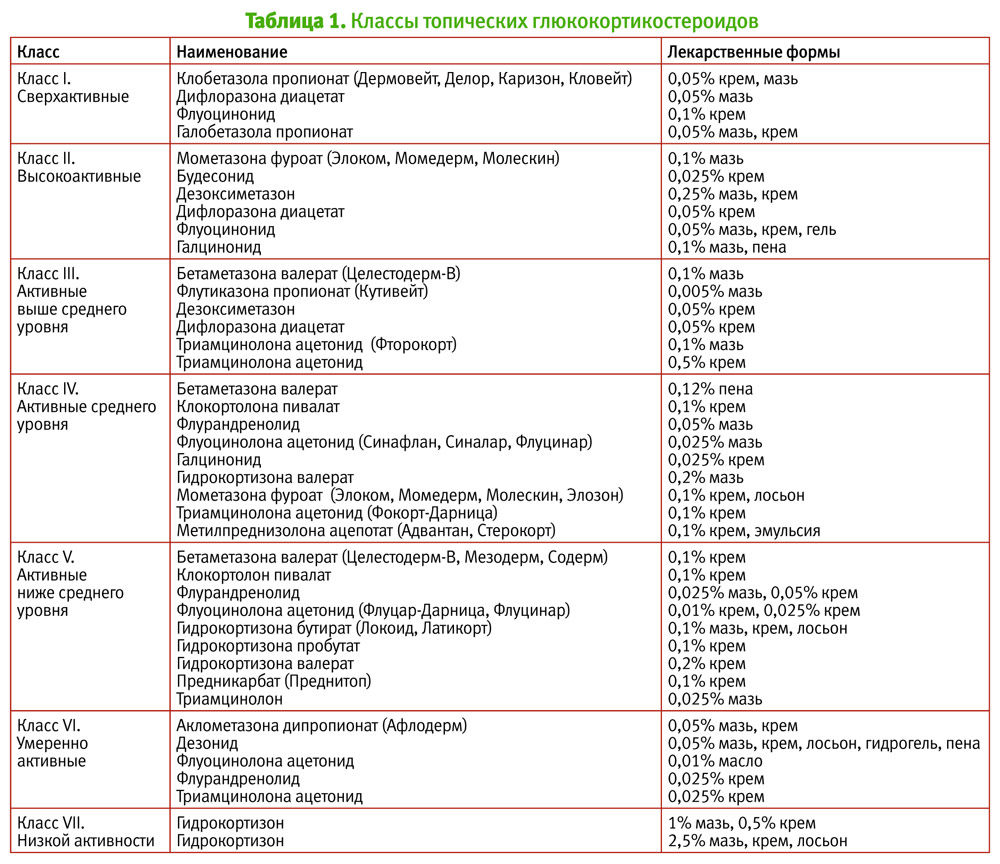
Хроническое экзематозное воспаление проявляется утолщением кожи, акцентированием кожных линий, экскориациями и растрескиванием кожи, сопровождается зудом от умеренного до интенсивного (рис. 3). Возрастные особенности высыпаний включают:
- поражение кожи лица, шеи и разгибательных поверхностей у детей раннего возраста;
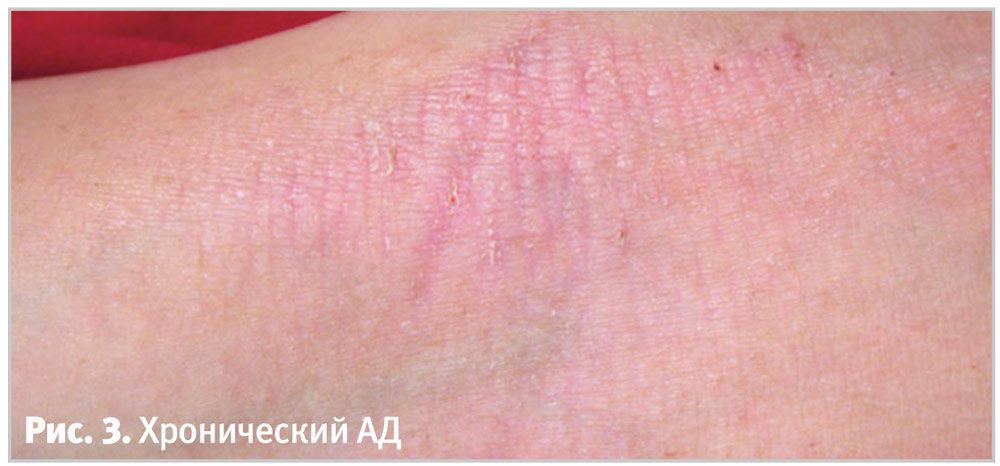
- наличие поражений сгибательных поверхностей при осмотре или в анамнезе у пациентов любого возраста;
- отсутствие высыпаний в паховых и подмышечных областях.
Основные критерии обязательно должны иметь место у пациента с АД и при наличии их в полном объеме диагноз АД можно считать установленным.
Важными клиническими критериями АД, которые встречаются в большинстве случаев и подтверждают диагноз АД, являются:
1) ранний возраст начала заболевания;
2) наличие атопии:
а) отягощенный атопическими заболеваниями персональный или семейный анамнез;
б) повышение уровня IgE;
3) сухость кожи.
И, наконец, к дополнительным клиническим критериям АД относят:
1) нетипичные сосудистые реакции (побледнение кожи лица, белый дермографизм);
2) фолликулярный кератоз/ихтиоз/гиперлинеарность ладоней/белый лишай;
3) глазные/периорбитальные изменения;
4) другие региональные изменения (периоральные/периаурикулярные поражения);
5) перифолликулярная локализация высыпаний/лихенификация/пруригинозные изменения.
Дополнительные признаки могут помочь в диагностике АД, но слишком неспецифичны, чтобы использоваться для выявления АД в качестве самостоятельных критериев.
Кроме того, в диагностические критерии АД 2003 года внесен перечень заболеваний, которые должны быть исключены у пациентов с подозреваемым АД (чесотка, аллергический контактный дерматит, себорейный дерматит, кожная Т-клеточная лимфома, ихтиозы, псориаз, фотодерматозы, иммунодефицитные заболевания).
Биопсия кожи и лабораторные исследования (в том числе и рутинное определение уровня IgE) обычно не требуются для диагностики АД, но они могут понадобиться для исключения других, клинически похожих на АД, заболеваний, особенно в случаях, когда стандартная терапия оказывается неэффективной.
Влияние АД на качество жизни пациентов и их семей не должно недооцениваться. Снижение качества жизни отмечается у почти 50% детей с АД за счет недосыпания и утомляемости (которые прямо коррелируют с выраженностью зуда и тяжестью кожных проявлений), ограничений в повседневной деятельности и депрессии. Дети с тяжелым АД часто имеют меньше друзей и реже участвуют в общественных мероприятиях, чем их сверстники. Дети с АД имеют более высокий риск депрессий, тревожных расстройств и других психических нарушений. Родители детей с АД также часто страдают от недостатка сна и депрессий, вызванных необходимостью тратить много времени и средств на лечение детей, ощущением безнадежности и чувством вины. Фактически, частота депрессий у матерей детей с АД вдвое выше, чем у матерей детей, больных бронхиальной астмой.
Для оценки тяжести течения АД было предложено 28 различных шкал, в том числе SCORAD, EASI, IGA, SASSAD, POEM, TISS и др. При этом «золотым стандартом» не признана ни одна из них. Эти шкалы используются, в основном, в клинических исследованиях, но не в клинической практике. На самом деле, наблюдая пациента с АД, клиницист может ограничиться общими вопросами об интенсивности зуда, динамике высыпаний, качестве сна, ограничениях в повседневной активности, а специальными шкалами пользоваться лишь в тех случаях, когда это действительно необходимо.
Кроме того, при наблюдении пациента с АД следует помнить о повышенном риске развития у него аллергического ринита, поллиноза, бронхиальной астмы, пищевой аллергии. При появлении симптомов, характерных для этих заболеваний, нужно провести соответствующее обследование и назначить лечение. Вообще, мультидисциплинарный подход к ведению пациентов с АД повсеместно приветствуется.
Лечение
Лечение АД включает 4 основных компонента, направленных на устранение кожных проявлений:
1) уход за кожей с целью восстановления и поддержания нормального кожного барьера;
2) применение местных противовоспалительных средств;
3) контроль зуда;
4) воздействие на инфекционные триггеры, своевременное распознавание и лечение инфекционных осложнений.
Обучение пациентов и их семей – другой важный фактор, который не стоит игнорировать. Для родителей заболевание ребенка может оказаться тяжелым испытанием, особенно если учесть, что АД протекает длительно, и даже на фоне адекватной терапии высыпания могут рецидивировать. Если родители осведомлены об особенностях АД и имеют реалистичные ожидания по поводу результатов лечения, их приверженность терапии выше, а уровень беспокойства – ниже. Как показывают исследования, эффективность лечения АД выше в семьях, где родители хорошо информированы. Составление письменных планов действия (памяток) для родителей, подобных тем, которые используются при бронхиальной астме, повышают комплаенс при лечении АД.
Уход за кожей – основа лечения АД. Сегодня существуют убедительные доказательства того, что уход за кожей, обеспечивающий восстановление ее барьерных функций, способствует сокращению частоты и уменьшению степени выраженности обострений АД, устранению зуда и связанного с ним беспокойства и расчесывания кожи, а также сопровождается уменьшением потребности в применении топических кортикостероидов.
Уход за кожей имеет 2 аспекта: увлажнение кожи и устранение раздражителей и триггеров обострений.
Увлажнение кожи должно проводиться как во время обострения АД (в дополнение к противовоспалительной терапии), так и постоянно в периоде ремиссии (даже в отсутствие клинических проявлений) – для профилактики обострений заболеваний. Увлажняющие мероприятия включают ванны, использование увлажняющих косметических средств и, иногда, использование влажных повязок.
Ванны при АД рекомендуются как составная часть лечения и ухода. Оптимальная частота и длительность ванн для детей с АД не определена, так как нет надежных научно обоснованных данных. Но в целом, рекомендуются ежедневные или 1 раз в 2–3 дня ванны, длительностью не более 20 мин., с использованием обычной теплой воды. Продолжительность и частота процедур титруется индивидуально, в зависимости от эффективности и переносимости в каждом конкретном случае. Рекомендуется при купании пользоваться не мылом, а нейтральными, с низкими значениями рН, гипоаллергенными моющими средствами для очищения загрязненных поверхностей. Нет никаких доказательств того, что добавление в воду масел, смягчающих средств и других добавок, а также использование кипяченой или кислой родниковой воды, имеет какой-либо существенный положительный эффект. Сразу же после купания на кожу должны быть нанесены увлажняющие средства, для того чтобы предотвратить ее дегидратацию.
Увлажняющие средства, которые применяются при АД, обычно содержат эмоленты (например, гликоль, глицерина стеарат, соевые стеролы), смягчающие кожу, гумектанты (глицерин, молочная кислота, мочевина), задерживающие влагу в коже, и окклюзионные агенты (вазелин, диметикон, минеральные масла), которые создают на поверхности кожи пленку, препятствующую потере жидкости. Кроме того, увлажняющий эффект косметического средства зависит от соотношения в нем липидов и воды. Чем больше липидов, тем сильнее увлажняющее действие. Самое высокое соотношение «липид-вода» имеют мази, они иногда на 100% состоят из липидов и применяются при очень сухой коже. Далее следуют кремы, в них липидов больше, чем воды, но они содержат консерванты и стабилизаторы, которые не позволяют компонентам отделяться друг от друга. Кремы лучше впитываются в кожу, чем мази, не оставляют ощущения сальности, но добавленные компоненты могут иногда вызывать жжение склонной к атопии кожи. В лосьонах воды больше, чем липидов, поэтому для достижения нужного уровня гидратации их приходится чаще наносить на кожу. В настоящее время на нашем рынке представлено множество увлажняющих средств, они обычно имеют обозначение «для сухой, очень сухой и склонной к атопии кожи».
Увлажняющие средства должны наноситься на кожу, по крайней мере, 1 раз в день, постоянно, независимо от того, имеются ли проявления АД.
Влажные обертывания с нанесением (или без) топических кортикостероидов рекомендуются для пациентов с выраженными проявлениями АД для ускорения достижения терапевтического эффекта. Влажные обертывания улучшают проникновение топических стероидов в кожу, уменьшают зуд и служат механической преградой для расчесывания. Техника их проведения следующая: после ванны кожа просушивается, на пораженные участки наносится топический стероид, на остальные участки кожи – увлажняющее средство, сверху на пораженные участки накладывается слой марли или хлопчатобумажной ткани, смоченной в теплой воде, а поверх ее – сухая хлопчатобумажная ткань. Ребенок должен быть укрыт одеялом или находиться в теплой комнате. Повязку можно оставить на 3–8 часов. Влажные обертывания могут использоваться непрерывно в течение 24–72 часов или раз в сутки (например, на ночь) в течение 1 недели. Такой способ лечения желательно проводить под контролем врача.
Полностью устранить провоцирующие факторы при АД практически невозможно, но можно постараться свести их воздействие к минимуму. Так, рекомендуется по возможности ограничивать контакт с аэроаллергенами и причинно-значимыми пищевыми аллергенами, избегать контакта с инфекционными (особенно вирусными) больными, не использовать мыло и грубые моющие средства, ароматы. Раздражать кожу может пот и слюна, одежда из грубой или воздухонепроницаемой ткани. Рекомендуется минимизировать стрессовые ситуации для ребенка, а при их возникновении – эффективно купировать. Оптимальным видом спорта для детей с АД является плавание. После плавания в бассейне нужно смыть хлорированную воду и нанести увлажняющее средство.
NB! Для лечения АД в большинстве случаев нет необходимости в использовании стероидов высокой активности
Местная противовоспалительная терапия применяется в периоде обострения АД. Первая линия терапии – топические глюкокортикостероиды (ГКС). При рациональном использовании они эффективны и безопасны. Однако в случаях неадекватного использования возрастает риск развития атрофии кожи, появления стрий, телеангиэктазий, а также системных эффектов, связанных с всасыванием препарата. Другие потенциальные побочные эффекты могут отмечаться при нанесении стероидов вокруг глаз (повышение внутриглазного давления, катаракта) или вокруг рта (периорифициальный дерматит). Опасения по поводу развития неблагоприятных эффектов нередко порождают «стероидофобию» у родителей и врачей. И хотя стероидофобия не коррелирует с тяжестью АД, она действительно приводит к тому, что топические стероиды недостаточно используются при этом заболевании.
Топические ГКС различаются по активности от VII класса (низкой активности) до I класса (сверхактивные) (табл. 2). Препараты I класса в 1800 раз мощнее наименее активных препаратов VII класса. Риск неблагоприятных эффектов прямо коррелирует с активностью стероидов. На степень активности влияет не только действующее вещество, но и его концентрация, а также лекарственная форма. Для лечения АД в большинстве случаев нет необходимости в использовании стероидов высокой активности. В повседневной практике обычно используются топические стероиды низкой активности (VI и VII классы) для лечения высыпаний в области лица, шеи и кожных складок; и умеренной активности (III, IV, и V классы) при локализации высыпаний на туловище и конечностях. Мази лучше переносятся, так как реже, чем кремы, вызывают ощущения жжения или покалывания, но ГКС в них более активны.
Топические ГКС наносятся тонким слоем несколько раз в день на пораженные участки кожи до тех пор, пока высыпания возвышаются над поверхностью кожи, зудят и интенсивно гиперемированы. Нет четких рекомендаций, в течение какого времени нужно использовать топические стероиды. Как только достигнут нужный клинический эффект, ГКС отменяют и назначают вновь при очередном обострении АД. Тем не менее, если в течение 1–2 недель лечения топическими стероидами явного улучшения не наблюдается, стоит пересмотреть диагноз или план лечения.
Топические ингибиторы кальциневрина (ТИК) – местные иммуносупрессоры, подавляющие T-клеточную функцию. В настоящее время применяются 2 препарата: такролимус (0,03 и 0,1% мази) и пимекролимус (1% крем). Оба одобрены как терапия второй линии (у детей старше 2 лет) для среднетяжелого и тяжелого АД. Недавний мета-анализ продемонстрировал, что оба препарата уменьшают воспаление и зуд при АД у детей, при этом такролимус более эффективен.
У ТИК отсутствуют неблагоприятные эффекты, характерные для топических ГКС, поэтому они могут быть рекомендованы для пациентов, имеющих осложнения от долгосрочного применения топических стероидов. Однако ТИК чаще вызывают жжение и покалывание кожи (такролимус>пимекролимус) и стоят дороже. Кроме того, сообщалось, что у лабораторных животных, получавших высокие дозы системных ингибиторов кальциневрина, развивались злокачественные опухоли. Также зарегистрированы редкие случаи развития лимфомы и рака кожи у взрослых, применявших ТИК, хотя причинно-следственные связи в этих случаях неясны. В любом случае, за более чем 15 лет применения ТИК у детей не было никаких сообщений о развитии онкологических заболеваний, и нет поводов беспокоиться о возможной абсорбции препаратов с развитием системной иммуносупрессии.
В последнее время появляются данные, что ТИК и топические стероиды могут иметь и профилактический эффект (при длительном постоянном применении), проявляющийся в удлинении ремиссии АД, однако долгосрочная безопасность подобных режимов лечения не изучалась.
Контроль зуда – важный компонент лечения АД, поскольку зуд часто беспокоит пациентов (даже в отсутствие явной сыпи), нарушает их сон, приводит к механическому повреждению кожи из-за расчесов (цикл «зуд–расчесывание»). Патофизиология зуда сложна и включает периферические и центральные факторы. Периферические факторы – это проникновение раздражителей (аэроаллергены, шерсть, пот, химические вещества) через дефектный эпидермальный барьер, трансэпидермальные потери воды, травмирование кожи при расчесывании, протеазная активность в коже. Центральные механизмы зуда опосредованы множеством различных медиаторов, роль гистамина среди которых весьма ограничена.
Для купирования зуда часто достаточно адекватного наружного увлажняющего и противовоспалительного лечения. Но иногда требуется дополнительная системная терапия. Оральные антигистаминные препараты не влияют на проявления АД, но могут уменьшать само ощущение зуда. Антигистаминные препараты І поколения должны с осторожностью применяться у детей раннего возраста, у которых чаще проявляются их неблагоприятные эффекты. Кроме того, у некоторых детей могут развиваться парадоксальные эффекты ажитации вместо успокоения. Неседативные антигистамины менее эффективны при зуде, но могут быть полезными для пациентов, у которых обострения АД связаны с действием конкретных аллергенов (например, пыльцевых).
Местные антигистаминные препараты НЕЭФФЕКТИВНЫ в лечении зуда при АД и содержат потенциальные раздражители и аллергены, которые могут ухудшить течение заболевания.
Профилактика и лечение инфекционных осложнений
Пациенты с АД, особенно плохо контролируемым, склонны к бактериальным и вирусным инфекциям кожи. Помимо нарушения целостности кожного барьера, при АД имеются нарушения экспрессии кожных противомикробных пептидов, дефекты toll-подобных рецепторов, иммунная дисрегуляция в виде сниженного рекрутирования иммунокомпетентных клеток.
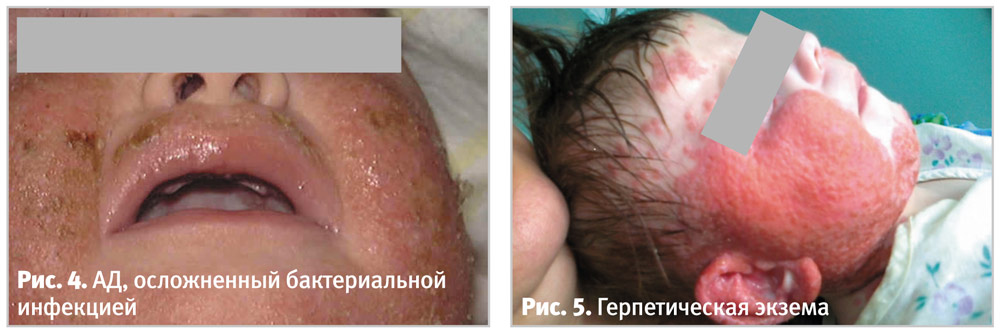
Около 90% пациентов с АД колонизированы S. aureus. Токсины, выделяемые большинством штаммов S. aureus, на коже ведут себя как суперантигены и могут непосредственно влиять на активность заболевания, несмотря на возможное отсутствие клинических признаков бактериальной суперинфекции. Местная активизация стафилококковой инфекции проявляется появлением пустул с мокнутием и корками цвета меда, а лихорадка и целлюлит указывают на инвазивный характер инфекции. Вторичная бактериальная инфекция нередко ассоциируется с обострением АД (рис. 4). Бакпосевы отделяемого из пустул могут быть полезны для идентификации причинно-значимого микроорганизма, но не всегда являются необходимыми. Частота выявления метициллин-резистентного S. aureus (MRSA) у пациентов с АД значительно варьирует, но отмечается тенденция к повышению распространенности этого микроорганизма.
Стрептококковые инфекции также могут иметь место при АД. Они проявляются появлением пустул, болезненных эрозий и лихорадки. Кроме того, при инвазивной инфекции может отмечаться вовлечение кожи лица или периорбитальной области.
При вторичном инфицировании кожи и отсутствии признаков системной инфекции в дополнение к увлажняющей и противовоспалительной терапии назначают местные противомикробные препараты (например, мупироцин) или используют комбинированные средства, содержащие топический ГКС и антимикробный препарат. При системной инфекции применяют пероральные или парентеральные антибиотики (в зависимости от степени тяжести инфекции). Препараты выбора – цефалоспорины І–II поколения и полусинтетические пенициллины (если нет подозрения на инфекцию MRSA). Возможность инфекции MRSA или другие причины стоит рассмотреть при неэффективности терапии.
Наиболее частыми вирусными инфекциями кожи при АД являются контагиозный моллюск, герпетическая экзема и недавно описанная атипичная энтеровирусная инфекция, вызванная вирусом Коксаки А6.
Герпетическая экзема характеризуется появлением мелких, часто сгруппированных, папуло-везикул, везикул с серозным и серозно-геморрагическим содержимым, а затем пустул. Везикулы и пустулы примерно одного размера, имеют куполообразную форму с пупкообразным вдавлением в центре и воспалительным валиком по периферии (рис. 5). Герпетическая экзема – потенциально угрожающее жизни состояние и требует системного лечения ацикловиром, адекватного обезболивания, а также ухода за кожей, местной противовоспалительной терапии и применения антимикробных средств в случае сопутствующей вторичной бактериальной инфекции.
При атипичной инфекции Коксаки А6 высыпания, характерные для болезни «нога–рука–рот», появляются на участках кожи, пораженной АД. В случаях, когда диагноз не ясен, показаны вирусологические исследования.
На основании представленной выше информации врач первичного звена в большинстве случаев может успешно лечить детей с АД. Если же пациенты с подозреваемым АД не отвечают на это лечение, требуется направление к детскому дерматологу. Другими показаниями для направления к дерматологу являются плохо контролируемый или генерализованный АД, рецидивирующие инфекции кожи (вирусные или бактериальные), подозрение на аллергический контактный дерматит, а также наличие нетипичных клинических симптомов и признаков. В случаях упорного, резистентного к терапии АД может быть назначена системная фототерапия или иммуносупрессивные препараты. Оральные стероиды в настоящее время не используются из-за возможных неблагоприятных побочных эффектов и высокой вероятности развития «синдрома рикошета».
Стоит также упомянуть о методах лечения АД, эффективность которых остается недоказанной. Так, не была доказана эффективность применения пробиотиков/пребиотиков, рыбьего жира, масла энотеры, масла огуречника, поливитаминных добавок, цинка, витамина D, витамина Е, витаминов B12 и B6. Нет необходимости исключать из рациона ребенка пищевые аллергены, если сенсибилизация к ним подтверждена только лабораторными тестами (кроме случаев развития аллергических реакций немедленного типа). Из-за недостатка научных данных не рекомендуется в настоящее время использовать специальные покрытия для мебели, предотвращающие контакт с аллергенами домашней пыли, а также использовать специальные циклы стирки (двойное полоскание), специальные моющие средства, носить одежду из специальных тканей (например, с пропиткой серебром или из натурального шелка). Нет научно обоснованных доказательств эффективности нетрадиционных методов лечения: китайской фитотерапии и массажа, ароматерапии, натуропатии, гипноза, акупунктуры и аутогемотерапии.
Заключение
Aтопический дерматит – заболевание, которое может существенно осложнять жизнь больным детям и их родителям, а также быть проблемой для наблюдающего их врача первичного звена. Хотя патогенез АД довольно сложен, недавние результаты научных исследований подтвердили ведущую роль нарушений барьерных функций кожи при этом заболевании. В связи с этим основные усилия в лечении АД должны быть направлены именно на методы наружной терапии. Наружная терапия главным образом включает постоянный уход за кожей с целью восстановления ее барьерных свойств и использование топических стероидов при обострении заболевания. Топические ГКС с низким и умеренным уровнем активности являются безопасными и эффективными для детей при правильном использовании. Ранняя диагностика и лечение инфекционных осложнений способствует улучшению результатов лечения. Поддержка пациентов и их семей, обучение и консультирование по вопросам патогенеза, специфического лечения и прогноза заболевания играют чрезвычайно важную роль в ведении пациентов с АД. ![]()


коментариев