Некротичний ентероколіт (НЕК) – набуте захворювання, що проявляється важким пошкодженням кишечника внаслідок дії комбінації різних чинників на відносно незрілий кишечник. Некротичний ентероколіт доношених новонароджених чи зрілих недоношених зазвичай розвивається у перший тиждень після народження
Найчастіше він пов'язаний з такими проблемами як кишкові аномалії (наприклад, агангліоз чи атрезія), перинатальний стрес, вроджені вади серця, вживання наркотиків матір'ю. Класичний некротичний ентероколіт недоношених новонароджених є найбільш поширеною формою захворювання. Чим більша незрілість немовляти, тим пізніше після народження цей стан маніфестує.
Частота НЕК — 1–3 випадки на 1000 народжених живими дітей, понад 90% випадків припадає на недоношених. У 50% недоношених дітей під час перебування у неонатальних відділеннях фіксують ознаки непереносимості ентеральних годувань. Принаймні у чверті з тих дітей розвивається некротичний ентероколіт.
НЕК діагностується у 4–11% недоношених дітей з дуже малою масою тіла при народженні (ДММТ): у 11,5% з масою при народженні 401–750 г, у 9% з масою 751–1000 г, у 6% з масою 1001–1250 г, у 4% з масою 1251–1500 г. Рівень летальності може досягати 50%.
Некротичний ентероколіт є провідною причиною смерті від шлунково-кишкових причин у недоношених дітей, загальне виживання не покращилась в останні три десятиліття (B. K. Patel, J. S. Shah, 2012 [1]; A. Maheshwari et al., 2011 [2]).
Перші описи НЕК в медичній літературі датуються 50-тими роками минулого століття. У подальшому можна прослідкувати певну хронологію зміни діагностичних підходів до НЕК [3–11]:
- Опис НЕК переважно у доношених дітей. У оригінальній класифікації (M. J. Bell, 1978, M. Walsh, 1986) головна увага приділялась клінічним стадіям НЕК для оцінки тяжкості захворювання (табл. 1).
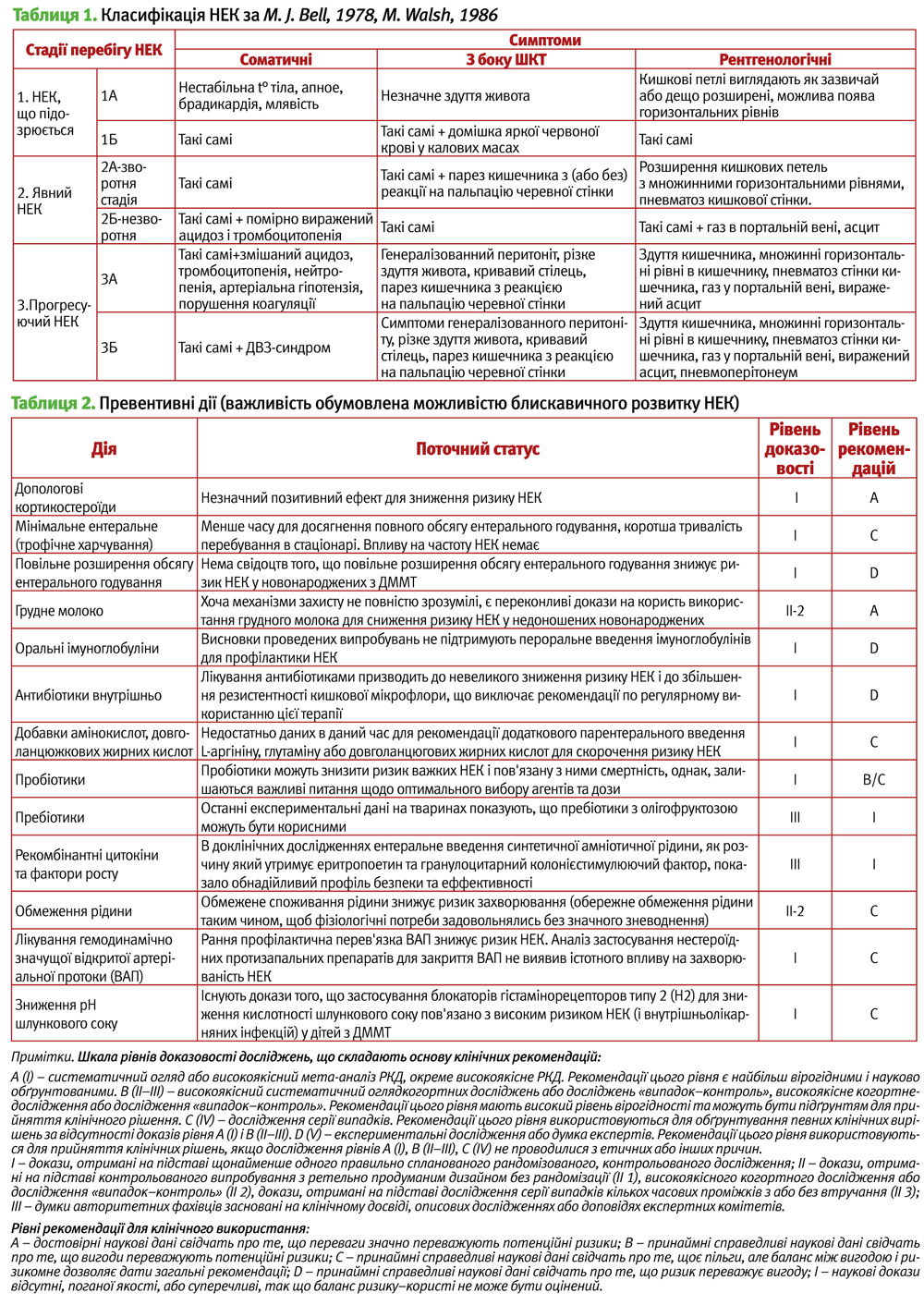
- Опис «нового НЕК» у глибоко недоношених дітей, які вижили.
- Інтерпретація I стадії класифікації M. J. Bell, M. Walsh з метою виключення інших причин парезу кишечника (наприклад, диференціації НЕК і проявів кишкової непрохідності внаслідок сепсису).
- Окремий розгляд випадків спонтанної кишкової перфорації.
- НЕК – єдине захворювання чи спектр захворювань? Виділення «НЕК-подібних захворювань».
- Поняття про «передумовленість» НЕК. Акцент на визначенні факторів ризику, для того, щоб збільшити ефективність профілактики і лікування.
Обгрунтуванням «передумовленості» НЕК були:
- наявність сумнівів у тому, що рання діагностика та втручання змінять результат захворювання;
- роль незрілих функцій Toll-подібних рецепторів у недоношених дітей у патогенезі НЕК (дисбаланс між TLR4 і TLR9 є одним з найбільш важливих чинників розвитку захворювання; у недоношених дітей вміст TLR4 залишається на високому рівні після народження; в умовах мікробної колонізації активація TLR4 призводить до недостатності кишкового бар'єру, транслокації бактерій, розвитку клінічних проявів НЕК; активація TLR4 посилює апоптоз і зменшує проліферацію та міграцію ентероцитів);
- можливі генетичні чинники розвитку НЕК (епідеміологічні дослідження виявили кілька генів, які можуть модифікувати тяжкість захворювання та / або його результат).
- Пропозиції щодо заміни класифікацій діагностично-лікувальним алгоритмом (табл. 4).

Істотними діагностичними проблемами на теперішній час є низька діагностична значимість на ранніх стадіях захворювання ознак харчової непереносимості і периферичних гемодинамічних розладів; мінливість ознак маніфестації і тяжкості, труднощі диференційної діагностики з сепсисом, ознаками кишкової непрохідності іншої етіології; висока специфічність, але низька чутливість і погана негативна прогностична цінність рентгенологічних ознак НЕК. Діагностичною проблемою є також можливість «блискавичного» перебігу НЕК, наявність спонтанної кишкової перфорації, як самостійного захворювання, а також труднощі диференційної діагностики НЕК та синдрому меконіальної обструкції (P. Gordon et al., 2012 [7]; J. Neu et al., 2011 [11]).
Блискавичний НЕК характеризується масивним некрозом кишечника, швидким прогресуванням і можливим розвитком летального результату протягом 48 годин. 66% смертей від НЕК обумовлені його блискавичним перебігом. Дві третини всіх перфорацій кишечника відбуваються в межах 30–48 годин. Зустрічається з частотою до 7–10% у дітей з вагою 1088±545 г [12].
Спонтанна перфорація кишечника (СПК) – окрема нозологічна форма, відмінна від III ст. НЕК. Перфорація відбувається у ділянці тонкого кишечника (зазвичай клубової кишки) без ознак некрозу. СПК зазвичай розвивається у дітей з екстремально малою масою тіла (ЕММТ) (669±52г), низьким гестаційним віком (24,4±0,8 тижня) і діагностується у віці 9,5±3,5 днів (діапазон 4–14 днів життя). СПК у новонароджених з екстремально малою масою тіла (£1000 г) часто пов'язана з грибковою інфекцією і сепсисом, викликаним коагулазонегативним стафілококом. Інші фактори ризику – постнатальне застосування стероїдів та індометацину, вроджений дефект м'язового шару кишкової стінки. Частота СПК становить 5,0–8,4% у новонароджених з ЕММТ (2–3% у дітей з ДММТ) (P. V. Gordon et al., 2009 [13]).
Меконіальна обструкція у новонароджених з ДММТ – визнана причина функціональної кишкової непрохідності. Це окрема патологія, притаманна новонародженим з ДММТ, яка може призводити до перфорації кишечника і тривалої госпіталізації. Предиктор розвитку меконіальної обструкції – зниження кишкової перфузії. Патологія характеризується поєднанням поганої перистальтики кишечника, «низької» обструкції в'язким меконієм (найбільш часто в дистальних відділах клубової кишки), відсутністю важких системних проявів, ознак перитоніту. Клінічні особливості: здуття живота, блювота з жовчю, петлі кишечника на рентгенограмі розширені, без рівнів рідини і пневматозу. Симптоми обструкції виникають через кілька днів після початкового періоду відходження меконію (за відсутності муковісцидозу і хвороби Гіршпрунга), зазвичай близько другого тижня життя. При ранній діагностиці можливе ефективне проведення консервативної терапії (2/3 випадків). Затримка у діагностиці та лікуванні пов'язана з ризиком перфорації і необхідністю тривалого парентерального харчування. Цілком можливо, що важке, тривале здуття проксимального відділу кишки викликає ішемію в антимезентеріальній частині кишечника, у результаті чого розвивається НЕК (J. Neu et al., 2011 [11]; P. V. Gordon et al., 2009 [13]; S. Garza-Cox et al., 2004 [14]; V. F. Paradiso et al., 2011 [15]; M. F. Siddiqui et al., 2012 [16]).
Все вищевказане призводить до вирішального значення високого індексу підозри у діагностиці ризику і, закономірно, формування НЕК-фобії та гіпердіагностики: НЕК-фобії на тлі початку і нарощування обсягу годувань, гіпердіагностики НЕК при наявності неспецифічних симптомів, гіпердіагностики НЕК через можливість «катастрофічного» перебігу.
Наслідками гіпердіагностики НЕК будуть (P. Gordon et al., 2012 [7]; D. J. Hackam et al., 2013 [10]):
- необхідність скасування ентерального харчування, необхідність проведення парентерального харчування, подовження періоду становлення ентерального харчування;
- тривале використання внутрішньовенного доступу, збільшення ризику тромбоемболічних ускладнень і внутрішньолікарняних інфекцій, збільшення ризику фунгемії;
- масивне використання антибактеріальних препаратів;
- пригноблення антибіотиками кишкової флори (колонізація лактобацилами і біфідобактеріями зменшує ризик НЕК за рахунок регуляції антагоністичних взаємодій TLR9/TLR4);
- і, в свою чергу, збільшення ризику розвитку НЕК.
Засобом протидії несприятливим наслідкам як запізнілої діагностики НЕК, так і гіпердіагностики є превентивні дії (табл. 2) та діагностично-лікувальні стратегії [1, 7, 10, 11, 17-21]. Ці стратегії можна розділити на три категорії: з доведеною або ймовірної ефективністю, з недоведеною ефективністю або обмежені дані та експериментальні стратегії.
Оскільки понад 90% дітей з діагнозом НЕК отримували до цього ентеральне харчування, на ефективність профілактики захворювання істотно впливає стратегія годування дітей з ДММТ (Cincinnati Children's Hospital Medical Center Guideline, 2010 [17]; L. A. Parker et al., 2013 [19]) (табл. 3).
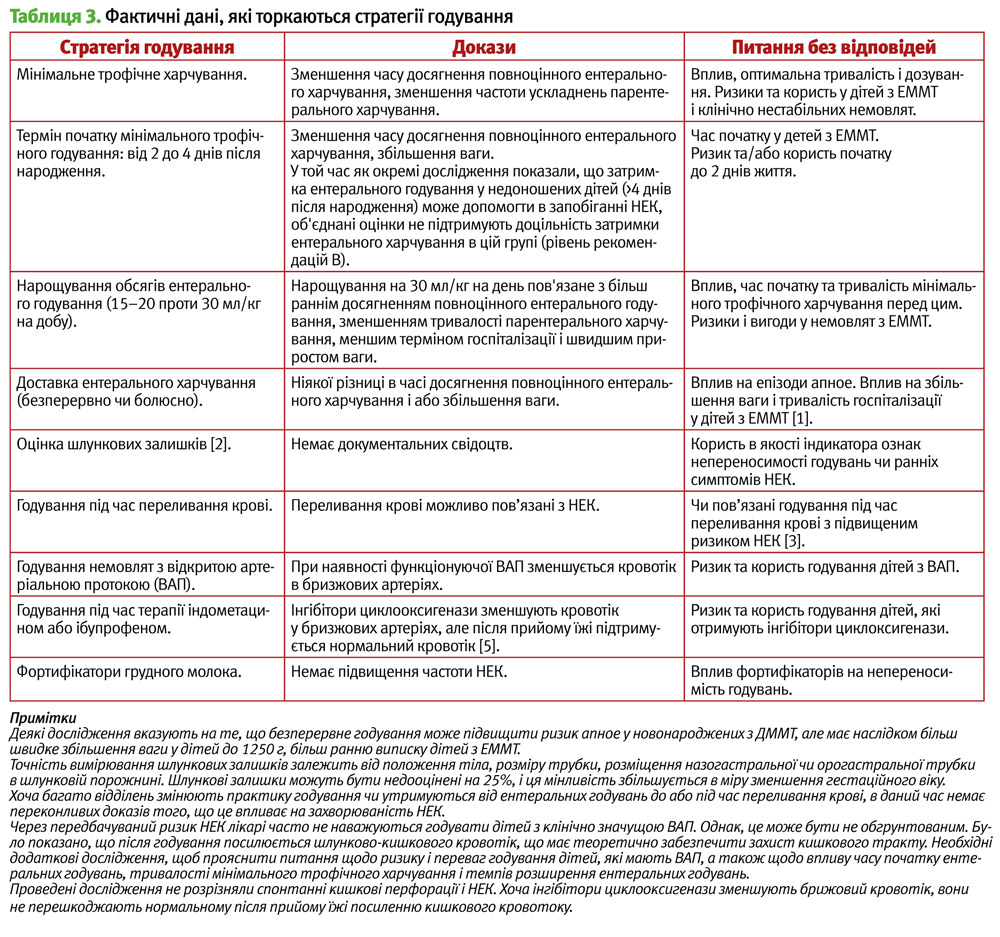
Існують рекомендації щодо рутинного використання пробіотиків у недоношених дітей, щоб знизити захворюваність на важкий НЕК (рівень рекомендацій В/С). При проведенні досліджень використовували змінні склади препаратів (Lactobacillus, Bifidobacterium, Saccharomyces boulardiї, суміші з двох або трьох пробіотиків) і різну тривалість курсу лікування пробіотиками. Вводилися пробіотики також різним чином: протягом протягом перших 24 годин життя, під час першого годування, або коли ентеральне годування добре переносилось. Тривалість використання – не менше двох тижнів. Хоча жодних офіційних рекомендацій щодо складу, часу або тривалості прийому препаратів не було встановлено, вважається доцільним призначення принаймні одного пробіотика у перші тижні життя і це повинно тривати протягом не менше двох тижнів (J. Neu et al., 2011 [11]; Cincinnati Children's Hospital Medical Center Guideline, 2010 [17]; L. A. Parker et al., 2013 [19]).
Пропонований діагностично-лікувальний алгоритм представлений у таблиці 4 ((J. Neu et al., 2011 [11]; Cincinnati Children's Hospital Medical Center Guideline, 2010 [17]; C. D. Downard et al., 2012 [18]; О. М. Горбатюк та співавт., 2013 [22]).
Поточний статус щодо рівня доказовості та рівня рекомендацій лікувальних заходів представлений у таблиці 5.

Зважаючи на те, що НЕК по суті є «міждисциплінарною» патологією, на даний час назріла необхідність спільного обговорення та затвердження неонатологами та дитячими хірургами нормативних документів щодо алгоритму ведення дітей з НЕК (О. М. Горбатюк та співавт., 2013 [22]).
Повний перелік літератури знаходиться у редакції.

коментариев