 «Мультидисциплинарный подход в гинекологии является чрезвычайно важным вопросом» – об этом сказала заместитель директора ГУ «Институт педиатрии, акушерства и гинекологии НАМН Украины», член-корреспондент НАМН Украины, д. мед. н., профессор Татьяна Феофановна Татарчук, открывая международную конференцию «Репродуктивное здоровье женщины в XXI веке».
«Мультидисциплинарный подход в гинекологии является чрезвычайно важным вопросом» – об этом сказала заместитель директора ГУ «Институт педиатрии, акушерства и гинекологии НАМН Украины», член-корреспондент НАМН Украины, д. мед. н., профессор Татьяна Феофановна Татарчук, открывая международную конференцию «Репродуктивное здоровье женщины в XXI веке».
Большой интерес вызвал доклад заместителя директора ГУ «Институт педиатрии, акушерства и гинекологии НАМН Украины», члена-корреспондента НАМН Украины, д. мед. н., профессора Татьяны Феофановны Татарчук. Она посвятила свое выступление лечению НЛФ с позиции доказательной медицины и начала его с того, что призналась, какой нелегкой ей показалась эта тема на начальном этапе поиска необходимой информации.
Т. Ф. Татарчук напомнила, что история изучения НЛФ начинается с 1937 года, а в 1950 году медицинскому миру были представлены критерии Нойса, однако сам термин «недостаточность лютеиновой фазы» начали употреблять через 50 лет, в 2002 году. НЛФ определяли как состояние, проявляющееся дефицитом прогестерона, укорочением лютеиновой фазы (менее 11 дней) и отставанием созревания эндометрия от фазы цикла более чем на 2 дня. НЛФ рассматривали как одну из основных причин нарушения менструального цикла, ПМС, нарушений фертильности, бесплодия, невынашивания, привычного невынашивания беременности.
Неоднозначным отношение к этому вопросу стало после появления в 2004 году публикации «Недостаточность лютеиновой фазы: миф или реальность?» Этот критический анализ представил данные, которые демонстрируют неточность гистологических исследований, применяемых с целью установления причин бесплодия и невынашивания, так как частота ошибки при осмотре одним и тем же гистологом в разное время колеблется, по данным анализа, в пределах 18–22%. Исходя из сказанного, профессор Т. Ф. Татарчук отметила, что важными для установления диагноза НЛФ являются определение концентрации прогестерона, УЗИ-мониторинг менструального цикла и тесты функциональной диагностики, которыми, к сожалению, пациентки часто пренебрегают. В докладе также содержались рекомендации обращать внимание на склонность пациентки к депрессиям, головной боли, другим симптомам ПМС.
Значительное внимание в своем докладе профессор Т.Ф. Татарчук уделила проблеме чувствительности желтого тела к стрессовому фактору. При кратковременном стрессовом воздействии, в соответствии с приведенными данными, при сохранении овуляторного цикла уровень прогестерона снижается у женщины на 50%. Этим, по мнению Татьяны Феофановны, объясняются случаи прерывания беременности после медового месяца, проведенного вдали от дома, ведь далекое путешествие является для организма кратковременным стрессом.
Профессор привела результаты исследования с участием 216 пациенток. В исследовании учитывали все причины невынашивания. Самый значимый клинический результат был получен и в группе, которой были назначены Циклодинон и прогестерон (Утрожестан 200 мг), который также обладает анксиолитическим и нейропротекторным эффектами.
Татьяна Феофановна также отметила, что лечение необходимо проводить минимум за один цикл до наступления планируемой беременности. При стресс-индуцированной НЛФ было показано, что даже на фоне овуляторных циклов будет иметь место дефицит выработки прогестерона желтым телом, а соответственно, и нарушение рецептивности эндометрия.
Таким женщинам показано назначение Утрожестана по 100 мг 2 раза в сутки, с 16 по 25 день, чтобы добиться синхронной трансформации эндометрия, что важно для успешной имплантации и формирования плаценты, которая в дальнейшем будет отвечать и за синтез прогестерона, и во многом определять нормальное течение беременности.
Согласно последним данным, даже в случае возникновения угрозы прерывания беременности, впервые мы ставим диагноз НЛФ на основании клиники и анамнестических данных и назначаем соответствующую терапию. В Кокрановском обзоре 2011 года показано, что назначение прогестагенов эффективно в лечении угрожающего аборта и сохраняет беременность на ранних сроках. Соблюдая принцип преемственности терапии, применение Утрожестана может быть продолжено при необходимости, так как беременность, наступившая на фоне НЛФ, часто сопровождается угрозой невынашивания за счет снижения синтеза прогестерона и всех его эффектов (иммунотолерантности, снижения токолитического эффекта).
Восполнение прогестерона (Утрожестан в дозе 200–300 мг/сут.) у таких женщин помогает избежать прерывания беременности, при кровомазаниях доза может быть повышена до 400 мг/сут., разделенная на 2 приема, вагинально или комбинированно (вагинально и перорально).
В конце своего выступления Татьяна Феофановна сделала определенные выводы. Применение комбинированной терапии, включающей воздействие на функциональную гиперпролактинемию, тревожно-депрессивные симптомы (Циклодинон) и гормональную поддержку лютеиновой фазы (Утрожестан), обеспечивает наибольшую эффективность как в отношении нормализации овуляторной функции, так и в отношении снижения стрессового напряжения у женщин со стресс-индуцированной НЛФ. Это обусловливает обоснованность комбинированной терапии.
Эмоциональным и насыщенным также был доклад «Преждевременные роды в XXI веке: синопсис и практика», представленный главным научным сотрудником акушерского отделения экстрагенитальной патологии беременных ГУ «Институт педиатрии, акушерства и гинекологии НАМН Украины», д. мед. н. Юлией Владимировной Давыдовой. Говоря об актуальности проблемы, она отметила, что в мире ежегодно рождаются почти 15 млн. недоношенных детей. По общемировой статистике – это каждый девятый ребенок. В то же время, в США это каждый восьмой ребенок, при том, что Соединенные Штаты тратят ежегодно 26 млрд. долларов на предотвращение ПР. Более миллиона недоношенных детей погибают в первую неделю жизни, 50% оставшихся в живых становятся глубокими инвалидами. Несмотря на то, что ПР были всегда, на сегодняшний день об их причине с точностью не известно ничего.
Ю. В. Давыдова напомнила, что известны четыре основные патогенетические причины ПР: воспаление, активация системы гипоталамус–гипофиз–надпочечники (в том числе вследствие стресса), перерастяжение матки (при многоплодной беременности) и децидуальные кровотечения. Возвращаясь к истории вопроса, Юлия Владимировна проанализировала определение ПР, применяемое в различные годы. В Европе о сохранении жизни недоношенных детей начали говорить лишь после окончания Второй мировой войны, связанной с огромными человеческими потерями. Когда жизнь каждого новорожденного приобрела очень важное значение, в различных странах начали задумываться о том, как эту жизнь сохранить, если ребенок родился раньше срока.
Изначально недоношенным считался ребенок с массой тела менее 2,5 кг, в 1961 году ВОЗ изменила формулировку, и преждевременными стали считать роды до 37 недели. В 1969 году формулировка была пересмотрена еще раз, и в этот период началась разработка токолитиков, появилось понятие перинатальной смертности, и в экономически развитых странах началась борьба за снижение ее показателей. Со временем изменилась трактовка понятия ПР, так как были определены большие расхождения между малой массой тела ребенка и сроком гестации. С начала 2000 годов речь идет о том, что причиной ПР является сочетание анатомических, структурных и функциональных изменений. Ю. В. Давыдова привела в своем выступлении данные, которые свидетельствуют о том, что из всех тактик в отношении снижения числа ПР наиболее эффективным является отказ от курения и применение прогестерона. В то же время, использование серкляжа (наложения шва на матку) эффективно лишь у определенной группы риска и только в странах с высоким уровнем доходов населения. Докладчица отметила, что в современных условиях в большинстве стран мира диагностика ПР основана преимущественно на субъективных данных, то есть, на боли в области матки, поясницы, внизу живота. Объективным методом оценки можно считать исследование структурных изменений шейки матки. Чтобы эффективно прогнозировать ПР, нужно уменьшить частоту смертей и инвалидности детей при положительном результате, а также избежать дорогостоящего и опасного лечения женщины при негативном результате.
Доказательными маркерами ПР, по словам Юлии Владимировны, являются фетальный фибронектин и длина шейки матки при трансвагинальном УЗИ. Если длина шейки матки составляет более 25 мм и тест на фетальный фибронектин отрицательный, лечение и госпитализация такой женщине не требуется. При появлении в результатах исследования положительного фибронектина при длине шейки матки более 25 мм рекомендуется немедленная госпитализация, мониторинг, возможно, кортикостероиды для профилактики респираторного дистресс-синдрома. Причем женщина должна быть госпитализирована на третий уровень перинатальной помощи.
Положительный фибронектин и длина шейки матки менее 25 мм являются показаниями не только к госпитализации, но и к острому токолизу, стероидной терапии и, возможно, назначению антибиотиков. Потребность в токолизе обсуждается при необходимости ввести кортикостероиды в ранние сроки беременности, когда требуется время для созревания легких плода и раскрытие шейки матки составляет менее 4 см. В такой ситуации острый токолиз позволит отсрочить ПР на 24–48 часов. Противопоказаниями к такому подходу являются артериальная гипертензия, кровотечения, тяжелые заболевания сердца.
Идеальным, по современным представлениям, должен быть токолитик, эффективный в 23–28 недели, требующий низких доз для достижения эффекта, с минимальными побочными эффектами и четкими показаниями к применению.
Отвечает этим требованиям, по мнению Ю. В. Давыдовой, микронизированный прогестерон.
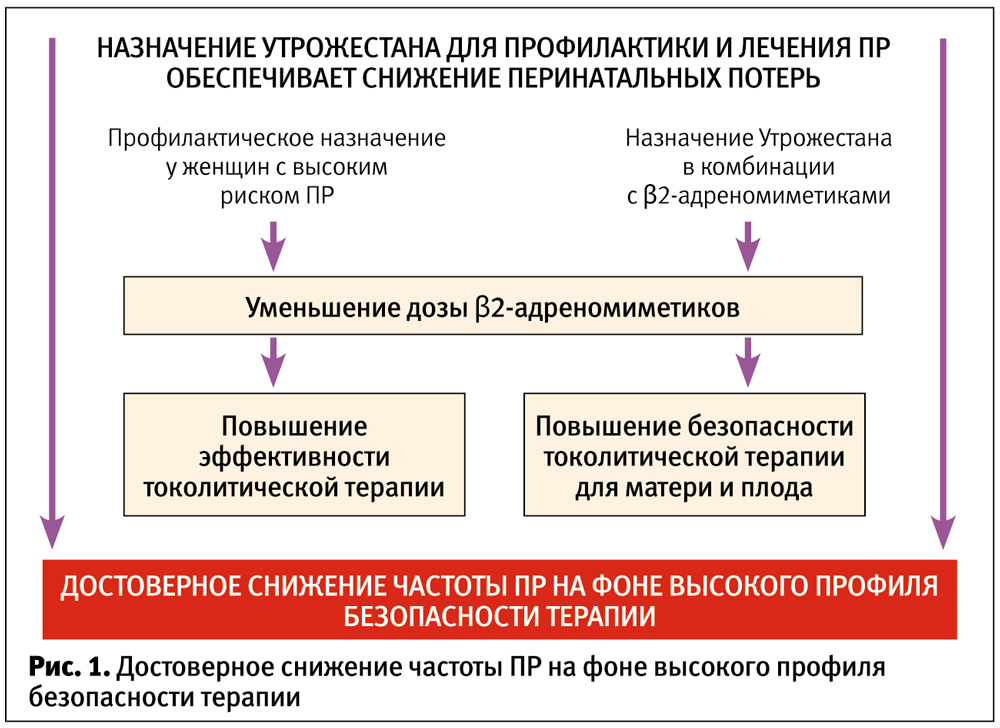
Назначение Утрожестана на ранних сроках предотвращает угрозу аборта, а на поздних – наступление ПР у женщин из групп риска. Сочетанный токолиз с b-миметиками позволяет, с одной стороны, повысить безопасность проводимой терапии за счет снижения дозы и длительности приема b-миметиков, а с другой стороны – более эффективно пролонгировать беременность (рис. 1).
Ю. В. Давыдова также привела данные исследования Хасан и Ромеро (2012) в отношении микронизированного прогестерона.
Результаты метаанализа свидетельствуют, что применение вагинальной формы прогестерона (Утрожестан) у женщин с анатомической короткой шейкой матки и ПР в анамнезе во II триместре снижает частоту ПР на 50% в сроке меньше 32 недель, на 45% – в сроке меньше 33 недель, и в сроке меньше 35 недель – на 38%.
Целесообразным, по мнению Юлии Владимировны, было бы создание алгоритма стратификации риска ПР – по аналогии со стратификацией сердечно-сосудистого риска. В условиях Украины такой подход позволил бы в оптимальные сроки направить пациентку на соответствующий уровень оказания перинатальной помощи.
Для группы низкого риска Юлия Владимировна и ее коллеги предлагают первичную популяционную профилактику, включающую информирование. У женщины должны быть оценены такие факторы риска как бактериальный вагиноз, укороченная шейка матки, прогестероновая недостаточность, анатомические изменения матки, многоплодная беременность, многоводие, врожденные патологии плода. Если таких состояний не выявлено, беременную наблюдают согласно Приказу МЗ Украины №417.
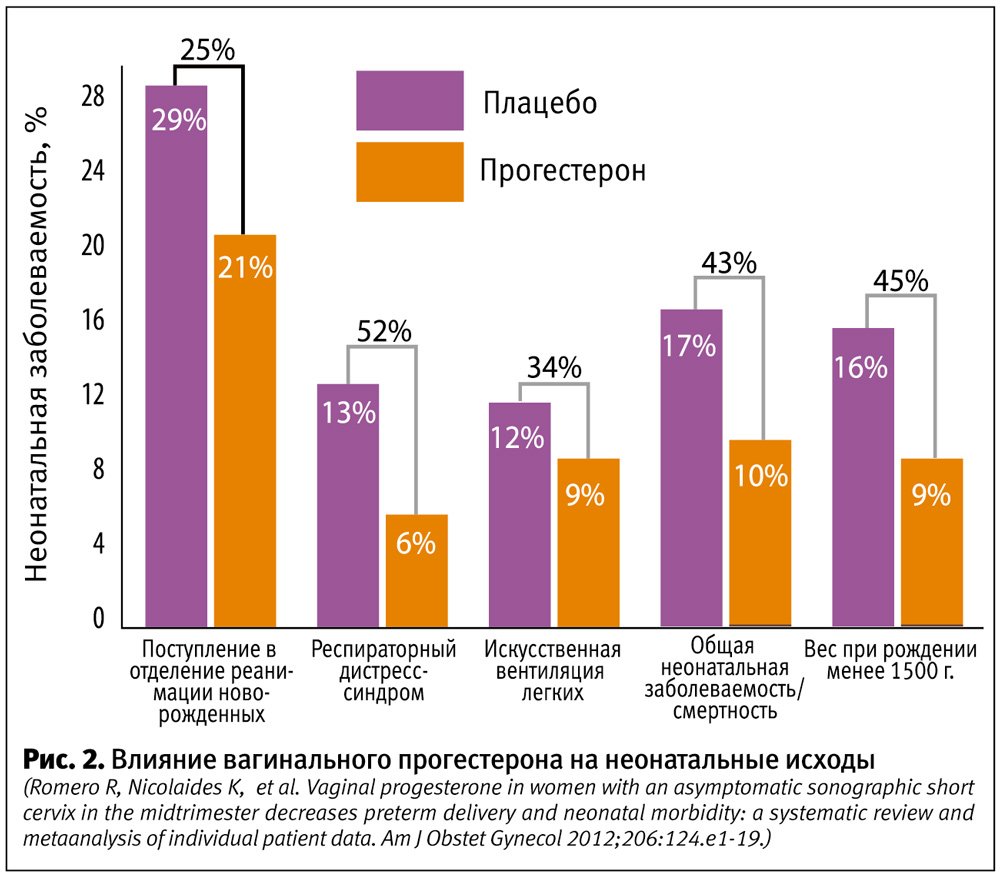
К группе высокого риска, требующей вторичной профилактики ПР, относят женщин с вновь выявленными факторами риска и отсутствием клинической симптоматики. Такой группе пациенток следует рекомендовать изменение режима наблюдения и объемов исследования. При необходимости им можно проводить динамическую цервикометрию, серкляж при доказанной несостоятельности шейки матки, применение прогестерона. Такие женщины должны быть направлены для консультирования в региональные перинатальные центры третьего уровня. При ПР до 34 недель все женщины должны быть направлены в региональный перинатальный центр третьего уровня и здесь при наличии клинической симптоматики необходима третичная профилактика. В частности, речь идет о применении прогестерона и нейропротекторном воздействии микронизированного прогестерона на центральную нервную систему плода и новорожденного (рис. 2). Резюмируя сказанное, Юлия Владимировна отметила, что риск повторных ПР может быть снижен у женщин с анамнестическими факторами риска и/или короткой шейкой матки путем введения прогестерона профилактически и селективным наложением серкляж.
Материал впервые напечатан в журнале «Здоровье женщины»
№3 (79) 2013.

коментарів